福州大学考研生物化学笔记知识讲解
- 格式:doc
- 大小:146.50 KB
- 文档页数:54

生物化学考试重点总结
1. 生物化学基本概念
- 生物大分子:蛋白质、核酸、多糖、脂质
- 酶:催化生化反应的生物催化剂
- 代谢路径:物质在生物体内相互转化的路径
2. 生物大分子的结构与功能
- 蛋白质:结构、功能、种类、合成和降解
- 核酸:DNA和RNA的结构、功能、复制和转录
- 多糖:单糖、二糖、多糖的结构、功能、合成和降解- 脂质:脂肪酸、甘油三酯、磷脂的结构、功能和代谢
3. 代谢途径与调控
- 糖代谢:糖酵解、糖异生、糖原代谢
- 脂肪代谢:脂肪酸氧化、甘油三酯合成、脂肪酸合成- 蛋白质代谢:蛋白质降解、蛋白质合成、氨基酸代谢- 核酸代谢:DNA和RNA的代谢途径及调控机制
4. 其他重点知识点
- 酶动力学:酶的活性、酶动力学参数、酶抑制剂
- 信号转导与调控:细胞信号传导、信号通路、蛋白质磷酸化- 生物膜:细胞膜结构、跨膜转运和信号传导
5. 实验技术
- 分子生物学实验技术:PCR、DNA测序、蛋白质电泳
- 生物化学分离和分析方法:色谱技术、质谱技术、光谱技术
以上是生物化学考试的重点内容总结,希望对你的备考有所帮助。
祝你考试顺利!。


生物化学重点绪论一、生物化学的的概念:生物化学(biochemistry)是利用化学的原理与方法去探讨生命的一门科学,它是介于化学、生物学及物理学之间的一门边缘学科。
二、生物化学的发展:1.叙述生物化学阶段:是生物化学发展的萌芽阶段,其主要的工作是分析和研究生物体的组成成分以及生物体的分泌物和排泄物。
2.动态生物化学阶段:是生物化学蓬勃发展的时期。
就在这一时期,人们基本上弄清了生物体内各种主要化学物质的代谢途径。
3.分子生物学阶段:这一阶段的主要研究工作就是探讨各种生物大分子的结构与其功能之间的关系。
三、生物化学研究的主要方面:1.生物体的物质组成:高等生物体主要由蛋白质、核酸、糖类、脂类以及水、无机盐等组成,此外还含有一些低分子物质。
2.物质代谢:物质代谢的基本过程主要包括三大步骤:消化、吸收→中间代谢→排泄。
其中,中间代谢过程是在细胞内进行的,最为复杂的化学变化过程,它包括合成代谢,分解代谢,物质互变,代谢调控,能量代谢几方面的内容。
3.细胞信号转导:细胞内存在多条信号转导途径,而这些途径之间通过一定的方式方式相互交织在一起,从而构成了非常复杂的信号转导网络,调控细胞的代谢、生理活动及生长分化。
4.生物分子的结构与功能:通过对生物大分子结构的理解,揭示结构与功能之间的关系。
5.遗传与繁殖:对生物体遗传与繁殖的分子机制的研究,也是现代生物化学与分子生物学研究的一个重要内容。
第一章蛋白质的结构与功能一、氨基酸:1.结构特点:氨基酸(amino acid)是蛋白质分子的基本组成单位。
构成天然蛋白质分子的氨基酸约有20种,除脯氨酸为α-亚氨基酸、甘氨酸不含手性碳原子外,其余氨基酸均为L-α-氨基酸。
2.分类:根据氨基酸的R基团的极性大小可将氨基酸分为四类:①非极性中性氨基酸(8种);②极性中性氨基酸(7种);③酸性氨基酸(Glu和Asp);④碱性氨基酸(Lys、Arg和His)。
二、肽键与肽链:肽键(peptide bond)是指由一分子氨基酸的α-羧基与另一分子氨基酸的α-氨基经脱水而形成的共价键(-CO-NH-)。

生物化学重点笔记哎呀,一提到生物化学,那可真是一门让人又爱又恨的学科啊!我还记得当初学习这门课的时候,那叫一个头大。
不过,经过一番“摸爬滚打”,我总算是整理出了一份自认为还不错的重点笔记。
先来说说蛋白质这个部分吧。
蛋白质可是生物体内的“大明星”,它们无处不在,而且功能繁多。
老师在课上讲的时候,那真是滔滔不绝,而我则是在下面奋笔疾书。
蛋白质的结构那是相当复杂,一级结构、二级结构、三级结构、四级结构,一个比一个让人眼花缭乱。
就说二级结构吧,有α螺旋、β折叠、β转角这些玩意儿。
α螺旋就像是一个拧得紧紧的麻花,氨基酸链绕着中心轴一圈一圈地转。
想象一下,那就是一条长长的“氨基酸项链”,被巧妙地扭成了螺旋的形状。
每个氨基酸之间的距离、角度,那都是有讲究的,稍微有点偏差,这螺旋可就“变形”啦。
β折叠呢,则像是把一张张纸叠在一起,氨基酸链在平面上伸展然后折叠回来。
这折叠的地方啊,就像是折纸的折痕,整整齐齐,规规矩矩。
有时候我就在想,这大自然可真是个神奇的“建筑师”,能设计出这么精妙的结构。
再说说酶吧,这也是生物化学里的一个重要角色。
酶就像是生物体内的“小工人”,勤勤恳恳地干活,加速各种化学反应。
比如说消化酶,它们在我们的胃肠道里努力工作,把吃进去的大分子食物分解成小分子,让身体能够吸收利用。
还记得有一次做实验,我们要测定一种酶的活性。
那真是小心翼翼啊,每一步操作都不敢马虎。
试剂的添加量要精确到微升,反应的温度和时间也要严格控制。
我眼睛紧紧盯着试管,心里默默祈祷着实验能成功。
当看到最终的数据符合预期时,那种喜悦简直无法形容,感觉自己就像是一个成功的“科学家”。
还有糖类和脂类,这俩也是生物体内的重要物质。
糖类就像是身体的“能量库”,给我们提供动力。
葡萄糖、果糖、蔗糖,各种各样的糖,都有着自己的特点和作用。
脂类呢,则像是身体的“保暖衣”和“储备粮”,既能保护内脏,又能在需要的时候提供能量。
在学习生物化学的过程中,我发现这门学科其实就像是一个神秘的世界,充满了未知和惊喜。

生物化学重点绪论一、生物化学的的概念:生物化学(biochemistry)是利用化学的原理与方法去探讨生命的一门科学,它是介于化学、生物学及物理学之间的一门边缘学科。
二、生物化学的发展:1.叙述生物化学阶段:是生物化学发展的萌芽阶段,其主要的工作是分析和研究生物体的组成成分以及生物体的分泌物和排泄物。
2.动态生物化学阶段:是生物化学蓬勃发展的时期。
就在这一时期,人们基本上弄清了生物体内各种主要化学物质的代谢途径。
3.分子生物学阶段:这一阶段的主要研究工作就是探讨各种生物大分子的结构与其功能之间的关系。
三、生物化学研究的主要方面:1.生物体的物质组成:高等生物体主要由蛋白质、核酸、糖类、脂类以及水、无机盐等组成,此外还含有一些低分子物质。
2.物质代谢:物质代谢的基本过程主要包括三大步骤:消化、吸收→中间代谢→排泄。
其中,中间代谢过程是在细胞内进行的,最为复杂的化学变化过程,它包括合成代谢,分解代谢,物质互变,代谢调控,能量代谢几方面的内容。
3.细胞信号转导:细胞内存在多条信号转导途径,而这些途径之间通过一定的方式方式相互交织在一起,从而构成了非常复杂的信号转导网络,调控细胞的代谢、生理活动及生长分化。
4.生物分子的结构与功能:通过对生物大分子结构的理解,揭示结构与功能之间的关系。
5.遗传与繁殖:对生物体遗传与繁殖的分子机制的研究,也是现代生物化学与分子生物学研究的一个重要内容。
第一章蛋白质的结构与功能一、氨基酸:1.结构特点:氨基酸(amino acid)是蛋白质分子的基本组成单位。
构成天然蛋白质分子的氨基酸约有20种,除脯氨酸为α-亚氨基酸、甘氨酸不含手性碳原子外,其余氨基酸均为L-α-氨基酸。
2.分类:根据氨基酸的R基团的极性大小可将氨基酸分为四类:①非极性中性氨基酸(8种);②极性中性氨基酸(7种);③酸性氨基酸(Glu和Asp);④碱性氨基酸(Lys、Arg和His)。
二、肽键与肽链:肽键(peptide bond)是指由一分子氨基酸的α-羧基与另一分子氨基酸的α-氨基经脱水而形成的共价键(-CO-NH-)。

生物化学各章知识点总结一、生物化学基本概念1. 生物化学的基本概念生物化学是在分子水平上研究生物体内各种生物分子之间的相互作用和生物体内生物分子的合成、转化和降解规律的一门学科。
生物体内的生物分子包括蛋白质、核酸、碳水化合物、脂类等,它们是生物体内最基本的能量来源和结构组分。
2. 生物大分子的结构和功能(1)蛋白质是生物体内最重要的大分子,是生命活动的基本组成单元,具有结构、酶、携氧、抗体等生物学功能。
(2)核酸是生物体遗传信息的基本载体,包括DNA和RNA两大类,是生物体的遗传物质,具有储存遗传信息和遗传信息传递的功能。
(3)碳水化合物是生物体内最常见的有机化合物,是生物体内能量转化和物质代谢的主要来源。
(4)脂类是生物体内主要的储存能量的物质,还在细胞膜的结构和功能中起重要作用。
二、蛋白质的结构和功能1. 蛋白质的结构(1)蛋白质的结构级别蛋白质的结构级别包括一级结构、二级结构、三级结构和四级结构。
一级结构是指蛋白质的氨基酸序列,二级结构是指蛋白质的α-螺旋、β-折叠等次级结构,三级结构是指蛋白质的立体构象,四级结构是指蛋白质的多肽链之间的相互作用。
(2)蛋白质的构象变化蛋白质的构象包括原生构象、变性构象和热力学稳定性构象。
蛋白质的构象变化直接影响着蛋白质的功能。
2. 蛋白质的功能蛋白质作为生物体内最主要的功能分子,具有结构、酶、携氧、抗体等多种功能。
其中,酶是蛋白质的主要功能之一,是细胞内代谢调节的主要媒介,参与了生物体内几乎所有的代谢过程。
三、酶的性质和功能1. 酶的结构和功能(1)酶的结构酶是一种大分子蛋白质,其结构由氨基酸残基序列决定,具有特定的三级结构和活性位点。
(2)酶的功能酶是生物体内最主要的催化剂,能够加速生物体内化学反应的进行,参与了生物体内的新陈代谢。
2. 酶的性质(1)酶的活性酶的活性受到多种因素的影响,包括温度、pH值、金属离子等。
(2)酶的抑制酶的活性可以被抑制,包括竞争性抑制、非竞争性抑制等。

生物化学知识点总整理生物化学是研究生物体化学组成和生命过程中化学变化规律的一门科学。
它是生命科学领域的重要基础学科,对于理解生命现象、疾病发生机制以及药物研发等方面都具有重要意义。
以下是对生物化学一些重要知识点的总整理。
一、生物大分子1、蛋白质蛋白质的组成:蛋白质由氨基酸通过肽键连接而成。
氨基酸有 20 种,分为必需氨基酸和非必需氨基酸。
蛋白质的结构:包括一级结构(氨基酸的线性排列顺序)、二级结构(如α螺旋、β折叠等)、三级结构(整条肽链的三维空间构象)和四级结构(多个亚基的组合)。
蛋白质的性质:具有两性解离、胶体性质、变性和复性等。
蛋白质的功能:催化、运输、调节、免疫防御、结构支持等。
2、核酸核酸的分类:包括脱氧核糖核酸(DNA)和核糖核酸(RNA)。
DNA 的结构:双螺旋结构,由两条反向平行的多核苷酸链围绕同一中心轴构成。
RNA 的种类:信使 RNA(mRNA)、转运 RNA(tRNA)和核糖体 RNA(rRNA)。
核酸的功能:DNA 是遗传信息的携带者,RNA 参与遗传信息的表达和调控。
3、糖类单糖:如葡萄糖、果糖、半乳糖等,是最简单的糖类。
寡糖:由 2 10 个单糖分子组成,如蔗糖、麦芽糖等。
多糖:包括淀粉、糖原、纤维素等,具有储存能量和构成结构的作用。
4、脂质脂肪:由甘油和脂肪酸组成,是生物体储存能量的重要形式。
磷脂:构成生物膜的重要成分。
固醇:如胆固醇,参与细胞膜的组成和激素的合成。
二、酶1、酶的概念:酶是具有催化作用的生物大分子,大多数是蛋白质。
2、酶的特性:高效性、专一性、可调节性和不稳定性。
3、酶的作用机制:通过降低反应的活化能来加速反应的进行。
4、影响酶活性的因素:温度、pH、底物浓度、酶浓度、抑制剂和激活剂等。
三、生物氧化1、生物氧化的概念:物质在生物体内进行的氧化分解过程,最终生成二氧化碳和水,并释放能量。
2、呼吸链:由一系列电子传递体组成,包括 NADH 呼吸链和FADH2 呼吸链。

(完整版)生物化学知识点重点整理1.生物化学的概述生物化学是研究生物体内化学组成、结构、功能和变化的学科,是生物学和化学的交叉学科。
它研究的内容包括生物大分子(蛋白质、核酸、多糖和脂质)、酶、代谢、信号传导等生物体内的化学过程和物质的转化。
生物化学的研究对于理解生命的机理和病理过程具有重要意义。
2.蛋白质结构与功能蛋白质是生物体中最重要的生化分子之一,它们具有结构多样性和功能多样性。
蛋白质的结构包括四级结构:一级结构是氨基酸的线性序列;二级结构是氨基酸间的氢键形成的α螺旋和β折叠;三级结构是螺旋和折叠的空间结构;四级结构是多个多肽链的组合形成的复合体。
蛋白质的功能包括催化酶活性、调节信号传导、结构支架等。
3.核酸结构与功能核酸是生物体中的遗传物质,包括脱氧核糖核酸(DNA)和核糖核酸(RNA)。
DNA是双螺旋结构,由磷酸二酯键连接的脱氧核苷酸组成。
RNA是单链结构,由磷酸二酯键连接的核苷酸组成。
核酸的功能包括存储遗传信息、传递遗传信息和调控基因表达。
4.代谢与能量转化代谢是生物体内的化学反应过程,包括合成反应和分解反应。
合成反应是通过合成物质来维持生物体的正常生理功能;分解反应是通过分解物质来提供能量。
能量转化是代谢过程中最重要的一环,包括能量的捕获、传递和释放。
生物体通过代谢和能量转化来获取能量、转化能量和维持生命活动。
5.酶的催化机制酶是生物体内催化反应的生物分子,能够加速化学反应的速率,降低反应的活化能。
酶的催化机制包括底物识别、底物结合、酶底物复合物的形成、催化反应和生成产物。
酶的催化过程中涉及到酶活性位点的氨基酸残基和底物之间的相互作用。
6.信号传导与细胞通讯细胞内和细胞间的信号传导是维持生物体内稳态和调节机体功能的重要手段。
信号传导包括外部信号的接受、内部信号的传递和效应的产生。
细胞间的信号传导有兴奋性传导和化学信号传导两种方式。
7.糖的分类与代谢糖是生物体内最重要的能量源,也是合成生物大分子的前体。

第一篇生物大分子的结构与功能第一章氨基酸和蛋白质一、组成蛋白质的20种氨基酸的分类1、非极性氨基酸包括:甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸、脯氨酸2、极性氨基酸极性中性氨基酸:色氨酸、酪氨酸、丝氨酸、半胱氨酸、蛋氨酸、天冬酰胺、谷氨酰胺、苏氨酸酸性氨基酸:天冬氨酸、谷氨酸碱性氨基酸:赖氨酸、精氨酸、组氨酸其中:属于芳香族氨基酸的是:色氨酸、酪氨酸、苯丙氨酸属于亚氨基酸的是:脯氨酸含硫氨基酸包括:半胱氨酸、蛋氨酸注意:在识记时可以只记第一个字,如碱性氨基酸包括:赖精组二、氨基酸的理化性质1、两性解离及等电点氨基酸分子中有游离的氨基和游离的羧基,能与酸或碱类物质结合成盐,故它是一种两性电解质。
在某一PH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性,此时溶液的PH称为该氨基酸的等电点。
2、氨基酸的紫外吸收性质芳香族氨基酸在280nm波长附近有最大的紫外吸收峰,由于大多数蛋白质含有这些氨基酸残基,氨基酸残基数与蛋白质含量成正比,故通过对280nm波长的紫外吸光度的测量可对蛋白质溶液进行定量分析。
3、茚三酮反应氨基酸的氨基与茚三酮水合物反应可生成蓝紫色化合物,此化合物最大吸收峰在570nm波长处。
由于此吸收峰值的大小与氨基酸释放出的氨量成正比,因此可作为氨基酸定量分析方法。
三、肽两分子氨基酸可借一分子所含的氨基与另一分子所带的羧基脱去1分子水缩合成最简单的二肽。
二肽中游离的氨基和羧基继续借脱水作用缩合连成多肽。
10个以内氨基酸连接而成多肽称为寡肽;39个氨基酸残基组成的促肾上腺皮质激素称为多肽;51个氨基酸残基组成的胰岛素归为蛋白质。
多肽连中的自由氨基末端称为N端,自由羧基末端称为C端,命名从N端指向C端。
人体内存在许多具有生物活性的肽,重要的有:谷胱甘肽(GSH):是由谷、半胱和甘氨酸组成的三肽。
半胱氨酸的巯基是该化合物的主要功能基团。
GSH的巯基具有还原性,可作为体内重要的还原剂保护体内蛋白质或酶分子中巯基免被氧化,使蛋白质或酶处于活性状态。

生物化学重点笔记生物化学是一门研究生物体化学组成和生命过程中化学变化的科学。
它是生命科学领域的重要基础学科,对于理解生命现象、疾病发生机制以及药物研发等方面都具有重要意义。
以下是生物化学的一些重点内容:一、蛋白质蛋白质是生物体中最重要的大分子之一,具有多种重要的功能,如催化、结构支持、运输、免疫防御等。
1、氨基酸氨基酸是构成蛋白质的基本单位。
人体中有 20 种常见的氨基酸,它们的结构通式为一个中心碳原子连接着一个氨基、一个羧基、一个氢原子和一个侧链基团。
根据侧链基团的性质,氨基酸可以分为酸性氨基酸、碱性氨基酸、中性氨基酸等。
2、蛋白质的结构蛋白质具有四级结构。
一级结构是指氨基酸通过肽键连接形成的线性多肽链,其序列决定了蛋白质的性质和功能。
二级结构包括α螺旋、β折叠和β转角等,是通过氢键维持的局部构象。
三级结构是多肽链在二级结构的基础上进一步折叠形成的三维结构,主要由疏水相互作用、氢键、离子键和范德华力等维持。
四级结构是指由两条或多条多肽链通过非共价键结合形成的具有特定功能的蛋白质复合物。
3、蛋白质的性质蛋白质具有两性解离、胶体性质、变性和复性等性质。
变性是指蛋白质在某些物理和化学因素的作用下,其空间结构被破坏,导致生物活性丧失。
复性则是指变性的蛋白质在适当条件下恢复其天然构象和生物活性。
二、核酸核酸包括脱氧核糖核酸(DNA)和核糖核酸(RNA),它们是遗传信息的携带者。
1、 DNADNA 是由两条反向平行的脱氧核苷酸链通过碱基互补配对形成的双螺旋结构。
其碱基包括腺嘌呤(A)、鸟嘌呤(G)、胸腺嘧啶(T)和胞嘧啶(C),A 与 T 配对,G 与 C 配对。
DNA 具有自我复制、转录和遗传信息传递等功能。
2、 RNARNA 包括信使 RNA(mRNA)、核糖体 RNA(rRNA)和转运RNA(tRNA)等。
mRNA 是从 DNA 转录而来的,携带遗传信息,指导蛋白质的合成。
rRNA 是核糖体的组成部分,参与蛋白质的合成。
生物化学重点知识归纳第一章绪论1.生物化学的发展过程大致分为三阶段:叙述生物化学、动态生物化学和机能生物化学。
2.生物化学研究的内容大体分为三部分:①生物体的物质组成及生物分子的结构与功能②代谢及其调节③基因表达及其调控第二章糖类化学1.糖类通常根据能否水解以及水解产物情况分为单糖、寡糖和多糖。
2.单糖的分类:①按所含C原子的数目分为:丙糖、丁糖......②按所含羰基的特点分为:醛糖和酮糖。
3.葡萄糖既是生物体内最丰富的单糖,又是许多寡糖和多糖的组成成分。
4.甘油醛是最简单的单糖。
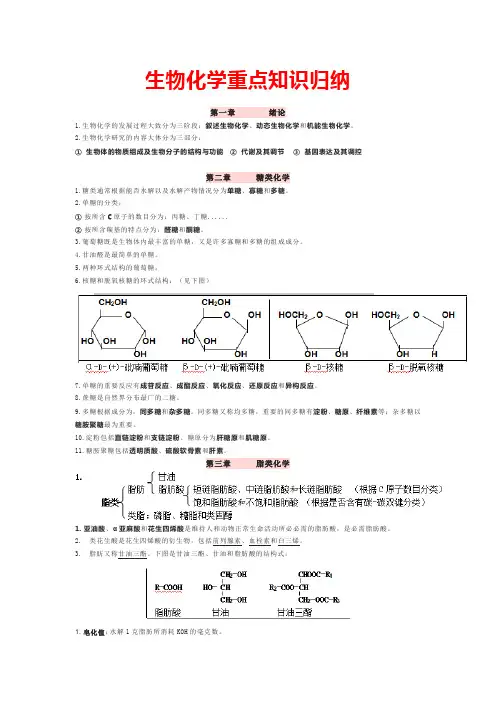
5.两种环式结构的葡萄糖:6.核糖和脱氧核糖的环式结构:(见下图)7.单糖的重要反应有成苷反应、成酯反应、氧化反应、还原反应和异构反应。
8.蔗糖是自然界分布最广的二糖。
9.多糖根据成分为:同多糖和杂多糖。
同多糖又称均多糖,重要的同多糖有淀粉、糖原、纤维素等;杂多糖以糖胺聚糖最为重要。
10.淀粉包括直链淀粉和支链淀粉。
糖原分为肝糖原和肌糖原。
11.糖胺聚糖包括透明质酸、硫酸软骨素和肝素。
第三章脂类化学1. 亚油酸、α亚麻酸和花生四烯酸是维持人和动物正常生命活动所必必需的脂肪酸,是必需脂肪酸。
2. 类花生酸是花生四烯酸的衍生物,包括前列腺素、血栓素和白三烯。
3. 脂肪又称甘油三酯。
下图是甘油三酯、甘油和脂肪酸的结构式:1. 皂化值:水解1克脂肪所消耗KOH的毫克数。
皂化值越大,表示脂肪中脂肪酸的平均分子量越小。
6.磷脂根据所含醇的不同分为甘油磷脂和鞘磷脂。
7.糖脂包括甘油糖脂和鞘糖脂。
8.类固醇是胆固醇及其衍生物,包括胆固醇、胆固醇脂、维生素D、胆汁酸和类固醇激素等。
9.胆汁酸有游离胆汁酸和结合胆汁酸两种形式。
10.类固醇激素包括肾上腺皮质激素(如醛固酮、皮质酮和皮质醇)和性激素(雄激素、雌激素和孕激素)。
11.肾上腺皮质激素具有升高血糖浓度和促进肾脏保钠排钾的作用。
其中皮质醇对血糖的调节作用较强,而对肾脏保钠排钾的作用很弱,所以称为糖皮质激素;醛固酮对水盐平衡的调节作用较强,所以称为盐皮质激素。
生物化学知识点生物化学是研究生物体内分子组成、结构和功能的学科。
其研究内容主要包括生物分子的合成、降解和转化过程,以及生物体内的能量转换、代谢调节和信号传导等方面。
以下是生物化学中的一些重要的知识点。
1. 无机物和有机物:无机物主要包括水、无机盐等,它们是构成生物体的基础物质。
而有机物则包括碳水化合物、脂类、蛋白质和核酸等,它们是构成生物体的重要有机分子。
2. 碳水化合物:碳水化合物是生物体内的重要能源来源,也是细胞壁的主要组成成分。
其中最常见的碳水化合物是葡萄糖,它通过细胞呼吸与氧气反应产生能量。
3. 脂类:脂类是生物体内的重要能源存储物质,它们包括脂肪、磷脂和类固醇等。
脂肪在细胞中形成脂滴,能够存储大量的能量。
磷脂是细胞膜的主要组成分子,它具有双层结构,起到了维持细胞完整性和选择性通透性的作用。
4. 蛋白质:蛋白质是生物体内最重要的有机分子之一,它们是构成细胞的基本结构单位。
蛋白质具有多种功能,包括酶、激素、抗体和传递物质等功能。
蛋白质的结构包括四级结构,即原始结构、二级结构(α-螺旋和β-折叠)、三级结构和四级结构(多个蛋白质链的组装形成的复合物)。
5. 核酸:核酸是生物体内的遗传物质,包括DNA和RNA。
DNA负责储存遗传信息,而RNA负责将DNA的信息转录成蛋白质的氨基酸序列。
核酸的结构是由磷酸、五碳糖和氮碱基组成的。
6. 代谢:代谢是生物体内的一系列化学反应过程,包括合成反应和降解反应。
合成反应是生物体利用外界物质合成新的有机物,降解反应是将有机物分解为小分子并释放能量。
代谢过程是由酶催化的。
7. 酶:酶是生物体内的催化剂,它们能够加速化学反应,但自身不参与反应。
酶可使活化能降低,从而加速反应速率。
酶的活性受到温度、pH值和底物浓度等因素的影响。
8. 能量转换:生物体内的能量转换主要通过细胞呼吸和光合作用实现。
细胞呼吸是将有机物通过氧化反应转化为二氧化碳和水,并释放出能量。
光合作用是植物利用太阳能将二氧化碳和水合成为有机物,并释放出氧气。
生物化学重点笔记生物化学是一门研究生物体化学组成和生命过程中化学变化规律的科学。
它涵盖了广泛的领域,从分子水平理解生命现象,对于医学、农业、食品科学等众多领域都具有重要意义。
以下是一些生物化学的重点知识。
一、蛋白质蛋白质是生物体内最为重要的大分子之一。
(一)结构1、一级结构:指蛋白质多肽链中氨基酸的排列顺序。
通过肽键连接氨基酸,形成线性的链状结构。
2、二级结构:包括α螺旋、β折叠等。
α螺旋是通过氢键维持稳定的右手螺旋结构;β折叠则是伸展的多肽链通过氢键形成的片层结构。
3、三级结构:是指整条多肽链在二级结构的基础上进一步折叠、盘绕形成的三维空间结构。
主要的化学键包括疏水作用、氢键、离子键和范德华力等。
4、四级结构:对于由多条多肽链组成的蛋白质,各条多肽链之间的相对空间位置关系即为四级结构。
(二)功能1、催化功能:如酶。
2、结构支持:如胶原蛋白构成结缔组织。
3、运输功能:如血红蛋白运输氧气。
4、免疫功能:例如抗体。
(三)蛋白质的性质1、两性解离:在不同的 pH 条件下,蛋白质会带上正电荷或负电荷。
2、沉淀反应:通过加入盐、有机溶剂等可使蛋白质沉淀。
3、变性与复性:变性是指蛋白质的空间结构被破坏,丧失活性;在一定条件下,变性的蛋白质有可能复性。
二、核酸核酸包括脱氧核糖核酸(DNA)和核糖核酸(RNA)。
(一)DNA1、结构:双螺旋结构,由两条反向平行的脱氧核苷酸链通过碱基互补配对形成。
2、功能:携带遗传信息,是遗传物质。
3、复制:半保留复制,保证了遗传信息的准确传递。
(二)RNA1、种类:包括信使 RNA(mRNA)、转运 RNA(tRNA)和核糖体 RNA(rRNA)。
2、 mRNA:携带遗传信息,指导蛋白质的合成。
3、 tRNA:在蛋白质合成过程中转运氨基酸。
4、 rRNA:参与核糖体的组成。
三、酶酶是生物体内具有催化作用的蛋白质或 RNA。
(一)特性1、高效性:能显著加快反应速度。
2、专一性:对特定的底物和反应具有高度的选择性。
生物化学的知识知识点梳理生物化学是研究生物体内化学成分、化学反应和化学过程的科学。
它涉及了生命现象中许多重要的基本成分和过程,包括蛋白质、核酸、糖类、脂类、酶、代谢途径等。
以下是生物化学的一些重要知识点的梳理。
1.生物分子:生物分子是指生命体中的化学组分,包括蛋白质、核酸、糖类和脂类。
蛋白质是生命体中最重要的一种生物分子,它们是由氨基酸组成的,具有结构和功能多样性。
核酸包括DNA和RNA,是遗传信息的存储和传递分子。
糖类是能提供能量的生物分子,常见的有单糖、双糖和多糖。
脂类包括甘油三酯、磷脂和类固醇等,它们在细胞膜组成、能量储存和信号传导等方面起着重要作用。
2.酶和酶反应:酶是生物体内催化化学反应的蛋白质分子,可以加速化学反应速率。
酶反应包括酶催化的氧化还原反应、酸碱反应和加成反应等。
酶反应符合酶学的基本原理,包括酶与底物之间的亲和力、酶活性的调节和抑制等。
3.代谢途径:代谢途径是生物体内分子转化的过程,是生物体生命活动的基础。
代谢途径包括葡萄糖代谢、脂肪酸代谢、氨基酸代谢、核酸代谢等。
这些代谢途径通过一系列的酶催化反应组成,产生能量和产物。
4.蛋白质结构和功能:蛋白质的结构包括一级结构、二级结构、三级结构和四级结构。
一级结构是指蛋白质的氨基酸序列,二级结构是指由氢键形成的α螺旋和β折叠,三级结构是指蛋白质在立体空间上的折叠形式,四级结构是由多个蛋白质亚单位组装而成的复合物。
蛋白质的功能包括结构支持、酶催化、运输、传导和免疫等多种生物学过程。
5.DNA结构和遗传信息的传递:DNA是双螺旋结构,由核苷酸组成,包括脱氧核糖和碱基对。
DNA的遗传信息通过碱基对的配对方式来传递,A与T之间形成两个氢键,G与C之间形成三个氢键。
DNA的复制、转录和翻译是生命体遗传信息传递的重要过程。
6.信号转导:信号转导是细胞内外信息的传递过程,涉及到激活和抑制信号通路的多个分子。
信号转导通常发生在细胞膜上的受体和细胞内的信号分子之间,通过级联反应将信号传递到细胞核,从而调控基因转录和细胞功能。
生物化学重点笔记生物化学是研究生物体的化学组成、结构、性质、功能以及生命过程中化学变化规律的一门科学。
它是生命科学领域的重要基础学科,对于理解生命现象、疾病发生机制以及药物研发等都具有重要意义。
以下是为您整理的生物化学重点笔记。
一、蛋白质化学1、蛋白质的组成与结构组成:蛋白质主要由碳、氢、氧、氮、硫等元素组成,其基本组成单位是氨基酸。
结构:蛋白质具有一级结构(氨基酸的排列顺序)、二级结构(如α螺旋、β折叠等)、三级结构(整条肽链的空间构象)和四级结构(多条肽链形成的复合物)。
2、蛋白质的性质两性解离:在一定的 pH 条件下,蛋白质可以解离成带正电荷或负电荷的离子。
胶体性质:蛋白质溶液是一种胶体溶液,具有丁达尔现象、布朗运动等特性。
变性与复性:在某些物理或化学因素作用下,蛋白质的空间结构被破坏,导致其理化性质和生物活性改变,称为变性;变性后的蛋白质在适当条件下可以恢复其原有的空间结构和生物活性,称为复性。
3、蛋白质的分离与纯化沉淀法:如盐析、有机溶剂沉淀等。
层析法:包括凝胶过滤层析、离子交换层析、亲和层析等。
电泳法:如聚丙烯酰胺凝胶电泳、等电聚焦电泳等。
二、核酸化学1、核酸的组成与结构组成:核酸分为脱氧核糖核酸(DNA)和核糖核酸(RNA),它们由核苷酸组成,核苷酸包括碱基、戊糖和磷酸。
结构:DNA 是双螺旋结构,RNA 有单链、双链等多种结构形式。
2、 DNA 的复制与转录DNA 复制:以亲代 DNA 为模板,按照碱基互补配对原则合成子代DNA 的过程。
转录:以 DNA 为模板合成 RNA 的过程。
3、 RNA 的种类与功能mRNA(信使 RNA):携带遗传信息,指导蛋白质合成。
tRNA(转运 RNA):在蛋白质合成中转运氨基酸。
rRNA(核糖体 RNA):参与核糖体的组成。
三、酶1、酶的本质与特性本质:酶是具有催化活性的蛋白质或 RNA。
特性:高效性、专一性、可调节性、不稳定性。
2、酶的催化机制降低反应的活化能:通过形成酶底物复合物,使反应更容易进行。
生物化学知识点总整理生物化学是研究生命体内分子结构、组成及其相互作用的化学学科。
它涵盖了许多重要的生物分子和反应过程,对于理解生命活动的分子基础和生物学功能至关重要。
下面是生物化学的一些重要知识点的总整理。
1.生物大分子:生物体内的大分子包括蛋白质、核酸、多糖和脂质等。
它们是生命的基础,参与了生物体内许多重要的结构和功能。
2.蛋白质:蛋白质是生物体内最重要的大分子之一、它们由氨基酸链组成,具有三级结构:一级结构是氨基酸的线性排列顺序,二级结构是通过氢键和范德华力形成的局部空间结构,三级结构是整个蛋白质折叠成特定的形状。
3.核酸:核酸是生物体内编码和传递遗传信息的分子。
DNA和RNA是两种最重要的核酸。
DNA通过碱基配对和双螺旋结构来存储和传递遗传信息,RNA则参与了蛋白质的合成过程中。
4.酶:酶是生物体内催化化学反应的蛋白质,可以加速反应速率。
酶与底物结合形成复合物,通过降低活化能来促进反应的进行。
5.代谢途径:生物体内的代谢活动通过一系列的化学反应途径进行。
这些途径包括糖酵解、柠檬酸循环、呼吸链和光合作用等。
代谢途径提供能量和合成生物分子所需的原料。
7.柠檬酸循环:柠檬酸循环是将葡萄糖代谢产生的乙酰辅酶A进一步氧化,产生更多的ATP、NADH和FADH28.呼吸链:呼吸链是将NADH和FADH2的电子逐步传递给氧气,生成水,并产生ATP的过程。
它包括细胞色素和膜蛋白等。
9.光合作用:光合作用是植物细胞中通过光能将水和二氧化碳转化为葡萄糖和氧气的过程。
光合作用产生的葡萄糖可以作为能量和碳源。
10.脂质:脂质是不溶于水的有机分子,包括脂肪酸、甘油和脂类等。
脂质在生物体内具有重要的结构和功能,如构成细胞膜、提供能量储存等。
11.生物膜:生物膜是由脂质和蛋白质共同组成的结构,包围着细胞和细胞器。
生物膜具有选择性渗透性,参与了许多生物活动,如物质输运、信号转导等。
12.分子遗传学:分子遗传学研究基因的组成和结构,以及基因的表达调控。
生物化学知识点总结完整版生物化学是研究生物体在细胞、组织和器官水平上的化学过程的一门学科。
它涉及了生命体内物质的合成、降解和转化过程,以及这些过程对生命活动的调控和影响。
生物化学知识点包括了生物分子的结构及功能、生物体内的代谢过程、遗传信息的传递及表达等内容。
下面就对生物化学的一些重要知识点进行总结:一、生物分子的结构和功能1. 蛋白质:蛋白质是生物体内最丰富的一类生物大分子,由氨基酸通过肽键连接而成。
蛋白质在生物体内起着结构支持、酶催化、运输、信号传导等重要功能。
2. 碳水化合物:碳水化合物是生物体内最基本的能量来源,也是构成细胞壁、核酸、多糖等物质的重要成分。
3. 脂类:脂类是生物体内主要的能量储存物质,同时也是细胞膜的主要构成成分。
4. 核酸:核酸是生物体内的遗传物质,包括DNA和RNA两类,它们负责存储遗传信息和传递遗传信息。
二、生物体内的代谢过程1. 糖代谢:糖代谢是生物体内重要的能量来源,包括糖原合成、糖原降解、糖酵解等过程。
2. 脂质代谢:脂质代谢包括脂肪酸的合成、分解和氧化,以及胆固醇的合成和降解。
3. 蛋白质代谢:蛋白质代谢包括蛋白质合成、降解和氨基酸的代谢。
4. 核酸代谢:核酸代谢包括核苷酸的合成和降解过程。
5. 能量代谢:生物体内能量的产生主要依靠有机物的氧化和磷酸化过程。
这些过程包括糖酵解、三羧酸循环和氧化磷酸化等。
三、遗传信息的传递和表达1. DNA的结构和功能:DNA是双螺旋结构,由脱氧核苷酸通过磷酸二酯键连接而成。
DNA负责存储遗传信息,并通过转录和翻译的过程进行表达。
2. RNA的结构和功能:RNA是单链结构,由核糖核苷酸通过磷酸二酯键连接而成。
RNA包括mRNA、tRNA和rRNA等,它们分别参与遗传信息的转录、转运和翻译。
3. 蛋白质合成的过程:蛋白质合成包括转录和翻译两个过程。
转录是指DNA的信息转录成RNA的过程,而翻译是指mRNA上的密码子与tRNA上的反密码子匹配,从而在核糖体上合成蛋白质的过程。
绪论
一、生物化学的的概念: 生物化学(biochemistry)是利用化学的原理与方法去探讨生命的一门科学,它是介于化学、生物学及物理学之间的一门边缘学科。
二、生物化学的发展: 1.叙述生物化学阶段:是生物化学发展的萌芽阶段,其主要的工作是分析和研究生物体的组成成分以及生物体的分泌物和排泄物。 2.动态生物化学阶段:是生物化学蓬勃发展的时期。就在这一时期,人们基本上弄清了生物体内各种主要化学物质的代谢途径。 3.分子生物学阶段:这一阶段的主要研究工作就是探讨各种生物大分子的结构与其功能之间的关系。
三、生物化学研究的主要方面: 1.生物体的物质组成:高等生物体主要由蛋白质、核酸、糖类、脂类以及水、无机盐等组成,此外还含有一些低分子物质。 2.物质代谢:物质代谢的基本过程主要包括三大步骤:消化、吸收→中间代谢→排泄。其中,中间代谢过程是在细胞内进行的,最为复杂的化学变化过程,它包括合成代谢,分解代谢,物质互变,代谢调控,能量代谢几方面的内容。 3.细胞信号转导:细胞内存在多条信号转导途径,而这些途径之间通过一定的方式方式相互交织在一起,从而构成了非常复杂的信号转导网络,调控细胞的代谢、生理活动及生长分化。 4.生物分子的结构与功能:通过对生物大分子结构的理解,揭示结构与功能之间的关系。 5.遗传与繁殖:对生物体遗传与繁殖的分子机制的研究,也是现代生物化学与分子生物学研究的一个重要内容。
四、生物化学的应用 1.农业 2.医药 3.营养 4.临床化学 5.药理学 6.毒理学
第一章 糖 第一节概述 一、定义 糖类(carbohydrate)是一类多元醇的醛衍生物或酮衍生物,或者称为多羟醛或多羟酮的聚合物。实际上糖类包括多羟醛、多羟酮、它们的缩聚物及其衍生物。 二、糖的分类 糖类物质是一大类物质的总称。根据其能否水解和水解后的产物,将糖类分为单糖(monosaccharides)、寡糖(oligosaccharides)、多糖(polysaccharide)。
第二节单糖的化学结构 一、名词解释 不对称碳原子(手性碳原子):连接四个不同原子或基团的碳原子。 镜象异构:两类彼此类似但不等同的,无论怎样放置,都无法叠和的物质,互为镜象。 非镜象异构体:有两个或两个以上不对称碳原子构型不同,它们之间就称为非镜象异构体。 差象异构体:仅一个不对称碳原子构型不同,两镜象非对映体异构物称为差象异构体。 端基异构体(异头物):在构型上,仅头部不同的分子,互为端基异构体。 构型:一个分子由于其中各原子特有的固定的空间排列,而使该分子所具有的特定的立体化学形式。
构象:一个分子中,不改变共价键结构,仅单键周围的原子旋转所产生的原子的空间排布。 D-型:互为镜象异构体的两类化合物,能使平面偏振光发生右旋的,其构型称为D型。 L-型:互为镜象异构体的两类化合物,能使平面偏振光发生左旋的,其构型成为L型。 a异头物和b-异头物: 在环状结构中,半缩醛碳原子也称异头碳原子或异头中心。异头碳的羟基与最末的手性碳原子的羟基具有相同取向的异构体称a异头物,具有相反取向的称b异头物。
醛糖:含醛基的单糖 酮糖:含酮基的单糖 呋喃糖:以五元环形式存在的单糖。 吡喃糖:以六元环形式存在的单糖。 二、单糖的开链结构 单糖分为醛糖和酮糖: 三、 单糖的环状结构 单糖通过半缩醛和半缩酮结构形成环状结构——糖上的一些氢氧根与同一分子上的醛基(或酮基)反应成环。
2. 五个碳原子的D-核糖在40℃的水中形成α-呋喃核糖(6%),β-呋喃核糖(18%),α-吡喃核糖(20%)和β-吡喃核糖(56%)。(呋喃型为五元环;吡喃型为六元环。)
3. D- 果糖,通过半缩酮结构,形成五元和六元环。在溶液中57%是β-D-吡喃果糖,31%是β-D-呋喃果糖,9%是α-D-呋喃果糖,3%是α-D-吡喃果糖,只有一小部分(<<1%)仍保持开链状态。
第三节单糖的理化性质 一、物理性质 1、旋光性一切糖类都有不对称碳原子,都具有旋光性。旋光性是鉴定糖的一个重要指标。 2、甜度各种糖的甜度不一,常以蔗糖的甜度为标准进行比较。 3、溶解度单糖分子中有多个羟基,增加了它的水溶性,尤其在热水中溶解度极大。但不溶于乙醚、丙酮等有机溶剂。
二、化学性质 (1)氧化作用及还原性 单糖含有醛基或酮基,因此具有醛或酮的特性。醛基具有还原性质,能还原许多金属化合物,单糖也具有此特性。
(2)与碱的作用 单糖在碱性溶液种极不稳定,很容易分解。分解的产物常因所用碱的强弱以及浓度的大小而不同。
(3)还原作用 单糖的碳基在一些还原剂(如钠汞齐、硼氢化钠等)的作用下,易被还原成羟基,醛糖被还原成一种糖醇,而酮糖可被还原成两种同分异构的糖醇。
(4)成酯作用 单糖分子具有多个醇性烃基,故具有醇的特性。醇的典型性质是能与酸缩和生成酯。 (5)成苷作用 单糖半缩醛结构上的羟基可与其它含羟基的化合物(如醇、酚等)发生缩和反应而生成缩醛式衍生物,称为糖苷(glycoside)。糖的半缩醛烃基与醇性烃基缩合后所生成的化学键称为糖苷键(glycosidic bond)。
第四节寡糖 一、二糖 1. 蔗糖(α-D-葡萄糖-[1→2]-β-D-果糖) 2. 乳糖,主要存在于各种动物的乳汁中(半乳糖-β[1→4]-葡萄糖) 3. 麦芽糖,麦芽糖的糖苷键是葡萄糖-α[1→4]-葡萄糖。 第五节多糖 可以将多糖分为均一多糖(一种类型单体的聚合物)和不均一多糖(两种或两种以上的糖类单体的聚合物)。
一、均一多糖 (一)糖原 糖原主要存在于动物体内的肝脏(肝糖原)和肌肉(肌糖原)中,以肝中含量多,所以有动物淀粉之称。在动物体中,糖原是储存葡萄糖的主要多糖。糖原是由葡萄糖分子通过以下化学键连接成长链而形成的:1) α-[1→4] 键 2) α-[1→6] 分支,大约一个分支含有8-12个葡萄糖。糖原与碘作用呈现红色,无还原性,没有成脎作用;糖原能溶于水及三氯醋酸,但不溶于乙醇及其其它有机溶剂。
(二)淀粉 淀粉广泛分布于自然界,尤其是在植物的种子(大米、小麦、玉米等)、根茎(马铃薯、红薯)及果实(花生、白果、板栗等)内储存甚多。在植物体中,葡萄糖以淀粉的形式储存。 a. 淀粉有两种形式:直链淀粉和支链淀粉。b.直链淀粉是没有分支的长链,由3000个葡萄糖分子通过α[1→4]糖苷键连接而成。c.支链淀粉的结构与动物的糖原十分相似。由葡萄糖分子通过以下结构连接成长链构成:1) a-[1→4] 键 2)α-[1→6]分支,大约每个分支含有24-30个葡萄糖。3) 典型的就是每个分子中有成百上千的葡萄糖残基存在。3、淀粉的一个重要的性质是与碘的反应,糖淀粉(直链)遇碘产生蓝色,胶淀粉(枝链)遇碘产生紫红色。利用这种颜色反应可以鉴别淀粉。
(三)纤维素 纤维素是构成植物细胞壁和支撑组织的重要成分。纤维素是由一个没有分支的以β[1→4]键相结合的葡萄糖聚合物构成。每个葡萄糖单体之间相应地旋转180°使得氢键在链中连接。链与链之间也有氢键形成。纤维素被纤维素酶水解,纤维素酶由原生动物,细菌(在反刍动物的胃肠道内)和真菌产生。纤维素在性质上与其它糖类的主要区别是在大部分普通溶剂中极其难溶解。例如纤维素不溶于水、稀酸和碱,也不溶于一般的有机溶剂。能与酸成酯。
(四)几丁质 几丁质是构成昆虫和甲壳纲外骨骼的糖类;也构成大部分真菌和藻类的细胞壁。由N-乙酰氨基葡糖的聚合物构成;乙酰基位于葡萄糖环的第二个碳上。相邻线间形成的氢键产生巨大的金属力。
二、不均一多糖 不均一多糖可分为三类:蛋白多糖,肽聚糖和糖蛋白。 1.蛋白多糖是多糖(称为糖胺聚糖)和核蛋白的络合物。糖胺聚糖是没有分支的,重复的二糖单元的聚合物。
2. 肽聚糖由不均一多糖链连上肽形成。存在于细菌的细胞壁中。不均一多糖由N-乙酰胞壁酸和N-乙酰氨基葡糖通过β[1→4]键连接构成。肽的部分是由D型和L型的氨基酸构成的四或五肽。
3.糖蛋白由蛋白质以共价键连接成的低聚糖构成。低聚糖蛋白通常含有1-30个残基,占分子质量的80%或者更多。糖蛋白按化学键类型的分为O-糖蛋白,N-糖蛋白。
第二章脂类 第一节概述 一、定义 脂是一类低溶于水而高溶于非极性溶剂的生物有机分子。对大多数脂质而言,其化学本质是脂肪酸和醇所形成的酯类及其衍生物。
二、分类脂可分成五类: i. 单纯脂 ii. 复合脂 iii. 萜类和类固醇及其衍生物 iv. 衍生脂系 v. 结合脂类 三、生物功能 脂类具有重要的生物功能 ① 供能贮能 ② 构成生物膜 ③ 协助脂溶性维生素的吸收,提供必需脂肪酸 ④ 保护和保温作用。
第二节甘油三酯 一、油和脂的定义 甘油三酯 ( 三脂酰甘油 ) 是植物和动物细胞贮脂 ( depotlipids ) 的主要部分。一般在室温下为液态的称为油( oils ),在室温下为固态的称为脂 ( fats ) ,有时也称为油脂或中性脂。
二、甘油 即 丙三醇 ,因具有甜味而得名。 三、脂肪酸 在高等动植物体内主要存在 12 碳以上的高级脂肪酸;绝大多数含有偶数碳原子,极少含有奇数碳原子。烃链有饱和的,有不饱和的,有的还有取代基(如羟脂酸)。不饱和脂肪酸钟有含 1 个双键的(称为单烯酸),有含 2 个以上双键的(称为多烯酸)。亚油酸( linoleic acid ) 亚麻酸( linolenic acid )是 . 必需脂肪酸。
脂肪酸的简写表示法是先写出碳原子数,再写双键数,最后表明双键的位置。 四、理化性质 油脂的理化性质主要决定于脂肪酸 。脂肪的一个主要的特性是一般不溶于水,而溶于乙醚、 丙酮 、 氯仿 、 石油醚及 四氯化碳 等非极性溶剂。脂肪的熔点取决于所含脂肪酸的成分,脂肪酸都由固定的熔点。动物脂肪 通常含软脂酸和硬脂酸较多,因此在常温下皆呈固态。植物油含有大量的油酸、亚油酸以及其它在常温下为液体的不饱和脂肪酸,因此,植物油在常温下为液体。脂肪虽不溶于水,但在乳化剂作用下,可变成很细小的颗粒,均匀地分散在水里面而形成稳定的乳状液,这个过程叫乳化作用( emulsification )。一切油脂都能被酸、碱和脂肪酶( lipase )所水解,水解的产物是甘油和各种高级脂肪酸。水解作用如在碱性溶液 ( NaOH 或 KOH ) 中进行(为不可逆反应),则产物是甘油和各种高级脂肪酸的盐(钠盐或钾盐),这个过程称为皂化作用( saponification )。不饱和脂肪酸中的双键在适当的温度和催化剂的作用下,可与氢或卤素起加成作用。与卤素的加成作用,称卤化作用( halogenation ) , 与氢加成,称氢化作用( hydrogenation )。天然油脂暴露在空气中相当时间后,就会产生一种刺鼻臭味,称为酸败( rancidity )。 光 、 热 、湿气 会加速油脂的酸败。