热力学第二定律4
- 格式:ppt
- 大小:411.02 KB
- 文档页数:20
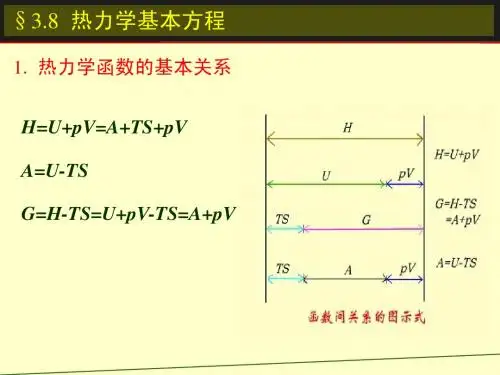

第四章热力学第二定律主要内容:4.1 自发过程及热力学第二定律4.2 卡诺循环与卡诺定理4.3熵的概念4.4Clausius不等式及熵增加原理4.5 熵变的计算及熵的物理意义4.6 热力学第三定律与规定熵4.7 亥姆霍兹能及吉布斯能4.8 热力学基本方程及麦克斯韦关系式4.9吉布斯自由能及温度、压力的关系§4.1 自发过程及热力学第二定律自发过程热力学第二定律1. 自发过程自发过程无需依靠消耗环境的作用(即不借助外力),就能自动进行的过程。
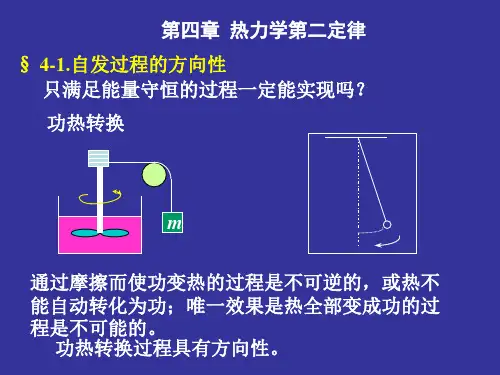
(1) 焦耳热功当量中功自动转变成热;(2) 气体向真空膨胀;(3) 热量从高温物体传入低温物体;(4) 浓度不等的溶液混合均匀;(5) 锌片与硫酸铜的置换反应等,它们的逆过程都不能自动进行。
当借助外力,系统恢复原状后,会给环境留下不可磨灭的影响。
自发过程的特征:1)自发过程总是单向趋于平衡;2)自发过程均具有不可逆性;3)自发过程具有对环境作功的能力,如配有合适的装置,则可从自发过程中获得可用的功。
如:温度传递;气体流动;系统自发过程达到平衡后,无环境作用系统是不可能自动反方向进行并回到原来状态;自发过程的不可逆性是指自然界中所有自发过程都具有热力学的不可逆性;2. 热力学第二定律克劳修斯(Clausius) 的说法:“不可能把热从低温物体传到高温物体,而不引起其它变化。
”—热传导的不可逆性开尔文(Kelvin)的说法:“不可能从单一热源取出热使之完全变为功,而不发生其它的变化。
”—摩擦生热的不可逆性二者说法是等效的,均指明某种自发过程的逆过程是不能自动进行的重要结论: (1)均指明过程的方向性;(2)自发过程存在内在的联系,可以从某一自发过程的不可逆性,便可以推导出其它自发过程的不可逆性。
理解:♦并非“功可以转变为热,而热不能完全变为功”,而是在不引起其它变化的条件下,热才不能完全转变为功。
如:理想气体等温膨胀。
♦第二类永动机:从单一热源吸热使之完全变为功而不留下任何影响。



第4节热力学第二定律【知识梳理与方法突破】1.热力学第二定律的理解(1)“自发地”过程就是不受外来干扰进行的自然过程,在热传递过程中,热量可以自发地从高温物体传到低温物体,却不能自发地从低温物体传到高温物体。
要将热量从低温物体传到高温物体,必须“对外界有影响或有外界的帮助”,就是要有外界对其做功才能完成。
电冰箱就是一例,它是靠电流做功把热量从低温处“搬”到高温处的。
(2)“不产生其他影响”的含义是发生的热力学宏观过程只在本系统内完成,对周围环境不产生热力学方面的影响。
如吸热、放热、做功等。
(3)热力学第二定律的每一种表述都揭示了大量分子参与的宏观过程的方向性。
如机械能可以全部转化为内能,内能却不可能全部转化为机械能而不引起其他变化,进一步揭示了各种有关热的物理过程都具有方向性。
(4)适用条件:只能适用于由很大数目分子所构成的系统及有限范围内的宏观过程。
而不适用于少量的微观体系,也不能把它扩展到无限的宇宙。
(5)热力学第二定律的两种表述是等价的,即一个说法是正确的,另一个说法也必然是正确的;如一个说法是错误的,另一个说法必然是不成立的。
2.热力学第一定律与第二定律的比较项目热力学第一定律热力学第二定律定律揭示的问题它从能量守恒的角度揭示了功、热量和内能改变量三者间的定量关系它指出自然界中出现的宏观过程是有方向性的机械能和内能的转化当摩擦力做功时,机械能可以全部转化为内能内能不可能在不引起其他变化的情况下全部转化为机械能热量的传递热量可以从高温物体自发地传到低温物体说明热量不能自发地从低温物体传到高温物体表述形式只有一种表述形式有多种表述形式联系两定律都是热力学基本定律,分别从不同角度揭示了与热现象有关的物理过程所遵循的规律,二者相互独立,又相互补充,都是热力学的理论基础3.能量耗散的理解(1)各种形式的能最终都转化为内能,流散到周围的环境中,分散在环境中的内能不管数量多么巨大,它也只能使地球、大气稍稍变暖一点,却再也不能自动聚集起来驱动机器做功了。




热力学第二定律四种表述热力学第二定律是热力学中的一条基本原理,它有四种常见的表述方式,分别是:1. 克劳修斯表述:任何热源不可能自发地从低温物体上吸热,然后把热传递给高温物体,而无需外界做功。
热力学第二定律的克劳修斯表述告诉我们,热量是无法从低温环境自发地转移到高温环境的,除非外界做功。
这个表述揭示了自然界中热量传递的偏向性,即热量总是自发地从高温物体传递到低温物体。
2. 开尔文表述:不可能从单一热源吸热使之完全变为有用功而不引起其他变化。
热力学第二定律的开尔文表述强调了热量与功的转换关系。
它告诉我们,无法通过单一热源吸热并将其完全转化为有用的功而不引起其他变化。
这个表述也暗示了热能的一部分必然会以无用的形式散失。
3. 普朗克表述:任何不可逆过程的熵产生必定大于零。
熵是描述系统混乱程度的物理量,热力学第二定律的普朗克表述指出,任何不可逆过程都会导致系统的熵增加,即系统的混乱程度增加。
熵的增加代表能量的分散和无序化,这也是不可逆过程不可逆的原因。
4. 卡诺表述:任何两个温度不同的物体之间,不论通过什么方式和介质,热量传递的效率都不可能达到100%。
热力学第二定律的卡诺表述指出,在两个温度不同的物体之间,无论通过何种方式和介质传递热量,始终无法实现100%的热量传递效率。
这是因为热力学第二定律强调了热量的不可逆性和熵的增加,无法将热量完全转化为有用的功。
这个表述也为卡诺热机的工作原理和效率提供了理论基础。
以上四种表述方式分别从不同的角度描述了热力学第二定律的内容和规律,对于理解能量转换和热传递的基本原理具有重要的指导意义。