高考化学元素周期律的综合复习及答案解析
- 格式:doc
- 大小:1.10 MB
- 文档页数:21

高考化学元素周期律的综合热点考点难点含答案一、元素周期律练习题(含详细答案解析)1.高温下,正硅酸锂(Li 4SiO 4)能与CO 2发生反应,对控制CO 2的排放具有重要的理论意义和实用价值。
完成下列填空:(1)硅原子核外电子占有_____种能量不同的轨道;Li 、C 、Si 的最高价氧化物中,属于原子晶体的是_____。
(2)钠元素的金属性比锂强,用原子结构的知识说明理由_____。
一定温度下,在2L 的密闭容器中,Li 4SiO 4与CO 2发生如下反应:Li 4SiO 4(s)+CO 2(g)Li 2SiO 3(s)+Li 2CO 3(s)。
(3)该反应的平衡常数表达式K=_____,反应20min ,测得容器内固体物质的质量增加了8.8g ,则0~20min 内CO 2的平均反应速率为_____。
(4)在T 1、T 2温度下,恒容容器中c(CO 2)随时间t 的变化关系如图所示。
该反应是_____反应(选填“放热”或“吸热”)。
若T 1温度下,达到平衡时c(CO 2)为amol·L -1,保持其他条件不变,通入一定量的CO 2,重新达到平衡时c(CO 2)为bmol·L -1。
试比较a 、b 的大小,并说明理由_____。
【答案】5 SiO 2 钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ()21c CO 0.005mol·L -1·min -1 放热 a=b ,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b【解析】【分析】【详解】(1)硅是14号元素,基态硅原子的核外电子排布式为1s 22s 22p 63s 23p 2,其核外电子共占有5种能量不同的轨道;Li 、C 、Si 的最高价氧化物分别为Li 2O 、CO 2、SiO 2,Li 2O 是离子晶体、CO 2是分子晶体、SiO 2是原子晶体,故答案为:5;SiO 2;(2) 钠元素的金属性比锂强,从原子结构解释:钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ,故答案为:钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ;(3)平衡常数等于生成物的平衡浓度幂之积除以反应物的平衡浓度幂之积,根据化学反应方程式Li 4SiO 4(s)+CO 2(g)Li 2SiO 3(s)+Li 2CO 3(s),反应物为气体的是二氧化碳,生成物均为固体,则平衡常数()21K=c CO ;反应中固体增加的质量即为消耗的CO 2的质量,反应20min 消耗的CO 2的质量为8.8g ,∆c(CO 2)=8.8g÷44g/mol÷2L=0.1mol·L -1,则0~20min 内CO 2的平均反应速率()()-12-1-12c CO 0.1mol L CO ===0.005mol L min t 20minυ∆⋅⋅⋅∆,故答案为:()21c CO ;0.005mol·L -1·min -1; (4)由图像分析可知,T 1先达到平衡,则温度T 1>T 2,T 2到T 1的过程是升温,c(CO 2)增大,平衡逆向移动,则该反应是放热反应;若T 1温度下,达到平衡时c(CO 2)为amol·L -1,保持其他条件不变,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b ,故答案为:放热;a=b ,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b 。

高考化学压轴题专题元素周期律的经典综合题含详细答案一、元素周期律练习题(含详细答案解析)1.高温下,正硅酸锂(Li 4SiO 4)能与CO 2发生反应,对控制CO 2的排放具有重要的理论意义和实用价值。
完成下列填空:(1)硅原子核外电子占有_____种能量不同的轨道;Li 、C 、Si 的最高价氧化物中,属于原子晶体的是_____。
(2)钠元素的金属性比锂强,用原子结构的知识说明理由_____。
一定温度下,在2L 的密闭容器中,Li 4SiO 4与CO 2发生如下反应:Li 4SiO 4(s)+CO 2(g)Li 2SiO 3(s)+Li 2CO 3(s)。
(3)该反应的平衡常数表达式K=_____,反应20min ,测得容器内固体物质的质量增加了8.8g ,则0~20min 内CO 2的平均反应速率为_____。
(4)在T 1、T 2温度下,恒容容器中c(CO 2)随时间t 的变化关系如图所示。
该反应是_____反应(选填“放热”或“吸热”)。
若T 1温度下,达到平衡时c(CO 2)为amol·L -1,保持其他条件不变,通入一定量的CO 2,重新达到平衡时c(CO 2)为bmol·L -1。
试比较a 、b 的大小,并说明理由_____。
【答案】5 SiO 2 钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ()21c CO 0.005mol·L -1·min -1 放热 a=b ,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b【解析】【分析】【详解】(1)硅是14号元素,基态硅原子的核外电子排布式为1s 22s 22p 63s 23p 2,其核外电子共占有5种能量不同的轨道;Li 、C 、Si 的最高价氧化物分别为Li 2O 、CO 2、SiO 2,Li 2O 是离子晶体、CO 2是分子晶体、SiO 2是原子晶体,故答案为:5;SiO 2;(2) 钠元素的金属性比锂强,从原子结构解释:钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ,故答案为:钠元素和锂元素均为第ⅠA 族元素,Na 原子有3个电子层,Li 原子有2个电子层,原子半径Na>Li ,则原子核对外层电子的吸引能力:Na<Li ,失电子能力:Na>Li ,因此金属性Na 强于Li ;(3)平衡常数等于生成物的平衡浓度幂之积除以反应物的平衡浓度幂之积,根据化学反应方程式Li 4SiO 4(s)+CO 2(g)Li 2SiO 3(s)+Li 2CO 3(s),反应物为气体的是二氧化碳,生成物均为固体,则平衡常数()21K=c CO ;反应中固体增加的质量即为消耗的CO 2的质量,反应20min 消耗的CO 2的质量为8.8g ,∆c(CO 2)=8.8g÷44g/mol÷2L=0.1mol·L -1,则0~20min 内CO 2的平均反应速率()()-12-1-12c CO 0.1mol L CO ===0.005mol L min t 20minυ∆⋅⋅⋅∆,故答案为:()21c CO ;0.005mol·L -1·min -1; (4)由图像分析可知,T 1先达到平衡,则温度T 1>T 2,T 2到T 1的过程是升温,c(CO 2)增大,平衡逆向移动,则该反应是放热反应;若T 1温度下,达到平衡时c(CO 2)为amol·L -1,保持其他条件不变,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b ,故答案为:放热;a=b ,通入一定量的CO 2,平衡会正向进行,但由于温度不变,该反应的平衡常数K=()21c CO 不变,故达到新平衡时c (CO 2)不变,即a=b 。

高考化学综合题专题复习【元素周期律】专题解析附答案解析一、元素周期律练习题(含详细答案解析)1.已知元素X 、Y 均为短周期元素,X 元素的一种核素常用于测文物的年代,Y 元素原子半径是所有原子中最小的,元素X 、Y 可形成两种常见化合物M 和N ,已知M 可以使高锰酸钾酸性溶液褪色,M 分子中所含X 元素的质量是Y 元素质量的6倍,且M 的相对分子质量为56。
N 是一种常用溶剂,它的实验式XY 。
回答下列问题:(1)符合条件的M 的有 ______种。
(2)任意写一种不带支链的M 的结构简式__________。
(3)若在N 与液溴的混合液中加入铁粉可以发生反应(在如图装置a 容器中反应),则:①写出a 容器中发生的所有反应的化学方程式:_____________。
②d 容器中NaOH 溶液的作用是_____________。
(4)在碘水中加入N 振荡静置后的现象是__________。
(5)等质量M 、N 完全燃烧时消耗O 2的物质的量较多的是________(填“M ”或“N ”)。
【答案】3 CH 2=CH -CH 2-CH 3 2Fe +3Br 2=2FeBr 3、+Br 23FeBr −−−→+HBr 吸收HBr 和Br 2,防止污染环境 溶液分层,下层无色,上层紫红色 M【解析】【分析】短周期元素X 元素的一种核素常用于测文物的年代,则X 为碳(C );Y 元素原子半径是所有原子中最小的,则Y 为氢(H )。
元素X 、Y 可形成两种常见化合物M 和N ,已知M 可以使高锰酸钾酸性溶液褪色,M 分子中所含X 元素的质量是Y 元素质量的6倍,且M 的相对分子质量为56,则M 为分子式C 4H 8的烯烃;N 是一种常用溶剂,它的实验式XY ,则N 为苯(C 6H 6)。
【详解】由以上分析可知,M 是分子式为C 4H 8的烯烃,N 是分子式为C 6H 6的苯。
(1)符合条件的M 有CH 2=CHCH 2CH 3、CH 3CH =CHCH 3、(CH 3)2C =CH 2,共3种。
全国高考化学元素周期律的综合高考真题汇总含答案解析一、元素周期律练习题(含详细答案解析)1.下表列出了①~⑩十种元素在周期表中的位置。
族周期ⅠA01①ⅡAⅢAⅣAⅤAⅥAⅦA2②④⑩3⑤⑥⑦③⑧⑨回答下列问题:(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________。
(2)这10种元素中,化学性质最不活泼的元素是_____________(填元素符号,下同),得电子能力最强的原子是__________________,失电子能力最强的单质与水反应的化学方程式是_________________________。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是____________________(填化学式)(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为 ______________________________。
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________。
【答案】 O=C=O Ne O 2Na+2H2O=2NaOH+H2↑ 2HClO4+Na2CO3=CO2↑+2NaClO4 +H2O H2S Al(OH) 3 +OH- = AlO2- +2 H2O H2O(或H2O2) Na2O(或Na2O2或NaH)【解析】【分析】从表中元素所在的位置,可推出①为氢(H),②为碳(C),③为磷(P),④为氧(O),⑤为钠(Na),⑥为镁(Mg),⑦为铝(Al),⑧为硫(S),⑨为氯(Cl),⑩为氖(Ne)。
高考化学元素周期律综合题汇编附详细答案一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF>H 2O >CH 4,最稳定的氢化物是HF ,其结构式为H -F ;(5)②和③按原子数1:2形成的化合物是CO 2,其电子式为:,CO 2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO 2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH ,⑦是Al ,其最高价氧化物的水化物是Al (OH )3,Al (OH )3表现两性,与碱反应的化学方程式为Al (OH )3+NaOH =NaAlO 2+2H 2O 。
高考化学综合题专题复习【元素周期律】专题解析含答案解析一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF>H 2O >CH 4,最稳定的氢化物是HF ,其结构式为H -F ;(5)②和③按原子数1:2形成的化合物是CO 2,其电子式为:,CO 2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO 2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH ,⑦是Al ,其最高价氧化物的水化物是Al (OH )3,Al (OH )3表现两性,与碱反应的化学方程式为Al (OH )3+NaOH =NaAlO 2+2H 2O 。
全国高考化学元素周期律的综合高考真题分类汇总及答案一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF>H2O>CH4,最稳定的氢化物是HF,其结构式为H-F;(5)②和③按原子数1:2形成的化合物是CO2,其电子式为:,CO2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH,⑦是Al,其最高价氧化物的水化物是Al(OH)3,Al(OH)3表现两性,与碱反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O。
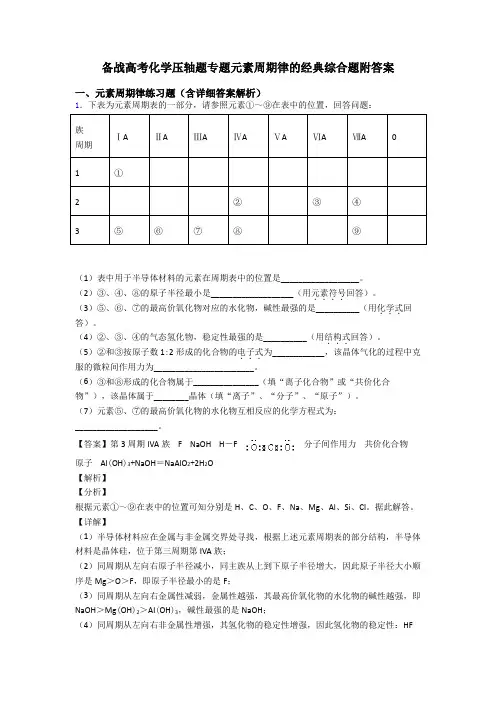
备战高考化学压轴题专题元素周期律的经典综合题附答案一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF>H2O>CH4,最稳定的氢化物是HF,其结构式为H-F;(5)②和③按原子数1:2形成的化合物是CO2,其电子式为:,CO2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH,⑦是Al,其最高价氧化物的水化物是Al(OH)3,Al(OH)3表现两性,与碱反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O。

2020-2021高考化学专题复习元素周期律的综合题含答案一、元素周期律练习题(含详细答案解析)1.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料。
下列叙述不正确的是()A.最高正价由低到高的顺序:Z、W、X、YB.原子半径由大到小的顺序:Z、W、X、YC.Z、W分别与X形成的化合物:均既能与酸又能与碱反应D.简单气态氢化物的稳定性由强到弱的顺序:Y、X、W【答案】A【解析】【分析】X、Y、Z、W原子序数依次增大,Y是至今发现的非金属性最强的元素,Y是F元素;X原子最外层有6个电子,X是O元素;Z在周期表中处于周期序数等于族序数的位置,Z位于第三周期、ⅢA族,Z是Al元素;W的单质广泛用作半导体材料,W是Si元素。
【详解】A.主族元素最高正价等于族序数(O、F除外),F没有正价,故A错误;B.电子层数越多半径越大,电子层数相同,质子数越多半径越小,原子半径由大到小的顺序:Al>Si>O>F,故B正确;C.Al2O3是两性氢氧化物既能与酸又能与碱反应,SiO2是酸性氧化物,能与碱反应生成硅酸盐,SiO2也能与氢氟酸反应生成SiF4气体和水,故C正确;D.非金属性越强,气态氢化物越稳定,简单气态氢化物的稳定性由强到弱的顺序:HF>H2O> SiH4,故D正确;故选A。
【点睛】本题考查元素周期表和元素周期律,熟记元素及其化合物特殊的性质是解题关键,明确氟是至今非金属性最强的元素,无正价,SiO2是酸性氧化物,但能与氢氟酸反应。
2.已知A、B、C、D、E、F均为短周期主族元素,且它们的原子序数依次增大.B和E同主族,A、B在元素周期表中处于相邻的位置,C元素原子在同周期主族元素中原子半径最大,D是地壳中含量最多的金属元素,E元素原子的最外层电子数是电子层数的2倍.请回答下列问题:(1)画出F的原子结构示意图_____。

高考化学压轴题专题复习——元素周期律的综合附答案解析一、元素周期律练习题(含详细答案解析)1.元素周期表是打开物质世界奧秘之门的一把金钥匙,1869年,门捷列夫发现了元素周期律并发表了元素周期表。
下图为元素周期表的一部分,回答下列问题。
(1).上述元素中化学性质最稳定的是________(填元素符号,下同) ,非金属性最强的是_____。
(2)c的最高价氧化物对应水化物的化学式为__________。
(3)h元素的原子结构示意图为__________,写出h单质的一种用途:__________。
(4)b、d、f三种元素原子半径由大到小的顺序是__________(用元素符号表示)。
(5)a、g、j的氢氧化物中碱性最强的是__________(填化学式),写出其溶液与g的氧化物反应的离子方程式:___________________________________。
【答案】Ar F HNO3制光电池 Mg>C>O KOH Al2O3 +2OH-=2AlO2- +H2O【解析】【分析】由元素周期表可知,a为Li、b为C、c为N、d为O、e为F、f为Mg、g为Al、h为Si、i 为Ar、j为K。
【详解】(1)0族元素的化学性质最稳定,故上述元素中化学性质最稳定的是Ar;F元素的非金属性最强;(2)c为N,其最高价氧化物对应的水化物为HNO3;(3)h为Si,核电荷数为14,原子的核外电子数也是14,Si的原子结构示意图为;Si单质的一种用途是可以制光电池;(4)b为C、d为O、f为Mg,当电子层数相同时,核电荷数越大原子半径越小;电子层数越多原子半径越大,故b、d、f三种元素原子半径由大到小的顺序是Mg>C>O;(5)a为Li、g为Al、j为K,K的金属性最强,金属性越强,最高价氧化物对应的水化物的碱性越强,故a、g、j的氢氧化物中碱性最强的是KOH;g的氧化物为Al2O3,Al2O3与KOH溶液反应的离子方程式为Al2O3 +2OH-=2AlO2- +H2O 。

元素周期律1.下列说法正确的是( )A.元素周期表里,主族元素所在的族序数等于原子核外电子数B.F是最活泼非金属,Li是最活泼金属C.元素周期表有7个主族,7个副族,1个0族,1个VIII族,共16纵行D.X2+的核外电子数目为18,则X在第四周期第IIA族【答案】D【解析】A项,主族元素的族序数=最外层电子数,不等于原子核外电子数,故A错误;B项,F为最活泼的非金属性,但同主族从上到下金属性增强,则Li不是最活泼的金属,故B错误;C项,周期表中8、9、10三个纵行为Ⅷ族,则元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共18个纵行,故C错误;D项,X2+的核外电子数目为18,则质子数为18+2=20,为Ca元素,原子结构中含4个电子层、最外层电子数为2,则X在第四周期第ⅧA族,故D正确;故选D。
2.某些含硒(Se)药物能增强人体免疫力。
Se 与S元属素于同主族元素,Se位于S的下一周期,下列说法错误的是( )A.氢化物的稳定性:H2S> H2SeB.晒元素位于第四周期VIA族C.Se2-的结构示意图为D.最高价氧化物对应水化物的酸性:H2SO4<H2SeO4【答案】D【解析】A项,同主族元素从上到下非金属性减弱,非金属性:S>Se,则简单氢化物稳定性:H2S>H2Se,故A正确;B项,Se 与S元属素于同主族元素,Se位于S的下一周期,晒元素位于第四周期VIA族,故B正确;C项,Se原子的核外电子总数为34,最外层得到2个电子形成Se2-,结构示意图为,故C正确;D项,元素的非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性:S>Se,,则最高价氧化物对应水化物的酸性:H2SO4>H2SeO4,故D错误;故选D。
3.(2020·江苏化学卷)下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是( ) A.NaOH的碱性比Mg(OH)2的强B.Cl2得到电子的能力比Br2的弱C.原子半径r:r(Br)>r(Cl)>r(Mg)>r(Na)D.原子的最外层电子数n:n(Na)<n(Mg)<n(Cl)<n(Br)【答案】A【解析】A项,同周期自左至右金属性减弱,所以金属性Na>Mg,则碱性NaOH>Mg(OH)2,故A正确;B项,同主族元素自上而下非金属性减弱,所以非金属性Cl>Br,所以Cl2得电子的能力比Br2强,故B错误;C项,电子层数越多原子半径越大,电子层数相同,核电荷数越小原子半径越大,所以原子半径:r(Br)>r(Na)>r(Mg)>r(Cl),故C错误;D项,Cl和Br为同主族元素,最外层电子数相等,故D错误。
高考化学元素周期律综合经典题附答案解析一、元素周期律练习题(含详细答案解析)1.已知A、B、C、D、E、F均为短周期主族元素,且它们的原子序数依次增大.B和E同主族,A、B在元素周期表中处于相邻的位置,C元素原子在同周期主族元素中原子半径最大,D是地壳中含量最多的金属元素,E元素原子的最外层电子数是电子层数的2倍.请回答下列问题:(1)画出F的原子结构示意图_____。
(2)B、C、E对应简单离子的半径由大到小的顺序为_____(用具体微粒符号表示)。
(3)A的气态氢化物与其最高价氧化物对应水化物反应,生成的化合物属于_____(填“离子化合物”或“共价化合物”)。
(4)加热条件下,B单质与C单质的反应产物的电子式为______。
(5)D元素最高价氧化物对应水化物与C元素最高价氧化物对应水化物的溶液反应的化学方程式为______。
【答案】 S2- > O2-> Na+离子化合物Al(OH)3 + NaOH = NaAlO2 + 2H2O【解析】【分析】A、B、C、D、E、F均为短周期主族元素,且它们的原子序数依次增大,B和E同主族,D 是地壳中含量最多的金属元素,则D为Al元素;E、F原子序数均大于Al,处于第三周期,而E元素原子的最外层电子数是电子层数的2倍,最外层电子数为6,故E为S元素,F为Cl;B和E同主族,则B为O元素;A、B在元素周期表中处于相邻的位置,A为N元素;C元素原子在同周期主族元素中原子半径最大,处于IA族,原子序数介于氧、铝之间,故C为Na,以此分析解答。
【详解】(1)根据上述分析可知:F为Cl元素,原子结构示意图为,故答案:。
(2)根据上述分析可知:B为O元素,C为Na元素,E为S元素,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:S2- > O2-> Na+,故答案为:S2- > O2-> Na+;(3)根据上述分析可知:A为N元素,A的气态氢化物、最高价氧化物对应水化物分别为氨气、硝酸,二者反应生成硝酸铵,属于离子化合物,故答案为:离子化合物;(4)根据上述分析可知:B为O元素,C为Na元素,加热条件下氧气与钠的反应生成Na2O2,含有离子键、共价键,所以电子式为:,故答案:;(5)根据上述分析可知:D为Al元素,C为Na元素。
高考化学元素周期律综合练习题附答案一、元素周期律练习题(含详细答案解析)1.下表列出了①~⑩十种元素在周期表中的位置。
族周期ⅠA01①ⅡAⅢAⅣAⅤAⅥAⅦA2②④⑩3⑤⑥⑦③⑧⑨回答下列问题:(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________。
(2)这10种元素中,化学性质最不活泼的元素是_____________(填元素符号,下同),得电子能力最强的原子是__________________,失电子能力最强的单质与水反应的化学方程式是_________________________。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是____________________(填化学式)(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为 ______________________________。
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________。
【答案】 O=C=O Ne O 2Na+2H2O=2NaOH+H2↑ 2HClO4+Na2CO3=CO2↑+2NaClO4 +H2O H2S Al(OH) 3 +OH- = AlO2- +2 H2O H2O(或H2O2) Na2O(或Na2O2或NaH)【解析】【分析】从表中元素所在的位置,可推出①为氢(H),②为碳(C),③为磷(P),④为氧(O),⑤为钠(Na),⑥为镁(Mg),⑦为铝(Al),⑧为硫(S),⑨为氯(Cl),⑩为氖(Ne)。
元素周期表1.发展历程2.编排原则例1.判断正误,正确的打“√”,错误的打“×”(1)现行元素周期表的编排依据是相对原子质量( )(2)一个横行即是一个周期,一个纵行即是一个族( )(3)最外层电子数相同的元素一定是同族元素( )(4)每一周期都是碱金属元素开始,稀有气体元素结束( ) 答案(1)×(2)×(3)×(4)×3、元素周期表的结构要点解释:常见族的特别名称:第ⅠA族(除氢):碱金属元素;第ⅦA族:卤族元素;0族:稀有气体元素。
点拨:例2.元素周期表中所含元素种类最多的族是哪一族?答案ⅢB族。
例3.现行元素周期表元素种类最多的周期是哪一周期?答案第六周期。
1.结构特点元素名称元素符号核电荷数原子结构示意图最外层电子数电子层数原子半径/nm碱金属元素锂Li 3]1 2 0.152钠Na 11]1 3 0.186钾K 19]1 4 0.227铷Rb 37]1 5 0.248铯Cs 55]1 6 0.265(2)得出结论:碱金属元素原子结构的共同点是最外层电子数均为1,不同点是电子层数和原子半径不同,其变化规律是随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大。
2.碱金属的性质(1)物理性质(2)化学性质2熔成小球,浮于水面,四处游动,有轻熔成小球,浮于水面,四处游动,有“嘶例4.判断正误,正确的打“√”,错误的打“×”(1)碱金属元素原子的次外层电子数都是8个( )(2)化合物中碱金属元素的化合价都为+1价( )(3)碱金属元素的原子半径随核电荷数的增大而增大( )(4)碱金属单质的化学性质活泼,易失电子发生还原反应( )(5)Li在空气中加热生成LiO2( )答案(1)×(2)√(3)√(4)×(5)×例5.钾与水(含酚酞)反应的实验现象能表明钾的一些性质,请连一连。
(1)钾浮在水面上A.钾与水反应放热且钾的熔点较低(2)钾熔化成闪亮的小球B.钾与水反应剧烈,放出的热使生成的H2燃烧(3)钾球四处游动,并有轻,微的爆鸣声C.钾的密度比水小(4)溶液变为红色D.钾与水反应后的溶液呈碱性答案(1)—C (2)—A (3)—B (4)—D例6.下列各组比较不正确的是( )A.锂与水反应不如钠与水反应剧烈B.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠C.熔、沸点:Li>Na>KD.碱性:LiOH<NaOH<KOH答案 B解析锂的活泼性比钠弱,与水反应不如钠剧烈,A正确;还原性:K>Na>Li,但K不能置换出NaCl溶液中的Na,而是先与H2O反应,B错误;碱金属元素从Li到Cs,熔、沸点逐渐降低,即Li>Na>K>Rb>Cs,C正确;从Li到Cs,碱金属元素的金属性逐渐增强,对应最高价氧化物的水化物的碱性依次增强,即碱性:LiOH<NaOH<KOH<RbOH<CsOH,D正确。
元素周期律和元素周期表(精练)完卷时间:50分钟一、选择题(每小题只有一个正确选项,共12*5分)1.(2020年全国统一考试化学试题(新课标Ⅲ))W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。
下列叙述正确的是A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>WC.元素X的含氧酸均为强酸D.Y的氧化物水化物为强碱【答案】D【解析】根据题干信息可知,W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW3与WZ相遇会产生白烟,则WX3为NH3,WZ为HCl,所以W为H元素,X为N元素,Z为Cl元素,又四种元素的核外电子总数满足X+Y=W+Z,则Y的核外电子总数为11,Y为Na元素。
根据上述分析可知,W为H元素,X为N元素,Y 为Na元素,Z为Cl元素,则A.Na为金属元素,非金属性最弱,非金属性Y<Z,A选项错误;B.同周期元素从左至右原子半径依次减小,同主族元素至上而下原子半径依次增大,则原子半径:Na>Cl>N>H,B 选项错误;C.N元素的含氧酸不一定全是强酸,如HNO2为弱酸,C选项错误;D.Y的氧化物水化物为NaOH,属于强碱,D选项正确;答案选D。
2.(北京市2020年普通高中学业水平等级性考试)已知:33As(砷)与P为同族元素。
下列说法不正确的是A.As原子核外最外层有5个电子B.AsH3的电子式是C.热稳定性:AsH3<PH3D.非金属性:As<Cl【答案】B【解析】A.As与P为同族元素,为VA族元素,则其原子核外最外层有5个电子,A说法正确;B.AsH3属于共价化合物,电子式与氨气相似,为,B说法不正确;C.非金属的非金属性越强,其气体氢化物越稳定,非金属性As<P,热稳定性:AsH3<PH3,C说法正确;D.同周期元素,原子序数越小,非金属性越强,非金属性:As<Cl,D说法正确;答案为B。
高考化学压轴题专题复习—元素周期律的综合含答案解析一、元素周期律练习题(含详细答案解析)1.Ⅰ.某化合物A由两种元素组成,可以发生如下的转化。
已知:标准状况下,气体B的密度是氢气的8倍。
请回答:(1)组成A的元素有_________,A的化学式是_________(2)请写出A与NaOH溶液反应的化学方程式_________(3)A可用于金属的冶炼,请写出A与Fe2O3的化学反应方程式_________Ⅱ.某实验小组做了如下实验:请回答:(1)写出硬质管中发生反应的化学方程式:_________(2)有同学认为乙醇的催化氧化反应产物中含有乙酸,请设计实验检验产物成分:_____。
【答案】Al、C Al4C3 Al4C3+4NaOH+4H2O=3CH4↑+4NaAlO2Al4C3+4Fe2O3=2Al2O3+8Fe+3CO2↑ CH3CH2OH+CuO=CH3CHO+Cu+H2O 将产生的气体分别通入两份新制氢氧化铜悬浊液中,标为A、B,对B进行加热,若A沉淀溶解,B出现砖红色沉淀,则既有乙酸也有乙醛;若A沉淀溶解,B无砖红色沉淀,则只有乙酸;若A沉淀不溶解,B出现砖红色沉淀,则只有乙醛【解析】【分析】Ⅰ.已知标准状况下,气体B的密度是氢气的8倍,则气体B的摩尔质量为16g/mol,应为CH4气体,则A中含有C元素,同时A能与氢氧化钠溶液反应,则A中含有Al元素,A为Al4C3,C为NaAlO2,NaAlO2溶液中通入过量二氧化碳得到D为氢氧化铝固体,进一步灼烧得到E为氧化铝,据此分析解答;Ⅱ.(1)乙醇被CuO氧化,反应生成乙醛、铜单质和水;(2)根据乙酸和乙醛与新制氢氧化铜悬浊液反应现象的不同分析比较。
【详解】Ⅰ. (1)由以上分析知,组成A的元素有Al、C,A的化学式是Al4C3,故答案为:Al、C;Al4C3;(2)Al4C3与NaOH溶液反应生成CH4和4NaAlO2,故反应的化学方程式为Al4C3+4NaOH+4H2O=3CH4↑+4NaAlO2;(3)Al4C3可用于金属的冶炼,其与Fe2O3反应生成Al2O3、Fe和CO2,故反应的化学反应方程式为Al4C3+4Fe2O3=2Al2O3+8Fe+3CO2↑;Ⅱ.(1)乙醇被CuO氧化,反应生成乙醛、铜单质和水,反应的化学方程式为CH3CH2OH+CuO=CH3CHO+Cu+H2O;(2)根据乙酸和乙醛性质的区别,可将产生的气体分别通入两份新制氢氧化铜悬浊液中,标为A、B,对B进行加热,若A沉淀溶解,B出现砖红色沉淀,则既有乙酸也有乙醛;若A 沉淀溶解,B无砖红色沉淀,则只有乙酸;若A沉淀不溶解,B出现砖红色沉淀,则只有乙醛。
全国高考化学元素周期律的综合高考模拟和真题分类汇总及答案解析一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF >H2O>CH4,最稳定的氢化物是HF,其结构式为H-F;(5)②和③按原子数1:2形成的化合物是CO2,其电子式为:,CO2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH,⑦是Al,其最高价氧化物的水化物是Al(OH)3,Al(OH)3表现两性,与碱反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O。
高考化学元素周期律的综合复习及答案解析一、元素周期律练习题(含详细答案解析)1.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期1①2②③④3⑤⑥⑦⑧⑨(1)表中用于半导体材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半径最小是___________________(用元素符号....回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是__________(用化学式...回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________(用结构式...回答)。
(5)②和③按原子数1:2形成的化合物的电子式...为____________,该晶体气化的过程中克服的微粒间作用力为_______________________。
(6)③和⑧形成的化合物属于_______________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:___________________。
【答案】第3周期IVA族 F NaOH H-F 分子间作用力共价化合物原子 Al(OH)3+NaOH=NaAlO2+2H2O【解析】【分析】根据元素①~⑨在表中的位置可知分别是H、C、O、F、Na、Mg、Al、Si、Cl。
据此解答。
【详解】(1)半导体材料应在金属与非金属交界处寻找,根据上述元素周期表的部分结构,半导体材料是晶体硅,位于第三周期第IVA族;(2)同周期从左向右原子半径减小,同主族从上到下原子半径增大,因此原子半径大小顺序是Mg>O>F,即原子半径最小的是F;(3)同周期从左向右金属性减弱,金属性越强,其最高价氧化物的水化物的碱性越强,即NaOH>Mg(OH)2>Al(OH)3,碱性最强的是NaOH;(4)同周期从左向右非金属性增强,其氢化物的稳定性增强,因此氢化物的稳定性:HF>H 2O >CH 4,最稳定的氢化物是HF ,其结构式为H -F ;(5)②和③按原子数1:2形成的化合物是CO 2,其电子式为:,CO 2属于分子晶体,熔化时克服分子间作用力;(6)③和⑧构成的化合物是SiO 2,属于共价化合物,其晶体为原子晶体;(7)⑤是钠元素,其最高价氧化物的水化物是NaOH ,⑦是Al ,其最高价氧化物的水化物是Al (OH )3,Al (OH )3表现两性,与碱反应的化学方程式为Al (OH )3+NaOH =NaAlO 2+2H 2O 。
2.已知元素X 、Y 均为短周期元素,X 元素的一种核素常用于测文物的年代,Y 元素原子半径是所有原子中最小的,元素X 、Y 可形成两种常见化合物M 和N ,已知M 可以使高锰酸钾酸性溶液褪色,M 分子中所含X 元素的质量是Y 元素质量的6倍,且M 的相对分子质量为56。
N 是一种常用溶剂,它的实验式XY 。
回答下列问题:(1)符合条件的M 的有 ______种。
(2)任意写一种不带支链的M 的结构简式__________。
(3)若在N 与液溴的混合液中加入铁粉可以发生反应(在如图装置a 容器中反应),则:①写出a 容器中发生的所有反应的化学方程式:_____________。
②d 容器中NaOH 溶液的作用是_____________。
(4)在碘水中加入N 振荡静置后的现象是__________。
(5)等质量M 、N 完全燃烧时消耗O 2的物质的量较多的是________(填“M ”或“N ”)。
【答案】3 CH 2=CH -CH 2-CH 3 2Fe +3Br 2=2FeBr 3、+Br 23FeBr −−−→+HBr 吸收HBr 和Br 2,防止污染环境 溶液分层,下层无色,上层紫红色M【解析】【分析】短周期元素X 元素的一种核素常用于测文物的年代,则X 为碳(C );Y 元素原子半径是所有原子中最小的,则Y 为氢(H )。
元素X 、Y 可形成两种常见化合物M 和N ,已知M 可以使高锰酸钾酸性溶液褪色,M 分子中所含X 元素的质量是Y 元素质量的6倍,且M 的相对分子质量为56,则M 为分子式C 4H 8的烯烃;N 是一种常用溶剂,它的实验式XY ,则N 为苯(C 6H 6)。
【详解】由以上分析可知,M 是分子式为C 4H 8的烯烃,N 是分子式为C 6H 6的苯。
(1)符合条件的M 有CH 2=CHCH 2CH 3、CH 3CH =CHCH 3、(CH 3)2C =CH 2,共3种。
答案为:3;(2)一种不带支链的M 的结构简式为CH 2=CHCH 2CH 3或CH 3CH =CHCH 3。
答案为:CH 2=CHCH 2CH 3或CH 3CH =CHCH 3;(3)①a 容器中,Fe 与Br 2发生反应生成FeBr 3、苯与Br 2在FeBr 3的催化作用下发生反应生成溴苯和溴化氢,发生的所有反应的化学方程式:2Fe +3Br 2=2FeBr 3、+Br 23FeBr −−−→ +HBr 。
答案为:2Fe +3Br 2=2FeBr 3、+Br 23FeBr −−−→ +HBr ;②不管是Br 2(g )还是HBr 都是大气污染物,都应除去,所以d 容器中NaOH 溶液的作用是吸收HBr 和Br 2,防止污染环境。
答案为:吸收HBr 和Br 2,防止污染环境;(4)在碘水中加入苯,由于碘溶于苯、苯难溶于水且密度比水小,所以振荡静置后的现象是溶液分层,下层无色,上层紫红色。
答案为:溶液分层,下层无色,上层紫红色;(5)M 中含氢量高于N 中含氢量,所以等质量M (C 4H 8)、N (C 6H 6)完全燃烧时消耗O 2的物质的量较多的是M 。
答案为:M 。
【点睛】计算耗氧量时,若质量一定,则先将化学式改写碳原子个数为1的最简式,然后比较氢原子数,氢原子数越多,耗氧越多;若物质的量一定,则看化学式,4个氢原子与1个碳原子的耗氧量相同,依据需要可进行互换。
3.元素周期表是打开物质世界奧秘之门的一把金钥匙 ,1869年,门捷列夫发现了元素周期律并发表了元素周期表。
下图为元素周期表的一部分,回答下列问题。
(1).上述元素中化学性质最稳定的是________(填元素符号,下同) ,非金属性最强的是_____。
(2)c 的最高价氧化物对应水化物的化学式为__________。
(3)h 元素的原子结构示意图为__________,写出h 单质的一种用途:__________。
(4)b 、d 、f 三种元素原子半径由大到小的顺序是__________(用元素符号表示)。
(5)a 、g 、j 的氢氧化物中碱性最强的是__________(填化学式),写出其溶液与g 的氧化物反应的离子方程式:___________________________________。
【答案】Ar F HNO 3制光电池 Mg>C>O KOH Al 2O 3 +2OH -=2AlO 2- +H 2O【解析】【分析】由元素周期表可知,a 为Li 、b 为C 、c 为N 、d 为O 、e 为F 、f 为Mg 、g 为Al 、h 为Si 、i为Ar、j为K。
【详解】(1)0族元素的化学性质最稳定,故上述元素中化学性质最稳定的是Ar;F元素的非金属性最强;(2)c为N,其最高价氧化物对应的水化物为HNO3;(3)h为Si,核电荷数为14,原子的核外电子数也是14,Si的原子结构示意图为;Si单质的一种用途是可以制光电池;(4)b为C、d为O、f为Mg,当电子层数相同时,核电荷数越大原子半径越小;电子层数越多原子半径越大,故b、d、f三种元素原子半径由大到小的顺序是Mg>C>O;(5)a为Li、g为Al、j为K,K的金属性最强,金属性越强,最高价氧化物对应的水化物的碱性越强,故a、g、j的氢氧化物中碱性最强的是KOH;g的氧化物为Al2O3,Al2O3与KOH溶液反应的离子方程式为Al2O3 +2OH-=2AlO2- +H2O 。
4.有四种短周期元素,它们的结构、性质等信息如下表所述:元素结构、性质等信息A 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂B B与A同周期,其最高价氧化物的水化物呈两性C元素的气态氢化物极易溶于水,可用作制冷剂D 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂请根据表中信息填写:(1)A原子的核外电子排布式________________.(2)B元素在周期表中的位置____________________;离子半径:B________A(填“大于”或“小于”).(3)C原子的电子排布图是_______________________,其原子核外有___个未成对电子,能量最高的电子为___轨道上的电子,其轨道呈___________形.(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为_______________________________,与D的氢化物的水化物反应的化学方程式为_____________________________.【答案】1s22s22p63s1第三周期第ⅢA族小于 3 2p 哑铃 Al(OH)3+NaOH═NaAlO2+2H2O 3HCl+Al(OH)3═AlCl3+3H2O【解析】【分析】A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂,所以A为Na元素;B与A同周期,其最高价氧化物的水化物呈两性,则B为Al元素;C元素的气态氢化物极易溶于水,可用作制冷剂,则C为N元素;D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,则D为Cl元素,据此回答;【详解】(1)A为钠元素,A原子的核外电子排布式1s22s22p63s1;答案为:1s22s22p63s1;(2)B为铝元素,B元素在周期表中的位置第三周期第ⅢA族,电子层数相同的离子,核电荷数越大,离子半径越小,所以铝离子半径小于钠离子;答案为:第3周期第ⅢA族;小于;(3)C为氮元素,C原子的基态原子的电子排布图是,其原子核外有3个未成对电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃;答案为:;3;2p;哑铃;(4)B为铝元素,A为Na元素,B的最高价氧化物对应的水化物与A的最高价氧化物的水化物反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O;D的氢化物HCl,氯化氢与氢氧化铝反应的离子方程式为:3HCl+Al(OH)3═AlCl3+3H2O;答案为:Al(OH)3+NaOH═NaAlO2+2H2O;3HCl+Al(OH)3═AlCl3+3H2O。