医用有机化学第11章_胺-2011
- 格式:ppt
- 大小:1.55 MB
- 文档页数:59

医用有机化学答案第1章绪论1.5.1什么是有机化合物?什么是有机化学?解:有机化合物是指碳、氢化合物及其衍生物。
仅由碳、氢两种元素组成的有机物称为烃类化合物,若还含有其他元素,则称为烃的衍生物。
有机化学是研究有机物的组成、结构、性质及其相互转化的一门科学。
1.5.2有机化合物的两种分类方法是什么?解:有机化合物一般是按分子基本骨架特征和官能团不同两种方法进行分类。
1.5.3σ键和π键是如何形成的?各自有何特点?解:由两个成键原子轨道向两个原子核间的联线(又称对称轴)方向发生最大重叠所形成的共价键叫σ键;由两个p轨道彼此平行―肩并肩‖重叠所形成的共价键叫π键。
σ键和π键主要的特点存在可以单独存在σ键π键不能单独存在,只与σ键同时存在成键p轨道平行重叠,重叠程度较小①键能小,不稳定;②电子云核约束小,易被极化;③成键的两个原子不能沿键轴自由旋转。
生成成键轨道沿键轴重叠,重叠程度大性质①键能较大,较稳定;②电子云受核约束大,不易极化;③成键的两个原子可沿键轴自由旋转。
1.5.4什么是键长、键角、键能及键的离解能?解:键长是指成键原子核间的平衡距离;键角是指两个共价键之间的夹角;当把一摩尔双原子分子AB(气态)的共价键断裂成A、B两原子(气态)时所需的能量称为A-B键的离解能,也就是它的键能。
但对于多原子分子来说,键能与键的离解能是不同的。
键的离解能的数据是指解离某个特定共价键的键能。
多原子分子中的同类型共价键的键能应该是各个键离解能的平均值。
键能是化学键强度的主要标志之一,在一定程度上反映了键的稳定性,相同类型的键中键能越大,键越稳定。
1.5.5用―部分电荷‖符号表示下列化合物的极性。
(1)CH3Br解:(2)CH3CH2OH(3)CH3O||COCH2CH3δ-O-+||δδC+OCH2CH3δδ+δ-(1)CH3-Br-δ+δδ+(2)CH3CH2-O-H(3)CH31.5.6键的极性和极化性有什么区别?解:极性是由成键原子电负性差异引起的,是分子固有的,是永久性的;键的极化只是在外电场的影响下产生的,是一种暂时现象,当除去外界电场后,就又恢复到原来的状态。
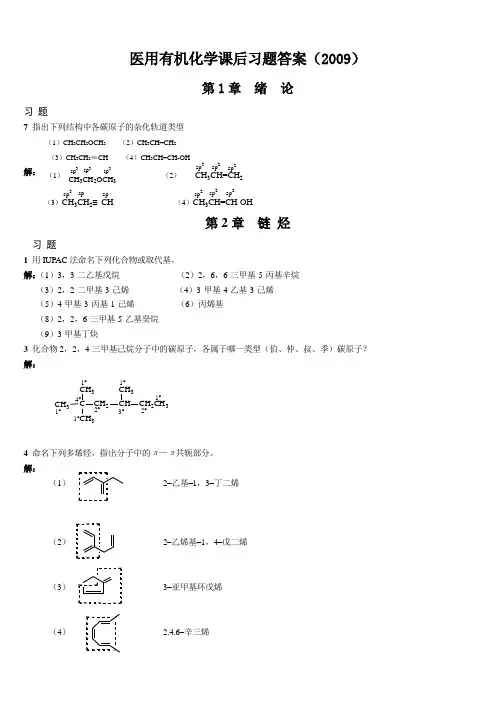
医用有机化学课后习题答案(2009)第1章 绪 论习 题7 指出下列结构中各碳原子的杂化轨道类型(1)CH 3CH 2OCH 3 (2)CH 3CH=CH 2 (3)CH 3CH 2≡CH (4)CH 3CH=CH-OH解:第2章 链 烃习 题1 用IUPAC 法命名下列化合物或取代基。
解:(1)3,3-二乙基戊烷 (2)2,6,6-三甲基-5-丙基辛烷 (3)2,2-二甲基-3-己烯 (4)3-甲基-4-乙基-3-己烯 (5)4-甲基-3-丙基-1-己烯 (6)丙烯基 (8)2,2,6-三甲基-5-乙基癸烷 (9)3-甲基丁炔3 化合物2,2,4-三甲基己烷分子中的碳原子,各属于哪一类型(伯、仲、叔、季)碳原子? 解:CH 3CCH 3CH 3CH 2CHCH 3CH 2CH 31°4°1°2°1°3°2°1°1°4 命名下列多烯烃,指出分子中的π—π共轭部分。
解:(1) 2–乙基–1,3–丁二烯(2) 2–乙烯基–1,4–戊二烯(3) 3–亚甲基环戊烯(4) 2.4.6–辛三烯spsp2sp 3sp 2sp 2spsp 2CH 3CH=CH 2sp 2(1) (2)(3)CH 3CH 2≡CH (4)CH 3CH=CH-OH CH 3CH 2OCH 3sp 3sp3sp 3sp 3(5)5–甲基–1.3–环己二烯(6)4–甲基–2.4–辛二烯9 将下列自由基按稳定性从大到小的次序排列: 解:(3)>(2)>(1)>(4)10 按稳定性增加的顺序排列下列物质,指出最稳定者分子中所含的共轭体系。
解:(1)d >b >c >a (2)d >c >b >a12下列化合物有无顺反异构现象?若有,写出它们的顺反异构体。
解:(1)无 (2)有C=CCH 3HH 2H 5C =CCH 3HHC 2H 5(3)有C =CHC =CH BrCl C 4H 9Br ClC 4H 9(4)有3C =CBrCl HCH 3C =CBr ClH(6)有C =CC 2H 5CH 3C 2H 5CHCH 3CH 3C =CC 2H 5CH 32H 5CHCH 3CH 314 经高锰酸钾氧化后得到下列产物,试写出原烯烃的结构式。

第11章 胺11.1 基本要求● 熟练掌握胺类化合物的结构特点和理化性质。
●掌握重氮化合物、偶氮化合物、酰胺、碳酰胺的化学性质。
11.2 基本知识点11.2.1 胺的分类和命名胺可视作NH 3的烃基衍生物。
NH 3中的一个氢被烃基取代所得的化合物称为伯胺(1°胺),两个氢被烃基取代所得的化合物称为仲胺(2°胺),三个氢被烃基取代所得的化合物称为叔胺(3°胺)。
要注意的是:胺的伯、仲、叔的含义与醇的不同。
相当于NH 4+中的四个氢被烃基取代所得的离子称为季铵离子。
季铵离子与酸根结合形成季铵盐,与OH -结合形成季铵碱。
NH 3 RNH 2 R 2NH R 3N C 6H 5CH 2N(CH 3) 3ClArNH 2 Ar 2NH Ar 3N C 6H 5CH 2N(C 2H 5) 3OH氨 1°胺 2°胺 3°胺 季铵盐、季铵碱命名时,先写出连于氮上的烃基名,然后以胺字作词尾即可。
对于复杂的胺,则可将 H 2N —(称氨基)、RNH —(称烷胺基)、R 2N (称二烷胺基)视作取代基而命名。
11.2.2 胺的结构氮原子的外层电子构型为2s 22p 3,在形成NH 3时氮首先进行不等性sp 3杂化。
氮用三个不等性sp 3杂化轨道与三个氢的s 轨道重叠,形成三个sp 3-s σ键,氮上尚有一对孤对电子占据另一个sp 3杂化轨道,这样便形成具有棱锥形结构的氨分子。
胺类化合物具有类似氨的结构。
甲胺、三甲胺结构如下:在芳香胺中,氮上孤对电子占据的不等性sp 3杂化轨道与苯环π电子轨道重叠,原来属于氮原子的一对孤对电子分布在由氮原子和苯环所组成的共轭体系中,见下图所示。
CH 33具有较多p 轨道性质,但仍具有一定的s 成份³11.2.3 胺的性质 1. 碱性和成盐2. 烃基化3. 酰基化4. Hinsberg 反应(鉴别伯胺、仲胺、叔胺)5. 与HNO 2反应6. 季铵盐的Hoffmann 消去反应RNH 2质子酸盐RNH 2RX R 2NH 3NRX RX4NXArNH RXArNH R2RXRXArNR 3XR 4NO H 3OHRNH 2′R ′COCl 或酐、酯2NCOR ′R ′COCl 或酐、酯R 2NH R 3一)R ′COCl 或酐、酯NaOH 溶液溶于NaOH(RNS O 2Ph )Na(固体)R 2NH PhSO 2Cl R 2NSO 2P hNaOH 溶液不溶于NaOH(固体)R 3N PhSO 2Cl(一)RNH 2PhSO 2ClRNHSO 2P h RNH 2HNO 2[R N N ]H 2ON 醇等混合物ArNH 22Ar N NX (重氮盐)R 2NH HNO 2R 2NN O(N -亚硝基胺)ArNH HNO 2ArN NX (黄色油状物)NNR 2HNO 2ONNR 2(对亚硝基化合物)C C HNR 3OHC CR 3N + H 2O7. 重氮盐的反应 取代反应:偶联反应:还原反应:8. 酰胺和碳酰胺的性质酰胺和碳酰胺除了具有羧酸衍生物的一般性质外,还具有下述性质。

临床等各专业第一学期《医用有机化学》练习试题一、单项选择题26、要使CH2=CHCOOH转变为CH2=CHCH2OH,可以选用下面哪个试剂()A、NaBH4B、LiAlH4C、Pt/H2D、无水ZnCl2 /浓HCl27、下列化合物按酸性强弱排序,正确的是()①丙酸、②β-羟基丙酸、③丙酮酸、④α-羟基丙酸。
A、④>③>②>①B、②>③>④>①C、③>④>②>①D、③>①>④>②28、下列化合物中的碱性顺序从大到小的排列正确的是()a、乙酰胺b、吡咯c、NH3d、二乙胺e、乙胺A、a>b>c>d>eB、d>e>c>a>bC、d>c >e>a>bD、e>d>c>a>b29、能与亚硝酸作用生成难溶于水的黄色油状物的化合物是()A、乙胺B、六氢吡啶C、苄胺D、N,N–二甲基酰胺30、下列化合物发生亲核加成反应,活性从大到小的顺序正确的是()①CH3CH2CHO ②O③C6H5COCH3④BrCH2CHOA、①>②>③>④B、②>①>④>③C、④>①>②>③D、④>①>③>②31、下列化合物发生氨解反应的最快的是()A、丙酰氯B、丙酸酐C、丙酸乙酯D、丙酰胺32、加热脱水生成α,β-不饱和酸的是()A、α-羟基丙酸B、β-羟基丁酸C、γ-羟基丁酸D、δ-羟基戊酸33、根据下列油脂的皂化值确定其平均相对分子质量最小的是( )A、豆油:189~195B、奶油:210~230C、牛油:190~200D、猪油:195~20334、与亚硝酸作用放出氮气的化合物是()A、H2NCONH2B、CH3NHCH2CH3C、C6H5CON(CH3)2D、(CH3)2NCH2CH335、加热后难以形成环酐的是()A、丙二酸B、丁二酸C、戊二酸D、顺丁烯二酸36、下列杂环化合物中没有芳香性的是()A、吡喃B、吡啶C、呋喃D、嘧啶37、关于结构命名正确的是( )A 、α-D-吡喃葡萄糖B 、α-D-吡喃半乳糖C 、β-D-吡喃葡萄糖D 、β-D-吡喃半乳糖38、丙氨酸的等电点pI=6.0,当pH=8.0时,构造式为( )A 、CH 3CHCOOH 2B 、 CH 3CHCOOH NH 3+C 、CH 3CHCOO -2D 、以上都不是39、不能发生酰化反应的是( )A 、 CH 3CH 2NHCH 3B 、 CH 3CH 2N(CH 3)2 40、下列化合物发生亲电反应的活性从大到小的顺序正确的是( )①吡咯 ②苯甲酸 ③苯A 、①>③>②B 、②>①>③C 、②>③>①D 、①>②>③41、下列哪个不是卵磷脂的水解产物 ( )A 、胆胺B 、胆碱C 、丙三醇D 、高级脂肪酸42、下列糖类分子水解可以得到D-果糖的是( )A 、纤维素B 、蔗糖C 、乳糖D 、淀粉43、既能和 FeCl 3 显色,又能发生碘仿反应的是( )H 3COCOCH 3H 3CO CHO CHO HOCOCH 3HO A. B.C. D.44、下列试剂可以鉴别甲醛、丙酮和苯乙酮的是( )A 、过量饱和的NaHSO 3溶液和Tollens 试剂B 、Tollens 试剂和Fehling 试剂C 、Benedict 试剂和Fehling 试剂D 、Tollens 试剂和Benedict 试剂45、加热不发生脱羧反应的是( )A 、 丁酸B 、 -丁酮酸C 、 草酰乙酸D 、 水杨酸二、双项选择题:(有两个正确答案,多选和少选均不给分。





(一)理论教学内容第一章绪论掌握有机化合物及有机化学的概念,有机化合物的特性及其结构理论;共价键的断裂及化学反应类型;有机化合物结构式的写法。
熟悉共价键参数的意义与有机化合物结构的关系;有机化合物的分类。
了解有机化学的发展概况;有机化学与临床医学的关系;学习和研究有机化合物一般步骤和方法。
第二章烷烃掌握烷烃的命名、结构、SP3杂化;一、二、三、四级碳原子和σ键的特征;同分异构现象;烷烃的构象稳定性及取代反应,熟悉烷烃的游离基取代反应历程。
了解游离基的稳定性次序个别烷烃。
第三章烯烃和炔烃掌握烯烃、二烯烃、炔烃的命名和结构;SP2、SP杂化;π键的特点;•烯烃的亲电加成反应、马氏加成规则;诱导效应与共轭效应,π-π键共轭,P-π共轭;共轭二烯烃的加成反应。
第四章环烃掌握脂环的命名,分子结构,环烷烃的取代与开环的反应;苯的结构及芳香性,闭合共轭体系及大Π键,苯环的亲电取代反应及其定位法则,苯同系物的侧链卤代与氧化反应;萜类的定义与分类。
熟悉环完烃的优势构象,a键,e键,环烷烃的稳定性;萘,蒽,菲及环戊烷多氢菲的结构,萘的磺化与加氢反应。
了解十氢化萘的构象,苯及其主要同系物萘、蒽的化学性质。
第五章顺反异构和对映体掌握顺反异构产生的条件,顺/反与Z/E构型的命名法,物质的稳定性与结构的关系。
熟悉手性碳原子,手性分子,D/L和R/S构型命名法。
左旋体,右旋体,内消旋体,外消旋体,对映体,非对映体及比旋光度的概念;Fischer投影式的写法。
了解环己烷二元取代衍生物的顺反异构及构象,分子的对称因素。
第六章卤代烃掌握一卤代烷的亲核取代反应,消除反应,生成格氏试剂的反应SN1•与SN2反应的历程。
熟悉扎依切夫规则,影响亲核取代反应的因素,不同类型卤代烃反应活性规律及与销酸银醇溶液的反应。
了解格氏试剂的用途及个别的卤代烃。
第七章醇,酚,醚掌握醇的命名,分类(伯,仲,叔醇),结构与化学性质(氧化与脱氢,脱水成烯,与无机酸成酯,与卢卡斯试剂反应);酚的结构与化学性质(弱酸性,氧化反应,苯环上的取代反应,与氯化铁的反应)。

医用有机化学教学大纲(供五年制临床医学、口腔、麻醉、护理、影像等本科专业用)一.课程概述《有机化学》是医学院校的一门重要的基础课,适用于临床医学、口腔、麻醉、护理、影像等本科专业教学。
本课程对有机化合物的分类、结构、命名、物理性质和化学性质进行了详细的介绍,对映异构一章介绍了有机化合物的对映异构现象,及构型的表示方法。
并对氨基酸、蛋白质和核酸的结构及理化性质进行了介绍。
使学生学了这门课程后,对有机化学中有机化合物的分子结构、化学性质和基本理论能够掌握。
了解与医学和药学相关的内容。
为后续课程如生物化学、药理学、生物学、卫生化学等理论课奠定基础。
本课程总学时为98学时,理论课48学时,自学讨论14学时,实验课36学时。
二.正文第一章绪论(2学时)目标为系统学习有机化学准备必要的基础知识。
内容有机化学和有机化合物的概念。
有机化学与医学的关系。
有机化合物的结构和特性,碳原子的杂化轨道,共价键的类型,参数,键的极化。
有机反应的类型,有机化合物得分类。
要求能够说明(1)有机化合物的结构和特性;(2)有机化合物的反应类型;(3)有机化合物的分类。
能够概述有机化学和有机化合物。
第二章饱和烃(4学时)目标掌握饱和烃的结构,化学性质和异构现象。
内容饱和烃的结构和命名。
碳链异构、构象异构、环烷烃的结构、分类、命名、环己烷的构象,饱和烃的化学性质。
要求能够说明(1)饱和烃的结构命名;(2)饱和烃的构象异构;(3)饱和烃的化学性质;能够概述乙烷的构象,环己烷的构象。
第三章不饱和烃(4学时)目标掌握不饱和烃的结构,化学性质和异构现象,理解电子效应和反应机理等基础理论。
内容不饱和烃的结构和命名,位置异构,顺反异构。
不饱和烃的物理性质,不饱和烃的化学性质,亲电加成反应机理和电子效应。
要求能够说明(1)不饱和烃的命名;(2)烯烃的异构现象;(3)不饱和烃的亲电加成能够概述不饱和烃的电子效应。
第四章芳香烃(4学时)目标掌握芳香烃的结构命名和化学性质和亲电取代反应机理及定位规律。
