【免费下载】有机立体第三章作业答案
- 格式:pdf
- 大小:464.72 KB
- 文档页数:6

有机化学课后习题参考答案完整版⽬录第⼀章绪论 0第⼆章饱和烃 (1)第三章不饱和烃 (5)第四章环烃 (13)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应⽤ (33)第⼋章醇酚醚 (43)第九章醛、酮、醌 (52)第⼗章羧酸及其衍⽣物 (63)第⼗⼀章取代酸 (71)第⼗⼆章含氮化合物 (78)第⼗三章含硫和含磷有机化合物 (86)第⼗四章碳⽔化合物 (89)第⼗五章氨基酸、多肽与蛋⽩质 (100)第⼗六章类脂化合物 (105)第⼗七章杂环化合物 (114)Fulin 湛师第⼀章绪论1.1扼要归纳典型的以离⼦键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于⽔中所得的溶液与NaBr 及KCl 各1mol 溶于⽔中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在⼀起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么?答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于⽔中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离⼦各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在⽔中是以分⼦状态存在,所以是两组不同的混合物。
1.3碳原⼦核外及氢原⼦核外各有⼏个电⼦?它们是怎样分布的?画出它们的轨道形状。
当四个氢原⼦与⼀个碳原⼦结合成甲烷(CH 4)时,碳原⼦核外有⼏个电⼦是⽤来与氢成键的?画出它们的轨道形状及甲烷分⼦的形状。
答案:C+624H CCH 4中C 中有4个电⼦与氢成键为SP 3杂化轨道,正四⾯体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电⼦式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H H HCC HH HH 或b.H C H c.H N Hd.H S H e.H O NOf.OC H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其⽅向。

思考题2.下列烯类单体适于何种机理聚合?自由基聚合、阳离子聚合还是阴离子聚合?并说明原因。
CH2=CHCl CH2=CCl2CH2=CHCN CH2=C(CN)2CH2=CHCH3CH2=C(CH3)2 CH2=CHC6H5CF2=CF2CH2=C(CN)COOR CH2=C(CH3)-CH=CH2答:CH2=CHCl:适合自由基聚合,Cl原子是吸电子基团,也有共轭效应,但均较弱。
CH2=CCl2:自由基及阴离子聚合,两个吸电子基团。
CH2=CHCN:自由基及阴离子聚合,CN为吸电子基团。
CH2=C(CN)2:阴离子聚合,两个吸电子基团(CN)。
CH2=CHCH3:配位聚合,甲基(CH3)供电性弱。
CH2=CHC6H5:三种机理均可,共轭体系。
CF2=CF2:自由基聚合,对称结构,但氟原子半径小。
CH2=C(CN)COOR:阴离子聚合,取代基为两个吸电子基(CN及COOR)CH2=C(CH3)-CH=CH2:三种机理均可,共轭体系。
3. 下列单体能否进行自由基聚合,并说明原因。
CH2=C(C6H5)2ClCH=CHCl CH2=C(CH3)C2H5CH3CH=CHCH3CH2=CHOCOCH3CH2=C(CH3)COOCH3CH3CH=CHCOOCH3CF2=CFCl答:CH2=C(C6H5)2:不能,两个苯基取代基位阻大小。
ClCH=CHCl:不能,对称结构。
CH2=C(CH3)C2H5:不能,二个推电子基,只能进行阳离子聚合。
CH3CH=CHCH3:不能,结构对称。
CH2=CHOCOCH3:醋酸乙烯酯,能,吸电子基团。
CH2=C(CH3)COOCH3:甲基丙烯酸甲酯,能。
CH3CH=CHCOOCH3:不能,1,2双取代,位阻效应。
CF2=CFCl:能,结构不对称,F原子小。
7.为什么说传统自由基聚合的激励特征是慢引发,快增长,速终止?在聚合过程中,聚合物的聚合度,转化率变化趋势如何?链引发反应是形成单体自由基活性种的反应。
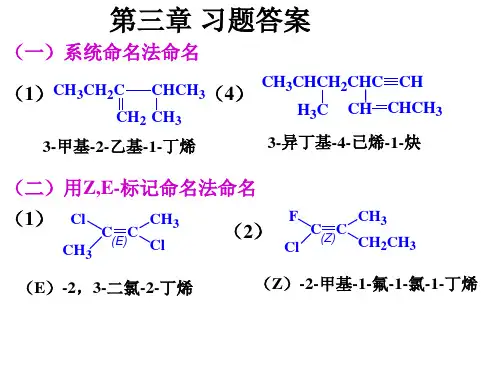


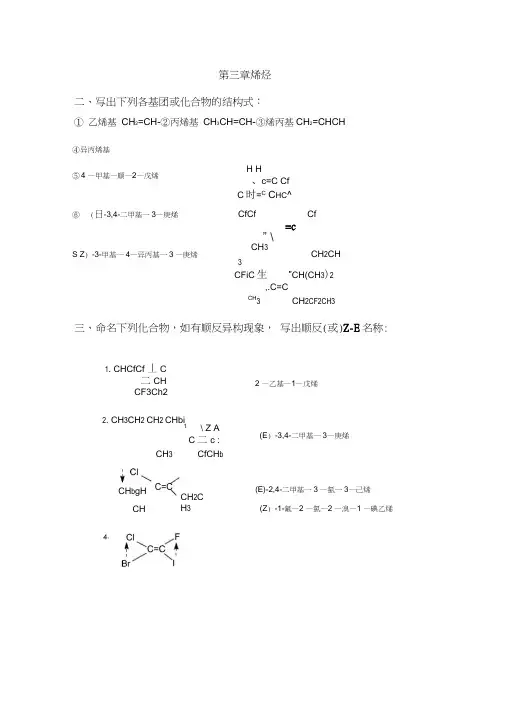
(Z ) -1-氟—2 —氯—2 —溴—1 —碘乙烯第三章烯烃二、写出下列各基团或化合物的结构式:① 乙烯基 CH 2=CH-②丙烯基 CH 3CH=CH-③烯丙基CH 2=CHCH ④ 异丙烯基 ⑤ 4 —甲基—顺—2—戊烯⑥ (日-3,4-二甲基一3—庚烯S Z ) -3-甲基一4—异丙基一3 —庚烯 H H 、c=C CfC 时=C C HC ^ CfCf Cf =c” \CH 3CH 2CH3CFiC 生 ”CH(CH 3)2,.C=CCH3 CH 2CF2CH3三、命名下列化合物,如有顺反异构现象, 写出顺反(或)Z-E 名称:1. CHCfCf 丄 C 二CHCF3Ch2 2 —乙基—1—戊烯2. CH 3CH 2 CH 2 CHbi1\ Z AC 二c : CH 3CfCH b(E ) -3,4-二甲基一3—庚烯CH b gHCH 2C H 3(E)-2,4-二甲基一3 —氯一3—己烯CH3a H <——寸——CXI ——(山L1J )——寸——CXI—a H <——寸——CXI ——(Z L1J )a H <——寸—a H <——寸——CXI ——(山-z)——寸——CXI—<——寸——CXI ——(z-z)a H <——寸——CXI; T一 £0£0\ 八工、_^-0T 0£0£0/ 一 O H O -V A 一 ; £0f t 4S S M S S n «—寸“,wa >——g ——«>H——寸o ——(山) a <——cxl ——础吐—— 9——M •9六、3-甲基-2-戊烯分别在下列条件下发生反应, 写出各反应式的 主要产物:H 2/Pd -CCHCHCHC 2CHHOBr(H 2O +Br 2)CHCH 3CH CCHCHCHC* CCHCH Cl Cl冷稀KMnO 4” CHC 十 CCHCHOH OHCHBHs/NaOHfQ CfC*CHCb€H i ------------------------- OHO 3 ,Zn-CH 3COOHHBr/过氧化物CHC+CHC 2CHBrCHICHCH=CQCh fcBr OH Cl 2低温CHCH 3CHCHCHO +CHCCHCHCH七、乙烯、丙烯、异丁烯在酸催化下与水加成生成的活性中间体分别中间体分别是:CHCf++CHCH CHCH3CH3CCH+中间体稳定性和反应速度顺序为:CHCf+<+CHCH CH <CH3CH b CcH+为:稳定性顺序及反应速度顺序是CH3 C—CH CH3I CH3 1 OH CHCH +ICH-C—CH CHCHCH CHCH-C— CHCH+CH CHH2OCH—p— CHCH+ OHCH CH I ICH-g — CHCHOH八、试以反应历程解释下列反应结果:H +(CH 3)3CCH=C 2H + H Z O ---------------(CH 3) 3CCHC 3H + (CH 3) 2严出的20HOH解:反应历程:严+(CH 3) 3CCH=CH + H ---------CH3-C —CH CH 3 +1H 2O+ CH 3 OH 2H +1f Cf C —fH CH 3CH 3CH化合物:CHCH 二CH + HBr ----------- a CH^HCHBrROORCF 3CH=CH + HBr CHjCfCfBr九、试给出经臭氧化,锌纷水解后生成下列产物的烯烃的结构:「 CfCfCHOHCHO 烯烃为:2.出岀-。

有机化学习题答案第三章第三章有机化学习题答案有机化学是化学领域中的一个重要分支,研究有机化合物的结构、性质和反应。
在学习有机化学的过程中,习题是一种非常有效的学习方法,可以帮助我们巩固知识,提高解决问题的能力。
本文将为大家提供一些有机化学习题的答案,希望能够对大家的学习有所帮助。
1. 以下哪个化合物是醛?A. 丙酮B. 甲醇C. 乙醇D. 丁醛答案:D. 丁醛解析:醛是一类含有羰基(C=O)的有机化合物,丁醛的结构中含有一个羰基,因此是醛。
2. 下列化合物中,哪个是酮?A. 乙醇B. 乙酸C. 丙酮D. 甲醛答案:C. 丙酮解析:酮是一类含有羰基(C=O)的有机化合物,丙酮的结构中含有一个羰基,因此是酮。
3. 以下哪个化合物是醇?A. 乙醇B. 甲醛C. 丙酮D. 乙酸答案:A. 乙醇解析:醇是一类含有羟基(-OH)的有机化合物,乙醇的结构中含有一个羟基,因此是醇。
4. 以下哪个化合物是酸?A. 乙醇B. 甲醛C. 丙酮D. 乙酸答案:D. 乙酸解析:酸是一类能够释放出H+离子的有机化合物,乙酸具有这样的性质,因此是酸。
5. 以下哪个化合物是醚?A. 乙醇B. 甲醛C. 丙酮D. 乙醚答案:D. 乙醚解析:醚是一类含有氧原子连接两个碳原子的有机化合物,乙醚的结构中含有这样的连接,因此是醚。
通过以上习题的解答,我们可以加深对有机化学中不同类别化合物的理解。
在解答习题的过程中,我们需要熟悉有机化合物的命名规则和结构特点,这样才能准确判断化合物的类别。
同时,通过解答习题,我们还可以加深对有机化学反应的理解,了解不同类别化合物的性质和反应规律。
有机化学是一个复杂而又有趣的学科,需要我们不断地学习和实践。
通过解答习题,我们可以提高自己的解决问题的能力,培养逻辑思维和分析问题的能力。
希望大家在学习有机化学的过程中能够善于运用习题,加深对知识的理解,提高学习效果。
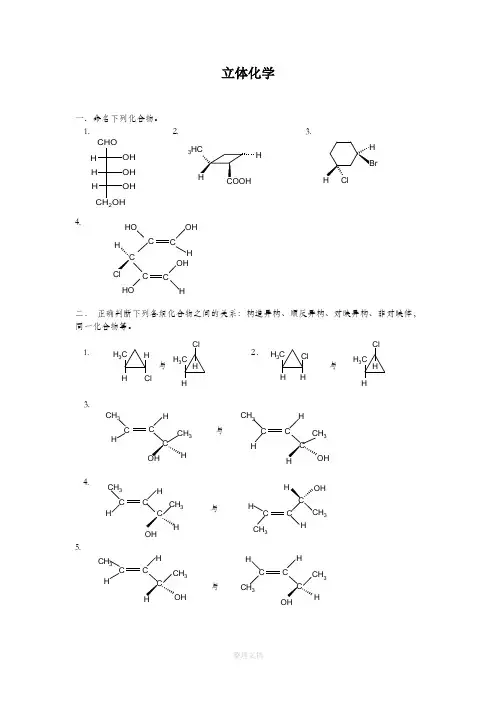
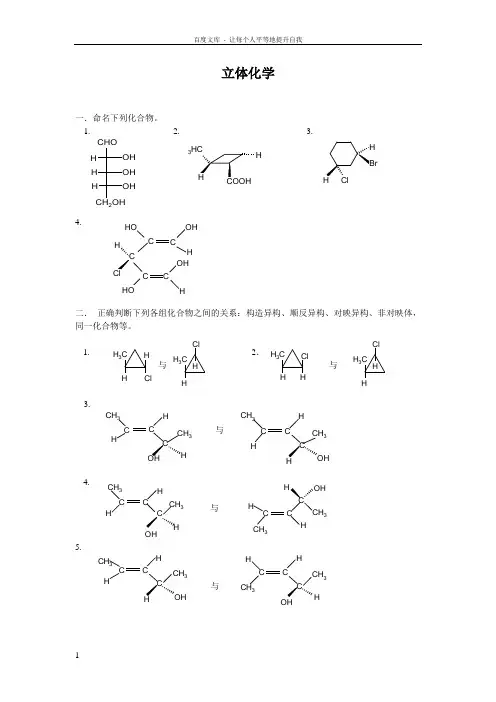
立体化学一.命名下列化合物。
1. 2. 3.4.二. 正确判断下列各组化合物之间的关系:构造异构、顺反异构、对映异构、非对映体,同一化合物等。
1.2. 与 与 3. 与4. 与5.与C CCCH 3HHCH 3HCCC CH 3HHCH 3OHH 3C H HClH 3C H HCl H 3C HH Cl H 3CH HClC CC CH 3H HCH 3HOHC CCCH 3HHCH 3OH C CCCH 3H HCH 3OH CCC CH 3HHCH 3HOH6.与7.与8.与9.与10.与三. 指出下述指定化合物与其他化合物之间的关系(对映体、非对映体或同一化合物)1.与(a)(b)(c) (d)2.与(c)CH3H OHCH=CH2CH3H HBrCl3CH3HH BrCl3CH2OHCH3HO HH OH3332OH2OHC CCH3HHO2OHCH3HOHCH=CH2CH333四.写出下列化合物的三维结构式。
1. (S )-2-羟基丙酸2. (S )—2—氯四氢呋喃3.(2R,3R )—2,3— 二氯丁烷4. (R )—4—甲基—3—氯—1—戊烯5.(1S,2R )—2—氯环戊醇6. (R)—3—氰基环戊酮7.(R )—3—甲基—3—甲氧基—4—己烯—2—酮8.(2E,4S )—4—氘代—2—氟—3—氯—2—戊烯9. (2R,3R )—2—溴—3—戊醇 10. (2S,4R )—4—氨基—2—氯戊酸 11. (S )—2—氯—1,4—环己二酮 12. (1S,3S )—3—甲基环己醇13. (2R,3S )—2—羟基—3—氯丁二酸 14.(2E,4S )—3—乙基—4—溴—2—戊烯 15. (1S,3S,5R )—1—甲基—3—硝基—5—氯环己烷 16. (3S,5R )—3,5—二甲基环己酮五.用Fisher 投影式完成下列题目。
1. 用Fisher 投影式写出3-氯—2—戊醇的所有异构体,并用R/S 标记其构型。
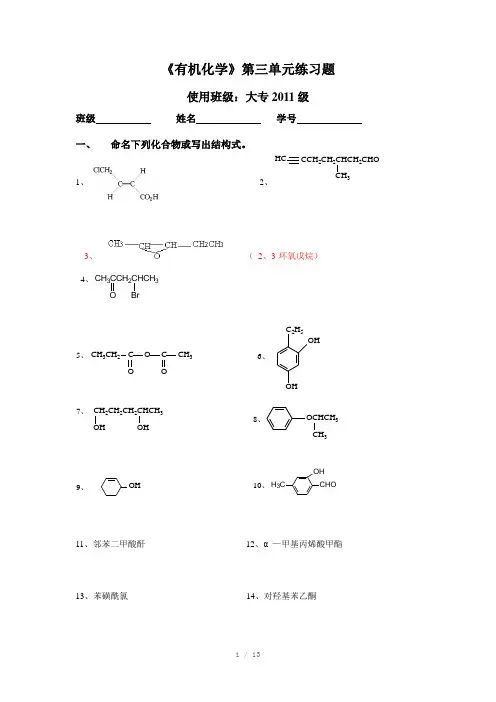
《有机化学》第三单元练习题使用班级:大专2011级班级姓名学号一、命名下列化合物或写出结构式。
1、2、HC CCH2CH2CHCH2CHOCH33、(2、3-环氧戊烷)4、CH3CCH2CHCH3CH3CH2C O CO O CH35、6、OH OHC2H5CH2CH2CH2CHCH3OHOCHCH3CH3 8、7、H3C OH CHO10、9、OH11、邻苯二甲酸酐12、α—甲基丙烯酸甲酯13、苯磺酰氯14、对羟基苯乙酮15、N-甲基-N-乙基乙酰胺16、肉桂酸17、苦味酸 18、仲丁醇19、己二腈 20、β-羟基丁醛二、 完成下列各反应式(把正确答案填在题中括号内)。
( )( )KMnO 4H +( )H 2SO 4浓OH1、CH 3CH 2CH 2CHO稀 HO( )LiAlH 4H 3O +( )2、稀 HO( )( )1)O 32)H 2O/Zn3、4、 + CH 3CH 2COCl( ) ( )( )Zn Hg HCl ,COOH 3( )( )25、6、( )7、() + ( )8、( )CH 3CH 2COClH 2Pd BaSO 4喹啉9、ONaHSO 3( )10、( )( )CH 3CH 2CH 2OH311、HCHO浓( )CHO12、( )OHBr 2213、CH 3COCH 3( ) ( )( ) 14、( )CH 3CH 2CHCH 2O +CH 3CH 2OH15、( )( )HIOCH(CH 3)216、CH 2CH 2CH 2CH 2CHO OHH ( )17、( )OOH C 2H 5( )Br C 2H 5Mg , CO 2 , H 3O +18、KCN① CH 3MgI ② H 2O HBr19、20、CH2CH 2COOC2H 5CH2CH2COOC2H5C2H5ONaH1)2)()OCOOC2H521、22、23、24、三、选择题(从A、B、C、D中选择一个正确答案的序号填在括号内)1、卢卡斯(Lucas)试验可用于下列哪一类化合物的鉴别()。
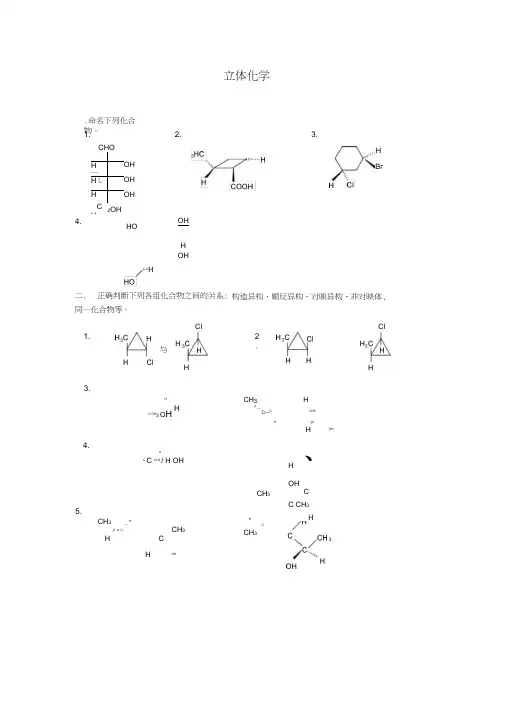
OH H OH二. 正确判断下列各组化合物之间的关系: 同一化合物等。
CH 3H3 _C —CCH3H/CHOHCH 3_ H.C = CCH 3 HC HOH.命名下列化合物。
1.2. 立体化学3.CHOOH H — OH H LHOHC H2OHBrHC CH1.与Cl H H2.Cl3.5.4.HCC CH3 / H OHCH 3H、OHC C CH 3H4.HO构造异构、顺反异构、对映异构、 非对映体, HC CH 3O HHHCCH 332.Cl6.HOH2OH OHCH2OH7.CH2OH HCH38.9. CH 3 CH3CHOHHCH=CH 2HO H CH2OHHCH3CH3CH=CH 2OH10.13111.VHO H(a)OH(c)CH3H I OHHCH3(c) (e) BrHCl HCH3(a)3HO(b)(d)HHCH3(d)CH3CH3HH --------- CH 3H --------- BrCH3三.指出下述指定化合物与其他化合物之间的关系(对映体、非对映体或同一化合物)2.四. 写出下列化合物的三维结构式。
2. ( S )— 2 —氯四氢呋喃4. ( R ) — 4 —甲基一3—氯一1 —戊烯5. ( 1S,2R )— 2 —氯环戊醇6. (R) — 3 —氰基环戊酮7.( R )— 3—甲基一3 —甲氧基一4—己烯一2—酮8. (2E,4S ) 4氘代 2氟 3氯 2戊烯 9. (2R,3R ) —2 —溴一3—戊醇 10. (2S,4R )4氨基2氯戊酸11. (S ) — 2 —氯一1,4 —环己二酮 12. (1S,3S ) —3—甲基环己醇13. (2R,3S )— 2 —羟基一3 —氯丁二酸14. (2E,4S ) — 3乙基 4—溴一2—戊烯15. (1S,3S,5R )— 1 —甲基一3—硝基一 5—氯环己烷16(3S,5R )— 3,5 —二甲基环己酮五. 用Fisher 投影式完成下列题目。
第二章烷烃 p463.写出下列化合物的构造简式:(1) 2,2,3,3-四甲基戊烷(2) 由一个丁基和一个异丙基组成的烷烃:(3) 含一个侧链和分子量为86的烷烃:(4) 分子量为100,同时含有伯,叔,季碳原子的烷烃(5) 3-ethyl-2-methylpentane(6) 2,2,5-trimethyl-4-propylheptane(7) 2,2,4,4-tetramethylhexane(8) 4-tert-butyl-5-methylnonane(1) 2,2,3,3-四甲基戊烷简式:CH3CH2(CH3)2(CH3)3(2) 由一个丁基和一个异丙基组成的烷烃:(3) 含一个侧链和分子量为86的烷烃:因为CnH2n+2=86 所以 n=6该烷烃为 C6H14,含一个支链甲烷的异构体为:(4) 分子量为100,同时含有伯,叔,季碳原子的烷烃(5) 3-ethyl-2-methylpentaneCH3CH(CH3)CH(C2H5)(6) 2,2,5-trimethyl-4-propylheptaneCH3C(CH3)2CH2CH(CH2CH2CH3)CH(CH3)CH2CH3(7) 2,2,4,4-tetramethylhexane(CH3)3CCH2C(CH3)2CH2CH3(8) 4-tert-butyl-5-methylnonaneCH3CH2CH2CH(C(CH3)3)CH(CH3)CH2CH2CH2CH36.(1)把下列三个透视式,写成楔形透视式和纽曼投影式,它们是不是不同的构象呢?HHHFCl ClHHHClCl FHHHFCl Cl(2)把下列两个楔形式,写成锯架透视式和纽曼投影式,它们是不是同一构象?(3)把下列两个纽曼投影式,写成锯架透视式和楔形透视式,它们是不是同一构象?HF F F HHHH FFF H答案:(1)前两者为同一构象,第三者为另一构象FClCl H HHClClFH HHHH HF Cl Cl(2)两者为不同构象H HH HCl ClHHClClClH ClClFHHClHClClH H H(3)两者为不同构象H F H HF FF HFHHF8.试估计下列烷烃按其沸点的高低排列成序(把沸点高的排在前面)(1)2-甲基戊烷(2)正己烷(3)正庚烷(4)十二烷答案:十二烷>正庚烷>正己烷>2-甲基戊烷因为烷烃的沸点随C原子数的增加而升高;同数C原子的烷烃随着支链的增加而下降。
1乙苯在光照下一元溴化的主要产物是2C6H6 (CH3)2CHCH2Cl 主要得到什么产物A.PhCH2CH(CH3)2 B。
PhC(CH3)3C. PhCH(CH3)CH2CH3 D.Ph(C H2)3CH33下列化合物中哪些有芳香性A. ABC B。
ADF C。
BCE D. CDEF4按硝化反应从易到难的成序是A.I > II > III 〉IV B.II〉I 〉III〉IVC。
I 〉II 〉IV>III D. II >I 〉IV > III5(CH3)3CBr与乙醇钠在乙醇溶液中反应,主要产物是()。
A。
(CH3)3COCH2CH3 B.(CH3)2C=CH2 C。
CH3CH=CHCH3 D。
CH3CH2OCH2CH36下列化合物哪个能生成稳定的格氏试剂()。
A. CH3CHClCH2OH B. CH3CH2CH2Br C.H2C=CHCH2Cl D。
CH3COCH2CH2Cl7下列化合物进行SN1反应时,哪一个反应速率最快()。
8化合物(I)和(II)与AgNO3醇溶液反应活性().A。
I>II B.II>IC。
相同 D. 无法比较9按SN1反应,下列化合物的反应活性顺序应是( )。
A.①>②>③>④B。
①>③>④>② C. ③>①>②>④D。
③>②>①>④10用KOH/C2H5OH处理主要产物为( ).A. 反-4-甲基—2—戊烯B。
顺—4-甲基-2-戊烯C。
2-甲基-2-戊烯D.反-2—甲基—2-戊烯11下列化合物进行SN1反应时,哪一个反应速率最快?12下列化合物进行SN2反应时,哪个反应速率最快?13在NaOH水溶液中,(CH3)3CX(I),(CH3)2CHX(II),CH3CH2CH2X(III),CH2=CHX(IV)各卤代烃的反应活性次序为:A。
I>II〉III>IV B。
I>II>IV〉III C. IV>I〉II〉III D. II I>II〉I>IV14(CH3)3CBr与乙醇钠在乙醇溶液中反应主要产物是:A. (CH3)3COCH2CH3 B。
2018-2019学年高中化学第三章有机化合物3.2.2 苯课后作业新人教版必修2编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2018-2019学年高中化学第三章有机化合物3.2.2 苯课后作业新人教版必修2)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2018-2019学年高中化学第三章有机化合物3.2.2 苯课后作业新人教版必修2的全部内容。
3.2.2 苯错误!一、选择题(每小题4分,共48分,每小题只有一个正确选项)1.下列关于苯的说法中,正确的是()A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃B.从苯的凯库勒式()看,苯分子中含有碳碳双键,应属于烯烃C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同2。
下列反应中属于取代反应的是( )A.苯与浓硝酸在浓硫酸作用下共热至50~60℃B.乙烯通入溴水中C.苯与氢气在催化剂作用下反应制得环己烷D.苯与溴水混合后,溴水层褪色3.下列有机物分子中,所有原子不可能处于同一平面的是()A.CH2===CH2(乙烯)B.CH2===CH—CH3(丙烯)4.苯乙烯是一种重要的有机化工原料,其结构简式为,它一般不可能具有的性质是( )A.易溶于水,不易溶于有机溶剂B.在空气中燃烧产生黑烟C.能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色D.能发生加成反应,在一定条件下可与4倍物质的量的氢气加成5.苯乙烯的结构简式为,该物质在一定条件下能和氢气发生完全加成,加成产物的一氯取代物有()A.7种B.6种C.5种D.4种6.已知:CH4+Br2错误!CH3Br+HBr;将甲苯()与液溴混合,加入铁粉,其反应产物可能有( )A.只有①②③ B.只有④⑤⑥⑦C.只有①⑤ D.①②③④⑤⑥⑦7.下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是()①SO2②CH3CH2CH===CH2③④CH3CH3A.①②③④B.③④C.①②④ D.①②8.下列反应中前者属于取代反应,后者属于加成反应的是()A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷C.苯与浓硝酸和浓硫酸的混合液加热反应;乙烯与水在一定条件下生成乙醇的反应D.在苯中滴入溴水,溴水层变无色;乙烯生成聚乙烯的反应9.下列物质中,在一定条件下既能发生加成反应,又能发生取代反应,但不能使酸性KMnO4溶液褪色的是( )A.甲烷 B.苯C.乙烯 D.乙烷10.已知某有机物的结构简式为判断下列说法中不正确的是()A.它可以使酸性KMnO4溶液褪色B.它可以使溴水褪色C.它可与Cl2发生取代反应D.1 mol该有机物燃烧消耗氧气为15 mol答案1.D 从苯的分子式C6H6看,其氢原子数未达饱和,应属不饱和烃,而苯不能使酸性KMnO4溶液褪色,是由于苯分子中的碳碳键是介于单键与双键之间的独特的键;苯的凯库勒式并未反映出苯的真实结构,只是由于习惯而沿用,不能由此来认定苯分子中含有双键,因而苯也不属于烯烃;在催化剂的作用下,苯与液溴反应生成了溴苯,发生的是取代反应而不是加成反应;苯分子为平面正六边形结构,其分子中6个碳原子之间的价键完全相同.2.A 苯与浓硝酸在浓硫酸作用下共热至50~60℃时发生取代反应生成硝基苯;B、C两项都发生加成反应;D项没有发生化学反应,属于物理变化。
有机立体化学课后题1、用邻苯二甲酸酐与1mol乙二醇、1mol丙三醇进行缩聚,用Carothers方程和Flory统计法计算凝胶点。
解:f?*2?1*2?1*?1?1?,pc??2f?1*31*2?1*3,f?3 ?pc?1(1?*1)1/2?2. 等摩尔的乙二醇和对苯二甲酸在280℃下封管内进行缩聚,平衡常数K=4,求最终Xn。
另在排除副产物水的条件下缩聚,欲得Xn?100,问体系中残留水分有多少?解:Xn?11?p??4?K?1?3Xn?11?pKpnwmol/L?Knw?100nw?4*103. 邻苯二甲酸酐与甘油或季戊四醇缩聚,两种基团数相等,试求:a. 平均官能度b. 按Carothers法求凝胶点c. 按统计法求凝胶点解:a、平均官能度: 1)甘油:f?3*2?2*33?22?1? 2)季戊四醇:f?b、 Carothers法: 1)甘油:pc?2*2?4*12f??? ?2)季戊四醇:pc?c、Flory统计法:1)甘油:pc?1[r?r?(f?2)11/2?,r?1,??1,r1,12)季戊四醇:pc?[r?r?(f?2)1/24. 等摩尔二元醇和二元酸缩聚,另加醋酸%,p=或时聚酯的聚合度多少?解:假设二元醇与二元酸的摩尔数各为1mol,则醋酸的摩尔数为。
Na=2mol,Nb=2mol, Nb?'r?NaNb?2Nb,?22?2*?当p=时, Xn?1?r1?r?2rp?12**?当p=时,1?r11?r?2rp1??2**5. 用2mol羟基酸为原料进行缩聚反应,另外加乙酸,如果反应进行到p=时,所得产物的聚合度是多少?r?22?2*?,Xn?1?r1?r?2rp?12**?501. 反应程度:参加反应的官能团与起始官能团总数之比。
转化率:参加反应的单体分子数与初始投料单体分子数之比。
线型缩聚:2官能度单体或2-2体系的单体进行缩聚反应,聚合过程中,分子链线形增长,最终获得线型聚合物的缩聚反应。
思考题
2.下列烯类单体适于何种机理聚合?自由基聚合、阳离子聚合还是阴离子聚合?并说明原因。
CH2=CHCl CH2=CCl2CH2=CHCN CH2=C(CN)2CH2=CHCH3CH2=C(CH3)2 CH2=CHC6H5CF2=CF2CH2=C(CN)COOR CH2=C(CH3)-CH=CH2
答:CH2=CHCl:适合自由基聚合,Cl原子是吸电子基团,也有共轭效应,但均较弱。
CH2=CCl2:自由基及阴离子聚合,两个吸电子基团。
CH2=CHCN:自由基及阴离子聚合,CN为吸电子基团。
CH2=C(CN)2:阴离子聚合,两个吸电子基团(CN)。
CH2=CHCH3:配位聚合,甲基(CH3)供电性弱。
CH2=CHC6H5:三种机理均可,共轭体系。
CF2=CF2:自由基聚合,对称结构,但氟原子半径小。
CH2=C(CN)COOR:阴离子聚合,取代基为两个吸电子基(CN及COOR)
CH2=C(CH3)-CH=CH2:三种机理均可,共轭体系。
3. 下列单体能否进行自由基聚合,并说明原因。
CH2=C(C6H5)2ClCH=CHCl CH2=C(CH3)C2H5CH3CH=CHCH3
CH2=CHOCOCH3CH2=C(CH3)COOCH3CH3CH=CHCOOCH3CF2=CFCl
答:CH2=C(C6H5)2:不能,两个苯基取代基位阻大小。
ClCH=CHCl:不能,对称结构。
CH2=C(CH3)C2H5:不能,二个推电子基,只能进行阳离子聚合。
CH3CH=CHCH3:不能,结构对称。
CH2=CHOCOCH3:醋酸乙烯酯,能,吸电子基团。
CH2=C(CH3)COOCH3:甲基丙烯酸甲酯,能。
CH3CH=CHCOOCH3:不能,1,2双取代,位阻效应。
CF2=CFCl:能,结构不对称,F原子小。
7.为什么说传统自由基聚合的激励特征是慢引发,快增长,速终止?在聚合过程中,聚合物
的聚合度,转化率变化趋势如何?
链引发反应是形成单体自由基活性种的反应。
此反应为吸热反应,活化能高E = 105~150 kJ/mol,故反应速度慢。
链增长反应为放热反应,聚合热约55~95kJ/mol,活化能低,约为20~34 kJ/mol,所以反应速率极高,在0.01~几秒钟内聚合度就可达几千至几万,难以控制。
链终止活化能很低仅8~21kJ/mol,甚至于零,终止速率常数极高,故自由基聚合为速终止。
自由基聚合时,引发剂是在较长时间内逐渐分解释放自由基的,因此单体是逐次与产生
的自由基作用增长的,故转化率随时间延长而逐渐增加。
而对产生的一个活性中心来说,它
值很大,因此瞬间内就可生成高聚物。
因此,从反应一开始
与单体间反应的活化能很低,k
p
有自由基生成时,聚合物分子量就很大,反应过程中任一时刻生成的聚合物分子量相差不大。
9.
13. 推导自由基聚合动力学方程时,作了哪些基本假定?
答:①等活性假定:链自由基的活性与链的长短无关,各步链增长速率常数相等。
②聚合度很大(长链假定):链引发所消耗的单体远小于链增长所消耗的单体。
③稳态假定:自由基的总浓度保持不变,呈稳态。
即自由基的生成速率等于自由基的消耗速率。
17. 动力学链长的定义是什么?与平均聚合度有何关系?链转移反应对动力学链长聚合度有
何影响?试举2-3例说明利用链转移反应来控制聚合度的工业应用,试用链转移常数数值来帮助说明。
答:在自由基聚合中,将一个活性中心由引发开始到活性中心消失期间消耗的单体分子数定义为动力学链长,用ν表示。
它等于链增长反应速率与链引发反应速率之比。
没有链转移时,平均聚合度= ν/(C/2 + D);有链转移时,1/平均聚合度=(C/2 + D)+
C M + C
I
[I]/[M] + C
S
[S]/[M]。
其中,C M、C I、C S分别是向单体、引发剂、溶剂转移的链转移常
数。
链转移反应对动力学链长和平均聚合度具有不同的影响。
链转移反应对动力学链长没有
影响,因为链转移后,动力学链尚未终止,因此动力学链长应该是每个初级自由基自链引发开始到活性中心真正死亡为止所消耗的单体分子数。
但是链转移反应通常使平均聚合度降低。
在实际生产中,常常应用链转移原理控制聚合度,如丁苯橡胶的分子量由十二硫醇来调节,乙烯和丙烯聚合时采用H2作为调节剂,氯乙烯的终止主要是向单体的链转移终止,因此工
业上通过温度来调节VC单体的链转移常数,从而达到调节PVC聚合度的目的。
19. 提高聚合温度和增加引发剂浓度,均可提高聚合速率,问哪一措施更好?
答:提高聚合温度和增加引发剂浓度,均可提高聚合速率,但同时均使聚合度降低。
但提高温度,将使副反应增多,采用引发剂浓度作为调节手段更为有效。
计算题
2.
5.
8.
15.
补充题
1.什么叫链转移反应?有几种形式?链转移反应会引起什么样的结果?
答:链自由基夺取其它分子上的原子,使原来的自由基终止,同时生成一个新的自由基,这种反应称为链转移反应。
链转移的形式包括:向单体、溶剂、引发剂、聚合物、外来试剂的转移反应。
向低分子转移的结果是使聚合物相对分子质量降低。
向大分子转移的结果是形成支链形高分子并且向大分子转移不影响产物的平均分子量,但使得分子量分布变宽。
2.解释引发效率、诱导分解和笼蔽效应。
引发效率:引发剂分解后,只有一部分用来引发单体聚合,将引发聚合部分的引发剂占引
发剂分解或消耗总量的分率称为引发效率,用f表示。
诱导分解:指自由基向引发剂的转移反应,反应结果为自由基总数不变,但白白消耗一个引发剂分子,使f下降。
笼蔽效应:由于聚合体系中引发剂的浓度低,引发剂分解生成的初级自由基处于溶剂分子的包围中,限制了自由基的扩散,导致初级自由基在笼内发生副反应,使f下降。