免疫组织化学及其在病理诊断中的应用共118页
- 格式:ppt
- 大小:10.72 MB
- 文档页数:118

免疫组化检查在病理诊断中得应用及其意义免疫组化就是利用抗原与抗体特异性结合得原理,通过化学反应使标记抗体得显色剂(荧光素、酶、金属离子、同位素) 显色来确定组织细胞内抗原(多肽与蛋白质),对其进行定位、定性及定量得研究,称为免疫组织化学。
免疫组化实验中常用得抗体为单克隆抗体与多克隆抗体。
实验所用主要为组织标本与细胞标本两大类,前者包括石蜡切片(病理大片与组织芯片)与冰冻切片,后者包括组织印片、细胞爬片与细胞涂片。
其中石蜡切片就是制作组织标本最常用、最基本得方法,对于组织形态保存好,且能作连续切片,有利于各种染色对照观察;还能长期存档,供回顾性研究;石蜡切片制作过程对组织内抗原暴露有一定得影响,但可进行抗原修复,就是免疫组化中首选得组织标本制作方法。
石蜡切片标本均用甲醛固定,使得细胞内抗原形成醛键、羧甲键而被封闭了部分抗原决定簇,同时蛋白之间发生交联而使抗原决定簇隐蔽。
所以要求在进行IHC染色时,需要先进行抗原修复或暴露,即将固定时分子之间所形成得交联破坏,而恢复抗原得原有空间形态。
常用得抗原修复方法有微波修复法,高压加热法,酶消化法,水煮加热法等,常用得修复液就是pH6、0得0、01 mol/L得柠檬酸盐缓冲液。
免疫组化常用得染色方法根据标记物得不同分为免疫荧光法,免疫酶标法,亲与组织化学法,后者就是以一种物质对某种组织成分具有高度亲合力为基础得检测方法。
这种方法敏感性更高,有利于微量抗原(抗体)在细胞或亚细胞水平得定位,其中生物素——抗生物素染色法最常用。
一、病理外检中常用抗体标记上皮类标记AE1/AE3最常用,胞浆阳性着色,细丝状,与低、中分子量角蛋白反应,肝细胞为阴性,而胆管细胞阳性,用于确定肿瘤为上皮源性;CAM5、2胞浆阳性着色,细丝状,包含CK8 与CK18,主要染色神经内分泌细胞与腺上皮,正常鳞状上皮阴性,用于染小细胞癌、胸腺瘤与梭形细胞癌、肝细胞癌:AE1/AE3 CAM5、2 (+),用于乳腺外得Paget’s病;CK34BE胞浆阳性着色,鳞状上皮与鳞状细胞癌阳性,用于染前列腺得基底层细胞,鉴别浸润癌,染涎腺肿瘤得肌上皮,用于染Mallory小体;EMA细胞膜/细胞浆阳性着色,上皮标记得替代品,浆细胞阳性,很好得内对照,用于染滑膜肉瘤、大细胞分化不良性淋巴瘤、L&H 富于淋巴细胞得结节状何杰金、脑膜瘤EMA(+)AE1/AE3(–)、浆细胞瘤;CK7与CK20胞浆阳性着色,两者联合应用可鉴别很多种癌得原发部位,CK7 常常在胃肠道得癌为阴性,CK20 只有胃肠道癌与Merkel 细胞癌阳性。


一、概述乳腺癌是女性常见的恶性肿瘤之一,在世界范围内造成了许多妇女的生命威胁。
乳腺癌的发生和发展与免疫系统紧密相关,因此免疫组织化学在乳腺病理学中的应用显得尤为重要。
在乳腺病理学中,免疫组织化学可以用于鉴定生物标志物、评估肿瘤的分子亚型、判断预后以及指导靶向治疗等方面。
目前,关于免疫组织化学在乳腺病理学中的应用尚没有达成一致的共识,本文旨在探讨免疫组织化学在乳腺病理学中的应用的共识,并提出相应的建议。
二、免疫组织化学在乳腺病理学中的应用概况1. 乳腺癌标志物的鉴定免疫组织化学可以用于鉴定乳腺癌的生物标志物,如雌激素受体(ER)、孕激素受体(PR)、人表皮生长因子受体2(HER2)、Ki-67等。
这对于确定乳腺癌的分子亚型、指导临床治疗具有重要意义。
2. 评估肿瘤的分子亚型免疫组织化学可以帮助鉴定乳腺癌的分子亚型,如激素受体阳性/HER2阴性型、三阴性型等。
不同分子亚型的乳腺癌具有不同的生物学行为和预后,因此对肿瘤分子亚型的准确评估对于指导临床治疗至关重要。
3. 判断乳腺癌的预后免疫组织化学可以评估乳腺癌的预后因素,如Ki-67的表达水平与预后的相关性。
通过免疫组织化学检测,可以及时发现高危患者,为临床预后评估和治疗提供参考依据。
4. 指导靶向治疗免疫组织化学可以帮助评估乳腺癌患者对于靶向治疗的应答情况,如HER2阳性患者对于Trastuzumab治疗的应答情况。
这有助于个体化治疗方案的制定和优化治疗效果。
三、免疫组织化学在乳腺病理学中的应用存在的问题和挑战1. 方法标准尚不一致目前,关于乳腺病理免疫组织化学检测的方法标准尚不一致,不同的实验室和医院可能采用不同的操作流程和标准,这可能会影响检测结果的准确性和可比性。
2. 生物标志物的解释存在争议针对乳腺癌生物标志物的解释存在争议,如在ER和PR的阳性定义标准、HER2的表达标准等方面。
这导致了不同实验室和医院对于生物标志物的诊断结果存在差异,这对于临床诊断和治疗带来了一定困扰。

免疫组化在临床诊断中的应用在临床病理诊断中,免疫组织化学(IHe)是一种很重要的技术和手段,从20世纪70年代开始,免疫组化技术就应用于病理诊断,对于诊断肿瘤、肿瘤分类、判断预后产生了巨大的影响,同时也扩展了人们对于各种疾病及肿瘤形成过程的认识,提高了病理诊断与研究水平。
但是,随着免疫组化的广泛应用,发现免疫组化技术存在一些局限性。
深入研究免疫组化原理和技术,必须熟悉各种抗体真阳性反应部位,实现实验室间免疫组化标准化,使免疫组化在病理诊断中发挥最大的辅助作用。
在病理诊断中,随着各种抗体新的用途不断被发现及越来越多的新型抗体的出现,免疫组化在肿瘤诊断及鉴别诊断、分类、预后判断等方面产生了重大的影响。
由于免疫组化技术也存在一些局限性,因此,深入研究免疫组化原理和技术,并努力实现规范化的操作,才能充分发挥免疫组化在病理的诊断及鉴别诊断、判断预后、指导临床治疗中的作用。
1.免疫组化技术观察组织切片中抗原的数量及其在组织中的分布情况,对抗原进行定位、定性及定量的研究,称为免疫组织化学,由于抗原与抗体特异性结合,因此通过免疫组化使标记抗体的显色剂(酶、荧光素、同位素、金属离子等等)显色来确定组织细胞内抗原(多肽和蛋白质)。
IHC所用标本主要为两大类:组织标本和细胞标本,其中制作组织标本最常用、最基本的方法是石蜡切片。
石蜡切片对于组织形态保存好,有利于各种染色对照观察,而且能长期保存;石蜡切片中使用的甲醛固定剂对组织内抗原暴露有一定的影响,但可进行抗原修复,是免疫组化中首选的组织标本制作方法。
2.免疫组化技术在临床诊断中的作用目前免疫组化技术应用于临床主要有以下几个方面:2.1肿瘤良恶性的判断对于反应性增生还是肿瘤性增生,可用免疫球蛋白(Ig)的轻链抗体检测B淋巴细胞增生的单克隆或多克隆性来区别。
在滤泡反应性增生时,滤泡反应中心的细胞不表达细胞凋亡蛋白(bc1-2),be1-2阴性;而在滤泡性淋巴瘤中,由于90%以上肿瘤性滤泡细胞有bc1-2的高表达,bc1-2阳性。



免疫组织化学检测在乳腺病理诊断中的价值1. 免疫组织化学检测在乳腺癌诊断中的应用乳腺癌是乳腺组织恶性病变的一种,具有高度异质性和侵袭性。
免疫组织化学检测可以通过检测肿瘤标志物在肿瘤细胞中的表达情况,帮助确定肿瘤类型、分级和分子亚型,对乳腺癌的诊断和治疗具有重要的指导意义。
通过检测雌激素受体(ER)、孕激素受体(PR)和人类表皮生长因子受体2(HER2)的表达情况,可以帮助确定患者的内分泌治疗和靶向治疗的方案,从而提高治疗的有效性和预后。
乳腺病理诊断中,往往需要鉴别良恶性肿瘤,尤其对于一些较难鉴别的病例,免疫组织化学检测可以通过检测不同标记物的表达情况,帮助鉴别良恶性肿瘤。
在乳腺纤维瘤和纤维腺瘤的鉴别诊断中,通过检测细胞角蛋白、平滑肌肌动蛋白、骨架蛋白等标记物的表达情况,可以帮助鉴别病变的来源和性质,对指导患者的治疗具有重要的意义。
乳腺癌是一种具有高度异质性的疾病,对患者的预后影响因素也非常复杂。
免疫组织化学检测可以通过检测肿瘤相关标记物在肿瘤细胞中的表达情况,帮助评估患者的预后。
通过检测Ki-67(肿瘤细胞增殖指数)、P53(抑癌基因突变)等标记物的表达情况,可以帮助评估患者的预后情况,指导患者的治疗和随访。
乳腺癌分子靶向治疗是目前乳腺癌治疗的重要手段,但是对于患者的分子亚型和靶向分子的表达情况要求较高。
免疫组织化学检测可以通过检测HER2、PD-L1等靶向分子的表达情况,帮助确定患者的分子亚型和靶向治疗方案,提高治疗的有效性和减少不必要的治疗。
免疫组织化学检测在乳腺病理诊断中发挥了重要的作用,但也面临一些挑战。
免疫组织化学检测的标记物选择、试剂的品质、操作的标准化等,都对检测结果产生影响。
未来,随着生物技术的不断发展和进步,我们有望开发出更加有效的标记物和检测方法,提高免疫组织化学检测的准确性和可靠性。



免疫组化技术在病理诊断中的应用在临床病理诊断中,免疫组织化学(Immunohistochemistry, IHC)技术是一种很重要的技术和手段,从20个世纪70年代开始,免疫组化技术就应用于病理诊断,对于肿瘤的诊断、分类以及预后的判断产生了巨大的影响,同时也扩展了人们对于各种疾病及肿瘤形成过程的认识,提高了病理诊断准确性。
就文献的复习,进一步巩固基础知识,深入学习这一技术的原理有利于日常临床病理诊断工作更好的开展以及对免疫组化技术进一步的研究与发展夯实基础。
IHC是组织化学的一种。
组织化学又可称为特殊染色,通过应用某些能与组织或细胞的化学成分进行特异性结合的显色试剂,定位地显示病变组织、细胞的特殊化学成分(如蛋白质、酶类、核酸、糖类、脂类等),同时又能保存组织原有的形态改变,达到形态与代谢的结合。
IHC是利用抗原—抗体的特异性结合反应来检测和定位组织中的某种化学物质的一种技术,由免疫学和传统的组织化学相结合而形成。
IHC不仅有较高的敏感性和特异性,同时具有将形态学改变与功能和代谢变化结合起来,直接在组织切片上原位确定某些蛋白质或多肽类物质的存在的特点。
IHC染色方法有很多,按标记物的性质可分为荧光法(荧光素标记)、酶法(辣根过氧化物酶、碱性磷酸酶等)、免疫金银和铁标记技术;按染色步骤可分为直接法、间接法;按结合方式可分为抗原—抗体结合,如标记的葡萄糖聚合物(labelled dextran polymer,LDP)法,以及亲和连接,如标记的链亲和素-生物素(labelled streptavidin-biotin,LSAB)法等,其中LSAB法和LDP法是最常使用的方法。
IHC在临床诊断中的应用主要有以下几个方面:1、肿瘤良恶性的判断。
由于反应性增生与肿瘤性增生在B淋巴细胞增生的克隆性上有区别,反应性增生呈现单克隆性增生,而肿瘤性增生呈现多克隆性,我们可以通过免疫球蛋白的轻链抗体来检测。
而增殖细胞核抗原(PCNA),周期素(Cycling),核抗原(Ki-67)通过对肿瘤细胞增生的程度作出评价,从而提示增生细胞的良恶性。
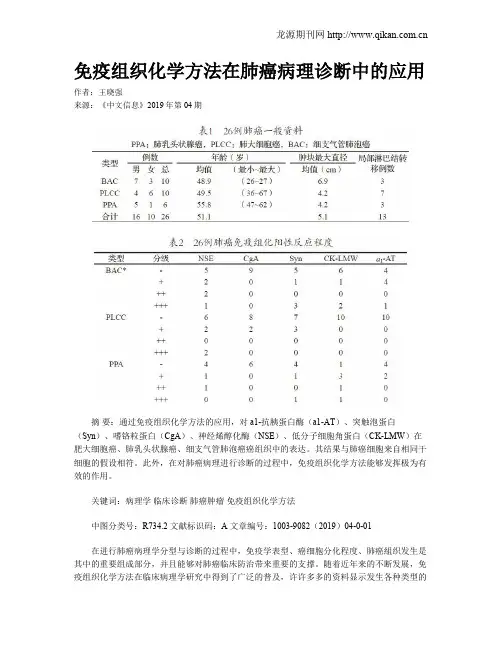
免疫组织化学方法在肺癌病理诊断中的应用作者:王晓强来源:《中文信息》2019年第04期摘要:通过免疫组织化学方法的应用,对a1-抗胰蛋白酶(a1-AT)、突触泡蛋白(Syn)、嗜铬粒蛋白(CgA)、神经烯醇化酶(NSE)、低分子细胞角蛋白(CK-LMW)在肥大细胞癌、肺乳头状腺癌、细支气管肺泡癌癌组织中的表达。
其结果与肺癌细胞来自相同干细胞的假设相符。
此外,在对肺癌病理进行诊断的过程中,免疫组织化学方法能够发挥极为有效的作用。
关键词:病理学临床诊断肺癌肿瘤免疫组织化学方法中图分类号:R734.2 文献标识码:A 文章编号:1003-9082(2019)04-0-01在进行肺癌病理学分型与诊断的过程中,免疫学表型、癌细胞分化程度、肺癌組织发生是其中的重要组成部分,并且能够对肺癌临床防治带来重要的支撑。
随着近年来的不断发展,免疫组织化学方法在临床病理学研究中得到了广泛的普及,许许多多的资料显示发生各种类型的肺癌组织,有很大可能是因为源自于共同的干细胞,这些干细胞来源于支气管黏膜上皮之中。
细胞在出现癌变的过程中,会产生多向性的分化,进而产生多样化的细胞表型,这为肺癌病理形态学的分型提供了重要的理论支撑。
在实际研究的过程中,可以通过光镜进行细致的观察,细支气管肺泡癌逐渐分化为了大细胞癌,肺乳头状腺癌的柱状癌细胞对a1-抗胰蛋白酶(Alpha 1-antitrypsin,a1-A)进行表达等一系列的现象。
通过对相关医学报道的分析发现,上述现象和肺癌细胞的治疗、诊断、表型、分化和评估预后等各个方面有着怎样的联系,这些仍需要进一步的深入研究。
一、材料与方法1.资料与标本收集吉林省卫生学院结合肺肿瘤国际组织学分类准则,收集了其附属医院2013年、2015年、2016年(下半年)大细胞肺癌和肺腺癌27例,细支气管肺泡癌23例(共50例),挑选出26例,每一例挑选癌组织蜡块2—3块,连续切片8—9张,准备对这些切片进行免疫组化染色。
病理诊断中免疫组化技术的应用作者:胡咏来源:《中国社区医师》2017年第19期摘要免疫组织化学是临床病理诊断中一种重要的手段,在肿瘤分类、诊断、预后判断等方面具有十分重要的应用价值,在临床得到广泛应用。
但免疫组化技术在病理诊断中也存在一定局限性。
本文探讨病理诊断中免疫组化技术的应用,希望能够为合理应用提供指导。
关键词病理诊断;免疫组化技术;应用免疫组化技术近年来由于具有准确、快速等诸多优点而在临床病理诊断中得到了越来越广泛的应用,并且已经成为病理诊断中不可或缺的重要手段。
这项技术在肿瘤诊断及鉴别诊断、预后判断等方面均具有显著的应用价值,但是也存在假阳性、假阴性等一定的局限性,因此加强病理诊断中免疫组化技术的应用研究具有十分重要的现实意义和作用。
病理诊断中免疫组化技术的应用肿瘤性质的判断:对B淋巴细胞增生的单克隆或多克隆性采用免疫球蛋白(Ig)的轻链抗体进行检测能够区别肿瘤是属于反应性增生还是肿瘤性增生。
如果患者的肿块性质为滤泡反应性增生,则细胞凋亡蛋白(bcl-21不会表达在滤泡反应中心的细胞中,而是呈现为bcl-2阴性;但是如果患者的肿块性质为滤泡性淋巴瘤,那么9/10以上的患者肿瘤性滤泡细胞中存在bel-2高表达的情况,并且bcl-2呈现为阳性;肿瘤细胞增生的程度能够通过周期素(cyclin)、增殖细胞核抗原(PCNA)、核抗原(Ki-67)等来进行有效评价,从而能够对增生细胞的良恶性进行准确的判断。
肿瘤分期的确定:肿瘤分期与患者是否出现血管侵袭、有无淋巴管以及是否浸润等有着密切的关系,因此肿瘤分期的确定对于患者的治疗以及预后效果的判断均具有十分重要的作用。
采用免疫组化技术能够通过Ⅳ型胶原以及层粘连蛋白的单克隆抗体来对基膜的主要成分进行清晰的显示,从而能够对原位癌和浸润癌进行准确的区分,如果出现上皮性癌未突破基膜则可以判定为原位癌,如果突破基膜的情况则可以判定患者为浸润癌;除此之外,标记物第8因子相关蛋白、Anti-HAP40抗体、D2-40等能够对血管和淋巴管内皮细胞进行清晰的显示,从而能够使肿瘤对血管或淋巴管的浸润清晰地显示。
免疫组化技术进展及在病理诊断中的应用免疫组织化学或免疫细胞化学是一种方法学,是用免疫学的方法把抗体标记上可见的颜色如荧光素、酶、某种金属等呈色物质,使抗体由不可见变为可见,来寻找检测组织细胞中的抗原,即组织细胞中的化学成分,所以也是用颜色的变化来判断组织细胞中的化学成分,从而达到诊断和研究疾病的目的。
近20年来,由于免疫组化技术的飞跃发展,特别是绝大多数抗体能够应用在福尔马林固定的石蜡切片上,因而大大促进了它在临床病理学上的应用。
1 免疫组化技术的进展1.1检测技术的进展自1941年Coons及其同事发表免疫荧光技术至今已有半个多世纪[1],嗣后免疫组化技术也逐步发展。
检测技术的进步主要表现在敏感性的提高,以及特异性增强,即可使用较少的抗体检测出针对性的抗原,而又有极少或没有非特异背景呈色。
此外,整个免疫染色时间也更加缩短。
这主要表现在以下几方面。
1.1.1检测步骤有直接法走向间接法。
包括一般间接二步法、PAP法、ABC法、LAB-SA法,现在大家认为以LAB-SA法最为优越[2]。
目前曾有将多聚体氧化酶直接连接在第一抗体上,用直接法染色,敏感度也大大提高,但毕竟存在每一单个一抗都需酶标记以及对核抗原效果不好的缺陷。
1.1.2标记物有荧光素、酶、胶质金等。
近年来,新出现的荧光素具有荧光更强、封片后不易褪色的特点,或是与其他荧光素可用相似波长的滤光片组合以激发荧光,但颜色不同,更有效的进行双重染色。
在胶质金作为标记物方面,使用银加强剂,可使用较小的胶质金标记二抗,经银加强剂及显示棕黑色或黑色,大大增强了敏感性[3]。
在酶标记方面,则仍以辣根氧化酶及碱性磷酸酶为常用。
1.1.3标记技术近年来,由于生化技术的进步,免疫组化中个别试剂的质量也大有提高,包括二抗的亲和力,标记物的质量等,从而提高了检测系统的灵敏度。
例如,Zymed的LAB-SA系统,由于生物素标记二抗,酶标链霉亲生物素蛋白新技术的应用,使得Zymed第二代LAB-SA产品比第一代产品,在敏感度上提高了2-4倍,同样有非常清晰的背景染色。
病理学中的免疫组织化学技术使用教程免疫组织化学技术是一种常见且广泛应用于病理学研究的分析方法。
它通过将特定的抗体与组织标本中的抗原相互作用,从而提供关于细胞或组织中蛋白质表达和定位的信息。
本文将为您介绍免疫组织化学技术的使用方法和注意事项。
一、实验所需材料和试剂在进行免疫组织化学实验之前,准备好以下材料和试剂是必要的:1. 抗体:选择特异性强、经过验证的一抗,可以有多种来源如商业供应商或自制。
2. 血液清晰剂:例如牛血清白蛋白(BSA)或牛血浆等。
3. 缓冲液:常用的有生理盐水、Tris缓冲液等。
4. 清洗液:例如磷酸盐缓冲液、Tween-20等。
5. 可可粉末或3,3'-二氨基联萘(DAB)显色底物。
6. 高质量的显微镜玻璃片、载玻片和封片剂。
二、步骤以下是进行免疫组织化学实验的通用步骤:1. 组织样本准备:采集病理标本并固定在适当的组织固定剂中,如4%的中性缓冲甲醛。
确保标本大小适宜,以便于透明度好和抗体能够充分作用。
2. 标本处理:将固定的组织样本进行去水和石蜡包埋等处理。
3. 反应抗原修复:使用热蒸汽或酶解剂(例如胰蛋白酶)进行抗原修复以恢复抗原的活性。
根据不同抗原的性质选择适当的修复方法。
4. 抗体染色:将组织样本与目标抗体进行孵育。
将抗体稀释到推荐浓度中,根据实验要求选择合适的时间和温度进行孵育。
5. 清洗:用缓冲液或PBS清洗标本,以去除未结合的抗体。
6. 二抗处理:加入适用于一抗的二抗,例如抗IgG。
二抗通常与标记物(如酶或荧光染料)结合,以便于检测。
7. 清洗:再次用缓冲液或PBS清洗标本,以去除未结合的二抗。
8. 显色:接下来加入可可粉末或DAB等显色底物,观察标本是否出现所需的显色反应。
9. 染色修复:在显色后,如果需要的话,可以执行染色修复以增强显色效果。
10. 去水和挂片:用梯度酒精进行去水,然后将样本挂片,以便于后续显微镜观察。
三、注意事项在进行免疫组织化学实验时,需要注意以下几点:1. 实验室安全:实验时应遵守实验室安全操作规范,戴上手套和口罩,避免接触到可能有害的试剂和组织样本。
免疫组织化学和天狼猩红双重染色技术在病理诊断中的应用【中图分类号】R446.7 【文献标识码】A 【文章编号】1672-5085(2009)20-0084-02【关键词】免疫组织化学组织化学双重染色天狼猩红染色免疫组织化学染色技术作为病理诊断的一种常规技术手段,在病理科疑难疾病的诊断过程中发挥着重要作用。
但是在某种程度上,单一的免疫组织化学染色降低了病理诊断和实验结果的可信度,必要时进行免役组织化学和组织化学双重染色可以帮助确诊。
我们在实践中摸索了免疫组织化学和天狼猩红双重染色方法,染色效果较为满意。
1材料与方法1.1材料和试剂常规梯度脱蜡,脱水试剂,免疫组织化学试剂盒。
载玻片,盖玻片。
自行制备天狼猩红染色剂和酸化水。
1.2双重染色方法选择结肠癌组织,制备石蜡切片,60℃-65℃的烤箱中烘烤12小时以上。
使用前再次烘烤,将加热的组织切片直接进入二甲苯溶液脱蜡,乙醇梯度脱水,3%HO2灭活内源性过氧化物酶的活性,专用微波炉进行抗原热修复,按SP法作免疫组化流程染色,DAB显色,显微镜下观察,蒸馏水终止染色,将免疫组化染色后的组织切片直接从终止的蒸馏水中取出,苏木素重染细胞核20分钟,盐酸酒精分化,流水返蓝约10分钟。
浸入苦味酸天狼猩红液1小时左右,染色时间的长短取决与试剂配置时间的长短和周围环境的湿度,此外,周围环境湿度高,染色时间也需要适当缩短,反之则需要适当延长。
此步染色时间的掌握比较重要,着色过浅也影响细胞形态学观察和实验结果。
然后入酸化水浸洗2次(时间不宜过长)滤纸吸净多余水份,梯度酒精脱水,无水酒精30分钟以上,二甲苯透明,中性树胶封固,盖玻片使用1%盐酸酒精处理。
2结果免疫组织化学染色和组织化学双重染色结果显示,通过免疫组织化学染色肿瘤细胞被染成棕黄色,在偏振光显微镜下观察可见天狼猩红染液将I型胶原染色为粉红色,III型胶原为绿色,通过双重染色可以清晰的观察到肿瘤细胞和胶原纤维的形态特点以及彼此之间的结构关系,肿瘤细胞侵犯间叶组织,肿瘤细胞同胶原蛋白交互排列。