
实验3 溶解热的测定
实验目的
1.测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应。
2.掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。
3.复习和掌握常用的测温技术。
实验原理
物质溶于溶剂中,一般伴随有热效应的发生。盐类的溶解通常包含着几个同时进行的过程:晶格的破坏、离子或分子的溶剂化、分子电离(对电解质而言)等。热效应的大小和符号决定于溶剂及溶质的性质和它们的相对量。
在热化学中,关于溶解过程的热效应,需要了解以下几个基本概念。
溶解热 在恒温恒压下,溶质B 溶于溶剂A(或溶于某浓度溶液)中产生的热效应,用
sol H ?表示。
摩尔积分溶解热 在恒温恒压下,1mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程产生的热效应。用sol m H ?表示。
sol sol m B
H
H n ??=
(1) 式中, B n 为溶解于溶剂A 中的溶质B 的物质的量。
摩尔微分溶解热 在恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以,,(
)A sol T P n B H n ???表示,简写为()A sol n B
H
n ???。 稀释热 在恒温恒压下,一定量的溶剂A 加到某浓度的溶液中使之稀释,所产生的热
效应。
摩尔积分稀释热 在恒温恒压下,在含有1mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以dil m H ?表示。
21dil m sol m sol m H H H ?=?-? (2) 式中,2sol m H ?、1sol m H ?为两种浓度的摩尔积分溶解热。
摩尔微分稀释热 在恒温恒压下,1mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应,以,,(
)B sol T P n A H n ???表示,简写为()B sol n A
H
n ???。 在恒温恒压下,对于指定的溶剂A 和溶质B ,溶解热的大小取决于A 和B 的物质的量,即 (,)sol A B H n n ?=?
(3)
由(3)式可推导得:
,,,,(
)()B A sol sol sol A T P n B T P n A B
H H
H n n n n ?????=+?? (4) 或 ,,,,()()B A sol sol A sol m T P n T P n B A B
H H n H n n n ?????=
+?? (5) 令0/A B n n n =,(5)改写为:
0,,,,(
)()B A sol sol sol m T P n T P n A B
H H
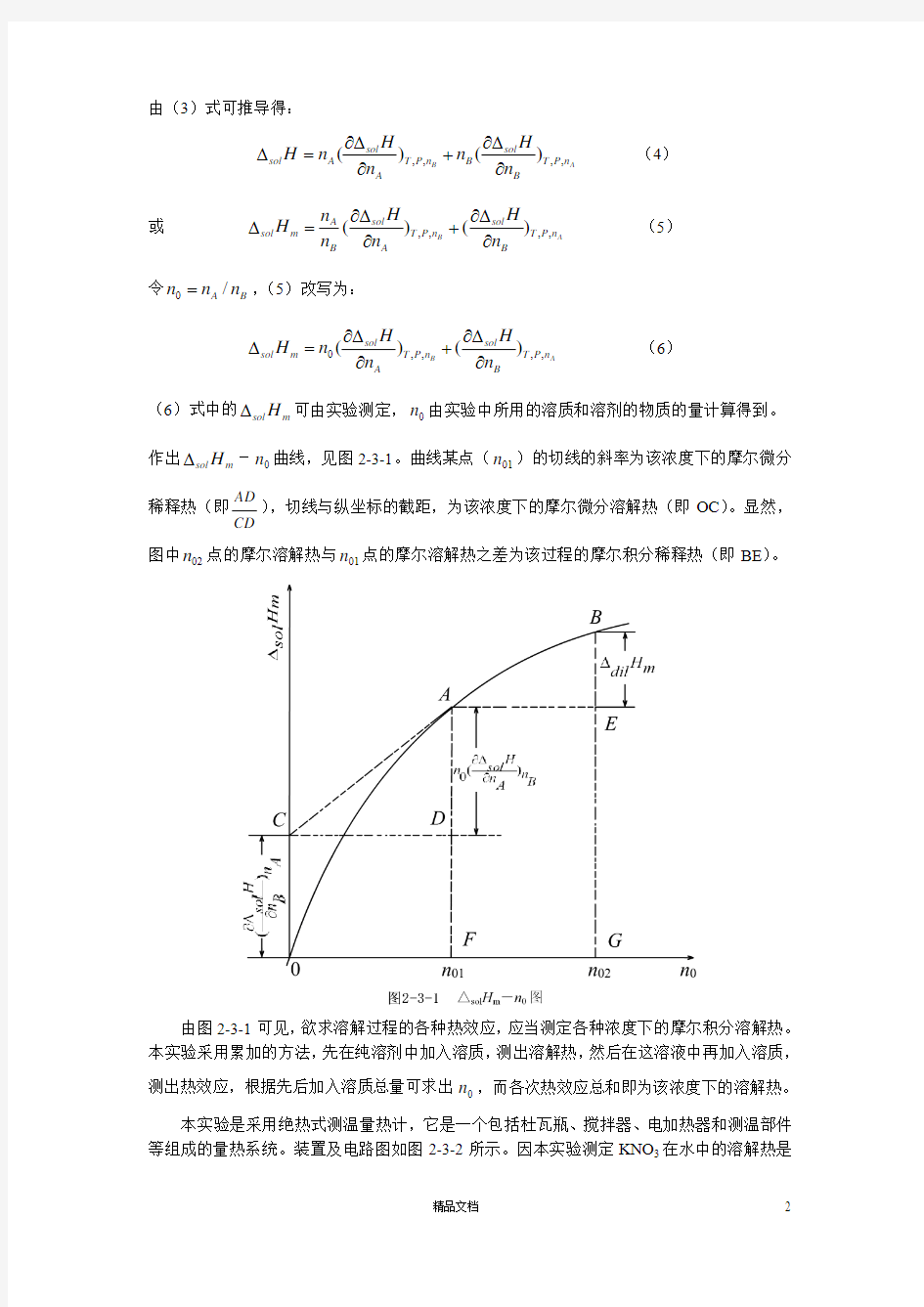
H n n n ?????=+?? (6) (6)式中的sol m H ?可由实验测定,0n 由实验中所用的溶质和溶剂的物质的量计算得到。 作出sol m H ?-0n 曲线,见图2-3-1。曲线某点(01n )的切线的斜率为该浓度下的摩尔微分稀释热(即
AD CD
),切线与纵坐标的截距,为该浓度下的摩尔微分溶解热(即OC )。显然,
图中02n 点的摩尔溶解热与01n 点的摩尔溶解热之差为该过程的摩尔积分稀释热(即BE )。
由图2-3-1可见,欲求溶解过程的各种热效应,应当测定各种浓度下的摩尔积分溶解热。本实验采用累加的方法,先在纯溶剂中加入溶质,测出溶解热,然后在这溶液中再加入溶质,测出热效应,根据先后加入溶质总量可求出0n ,而各次热效应总和即为该浓度下的溶解热。 本实验是采用绝热式测温量热计,它是一个包括杜瓦瓶、搅拌器、电加热器和测温部件等组成的量热系统。装置及电路图如图2-3-2所示。因本实验测定KNO 3在水中的溶解热是
一个吸热过程,热量的标定可用电热补偿法,即先测定体系的起始温度,溶解过程中体系温度随吸热反应进行而降低,再用电加热法使体系升温至起始温度,根据所消耗电能求出热效应Q 。再由下式可求算出溶解热
2121sol T T H Q
T T -?=''
- , 2
Q I RT = (7)
式中,1T 、2T 为加入溶质始末的体系的温度;Q 为使体系从2T '升至1T '时的电热(J ); 2T '、1T '为电加热始末的体系温度,I 为电流强度(A );R 为加热器电阻(Ω);T 为通电加热时间(S )。
本实验采用热敏电阻测温系统(详见附录温度的测量与控制),(21T T -)为溶解过程校正后的峰高,(21T T ''-)为加热过程校正后的峰高。
实验用品
保温瓶(750ml )1个,加样管,磁力搅拌器1台,热敏电阻测温装置1套,加热器,直流稳压稳流电源,精密毫安表,秒表,容量瓶(500ml ),烧杯(1000ml ),温度计,研钵1只,称量瓶,分析天平(公用),高精度万用表(公用)。
KNO 3(AR )
实验步骤
1.欲使溶解热能准确测量,要求仪器装置绝热良好,体系和环境间的热交换尽量稳定并降至最小。仪器装置如图2-3-2所示,采用保温瓶并加盖,以减少辐射、传导、对流、蒸发等热交换途径。
2.测量室温,取不少于500ml 的去离子水,根据室温调节水的温度,使之尽量接近室温,量取500ml 注入保温瓶内。这样体系温度与室温(环境)接近,减少体系与环境的热交换。按图2-3-2将装置安装好,记录仪量程20mv ,走纸速度4mm/min 。
3.在天平上准确称量约5g 左右(已研细并烘干)的KNO 3待用。
4.开动搅拌器,调节测温电桥平衡调节旋钮,使记录仪的记录笔处于记录纸的中间位置,待温度基本稳定后,记录约4min (约记录纸的1格半)。直流稳压稳流电源调至稳流,打开电源开始加热,同时将电流值调至950mA 左右(此后不要再调节电流),温度升高,记录笔升至约70格左右(记录纸上的刻度),关闭电源停止加热。待记录仪记录约8min 左右,加入称量好的KNO 3。此时由于KNO 3溶解吸热,温度降低,记录笔降低,待温度稳定后再记录约8min 左右。
严格的操作应将样品装在蜡封样品管中,放在保温瓶中恒温,加样时用玻璃棒戳破管底,样品溶入溶液。本实验采用称量瓶装样品,直接倒入。由减量法求出样品质量。
5.打开加热电源加热,同时打开秒表计时,待记录笔升至80格左右(加热使温度升高的格数,以下次加入KNO 3的量决定),关闭电源停止加热,同时停止计时,记下加热时间。再记录约8min 左右。整个过程如图2-3-3所示。
6.按上述步骤依次加入约6、7、8、8、7和6g 的KNO 3。
7.测量实验所用加热器的阻值R 。
数据处理
1.采用雷诺图解法(如图2-3-3所示),校正各步加热、溶解过程的峰高(详见燃烧热测定实验)。
2.分别计算出各次加入样品B 后的热效应,按(1)式计算出摩尔积分溶解热sol m H ?,并分别计算出对应的2/H
O
B o n n n =。
3.将sol m H ?与0n 列表并作图。从图中分别求出0n 为80、100、200、300、400处的摩尔积分溶解热、微分溶解热、微分稀释热。再从图中求出0n 为80→100、100→200、200→300、300→400过程的摩尔稀释热。
思考题
1.如何用本装置测定液体的比热?
2.如果反应是放热的如何进行实验?
3.温度和浓度对溶解热有无影响?如何从实验温度下的溶解热计算其它温度下的溶解热?
注意事项
1.加热时注意加热时间,不要使温度过高超过记录仪量程。加热温度的高低,以下次实验加入样品的量决定,如下次实验样品量较大,加热温度高些,反之要低些。尽量开始温度(环境温度)处于反应前后中间。
2.加样时要将样品全部加入反应器中,不要粘附在加样管上。
3.样品应预先研磨至60目以上。
4.开始时溶剂(去离子水)温度应尽量调至与室温一致。
进一步的讨论
1.加热器制作
加热器电阻丝可选小功率电炉丝(200W左右)或用直径约0.1mm的康铜丝,根据电源功率和加热电流算出阻值,根据阻值截相应长度。采用双绕法紧缠在玻璃棒上,或穿入U 型管内,加入液体石蜡。注意电阻丝尽量接近顶部,使之能够完全浸入液体内。
2.温度的测量
本实验温度测量采用热敏电阻测温系统,也可用贝克曼温度计测量,但贝克曼温度计使用不如热敏电阻使用方便。一般不采用热电偶测量,因为本实验温度变化范围比较小,热电势太小,达不到测量精度。
3.用简易量热计除测定溶解热外,也可以测定中和热、生成热、混合热、比热容等等。实验方法基本相同。但要根据需要,重新设计合适的样品管或反应池。下面介绍几种简易的样品容器,见图2-3-4、图2-3-5、图2-3-6、图2-3-7所示。
4.本实验方法对吸热过程的测量比较容易。对放热过程则可用图2-3-8所示方法。图中(a)是让放热过程和电热过程连续画在记录纸上,此方法误差较大。在量热计中装一冷却管,如图中(c),放热过程后,通入冷水将溶液温度复原,过程如图中(b)所示,然后再
电标定仪器常数。
5.参考数据
表2-3-1 某些物质的积分溶解热
物质(B)nB:nA t/℃△sol H m/(k J·mol-1) AlCl31:400 18 -325.93
CaCl21:400 18 -75.270
KF 1:110 15 -17.196 MgCl21:800 -154.75
KNO31:200 18
25
+35.392
+34.899
NH4Cl 1:200 +26.493
KCl 1:200 18
25
+18.602
+17.556
NH4NO31:200 +16.28
参考资料
1.北京大学化学院物理化学实验教学组.物理化学实验.北京:北京大学出版社,2002.37~40。
2. 清华大学化学系物理化学实验编写组.物理化学实验.北京:清华大学出版社,1991.135~140。
3.四川大学化学化工学院,罗澄源,向明礼等.物理化学实验(第四版).北京:高等教育出版社,2005.47~49。
溶解热测定 姓名 学号 班级 实验日期 1 实验目的 (1)了解电热补偿法测定热效应的基本原理。 (2)用电热补偿法测定硝酸钾在水中的积分溶解热,通过计算或作图求出硝酸钾在水中的微分溶解热、积分溶解热和微分冲淡热。 (3)掌握用微机采集数据、处理数据的实验方法和实验技术。 2 实验原理 溶解热:恒温恒压下,物质的量为2n 的溶质溶于物质的量为1n 的溶剂(或溶于某浓度溶液)中产生的热效应,用Q 表示。 积分溶解热:恒温恒压下,1mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程产生的热效应。用s Q 表示。 微分溶解热:恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以1 2n n Q ???? ????表示。 冲淡热:恒温恒压下,一定量的溶剂A 加到某浓度的溶液使之稀释所产生的热效应。 积分冲淡热:恒温恒压下,在含有1mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液的过程中产生的热效应,以d Q 表示。 微分冲淡热:恒温恒压下,1mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应, 以21n n Q ???? ????或2 0n s n Q ???? ????表示。 它们之间关系可表示为: s Q n Q =2 令021n n n = 2 1002n s n s n Q n n Q Q ???? ????+???? ????= ()()0201n s n s d Q Q Q -= 积分溶解热s Q 可由实验测得,其他三种热效应则可通过0n Q s -曲线求得,曲线某点的切线的斜率为该浓度下的摩尔微分稀释热,切线与纵坐标的截距,为该浓度下的摩尔微分溶解热 (即OC )。显然,图中A 点的摩尔溶解热与B 点的摩尔溶解热之差为该过程的摩尔积分稀释热(即BE )。
物理化学实验报告 溶解热的测定 实验时间:2018年4月日 姓名:刘双 班级: 学号: 1.实验目的 (1)了解电热补偿法测量热效应的基本原理。 (2)用电热补偿法测定硝酸钾在水中的积分溶解热,通过计算或者作图求出硝酸钾在水中的微分溶解热、积分冲淡热和微分冲淡热。 (3)掌握微机采集数据、处理数据的实验方法和实验技术。 2.实验原理 物质溶解于溶剂过程的热效应称为溶解热,物质溶解过程包括晶体点阵的破坏、离子或分子的溶剂化、分子电离(对电解质而言)等过程,这些过程热效应的代数和就是溶解过程的热效应,溶解热包括积分(或变浓)溶解热和微分(或定浓)溶解热。把溶剂加到溶液中使之稀释,其热效应称为冲淡热。包括积分(或变浓)冲淡热和微分(或定浓)冲淡热。 溶解热Q:在恒温、恒压下,物质的量为n2的溶质溶于物质的量为n1的溶剂(或溶于某浓度的溶液)中产生的热效应。 积分溶解热Qs:在恒温、恒压下,1mol溶质溶于物质的量为n1的溶剂中产生的热效应。 微分溶解热(ee ee2)e 1 :在恒温、恒压下,1mol溶质溶于某一确定浓度的无限量的溶液中 的热效应。 冲淡热:在恒温、恒压下,物质的量为n1的溶剂加入到某浓度的溶液中产生的热效应。 积分冲淡热Q d:在恒温、恒压下,把原含1mol溶质和n02mol溶剂的溶液冲淡到含溶剂为n01mol时的热效应,为某两浓度的积分溶解热之差。 微分冲淡热(ee ee1) e2 或(eee ee0 ) e2 :在恒温、恒压下,1mol溶剂加入到某一确定浓度的无 限量的溶液中产生的热效应。 它们之间的关系可表示为:
dQ=(ee ee1) e2 ee1+( ee ee2 ) e1 ee2 上式在比值e1 e2 恒定下积分,得: e=(ee ee1 ) e2 e1+( ee ee2 ) e1 e2 ee2=ee,令:e1 n2 =e0,则有: ( ?Q ?n1 )=[ ?(n2Q s ?(n2n0) ]=( ?Q s ?n0 ) Q d=(ee)e01?(ee)e02 其中积分溶解热ee可以直接由实验测定,其他三种可以由ee?e0曲线求得。 欲求溶解过程中的各种热效应,应先测量各种浓度下的的积分溶解热。可采用累加的方法,先在纯溶剂中加入溶质,测出热效应,然后再这溶液中再加入溶质,测出热效应,根据先后加入的溶质的总量可计算出n0,而各次热效应总和即为该浓度下的溶解热。本实验测量硝酸钾溶解在水中的溶解热,是一个溶解过程中温度随反应的进行而降低的吸热反应,故采用电热补偿法测定。先测定体系的初始温度T,当反应进行后温度不断降低时,由电加热法使体系复原到起始温度,根据所耗电能求出热效应Q。 3.仪器和试剂 反应热测量数据采集接口装置: NDRH-1型,温度测量范围0~40℃,温度测量分辨率0.001℃,电压测量范围0~20V,电压测量分辨率0.01V,电流测量范围0~2A,电流测量分辨率0.01A。 精密稳流电源:YP-2B型。 微机、打印机。 量热计(包括杜瓦瓶,搅拌器,加热器,搅拌子)。 称量瓶8只,毛笔,研钵。 硝酸钾(A.R.) 4.实验操作 (1)取8个称量瓶,分别编号。 (2)取KNO3于研钵中,研磨充分。 (3)分别称量约 2.5、1.5、2.5、3.0、3.5、4.0、4.0、4.5g 研磨后的硝酸钾,放入 8 个称量瓶中,并精确称量瓶子与药品的总质量。记录下所称量的数据。
实验1 溶解热的测定 注意事项: 1.本实验应确保样品充分溶解,因此实验前必须充分研磨样品。已进行研磨和烘干处理的样品位于靠窗口 的烘箱中。实验中每位同学使用完样品后必须及时研磨好足够的样品,并放入靠窗口的烘箱进行烘干处理,以备下一位同学使用。 2.硝酸钾加入快慢的控制,是实验成败的关键。加得太快,会使温差过大,体系与环境的热交换加快,测 得的溶解热偏低,另外加样太快会致使磁子陷住不能正常搅拌。加得太慢,一旦温度升到一个较高的值,即使加入所有硝酸钾也无法使温差回到零度以下,导致实验失败。一般ΔT控制在-0.3℃左右为宜,最低不要超过-0.5℃,但要始终为负值。实验中要时刻注意温差的变化,掌握好加料的时间和量。在每组实验完后,温差回升到0℃以上,此时升温较快,需要及时加入较多的硝酸钾,否则温差可能再无法回到负值。 3.实验时需控制合适的搅拌速度。搅拌太快,会以功的形式向系统中引入能量;搅拌太慢,会因水的传热 性差而导致Q s值偏低,而且硝酸钾难以完全溶解,若实验结束发现有未溶解的硝酸钾,应重做实验。 4.数据采集过程中,切记不要进行任何其它操作,否则需要重新采集数据。 5.将仪器放置在无强电磁场干扰的区域内。 6.不要将仪器放置在通风的环境中,尽量保持仪器附近的气流稳定。 实验步骤: 1.称硝酸钾26 g。(已进行研磨和烘干处理),放入干燥器中。 2.将8个称量瓶编号。在台称上称量,依次加入约2.5、1.5、2.5、 3.0、3.5、 4.0、4.0、和4.5 g硝酸钾, 再用分析天平称出准确数据,把称量瓶依次放入干燥器中待用。 3.量取200 mL去离子水于保温杯内,打开反应热测量数据采集接口装置的电源,将温度传感器擦干置于 空气中,预热3 min,但不要打开恒流源及搅拌器电源。 4.4个菜单项:1)参数矫正; 2)开始实验;3)数据处理;4)退出。 1)参数矫正 参数矫正菜单中有‘电压参数矫正’和‘电流参数矫正’两个子菜单项,电压参数和电流参数一般情况下不需矫正。 2)开始实验 首先选择串口com 1 搅拌器电源,把保温杯放在磁力搅拌器上,调节磁子的转速,将带有加热器及漏斗的盖子放好,测量加热器功率,并调节恒流源,使加热器功率在2.25~2.3 W之间,同时将温度传感器也放入其内。按下回车键,测量水温。(注意温度传感器探头不要与搅拌磁子和加热电阻丝相接触)。这时不要再调节功率。
实验名称测定冰的熔解热 一、前言 物质从固相转变为液相的相变过程称为熔解。一定压强下晶体开始熔解时的温度称为该晶体在此压强下的熔点。对于晶体而言,熔解是组成物质的粒子由规则排列向不规则排列的过程,破坏晶体的点阵结构需要能量,因此,晶体在熔解过程中虽吸收能量,但其温度却保持不变。物质的某种晶体熔解成为同温度的液体所吸收的能量,叫做该晶体的熔解潜热。 二、实验目的 1、学习用混合量热法测定冰的熔解热。 2、应用有物态变化时的热交换定律来计算冰的溶解热。 3、了解一种粗略修正散热的方法——抵偿法。 三、实验原理 本实验用混合量热法测定冰的熔解热。其基本做法如下:把待测系统A和一个已知热容的系统B混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统C (C=A+B).这样A(或B)所放出的热量,全部为B(或A)所吸收。因为已知热容的系统在实验过程中所传递的热量Q,是可以由其温度的改变△T 和热容C计算出来,即Q = C△T,因此待测系统在实验过程中所传递的热量也就知道了。 实验时,量热器装有热水(约高于室温10℃,占内筒容积1/2),然后放入适量冰块, 冰溶解后混合系统将达到热平衡。此过程中,原实验系统放热,设为Q 放 ,冰吸热溶成水, 继续吸热使系统达到热平衡温度,设吸收的总热量为Q 吸 。 因为是孤立系统,则有Q 放= Q 吸 (1) 设混合前实验系统的温度为T1,其中热水质量为m1(比热容为c1),内筒的质量为m2(比热容为c2),搅拌器的质量为m3(比热容为c3)。冰的质量为M(冰的温度和冰的熔点均认为是0℃,设为T0),数字温度计浸入水中的部分放出的热量忽略不计。设混
华南师范大学实验报告 课程名称 物理化学实验 实验项目 溶解热的测定 【实验目的】 1.用量热计简单测定硝酸钾在水中的溶解热。 2.掌握贝克曼温度计的调节和使用。 【实验原理】 盐类的溶解往往同时进行着两个过程:一是晶格破坏,为吸热过程;二是离子的溶剂化,为放热过程。溶解热是这两种热效应的总和。最终是吸热还是放热,则由这两种热效应的相对大小来决定。 本实验在定压、不做非体积功的绝热体系中进行时,体系的总焓保持不变,根据热平衡,即可计算过程所涉及的热效应。 T C C W C W W M H m sol ??++-=?][322111 )( (3.1) 式中: m Sol H ?为盐在溶液温度和浓度下的积分溶解热,单位:kJ ·mo1–1; 1W 为溶质的质量,单位:kg ; T ?为溶解过程的真实温差,单位:K ; 2W 为水的质量,单位:kg ; M 为溶质的摩尔质量,单位:kg ·mo1–1 ; 21C C 、分别为溶质和水的比热,单位:11--?K kg kJ ; 度升 3C 为量热计的热容(指除溶液外,使体系温高1℃所需要的热量) ,单位:kJ 。 实验测得W 1、W 2、ΔT 及量热计的热容后,即 可按 图3.1溶解热测定装配图 1.磁力搅拌器; 2.搅拌磁子; 3.杜瓦瓶; 4.漏斗; 5.传感器; 6.SWC —IIC 数字贝克曼温度仪.
(3.1)式算出熔解热m Sol H 。 【仪器与药品 】 溶解热测量装置一套(如图3.1所示);500ml 量筒一个;KCl(A.R.) ;KNO 3(A.R.) 【实验步骤】 1.量热计热容的测定: 本实验采用氯化钾在水中的溶解热来标定量热计热容3C 。为此,先在干净的量热计中装入500m1蒸馏水,将与贝克曼温度计接好的传感器插入量热计中,放在磁力搅拌器上,启动搅拌器, 保持60-90转/分钟的搅拌速度,此时,数字显示应在室温附近,至温度变化基本稳定后,每分钟准确记录读数一次,连续8次后,打开量热计盖,立即将称量好的10克氯化钾(准确至0.01克)迅速加入量热计中,盖上盖,继续搅拌,每分钟记录一次读数,读取12次即可停止。然后用普通水银温度计测出量热计中溶液的温度,倒掉溶液。 2.硝酸钾溶解热的测定:用硝酸钾代替氯化钾重复上述实验,区别是称取硝酸钾的质量为7克(准确至0.01g)。完成一次实验后,溶液不倒掉。同样连续读数8次后,再向溶液中加入7克硝酸钾,再读取12次温度完成第二次测量。实验结束,倒掉溶液 【数据的处理】 1.各样品溶解前后温差的雷诺校正图
溶解热的测定 名字:程伊伊学号:06 班级:药学日期:2016.3.15 (一)实验原理 1.溶解热概念溶质溶解于溶剂的过程由溶质晶格破坏、电离的吸热过程和溶质溶剂化的放热过程组成,总的热效应取决于两者之和,可能是吸热的,也可能是放热的。在一定温度和压力下,热效应的大小与溶质和溶剂的相对量有关,例如硝酸钾溶解在水中的热效应(吸热)随溶剂水的量增加而增加。 2.电热补偿法原理硝酸钾溶解于水的过程是吸热过程,反应热可以用电热补偿法来进行测定。其基本做法是,在反应前确定系统的温度,在反应中,给予系统电加热,直到反应结束后,系统的温度恢复到起始状态,计算电热量即为反应热。 △Hm=Cp*△T1*M/m Cp=Q/△T2 Q=IVt (二)实验步骤 (1)在分析天平上称取1份重量为8.2345g的硝酸钾样品,放在干燥器中待用。 (2)将蒸馏水加入干燥的保温杯中,同时记录水温,作为实验温度。 (3)插上电源,搭好装置,开启磁力搅拌器,调整转速。观察数字贝克曼温度计,记录初始温度T1,每1min观察1次,记录3次,直至恒温。 (4)将预先称好的硝酸钾8.2345g迅速、全部倒入保温杯中,盖好瓶盖,磁力搅拌器均匀地搅拌,由于硝酸钾溶解为吸热过程,溶解时温度下降,每30s读取温度一次,直至温度不变,即为T2。T2每1min观察1次,记录3次。 (5)开启电源,接上加热器,调整功率(电压约10V,电流约1A),准确记录电流电压值。当贝克曼温度计度数上升0.5℃时,记作标记温度,并按下秒表开始计时。 (6)计时的同时,观察温度上升,直至接近T1,取下加热器,记录温度T3,每1min 观察1次,记录3次。 (三)数据记录和处理 实验温度的测定 通电时间:3min14s 电流:1.435A 电压:10.46V 实验温度:13.92℃ 每1min记录1次第1次第2次第3次 T1 13.93 13.93 13.93 T2 11.16 11.14 11.13 T3 14.18 14.22 14.26
实验3 溶解热的测定 坂井优 2013080091 化32 同组实验者:郑少冬 实验日期:2015-11-26 提交报告日期:2012-12-4 带实验老师: 1 引言 1.1 实验目的 1.测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应。 2.掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。 3.复习和掌握常用的测温技术。 1.2 实验原理 1.2.1 基本实验原理 物质溶于溶剂中,一般伴随有热效应的发生。盐类的溶解通常包含着几个同时进行的过程:晶格的破坏、离子或分子的溶剂化、分子电离(对电解质而言)等。热效应的大小和符号决定于溶剂及溶质的性质和它们的相对量。 在热化学中,关于溶解过程的热效应,需要了解以下几个基本概念。 溶解热 在恒温恒压下,溶质B 溶于溶剂A(或溶于某浓度溶液)中产生的热效应,用sol H ?表示。 摩尔积分溶解热 在恒温恒压下,1mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程产生的热效应。用sol m H ?表示。 sol sol m B H H n ??= (1) 式中, B n 为溶解于溶剂A 中的溶质B 的物质的量。 摩尔微分溶解热 在恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以,,( )A sol T P n B H n ???表示,简写为()A sol n B H n ???。 稀释热 在恒温恒压下,一定量的溶剂A 加到某浓度的溶液中使之稀释,所产生的热效应。 摩尔积分稀释热 在恒温恒压下,在含有1mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以dil m H ?表示。 21dil m sol m sol m H H H ?=?-? (2) 式中,2sol m H ?、1sol m H ?为两种浓度的摩尔积分溶解热。
学号:201114120222 基础物理化学实验报告 实验名称:溶解热的测定 应用化学二班班级 03 组号 实验人姓名: xx 同组人姓名:xxxxx 指导老师:李旭老师 实验日期: 2013-11-19 湘南学院化学与生命科学系
一、实验目的 1、掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。 2、用电热补偿法测定KNO3在不同浓度水溶液中的积分溶解热。 3、用作图法求KNO3在水中的微分冲淡热、积分冲淡热和微分溶解热。 二、实验原理 1、在热化学中,关于溶解过程的热效应,有下列几个基本概念。 溶解热:在恒温恒压下,n 2mol 溶质溶于n 1mol 溶剂(或溶于某浓度溶液)中产生的热效应,用Q 表示,溶解热可分为积分(或称变浓)溶解热和微分(或称定浓)溶解热。 积分溶解热:在恒温恒压下,1mol 溶质溶于n 0mol 溶剂中产生的热效应,用Qs 表示。 微分溶解热:在恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以 表示简写为 。 冲淡热:在恒温恒压下,1mol 溶剂加到某浓度的溶液中使之冲淡所产生的热效应。冲淡热也可分为积分(或变浓)冲淡热和微分(或定浓)冲淡热两种。 积分冲淡热:在恒温恒压下,把原含1mol 溶质及n 01mol 溶剂的溶液冲淡到含溶剂为n 02时的热效应,亦即为某两浓度溶液的积分溶解热之差,以Qd 表示。 微分冲淡热 在恒温恒压下,1mol 溶剂加入某一确定浓度的无限量的溶液中产生的热效应,以 可以简写为 。 2、积分溶解热QS 可由实验直接测定,其它三种热效应则通过QS -n 0曲线求得。 设纯溶剂和纯溶质的摩尔焓分别为m H (1)和Hm ? (2),当溶质溶解于溶剂变成溶液后,在溶液中溶剂和溶质的偏摩尔焓分别为H 1,m 和H 2,m ,对于由n 1mol 溶剂和n 2mol 溶质组成的体系,在溶解前体系总焓为H 。 H =n1Hm(1)+n2Hm(2) (1) 设溶液的焓为H ′, H ′=n1H1,m +n2H2,m (2) 此混合(即溶解)过程的焓变为 H H H nA Hm A H*m A nB Hm B H*m B ??==+(,,)(,,) nA Hm A nB Hm B =?+?,, 式中,Hm ?,A 即为该浓度溶液的微分稀释热,ΔHm ,B 即为该浓度溶液的1,,2n p T n Q ???? ????1 2n n Q ???? ????2,,2n p T n Q ???? ????22n n Q ???? ????
南昌大学物理化学实验 溶解热的测定实验报告一、 实验目的 1 .了解电热补偿法测定热效应的基本原理及仪器使用。 2.测定硝酸钾在水中的积分溶解热,并用作图法求得其微分稀释热、积分稀释热和微分溶解热。 二、 基本原理1.物质溶解于溶剂过程的热效应称为溶解热。它有积分(或变浓)溶解热和微分(或定浓)溶解热两种。前者是1mol 溶质溶解在n 0mol 溶剂中时所产生的热效应,以Q s 表示。后者是1mol 溶质溶解在无限量某一定浓度溶液中时所产生的热效应,即。 溶剂加到溶液中使之稀释时所产生的热效应称为稀释热。它也有积分(或变浓)稀释热和微分(或定浓)稀释热两种。前者是把原含1mol 溶质和n 01mol 溶剂的溶液稀释到含溶剂n 02mol 时所产生的热效应,以Q d 表示,显然。后者是1mol 溶剂加到无限量某一定浓度溶液中时所产生的热效应,即。 2.积分溶解热由实验直接测定,其它三种热效应则需通过作图来求:设纯溶剂、纯溶质的摩尔焓分别为H *m ,A 和H *m ,B ,一定浓度溶液中溶剂和溶质的偏摩尔焓分别为H m ,A 和H m ,B ,若由n A mol 溶剂和n B mol 溶质混合形成溶液,则混合前的总焓为 H = n A H *m ,A + n B H *m ,B (1)混合后的总焓为 H ? = n A H m ,A + n B H m ,B (2)此混合(即溶解)过程的焓变为 ΔH = H ? – H = n A (H m ,A – H *m ,A )+ n B (H m ,B – H *m ,B ) = n A ΔH m ,A + n B ΔH m ,B (3)根据定义,ΔH m ,A 即为该浓度溶液的微分稀释热,ΔH m ,B 即为该浓度溶液的微分溶解热,积分溶解热则为: 故在Q s ~ n 0图上,某点切线的斜率即为该浓度溶液的微分稀释热,截距即为该浓度溶液的微分溶解热。如图所示:、管路敷设技术通过管线敷设技术,不仅可以解决吊顶层配置不规范问题,而且可保障各类管路习题到位。在管路敷设过程中,要加强看护关于管路高中资料试卷连接管口处理高中资料试卷弯扁度固定盒位置保护层防腐跨接地线弯曲半径标高等,要求技术交底。管线敷设技术中包含线槽、管架等多项方式,为解决高中语文电气课件中管壁薄、接口不严等问题,合理利用管线敷设技术。线缆敷设原则:在分线盒处,当不同电压回路交叉时,应采用金属隔板进行隔开处理;同一线槽内,强电回路须同时切断习题电源,线缆敷设完毕,要进行检查和检测处理。、电气课件中调试对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料试卷相互作用与相互关系,根据生产工艺高中资料试卷要求,对电气设备进行空载与带负荷下高中资料试卷调控试验;对设备进行调整使其在正常工况下与过度工作下都可以正常工作;对于继电保护进行整核对定值,审核与校对图纸,编写复杂设备与装置高中资料试卷调试方案,编写重要设备高中资料试卷试验方案以及系统启动方案;对整套启动过程中高中资料试卷电气设备进行调试工作并且进行过关运行高中资料试卷技术指导。对于调试过程中高中资料试卷技术问题,作为调试人员,需要在事前掌握图纸资料、设备制造厂家出具高中资料试卷试验报告与相关技术资料,并且了解现场设备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。、电气设备调试高中资料试卷技术电力保护装置调试技术,电力保护高中资料试卷配置技术是指机组在进行继电保护高中资料试卷总体配置时,需要在最大限度内来确保机组高中资料试卷安全,并且尽可能地缩小故障高中资料试卷破坏范围,或者对某些异常高中资料试卷工况进行自动处理,尤其要避免错误高中资料试卷保护装置动作,并且拒绝动作,来避免不必要高中资料试卷突然停机。因此,电力高中资料试卷保护装置调试技术,要求电力保护装置做到准确灵活。对于差动保护装置高中资料试卷调试技术是指发电机一变压器组在发生内部故障时,需要进行外部电源高中资料试卷切除从而采用高中资料试卷主要保护装置。
学院:信息工程学院 班级:通信152 学号:6102215051 姓名:潘鑫华 实验时间:第六周星期二下午八九十节
T T' θ J K T 1 T 1' 实验名称 测定冰的熔解热 一、实验目的 1、学习用混合量热法测定冰的熔解热。 2、应用有物态变化时的热交换定律来计算冰的溶解热。 3、了解一种粗略修正散热的方法——抵偿法。 二、实验原理 本实验用混合量热法测定冰的熔解热。其基本做法如下:把待测系统 A 和一个已知热容的系统 B 混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统 C (C =A +B ).这样 A (或 B )所放出的热量,全部为 B (或 A )所吸收。因为已知热容的系统在实验过程中所传递的热量 Q ,是可以由其温度的改变 △T 和热容 C 计算出来,即 Q = C △T ,因此待测系统在实验过程中所传递的热量也就知道了。 实验时,量热器装有热水(约高于室温10℃,占内筒容积1/2),然后放入适量冰块,冰溶解后混合系统将达到热平衡。此过程中,原实验系统放热,设为 Q 放 ,冰吸热溶成水,继续吸热使系统达到热平衡温度,设吸收的总热量为 Q 吸。 因为是孤立系统,则有Q 放= Q 吸 (1) 设混合前实验系统的温度为T 1,其中热水质量为m2(比热容为c0)。冰的质量为m1(冰的温度和冰的熔点均认为是0℃,设为T 0),数字温度计浸入水中的部分放出的热量忽略不计。设混合后系统达到热平衡的温度为T ℃(此时应低于室温10℃左右),冰的溶解热由L 表示,根据(1)式有 ML +m1c0(T - T 0)=m2c0(T 1- T ) 因T r=0℃,所以冰的溶解热为: L=[m2c0(T1-T2)-T2c0m1]/m1 (2) 综上所述,保持实验系统为孤立系统是混合量热法所要求的基本实验条件。为此整个实验在量热器内进行,但由于实验系统不可能与环境温度始终一致,因此不满足绝热条件,可能会吸收或散失能量。所以当实验过程中系统与外界的热量交换不能忽略
溶解热的测定 吴大维 2006030027 生64 同组实验者:王若蛟 实验日期:2008年5月16日 提交报告日期:2008年5月30日 指导教师:张连庆 1 引言 1.1 实验目的 1.测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应。 2.掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。 3.复习和掌握常用的测温技术。 1.2 实验原理 1.2.1 基本实验原理 物质溶于溶剂中,一般伴随有热效应的发生。盐类的溶解通常包含着几个同时进行的过程:晶格的破坏、离子或分子的溶剂化、分子电离(对电解质而言)等。热效应的大小和符号决定于溶剂及溶质的性质和它们的相对量。 在热化学中,关于溶解过程的热效应,需要了解以下几个基本概念。 溶解热 在恒温恒压下,溶质B 溶于溶剂A(或溶于某浓度溶液)中产生的热效应,用sol H ?表示。 摩尔积分溶解热 在恒温恒压下,1mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程产生的热效应。用sol m H ?表示。 sol sol m B H H n ??= (1) 式中, B n 为溶解于溶剂A 中的溶质B 的物质的量。 摩尔微分溶解热 在恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以,,( )A sol T P n B H n ???表示,简写为()A sol n B H n ???。 稀释热 在恒温恒压下,一定量的溶剂A 加到某浓度的溶液中使之稀释,所产生的热效应。 摩尔积分稀释热 在恒温恒压下,在含有1mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以dil m H ?表示。 21dil m sol m sol m H H H ?=?-? (2) 式中,2sol m H ?、1sol m H ?为两种浓度的摩尔积分溶解热。
第次课 4 学时
实验3 溶解热的测定 一、实验目的 1.用量热计简单测定硝酸钾在水中的溶解热。 2.掌握贝克曼温度计的调节和使用。 二、实验原理 盐类的溶解往往同时进行着两个过程:一是晶格破坏,为吸热过程;二是离子的溶 剂化,为放热过程。溶解热是这两种热效应的总和。最终是吸热还是放热,则由这两种热效应的相对大小来决定。 本实验在定压、不做非体积功的绝热体系中进行时,体系的总焓保持不变,根据热平衡,即可计算过程所涉及的热效应。 T C C W C W W M H m s o l ??++-=?][322111 )( (3.1) 式中: m Sol H ?为盐在溶液温度和浓度下的积分溶解热,单位:kJ·mo1–1; 1W 为溶质的质量,单位:kg ; T ?为溶解过程的真实温差,单位:K ; 2W 为水的质量,单位:kg ; M 为溶质的摩尔质量,单位:kg·mo1–1; 21C C 、分别为溶质和水的比热,单位:11--?K kg kJ ; 3C 为量热计的热容(指除溶液外,使体系温度升高1℃所需要的热量) ,单位:kJ 。 实验测得W 1、W 2、ΔT 及量热计的热容后,即可按(3.1)式算出熔解热m Sol H ?。 三、仪器与药品 溶解热测量装置一套(如图3.1所示);500ml 量筒一个;KCl(A.R.) ;KNO 3(A.R.) 四、实验步骤 1.量热计热容的测定: 本实验采用氯化钾在水中的溶解热来标定量热计热容3C 。为此,先在干净的量热计中装入500m1蒸馏水,将与贝克曼温度计接好的传感器插入量热计中,放在磁力搅拌器上,启动搅拌器, 保持60-90转/分钟的搅拌速度,此时,数字显示应在室温附近,至 图3.1溶解热测定装配图 1.磁力搅拌器; 2.搅拌磁子; 3.杜瓦瓶; 4.漏斗; 5.传感器; 6.SWC —IIC 数字贝克曼温度仪.
实验三溶解热的测定 1 实验目的及要求 1.了解电热补偿法测定热效应的基本原理。 2.通过用电热补偿法测定硝酸钾在水中的积分溶解热,并用作图法求出硝酸钾在水中的微分冲淡热,积分冲淡热和微分溶解热。 2实验原理 1)物质溶解于溶剂过程的热效应称为溶解热。它有积分溶解热和微分溶解热两种。前者指在定温定压下把1摩尔溶质溶解在n摩尔的溶剂中时所产生的热效应,由于过程中溶液的浓度逐渐改变,因此也称为变浓溶解热以Q表示。后者指在定温定压下把1摩尔溶质溶解在无限量的某一定浓度的溶液中所产生的热效应。由于在溶解过程中溶液浓度可实际上视为不变,因此也称为定浓溶解热,以 表示。 把溶剂加到溶液中使之稀释,其热效应称为冲淡热。它有积分(或变浓)冲淡热和微分(或定浓)冲淡热两种。通常都以对含有1摩尔溶质的溶液的冲淡情况而言。前者系指在定温定压下把原为含1摩尔溶质和n01摩尔溶剂的溶液冲淡到含溶剂为n02时的热效应,亦即为某两浓度的积分溶解热之差,以Q d表示。后者系1摩尔溶剂加到某一 浓度的无限量溶液中所产生的热效应,以 2)积分溶解热由实验直接测定,其它三种热效应则可通过Q s~n0曲线求得: 设纯溶剂、纯溶质的摩尔焓分别为和,溶液中溶剂和溶质的偏摩尔焓分别为和,对于n1摩尔溶剂和n2摩尔溶质所组成的体系而言,在溶剂和溶质未混合前 (4.1) 当混合成溶液后 (4.2) 因此溶解过程的热效应为 (4.3)式中△H1为溶剂在指定浓度溶液中溶质与纯溶质摩尔焓的差。即为微分溶解热。根据积分溶解热的定义: (4.4) 所以在Q s~n01图上,不同Q s点的切线斜率为对应于该浓度溶液的微分冲淡热,即 该切线在纵坐标的截距OC,即为相应于该浓度溶液的微分溶解热.而在含有1摩尔溶质的溶液中加入溶剂使溶剂量由n02摩尔增至n01摩尔过程的积分冲淡热 Q d=(Q s)n01一(Q s)n02= BG—EG。
溶解热测定 (物化试验得好好做) 一、实验目的 1、设计简单量热计测定某物质在水中的积分溶解焓。 2、复习和掌握常用的量热技术与测温方法。 3、由作图法求出该物质在水中的摩尔稀释焓、微分溶解焓、微分稀释焓。 二、实验原理 溶解热,即为一定量的物质溶于一定量的溶剂中所产生的热效应。溶解热除了与溶剂量及溶质量有关外,还与体系所处的温度及压力有关。溶解热分为积分溶解热和微分溶解热。 积分溶解热即在等温等压条件下,1mol溶质溶解在一定量的溶剂中形成某指定浓度的溶液时的焓变。也即为此溶解过程的热效应。它是溶液组成的函数,若形成溶液的浓度趋近于零,积分溶解热也趋近于一定值,称为无限稀释积分溶解热。积分溶解热是溶解时所产生的热量的总和,可由实验直接测定。 微分溶解热即在等温等压下,在大量给定浓度的溶液里加入一摩尔溶质时所产生的热效应,它可表示为(ЭΔsolH/ЭnB)T、P、nA ,因溶液的量很大,所以尽管加入一摩尔溶质,浓度仍可视为不变。微分热难以直接测量,但可通过实验,用间接的方法求得。 溶解热的测量可通过绝热测温式量热计进行,它是在绝热恒压不作非体积功的条件下,通过测定量热系统的温度变化,而推算出该系统在等温等压下的热效应。 本实验采用标准物质法进行量热计能当量的标定。利用1molKCl溶于200mol水中的积分溶解热数据进行量热计的标定。当上述溶解过程在恒压绝热式量热计中进行时,可设计以下途径完成: 上述途径中:△H = △H1+△H2 = 0 →△H2 = -△H1
△H1 = [n1Cp,m (KCL,S)+ n2Cp,m(H2O,l)+ K ]×(T2- T1) △H2 = n1ΔsolHm K = -[n1Cp,m(KCL,S)+ n2Cp,m(H2O,l)+(n1ΔsolHm )/(T2- T1)] = -[m1Cp(KCL,S)+ m2Cp(H2O,l)+(m1ΔsolHm )/(M1 △T)] 式中m1 、m2 分别为溶解过程加入的KCl(S)和H2O(l)的质量;Cp,m为物质的恒压比热容,既单位质量的物质的等压热容,Cp(KCl,S)=0.699 kJ/(kg·K),Cp(H2O,l)= 4.184 kJ/(kg·K);M1为KCl的摩尔质量,△T =(T2- T1)即为溶解前后系统温度的差值;ΔsolHm 为1molKCl溶解于200 molH2O的积分溶解热,其不同温度下的积分溶解热数值见附录。通过公式式可计算量热计的K值。 本实验测定1mol的KNO3溶于200mol的H2O的溶解过程的积分溶解热,途径如下 ΔsolH = -[n1Cp,m (KNO3,S)+ n2Cp,m(H2O,l)+ K ]×(T2- T1) = -[ m1Cp(KNO3,S)+ m2Cp(H2O,l)+ K ]×(T2- T1) 摩尔溶解热ΔsolH m = ΔsolH/n1 同理m1,m2 :分别为溶解过程加入的KNO3(S)和H2O(l)的质量;Cp物质的恒压比热容,既单位质量的物质的等压热容,Cp(KNO3,S)=0.9522KJ.Kg-1.K-1,△T =(T2- T1 ):溶解前后系统温度的差值(需经过雷诺校正) ;n1:所加入的KNO3摩尔数 通过公式,既可求得1mol的KNO3溶于200mol的H2O的溶解过程的积分溶解热。 三、仪器与试剂 1、仪器:广口保温瓶、磁力搅拌器、贝克曼温度计、1/10℃温度计、容量瓶(200ml)、停表(1个) 2、试剂:氯化钾(分析纯)、硝酸钾(分析纯) 四、实验步骤 1.量热计的标定 (1)在称量瓶中准确称取4.1413克的KCl, 并记下装有KCL的称量瓶的总重量。 (2) 用容量瓶准确量取200mL室温下的蒸馏水(密度为ρ=1Kg.dm-3),倒入广口保温杯中。
溶解热的测定实验报告 一·实验目的 1.用简单量热计测定硝酸钾的溶解热 2·学习量热计热容的标定方法 3·非绝热因素对实验影响的校正 4·学会使用《计算机全程管理系统》 二·实验原理 无机盐类的溶解,同时进行晶格的破坏(吸热)和离子的溶剂化(放热)过程。将杜瓦瓶看作绝热体系,当盐溶于水中时,有如下热平衡: ΔH(W/M)=KΔT1 式中,K为量热计热容 上述过程完成后,进行电标定,用点加热器加热,又有平衡:IVt=K ΔT2 左边是加热电功的计算 由此可得: ΔH=(M/W)IVt(ΔT1/ΔT2) 由于在此两过程中,体系温度变化小,一般在1度左右,必须使用贝克曼温度计或精密电子温差仪,才能读到千分位,达到实验的要求。 也可以使用热敏电阻作为测温元件,它作为直流电桥的一个臂。热敏电阻因温度变化而电阻发生变化,电桥即有电阻输出。
用自动平衡记录仪记录,或经放大后由计算机采集,用无纸记录仪记录。 由于温度变化小,可认为电桥输出与温度变化成正比。如果以上两过程为l1和l2,可用下式计算溶解热: ΔH=(W/M)IVt(l1/ l2) 由于杜瓦瓶并非真正的绝热体系,实验过程中实际有微小的热交换。必须对温度进行校正。采用外推法,从时间-温度曲线上反映前后平均温度的点引时间坐标的垂线,与反应前后温度变化的延长线香蕉,交点的距离为l1和l2 三·仪器与试剂 500mL杜瓦瓶,装配有加热电炉丝和固体试样加料漏斗克曼温度计或精密温差仪或测温热电阻(配有电桥) 电磁(或电动)搅拌仪直流稳压电源(0~30V,0~2A)直流电流表(0.5级,0~1.5A)500mL量筒停表 记录仪分析纯硝酸钾 四·试验步骤 1·杜瓦瓶中用量筒加450mL水,装置好量热计,开始搅拌。调节输出为0,开启记录仪,记录体系温度稳定过程。 2·分析天平称取硝酸钾(前先碾成细粉,约3.3g),在量热计温度稳定3~5分钟后,从加料漏斗加入,记录仪记录过程温度变化。注意:加料漏斗加料前后应加盖,以减少体系与环境的热交换)3·待温度没有明显变化后约3分钟停止记录。
熔解热的测定 一、实验目的 1、用简单量热计测定硝酸钾的溶解热。 2、学习量热计热容的标定方法。 3、非绝热因素对实验的影响校正。 4、学会使用《计算机全过程管理系统》。 二、实验原理 无机盐类的溶解,同时进行晶格的破坏和离子的溶剂化过程。将杜瓦瓶看作绝 热体系,当盐溶于水中时,有如下热平衡: △H(W/M)=K△T1 式中,K为量热计容量。 上述过程完成后,进行电标定,用电加热器加热,又有如下平衡: IVt=K△T2 左边是加热电功的计算。 由此可得: △H=(M/W) IVt .(△T1/△T2) 由于在此两过程中,体系温度变化小,一般在1度左右。必须使用贝壳曼温度计或 精密电子温差仪,才能读到千分位,达到实验的要求。 使用热敏电阻作为测温元件,它作为直流电桥的一个臂。温度变化小,可认为电桥输出与温度变化成正比,△T∝l(l为记录仪记录的变化)。由以上两个过程可用下式计算。 △H 溶解W/M = IVtl 1 /l 2 由于杜瓦瓶并非真正的绝热体系,实验过程中实际有微小的热交换。必须对温差进行校正。采用外推法,从时间-温度曲线上反应前后平均温度的点引时间坐标 的垂线,与反应前后温度变化的延长线相交,交点的距离为l 1和l 2 。 三、仪器与试剂 1.500ml杜瓦瓶,装配有加热电炉丝和固体试样加料漏斗; 2.贝克曼温度计或精密温差仪或测温热电阻;电磁搅拌仪; 3.直流稳压电源(0~30v,0~2A);直流电流表(0.5级,0~1.5A);直流电压表(0.5级,0~10v); 4.500ml量筒;记录仪; 5.分析纯硝酸钾。 四、主要实验步骤 1、溶解过程 1. 清洗实验仪器
实验四溶解热的测定 一、实验目的 1.用电热补偿法测定KNO3在不同浓度水溶液中的积分溶解热。 2.用作图法求KNO3在水中的微分冲淡热、积分冲淡热和微分溶解热。 二、预习要求 1.复习溶解过程热效应的几个基本概念。 2.掌握电热补偿法测定热效应的基本原理。 3.了解如何从实验所得数据求KNO3的积分溶解热及其它三种热效应。 4.了解影响本实验结果的因素有那些。 三、实验原理 1.在热化学中,关于溶解过程的热效应,引进下列几个基本概念。 溶解热在恒温恒压下,n2摩尔溶质溶于n1摩尔溶剂(或溶于某浓度的溶液)中产生的热效应,用Q表示,溶解热可分为积分(或称变浓)溶解热和微分(或称定浓)溶解热。 积分溶解热在恒温恒压下,一摩尔溶质溶于n0摩尔溶剂中产生的热效应,用Q s表示。 微分溶解热在恒温恒压下,一摩尔溶质溶于某一确定浓度的无限量的溶液 中产生的热效应,以表示,简写为。 冲淡热在恒温恒压下,一摩尔溶剂加到某浓度的溶液中使之冲淡所产生的热效应。冲淡热也可分为积分(或变浓)冲淡热和微分(或定浓)冲淡热两种。
积分冲淡热在恒温恒压下,把原含一摩尔溶质及n01摩尔溶剂的溶液冲淡到含溶剂为n02时的热效应,亦即为某两浓度溶液的积分溶解热之差,以Qd表示。 微分冲淡热在恒温恒压下,一摩尔溶剂加入某一确定浓度的无限量的溶液 中产生的热效应,以表示,简写为。 2.积分溶解热(Q S)可由实验直接测定,其它三种热效应则通过Q S—n0曲线求得。 设纯溶剂和纯溶质的摩尔焓分别为H m(1)和H m(2),当溶质溶解于溶剂变成溶液后,在溶液中溶剂和溶质的偏摩尔焓分别为H1,m和H2,m,对于由n1摩尔溶剂和n2摩尔溶质组成的体系,在溶解前体系总焓为H。 H=n1H m(1)+n2H m(2) (1) 设溶液的焓为H′, H′=n1H1,m+n2H2,m (2) 因此溶解过程热效应Q为 Q =Δmix H=H - H= n1[H1。m –H m(1)]+n2[H2,m–H m(2)] =n1Δmix H m(1)+n2Δmix H m(2) (3) (3)式中,Δmix H m (1)为微分冲淡热,Δmix H m (2)为微分溶解热。根据上述定义,积分溶解热Q S为 (4)
溶解热的测定 1 引言 1.1 实验目的 1. 测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应。 2. 掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。 3. 复习和掌握常用的测温技术 1.2 实验原理 在热化学中,关于溶解过程的热效应,有以下几个基本概念 溶解热 在恒温恒压下,溶质B 溶于溶剂A (或溶于某浓度溶液)中产生的热效应,用Δsol H 表示 摩尔积分溶解热 在恒温恒压下,1 mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程的热效应,用Δsol H m 表示: Δsol H m = Δsol H B 式中:n B 是溶解于溶剂A 中的溶质B 的物质的量 摩尔微分溶解热 在恒温恒压下,1 mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以 ( ?Δsol H ?n B ) T,p,n A 表示,简写为(?Δsol H ?n B )n A 稀释热 在恒温恒压下,一定量的溶剂A 加到某浓度的溶液中使之稀释,所产生的热效应 摩尔积分稀释热 在恒温恒压下,在含有1 mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以Δdil H m 表示: Δdil H m =Δsol H m2?Δsol H m1 摩尔微分稀释热 在恒温恒压下,1 mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应 在恒温恒压下,对于指定的溶剂A 和溶质B ,溶解热的大小取决于A 和B 的物质的量,即 Δsol H =f(n A ,n B ) 取全微分 Δsol H =n A (eΔsol H A )n B +n B (eΔsol H B )n A
实验七 溶解热的测定 一、实验目的 1.掌握采用电热补偿法测定热效应的基本原理。 2.用电热补偿法测定硝酸钾在水中的积分溶解热,并用作图法求出硝酸钾在水中的微分溶解热、积分稀释热和微分稀释热。 3.掌握溶解热测定仪器的使用。 二、实验原理 物质溶解过程所产生的热效应称为溶解热,可分为积分溶解热和微分溶解热两种。积分溶解热是指定温定压下把1mol 物质溶解在n 0mol 溶剂中时所产生的热效应。由于在溶解过程中溶液浓度不断改变,因此又称为变浓溶解热,以△sol H 表示。微分溶解热是指在定温定压下把1mol 物质溶解在无限量某一定浓度溶液中所产生的热效应,以表示.在溶解过程中浓度可视为不变,因此又称为定浓度溶解热,以0 ,,)(n p T sol n H ???表示,即定温、定压、定溶剂状态下,由微小的溶质增量所引起的热量变化。 稀释热是指溶剂添加到溶液中,使溶液稀释过程中的热效应,又称为冲淡热。它也有积分(变浓)稀释热和微分(定浓)稀释热两种。积分稀释热是指在定温定压下把原为含1mol 溶质和n 01mol 溶剂的溶液冲淡到含n 02mol 溶剂时的热效应,它为两浓度的积分溶解热之差。微分冲淡热是指将1mol 溶剂加到某一浓度的无限量溶液中所产生的热效应,以n p T sol n H ,,0 )(???表示,即定温、定压、定溶质状态下,由微小的溶剂增量所引起的热量变化。 积分溶解热的大小与浓度有关,但不 具有线性关系。通过实验测定,可绘制出 一条积分溶解热△sol H 与相对于1mol 溶 质的溶剂量n 0之间的关系曲线,如图1 所示,其他三种热效应由△sol H~n 0曲线求 得。 设纯溶剂、纯溶质的摩尔焓分别为 H m1和H m2,溶液中溶剂和溶质的偏摩尔 焓分别为H 1和H 2,对于由n 1mol 溶剂和 n 2mol 溶质组成的体系,在溶质和溶剂未 混合前,体系总焓为: 图1