
第二章化学反应工程基础
本章学习重点:
(1)如何根据反应的特点与反应器的性能特征来正确选择反应器的形式与操作方式(2)造成非理想流动的原因及其测定描述,非理想流动对化学反应的影响。
第一节化学反应和反应器的分类
第二节均相反应动力学
第三节理想反应器的设计
第四节理想混合反应器的热稳定性
第五节连续流动反应器的停留时间分布
第六节流动模型
第七节停留时间分布与化学反应
第一节化学反应和反应器分类
1、化学反应的分类
2、反应器的分类
3、连续流动反应器内流体流动的两种理想形态
1、化学反应的分类
(1)按化学反应的特性分类
(2)按反应物料的相态分类
(3)按反应过程进行的条件分类
(1)按化学反应的特性分类
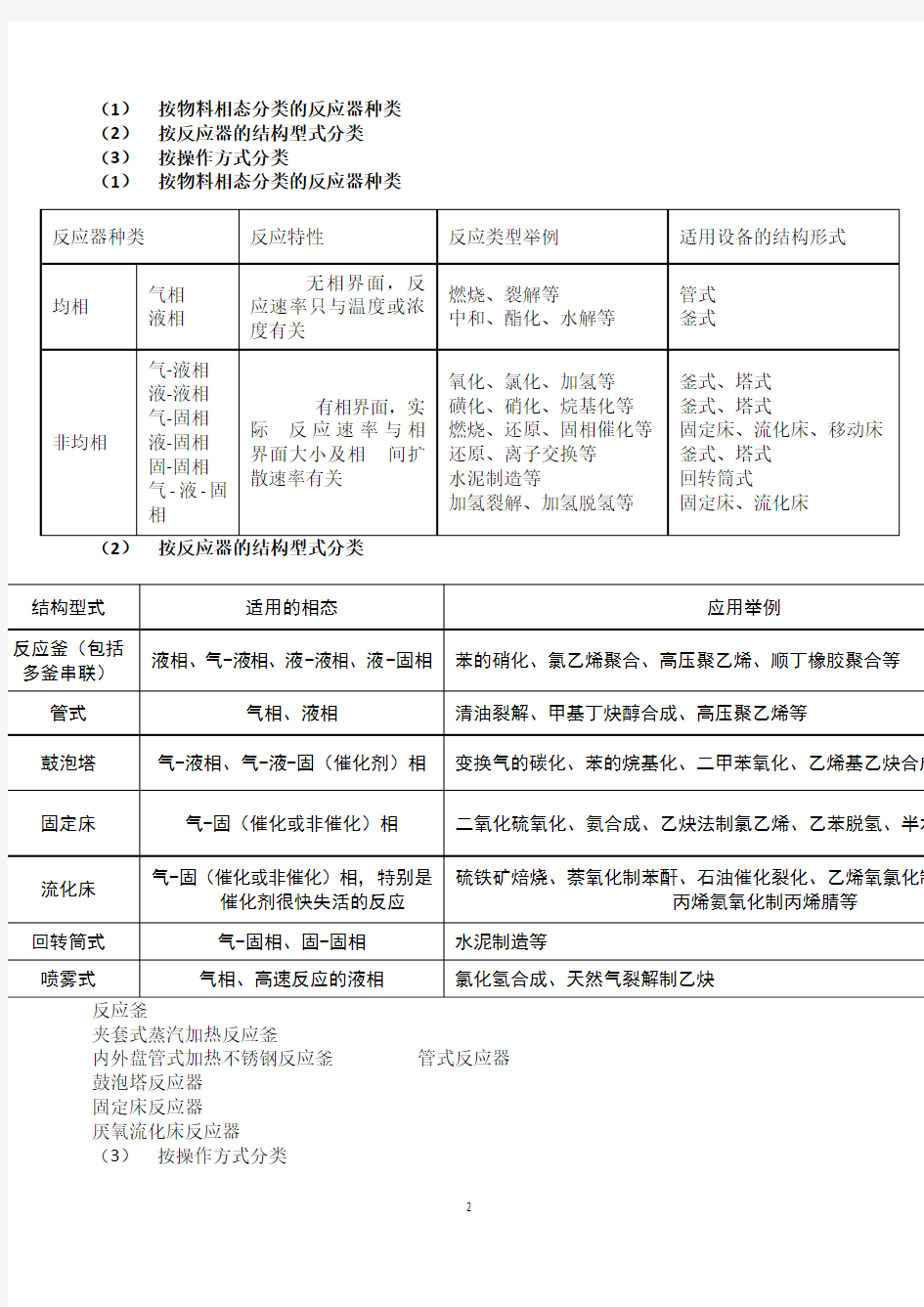
(1)按物料相态分类的反应器种类
(2)按反应器的结构型式分类
(3)按操作方式分类
(1)按物料相态分类的反应器种类
夹套式蒸汽加热反应釜
内外盘管式加热不锈钢反应釜管式反应器鼓泡塔反应器
固定床反应器
厌氧流化床反应器
(3)按操作方式分类
间歇反应器
间歇反应器特点:
1、反应物料一次加入,产物一次取出。
2、非稳态操作,反应器内浓度、温度随反应时间连续变化。
3、同一瞬时,反应器内各点温度相同、浓度相同。
连续反应器
连续反应器特点:
1、反应物料连续加
入,反应产物连续
引出。
2、稳态操作,反应
器内任一点的组成
不随时间改变
半连续反应器特点:
1、某些反应物料一次加入,其余物料连续加入,或者将某种产物连续取出。
2、非稳态操作。
3、连续流动反应器内流体流动的两种理想形态
平推流反应器
平推流反应器特点:
1、在稳态操作时,在反应器的每个截面上,物料浓度不随时间变化。
2、所有物料质点在反应器中的停留时间都相同。
2、反应器内物料浓度沿着流动方向改变,故反应速率随空间位置改变,即反应速率的变化只限于反应器的轴向。
理想混合流反应器特点:
1. 物料连续以恒定的流速流入、流出反应器,稳态操作。
2. 反应器内各空间位置温度、浓度均一。
3. 反应器内浓度、温度与出口处浓度、温度相同。
第二节均相反应动力学
?均相反应是指在均一的液相或气相中进行的反应
?均相反应动力学内容:研究化学反应本身的速度规律,即物料的浓度,温度,催化剂等因素对化学反应速度的影响。
即Rp~(C,T,Cats)
均相反应动力学没有考虑到物理因素的影响,仅研究化学反应内在规律
1、反应速率
定义:对均相反应而言,反应速率可定义为单位时间,单位反应体积中所生成(消失)的某组分的摩尔数。即
+:表示i组分的生成速率
-:表示i组分的消失速率
对反应:aA + Bb lL + mM
各组分的反应速率:
它们之间
幂函数形式
k: 反应速率常数
α1,α
2
:实验测定常数总级数n=α
1
+α
2
对基元反应:α1=aα2=b 复杂反应:n需实验测定
k遵循Arrehnies方程:k = A
e-E/RT
– E/RT
lnk =lnA
dlnk/dT = E/RT2
(1) 反应对T敏感
(2) (低温)
所以,T对K的响在低温下更敏感
2、等温、恒容、单一反应动力学方程式
单一反应是指用一个化学反应式和一个动力学方程式便能代表的反应。为简化起见,只研究、等温、恒容、单一反应动力学
不可逆反应
●一级不可逆反应
●二级不可逆反应
可逆反应
● 一级可逆反应 ● 二级可逆反应 2.1 一级不可逆方程
对于等温系统,k 为常数,初始条件: t=0 C A =C A0
一级不可逆反应C —t 关系
2.2 二级不可逆方程
可按一级不可逆反应的情况作类似的处理,有如下反应:
因为A,B 等摩尔消耗,所以C A0x A = C B0x B 令M =C B0/C A0
A
S
(1)M =1 即 C A0=C B0 C A =C B
(2)M≠1 即 C A0≠C B0 C A ≠C B
不可逆二级反应的C —t 关系 左:CA0≠CB0;右:CA0=CB0
2.3 一级可逆方程
若t=0,C R0=0,则C A + C R = C A0
可逆一级反应C —t 图
2、 复合反应
复合反应是几个反应同时进行的,常见的复合反应有平行反应,连锁反应,平行-连锁反应
等。
?平行反应
?连串反应
3.1 平行反应
积分: t = 0 C R0=C S0=0
一级平行反应C-t 图 3.2 连串反应
积分: t=0 C A =C A0
C R0=C S0=0 积分公式
公式形式
积分结果
令 dC R /dt =0 得:
各组分浓度变化:
3
、 等温变容过程
对于定容或变容体系,组分I 的变化速率为:
? 对恒容:
? 对变容:r i 的变化不仅有dC i /dt 变化,而且体系V 变化,C i /V ,dV/dt 都变化。
我们通常用膨胀率ε来表征变容的程度
4.1 膨胀率
定义:当物系体积随转化率x 线性变化时,反应物 A 全部转化后系统体积的变化率。
例:有一等温气相反应,计算εA
①反应开始时,只有A
结束时,只有P
n∝V εA=(2-1)/1=1
②若开始时,除A以外,还有50%的惰性气体,ε
=?反应开始时,A 1mol惰性气体1mol,
A
共2mol;结束后,P 2mol惰性气体1mol,共3mol
ε
=(3-2)/2=0.5
A
时,不仅要考虑反应的计量关系,还要考虑系统中是否存在惰性气体注意:计算ε
A
εA的运用前提:系统V随x呈线性变化
4.2 动力学方程及积分表达式
C4H102C H+ H
例:在700℃及3kg/cm2恒压下发生下列反应
反应开始时,系统中含C4H10为116kg ,当反应完成50%时,丁烷分压以2.4kg/cm2.s 速率发生变化,求下列项次的变化速率:①乙烯分压 ②H2的摩尔数 ③丁烷的摩尔分率
解: 反应开始时: y C4H10=1 pA=yAp x=0.5 y C4H10=1/4 pA=(1/4)p y C2H4=1/4 pA=(2/4)p y H2=1/4 pA=(1/4)p (1)
C 4H 10
2C 2H 4 + H 2
x=0x=0.5
2mol 001mol
2mol 1mol
(2)
(3)
5、均相反应动力学的建立
5.1 微分法
5.2 积分法(试差法)
微分法(图解法)
a.先假定一个反应机理,并从它求出动力学方程式,其型式为:
b.实验数据CA(xA)、t作图,得一光滑曲线,在相应浓度位置求取曲线的斜率,此斜率就代表该组成下的反应速率,如下图a.
c.将上一步骤所得的dCA/dt各对f(CA)作图,若得一通过原点的直线,表明假定机理与实验数据相复合。否则需重新假定一动力学方程加以检验,此步骤如下图b所示
图微分法检测动力学方程图解程序
(a)斜率为dCA/dt的曲线; (b)斜率为k的曲线
如:
动力学方程
使CA0=CB0, 则
取对数
以lgrA~lgCA作图得一直线,斜率为n,截距为lgk
改变CA0\CB0,测初始反应速率,作图可得微分法(最小二乘法)
积分法(试差法)
a.写出反应速率方程的积分式:
b.求积分式的解
c.做f(C)~t图,直线斜率则为k值
例:
假定速率方程为:
将上式积分:Array
实验数据CA(xA) 、t作图,得一条直线。如果将实验数据标绘上去能与直线满意拟合,则推
测的动力学方程可取,否则应采用另一动力学方程并加以检验。
积分法检验速率方程图解程序
第三节理想反应器的设计
设计中主要解决的问题:
(a)提高反应物料进行反应所需要的容积,保证设备有一定的生产能力。
(b)具有足够的传热面积,保证反应过程中热量的传递,使反应指控在最适合的温度下进行。
(c)保证参加反应的物料均匀混合。
物料衡算
物料衡算的理论基础是质量守恒定律,即反应前后的物料质量应该相等。
上式是普遍的物料衡算式,无论对流动系统或间歇系统均可适用。
热量衡算
热量衡算的依据是能量守恒定律,对于流动系统和间歇系统可列出均可适用的普遍的热量衡
算式:
1、间歇反应器
反应时间的确定:
进入量=流出量+反应掉的量+(累积量)
反应掉的量=-(累积量)
恒容时:
间歇反应器的容积计算:
?ta 停驻时间,tR反应时间,每小时处理物料体积为v0
?
?间歇釜设计方程图示a
?间歇釜设计方程图示b
有效体积:VR=(ta+tR)v0
设计实际体积:V=VR/ψ
不起泡沸腾,ψ=0.75~0.85
起泡沸腾,ψ=0.4~0.6
间歇釜设计方程图示
间歇釜设计方程图示
2 、平推流反应器
反应物A的流入速度=流出速度+消失速度
F A0dx A=r A dV
所以
或
平推流反应器的图解计算示意图
平推流反应器的图解计算示意图
(a)适用一般场合;(b)仅适用恒容过程
3、理想混合反应器
化学反应工程考试总结 一、填空题: 1.所谓“三传一反”是化学反应工程学的基础,其中“三传”是指质量传递、热量传递 和动量传递,“一反”是指反应动力学。 2.各种操作因素对于复杂反应的影响虽然各不相同,但通常温度升高有利于活化能高 的反应的选择性,反应物浓度升高有利于反应级数大的反应的选择性。 3.测定非理想流动的停留时间分布函数时,两种最常见的示踪物输入方法为脉冲示踪法 和阶跃示踪法。 4.在均相反应动力学中,利用实验数据求取化学反应速度方程式的两种最主要的方法为 积分法和微分法。 5.多级混合模型的唯一模型参数为串联的全混区的个数N ,轴向扩散模型的唯一模 型参数为Pe(或Ez / uL)。 6.工业催化剂性能优劣的三种最主要的性质是活性、选择性和稳定性。 7.平推流反应器的E函数表达式为 , () 0, t t E t t t ?∞= ? =? ≠ ?? ,其无因次方差2θσ= 0 ,而全混流反应器的无因次方差2θσ= 1 。 8.某反应速率常数的单位为m3 / (mol? hr ),该反应为 2 级反应。 9.对于反应22 A B R +→,各物质反应速率之间的关系为(-r A):(-r B):r R=1:2:2 。 10.平推流反应器和全混流反应器中平推流更适合于目的产物是中间产物的串联反 应。 11.某反应的计量方程为A R S →+,则其反应速率表达式不能确定。 12.物质A按一级不可逆反应在一间歇反应器中分解,在67℃时转化50%需要30 min, 而 在80 ℃时达到同样的转化率仅需20秒,该反应的活化能为 3.46×105(J / mol ) 。 13.反应级数不可能(可能/不可能)大于3。 14.对于单一反应,在相同的处理量和最终转化率条件下,选择反应器时主要考虑反应器 的大小;而对于复合反应,选择反应器时主要考虑的则是目的产物的收率;15.完全混合反应器(全混流反应器)内物料的温度和浓度均一,并且等于 (大于/小于/等于)反应器出口物料的温度和浓度。
化学反应工程知识点 —郭锴主编 1、化学反应工程学不仅研究化学反应速率与反应条件之间的关系,即化学反应动力学,而且着重研究传递过程对宏观化学反应速率的影响,研究不同类型反应器的特点及其与化学反应结果之间的关系。 2、任何化工生产,从原料到产品都可以概括为原料的预处理、化学反应过程和产物的后处理这三个部分,而化学反应过程是整个化工生产的核心。 3.化学反应工程的基本研究方法是数学模型法。数学模型法是对复杂的、难以用数学全面描述的客观实体,人为地做某些假定,设想出一个简化模型,并通过对简化模型的数学求解,达到利用简单数学方程描述复杂物理过程的目的。模型必须具有等效性,而且要与被描述的实体的那一方面的特性相似;模型必须进行合理简化,简化模型既要反映客观实体,又有便于数学求解和使用。 4.反应器按型式来分类可以分为管式反应器、槽式反应器(釜式反应器)和塔式反应器。 5反应器按传热条件分类,分为等温反应器、绝热反应器和非等温非绝热反应器。 第一章 均相单一反应动力学和理想反应器 1、目前普遍使用关键组分A 的转化率来描述一个化学反应进行的程度,其定义为:0 0A A A A A A n n n x -==组分的起始量组分量转化了的 2、化学反应速率定义(严格定义)为单位反应体系内反应程度随时
间的变化率。其数学表达式为dt d V r ξ1=。 3、对于反应D C B A 432+=+,反应物A 的消耗速率表达式为dt dn V r A A 1-=-;反应产物C 的生成速率表达式为:dt dn V r C C 1= 4.反应动力学方程:定量描述反应速率与影响反应速率之间的关系式称为反应动力学方程。大量的实验表明,均相反应的速率是反应物系的组成、温度和压力的函数。 5.阿累尼乌斯关系式为RT E C C e k k -=0,其中活化能反应了反应速率对温 度变化的敏感程度。 6、半衰期:是指转化率从0变为50%所需时间为该反应的半衰期。 7、反应器的开发大致有下述三个任务:①根据化学反应动力学特性来选择合适的反应器型式;②结合动力学和反应器两方面特性来确定操作方式和优化操条件;③根据给定的产量对反应装置进行设计计算,确定反应器的几何尺寸并进行评价。 8.在停留时间相同的物料之间的均匀化过程,称之为简单混合。而停留时间不同的物料之间的均匀化过程,称之为返混。 9.根据返混情况不同反应器被分为以下类型:间歇反应器、理想置换反应器(又称平推流反应器或活塞流反应器)、全混流反应器(又称为连续操作的充分搅拌槽式反应器)。 10.反应器设计计算所涉及的基础方程式就是动力学方程式、物料衡算方程式和热量衡算方程式,其中物料衡算所针对的具体体系称为体积元。 11、停留时间又称接触时间,用于连续流动反应器,指流体微元从反
第三章 理想流动反应器 概述 按照操作方式,可以分为间歇过程和连续过程,相应的反应器为间歇反应器和流动反应器。 对于间歇反应器,物料一次性加入,反应一定时间后把产物一次性取出,反应是分批进行的。物料在反应器内的流动状况是相同的,经历的反应时间也是相同的。 对于流动反应器,物料不断地加入反应器,又不断地离开反应器。 考察物料在反应器内的流动状况。有的物料正常的通过反应器,有的物料进入反应器的死角,有的物料短路(即近路)通过反应器,有的物料在反应器内回流。 在流动反应器中物料的流动状况不相同,造成物料浓度不均匀,经历的反应时间不相同,直接影响反应结果。 物料在反应器内的流动状况看不见摸不着。人们采用流动模型来描述物料在反应器内的流动状况。流动模型分类如下: 理想流动模型 流动模型 非理想流动模型 特别强调的是,对于流动反应器,必须考虑物料在反应器内的流动状况;流动模型是专指反应器而言的。 第一节 流动模型概述 3-1 反应器中流体的流动模型 平推流模型 全混流模型
一、物料质点、年龄、奉命及其返混 1.物料质点 物料质点是指代表物料特性的微元或微团。物料由无数个质点组成。 2.物料质点的年龄和寿命 年龄是对反应器内质点而言,指从进入反应器开始到某一时刻,称为年龄。 寿命是对离开反应器的质点而言,指从进入反应器开始到离开反应器的时间。 3.返混 (1)返混指流动反应器内不同年龄质点间的混合。 在间歇反应器中,物料同时进入反应器,质点的年龄都相同,所以没有返混。 在流动反应器中,存在死角、短路和回流等工程因素,不同年具的质点混合在一起,所以有返混。 (2)返混的原因 a.机械搅拌引起物料质点的运动方向和主体流动方向相反,不 同年龄的质点混合在一起; b.反应器结构造成物料流速不均匀,例如死角、分布器等。 造成返混的各种因素统称为工程因素。在流动反应器中,不可避免的存在工程因素,而且带有随机性,所以在流动反应器中都存在着返混,只是返混程度有所不同而已。
1.过程工业包括哪些过程? 2.什么是化工产品生产的关键过程。 3.化工过程可以同时发生在很宽的时间尺度和空间尺度上,都有哪些尺度? 4.什么是数学模型? 5.按照反应的可逆性,化学反应分为哪些类型? 6.按照反应的热效应,化学反应分为哪些类型? 7.按照压力的操作条件,反应过程分为哪些类型? 8.按照操作方法,反应过程分为哪些类型? 9.根据操作方法的不同,工业反应器可分为哪些类型? 10.釜式反应器和槽式反应器的区别是什么? 11.什么是停留时间分布? 12.什么是寿命分布? 13.什么是年龄分布? 14.什么是流动模型? 15.什么是流动的数学模型? 16.理想流动模型进行的两种极限情况是哪些? 17.平推流模型的特点有哪些? 18.全混流模型的特点有哪些? 19.化学反应过程主要包括哪两方面的内容? 20.按照是否使用催化剂,化学反应分为哪些类型? 21.按照反应物系相态分类,化学反应分为哪些类型? 22.什么是转化率? 23.什么是化学膨胀因子? 24.什么是同时反应? 25.什么是平行反应? 26.什么是连串反应? 27.什么是收率? 28.什么是选择率? 29.选择率,收率和转化率之间的关系是? 30.什么是间歇系统的反应速率? 31.什么是空间速度?空间速度和接触时间什么关系? 32.什么是液空速? 33.什么是湿空速? 34.什么是干空速? 35.提问:已知NA0,XA,CA0,VS0,τ0,试建立rA和XA,CA0,τ0之间的关系式。 36.化学计量式的左边,右边及等号各代表什么含义? 37.写出反应速率常数,并指出各字母代表的含义。 38.体积反应速率常数,表面反应速率常数和质量反应速率常数之间存在怎样的关系? 39.反应速率从常数和温度之间存在怎样的关系? 40.对于不可逆的单一反应,温度对其有怎样的影响? 41.对于不可逆的单一反应,为了获得较大的反应速率,在实际生产中还应考虑哪些问题? 42.对于可逆吸热的单一反应,温度对其有怎样的影响? 43.对于平行反应,反应物A1的消耗速率和产物A3,A4生成速率之间的关系是什么?
一、单项选择题: (每题2分,共20分) 1.反应器中等温进行着A →P(1)和A →R(2)两个反应,当降低A 的浓度后,发现反应生成P 的量显著降低,而R 的生成量略降低,表明(A ) A .反应(1)对A 的反应级数大于反应(2) B .反应(1) 对A 的反应级数小于反应 (2) C .反应(1)的活化能小于反应(2) D .反应(1)的反应速率常数大于反应(2) 2.四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值2θσ为( B ) A . 1.0 B. 0.25 C .0.50 D .0 3.对一平行—连串反应R A Q P A ?→??→??→?) 3()2()1(,P 为目的产物,若活化能次序为:E 2
第二章均相反应动力学基础 均相反应均相反应是指参予反应的各物质均处同一个相内进行化学反应。 在一个相中的反应物料是以分子尺度混合的,要求: ①必须是均相体系 (微观条件) ②强烈的混合手段 (宏观条件) ③反应速率远小于分子扩散速度 一、计量方程 反应物计量系数为负,生成物计量系数为正。 计量方程表示物质量之间关系,与实际反应历程无关; 计量系数只有一个公因子; 用一个计量方程表示物质量之间关系的体系称为单一反应,反之称为复合反应。 二、化学反应速率 单位时间、单位反应容积内组分的物质的量(摩尔数)的变化称之为该组分的反应速率。 反应物: 生成物: 对于反应 三、化学反应速率方程 r 是反应物系的组成、温度和压力的函数。 3 2223NH H N =+032223=--N H NH A A A dn r Vd d t C dt =- =-R R R dn r Vdt dC dt == A B S R A B S R αααα+=+S A B R A B S R r r r r αααα= = = A A A B r [k (T)][f( C ,C ,)] =
有两类;双曲函数型和幂函数型。 k-化学反应速率常数; a(b)-反应级数。 (1)反应级数 (i) 反应级数与反应机理无直接的关系,也不等于各组份的计量系数; (ii) 反应级数表明反应速率对各组分浓度的敏感程度; (iii) 反应级数是由实验获得的经验值,只能在获得其值的实验条件范围内加以应用。 (2)反应速率常数k [k]: s -1 ·(mol/m 3)1-n E :是活化能,把反应分子“激发”到可进行反应的“活化状态”时所需的能量。 E 愈大,通常所需的反应温度亦愈高,反应速率对温度就愈敏感。 k 0 —指前因子,其单位与反应速率常数相同; E — 化学反应的活化能,J/mol ; R — 气体常数,8.314J/(mol .K)。 a b A A B r kC C =2 2 2 0.5 12H Br HBr HBr Br k c c r c k c = + exp[]E k k RT =-01 ln ln E k k R T =-? lnk 1/T
3 釜式反应器 3.1在等温间歇反应器中进行乙酸乙酯皂化反应: 325325+→+CH COOC H NaOH CH COONa C H OH 该反应对乙酸乙酯及氢氧化钠均为一级。反应开始时乙酸乙酯及氢氧化钠的浓度均为0.02mol/l ,反应速率常数等于5.6l/mol.min 。要求最终转化率达到95%。试问: (1) (1) 当反应器的反应体积为1m 3时,需要多长的反应时间? (2) (2) 若反应器的反应体积为2m 3,,所需的反应时间又是多少? 解:(1)002220 00001()(1)110.95169.6min(2.83) 5.60.0210.95 ===?---= ?=?-??Af Af X X A A A A A A A A A A A dX dX X t C C R k C X kC X h (2) 因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为2.83h 。 3.2拟在等温间歇反应器中进行氯乙醇的皂化反应: 223222+→++CH ClCH OH NaHCO CH OHCH OH NaCl CO 以生产乙二醇,产量为20㎏/h ,使用15%(重量)的NaHCO 3水溶液及30%(重量)的氯乙醇水溶液作原料,反应器装料中氯乙醇和碳酸氢钠的摩尔比为1:1,混合液的比重为1.02。该反应对氯乙醇和碳酸氢钠均为一级,在反应温度下反应速率常数等于5.2l/mol.h ,要求转化率达到95%。 (1) (1) 若辅助时间为0.5h ,试计算反应器的有效体积; (2) (2) 若装填系数取0.75,试计算反应器的实际体积。 解:氯乙醇,碳酸氢钠,和乙二醇的分子量分别为80.5,84 和 62kg/kmol,每小时产乙二醇:20/62=0.3226 kmol/h 每小时需氯乙醇:0.326680.5 91.11/0.9530%?=?kg h 每小时需碳酸氢钠:0.326684 190.2/0.9515%?=?kg h 原料体积流量: 091.11190.2 275.8/1.02+= =Q l h 氯乙醇初始浓度:00.32661000 1.231/0.95275.8?==?A C mol l 反应时间: 02000110.95 2.968(1) 5.2 1.23110.95===?=-?-??Af Af X X A A A A B A A dX dX t C h kC C kC X 反应体积:0(')275.8(2.9680.5)956.5=+=?+=r V Q t t l
4?从反应器停留时间分布测定中 ,求得无因次方差「二 _ 0.98 ,反应器可视为 XXX 大学 化学反应工程 试题B (开)卷 (答案)2011 — 2012学年第一学 期 一、单项选择题: (每题2分,共20分) 1.反应器中等温进行着 A T P (1)和A T R (2)两个反应,当降低 A 的浓度后,发现反 应生成P 的量显著降低,而 R 的生成量略降低,表明 () A .反应(1)对A 的反应级数大于反应 (2) B .反应(1)对A 的反应级数小于反应 C .反应(1)的活化能小于反应 (2) D .反应(1)的反应速率常数大于反应 2 一为() 2?四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值 A . 1.0 B. 0.25 C . 0.50 A (1) > A ⑶ > D . 0 P —-(2), Q 3. 对一平行一连串反应 为了目的产物的收率最大, A .先高后低 B.先低后高 C .高温操作 4. 两个等体积的全混流反应器进行串联操作, 与第二釜的反应速率-広2之间的关系为( A . -r Ai > -r A2 B . -r Ai 则最佳操作温度序列为( ,P 为目的产物,若活化能次序为:E 2 第一章 绪论 1. 化学反应工程是一门研究______________的科学。(化学反应的工程问题) 2. 化学反应工程是一门研究化学反应的工程问题的科学,既以_______作为研究对象,又以_______为研究对象的学科体系。(化学反应、工程问题) 3. _______是化学反应工程的基础。( 三传一反) 4. 化学反应过程按操作方法分为_______、_______、_______操作。(分批式操作、连续式操作、半分批式) 5. 化学反应工程中的“三传一反”中的三传是指_______、_______、_______。(传质、传热、动量传递) 6. 不论是设计、放大或控制,都需要对研究对象作出定量的描述,也就要用数学式来表达个参数间的关系,简称_______。(数学模型) 7. 在建立数学模型时,根据基础资料建立物料、热量和动量衡算式的一般式为_______。(累积量=输入量-输出量) 第二章 均相反应动力学 1. 均相反应是指_。(参与反应的物质均处于同一相) 2. aA + bB pP + sS 对于反应,则=P r _______)(A r -。(a p ) 3.着眼反应组分K 的转化率的定义式为_______。( 00 K K K K n n n -=χ) 4.当计量方程中计量系数的代数和等于零时,这种反应称为_______,否则称为_______。(等分子反应、非等分子反应) 5. 化学反应速率式为βαB A C A C C K r =-,用浓度表示的速率常数为C K ,假定符合理想气体状态方程,如用压力表示的速率常数P K ,则C K =_______P K 。()()(βα+RT ) 6. 化学反应的总级数为n ,如用浓度表示的速率常数为C K ,用逸度表示的速率常数f K ,则 C K =_______f K 。(n RT )() 7. 化学反应的总级数为n ,如用浓度表示的速率常数为C K ,用气体摩尔分率表示的速率常数y K ,则 C K =_______y K 。(n p RT ???? ??) 10. 活化能的大小直接反映了______________对温度的敏感程度。(反应速率) 12.生成主产物的反应称为_______,其它的均为_______。(主反应、副反应) 13. 平行反应A P(主) S(副)均为一级不可逆反应,若主E >副E ,选择性S p 与_______无关,仅是_______ 3 釜式反应器 3、1在等温间歇反应器中进行乙酸乙酯皂化反应: 325325+→+CH COOC H NaOH CH COONa C H OH 该反应对乙酸乙酯及氢氧化钠均为一级。反应开始时乙酸乙酯及氢氧化钠的浓度均为0、02mol/l,反应速率常数等于5、6l/mol 、min 。要求最终转化率达到95%。试问: (1) (1) 当反应器的反应体积为1m 3时,需要多长的反应时间? (2) (2) 若反应器的反应体积为2m 3,,所需的反应时间又就是多少? 解:(1)002220 00001()(1)110.95 169.6min(2.83)5.60.0210.95 ===?---=?=?-? ?Af Af X X A A A A A A A A A A A dX dX X t C C R k C X kC X h (2) 因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为2、83h 。 3、2拟在等温间歇反应器中进行氯乙醇的皂化反应: 223222+→++CH ClCH OH NaHCO CH OHCH OH NaCl CO 以生产乙二醇,产量为20㎏/h,使用15%(重量)的NaHCO 3水溶液及30%(重量)的氯乙醇水溶液作原料,反应器装料中氯乙醇与碳酸氢钠的摩尔比为1:1,混合液的比重为1、02。该反应对氯乙醇与碳酸氢钠均为一级,在反应温度下反应速率常数等于5、2l/mol 、h,要求转化率达到95%。 (1) (1) 若辅助时间为0、5h,试计算反应器的有效体积; (2) (2) 若装填系数取0、75,试计算反应器的实际体积。 解:氯乙醇,碳酸氢钠,与乙二醇的分子量分别为80、5,84 与 62kg/kmol,每小时产乙二醇:20/62=0、3226 kmol/h 每小时需氯乙醇:0.326680.5 91.11/0.9530%?=?kg h 每小时需碳酸氢钠:0.326684 190.2/0.9515%?=?kg h 原料体积流量:091.11190.2275.8/1.02+==Q l h 氯乙醇初始浓度:00.32661000 1.231/0.95275.8?==?A C mol l 反应时间: 02000110.95 2.968(1) 5.2 1.23110.95===?=-?-??Af Af X X A A A A B A A dX dX t C h kC C kC X 反应体积:0(')275.8(2.9680.5)956.5=+=?+=r V Q t t l (2) (2) 反应器的实际体积: 956.512750.75= ==r V V l f 第一章习题 1 化学反应式与化学计量方程有何异同?化学反应式中计量系数与化学计量方程中的计量系数有何关系? 答:化学反应式中计量系数恒为正值,化学计量方程中反应物的计量系数与化学反应式中数值相同,符号相反,对于产物二者相同。 2 何谓基元反应?基元反应的动力学方程中活化能与反应级数的含义是什么? 何谓非基元反应?非基元反应的动力学方程中活化能与反应级数含义是什么? 答:如果反应物严格按照化学反应式一步直接转化生成产物,该反应是基元反应。基元反应符合质量作用定律。基元反应的活化能指1摩尔活化分子的平均能量比普通分子的平均能量的高出值。基元反应的反应级数是该反应的反应分子数。一切不符合质量作用定律的反应都是非基元反应。非基元反应的活化能没有明确的物理意义,仅决定了反应速率对温度的敏感程度。非基元反应的反应级数是经验数值,决定了反应速率对反应物浓度的敏感程度。 3 若将反应速率写成t c r d d A A - =-,有什么条件? 答:化学反应的进行不引起物系体积的变化,即恒容。 4 为什么均相液相反应过程的动力学方程实验测定采用间歇反应器? 答:在间歇反应器中可以直接得到反应时间和反应程度的关系,而这种关系仅是动力学方程的直接积分,与反应器大小和投料量无关。 5 现有如下基元反应过程,请写出各组分生成速率与浓度之间关系。 (1)A+2B →C (2)A+2B →C (3)2A+2B →C A+C →D B+C →D A+C →D C+D →E 解 (1) D 4C A 3D D 4C A 3C 22 B A 1C C 22B A 1B D 4C A 3C 22 B A 1A 22c k c c k r c k c c k c k c c k r c k c c k r c k c c k c k c c k r -=+--=+-=+-+-= (2) E 6D C 5D 4C B 3D E 6D C 5D 4C B 3C 22 B A 1C D 4C B 3C 22B A 1B C 22 B A 1A 22c k c c k c k c c k r c k c c k c k c c k c k c c k r c k c c k c k c c k r c k c c k r +--=+-+--=+-+-=+-= (3) D 4C A 3D D 4C A 3C 22 B 2A 1C C 22B 2A 1B D 4C A 3C 22 B 2A 1A 2222c k c c k r c k c c k c k c c k r c k c c k r c k c c k c k c c k r -=+--=+-=+-+-= 6 气相基元反应A+2B →2P 在30℃和常压下的反应速率常数k c =2.65× 104m 6kmol -2s -1。现以气相分压来表示速率方程,即(?r A )=k P p A p B 2 ,求k P =?(假定气体为理想气体) 解 ()3 -1-363111 2643c P 2 B A p A 2 B A c 2 B A c A 1264c kPa s m kmol 10655.1K 303K kmol kJ 314.8s kmol m 1065.2)(s kmol m 1065.2K 30330273--------??=???= ==-? ? ? ??==-= ?==+=RT k k p p k r RT p RT p k c c k r RT p c k T 《化学反应工程》试题 XXX大学化学反应工程试题B(开)卷 (答案)2011—2012学年第一学期 一、单项选择题:(每题2分,共20分) 1.反应器中等温进行着A→P(1)和A→R(2)两个反应,当降低A的浓度后,发现反应生成P的量显著降低,而R的生成量略降低,表明(A ) A.反应(1)对A的反应级数大于反应(2) B.反应(1) 对A的反应级数小于反应(2) C.反应(1)的活化能小于反应(2) D.反应(1)的反应速率常数大于反应(2) 2.四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值为( B ) A. 1.0 B. 0.25 C.0.50 D.0 3.对一平行—连串反应,P为目的产物,若活化能次序为:E2 《化学反应工程》试题库 一、填空题 1. 质量传递、热量传递、动量传递和和化学反应称为三传一 反? 2. 物料衡算和能量衡算的一般表达式为输入-输出二累 积_____________ 。 3. 着眼组分A 转化率X A的定义式为 X A=( n A—n A)/ _____________ 。 4. 总反应级数不可能大于£—。 5. 反应速率-r A=kC A C B的单位为kmol/(m3? h).速率常数k的因次为 nV(kmol ? h ) 。 6. 反应速率-r A=kC A的单位为kmol/kg ? h.速率常数k的因次为mVkg ? h 。 7. 反应速率.kc A/2的单位为mol/L ? s.速率常数k的因次为 (mol) 1/2? L-1/2? s 。 8. 反应速率常数k与温度T的关系为lnk 10000 102.其活化能为 T mol 。 9. 某反应在500K时的反应速率常数k是400K时的103倍.则600K 时的反应速率常数k时是400K时的10 5倍。 10. 某反应在450C时的反应速率是400C时的10倍.则该反应的活化 能为(设浓度不变)mol 。 11. 非等分子反应2SO+Q==2SQ的膨胀因子sq等于________ 。 12. 非等分子反应N2+3H2==2NH的膨胀因子H2等于-2/3 。 13. 反应N b+3H2==2NH中(& )= 1/3 (仏)二1/2 扁3 14. 在平推流反应器中进行等温一级不可逆反应.反应物初浓度为G°. 转化率为X A.当反应器体积增大到n倍时.反应物A的出口浓度为 C A0(1-X A)n . 转化率为1-(1- X A”。 15. 在全混流反应器中进行等温一级不可逆反应.反应物初浓度为C A0. 转化率为X A.当反应器体积增大到n倍时.反应物A的出口浓度为 匚些.转化率为nxA—。 1 (n 1)X A 1 (n 1)X A 16. 反应活化能E越大.反应速率对温度越敏感。 17. 对于特定的活化能.温度越低温度对反应速率的影响越大。 18. 某平行反应主副产物分别为P和S选择性S的定义为(n P-g)/ (n s- n s0) 化学反应工程原理 一、选择题 1、气相反应 CO + 3H 2 CH 4 + H 2O 进料时无惰性气体,CO 与2H 以1∶2摩尔比进料, 则膨胀因子CO δ=__A_。 A. -2 B. -1 C. 1 D. 2 2、一级连串反应A S K 1 K 2 P 在间歇式反应器中,则目的产物P 的最大浓度=m ax ,P C ___A____。 A. 1 22 )(210K K K A K K C - B. 2 2/1120 ]1)/[(+K K C A C. 122 )(120K K K A K K C - D. 2 2/1210]1)/[(+K K C A 3、串联反应A → P (目的)→R + S ,目的产物P 与副产物S 的选择性 P S =__C_。 A. A A P P n n n n --00 B. 0 A P P n n n - C. 0 0S S P P n n n n -- D. 0 0R R P P n n n n -- 4、全混流反应器的容积效率η=1.0时,该反应的反应级数n___B__。 A. <0 B. =0 C. ≥0 D. >0 5 、对于单一反应组分的平行反应A P(主) S(副),其瞬间收率P ?随A C 增大而单调下降,则最适合的反应器为 ____B__。 A. 平推流反应器 B. 全混流反应器 C. 多釜串联全混流反应器 D. 全混流串接平推流反应器 6、对于反应级数n >0的不可逆等温反应,为降低反应器容积,应选用____A___。 A. 平推流反应器 B. 全混流反应器 C. 循环操作的平推流反应器 D. 全混流串接平推流反应器 7 、一级不可逆液相反应 A 2R ,3 0/30.2m kmol C A =, 出口转化率 7.0=A x ,每批操作时间 h t t 06.20=+,装置的生产能力为50000 kg 产物R/天,R M =60,则反应器的体积V 为_C_3 m 。 A. 19.6 B. 20.2 C. 22.2 D. 23.4 8、在间歇反应器中进行等温一级反应A → B , s l mol C r A A ?=-/01.0,当l mol C A /10=时,求反应至 l mol C A /01.0=所需时间t=____B___秒。 A. 400 B. 460 C. 500 D. 560 9、一级连串反应A → P → S 在全混流釜式反应器中进行,使目的产物P 浓度最大时的最优空时 = opt τ_____D__。 A. 1 212) /ln(K K K K - B. 1 221)/ln(K K K K - C. 2 112)/ln(K K K K D. 2 11K K 10、分批式操作的完全混合反应器非生产性时间0t 不包括下列哪一项____B___。 解:01A A A x c kt x = - 把数据代入得100.2m in A c k -= 当x A =0.75时解得t=15min 所以,增加的时间为15-5=10min 3-2 解:() ()11 0111n n A A x n c kt ---=+- (式A ) 把x A =0.75和t=10min 代入解得1 0.1n A c k -= 再把t=30min 代入(式A )解得x A =1.25 所以,转化率应为1 3-3 解:设反应动力学方程为:n A A dc kc dt -= 则()()11 0111n n A A x n c kt ---=+-,且c A0=1 因此有 ()()() ()1110.811810.91118 n n n k n k ---=+--=+- 解得:n=2;k=0.5L/mo l ·min -1 3-4 1)计算进料中酸、醇和水的摩尔浓度c A0、c B0、c S0(注意进料中水的浓度c S0不为0)。 2)列出当酸的转化率为x A 时,各组分浓度的表示式: ()0000001A A A B B A A R A A S S A A c c x c c c x c c x c c c x =-=-==+ 3)将上列各式及各组分初浓度代入反应速率式,整理得 ()6 2 7.9310 10.220.1 2.58A A A dx x x dt -=-?-+ 4)计算转化率达35%所需的时间为 () 0.356 20 7.9310 10.220.1 2.58A A A dx t x x -= ?-+? 上述积分可查积分表用公式计算,也可用MA TLAB 语言的quad 解算子计算,结果为 71532t s h =≈ 5)计算所需反应器体积。先计算每天的反应批数,再计算每m 3反应体积每天的生产量,然后再计算达到要求产量所需反应器体积。答案为 V R =51.9m 3 1.化学反应工程是一门研究______________的科学。 2.化学反应速率式为β α B A C A C C K r =-,如用浓度表示的速率常数为C K ,用压力表示的速率常数 P K ,则C K =_______P K 。 3. 平行反应 A P(主) S(副)均为一级不可逆反应,若主E >副E ,选择性S p 与_______无关,仅是_______的函数。 4.对于反应级数n >0的反应,为降低反应器容积,应选用_______反应器为宜。 5.对于恒容的平推流管式反应器_______、_______、_______一致。 6.若流体是分子尺度作为独立运动单元来进行混合,这种流体称为_______。 7.流体的混合程度常用_______、_______来描述。 8.催化剂在使用过程中,可能因晶体结构变化、融合等导致表面积减少造成的_______失活,也可能由于化学物质造成的中毒或物料发生分解而造成的_______失活。 9.对于多孔性的催化剂,分子扩散很复杂,当微孔孔径在约_______时,分子与孔壁的碰撞为扩散阻力的主要因素。 10.绝热床反应器由于没有径向床壁传热,一般可以当作平推流处理,只考虑流体流动方向上有温度和浓度的变化,因此一般可用_______模型来计算。 11.对于可逆的放热反应,存在着使反应速率最大的最优温度opt T 和平衡温度eq T ,二者的关系为______________。 12.描述流化床的气泡两相模型,以0U 的气速进入床层的气体中,一部分在乳相中以起始流化 速度mf U 通过,而其余部分_______则全部以气泡的形式通过。 13.描述流化床的数学模型,对于气、乳两相的流动模式一般认为_______相为平推流,而对_______相则有种种不同的流型。 14.多相反应过程是指同时存在_______相态的反应系统所进行的反应过程。 II.1.一级连串反应A → P → S 在全混流釜式反应器中进行,使目的产物P 浓度最大时的最优 空时 = opt τ_______。 A. 1212)/ln(K K K K - B. 1221) /ln(K K K K - C. 2 112)/ln(K K K K D. 211K K 2.全混流反应器的容积效率η小于1.0时,且随着A χ的增大而减小,此时该反应的反应级数n_______。 A. <0 B. =0 C. ≥0 D. >0 3.当反应级数n_______时,微观流体具有比宏观流体高的出口转化率。 A. =0 B. =1 C. >1 D. <1 4.轴向分散模型的物料衡算方程的初始条件和边界条件与_______无关。 A. 示踪剂的种类 B. 示踪剂的输入方式 C. 管内的流动状态 D. 检测位置 5.对于气-液相反应几乎全部在液相中进行的极慢反应,为提高反应速率,应选用_______装置。A. 填料塔 B. 喷洒塔 C. 鼓泡塔 D. 搅拌釜 6.催化剂在使用过程中会逐渐失活,其失活速率式为d m i d C k dt d ψψ =- ,当平行失活对反应物有强内扩散阻力时,d 为_______。 第一章 1. 化学反应工程是一门研究 (化学反应个工程问题)的科学。 2. 所谓数学模型是指 (用数学方法表达各变量间的关系)。 3. 化学反应器的数学模型包括 (动力学方程式、 物料横算式子、 热量衡算式、 动量衡算式 和 参数计算式) 4. 所谓控制体积是指 (能把反应速率视作定值的最大空间范围)。 5. 模型参数随空间而变化的数学模型称为 ( 分布参数模型)。 6. 模型参数随时间而变化的数学模型称为 (非定态模型)。 7. 建立物料、热量和动量衡算方程的一般式为 (累积量=输入量-输出量)。 第二章 1. 均相反应是指 (在均一的液相或气相中进行的反应)。 2. 对于反应aA + bB → pP + sS ,则r P =( p/a )r A 。 3.着眼反应物A 的转化率的定义式为(转化率Xa=转化了的物料A 的量/反应开始的物料A 的量)。 4. 产物P 的收率ΦP 与得率ХP 和转化率x A 间的关系为( Xp/Xa )。 5. 化学反应速率式为r A =k C C A αC B β,用浓度表示的速率常数为k C ,假定符合理想气体状态方 程,如用压力表示的速率常数k P ,则k C =[ (RT)的a+B 次方]k P 。 6.对反应aA + bB → pP + sS 的膨胀因子的定义式为 (P+S )-(A+B))/A 。 7.膨胀率的物理意义为 (反应物A 全部转化后系统的体积变化率)。 8. 活化能的大小直接反映了 (反应速率) 对温度变化的敏感程度。 9. 反应级数的大小直接反映了(反应速率) 对浓度变化的敏感程度。 10.对复合反应,生成主产物的反应称为 (主反应),其它的均为(副反应)。 11. 平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,选择性S p 与 (A 的浓度) 无关,仅是 (A 的浓度) 的函数。 12. 如果平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,提高选择性S P 应(提到 温度)。 13. 一级连串反应A → P → S 在平推流反应器中,为提高目的产物P 的收率,应(降 低)k 2/k 1。 14. 产物P 的收率的定义式为 (生成的全部P 的物质的量/反应掉的全部A 的物质的量) 15. 产物P 的瞬时收率φP 的定义式为(生成的物质的量/反应的A 的物质的量) 16. 产物P 的选择性S P 的定义式为(单位时间内产物P 的物质的量/单位时间内生成产物S 的物质的量) 17. 由A 和B 进行均相二级不可逆反应αA A+αB B = αS S ,速率方程为: r A =-dC A /dt=kC A C b 。 求: (1)当C A0/C B0=αA /αB 时的积分式 (2)当C A0/C B0=λ≠αA /αB 时的积分式 18. 反应A → B 为n 级不可逆反应。已知在300K 时要使A 的转化率达到20%需12.6min ,而在340K 时达到同样的转化率仅需3.20min ,求该反应的活化能E 。 第三章 1. 理想反应器是指(理想混合反应器 平推流反应器)。 2. 全混流反应器的空时τ是 (反应器容积) 与(进料的体积流量)之比。 3. 全混流反应器的放热速率Q G ={ 00()A A Hr Ft y x ? }。 4. 全混流反应器的移热速率Q r ={ 012()pm Ft C T T - } 5. 全混流反应器的定常态操作点的判据为{ G r Q Q = }。 6. 全混流反应器处于热稳定的定常态操作点的判据为{ G r Q Q = G r dQ dQ dT dT > }。化学反应工程复习题 (1)
化学反应工程第三章答案
化学反应工程第二版课后答案
化学反应工程期末考试试题及答案
《化学反应工程》试题和答案基础部分
化学反应工程期末考试真题
化学反应工程原理第二版(华东理工大学版)第三章答案
化学反应工程期末试卷试题(附答案)
化学反应工程基本概念