
第二章化学反应工程基础
本章学习重点:
(1)如何根据反应的特点与反应器的性能特征来正确选择反应器的形式与操作方式(2)造成非理想流动的原因及其测定描述,非理想流动对化学反应的影响。
第一节化学反应和反应器的分类
第二节均相反应动力学
第三节理想反应器的设计
第四节理想混合反应器的热稳定性
第五节连续流动反应器的停留时间分布
第六节流动模型
第七节停留时间分布与化学反应
第一节化学反应和反应器分类
1、化学反应的分类
2、反应器的分类
3、连续流动反应器内流体流动的两种理想形态
1、化学反应的分类
(1)按化学反应的特性分类
(2)按反应物料的相态分类
(3)按反应过程进行的条件分类
(1)按化学反应的特性分类
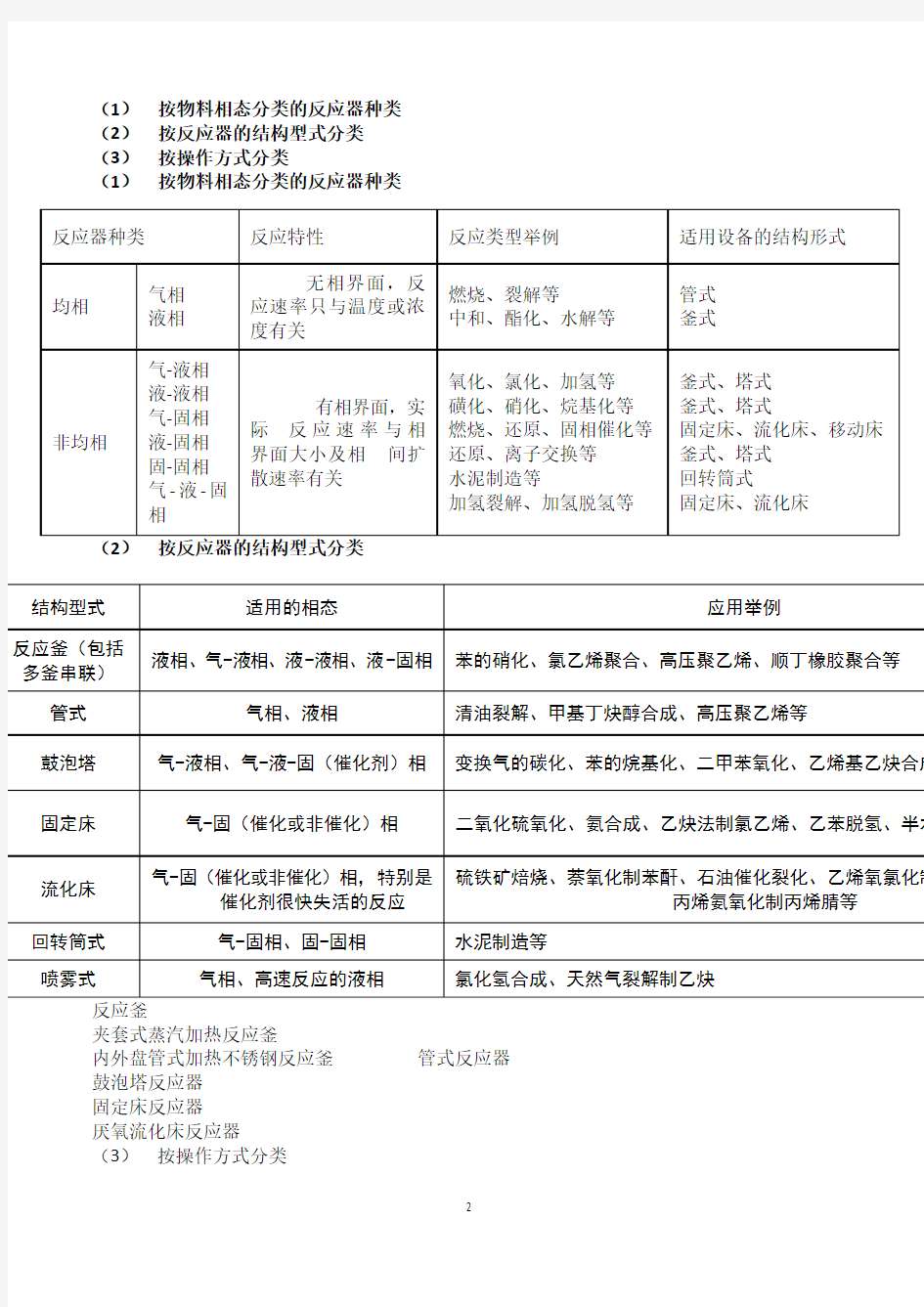
(1)按物料相态分类的反应器种类
(2)按反应器的结构型式分类
(3)按操作方式分类
(1)按物料相态分类的反应器种类
夹套式蒸汽加热反应釜
内外盘管式加热不锈钢反应釜管式反应器鼓泡塔反应器
固定床反应器
厌氧流化床反应器
(3)按操作方式分类
间歇反应器
间歇反应器特点:
1、反应物料一次加入,产物一次取出。
2、非稳态操作,反应器内浓度、温度随反应时间连续变化。
3、同一瞬时,反应器内各点温度相同、浓度相同。
连续反应器
连续反应器特点:
1、反应物料连续加
入,反应产物连续
引出。
2、稳态操作,反应
器内任一点的组成
不随时间改变
半连续反应器特点:
1、某些反应物料一次加入,其余物料连续加入,或者将某种产物连续取出。
2、非稳态操作。
3、连续流动反应器内流体流动的两种理想形态
平推流反应器
平推流反应器特点:
1、在稳态操作时,在反应器的每个截面上,物料浓度不随时间变化。
2、所有物料质点在反应器中的停留时间都相同。
2、反应器内物料浓度沿着流动方向改变,故反应速率随空间位置改变,即反应速率的变化只限于反应器的轴向。
理想混合流反应器特点:
1. 物料连续以恒定的流速流入、流出反应器,稳态操作。
2. 反应器内各空间位置温度、浓度均一。
3. 反应器内浓度、温度与出口处浓度、温度相同。
第二节均相反应动力学
?均相反应是指在均一的液相或气相中进行的反应
?均相反应动力学内容:研究化学反应本身的速度规律,即物料的浓度,温度,催化剂等因素对化学反应速度的影响。
即Rp~(C,T,Cats)
化学反应工程考试总结 一、填空题: 1.所谓“三传一反”是化学反应工程学的基础,其中“三传”是指质量传递、热量传递 和动量传递,“一反”是指反应动力学。 2.各种操作因素对于复杂反应的影响虽然各不相同,但通常温度升高有利于活化能高 的反应的选择性,反应物浓度升高有利于反应级数大的反应的选择性。 3.测定非理想流动的停留时间分布函数时,两种最常见的示踪物输入方法为脉冲示踪法 和阶跃示踪法。 4.在均相反应动力学中,利用实验数据求取化学反应速度方程式的两种最主要的方法为 积分法和微分法。 5.多级混合模型的唯一模型参数为串联的全混区的个数N ,轴向扩散模型的唯一模 型参数为Pe(或Ez / uL)。 6.工业催化剂性能优劣的三种最主要的性质是活性、选择性和稳定性。 7.平推流反应器的E函数表达式为 , () 0, t t E t t t ?∞= ? =? ≠ ?? ,其无因次方差2θσ= 0 ,而全混流反应器的无因次方差2θσ= 1 。 8.某反应速率常数的单位为m3 / (mol? hr ),该反应为 2 级反应。 9.对于反应22 A B R +→,各物质反应速率之间的关系为(-r A):(-r B):r R=1:2:2 。 10.平推流反应器和全混流反应器中平推流更适合于目的产物是中间产物的串联反 应。 11.某反应的计量方程为A R S →+,则其反应速率表达式不能确定。 12.物质A按一级不可逆反应在一间歇反应器中分解,在67℃时转化50%需要30 min, 而 在80 ℃时达到同样的转化率仅需20秒,该反应的活化能为 3.46×105(J / mol ) 。 13.反应级数不可能(可能/不可能)大于3。 14.对于单一反应,在相同的处理量和最终转化率条件下,选择反应器时主要考虑反应器 的大小;而对于复合反应,选择反应器时主要考虑的则是目的产物的收率;15.完全混合反应器(全混流反应器)内物料的温度和浓度均一,并且等于 (大于/小于/等于)反应器出口物料的温度和浓度。
1、平推流的F(t)~t和E(t)~t曲线有何特征?并画图说明。 答: 平推流的F(t)~t曲线特征:F(t)= 平推流的E(t)~t曲线特征:E(t)={ 2、理想吸附应符合哪些条件? 答:①均匀表面(理想表面):即催化剂表面各处的吸附能力是均一的,吸附热于表面已被吸附的程度如何无关②单分子层吸附③被吸附的分子间互不影响④吸附的机理均相同,吸附形成的络合物亦均相同⑤吸附与脱附可以建立动态平衡 3、测定停留时间分布需要借助示踪剂,示踪剂应满足哪些条件? 答:采用何种示踪剂,要根据物料的物态、相系及其反应器的类型等情况而定。 A不应与主流体发生反应 B与所研究的流体完全互溶,除了显著区别与主流体的某一可检测性质外,二者应具有尽可能相同的物理性质 C便于检测:本身应具有或者易于转变为电信号或者光信号的特点,并且浓度很低时也能够检测 D加入示踪剂不影响所研究流体的流动状态 E不被反应器表面及其反应器内部的固体填充物吸附,用于多相系统检测的失踪剂不发生相间的转移 4、什么是返混,简述返混对复合反应体系的影响。 答:返混是指不同停留时间的物料粒子间的混合,或者不同时间进入反应器的物料间的混合。 对平行反应:若主反应级数高于副反应级数,返混使主产物选择率下降,若主反应级数低于副反应级数,返混使主产物选择率提高。 对连串反应:返混使反应物浓度降低,产物浓度提高,因而使主产物的选择率下降。5、什么是反应器的热稳定性?全混釜稳定操作的必要条件是什么? 答:反应器的热稳定性是指当操作参数受外界干扰,偏离正常值,出现微小变化时,反应能否正常进行,当外界干扰取消时,操作状态能否自动恢复到规定的正常值。 全混釜稳定操作的必要条件:Q r=Q G dQ r∕dT>dQ G/dT 6、选择操作温度的一般原则是什么? 答:①反应的热效应不大,反应热较小,活化能较低,而且在相当广的温度范围内,反应的选择性变化很小,则可采用既不供热也不出去热量的绝热操作是最方便的,反应放出或吸收的热量由系统中物料本身温度的升高或者降低来平衡,这种操作温度的变化范围不应超过工艺上许可的范围。 ②对中等热效应的反应,一般先考虑采用绝热操作,因此绝热反应器结构简单,经济,但应对收率、操作费用、反应器大小方面全盘衡量,最后才确定采用绝热或变温的方式。若为液相反应,可采用具有夹套或者盘管的釜式反应器,以便控制在等温下操作。 ③对热效应较大的反应,要求在整个反应过程中同时进行有效地热交换。 ④对极为快速的反应,一般考虑采用绝热操作,或者利用溶剂的蒸发来控制温度。 7、平推流与全混流是流体在反应器中流动的两种极端模型,二者各有何特点?并进行比 较。
《化学反应工程》课程综合复习资料 一、填空题 1、全混流反应器的E 函数表达式为 ,其无因次方差2 θσ= ,而平推流反应器的无因次方差2θσ= 。 2、工业催化剂性能优劣的三种最主要的性质是 、 、和 。 3、在间歇反应器中进行一恒压气相反应32A B R +→,原料为A 和B 的混合物,其中A 含量为20%(mol),若物料初始体积为2升,则A 转化50%时,物料的总体积为 。 4、基元反应的分子数 (可能/不可能)是小数。 5、某液相反应A R →于50℃下在间歇反应器中进行,反应物A 转化80%需要10min ,如果于相同条件下在平推流反应器中进行,则达到同样的转化率需要的空时为 ;如果同样条件下在全混流反应器中进行,达到同样的转化率需要的空时 。 6、测定非理想流动的停留时间分布函数时,两种最常见的示踪物输入方法为 和 。 7、完全混合反应器(全混流反应器)内物料的温度和浓度 ,并且 (大于/小于/等于)反应器出口物料的温度和浓度。 8、多级混合模型的唯一模型参数为 ,轴向扩散模型的唯一模型参数为: 。 9、对于单一反应,在相同的处理量和最终转化率条件下,选择反应器时主要考虑 ;而对于复合反应,选择反应器时主要考虑的则是 。 10、对于反应23A B R +→,各物质反应速率之间的关系为:(-r A ):(-r B ):r R = 。 11、某重油催化裂化装置处理量为100吨重油/h ,未转化重油为6吨/h ,汽油产量为42吨/h ,则重油的转化率为_ _,工业上汽油的收率及选择性为_ _和_ _。 12、某反应的计量方程为A R S →+,则其反应速率表达式 。 13、反应级数 (可能/不可能)大于3, (可能/不可能)是0,基元反应的分子数 (可能/不可能)是0。 14、在一个完整的气—固相催化反应的七大步骤中,属于本征动力学范畴的三步为 、 和 。 15、在均相反应动力学中,利用实验数据求取化学反应速率方程式的两种最主要的方法为 和 。 16、对于一个在全混流反应器里进行的放热反应,一般可以出现三个定常态操作点M 1、M 2、M 3,如下图所示,其中M 1和M 3这两点我们称之为 的定常态操作点,M 2则称为 的定常态操作点。实际操作时,我们一般选择M 1、M 2、M 3中 做为操作点。 17、某一级液相反应在间歇式反应器中进行,5min 转化率为50%,则转化率达到80%需时间_____min 。 18、某反应的速率方程式为n A A r kC -= mol/(m 3 .h),则反应级数n 为2时,k 的单位为 _。 19、某反应的计量方程为A R S →+,则其反应速率表达式 。
化学反应工程原理 一、选择题 1、气相反应 CO + 3H 2 CH 4 + H 2O 进料时无惰性气体,CO 与2H 以1∶2摩尔比进料, 则膨胀因子CO δ=__A_。 A. -2 B. -1 C. 1 D. 2 2、一级连串反应A S K 1 K 2 P 在间歇式反应器中,则目的产物P 的最大浓度=m ax ,P C ___A____。 A. 1 22 )(210K K K A K K C - B. 2 2/1120 ]1)/[(+K K C A C. 122 )(120K K K A K K C - D. 2 2/1210]1)/[(+K K C A 3、串联反应A → P (目的)→R + S ,目的产物P 与副产物S 的选择性 P S =__C_。 A. A A P P n n n n --00 B. 0 A P P n n n - C. 0 0S S P P n n n n -- D. 0 0R R P P n n n n -- 4、全混流反应器的容积效率η=1.0时,该反应的反应级数n___B__。 A. <0 B. =0 C. ≥0 D. >0 5 、对于单一反应组分的平行反应A P(主) S(副),其瞬间收率P ?随A C 增大而单调下降,则最适合的反应器为 ____B__。 A. 平推流反应器 B. 全混流反应器 C. 多釜串联全混流反应器 D. 全混流串接平推流反应器 6、对于反应级数n >0的不可逆等温反应,为降低反应器容积,应选用____A___。 A. 平推流反应器 B. 全混流反应器 C. 循环操作的平推流反应器 D. 全混流串接平推流反应器 7 、一级不可逆液相反应 A 2R ,3 0/30.2m kmol C A =, 出口转化率 7.0=A x ,每批操作时间 h t t 06.20=+,装置的生产能力为50000 kg 产物R/天,R M =60,则反应器的体积V 为_C_3 m 。 A. 19.6 B. 20.2 C. 22.2 D. 23.4 8、在间歇反应器中进行等温一级反应A → B , s l mol C r A A ?=-/01.0,当l mol C A /10=时,求反应至 l mol C A /01.0=所需时间t=____B___秒。 A. 400 B. 460 C. 500 D. 560 9、一级连串反应A → P → S 在全混流釜式反应器中进行,使目的产物P 浓度最大时的最优空时 = opt τ_____D__。 A. 1 212) /ln(K K K K - B. 1 221)/ln(K K K K - C. 2 112)/ln(K K K K D. 2 11K K 10、分批式操作的完全混合反应器非生产性时间0t 不包括下列哪一项____B___。
第一章 1 1. 化学反应工程是一门研究 (化学反应个工程问题)的科学。 2 2. 所谓数学模型是指 (用数学方法表达各变量间的关系)。 3 3. 化学反应器的数学模型包括(动力学方程式、物料横算式子、4 热量衡算式、动量衡算式和参数计算式) 5 4. 所谓控制体积是指(能把反应速率视作定值的最大空间范围)。6 5. 模型参数随空间而变化的数学模型称为(分布参数模型)。 7 6. 模型参数随时间而变化的数学模型称为(非定态模型)。 8 7. 建立物料、热量和动量衡算方程的一般式为 (累积量=输入量-输出 9 量)。 10 第二章 11 1. 均相反应是指 (在均一的液相或气相中进行的反应)。 12 2. 对于反应aA + bB → pP + sS,则r P =( p/a )r A 。 13 3.着眼反应物A的转化率的定义式为(转化率Xa=转化了的物料A的量/反应开14 始的物料A的量)。 15 4. 产物P的收率Φ P 与得率Х P 和转化率x A 间的关系为( Xp/Xa )。 16 17 5. 化学反应速率式为r A =k C C A αC B β,用浓度表示的速率常数为k C ,假定符合 18 理想气体状态方程,如用压力表示的速率常数k P ,则k C =[ (RT)的a+B次方]k P 。 19 6.对反应aA + bB → pP + sS的膨胀因子的定义式为(P+S)-(A+B))/A 。 20
7.膨胀率的物理意义为 (反应物A全部转化后系统的体积变化率)。 21 8. 活化能的大小直接反映了 (反应速率) 对温度变化的敏感程度。 22 9. 反应级数的大小直接反映了(反应速率) 对浓度变化的敏感程度。 23 10.对复合反应,生成主产物的反应称为 (主反应),其它的均为(副反应)。 24 11. 平行反应A → P、A → S 均为一级不可逆反应,若E 1>E 2 ,选择性 25 S p 与 (A的浓度)无关,仅是 (A的浓度) 的函数。 26 12. 如果平行反应A → P、A → S均为一级不可逆反应,若E 1>E 2 ,提 27 高选择性S P 应(提到温度)。 28 13. 一级连串反应A → P → S在平推流反应器中,为提高目的产物P的收29 率,应(降低)k 2/k 1 。 30 14. 产物P的收率的定义式为 (生成的全部P的物质的量/反应掉的全部A 31 的物质的量) 32 15. 产物P的瞬时收率φ P 的定义式为(生成的物质的量/反应的A的物质的量) 33 16. 产物P的选择性S P 的定义式为(单位时间内产物P的物质的量/单位时 34 间内生成产物S的物质的量) 35 17. 由A和B进行均相二级不可逆反应α A A+α B B = α S S,速率方程为: 36 r A =-dC A /dt=kC A C b 。 37 求:(1)当C A0/C B0 =α A /α B 时的积分式 38 (2)当C A0/C B0 =λ≠α A /α B 时的积分式 39
《化学反应工程》试题及答案
————————————————————————————————作者:————————————————————————————————日期:
《化学反应工程》试题 一、填空题 1. 质量传递 、 热量传递 、 动量传递 和化学反应 称为三传一反. 2. 物料衡算和能量衡算的一般表达式为 输入-输出=累积 。 3. 着眼组分A 转化率x A 的定义式为 x A =(n A0-n A )/n A0 。 4. 总反应级数不可能大于 3 。 5. 反应速率-r A =kC A C B 的单位为kmol/m 3·h ,速率常数k 的因次为 m 3/kmol ·h 。 6. 反应速率-r A =kC A 的单位为kmol/kg ·h ,速率常数k 的因次为 m 3/kg ·h 。 7. 反应速率2 /1A A kC r =-的单位为mol/L ·s ,速率常数k 的因次为 (mol)1/2·L -1/2·s 。 8. 反应速率常数k 与温度T 的关系为2.1010000 lg +- =T k , 其活化能为 83.14kJ/mol 。 9. 某反应在500K 时的反应速率常数k 是400K 时的103倍,则600K 时的反应速率常数k 时是400K 时的 105 倍。 10. 某反应在450℃时的反应速率是400℃时的10倍,则该反应的活化能为(设浓度不变) 186.3kJ/mol 。 11. 非等分子反应2SO 2+O 2==2SO 3的膨胀因子2SO δ等于 -0.5 。 12. 非等分子反应N 2+3H 2==2NH 3的膨胀因子2H δ等于 –2/3 。 13. 反应N 2+3H 2==2NH 3中(2N r -)= 1/3 (2H r -)= 1/2 3NH r 14. 在平推流反应器中进行等温一级不可逆反应,反应物初浓度为C A0,转化率为x A ,当反应器体积增大到n 倍时,反应物A 的出口浓度为 C A0(1-x A )n ,转化率为 1-(1-x A )n 。 15. 在全混流反应器中进行等温一级不可逆反应,反应物初浓度为C A0,转化率为x A ,当反应器体积增大到n 倍时,反应物A 的出口浓度为 A A x n x )1(11-+-,转化率为A A x n nx )1(1-+。 16. 反应活化能E 越 大 ,反应速率对温度越敏感。 17. 对于特定的活化能,温度越低温度对反应速率的影响越 大 。 18. 某平行反应主副产物分别为P 和S ,选择性S P 的定义为 (n P -n P0)/ (n S -n S0) 。 19. 某反应目的产物和着眼组分分别为P 和A 其收率ΦP 的定义为 (n P -n P0)/ (n A0-n A ) 。 20. 均相自催化反应其反应速率的主要特征是随时间非单调变化,存在最大的反应速率 。 21. 根据反应机理推导反应动力学常采用的方法有 速率控制步骤 、 拟平衡态 。 22. 对于连续操作系统,定常态操作是指 温度及各组分浓度不随时间变化 。 23. 返混的定义: 不同停留时间流体微团间的混合 。
第一章 绪论 1. 化学反应工程是一门研究______________的科学。(化学反应的工程问题) 2. 化学反应工程是一门研究化学反应的工程问题的科学,既以_______作为研究对象,又以_______为研究对象的学科体系。(化学反应、工程问题) 3. _______是化学反应工程的基础。( 三传一反) 4. 化学反应过程按操作方法分为_______、_______、_______操作。(分批式操作、连续式操作、半分批式) 5. 化学反应工程中的“三传一反”中的三传是指_______、_______、_______。(传质、传热、动量传递) 6. 不论是设计、放大或控制,都需要对研究对象作出定量的描述,也就要用数学式来表达个参数间的关系,简称_______。(数学模型) 7. 在建立数学模型时,根据基础资料建立物料、热量和动量衡算式的一般式为_______。(累积量=输入量-输出量) 第二章 均相反应动力学 1. 均相反应是指_。(参与反应的物质均处于同一相) 2. aA + bB pP + sS 对于反应,则=P r _______)(A r -。(a p ) 3.着眼反应组分K 的转化率的定义式为_______。( 00 K K K K n n n -=χ) 4.当计量方程中计量系数的代数和等于零时,这种反应称为_______,否则称为_______。(等分子反应、非等分子反应) 5. 化学反应速率式为βαB A C A C C K r =-,用浓度表示的速率常数为C K ,假定符合理想气体状态方程,如用压力表示的速率常数P K ,则C K =_______P K 。()()(βα+RT ) 6. 化学反应的总级数为n ,如用浓度表示的速率常数为C K ,用逸度表示的速率常数f K ,则 C K =_______f K 。(n RT )() 7. 化学反应的总级数为n ,如用浓度表示的速率常数为C K ,用气体摩尔分率表示的速率常数y K ,则 C K =_______y K 。(n p RT ???? ??) 10. 活化能的大小直接反映了______________对温度的敏感程度。(反应速率) 12.生成主产物的反应称为_______,其它的均为_______。(主反应、副反应) 13. 平行反应A P(主) S(副)均为一级不可逆反应,若主E >副E ,选择性S p 与_______无关,仅是_______
、绪论 1. 研究对象是工业反应过程或工业反应器 研究目的是实现工业反应过程的优化 2. 决策变量:反应器结构、操作方式、工艺条件 3. 优化指标一一技术指标:反应速率、选择性、能耗 掌握转化率、收率与选择性的概念 4. 工程思维方法 1. 反应类型:简单反应、自催化、可逆、平行、串联反应 基本特征、分析判断 2. 化学反应速率的工程表示 3. 工业反应动力学规律可表示为: r i f c (G ) f T (T ) a )浓度效应——n 工程意义是:反应速率对浓度变化的敏感程 度。 b )温度效应——E 工程意义是:反应速率对温度变化的敏感程 度。 E ---- cal/mol , j/mol T ----- K R = 1.987cal/mol.K = 8.314 j/mol.K 化学反应动力学 反应速率= 反应量 (反应时间)(反应 已知两个温度下的反应速率常数 k , 可以按下式计算活化能 工程问题 动力学问题
三、PFR与CSTR基本方程 1.理想间歇:t V R V o c Af dC A CA0( J ) x Af dx A XA0( J ) 2.理想PFR V R V o C Af dc A C A0 ( J) C A0 x Af dx A x A 0(「A) 3. CSTR 4. 图解法 V R C A0 C A C A0X A T /C A0 0 X Af X A 四、简单反应的计算 n=1,0,2级反应特征C A C A0(1 X A)浓度、转化率、反应时间关系式 基本关系式PFR(间歇)CSTR V R C Af dC A V R C A0 C A p V。C A0 (:)m v (「A) PFF H CSTR CSTR>PFR C A0X A k p C A0 X A k p n=0 n=1 n=2 C A0 kC A . 11 k p 丁 C A C A0 k p 1吒C A0
27060 化学反应工程 南京工业大学编(高纲号0322) Ⅰ课程性质、地位和任务 “化学反应工程”是化学工程学科的一个分支,是化学工程与工艺专业学生必修的一门专业基础技术课程。它以工业反应过程为主要研究对象,研究反应过程速率及其变化规律;研究反应器内的传递特性及其对化学反应的影响。为学生今后从事化工反应技术开发、反应器的设计与放大、反应过程操作优化等诸方面工作奠定基础。 本课程在学生学习了“高等数学”、“大学物理”、“化学”、“物理化学”、“化工原理”等课程基础上进行。课程总学时为100,即5学分。 通过本课程的学习,学生应比较牢固地掌握化学反应工程的基本原理和计算方法,应能联系化工实际,在反应工程理论的指导下,对反应过程和反应器进行初步的分析和设计计算。 Ⅱ自学考试要求 第一章绪论 (一)主要内容 1.化学反应工程的研究内容 2.化学反应工程的研究方法 3.化学反应工程的学科系统的编排 (二)自学考试要求 1.化学反应工程的研究内容 理解化学反应工程学是研究化学反应的工程问题的科学;传递过程(即反应器内的动量、热量和质量传递,简称“三传”)与反应动力学是构成化学反应工程最基本的两个支柱等说法的含义。理解化学反应工程学与相关学科的联系,化学反应工程本身的专门范畴。 2.化学反应工程的研究方法 理解化学反应工程的基本研究方法是数学模型法,数学模型的主要内容及其相互关系, 了解数学模拟放大法的大体步骤。 3.化学反应工程的学科系统和编排 理解按反应操作方式、反应器型式、和化学反应相态进行分类的方法;本课程编排的原 则和方法。 绪论部分在初次学习时,只能做到大体了解、待全部内容学习完毕后,应重新学习绪论, 才能做到理解。 第二章均相反应的动力学基础
《化学反应工程》试题库 一、填空题 1. 质量传递、热量传递、动量传递和和化学反应称为三传一 反? 2. 物料衡算和能量衡算的一般表达式为输入-输出二累 积_____________ 。 3. 着眼组分A 转化率X A的定义式为 X A=( n A—n A)/ _____________ 。 4. 总反应级数不可能大于£—。 5. 反应速率-r A=kC A C B的单位为kmol/(m3? h).速率常数k的因次为 nV(kmol ? h ) 。 6. 反应速率-r A=kC A的单位为kmol/kg ? h.速率常数k的因次为mVkg ? h 。 7. 反应速率.kc A/2的单位为mol/L ? s.速率常数k的因次为 (mol) 1/2? L-1/2? s 。 8. 反应速率常数k与温度T的关系为lnk 10000 102.其活化能为 T mol 。 9. 某反应在500K时的反应速率常数k是400K时的103倍.则600K
时的反应速率常数k时是400K时的10 5倍。 10. 某反应在450C时的反应速率是400C时的10倍.则该反应的活化 能为(设浓度不变)mol 。 11. 非等分子反应2SO+Q==2SQ的膨胀因子sq等于________ 。 12. 非等分子反应N2+3H2==2NH的膨胀因子H2等于-2/3 。 13. 反应N b+3H2==2NH中(& )= 1/3 (仏)二1/2 扁3 14. 在平推流反应器中进行等温一级不可逆反应.反应物初浓度为G°. 转化率为X A.当反应器体积增大到n倍时.反应物A的出口浓度为 C A0(1-X A)n . 转化率为1-(1- X A”。 15. 在全混流反应器中进行等温一级不可逆反应.反应物初浓度为C A0. 转化率为X A.当反应器体积增大到n倍时.反应物A的出口浓度为 匚些.转化率为nxA—。 1 (n 1)X A 1 (n 1)X A 16. 反应活化能E越大.反应速率对温度越敏感。 17. 对于特定的活化能.温度越低温度对反应速率的影响越大。 18. 某平行反应主副产物分别为P和S选择性S的定义为(n P-g)/ (n s- n s0)
化学工程的发展与展望 化学工程的发展与展 化学工程是将化学过程和物理过程的基础理论研究与工业化学相结合的学科,不仅是一门具有百年历史的成熟基础学科,也是充满朝气、与时俱进的学科。 1 化学工程的兴起 几千年来过滤、蒸发、结晶等操作在生产中被广泛的应用,但在相当长的时期里,这些操作都是规模很小的手工作业。化学工程这一学科,是在 19 世纪后期随着大规模制造化学工业产品的生产过程的发展而诞生的。 19 世纪70 年代,各种基础化学品的生产等都有了相当的规模,化学工业有了许多杰出的成就。如索尔维法制碱中所用的纯碱碳化塔,高 20 余米,在其中同时进行化学吸收 、结晶、沉降等过程,但是人们还没有从其中找出共有的规律。1880 年,“化学工程” 第一次被英国学者 George E.Davis 正式提出,1888 年,美国麻省理工学院开设了第一个以“化学工程”命名的课程,标志着化学工程学科的诞生。1915 年,本文由论文联盟https://www.doczj.com/doc/a76859307.html, 收集整理美国学者 Arthur D. Little 提出了“单元操作”,将各种化学品的工业生产工艺分解为若干独立的物理操作单元,并阐明了即使是不同的工艺,只要是相同操作单元就遵循的相同原理。 1920 年,在美国麻省理工学院,化学工程从化学系分离出来,成为一个独立的系。1923 年华克尔、刘易斯和 W.H.麦克亚共同写的《化工原理》一书出版,奠定了化学工程作为一门独立的工程学科的基础。 2化学工程的发展 2.120 世纪前叶,化学工程二级学科应运而生 在20 世纪前叶,化学工程学科的发展促进了许多化学工艺的问世,如美国用丙烯合成出异丙醇,被誉为是石油化工的开端。这些化学工艺的出现,许多化学工程二级学科应运而生。 化学热力学,化学反应工程,传递过程,化工系统工程,化工控制工程等多个二级学科相继诞生。 2.220 世纪50~60 年代,化学工程完成了从单元操作到
第一章 1. 化学反应工程是一门研究 (化学反应个工程问题)的科学。 2. 所谓数学模型是指 (用数学方法表达各变量间的关系)。 3. 化学反应器的数学模型包括 (动力学方程式、 物料横算式子、 热量衡算式、 动量衡算式 和 参数计算式) 4. 所谓控制体积是指 (能把反应速率视作定值的最大空间范围)。 5. 模型参数随空间而变化的数学模型称为 ( 分布参数模型)。 6. 模型参数随时间而变化的数学模型称为 (非定态模型)。 7. 建立物料、热量和动量衡算方程的一般式为 (累积量=输入量-输出量)。 第二章 1. 均相反应是指 (在均一的液相或气相中进行的反应)。 2. 对于反应aA + bB → pP + sS ,则r P =( p/a )r A 。 3.着眼反应物A 的转化率的定义式为(转化率Xa=转化了的物料A 的量/反应开始的物料A 的量)。 4. 产物P 的收率ΦP 与得率ХP 和转化率x A 间的关系为( Xp/Xa )。 5. 化学反应速率式为r A =k C C A αC B β,用浓度表示的速率常数为k C ,假定符合理想气体状态方 程,如用压力表示的速率常数k P ,则k C =[ (RT)的a+B 次方]k P 。 6.对反应aA + bB → pP + sS 的膨胀因子的定义式为 (P+S )-(A+B))/A 。 7.膨胀率的物理意义为 (反应物A 全部转化后系统的体积变化率)。 8. 活化能的大小直接反映了 (反应速率) 对温度变化的敏感程度。 9. 反应级数的大小直接反映了(反应速率) 对浓度变化的敏感程度。 10.对复合反应,生成主产物的反应称为 (主反应),其它的均为(副反应)。 11. 平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,选择性S p 与 (A 的浓度) 无关,仅是 (A 的浓度) 的函数。 12. 如果平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,提高选择性S P 应(提到 温度)。 13. 一级连串反应A → P → S 在平推流反应器中,为提高目的产物P 的收率,应(降 低)k 2/k 1。 14. 产物P 的收率的定义式为 (生成的全部P 的物质的量/反应掉的全部A 的物质的量) 15. 产物P 的瞬时收率φP 的定义式为(生成的物质的量/反应的A 的物质的量) 16. 产物P 的选择性S P 的定义式为(单位时间内产物P 的物质的量/单位时间内生成产物S 的物质的量) 17. 由A 和B 进行均相二级不可逆反应αA A+αB B = αS S ,速率方程为: r A =-dC A /dt=kC A C b 。 求: (1)当C A0/C B0=αA /αB 时的积分式 (2)当C A0/C B0=λ≠αA /αB 时的积分式 18. 反应A → B 为n 级不可逆反应。已知在300K 时要使A 的转化率达到20%需12.6min ,而在340K 时达到同样的转化率仅需3.20min ,求该反应的活化能E 。 第三章 1. 理想反应器是指(理想混合反应器 平推流反应器)。 2. 全混流反应器的空时τ是 (反应器容积) 与(进料的体积流量)之比。 3. 全混流反应器的放热速率Q G ={ 00()A A Hr Ft y x ? }。 4. 全混流反应器的移热速率Q r ={ 012()pm Ft C T T - } 5. 全混流反应器的定常态操作点的判据为{ G r Q Q = }。 6. 全混流反应器处于热稳定的定常态操作点的判据为{ G r Q Q = G r dQ dQ dT dT > }。
化学反应工程考试题
第一章 绪论 1.“三传一反”是化学反应工程的基础,其中所谓的一反是指__反应动力学__。 2.“三传一反”是化学反应工程的基础,下列不属于三传的是_______。 “三传”指的是质量传递、流量传递、动量传递 3. 一级连串反应在全混流釜式反应器中,则目的 产物P 的最大浓度_____、 _ _。 4. 一级连串反应在平推流反应器中,则目的产物 P 的最大浓度__、 ____。 5. 一级连串反应在间歇式全混流反应器中,则目 的产物P 的最大浓度_ 、 _。 6. 一级连串反应在平推流反应器中,为提高目的 产物P 的收率,应__降低__。 7. 化学反应速率式为 ,如用浓度表示的速率常数为, 用压力表示的速率常数为,则=__D__。 A. B. C. D. 8.反应,,则反应级数n=__B___。 A. 0 B. 1 C. 2 D. 3 9.反应A + B → C ,已知,则反应级数n=___B____。 A S K 1 K 2 P =max ,P C 2 2/1120 ]1)/[(+K K C A = opt τ2 11K K A S K 1 K 2 P =max ,P C 1 22 )(2 10K K K A K K C -= opt t 1 221) /ln(K K K K -A S K 1 K 2 P =max ,P C 1 22 )(2 10K K K A K K C -=opt t 1 221)/ln(K K K K -A S K 1 K 2 P 12/k k β αB A C A C C K r =-C K P K P K C K β α+-)(RT ) ()(βα+RT ) ()(βα-RT )()(βα+-RT C 4H 2C 2H 4 + H 2 1 0.2-=s k 1 15.0-=s k
《化学反应工程原理》复习思考题 第一章绪论 1、了解化学反应工程的研究内容和研究方法。 2、几个常用指标的定义及计算:转化率、选择性、收率。 第二章化学反应动力学 1、化学反应速率的工程表示,气固相催化反应及气液相非均相反应反应区的取法。 2、反应速率常数的单位及其换算。 3、复杂反应的反应速率表达式(可逆、平行、连串、自催化)。 4、气固相催化反应的步骤及基本特征。 5、物理吸附与化学吸附的特点。 6、理想吸附等温方程的导出及应用(单组分吸附、解离吸附、混合吸附)。 7、气固相催化反应动力学方程的推导步骤。 8、不同控制步骤的理想吸附模型的动力学方程的推导。 9、由已知的动力学方程推测反应机理。 第三章理想间歇反应器与典型化学反应的基本特征 1、反应器设计的基本方程式。 2、理想间歇反应器的特点。 3、理想间歇反应器等温、等容一级、二级反应反应时间的计算及反应器体积的计算。 4、自催化反应的特点及最佳工艺条件的确定及最佳反应器形式的选择。 5、理想间歇反应器最优反应时间的计算. 7、可逆反应的反应速率,分析其浓度效应及温度效应。 8、平行反应选择率的浓度效应及温度效应分析。 9、平行反应反应器形式和操作方式的选择。 10、串连反应反应物及产物的浓度分布,t opt C p.max的计算。 11、串连反应的温度效应及浓度效应分析。 第四章理想管式反应器
1、理想管式反应器的特点。 2、理想管式反应器内进行一级、二级等容、变容反应的计算。 3、空时、空速、停留时间的概念及计算。 4、膨胀率、膨胀因子的定义,变分子数反应过程反应器的计算。 第五章理想连续流动釜式反应器 1、全混流反应器的特点。 2、全混流反应器的基础方程及应用。 3、全混釜中进行零级、一级、二级等温、等容反应时的解析法计算。 4、全混釜的图解计算原理及图解示意。 5、全混流反应器中的浓度分布与返混,返混对反应的影响。 6、返混产生的原因及限制返混的措施。 7、多釜串联反应器进行一级、二级不可逆反应的解析法计算。 8、多釜串联反应器的图解法计算原理。 第七章化学反应过程的优化 1、简单反应过程平推流反应器与全混流反应器的比较及反应器形式的选择。 2、多釜串连反应器串连段数的选择分析。 3、自催化反应反应器的选型分析。 4、可逆放热反应速率随温度的变化规律,平衡温度和最优温度的概念。 5、平行反应选择率的温度效应及浓度效应分析,反应器的选型,操作方式的确定。 6、串连反应影响选择率和收率的因素分析,反应器的选型及操作方式的确定。 7、平推流与全混釜的组合方式及其计算。 第八章气固相催化反应过程的传递现象 1、气固相催化反应的全过程及特点。 2、等温条件下催化剂颗粒的外部效率因子的定义。 3、外扩散、内扩散对平行反应、连串反应选择性的影响分析。 4、气体流速对外扩散的影响分析。 5、等温条件下催化剂颗粒的内部效率因子的定义。
知识点1.绪论 一、主要讲解内容 介绍化学反应工程相关的基本知识,包括化学反应工程的定义、化学反应工程学科的发展、化学反应工程的任务、化学反应工程和其他学科的关系。 二、学习要求 本章要求学生能够掌握化学反应工程的定义,明确化学反应工程的任务。 三、视频(已录制完成) 四、讲义 1.1化学反应工程的定义 在工业规模上开发和应用化学反应的工程活动。 1.2化学反应工程学科的发展 自然界的物质的运动或变化过程由物理或化学的两类,物理过程不牵涉化学反应,但化学过程却总是与物理因素有着紧密联系。所以化学反应过程是物理与化学两类因素综合体。 远溯古代,陶瓷制作、酿酒等工艺,但直到本世纪五十年代一直还未形成一门专门研究的独立学科,到1957年举行的第一次欧洲反应工程会议上确立了这一学科的名称。 1.3 化学反应工程的任务 化学反应工程学是一门研究化学反应的工程问题的科学,既以化学反应作为研究对象,又以工程问题为研究对象,把二者结合起来的学科体系。其主要任务包括:分析化学反应的特点、确定合适的反应条件;选择合适的反应器并对其进行最优化设计;对反应器进行最优操作和控制。 1.4 化学反应工程和其他学科的关系 a. 数学,微积分、方程的解析求解和数值求解、极值问题等,均是化学反应工程问题求解的基础。 b. 反应动力学:专门阐明学反应速率与各项物理因素(如温度、压力、催化剂等)之间的定量关系。为实现某一反应,要选定合易的条件及反应器的结构型式、尺寸和处
理能力等,这些都依赖于对反应动力学特性的认识。 c. 化工热力学:确定物系的各种物性常数(热容、研所引资、反应热等),看化学反应是否能进行及其反应程度。为化学反应工程提供反应热、反应平衡常数等基础数据。 d. 催化作用 e. 传递工程和流体力学:装置中有动量、热量、质量传递(三传),当规模放大时,出现放大效应。“三传一反”是三传和反应动力学。 五、小结 本章介绍了化学反应工程的定义、学科的发展、任务极其与数学、化工热力学、催化作用及传递工程等学科之间的密切关系。 六、自测题 1.三传一反是指动量传递、热量传递、质量传递和反应动力学。
(1) 简述活塞流模型和全混流模型的基本特征。 (2) 根据缩芯模型,描述S H 2和ZnO 反应的宏观步骤 (3) 对于快速的一级不可逆的气液反应,写出其宏观反应速率的表达式(指明 式中各参数的含义)。 (4) 对于一级不可逆的气固相催化反应,写出其宏观反应速率的表达式(指明 式中各参数的含义)。 1.简述理想反应器的种类 答:通常所指的理想反应器有两类:理想混合(完全混合)反应器和平推流(活 塞流或挤出流)反应器。所谓完全混合流反应器是指器内的反应流体瞬间达到完 全混合,器内物料与反应器出口物料具有相同的温度和浓度。所谓平推流反应器 是指器内反应物料以相同的流速和一致的方向进行移动,不存在不同停留时间的 物料的混合,所有的物料在器内具有相同的停留时间。 2.简述分批式操作的完全混合反应器 答:反应物料一次性投入反应器内,在反应过程中,不再向器内投料,也不出料,待达到反应要求的转化率后,一次性出料,每批操作所需生产时间为反应时间与 非生产性时间之和,非生产性时间包括加料、排料和物料加热、冷却等用于非反 应的一切辅助时间。 3.简述等温恒容平推流反应器空时、反应时间、停留时间三者关系 答:空时是反应器的有效容积与进料流体的容积流速之比。反应时间是反应物料 进入反应器后从实际发生反应的时刻起到反应达某一程度所需的反应时间。停留 时间是指反应物进入反应器的时刻算起到离开反应器内共停留了多少时间。由于 平推流反应器内物料不发生返混,具有相同的停留时间且等于反应时间,恒容时 的空时等于体积流速之比,所以三者相等。 4.对于可逆放热反应如何选择操作温度 答:1)对于放热反应,要使反应速率尽可能保持最大,必须随转化率的提高,按 最优温度曲线相应降低温度; 2)这是由于可逆放热反应,由于逆反应速率也随反应温度的提高而提高,净 反应速率出现一极大值; 3)而温度的进一步提高将导致正逆反应速率相等而达到化学平衡。 5.对于反应,21A R C k r =,1E ;A S C k r 2=,2E ,当1E >2E 时如何选择操作温度可以 提高产物的收率 答:对于平行反应A RT E E A RT E RT E S R R C e k k C e k e k r r S 12212010/20/10---===,所以,当1E >2E 时应尽可 能提高反应温度,方可提高R 的选择性,提高R 的收率。
化学反应工程 单选题 1. 对于反应级数n >0的不可逆气相等温反应,为降低反应器体积,应选用_______。(A ) (A )平推流反应器 (B )全混流反应器 (C )平推流串接全混流反应器 (D )全混流串接平推流反应器 2. 分批式操作的完全混合反应器非生产性时间不包括下列哪一项_______。(P22) (A )加料时间 (B )反应时间 (C )物料冷却时间 (D )清洗釜所用时间 3. 下列单位不属于反应速率的是_______。(P13) (A )mol/(g ﹒s) (B )m 3/s (C )mol/(m 2﹒s) (D )mol/(m 3﹒s) 4.反应 A B C →+,12.50 k s -=,则反应级数为_______。(P 13) A . 0 ( B )1 ( C )2 ( D )3 5. 反应NaOH + HCl NaCl + H 2O ,已知mol s l k /1.0?=,则反应级数 n=_______。(P 13) (A )0 (B )1 (C )2 (D )3 6. 气相基元反应 B A →2,进料时反应物A 和稀释剂C 以等摩尔比加入,则膨胀率为_______。(P58) (A )-1 (B )-0.25 (C )0.25 (D )0.5 7. 下面反应器中不属于理想反应器的是_______。(P21) (A )间歇反应器 (B )全混流反应器 (C )平推流反应器 (D )膜反应器 8. 下面哪种反应器组合形式可以最大程度降低反应器体积_______。(B ) (A )平推流反应器串联 (B )全混流反应器串联 (C )平推流反应器并联 (D )全混流反应器并联 9. 在间歇反应器中进行等温一级反应A → B ,0.01 /A A r C mol L s -=?,当C A0=1 mol/L 时,求反应至C A0=0.01 mol/L 所需时间t=_______秒。(P43) (A )400 (B )460 (C )500 (D )560
化学反应工程名词解释 1.返混:不同年龄粒子之间之间的混合;或是指反应器中逗留了不同时间,因而具有不同的性质的物料粒子之间的混合或即经历了不同的反应时间的物料粒子之间的混合,又称逆向混合。(上述只要答对一种情况给3分)。2.临界流化速度:是指刚刚能使粒子流化起来的气体空床流速。 3.模型法:就是通过对复杂的实际过程的分析,进行合理的简化,然后用一定的数学方法予以描述,使其符合实际过程的规律性,然后加以求解。4. 速率控制步骤:是指一个连串过程速率(度)最小,而且比其他步骤的速 率(度)小得多的步骤,它的速度决定着整个过程的速度,称为速率控制步骤。 5.速率方程:在溶剂及催化剂和压力一定的情况下,定量描述反应速率与温度及浓度的关系的关系式。 6.非理想流动:凡是流动状况偏离平推流和全混流这两种理想情况的流动,统称非理想流动。 7.颗粒带出速度:当气速增大到某一速度时,流体对颗粒的曳力和颗粒的重力相等,则颗粒就会被气流所带走,这一速度称带出速度。(或是指流体速度大于固体颗粒在流体中的沉降速度时,颗粒粒子被气流带出床层,这个速度叫做带出速度或称终端速度。) 8. 固定床反应器:凡是流体通过固定的固体物料所形成的床层而进行反应的装置都称固定床反应器。 9.理想反应器:是指能以活塞流或全混流来描述其流动状况的反应器。10.停留时间:是指流体以进入系统时算起,到其离开系统时为止,在系统内总共经历的时间,即流体从系统的进口至出口所耗费的时间: 11. 多段绝热反应器:是指多次在绝热条件下进行反应,反应一次之后经过换 热以满足所需温度条件,再进行下一次的绝热反应。每反应一次,称为一段,一个反应器可做成一段,也可以将数段合并在一起组成一个多段反应器固定床催化反应器: 12.空速:在规定条件下,单位时间内进入反应器的物料体积相当于几个反应器的容积,或单位时间内通过单位反应器容积的物料体积,称为空速