
一、建立计量标准的目的
为使计量器具量值传递的准确可靠,保证我单位检验检测数据的准确、可靠,本单位最高标准是根据《中华人民共和国计量法》申请建立计量标准。
二、计量标准的工作原理及其组成
该装置采用比较法对催化燃烧原理甲烷测定器进行检定,用不确定度<3%的空气中甲烷标准气体,在被检仪器规定的校准流量下与被检仪器直接比较,从而测试出被检仪器的基本误差、报警误差等参数。
检定原理图如下:
空气中甲烷标准气体
减压
微调器
催化燃烧甲
烷测定器检
定装置
催化燃烧
式甲烷测
定器
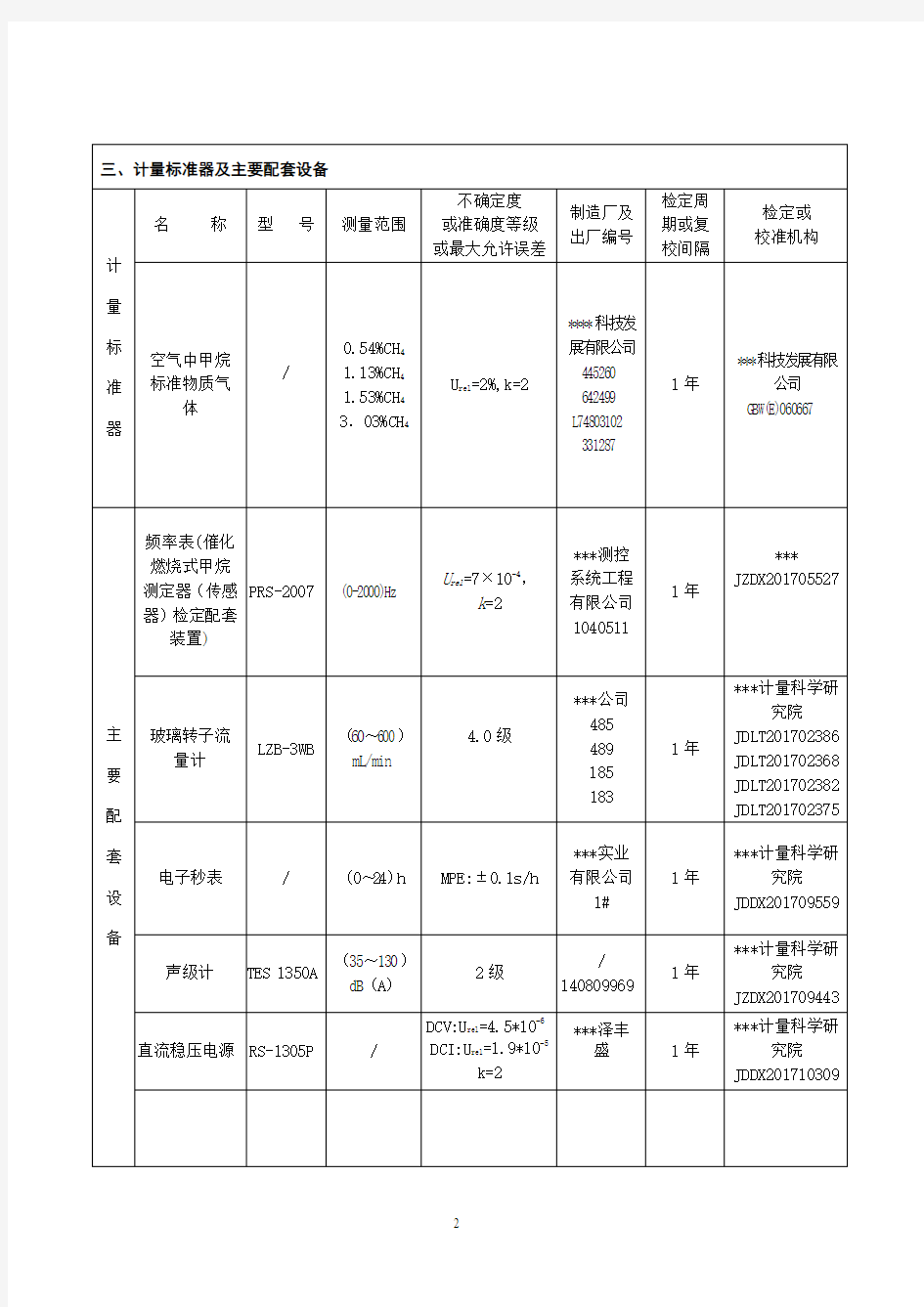
三、计量标准器及主要配套设备
计量标准器名称型号测量范围
不确定度
或准确度等级
或最大允许误差
制造厂及
出厂编号
检定周
期或复
校间隔
检定或
校准机构
空气中甲烷
标准物质气
体
/
0.54%CH4
1.13%CH4
1.53%CH4
3.03%CH4
U rel=2%,k=2
****科技发
展有限公司
445260
642499
L74803102
331287
1年
***科技发展有限
公司
GBW(E)060667
主要配套设备
频率表(催化
燃烧式甲烷
测定器(传感
器)检定配套
装置)
PRS-2007 (0-2000)Hz
U rel=7×10-4,
k=2
***测控
系统工程
有限公司
1040511
1年
***
JZDX201705527
玻璃转子流
量计
LZB-3WB
(60~600)
mL/min
4.0级
***公司
485
489
185
183
1年
***计量科学研
究院
JDLT201702386
JDLT201702368
JDLT201702382
JDLT201702375 电子秒表/ (0~24)h MPE:±0.1s/h
***实业
有限公司
1#
1年
***计量科学研
究院
JDDX201709559 声级计TES 1350A
(35~130)
dB(A)
2级
/
140809969
1年
***计量科学研
究院
JZDX201709443 直流稳压电源RS-1305P /
DCV:U rel=4.5*10-6
DCI:U rel=1.9*10-5
k=2
***泽丰
盛1年
***计量科学研
究院
JDDX201710309
四、计量标准的主要技术指标
1.空气中甲烷标准气体:
浓度范围:(0.00~4.00)%CH
4
=2%,k=2
不确定度:U
rel
2.流量调节范围:
(60~600)ml/min
准确度:4.0级
3.频率测量范围:
(0~2000)Hz
准确度:U rel=7*10-5,k=2
五、环境条件
序号项目要求实际情况结论
1 温度(15~35)℃(15~35)℃合格
2 湿度<85% <85% 合格
3 周围环境无影响检定的干扰气体无影响检定的干扰气体合格
4
5
6
六、计量标准的量值溯源和传递框图
上一级计量器具
本单位计量标准器具
工作计量器具
计量标准名称:空气中一氧化碳标
准气体
不确定度等级:U rel=1%(k=2)
保存机构:中国计量科学研究院
间接比较法
计量标准名称:空气中一氧化碳标准气
体
测量范围:(0~4)%CH4
最大允许误差:U rel=2%(k=2)
直接比较法
催化燃烧型甲烷报警仪
量程(%CH4):0≤X≤1 1<X≤2 2<X≤4 MPE(%CH4):±0.10 ±0.20 ±0.30
七、计量标准的稳定性考核
本项标准不做稳定性考核。
注:应当提供《计量标准的稳定性考核记录》。
注:应当提供《检定或校准结果的重复性试验记录》。
八、检定或校准结果的重复性试验
催化燃烧式甲烷测定器检定装置检定装置采用实物标准(国家二级标准物质——空气甲烷标准气体)作为标准器进行直接测量检定,故重复性考核如下:
在装置正常工作的条件下,选一台催化燃烧甲烷报警仪1065#
,测量范围(0~4)%CH 4使用本装置分别对仪器进行等精密度直接测量10次,10次测量如下:
试验时间:2017年9月17日
试验条件:温度:20℃ 湿度:60%RH
测量值(%CH 4)
1 2 3 4 5 6 7 8 9 10 y
s (y i ) 3.06
2.98
3.05
3.05
2.98
3.04
2.99
3.06
3.02
3.05
3.03
0.03
s (y i )=
1
)
(1
2
--∑=n y yi n
i =0.03
试验人员:陈钰
九、检定或校准结果的不确定度评定
1.测量方法
按照JJG678-2007规程,采用比较法,把不确定度不大于3%的空气中甲烷标准气体,按规定的流量通入甲烷报警仪(或测定器)。
用3次测量结果的平均值作为测量结果,温度影响可忽略不计。
2.数学模型
M x =M s +δ
M X ——测量结果;M S ——仪器显示值;δ——标准气体对测量结果的影响;
3. 测量不确定度分量
3.1仪器显示值的不确定度分量u 1
按规定流量通入0.54%CH 4、1.53 CH 4、3.05 CH 4的甲烷标准气体,对三个检定点检定的不确定度分量结果为:
3.06 2.98 3.05 3.05 2.98 3.04 2.99 3.06 3.02 3.05
平均值为:3.03%CH 4
单次测量的实验标准偏差s=0.03%CH 4
不确定度分量为:u 1=0.03/3/3.03×100%=0.57% 3.2甲烷标准气体的相对不确定度分量u 2 甲烷标准气体的相对不确定度为2%,k=2则: 不确定度分量为: u 2=2%/2=1% 3.3通气流量引入的不确定度分量u 3
流量在误差允许范围内引起市值的变化为0.01% CH 4,在1.13% CH 4测量点的相对不确定度分量最大,其相对不确定度分量为
u 3=0.01/1.12/=0.52% 4.相对不确定度分量一览
仪器显示值的重复性分量 u 1=0.57% 甲烷标准气体分量 u 2=1% 流量引入的不确定度分量 u 3=0.52% 5.合成标准不确定度u c
u
c =
%
26
.1
52
.0
1
57
.02
2
2
2
3
2
2
2
1
=
+
+
=
+
+u
u
u
6.扩展不确定度
U=ku
c
=1.26%×2=2.5%(k=2)
7.测量不确定度的报告
测量结果为3次显示值的平均值,扩展不确定度为:U=2.5% k=2
十、检定或校准结果的验证
送一台甲烷检测报警仪到法定计量检定机构检定,再由本标准检定结果分别如下:
测量点X%CH4 法定计量检定
机构测出的基
本误差Y%CH4
本标准测
出的基本
误差Y0%CH4
(Y-Y0)/X
绝对值%
本计量标准的
不确定度U%
省所不确
定度U0
2
2
U
U+%
1.13 -0.01 0.02 0.01
2.3 1.1 2.51
由上表可知:(Y-Y
0)/X≤2
2
U
U+
因此,该计量标准检定结果得到验证,可以满足计量检定的需要。
十一、结论
经过试验验证,所建计量标准符合国家计量检定系统表和计量检定的要求,能够开展相应的检定。
十二、附加说明
化学反应方程式 班级学号姓名得分 一、选择题 6.配平化学方程式,判断所配系数是否正确的依据是() A.反应前后各种物质的质量是否相等 B.反应前后各化学式前的系数之和是否相等 C.各种元素的种类是否相等 D.反应前后各种元素原子总数是否相等 二、填空题 ★22、右图中A~H都是初中化学中常见的物质,已知A、B为黑色固体,D为红色固体单质,F为红色粉末,G是最常用的金属之一。它们的转化关系如图所示。请回答: B的化学式为。 ②E+F→G是工业炼铁的原理,写出这个化学方程式。 ③G +H→D是古代湿法炼铜的方法,写出这个方程式。 ★19、学习化学能使我们更好地认识各种现象,合理地解决实际问题。右图是化学实验中常用的火柴,已知火柴头含有硫、氯酸钾、二氧化锰等,火柴盒侧面含有红磷、三硫化二锑等,试回答以下问题: (1)锑的元素符号是Sb,则三硫化二锑的化学式为。硫在空气中燃烧的化学方程式为。 (2)火柴梗主要成分是纤维素,纤维素属于。(填字母序号) A.蛋白质 B.糖类 C.油脂 (3)火柴盒侧面使用红磷而不使用白磷,其原因之一是因为红磷的着火点(填“高” 或“低”),火柴划燃后时会产生白烟,白烟的化学式为。 二.填空题与简答题(化学方程式每空2分,其余每空1分,共30分) ★17、化学与我们的生活息息相关。请从A.二氧化硫B.二氧化碳C.氢氧化钠D.碳酸氢钠E.水F.酒精
G. 石油H.煤 以上八种物质中选择适当的字母序号填空: ①治疗胃酸过多的药剂是 ②被誉为“工业的血液”的是 ③能产生温室效应的气体是 ④最常见的溶剂是 ★6.某研究学习小组经过查阅资料发现,锰(Mn )也能排入下列金属活动性顺序中: K 、Ca 、Na 、Mg 、Al 、Mn 、Zn 、 ① 、 ② 、 ③ 、( ④ )、Cu 、 ⑤ 、 ⑥、Pt 、Au (1)上述金属活动性顺序中⑥的元素符号是 ; (2)已知在化合物中锰元素显+2价.写出锰与硫酸铜(CuSO 4)溶液反应的化学方程式 ★4。A ~F 都是初中化学中的常见物质,其中B 常作饼干干燥剂,吸水后放热生成D ,F 固体易潮解,常用于肥皂工业,各物质间有如图所示转化关系(反应条件、其他反应物及多余产物均已略去)。 ⑴请写出下列物质的化学式: B ;C 。 ⑵写出D 与E 反应的化学方程式 。 ★3. Ⅰ.硫铁矿(主要成分是FeS 2)是一种铁矿石。用1000t 含FeS 260%的硫铁矿,理论上可以炼出 吨铁。(假设在反应过程中FeS 2中的铁元素全部转化成铁单质,且杂质中不含铁) Ⅱ.由于地震和海啸,日本福岛第一核电站发生严重的核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(主要成分是碘化钾KI ),以降低放射性碘-131对人体的伤害。 某兴趣小组为了测定某未知碘片中碘化钾的含量,进行了如下图实验: (查阅资料知:碘化钾易溶于水,而碘化银是不溶于水的黄色沉淀) (1)上述步骤③中“物质M”的化学式为 ,其与碘化钾反应的化学方程式是 。 (2)步骤③中“X 操作”是 。该操作与步骤①中的操作都要用到除烧杯外的另一种玻璃仪器,它是 ,它在步骤②中的作用是 。 (3)通过计算,一片未知碘片中含KI 的质量是 毫克。 ★6、已知它们是初中化学常见的物质, 是由C 、H 、O 、Fe 四种元素组成,
烃及其含氧衍生物的燃烧通式: 烃:CxHy+(x+y/4)O2→xCO2+y/2H2O 烃的含氧衍生物:CxHyOz+(x+y/4-z/2)O2 ? xCO2+y/2H2O 规律1:耗氧量大小的比较 (1)等质量的烃(CxHy)完全燃烧时,耗氧量及生成的CO2和H2O的量均决定于y/x的比值大小。比 值越大,耗氧 越多。相同质量的有机物中,烷烃中CH 4耗氧量最大;炔烃中,以C 2 H 2 耗氧量最少;苯及其同系 物中以C 6H 6 的耗氧量最少;具有相同最简式的不同有机物完全燃烧时,耗氧量相等。 (2)等质量具有相同最简式的有机物完全燃烧时,其耗氧量相等,燃烧产物相同,比例亦相同。等物质 的量的各种有机物(只含C、H、O)完全燃烧时,分子式中相差若干个“CO 2”部分或“H 2 O”部分, 其耗氧量相等。 (3)等物质的量的烃(CxHy)及其含氧衍生物(CxHyOz)完全燃烧时的耗氧量取决于x+y/4-z/2,其值越 大,耗氧量越多。 (4)等物质的量的不饱和烃与该烃和水加成的产物(如乙烯与乙醇、乙炔与乙醛等)或加成产物的同分异 构完全燃烧,耗氧量相等。即每增加一个氧原子便内耗两个氢原子。 规律2:气态烃(CxHy)在氧气中完全燃烧后(反应前后温度不变且高于100℃): 若y=4,V总不变;(有CH4、C2H4、C3H4、C4H4) 若y<4,V总减小,压强减小;(只有乙炔) 若y>4,V总增大,压强增大。 有机分子结构的确定: 物理方法:红外光谱仪→红外光谱确定化学键或官能团 核磁共振仪→核磁共振仪氢谱确定不同化学环境的氢原子种数及个数比 相对分子质量的测定——质谱法
催化燃烧的基本原理 催化燃烧是典型的气-固相催化反应,其实质是活性氧参与的深度氧化作用。在催化燃烧过程中,催化剂的作用是降低活化能,同时催化剂表面具有吸附作用,使反应物分子富集于表面提高了反应速率,加快了反应的进行。借助催化剂可使有机废气在较低的起燃温度条件下,发生无焰燃烧,并氧化分解为CO2和H20, 同时放出大量热能,其反应过程为: 2 催化燃烧的特点及经济性 2.1催化燃烧的特点 2.1.1起燃温度低,节省能源 有机废气催化燃烧与直接燃烧相比,具有起燃温度低,能耗也小的显著特点。在某些情况下,达到起燃温度后便无需外界供热。 二、催化剂及燃烧动力学 2.1催化剂的主要性能指标 在空速较高,温度较低的条件下,有机废气的燃烧反应转化率接近100%,表明该催化剂的活性较高[9]。催化剂的活性分诱导活化、稳定、衰老失活3 个阶段,有一定的使用限期,工业上实用催化剂的寿命一般在2年以上。使用期的长短与最佳活性结构的稳定性有关,而稳定性取决于耐热、抗毒的能力。对催化燃烧所用催化剂则要求具有较高的耐热和抗毒的性能。有机废气的催化燃烧一般不会在很严格的操作条件下进行,这是由于废气的浓度、流量、成分等往往不稳定,因此要求催化剂具有较宽的操作条件适应性。催化燃烧工艺的操作空速较大,气流对催化剂的冲击力较强,同时由于床层温度会升降,造成热胀冷缩,易使催化剂载体破裂,因而催化剂要具有较大的机械强度和良好的抗热胀冷缩性能。 2.2催化剂种类 目前催化剂的种类已相当多,按活性成分大体可分3 类。2.2.1贵金属催化剂 铂、钯、钌等贵金属对烃类及其衍生物的氧化都具有很高的催化活性,且使用寿命长,适用范围广,易于回收,因而是最常用的废气燃烧催化剂。如我国最早采用的Pt-Al203 催化剂就属于此类催化剂。但由于其资源稀少,价格昂贵,耐中毒性差,人们一直努力寻找替代品或尽量减少其用量。2.2.2过渡金属氢化物催化剂 作为取代贵金属催化剂,采用氧化性较强的过渡金属氧化物,对甲烷等烃类和一氧化碳亦具有较高的活性,同时降低了催化剂的成本,常见的有Mn0x、CoOx和CuOx等催化剂。大连理工大学研制的含Mn02催化剂,在130C及空速13000h-1 的条件下能消除甲醇蒸气,对乙醛、丙酮、苯蒸气的清除也很有效果。
第2讲燃烧和灭火实验 【核心重点】 一、燃烧的条件(同时符合)二、灭火的原理(符合其一)(1)可燃物(1)清除可燃物 (2)与氧气(或空气)接触(2)隔绝氧气(或空气) (3)达到燃烧所需的最低温度(也叫着火点)(3)降温至着火点以下 反应装置: ①③/③④对比 说明可燃物燃烧 必须与氧气接触; ①②对比说明 可燃物燃烧必须 达到着火点; 【实验改进】 通常状况下, 白磷的着火点 为40℃,红磷 的着火点为 240℃。某化学 兴趣小组的同 学按下图所示 实验探究可燃物燃烧的条件。得到的实验事实如下: ①实验Ⅰ、Ⅲ中,放在热水中的白磷不燃烧; ②常温时1、2号试管内的白磷、红磷不燃烧; ③热水中的1号试管内白磷燃烧,2号试管内红磷不燃烧; ④实验Ⅲ中,玻璃管上的气球变鼓; ⑤实验Ⅳ中,倒扣在热水中的3号试管内的白磷燃烧。 上述实验中,能说明可燃物燃烧必须达到着火点的相关事实是 ①和② B. ②和③ C. ①和④ D. ①和⑤
【答案】B 【考查难点】 【实例训练】 某化学兴趣小组的同学利用如下图所示装置(固定装置已略去)探究燃烧等相关实验。已知,白磷(过量)的着火点40℃;该装置气密性良好,瓶内空气体积为230mL ,注射器中水的体积为50mL ,且生石灰适量。 实验步骤及部分现象记录如下表。请回答下列问题。 ⑴ 步骤Ⅰ中,导致小蜡烛熄灭的原因是 。 ⑵ 步骤Ⅱ中,可观察到气球的变化是 ;白磷燃烧的原因是 ;白磷燃烧的化学方程式为 。 ⑶ 在步骤Ⅲ中,该兴趣小组的同学继续实验,测定空气中氧气的含量。具体操作是:待白磷熄灭并冷却后,_______________,观察到_________________现象。 【答案】(1)生成CO 2受热上升,隔绝O 2 ; (2)先变鼓,后变瘪;生石灰与水反应放热,使温度升高达到白磷着火点,并与O 2接触;4P+5O 2点燃 2P 2O 5 (3)打开弹簧夹;注射器中的水自动喷出来,还剩下约4mL 时停止下流。 实验现象 原因 Ⅰ 高蜡烛先熄灭 生成CO 2受热上升,隔绝O 2 Ⅱ 矮蜡烛先熄灭 CO 2密度大于空气,隔绝O 2 实验步骤 操作 现象 步骤Ⅰ 点燃燃烧匙中的小蜡烛后,立即伸入集气瓶中并塞紧塞子。 燃着的小蜡烛很快就熄灭了。 步骤Ⅱ 打开弹簧夹,由注射器向集气瓶中加入少量水,夹紧弹簧夹。 白磷燃烧。 步骤Ⅲ … …
考点20 燃烧与燃料 (18仙桃)20.充分燃烧1kg天然气和煤所产生CO2和SO2的质量如上图所示。下列说法不.正确 ..的是 A.等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大 B.煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体 C.煤、天然气及石油等是重要的化石燃料,属于不可再生能源 D.由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量 (18长春)6.有关甲烷(CH4)的说法中,正确的是 A.甲烷分子由碳原子和氢原子构成 B.相对分子质量是16g C.碳元素和氢元素的质量比是1︰4 D.碳元素比氢元素的质量分数小 (8黄冈)25、一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO2的质量为 A.5.6g B.8.8g C.4.4g D.4.8g (18安顺)3、纯净物X在氧气中完全燃烧的化学方程式为:X + 2O2 CO2 + 2H2O。下列说法不正确的是() A.该反应前后原子的种类发生改变 B.X是最简单的有机化合物 C.该反应的生成物都是氧化物 D.X是天然气的主要成分 (18宁波)8.下图是某化学反应的微观示意图。下列说法中错误的是 A.甲是最简单的有机物 B.反应前后原子种类没有发生改变 C.反应生成的丙和丁的分子个数比为1:2 D.一个甲分子是由两个氢分子和一个碳原子构成
(18雅安)1.据《易经》记载:“泽中有火”,“上火下泽”。泽,指湖泊池沼。“泽中有火” 是对“X气体”在湖泊池沼水面上起火现象的描述。这里“X气体”是指 A.一氧化碳B.甲烷C.氧气D.氢气 (18哈尔滨)30.(3分)下图是甲烷与氧气反应的微观模拟图,请回答下列问题: (1)在甲、丙图中将相关粒子图形补充完整甲补充一个氧分子、丙中补充一个水分子 (2)A、B、C、D对应的物质都是由分子构成的 (3)画出比一个C分子多两个质子的离子结构示意图。 (18海南)18.天然气不仅可以作燃料,而且是一种重要的化工原料。 (1)天然气重整可以得到合成气,其反应的微观示意图如下: 反应物生成物 写出上述反应的化学方程式。 (2)用不同催化剂可使合成气合成不同的物质。下列物质仅以合成气为原料不 .能.得到的 .可 是(填序号)。 A.甲醛(CH2O) B.甲醇(CH3OH) C.尿素[CO(NH2)2] (18海南)19.现有一份氧元素质量分数为89.5%的过氧化氢溶液,加入M nO2 充分反应后,得到液体的质量为 90g(不考虑操作过程中液体的损失),则生成氧气的质量为 。 g(精确到小数点后1位) (18广东)19.(5分)天然气可以在一定条件下合成甲醇。 (1)请把“题19图”中反应物的微观示意图补画齐全。
do i:10.3969/j .iss n.1002-154X .2009.08.016 甲烷催化燃烧催化剂催化理论与 应用研究进展 陆富生 (淮安市产品质量监督检验所,江苏淮安223001) 摘 要 概述了甲烷催化燃烧催化剂的研究现状,从组成甲烷燃烧催化剂的3个部分(基体、活性组分、氧化物载体)分别加以论述。通过掺杂一些金属和金属氧化物,不但可以提高高活性贵金属催化剂的热分解温度,还可以提高高温催化剂(如钙钛矿和六铝酸盐材料等)的催化活性。最后简要综述了甲烷催化燃烧反应机理。关键词 催化燃烧 甲烷 贵金属催化剂 金属氧化物催化剂 收稿日期:2009-07-15 作者简介:陆富生(1981~),男,硕士生,从事催化材料方面的研究,E -mail:fnlfs@https://www.doczj.com/doc/dc17129688.html, Research Progess of the Cat for M ethane Cat alyti c Co mbusti on i n the Theory and Appli cati on Lu Fusheng (Huaian I nstitute of Supervisi on and I ns pecti on on Pr oduct Quality,J iangsu Huaian 223001) Abstract The recent research p r ogress and devel opments of the catalysts f or methane catalytic com -busti on were described .The catalysts f or methane catalytic combusti on which was composed in three parts (base,active constit 2uent and oxide support )were als o discussed .It is shown that the additi on of metals and metal -oxides i m p r oves the ther mal stability of noble metal catalysts and metal -oxide catalysts such as per ovskites and hexaalum inates,and brings benefit t o activity in methane catalytic combusti on .Finally,the reacti on mechanis m f or methane catalytic com 2busti on was summarized si m p ly . Keywords catalytic combusti on methan noble metal catalysts metal -oxide catalysts 随着人们对环境污染和能源短缺问题的日益重视,天然气以储量丰富、价格低廉、使用方便、热效率高、污染小等优点,被认为是目前最清洁的能源之一。但由于其主要成分甲烷的燃烧温度很高(1600℃),天然气在空气中的燃烧产物NO x ,CO 等也可造成环境污染。催化燃烧被认为是解决这一问题最有效的途径。 甲烷是最稳定的烃类,通常很难活化或氧化,且甲烷催化燃烧工作温度较高,燃烧反应过程中会产生大量水蒸气,同时天然气中含少量硫,因此甲烷催化燃烧催化剂必须具备较高的活性和较高的水热稳定 性,以及一定的抗中毒能力。而通常催化剂活性与稳定性是矛盾的,因此开发高效稳定的甲烷低温催化燃烧催化剂引起国内外研究者极大的兴趣,同时进行了大量相关研究,并取得了一定的成果。 1甲烷燃烧催化剂体系 甲烷燃烧的催化剂体系一般由活性组分、氧化物载体和基体组成。1.1 基体 (1)陶瓷基体 最常用的是堇青石(5Si O 2?3A l 2O 3?2Mg O )陶 第23卷第8期2009年8月 化工时刊 Chem i ca l I ndu s try Ti m e s Vo l .23,No.8 Aug.8.2009
收稿日期:2002207219. 第一作者:周长军,男,1976年生,硕士,现在美国攻读博士学位.联系人:朱月香.Tel:(010)62751718;Fax:(010)62753937;E 2mail:zhu yx@https://www.doczj.com/doc/dc17129688.html,. 基金项目:国家重点基础研究发展规划项目(G2000077503)和国家自然科学基金资助项目(29803001). 文章编号:025329837(2003)0320229204 研究论文:229~232 SnCuO 催化剂上甲烷的催化燃烧性能 周长军, 林 伟, 朱月香, 谢有畅 (北京大学化学与分子工程学院分子动态与稳态结构国家重点实验室,北京100871) 摘要:采用双股并流共沉淀法制备了SnCuO 系列催化剂,测定了它们对甲烷燃烧反应的催化活性及抗硫中毒性能,并采用 XRD,BET,XPS,DTA 2TG 和FT 2IR 等技术对催化剂进行了表征.比表面积和活性测试结果表明,SnCuO 系列样品的比表面 积均大于纯氧化物,其低温催化活性大大高于纯氧化物.在Sn ΠCu 原子数比接近1时,其比表面积最大(超过100m 2 Πg ).具有最大比表面积的样品SnCu4和SnCu5的活性最高.进一步测定了SnCu4样品的抗硫中毒性能.结果发现,在500℃下,反应刚开始时甲烷的转化率为98%,随着SO 2的不断通入,催化剂的活性逐渐降低,到12h 后基本稳定,此时甲烷转化率仅为 50%.采用FT 2IR 和热重分析方法对SnCu4硫中毒的机理进行了研究,发现其中毒原因在于SnCuO 系列催化剂中的CuO 与SO 2反应几乎完全转化为CuSO 4,导致催化剂活性降低. 关键词:甲烷,催化燃烧,氧化锡,氧化铜,硫中毒中图分类号:O643 文献标识码:A CatalyticCombustionofMethaneoverSnCuOCatal ysts ZHOUChan gjun ,LINWei ,ZHUYuexian g 3 ,XIEYouchan g (State Key Laborator y for Structural Chemistr y of Unstable and Stable S pecies,College of Chemistr y and Molecular Engineerin g ,Peking Universit y ,Beijin g 100871,China ) Abstract :Catalyticcombustionofmethaneisaneffectivewa ytoutilizeitasanener gysource,orto preventit from pollutin gtheatmos phere.Itwasfoundthatthebinar ymetaloxidesbasedonSnO 2displayed quitehi ghac 2tivit yforthedee poxidationofmethane.Thebinar ySnCuOcatal ystswere preparedb yamodifiedco 2precipitati 2onmethodandcharacterizedb yXRD,BET,XPS,DTA 2TGandFT 2IR.Thecatal yticactivit yofthecatal ysts formethanecombustionaswellastheirresistancetosulfur poisoningwereinvesti gated.Theresultsshowedthat thesurfaceareasofallSnCuOcatal ystsarebi ggerthan pureSnO 2orCuO,es peciallyforthesam pleswith n (Sn )Πn (Cu )≈1,theirs pecificsurfaceareasarebi ggerthan100m 2 Πg.Thecatal yticactivit yofthecatal ystsat lowtem peratureishi gherthan pureSnO 2orCuO.SnCu4andSnCu5withthebi ggests pecificsurfaceareashow thehi ghestcatal yticactivit y.Forsam pleSnCu4,theresistancetosulfur poisoning,whichisanim portantfactor forthecatal ysts,wasalsoinvesti gated.SO 2wasaddedintothesource gas (φ(SO 2)=0102%)andthecatal ytic activit ywasmeasuredat500℃.TheCH 4conversionwas98%atthebe ginnin g,butdecreased graduallyand keptstableafter12hwithCH 4conversionof50%.Themechanismofsulfur poisoningwasfurtherstudiedb y FT 2IRandDTA 2TGmethodsanditwasfoundthatthedeactivationofthecatal ystsunderSO 2isduetotransfor 2mationofCuOintoCuSO 4. Ke ywords :methane,catal yticcombustion,tinoxide,co pperoxide,sulfur poisoning 通过催化燃烧将有机废气转化为无害的CO 2和水是处理有机废气的有效方法.甲烷是一种工业 生产中大量排放的废气,采用催化燃烧的方法将其 转化,不仅可以消除它对大气的污染,而且还可以回 第24卷第3期 Vol.24No.3 催 化 学 报 ChineseJournalofCatal ysis 2003年3月 March2003
甲烷的化学性质 【实验目的】 1、探究甲烷的重要化学性质。 2、掌握对物质燃烧产物的定性检验方法。 3、熟悉有关实验操作,提高实验操作的基本技能。 4、培养仔细观察实验现象、认真思考现象产生原因的科学态度。 【知识支持】 1、如何检测可燃性气体的燃烧产物? 2、如何收集按一定比例组成的甲烷和氯气的混合气体? 【实验内容】 试剂:甲烷,澄清石灰水,酸性高锰酸钾溶液,溴水,饱和食盐水(收集氯气用),氯气等。仪器:储气瓶(分别盛有甲烷、氯气),干燥的小烧杯,大试管(带橡胶塞),铁 架台(带铁夹),小试管 实验步骤: 实验1 (1)从盛有甲烷的储气瓶中缓缓放出甲烷气体,在导气管尖嘴处将其点 燃,观察气体燃烧时火焰的颜色。 现象。 结论。 (2)检验燃烧产物的操作: 。 现象 。 结论及解释 实验2 将甲烷气体分别通入酸性KMnO4溶液和溴水中,观察现象。 现象。 结论。
实验3 (1)取一支大试管,用排饱和食盐水的方法收集体积比1:4的甲烷和氯气,用橡胶塞塞好管口,放在光亮的地方(不可日光直射,以免引起爆炸)约3分钟,观察发生的现象。 现象 。 结论 。(2)将上述试管倒立在水槽中,并取下橡胶塞,观察现象。 现象 。 结论及解释 。 请完成反应方程式。 注意:CH2Cl2 、CHCl3、CCl4是液体。 【问题探究】 1、(1)能否利用CH4和Cl2在光照条件下的取代反应制取纯净的氯仿?为什么? (2)在此实验中,若将NaCl溶液换成Na2SiO3溶液,有什么现象产生? 2、家庭使用天然气做燃料时,应注意哪些事项? 3、CCl4为什么不能燃烧?CO2、SF6等也不能在空气中燃烧,其原因与CCl4一样吗? 4、同样是液态有机物,四氯化碳和氯仿都是良好的有机溶剂,而二氯甲烷却不是,为什么? 。
七单元测试题 一、选择题:(20分) 1、古语道:“人要实,火要虚。”此话的意思是说做人要脚踏地,才能事业有成;可燃物要架空一些,才能燃烧更旺,“火要虚”的目的是( ) A、降低可燃物的着火点 B、增大可燃物的能量 C、增大空气中氧气的含量 D、增大加燃物与空气的撞触面积 2、储存烟花爆竹的仓库应贴上的标志是() 3、如图,将两支燃着的蜡烛罩上茶杯,过了一会儿高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是()A、用湿毛巾后住鼻子B、成站立姿势跑出 C、伏低身子逃出 D、淋湿衣服爬出 4、学习化学的目的,并不在于要成为化学家,更重要的是善于用化学知 识去分析、解决生产、生活中的问题。从化学角度看,下列说法错误的 是() A、进入小煤窑严禁吸烟 B、夜晚发现液化气泄漏,立即开灯检查 C、面粉厂、加油站严禁吸烟 D、炒菜时油锅着火,可盖锅盖灭火 5、为确保生命安全,下列处理事故的方法正确的是() A、进入深洞,燃着的火把熄灭后继续前进 B、厨房内管道煤气(主要成分是CO)泄漏,马上点火燃尽 C、桌面上酒精灯内酒精洒出,着火燃烧,立即用湿抹布盖灭 D、电线线路老化导致火灾发生时,应立刻用水灭火 6、《中学生日常行为规范》中规定,中学生不准吸烟。因为吸烟不仅危害身体健康,而且乱扔烟头容易引发火灾。烟头在火灾中所起的作用是() A、提供可燃物 B、提供氧气 C、降低可燃物的着火点 D、使可燃物达到燃烧的温度 7、氢气是一种绿色能源,科学家们最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气
的新技术,其中海水分解可以用化学方程式表示为:2H2O 2H2↑+O2↑下列说法中,不正确的 是() A、TiO2在反应中作氧化剂 B、水分解不产生污染物 C、TiO2在反应中作催化剂 D、该技术可以将太阳能转化为氢能 8、以下行为与对应的原理解释不相关联或错误的是()。 A.喷射二氧化碳扑灭木材火灾------二氧化碳不可、也不支持燃烧,且隔绝空气 B. 洒水扑灭火灾------降低可燃物的着火点 C. 用隔离带扑灭森林火灾------使可燃物脱离燃烧环境 D. 用黄沙扑灭酒精着火------使之与空气隔绝 9、下列各组物质的名称、俗名、化学式不能表示同一种物质的是() A.甲烷、甲醇、CH4 B.乙醇、酒精、C2H5OH C.甲烷、沼气、CH4 D.一氧化碳、煤气、CO 10、2012年5月18日开始,伦敦奥运圣火只在英国境内传递。采集圣火的唯一方式是在奥林匹克的赫拉神庙前利用凹面镜集中阳光来引燃火种。下列说法不正确的是() A.阳光为火种的燃烧提供了热量,使其达到着火点 B.火炬燃烧时,化学能转化为热能和光能 C.强风和大雨下火炬仍可以保持燃烧,是因为火炬燃料的燃烧不受燃烧的条件影响 D.火炬内装的燃料丙烷(C3H8)属于可燃物 二、填空题(33分) 1、在氧气、氢气、二氧化碳、一氧化碳、甲烷等气体中,选择正确答案用化学式填在相应的空格里,并写出有关反应的化学方程式。 (1)能灭火的气体是________。(2)天然气的主要成分是_________________。 (3)人类维持生命,不可缺少的气体是_____________。 (4)能使带火星的木条复燃的气体是___________________。 (5)能在空气中燃烧,产物不会污染空气的理想燃料是______,该燃料发生燃烧,反应的化学方程为:______________________________。 (6)能溶于水,水溶液能使紫色石蕊试液变成红色的气体是________,该气体与水反应的化学方程 式为:____________________________。 (7)能使澄清石灰水变浑浊的气体是___________,反应的化学方程式为:_________________________________。 (8)煤气的主要成分是_________,它与氧化铜反应的化学方程式为:
【教学资源】 探究甲烷燃烧的产物 湖北省石首市文峰中学刘涛 果果查阅资料知道:2017年5月,我国在南海海域成功开采可燃冰。可燃冰外观像冰,主要成份是甲烷水合物(甲烷分子和水分子组成),可表示为CH4?nH2O,在开采过程中,若甲烷泄漏会导致严重的温室效应。果果对甲烷燃烧的产物产生了兴趣,设计实验探究:【提出问题】甲烷燃烧后生成哪些物质? 【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO; ②白色无水CuSO4粉末遇水变蓝色; ③C O与人体内的血红蛋白结合,会造成人中毒缺氧。 【猜想与假设】猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O 【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过C﹣G装置(部分夹持、固 定装置省略)进行验证: ⑴装置A、B中标有数字的仪器名称①酒精灯,②锥形瓶。 若选用过氧化氢溶液和二氧化锰来制取氧气,应选用的发生装置是(填序号)。该反应的化学方程式为,该反应的基本类型为。 ⑵实验过程中观察到C中白色粉末变为蓝色,D、G中澄清石灰水变浑浊,F中红色粉末 变成黑色,由此推断猜想(填数字序号)成立。 ⑶实验过程中D装置的作用是;该反应的化学方程式是。 ⑷实验过程中用纯净O2而不用空气的原因是。 ⑸实验过程中C、D装置的顺序不能颠倒,原因是。 【反思与交流】日常生活中,使用含碳燃料一定要注意通风,防止中毒。 参考答案 ⑴酒精灯;锥形瓶;B;2H2O22H2O+O2↑;化合反应; ⑵三; ⑶检验二氧化碳;CO2+Ca(OH)2=CaCO3↓+H2O;
⑷空气中含有水蒸气和二氧化碳,影响检验结果。 ⑸气体通过澄清石灰水时会带出水蒸气。 【反思与交流】一氧化碳(或CO)。 同步训练 1.我国首次在南海成功试采海域可燃冰。可燃冰是一种主要含有甲烷水合物的化石燃料,下列关于可燃冰的认识,正确的是() A.一种化合物B.一种高效清洁能源 C.一种可再生能源D.一种可以燃烧的固态水 2.2017年,我国海域可燃冰开采取得重大突破。下列有关可燃冰的叙述正确的是()A.可燃冰是一种纯净物 B.可燃冰在常温常压下不易长久保存 C.可燃冰的成功开发利用使“水变油”成为可能 D.可燃冰作为一种清洁能源对环境没有任何危害 3.我国首次在南海神孤海域试采“可燃冰”(天然气水合物)成功。下列关于“可燃冰”说法正确的是() A.“可燃冰”外形像冰,是天然气冷却后得到的固体 B.“可燃冰”燃烧后几乎不产生残渣和废气,被誉为“绿色能源” C.通常状况下,天然气和水就能结合成“可燃冰“” D.“可燃冰”储量巨大,属于可再生能源 4.目前,我国在可燃冰的开采技术上处于世界领先水平。可燃冰将成为未来新能源,外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等物质。可燃冰在低温和高压条件下形成.1体积可燃冰可储载100~200倍体积的甲烷气体,具有能量高,燃烧值大等优点。 ⑴可燃冰属于_____(填“可再生”或“不可再生”)资源。为缓解能源危机,人们还必须积极开发利用新能源,请写出两种新能源_______________;
广州和风环境技术有限公司 https://www.doczj.com/doc/dc17129688.html,/ 催化燃烧的性质是什么 催化燃烧是借助催化剂在低温下(200~400℃)下,实现对有机物的完全氧化,因此,能耗少,操作简便,安全,净化效率高,在有机废气特别是回收价值不大的有机废气净化方面,比如化工,喷漆、绝缘材料、漆包线、涂料生产等行业应用较广,已有不少定型设备可供选用。 一、催化原理及装置组成 (1)催化剂定义催化剂是一种能提高化学反应速率,控制反应方向,在反应前后本身的化学性质不发生改变的物质。 (2)催化作用机理催化作用的机理是一个很复杂的问题,这里仅做简介。在一个化学反应过程中,催化剂的加入并不能改变原有的化学平衡,所改变的仅是化学反应的速度,而在反应前后,催化剂本身的性质并不发生变化。那么,催化剂是怎样加速了反应速度呢了既然反应前后催化剂不发生变化,那么催化剂到底参加了反应没有?实际上,催化剂本身参加了反应,正是由于它的参加,使反应改变了原有的途径,使反应的活化能降低,从而加速了反应速度。例如反应A+B →C是通过中间活性结合物(AB)过渡而成的,即:A+B→[AB]→C 其反应速度较慢。当加入催化剂K后,反应从一条很容易进行的途径实现:A+B+2K →[AK]+[BK]→[CK]+K→C+2K 中间不再需要[AB]向C的过渡,从而加快了反应速度,而催化剂并未改变性质。 (3)催化燃烧的工艺组成不同的排放场合和不同的废气,有不同的工艺流程。但不论采取哪种工艺流程,都由如下工艺单元组成。 ①废气预处理为了避免催化剂床层的堵塞和催化剂中毒,废气在进入床层之前必须进行预处理,以除去废气中的粉尘、液滴及催化剂的毒物。 ②预热装置预热装置包括废气预热装置和催化剂燃烧器预热装置。因为催化剂都有一个催化活性温度,对催化燃烧来说称催化剂起燃温度,必须使废气和床层的温度达到起燃温度才能进行催化燃烧,因此,必须设置预热装置。但对于排出的废气本身温度就较高的场合,如漆包线、绝缘材料、烤漆等烘干排气,温度
初三化学第四章第一节《燃烧与灭火》练习题 姓名________学号_______ 同步练习(一) 1、通常使可燃物燃烧的条件是() (1)可燃物跟氧气(或空气)接触(2)将可燃物加热 (3)使可燃物跟气体接触(4)达到可燃物的着火点 (A)(1)和(2)(B)(3)和(4) (C)(2)和(4)(D)(1)和(4) 2、下列物质中,着火点最低的是() (A)白磷(B)红磷(C)木材(D)煤炭 3、下列现象中,一定由化学变化引起的是() (A)发光发热(B)爆炸(C)燃烧(D)蒸发 4、关于燃烧,下列说法正确的是() (A)可燃物燃烧时,一定有发光、发热的现象 (B)都是有氧气参与的反应 (C)可燃物燃烧时一定有火焰产生 (D)在纯氧中任何物质都可以燃烧 5、下列场所中,宜贴上“严禁烟火”标语的是() (A)石灰窑厂(B)炼铁厂 (C)面粉加工厂(D)制冰厂 6、点燃下列混合气体,有可能发生爆炸的是() (A)汽油蒸气和氮气(B)氢气和乙醚蒸气 (C)酒精蒸气和空气(D)二氧化碳和天然气 7、点燃的火柴竖直向上,火柴梗不易继续燃烧,其原因主要是() (A)火柴梗温度达不到着火点(B)火柴梗着火点较高 (C)火柴梗潮湿不易燃烧(D)火柴梗接触氧气较少 8、写出下列反应的化学方程式,并描述实验现象 (1)白磷在空气中燃烧 化学方程式____________________ , 现象_______________________________________; (2)金属钠在氯气中燃烧 化学方程式_____________________, 现象_______________________________________; (3)镁带在二氧化碳中燃烧 化学方程式____________________ , 现象____________________________________________。 9、钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气,钠+水→氢氧化钠+氢气, 但是它与煤油不会发生反应。 用刀切一块金属钠投入盛有蒸馏水的烧杯中,可以看到钠块浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成银白色小球,甚至会使钠和水生成的氢气都发生燃烧。 如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮
2014年11月第22卷第11期 工业催化INDUSTRIAL CATALYSIS Nov.2014Vol.22 No.11综述与展望 收稿日期:2014-04-08 作者简介:蒋 赛,1988年生,男,在读博士研究生。 通讯联系人:季生福,教授,博士研究生导师。甲烷催化燃烧反应工艺研究进展 蒋 赛,郭紫琪,季生福* (北京化工大学化工资源有效利用国家重点实验室,北京100029) 摘 要:甲烷催化燃烧是一种清洁高效的甲烷燃烧技术,在节能减排中具有重要的应用价值。从催化剂、反应工艺和过程强化等方面对近年来甲烷催化燃烧技术进行综述,重点介绍颗粒催化剂固定床反应工艺、整体式催化剂反应工艺、流化床反应工艺和吸放热耦合反应工艺研究进展。用于固定床反应器的颗粒催化剂主要为负载型贵金属催化剂和非贵金属氧化物催化剂。贵金属催化剂活性好,起燃温度低,适合低浓度甲烷的催化燃烧。非贵金属氧化物催化剂耐高温性好,适合较高浓度甲烷燃烧体系。整体式催化剂的甲烷催化燃烧反应工艺中,最常用的是蜂窝陶瓷和金属合金等整体式催化剂的多段式催化燃烧反应器的设计。设计直接采用多段式整体催化剂,催化剂的位置不同,发挥的催化作用也不同。流化床催化燃烧装置具有燃烧过程接触面积广、热容量大和换热效率高等特点,可有效避免传统的固定床催化燃烧反应工艺存在的问题,非常适合应用于低浓度甲烷的催化燃烧过程。利用甲烷催化燃烧强放热的特点,将催化燃烧产生的热量进行时间或空间的耦合,可以开发出吸-放热耦合反应工艺。其中,固定床催化反应器中的流向变换强制周期操作作为一种高效的过程强化技术,在节约反应器成本的同时,可以提高反应热量的利用率。 关键词:能源化学;甲烷;催化燃烧;反应工艺;固定床;流化床 doi :10.3969/j.issn.1008-1143.2014.11.002 中图分类号:TQ517.5;X701 文献标识码:A 文章编号:1008-1143(2014)11-0816-09 Progress in reaction process for catalytic combustion of methane JIANG Sai ,GUO Ziqi ,JI Shengfu * (State Key Laboratory of Chemical Resource Engineering ,Beijing University of Chemical Technology ,Beijing 100029,China ) Abstract :Compared with the conventional flame combustion ,the catalytic combustion of methane is a clean and efficient methane burning technology.It possesses an importance application value in the energy saving and the emission reduction.In this paper ,the recent research progress in methane catalytic com-bustion such as the catalysts ,catalytic combustion process ,and methane catalytic combustion process intensification technologies were reviewed.Moreover ,the methane catalytic combustion reaction process of the fixed bed with the particle catalysts ,the monolithic catalysts ,the fluidized bed ,and the coupling of exothermic and endothermic reaction process were focused.The particle catalysts used in the fixed bed reactor mainly were noble metal catalysts and non-noble metal oxide catalysts.Noble metal catalysts with high activity and low light-off temperature were suitable for catalytic combustion of methane with low con-centration.Non-noble metal oxide catalysts with good resistance to high temperature were suitable for com-bustion system of methane with high concentration.Monolithic catalysts for methane catalytic combustion commonly used honeycomb ceramics and metal alloy as monolithic carriers.Monolithic catalysts were
万方数据
万方数据
万方数据
万方数据
甲烷-空气贫燃料预混燃烧的数值模拟 作者:吴振宇, 王成军, 王朝晖, 王丹丹, WU Zhen-yu, WANG Cheng-jun, WANG Zhao-hui , WANG Dan-dan 作者单位:吴振宇,王成军,王丹丹,WU Zhen-yu,WANG Cheng-jun,WANG Dan-dan(沈阳航空航天大学,辽宁,沈阳,110136), 王朝晖,WANG Zhao-hui(中国航空动力机械研究所,湖南,株洲,412002)刊名: 沈阳航空航天大学学报 英文刊名:JOURNAL OF SHENYANG INSTITUTE OF AERONAUTICAL ENGINEERING 年,卷(期):2011,28(2) 被引用次数:1次 参考文献(9条) 1.张健;周力行突扩回流与大速差射流回流湍流气-固两相流动的数值模拟 1996(02) 2.张健;周力行突扩燃烧室湍流预混燃烧温度场的测量[期刊论文]-航空动力学报 1995(04) 3.王朝晖;王成军;王丹丹燃气轮机燃烧室燃烧气体燃料的数值模拟[期刊论文]-沈阳航空工业学院学报 2010(02) 4.Kee R J;Rupley F M;Miller J A The Chemkin thermodynamic data base 1990 5.Peters N Fifteen Lectures on Laminar and Turbulent Combustion 1992 6.李宇红;祁海鹰;张宏武甲烷预混燃烧火焰的详细数值模拟[期刊论文]-工程热物理学报 2002(01) 7.Igor V Novosselov;Philip C Malte,Development and Application of an Eight-step Global Mechan-ism for CFD and CRN Simulations of Lean-pre-mixed Combustors ASME GT2007-27990 2007 8.蒲宁;徐让书;吴超航空发动机燃烧室流动数值计算中湍流模型的比较[期刊论文]-沈阳航空工业学院学报 2008(05) 9.ANSYS.Inc FLUENT 6.3 User's Guide 2006 本文读者也读过(10条) 1.雷艳.张红光.白小磊.韩雪娇.王欣甲烷-氢气体燃料的定容燃烧研究[会议论文]-2010 2.邓凯脉动燃烧下甲烷部分预混火焰Nox生成机理和排放规律研究[学位论文]2010 3.任广旭.霍志成.刘秀娟.Ren Guangxu.Huo Zhicheng.Liu Xiujuan基于相似理论的航空发动机燃烧室工作过程试验模化研究[期刊论文]-工程与试验2010,50(2) 4.徐华胜.小城徐华胜燃烧室技术专家[期刊论文]-航空制造技术2011(5) 5.张磊磊.谭迎新.王星河.王高.ZHANG Leilei.TAN Yingxin.WANG Xinghe.WANG Gao甲烷-空气混合气燃烧过程的高速摄影测量[期刊论文]-测试技术学报2011,25(3) 6.吉倩.赵晨光.张宝诚.马洪安.JI Qian.ZHAO Chen-guang.ZHANG Bao-cheng.MA Hong-an某航空发动机环形燃烧室CO和UHC的数值计算[期刊论文]-沈阳航空航天大学学报2011,28(2) 7.乔伟彪.马贵阳.陈杨.杜明俊.齐国栋.QIAO Wei-biao.MA Gui-yang.CHEN Yang.DU Ming-jun.QI Guo-dong燃烧器不同因素对燃料转化率影响的数值计算[期刊论文]-化学工程2011,39(5) 8.李成兵.吴国栋.周宁.罗勇.LI Chengbing.WU Guodong.ZHOU Ning.LUO Yong N2/CO2/H2O抑制甲烷燃烧数值分析[期刊论文]-中国科学技术大学学报2010,40(3) 9.张红光.白小磊.韩雪娇.孙娜.ZHANG Hong-guang.BAI Xiao-lei.HAN Xue-jiao.SUN Na甲烷掺混氢气的燃烧特性试验研究[期刊论文]-兵工学报2011,32(2) 10.胡婷婷.吕海港.张彦.双少敏.董川CH_4+O_2→·CH_3+HO_2·反应机理:CASPT2量子化学研究[期刊论文]-分析化学2009,37(z1) 引证文献(1条)