
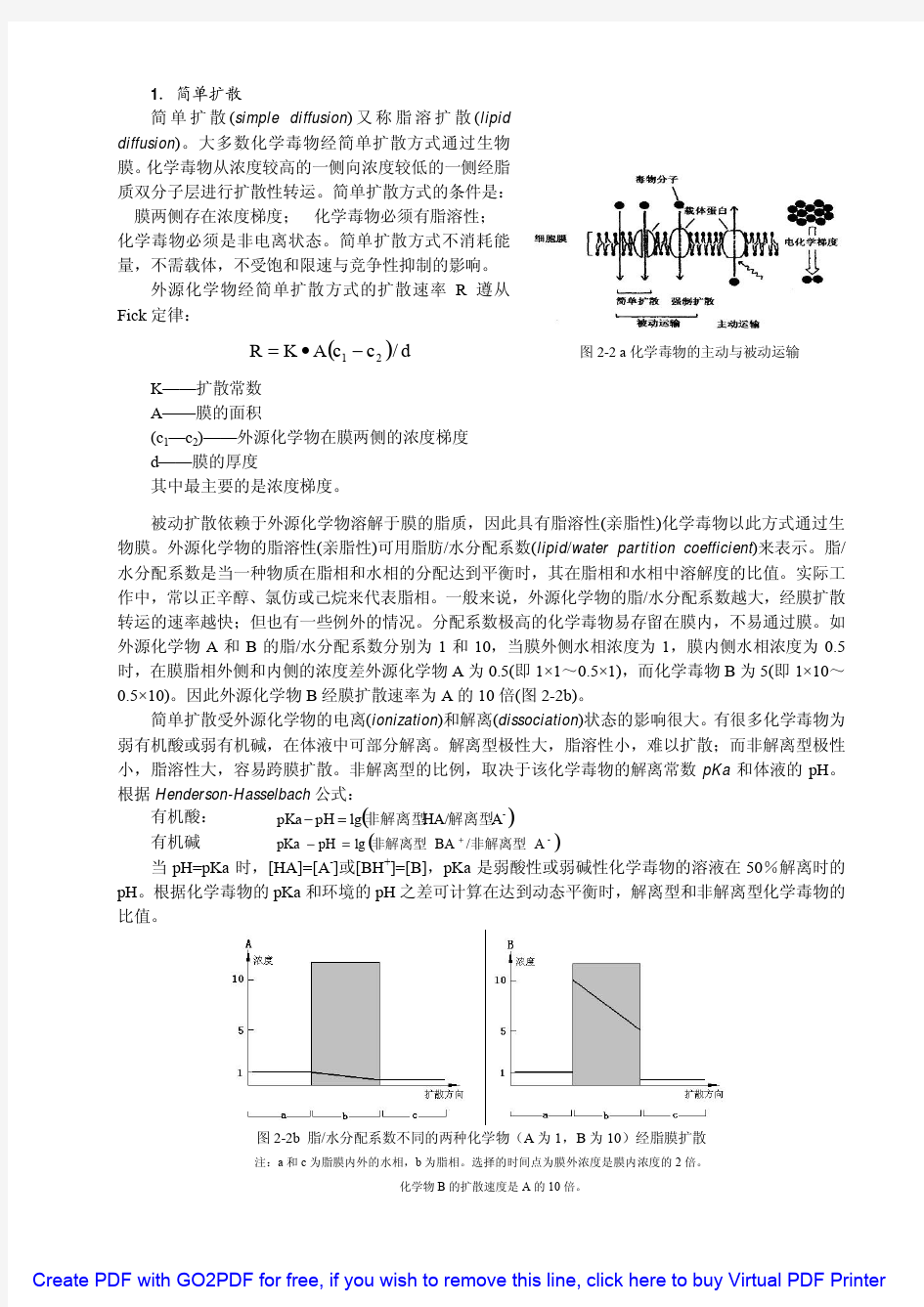
第二章课后习题答案 1.计算赖氨酸的ε-NH3+20%被解离时的溶液PH。 解:pH = pKa + lg20% pKa = 10.53 pH = 10.53 + lg20% = 9.9 2.计算谷氨酸的γ-COOH三分之二被解离时的溶液pH。 解:pH = pKa + lg((2/3)/(1/3))=4.6 pKa = 4.25 3.计算下列物质0.3mol/L溶液的pH:(a)亮氨酸盐酸盐;(b)亮氨酸钠盐;(c)等电亮氨酸。解:a:pH=2.36+ lg(C(H+)/0.3)=1.46 b: pH=9.60+lg(0.3/C(OH+))=11.5 c:pH=pI=1/2(2.36+9.60)=5.98 4.计算下列氨基酸的pI值:丙氨酸、半胱氨酸、谷氨酸和精氨酸。 解:pI = 1/2(pKa1+ pKa2) pI(Ala) = 1/2(2.34+9.69)= 6.02 pI(Cys) = 1/2(1.71+10.78)= 5.02 pI(Glu) = 1/2(2.19+4.25)= 3.22 pI(Ala) = 1/2(9.04+12.48)= 10.76 5. 向1L1mol/L的处于等电点的甘氨酸溶液加入0.3molHCl,问所得溶液的pH是多少?如果加入0.3mol NaOH以代替HCl时,pH将是多少? 解:pH1=pKa1+lg(7/3)=2.71 pH2=pKa2+lg(3/7)=9.23 6.计算0.25mol/L的组氨酸溶液在pH6.4时各种离子形式的浓度(mol/L)。 解:由pH=pK1+lg(His+/ His2+)=pKr+lg(His0/His+)=pK2+lg(His-/ His0)得His2+为1.87×10-6,His+为0.071,His0为0.179 His-3.0×10-4 7.说明用含一个结晶水的固体组氨酸盐酸盐(相对分子质量=209.6;咪唑基pKa=6.0)和1mol/L KOH配制1LpH6.5的0.2mol/L组氨酸盐缓冲液的方法 解:取组氨酸盐酸盐41.92g(0.2mol),加入352ml 1mol/L KOH,用水稀释至1L。 8. L-亮氨酸溶液(3.0g/50ml 6mol/L HCl)在20cm旋光管中测得的旋光度为+1.81o。计算L-亮氨酸在6mol/L HCl中的比旋。 解:c=3.0/50=0.06g/ml l=2dm. +1.81=[a]*0.06*2 得:[a]= +15.1o 9.甘氨酸在溶剂A中的溶解度为在溶剂B中的4倍,苯丙氨酸在溶剂A中的溶解度为溶剂B 中的两倍。利用在溶剂A和B之间的逆流分溶方法将甘氨酸和苯丙氨酸分开。在起始溶液中甘氨酸含量为100mg ,苯丙氨酸为81mg ,试回答下列问题:(1)利用由4个分溶管组成的逆流分溶系统时,甘氨酸和苯丙氨酸各在哪一号分溶管中含量最高?解:根据逆流分溶原理,可得: 对于Gly:Kd = C A/C B = 4 = q(动相)/p(静相) p+q= (1/5 + 4/5) 4个分溶管分溶3次:(1/5 + 4/5)3=1/125+2/125+48/125+64/125
氨基酸;分子中同时含有氨基和羧基的有机化合物(或分子中含有氨基的羧酸),叫氨基酸。两性电解质;氨基酸分子既含有酸性的-COOH,又含有碱性的-NH2。前者能提供质子变成-COO-,后者能接受质子变成-NH+3。因此,被称为两性电解质。 等电点;使分子处于兼性分子状态,在电场中不迁移(分子的净电荷为零)的pH值,称为该分子的等电点。 茚三酮反应;在加热条件下,氨基酸或肽与茚三酮反应生成蓝紫色(与脯氨酸反应生成黄色)化合物的反应。 构型;一个有机分子中各个原子特定的空间排布。这种排布不经过共价键的断裂和重新形成是不会改变的。 蛋白质的一级结构;是指肽链中的氨基酸种类、数量和排列顺序,它是由编码它的基因决定的。不同蛋白质具有不同的一级结构。其内容包括:(1)多肽链的数目;(2)每一条多肽链中末端氨基酸的种类;(3)链内和链间二硫键的位置和数目;(4)多肽链中氨基酸的数目、种类和排列顺序。 蛋白质的超二级结构:指二级结构的组合,已知的超二级结构有三种基本形式:αα,βαβ,βββ。二级结构是通过骨架上的羰基和酰胺基团之间形成的氢键维持的。 结构域:在蛋白质三级结构内的独立折叠单元。结构域通常都是几个超二级结构单元的组合。蛋白质的三级结构:蛋白质分子处于它的天然折叠状态的三维构象。三级结构是在二级结构的基础上进一步盘绕、折叠形成的。 蛋白质的四级结构:多亚基蛋白质的三维结构。实际上是具有三级结构的多肽链(亚基)以适当方式聚合所呈现出的三维结构。 盐溶:在蛋白质水溶液中,加入少量的中性盐,如硫酸铵、硫酸钠、氯化钠等,会增加蛋白质分子表面的电荷,增强蛋白质分子与水分子的作用,从而使蛋白质在水溶液中的溶解度增大。这种现象称为盐溶。 凝胶电泳:以凝胶为介质,在电场作用下分离蛋白质或核酸等分子的分离纯化技术。 大多数蛋白质中氮的含量较恒定,平均为16%,如测得1克样品含氮量为10mg,则蛋白质含量为6.25g。 蛋白质的二级结构最基本的有两种类型,它们是α-螺旋结构和β-折叠结构。 α-螺旋结构是由同一肽链的_C=O_和_N=H_间的氢键维持的,螺距为0.54nm,每圈螺旋含3.6个氨基酸残基,每个氨基酸残基沿轴上升高度为0.15n m。天然蛋白质分子中的α-螺旋大多属于右手螺旋(旋光性)。 维持蛋白质一级结构的化学键有肽键和二硫键;维持二级结构靠氢键;维持三级结构和四级结构靠次级键,其中包括氢键;离子键;疏水键;范德华力。 电泳法分离蛋白质的原理,是在一定的pH条件下,不同蛋白质的带电荷量、分子大小和分子形状不同,因而在电场中移动的方向和速率不同,从而使蛋白质得到分离。 变性蛋白质的主要特征是生物活性改变,其次是物理化学性质改变和溶解度降低。 蛋白质主要构象的结构单元包括α-螺旋;β-折叠;β-转角;无规卷曲。 蛋白质的一级结构内容:蛋白质一级结构指蛋白质多肽链中氨基酸残基的排列顺序。因为蛋白质分子肽链的排列顺序包含了自动形成复杂的三维结构所需要的全部信息,一级结构决定其高级结构。 蛋白质的空间结构:蛋白质的空间结构是指蛋白质分子中原子和基团在三维空间上的排列、分布及肽链走向。蛋白质的空间结构决定蛋白质的功能。空间结构与蛋白质各自的功能是相适应的。 α-螺旋结构;β-折叠结构:多肽链主链绕中心轴旋转,形成棒状螺旋结构,每个螺旋含有3.6个氨基酸残基,共有13个原子。螺距为0.54nm,氨基酸之间的轴心距为0.15nm;α-螺旋结构的稳定主要靠链内氢键,每个氨基酸的N-H与前面第四个氨基酸的C=O 形成氢键;
第八章外源化学物致癌作用 一、名词解释 1.化学致癌物 2.终致癌物 3.引发剂 4.促长剂 5.助致癌物 二、选择题 1. 确证的人类致癌物必须有 A.人类流行病学及动物致癌实验方面充分的证据 B.经动物实验及流行病学调查研究,并有一定的线索 C.充分流行病学调查研究的结果 D.已建立了动物模型 2. 60年代初期,震惊世界的反应停(thalidomide)事件,首次让人们认识到A.化学物的致畸性 B.化学物的致癌性 C.化学物的致突变性 D.药物的致癌性 3. 判别化学物质致癌性所使用的系统不包括 A.一般毒性试验 B.短期试验 C.动物诱癌试验 C.人类流行病学研究 4. 化学致癌的阶段学说,认为化学致癌是多阶段过程,至少分为三个阶段,这三个阶段的先后次序为 A.启动、进展、促癌 B.启动、促癌、进展
C.促癌、进展、启动 D.促癌、启动、进展 E.进展、启动、促癌 5. 恶性转化细胞的特征不包括 A.细胞形态改变 B.细胞生长能力改变 C.细胞生化表型改变 D.细胞坏死 6. 关于癌症病因的下列叙述中,正确的是 A.癌症是由单种病因诱发的 B.癌症是由生物因素诱发的 C.癌症是由物理因素、化学因素和环境因素诱发的 D.人类癌症90%与环境因素有关,其中主要是辐射致癌和病毒致癌E.人类癌症90%与环境因素有关,其中主要是化学因素 7、关于前(间接)致癌物的叙述,正确的是 A.必须经代谢活化才具有致癌活性的化学物质称为前致癌物 B.细胞色素P-450依赖性加氧酶是最重要的代谢解毒酶 C.催化二相结合反应的代谢酶没有代谢活化作用 D.前致癌物是亲电子剂,与DNA能直接反应 E.致癌物经代谢活化产生的活性代谢产物为终致癌物 8. The process of decision point carcinogen testing A. is limited to the evaluation of promoters of carcinogenicity. B. evaluates only in vitro tests for carcinogenicity. C. requires evaluation of all possible tests for carcinogenesis. D. evaluates a number of systematic, sequential tests for carcinogenicity. 9. The correct sequential chronological steps in carcinogenesis are A. bioactivation, progression, promotion, initiation. B. initiation, bioactivation, progression, promotion.
第二章核酸的结构与功能 一、名词解释 1.核酸2.核苷3.核苷酸4.稀有碱基5.碱基对6.DNA的一级结构7.核酸的变性8.Tm值9.DNA的复性10.核酸的杂交 二、填空题 11.核酸可分为____和____两大类,其中____主要存在于____中,而____主要存在于____。12.核酸完全水解生成的产物有____、____和____,其中糖基有____、____,碱基有____和____两大类。 13.生物体内的嘌呤碱主要有____和____,嘧啶碱主要有____、____和____。某些RNA分子中还含有微量的其它碱基,称为____。 14.DNA和RNA分子在物质组成上有所不同,主要表现在____和____的不同,DNA分子中存在的是____和____,RNA分子中存在的是____和____。 15.RNA的基本组成单位是____、____、____、____,DNA的基本组成单位是____、____、____、____,它们通过____键相互连接形成多核苷酸链。 16.DNA的二级结构是____结构,其中碱基组成的共同特点是(若按摩尔数计算)____、____、____。 17.测知某一DNA样品中,A=0.53mol、C=0.25mol、那么T= ____mol,G= ____mol。18.嘌呤环上的第____位氮原子与戊糖的第____位碳原子相连形成____键,通过这种键相连而成的化合物叫____。 19.嘧啶环上的第____位氮原子与戊糖的第____位碳原子相连形成____键,通过这种键相连而成的化合物叫____。 20.体内有两个主要的环核苷酸是____、____,它们的主要生理功用是____。 21.写出下列核苷酸符号的中文名称:A TP____、dCDP____。 22.DNA分子中,两条链通过碱基间的____相连,碱基间的配对原则是____对____、____对____。 23.DNA二级结构的重要特点是形成____结构,此结构属于____螺旋,此结构内部是由____通过____相连维持,其纵向结构的维系力是____。 24.因为核酸分子中含有____和____碱基,而这两类物质又均含有____结构,故使核酸对____波长的紫外线有吸收作用。 25.DNA双螺旋直径为____nm,双螺旋每隔____nm转一圈,约相当于____个碱基对。戊糖和磷酸基位于双螺旋____侧、碱基位于____侧。 26、核酸双螺旋结构中具有严格的碱基配对关系,在DNA分子中A对____、在RNA分子中A对____、它们之间均可形成____个氢键,在DNA和RNA分子中G始终与____配对、它们之间可形成____个氢键。 27.DNA的Tm值的大小与其分子中所含的____的种类、数量及比例有关,也与分子的____有关。若含的A-T配对较多其值则____、含的G-C配对较多其值则____,分子越长其Tm 值也越____。 28.Tm值是DNA的变性温度,如果DNA是不均一的,其Tm值范围____,如果DNA是均一的其Tm值范围____。 29.组成核酸的元素有____、____、____、____、____等,其中____的含量比较稳定,约占核酸总量的____,可通过测定____的含量来计算样品中核酸的含量。 30.DNA双螺旋结构的维系力主要有____和____。 31.一般来说DNA分子中G、C含量高分子较稳定,同时比重也较____、解链温度也____。
考试范围 一、生物大分子的结构与功能 1.蛋白质 2.核酸 3.酶 二、物质代谢 4.糖代谢 5.脂类代谢 6.氨基酸代谢 7.核苷酸代谢 第一节蛋白质的结构与功能 大纲解读: 1.蛋白质的分子组成 (1)蛋白质的平均含氮量 (2)L-α-氨基酸的结构通式 (3)20种L-α-氨基酸的分类 2.氨基酸的性质 3.蛋白质的分子结构 4.蛋白质结构与功能的关系 (1)血红蛋白的分子结构 (2)血红蛋白空间结构与运氧功能关系 (3)协同效应、别构效应的概念 5.蛋白质的性质 一、蛋白质的分子组成 1.蛋白样品的平均含氮量 2.L-α-氨基酸的结构通式 3.20种L-α-氨基酸的分类以及名称 (一)蛋白样品的平均含氮量 1.组成蛋白质的元素及含量
(1 )主要元素:碳(50~55% )、氢(6~8%)、氧(19~24%)、氮(16%)、硫(0~ 4%) (2)其他:磷、铁、锰、锌、碘等(元素组成) 2.蛋白质含量测定(测氮法) (1)蛋白质的平均含氮量为16%,即每克氮相当于6.25克蛋白质。 (2)每克样品中蛋白质的含量=每克样品的含氮量×6.25 A型题: 测得某一蛋白质样品(奶粉)含氮量为0.40克,此样品约含蛋白质()克。 A.2.0 B.2.5 C.3.0 D.3.5 E.4.0 [答疑编号111020801:针对该题提问] 『正确答案』B 『答案解析』每克样品中蛋白质的含量=每克样品的含氮量×6.25= 0.40×6.25=2.5克。 (二)蛋白质的基本组成单位 1.氨基酸是组成蛋白质的基本单位。 2.氨基酸通式: 3.存在自然界中的氨基酸有300余种,但组成人体蛋白质的氨基酸仅有20种,且均属L-氨基酸(甘氨酸除外)。甘氨酸的结构式: 4.特殊氨基酸: 脯氨酸(亚氨基酸)结构式: 5.氨基酸分类: (1)非极性疏水性氨基酸:甘、丙、缬、亮、异亮氨基酸、苯丙、脯氨酸(亚氨基酸)(7种)。
第二章环境化学物的生物转运和生物转化 【选择题】 1.外源化学物经消化道吸收的主要方式是 A.通过营养物质作载体 B.滤过 C.简单扩散 D.载体扩散 2.影响化学物质经呼吸道吸收的因素是 A.肺泡的通气量与血流量之比 B.溶解度 C.气血分配系数 D.以上都是 3.pKa为 4.2的有机酸(苯甲酸)在消化道中吸收最好的部位是 A.胃 B.十二指肠 C.小肠 D.结肠 4.血脑及胎盘屏障受以下因素的影响 A.动物种属 B.年龄 C.生理状态 D.以上都是 5.毒物排泄的主要途径是 A.肠道 B.唾液 C.汗液 D.肾脏 6.肾脏排泄主要的机理是 A.肾小球简单扩散 B.肾小球主动转运 C.肾小球滤过 D.肾小管主动转运 7.外源化学物生物转化的两重性表现在 A.N一氧化.苯胺N羟基苯胺(毒性增强) B.脱硫反应,对硫磷对氧磷(水溶性增加,毒性增强) C.环氧化,苯并(α)芘7,8-二醇-9,10环氧化物(致癌) D.以上都是生物转化两重性的典型例子 8.外来化合物代谢酶的诱导是指 A.某些化合物可使某些代谢酶活力增强 B.酶的含量增加 C.生物转化速度增高
D.以上都是 9.对于呈气体状态或易挥发的化学毒物的排泄,下列哪一项描述是正确的A.通过主动转运的方式经肺泡壁排出气体 B.排出的速度与吸收的速度成正比 C.血液中溶解度低可减缓其排除速度 D.肺通气量加大可加速其排除速度 10.能沿浓度梯度扩散,需要载体参加但不消耗能量的转运方式称为A.简单扩散 B.主动转运 C.易化扩散 D.滤过 11.外源化学物在体内生物转化的最主要器官是 A.肝 B.肾 C.肺 D.小肠 12.外源化学物生物转化的I相反应,不包括下列哪一种反应 A.甲基化 B.羟化 C.共氧化 D.环氧化 13.外源化学物在器官和组织中的分布最主要受哪项因素影响 A.化学毒物与器官的亲和力 B.血流量 C.特定部位的屏障作用 D.器官和组织所在部位 14.外源化学物在胃肠道吸收的主要方式为 A.简单扩散 B.主动转运 C.易化扩散 D.胞吞 15.外源化学物经皮吸收必须具备下述哪项条件 A.水溶性 B.脂溶性 C.水溶性和脂溶性 D.分子量小于100 16.外源化学物在消化道吸收的主要部位是 A.食管 B.胃 C.小肠 D.大肠 17. 外源化学物体内生物转化I相反应的酶主要存在于
第三章外源化学物在体内的生物转运与生物转化 机体对外源化学物的处置包括:吸收(absorption)、分布(distribution)、代谢(metabolism)和排泄(excrection)四个过程(ADME) 1.在这四个过程中,吸收、分布和排泄具有共性,即都是外源化学物穿越生物 膜的过程,且其本身的结构和性质不发生变化,故统称为生物转运(biotransportation) 2.外源化学物转化为新的衍生物的过程,形成的产物结构与性质均发生了改变, 故称之为生物转化(biotransformation)或代谢转化(metabolic transformation)3.代谢过程与排泄过程合称为消除(elimination) 第一节生物转运 一生物膜的结构与功能 质膜:包围在细胞外的膜称为细胞膜。 细胞核和各种细胞器外面也包围有膜。 质膜和各种细胞器的膜结构统称为生物膜。 二、外源化学物通过生物膜的方式 1.被动运输(passive transport) (1)简单扩散(simple diffusion) 定义: 特点: 1)此种转运的外源化合物的特点:具有脂溶性 脂溶性的高低可用脂/水分配系数(lipid/water partition coefficient)表示,即当一种物质在脂相和水相之间的分配达到平衡时,其在脂相和水相中溶解度的比值。一般情况下,分配系数越大,越易溶解与脂肪,经简单扩散转运的速率也越快。但由于扩散需要生物膜的脂相,还要通过水相,故分配系数极高、只能全部溶解于脂肪的物质难以通过简单扩散方式跨膜转运。 2)外源化学物的解离状态对简单扩散可产生重要影响。 处于解离态的物质极性大,脂溶性差,不易通过生物膜的脂相进行扩散;而处于非解离态的物质情况与之相反。 弱有机酸和弱有机碱类物质在体液中处于解离态和非解离态的比例取决于其本身的解离常数pKa(该物质50%解离时的pH值)和体液的pH值。 有机酸:pKa-pH=log(非解离态HA)/(解离态A—) 有机碱:pKa-pH=log(解离态BH+)/(非解离态B) 弱有机酸在酸性环境中、弱有机碱在碱性环境中多处于非解离态,易透过生物膜转运。 (2)滤过 定义:外源化学物通过生物膜上亲水性孔道的过程。 2.特殊转运 (1)主动转运 定义: 特点: (2)易化扩散
环境生物化学考试复习资料(一) 糖类化学 1、糖的概念:多羟基醛或酮及其缩聚物和衍生物的总称。 2、糖的分类:单糖、寡糖、多糖、结合糖。 3、糖的功能:a、作为能源物质b、作为结构成分c、参与构成生物活性物质 d、作为合成其他生物分子的碳源。 4、寡糖:麦芽糖、乳糖、蔗糖。(注意这三种糖的不同点,例如还原性。蔗糖是没有还原性的)。 5、典型的多糖:植物体内:纤维素动物体内:糖原。 脂类化学 1、单脂:是由各种高级脂肪酸与甘油或高级一元醇所生成的酯。 2、脂类的胜利作用:1)储存能量2)是重要的生物活性物质,如激素、第二信 使、维生素等。3)是生物细胞膜的重要结构成分,如磷脂、胆固醇等。 4)保温和保护作用 3、脂肪的结构: 4、脂肪的化学性质(掌握皂化值和碘值的计算):1)水解和皂化:一切脂肪都能被酸、碱及脂酶水解,产生甘油和脂酸 皂化作用—脂酰甘油在氢氧化钠或氢氧化钾作用下水解生成的脂肪酸盐的反应。 皂化值—完全皂化1g油或脂所消耗的氢氧化钾毫克数 各种来源不同的油脂都有不同的皂化值,根据皂化值大小可大致估计油脂的平均相对分子量,也可用来检验油脂的质量高低。 2)氢化和卤化 氢化—不饱和脂肪在有催化剂如金属镍的影响下,其脂酸的双键上可加入H 而成饱和脂 卤化—油脂中不饱和键可与卤素发生加成作用,生成卤代脂肪酸 碘值指100克油脂所能吸收的碘的克数。 碘值可用来表示油脂的不饱和度,碘值越大,表示油脂的脂肪酸不饱和程度
越高。 3)氧化 脂类所含的不饱和脂酸与分子氧作用后,可产生脂酸过氧化物。 4)酸败 油脂在空气中暴露过久即产生难闻的臭味,这种现象称为“酸败”。酸败的化学本质是由于油脂水解放出游离的脂肪酸,后者再氧化成醛或酮而发出臭味。 酸值—中和1g油脂中的游离脂肪酸所消耗的KOH的毫克数 酸值可用来检验油脂的新鲜程度 5、磷脂是由甘油、脂肪酸、磷酸及含氮碱性化合物或其他成分组成,其结构如下: 6、磷脂的特点:甘油分子中两个羟基被脂肪酸基酯化,成为疏水性的非极性尾,第三个羟基与磷酸结合,并带有一个亲水性的有机碱,因此成为亲水性的极性头。因此,磷脂是两性脂类。(亲水头部,疏水尾部) 7、生物膜的最基本成分:由脂类、蛋白质、少量糖类构成,膜脂是膜的基本骨架,膜蛋白是膜功能的主要体现者。脂类约占40%,蛋白质约占60%。 生物膜的结构:由脂类双分子层组成膜的基本骨架,脂质分子的亲水头部位于膜的两侧,而疏水尾部两两相对位于中间;蛋白质以不同程度镶嵌或贯穿其中。流动镶嵌模型:较为广泛接受的模型是流动镶嵌模型,该模型突出了膜的流动性,显示了膜蛋白的不对称性。 不对称性:膜组分的不对称分布,即构成模组分的脂质、蛋白质和糖类在膜两侧的分布都是不对称的。 流动性:膜脂和膜蛋白的运动状态,主要指脂质分子的侧向运动。 生物膜的特点:具有选择透过性,称为半透膜。 蛋白质化学 1、蛋白质中氮的含量为16%。 凯氏定氮法(计算题):蛋白质的平均含氮量为16%,即1克N相当于6.25克蛋白质(100÷16=),由此可估算蛋白质含量。 只要测定出样品中的含氮量即可测知其蛋白质的含量。即:每克样品中含N的
1、 糖类物质是多羟基醛和多羟基酮的化合物及其衍生物。 2、 糖类物质的主要生物学功能是作为能源物质以满足生命活动的需要。 3、 单糖是指不能分解为更小分子的糖类,最常见的已醛糖是葡萄糖,已酮糖是果糖。 4、 麦芽糖是由两个葡萄糖分子组成,它们之间通过 (1 4)糖苷键相连。 5、 乳糖是由葡萄糖和半乳糖组成,它们之间通过(1 4)糖苷键相连。 6、 糖原、淀粉和纤维素都是由葡萄糖组成的均一多糖。 8、 直链淀粉的构象是 卷曲成螺旋形.环境生物化学(糖化学) 二、 计算 1. 某麦芽糖溶液的比旋度为+37?,测定使用的比色管长度为10cm ,已知麦芽糖的比旋度 [α]D20=+138,请问麦芽糖溶液的浓度是多少? 2.某种α-和β-D 甘露糖平衡混合物的 为+14.5。 。求该平衡混合物中的α-和β-D 甘露糖 的比率(纯α- D 甘露糖的 为+29.3。,纯β-D 甘露糖的 为-16.3。 ) 三、问答题 1 .溶液中D-葡萄糖主要以α和β异头体形式的D-吡喃葡萄糖存在,两者都是非还原性的。为什么D-葡萄糖溶液是强还原剂? 因为溶液中存在一些具有还原性的开链葡萄糖。由于反应,在糖的开链结构和非还原性的环状形式之间存在的平衡被打破,导致更多的开链形式生成。最终,所有的葡萄糖通过开链的形式发生反应。 2.解释葡萄糖溶于水的变旋现象。 因为单糖分子中的醛基会和其他碳原子的羟基发生成环反应。成环后形成的半缩醛羟基在空间排布位置的不同将导致不同的异构体,因此会不止一个比旋光度;在成环过程中该羟基的位置会不断改变,最终达到平衡,所以有变旋现象。简单说变旋的原因是糖从一种结构α 型与β型的互变。 另外,由于糖的醛基在成环后变成了半缩醛羟基,其性质不如醛基活泼,因而不能与亚硫酸氢钠发生加成反应。 3.戊醛糖和戊酮糖各有多少个旋光异构体(包括α和β异构体)? 1. 如何鉴别核糖、葡萄糖、果糖、蔗糖和淀粉? []25D α[]25D α[]25D α
第一章绪论 第一节概述 一、生物化学的概念与涵义(幻灯PPt) 概念:生物化学是生物学与化学交叉而产生的一个边缘学科,它是利用化学的理论和方法作为主要手段(而不是唯一的手段)来研究生物的一门科学。因此,他又被称为生命的化学。所以,要学好生物化学要有化学的各种基础知识。 涵义:更具体来说是以生物体为对象,研究生命化学本质及其变化规律,通过对这些规律的了解来探索生长、发育、衰老、遗传、学习、记忆思维及其疾病的产生根源等复杂生命现象的本质及其规律。并将这些知识应用于工、农、医等实践领域以期改造自然,改善自己,增强生命力,创造人与自然的和谐与发展的社会环境,造福于子孙万代。 分支:生物化学从不同角度研究,又产生出许多分支。(幻灯PPt) 因研究对象不同分为概括起来称为普通生物化学。 我们所研究的就是普通生物化学的课程所涉及的问题。 二、生物化学的研究内容:(幻灯ppt) 静态生化:顾名思义,机体的化学组成、结构、性质、功能。 动态生化:体内各种物质的化学变化及与外界进行信息物质和能量变换。 功能生化:重要生命物质的结构与功能的关系,环境对机体的影响,从分子水平上阐明 生命现象的机制与规律。 第二节生物化学与其他生命科学的关系 一、生物化学是分子水平的生物学(幻灯ppt) 从生物的发展历史看,人们对生物体(生命现象)的认识是从宏观到微观,从形态结构到生理功能。从器官(如眼、心脏、脑)→组织(组成器官的细胞种类形态连接方式)→细胞(有机体基本的功能单位)→细胞结构→分子水平(细胞的物质结构)→元素 (超分子结构、大分子、小分子)板书 生物化学的发展历程:19世纪末以前,人们主要是通过生物体内的化学变化来认识生物体的生理机能。到了19世纪末期至20世纪初期,生物化学才成为一门独立的学科。 40年代末50年代初,随着对量的质、酶、核酸、糖类、脂类等生物大分子结构、性质、功能和代谢的初步探明,越来越多的科学工作者被吸引着,起来越广的学科向其靠拢,使生物化学跨入了突飞猛进的发展时代。. 生物化学的成就又带动了生命科学向分子水平的展。生物学的各分支学科又衍生出分子水平的新学科。如: 分子分类学——如细菌,过去主要由观察形态,现在以rRNA的分子结构为基础。 分子遗传学——遗传物质的分子结构,如基因的分子结构、染色体等。 人类基因组、动物基因组被破译、植物基因组被解读,给医药卫生、农业等带来革命性变化。 分子免疫学——免疫的分子结构及作用原理。 对于人及动物特殊病的诊断治疗开辟了新的前景。
生物化学(本科)第二章蛋白质的结构与功能 随堂练习与参考答案 第一节蛋白质的分子组成第二节蛋白质的结构第三节蛋白质的结构与理化性质之间的关系第四节蛋白质的结构与功能的关系第五节蛋白质的分类第六节血浆蛋白质 1. (单选题)测得某一蛋白质溶液N元素的含量为4 g/L,则该溶液中蛋白质含量约为 A.16 g/L B.20 g/L C.25 g/L D.30 g/L E.40 g/L 参考答案:C 2. (单选题)组成蛋白质的氨基酸基本上属于 A.L-β-氨基酸 B.D-β-氨基酸 C.L-α-氨基酸
D.D-α-氨基酸 E.L、D-α-氨基酸 参考答案:C 3. (单选题)属于碱性氨基酸的是 A.精氨酸 B.赖氨酸 C.组氨酸 D.A+B E.A+B+C 参考答案:E 4. (单选题)下列有关肽的叙述,错误的是 A.肽是两个以上氨基酸借肽键连接而成的化合物B.组成肽的氨基酸分子都不完整 C.多肽与蛋白质分子之间无明确的分界线 D.氨基酸一旦生成肽,完全失去其原有的理化性质E.根据N末端数目,可得知蛋白质的亚基数 参考答案:E
5. (单选题)维系蛋白质二级结构稳定的化学键是A.盐键 B.二硫键 C.肽键 D.疏水键 E.氢键 参考答案:E 6. (单选题)蛋白质α-螺旋的特点有 A.多为左手螺旋 B.螺旋方向与长轴垂直 C.氨基酸侧链伸向螺旋外侧 D.肽键平面充分伸展 E.靠盐键维系稳定性 参考答案:C 7. (单选题)有关蛋白质三级结构的描述,错误的是A.具有三级结构的多肽链都有生物学活性B.亲水基团多位于三级结构的表面
C.三级结构的稳定性由次级键维系 D.三级结构是单体蛋白质或亚基的空间结构 E.三级结构是各个单键旋转自由度受到各种限制的结果参考答案:A 8. (单选题)关于蛋白质亚基的描述,正确的是 A.一条多肽链卷曲成螺旋结构 B.两条以上多肽链卷曲成二级结构 C.两条以上多肽链与辅基结合成蛋白质 D.每个亚基都有各自的三级结构 E.以上都不正确 参考答案:D 9. (单选题)蛋白质的空间构象主要取决于 A.肽链氨基酸的序列 B.α-螺旋和β-折叠 C.肽链中的氨基酸侧链 D.肽链中的肽键 E.肽链中的二硫键位置
《环境生物化学》习题答案 一、单项选择题(本大题共150小题,每小题2分,共300分) 1.核酸中核苷酸之间的连接方式是:(C ) A、2’,5’—磷酸二酯键 B、氢键 C、3’,5’—磷酸二酯键 D、糖苷键 2.tRNA的分子结构特征是:(A ) A、有反密码环和3’—端有—CCA序列 B、有密码环 C、有反密码环和5’—端有—CCA序列 D、5’—端有—CCA序列 3.热变性的DNA分子在适当条件下可以复性,条件之一是( B ) A、骤然冷却 B、缓慢冷却 C、浓缩 D、加入浓的无机盐 4.下面关于Watson-Crick DNA双螺旋结构模型的叙述中哪一项是正确的?(A ) A、两条单链的走向是反平行的 B、碱基A和G配对 C、碱基之间共价结合 D、磷酸戊糖主链位于双螺旋内侧 5.在适宜条件下,核酸分子两条链通过杂交作用可自行形成双螺旋的原因是由于(D ) A、DNA的Tm值 B、序列的重复程度 C、核酸链的长短 D、碱基序列的互补 6.下列关于mRNA描述哪项是错误的?(A ) A、原核细胞的mRNA在翻译开始前需加“PolyA”尾巴。 B、真核细胞mRNA在3’端有特殊的“尾巴”结构。 C、真核细胞mRNA在5’端有特殊的“帽子”结构。 D、原核细胞mRNA不需要进一步加工。 7.酶促反应中决定酶专一性的部分是( A ) A、酶蛋白 B、底物 C、辅酶或辅基 D、催化基团 8.tRNA的三级结构是(B ) A、三叶草叶形结构 B、倒L形结构 C、双螺旋结构 D、发夹结构 9.在寡聚蛋白质中,亚基间的立体排布、相互作用以及接触部位间的空间结构称之谓( C ) A、三级结构 B、缔合现象 C、四级结构 D、变构现象 10.形成稳定的肽链空间结构,非常重要的一点是肽键中的四个原子以及和它相邻的两个α-碳原子处于 ( C ) A、不断绕动状态 B、可以相对自由旋转 C、同一平面 D、随不同外界环境而变化的状态 11.甘氨酸的解离常数是pK1=2.34, pK2=9.60 ,它的等电点(pI)是( B ) A、7.26 B、5.97