第三章不饱和脂肪烃(Unsaturated Hydrocarbons)
凡分子中含有碳碳双键或碳碳叁键的烃成为不饱和烃。
第一节烯烃
一.双键的电子结构
以乙烯为例:
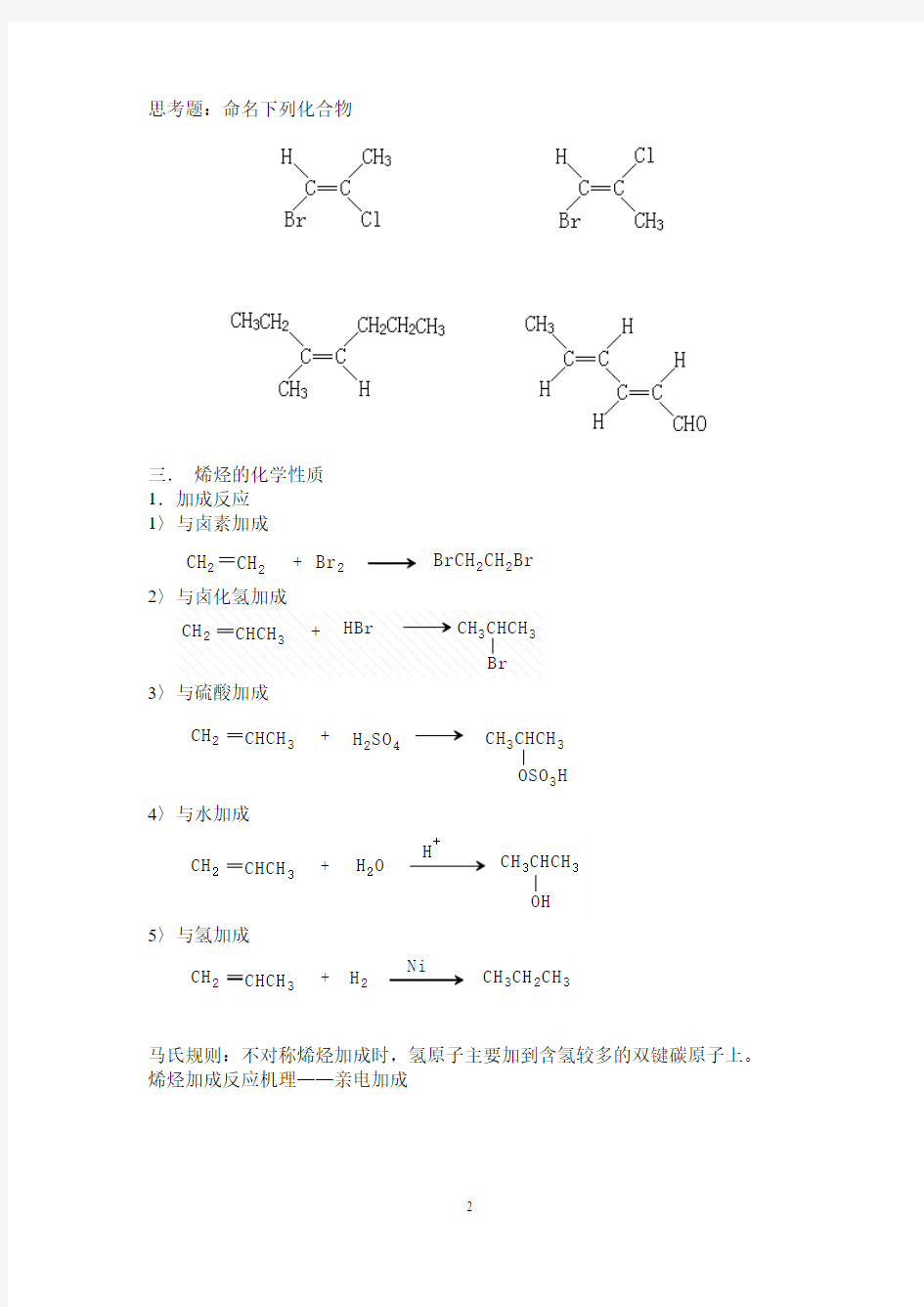
在乙烯分子中,碳原子采取sp2杂化。三个sp2杂化轨道的对称轴处在同一个平面上,互成120°的角,另有一个p轨道不参与杂化,而形成另一类型的共价键π键。
乙烯分子中有一个C-Cσ键和四个C-Hσ键,未杂化的p轨道可以“肩并肩”平行重叠成键,形成π键。构成π键的电子叫做π电子。
二.烯烃的异构现象及命名
1.结构异构现象及特点
烯烃的结构异构现象,除碳链异构外,还有双键的位置异构。
顺反异构的特点:
分子中有两个不能自由旋转(或旋转受阻)的原子,这两个原子分别连着两个不同的原子或集团。
2.几何异构体的命名
1〉顺/反命名
顺-2-丁烯反-2-丁烯
2〉Z/E命名
Z-1,2-二氯-1-溴乙烯E-1,2-二氯-1-溴乙烯
(反-1,2-二氯-1-溴乙烯)(顺-1,2-二氯-1-溴乙烯)
思考题:命名下列化合物
三.烯烃的化学性质
1.加成反应
1〉与卤素加成
2
3〉与硫酸加成
4〉与水加成
5
马氏规则:不对称烯烃加成时,氢原子主要加到含氢较多的双键碳原子上。烯烃加成反应机理——亲电加成
2.诱导效应
由于某些吸电子基团或斥电子基团的存在,使邻近共价键的极性发生改变,我们说这些基团对该共价键发生了诱导效应。
由吸电子基团引起的诱导效应记作–I;
由斥电子基团引起的诱导效应记作+I。
诱导效应的特点:
1〉诱导效应的强弱取决于基团的吸电子或斥电子的能力。
2〉诱导效应可以沿共价键传递,但很快消弱,一般间隔三个以上的共价键的影响可忽略不计。
3〉诱导效应有叠加性。
3.马氏规则的解释
在不对称烯烃的亲电加成中,亲电试剂总是加到电子密度较高的双键碳原子上。
4.过氧化物效应
由于过氧化物(ROOR)的存在,出现反马氏规则现象,这类反应属于自由及加成反应。
5.氧化反应
2〉高锰酸钾氧化
3〉臭氧氧化
由醛酮结构的测定,就可推到原来的结构。如:
2-甲基丙烯甲醛丙酮
四.亲电加成反应机理
首先试剂分子异裂为两个离子:
第一步:亲电试剂进攻烯烃的双键;
亲电试剂中间体
第二步:正碳离子很活泼,马上与反应体系中的亲核试剂结合,完成加成反应。
第二节二烯烃
一.二烯烃的分类
1〉隔离二烯烃:两个双键被二个或多个单键隔开;
2〉聚集二烯烃:两个双键连在一个碳原子上;
3〉共轭二烯烃:两个双键之间自只被一个单键隔开;
二.共轭体系和共轭效应
1.共轭二烯烃的结构和π—π共轭
1,3-丁二烯是最简单共轭二烯烃。1,3-丁二烯π电子的离域如下图:
由于π电子的离域,就是1,3-丁二烯分子中的C2~C3之间也具有部分双键性质,除了单双键的差别减小外,整个体系的能量也降低了,体系更稳定了。共轭体系中的这种π电子的离域效应就为共轭效应。
2.p-π共轭
与π键相连的原子,如果有p轨道的未共用电子对,那么,这样的p轨道也可与π键产生共轭,这就是p-π共轭。
3.σ—π超共轭
与碳碳双键相连的饱和碳原子上C-Hσ键可与π键产生共轭,这种共轭很微弱,成为σ—π共轭。
4.σ-p 超共轭
C-Hσ键的σ轨道也可与中心碳原子的p 轨道有稍许重叠而成σ-p 超共轭。
自由基的稳定性:
正碳离子的稳定性:
第三节 炔烃
一. 炔烃的结构
以乙炔为例: 在乙炔分子中,两个碳原子各以一个sp 轨道互相重叠,形成一个C-Cσ键,每个碳原子又各以一个sp 轨道分别与一个氢原子的1s 轨道重叠形成C-Hσ键。每个碳原子还有两个互相垂直的未杂化的p 轨道,它们与另一碳的两个p 轨道两两相互侧面重叠形成两个互相垂直的π键。
乙炔分子中的π键和σ键
二. 炔烃的化学性质 1.加成反应
亲电加成比烯烃困难;
亲核加成比烯烃容易。
H C C H
2.氧化反应
3.金属炔化物的生成
白色
第四节萜烯类化合物
萜类亦称萜烯类,是香精油的主要成分。某些植物的叶,花或果实用水蒸汽蒸馏的方法,可以得到有香味的油状液体,称为香精油。原来把存于香精油中的脂环烃C10H16叫做萜。后来又发现了不少与萜具有类似构造的含氧衍生物,以及挥发性不大的含有15,20,30,40甚至50个碳的化合物。现在把存在于自然界的这一类化合物都叫萜。不管它们是烃类或是含氧衍生物。
至少两个异戊二烯链节首尾相连的化合物为萜类化合物:
萜类化合物具有以下结构特点:
1.碳原子为5n个;
1〉单萜它含有两个异戊二烯单位(C10)
2〉倍半萜它含有三个异戊二烯单位(C15)
3〉双萜它含有四个异戊二烯单位(C20)
4〉三萜它含有六个异戊二烯单位(C30)
5〉四萜它含有八个异戊二烯单位(C40)
2.异戊二烯链节首尾相连,只与碳架有关,与碳的连接方式无关;
3.萜类化合物包括萜烯,饱和部分饱和的各种烃类以及它们的衍生物,如:醇,醛,酮,酯。
薄荷醇(单萜)
在医药上用作兴奋剂.薄荷醇具有芳香凉爽气味.又有杀菌功效
莰酮(樟脑)(单萜)
《有机化学》(第四版)第三章-不饱和烃(习题答案)
第三章不饱和烃 思考题 习题3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。(P69) 解:C6H12有13个构造异构体,其中4个有顺反异构体: CH2=CHCH2CH2CH2CH3CH3CH=CHCH2CH2CH3CH3CH2CH=CHCH2CH3 (Z,E) (Z,E) CH2=CCH2CH2CH3 CH3CH2=CHCHCH2CH3 CH3 CH2=CHCH2CHCH3 CH3 CH3C=CHCH2CH3 3CH3CH=CCH2CH3 CH3 CH3CH=CH2CHCH3 3 (Z,E) (Z,E) CH2=CHCCH3 CH3 CH3CH2=CCHCH3 CH3 CH3 CH3C=CCH3 CH3 CH3 CH22CH3 CH2CH3 C6H10有7个构造异构体: CH CCH2CH2CH2CH3CH3C CCH2CH2CH3CH3CH2C CCH2CH3 CH CCHCH2CH3 3CH CCH2CHCH3 3 CH CC(CH3)3CH3C CCHCH3 3 习题3.2 用衍生物命名法或系统命名法命名下列各化合物:(P74) (1) (CH3)2CHCH=CHCH(CH3)2对称二异丙基乙烯
or 2,5-二甲基-3-己烯 (2) (CH 3)2CHCH 2CH=CHCHCH 2CH 3 CH 3 1234567 8 2,6-二甲基-4-辛烯 (3) CH 3CH 2C CCH 2CH 3 1 2 3 45 6 二乙基乙炔 or 3-己炔 (4) CH 3CH 2C(CH 3)2C CH 1 2 3 4 5 3,3-二甲基-1-戊炔 (5) CH 2=CHCH 2C CH 12345 1-戊烯-4-炔 (6) HC C C=C CH=CH 2 CH 2CH 2CH 3CH 2CH 2CH 3 1 2 3 4 5 6 3,4-二丙基-1,3-己二烯 -5-炔 (7) CH 3 CH 3 2,3-二甲基环己烯 (8) CH 3CH 3 5,6-二甲基-1,3-环己二烯 习题3.3 用Z,E-命名法命名下列各化合物:(P74) (1) ↑C=C CH 2CH 3 H Cl Br ↑ (Z)-1-氯-1-溴 -1-丁烯 (2) ↓C=C F CH 3Cl CH 3 CH 2 ↑ (E)-2-氟-3-氯-2- 戊烯
第三章不饱和烃 学习指导: 1.烯烃的异构和命名:构造异构和顺反异构(顺式、反式和Z、E表示法); 2. 烯烃的化学性质:双键的加成反应—催化加氢和亲电加成(亲电加成反应历程,不对称加成规则,诱 导效应,过氧化物效应、双键的氧化反应(高锰酸钾氧化,臭氧化,催化氧化)、—氢原子的反应(氯化); 3、炔烃的命名和异构; 4、炔烃的化学性质:亲电加成反应;氧化反应(高锰酸钾氧化,臭氧化);炔烃的 活泼氢反应(酸性,金属炔化物的生成) 5、烯烃的制备(醇脱水,氯代烷脱氯化氢);炔烃的制备(二卤代烷脱卤化氢,炔烃的烷基化)。 6. 二烯烃的分类和命名; 7. 共轭二烯烃的化学性质:加成反应(1、4—加成和1、2—加成)双烯合成(Diels-Alder反应) 习题 一、命名下列各物种或写出结构式。 1、写出的系统名称。 2、写出(Z)-3-甲基-4-异丙基-3-庚烯的构型式。 3、写出的系统名称。 写出的系统名称。 4、 二、完成下列各反应式(把正确答案填在题中括号内)。 1、 2、( ) 3、 4、
5、 6、 7、 三、理化性质比较题(根据题目要求解答下列各题)。 1、排列下列烯烃与HCl加成的活性次序: (A) (CH3)2C == CH2 (B) CH2 == CH2 (C) CH3CH == CH2 (D) CF3CH == CH2 2、将下列碳正离子按稳定性大小排序: 3、将下列碳正离子按稳定性大小排列: 4、排列与下列化合物进行双烯加成的活性次序: 5、比较下列化合物与1, 3-丁二烯进行Diels-Alder反应的活性大小: 6、由下列哪一组试剂经Diels-Alder反应生成产物?
第三章不饱和烃 3.1用系统命名法命名下列化合物 a. b.c. (CH 3CH 2)2C=CH 2CH 3CH 2CH 2CCH 2(CH 2)2CH 3 2 CH 3C=CHCHCH 2CH 3 C 2H 5CH 3 d. (CH 3)2CHCH 2CH=C(CH 3)2 答案: a. 2-乙基-1-丁烯 2-ethyl -1-butene b. 2-丙基-1-己烯 2-propyl -1-hexene c. 3,5-二甲基-3-庚烯 3,5-dimethyl -3-heptene d. 2,5-二甲基-2-己烯 2,5-dimethyl -2-hexene 3.2写出下列化合物的结构式或构型式,如命名有误,予以更正。 a. 2,4-二甲基-2-戊烯 b. 3-丁烯 c. 3,3,5-三甲基-1-庚烯 d. 2-乙基-1-戊烯 e.异丁烯 f. 3,4-二甲基-4-戊烯 g. 反-3,4-二甲基-3-己烯 h. 2-甲基-3-丙基-2-戊烯 答案: a. b.错,应为1-丁烯 c. d. e. f. 错,应为2,3-二甲基-1-戊烯 g. h. 错,应为2-甲基-3-乙基-2-己烯 3.3写出分子式C 5H 10的烯烃的各种异构体的结构式,如有顺反异构,写出它们的构型式,并用系统命名法命名。 pent-1-ene (E )-pent-2-ene (Z )-pent-2-ene 3-methylbut-1-ene
2-methylbut-2-ene2-methylbut-1-ene 3.4用系统命名法命名下列键线式的烯烃,指出其中的sp2及sp3杂化碳原子。分子中的σ键有几个是sp2-sp3型的,几个是sp3-sp3型的? 3-ethylhex-3-ene 3-乙基-3-己烯,形成双键的碳原子为sp2杂化,其余为sp3杂化,σ键有3个是sp2-sp3型的,3个是sp3-sp3型的,1个是sp2-sp2型的。 3.5写出下列化合物的缩写结构式 答案:a、(CH3)2CHCH2OH;b、[(CH3)2CH]2CO;c、环戊烯;d、(CH3)2CHCH2CH2Cl 3.6将下列化合物写成键线式 A、O ;b、;c、 Cl ; d 、
第三章不饱和脂肪烃 一、分子中只含有一个碳碳双键的烯烃称为单烯烃。C n H2n 由于π键存 在,C-Cσ键不能 自由旋转,存 在顺反异构。烯碳SP2杂化,三个σ键,一个π键。 π电子极化度比σ键大 二、命名三步 1、选择主链 2、编号 3、书写名称(如下) 1、选择含有双键的最长碳链为主链; 2、应使双键的位次尽可能的小,从靠近双键一端(即官能团)开始编号; 3、 1) 2)顺反异构体命名标记法,两种:顺反标记法及Z\E标记法(对于取代基不同的烯烃,很难用顺或反来表示,则用Z,E表示。) A、顺反标记法 B、Z\E标记法:当两个“较优”基团位于双键同侧时,用Z标记其构型;位于异侧时,用E标记其构型。 优先基团选择规律:I>Br>Cl>S>P>F>O>N>C>D>H
一、 重点 二、命名三步 1、选择主链 2、编号 3、书写名称 1、 2、 3、 1) 2) S---single 单键
三、共轭 1、CH2=CH-CH=CH2 1) 2) 3) 2、共轭体系分类 1) 2)P、π共轭 如 类似的还有 3)σ、π超共轭 3、 1)吸电子共轭基团(能降低共轭体系共轭电子云密度)-NO2 -CN -COOH -CHO -COR等 2)给电子共轭基团(能提高共轭体系共轭电子云密度)-OH -OR -OCOR -NH2 -NHCOR等 丁二烯共轭导致,键长平均化,分子平面化,能量降低
一、炔烃的命名:命名类似于烯烃 二、烯炔的命名 1、三个步骤,遵循的原则 1)选择含有双键和叁键最长碳链为主链。从最先遇到双键或叁键的一端开始; 2)以双键在前、叁键在后、主链碳数放在“烯”前面的原则书写名称。 3)若在主链两端等距离处遇到双键或叁键时,编号要从靠近双键的一端开始。 2、例 补充
第三章 不饱和烃 思考题 习题3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。(P69) 解:C 6H 12有13个构造异构体,其中4个有顺反异构体: C H 2=C H C H 2C H 2C H 2C H 3 C H 3C H =C H C H 2C H 2C H 3 C H 3C H 2C H =C H C H 2C H 3 (Z ,E ) (Z ,E ) C H 2=CC H 2C H 2C H 3C H 3 C H 2=C H C H C H 2C H 3 C H 3 C H 2=C H C H 2C H C H 3 C H 3 C H 3C =C H C H 2C H 3 C H 3 C H 3C H =C C H 2C H 3 C H 3C H 3C H =C H 2C H C H 3 C H 3 (Z ,E ) (Z ,E ) C H 2=C H C C H 3 C H 3 C H 3 C H 2=C C H C H 3 C H 3 C H 3 C H 3C =C C H 3 C H 3C H 3 C H 2=C C H 2C H 3 C H 2C H 3 C 6H 10有7个构造异构体: C H C C H 2C H 2C H 2C H 3C H 3C C C H 2C H 2C H 3 C H 3C H 2C C C H 2C H 3 C H C C H C H 2C H 3C H 3 C H C C H 2C H C H 3 C H 3 C H C C (C H 3)3 C H 3C C C H C H 3C H 3 习题3.2 用衍生物命名法或系统命名法命名下列各化合物:(P74) (1) (CH 3)2CH CH =CH CH (CH 3)2 对称二异丙基乙烯 or 2,5-二甲基-3-己烯 (2) (C H 3)2C H C H 2C H =C H C H C H 2C H 3 C H 3 1 2 3 4 5 6 7 8 2,6-二甲基-4-辛烯 (3) C H 3C H 2 C C C H 2C H 3123 456 二乙基乙炔 or 3-己炔
实验七 不饱和烃的性质 实验目的: 学习乙烯和乙炔的制备方法及验证不饱和烃的性质 1) 乙烯的制备 CH 3CH 2OH 24160-170℃CH 2=CH 2 仪器装置: 95%C 2H 5OH 98%H 2SO 4河沙10%NaOH 排水集气 实验步骤: 在125ml 的蒸馏烧瓶口插入一个漏斗,通过这个漏斗加入95%酒精4ml ,浓硫酸12ml (比重1.84),边加边摇,加完后,再放入干净的河砂4g ,塞上带有温度计(200℃或250℃) 的软木寒,温度计的水银球应浸入反应液中,蒸馏烧瓶的支管通过橡皮管和玻璃导气管与作洗气用的试管相连,试管中盛有15ml 的l0%氢氧化钠溶液。 按照上图把仪器连接好,检查不漏气后,强热反应物,使反应物的温度迅速地上升到 160—170℃,调节火焰,保持此范围的温度和保持乙烯气流均匀地发生。估计空气被排尽 后,利用排水集气法收集两支试管(20 x150 mm)的乙烯(供性质试验),然后即作燃烧试验。 实验注释: (1) 乙醇与浓硫酸作用,首先生成硫酸氢乙酯。反应放热.故必要时可誛在冷水中冷却 片刻。边加边摇可防止乙醇的碳化。 CH 3CH 2OH + H 2SO 4CH 3CH 2OSO 2OH + H 2O (2)河砂应先用稀盐酸洗涤,除去可能夹杂着的石灰质(因为石灰质与硫酸作用生成的 硫酸钙会增加反应物沸腾的因难),然后用水洗涤,干燥备用。河砂的作用是: (a)作硫酸氢乙酯分解为乙烯的催化剂。 (b)减少泡沫生成,以使反应顺利进行。 (3)因为浓硫酸是氧化剂,会将乙醇氧化成一氧化碳、二氧化碳等,同时,硫酸本身 被还原成二氧化硫。这些气体随乙烯—起出来,将它们通过氢氧化钠溶液,便可除去二氧化硫与二氧化碳等.在乙烯中虽杂有—氧化碳,但它与溴和高锰酸钾试液均不起作用,故不除去也无妨碍。 (4)硫酸氢乙酯与乙醇在170℃分解生成乙烯,但在140℃时则生成乙醚,故实验中要 求强热使温度迅速达到l50℃以上,这样便可减少乙醚生成的机会,但当乙烯开始生成时,则加热不宜过剧。否则,将会有大量泡沫产生,使实验难以顺利进行。 (5)通常的汽油、煤油中含有少量不饱和烃,若是石油裂化得的产品,不饱和烃的含 量则更多,故可作为烯烃性质试验的样品,但有色的汽油或煤油须蒸馏制得无色的汽油和煤油,才能使用。 2) 乙烯的性质: (1)可燃性 用安全点火法(参阅甲烷的燃烧)做燃烧试验。注意与甲烷的燃烧试验情
《有机化学》(第四版)第三章不饱和烃(习 题答案)
第三章不饱和烃 思考题 习题 3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。(P69) 解:C6H12有13个构造异构体,其中4个有顺反异构体: CH2=CHCH2CH2CH2CH3CH3CH=CHCH2CH2CH3CH3CH2CH=CHCH2CH3 (Z,E) (Z,E) CH2=CCH2CH2CH3 3CH2=CHCHCH2CH3 3 CH2=CHCH2CHCH3 3 CH3C=CHCH2CH3 CH3CH3CH=CCH2CH3 CH3 CH3CH=CH2CHCH3 CH3 (Z,E) (Z,E) CH2=CHCCH3 CH3 CH3CH2=CCHCH3 CH3 CH3 CH3C=CCH3 CH3 CH3 CH2=CCH2CH3 CH2CH3 C6H10有7个构造异构体: CH CCH2CH2CH2CH3CH3C CCH2CH2CH3CH3CH2C CCH2CH3 CH CCHCH2CH3 3CH CCH2CHCH3 3 CH CC(CH3)3CH3C CCHCH3 3 习题3.2 用衍生物命名法或系统命名法命名下列各化合物:(P74) (1) (CH3)2CHCH=CHCH(CH3)2对称二异丙基乙烯 or 2,5-二甲基-3-己烯
(2) (CH 3)2CHCH 2CH=CHCHCH 2CH 3 3 1234567 8 2,6-二甲基-4-辛烯 (3) CH 3CH 2C CCH 2CH 31 2 3 456 二乙基乙炔 or 3-己炔 (4) CH 3CH 2C(CH 3)2C CH 1 2 3 4 5 3,3-二甲基-1-戊炔 (5) CH 2=CHCH 2C CH 1 2 3 4 5 1-戊烯-4-炔 (6) HC C C=C CH=CH 2CH 2CH 2CH 3 2CH 2CH 3 1 23 45 6 3,4-二丙基-1,3-己二烯-5-炔 (7) CH 3 CH 3 2,3-二甲基环己烯 (8) CH 3 CH 3 5,6-二甲基-1,3-环己二烯 习题3.3 用Z,E-命名法命名下列各化合物:(P74) (1) ↑ C=C CH 2CH 3H Cl Br ↑ (Z)-1-氯-1-溴-1-丁烯 (2) ↓ C=C F CH 3Cl CH 3CH 2 ↑ (E)-2-氟-3-氯-2-戊烯 (3) ↑ C=C CH 2CH 3CH 2CH 2CH 3H CH 3↓ (E)-3-乙基-2-己烯 (4) ↓ C=C CH(CH 3)2 CH 2CH 2CH 3CH 3 H ↑ (E)-3-异丙基-2-己烯
第一节脂肪烃 【学习目标】 学习目标 1、了解烷烃、烯烃、炔烃物理性质的变化与分子中碳原子数目的关系; 2、了解、掌握烷烃、烯烃、炔烃的结构特点和主要化学性质以及乙炔的实验室制法; 3、根据有机化合物组成和结构的特点,认识加成、取代反应。 学习重点:烷烃和烯烃的结构特点和主要化学性质 学习难点:烯烃的顺反异构 【知识要点】 一、前言: 1、烃的衍生物: 烃分子中的氢原子被其他原子或原子团取代的产物称为烃的衍生物;如烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。 2、有机反应的特点: ①反应缓慢。有机分子中的原子一般以共价键结合,有机反应是分子之间的反应; ②反应产物复杂。有机物往往具有多个反应部位,在生成主要产物的同时,往往伴有其他副产物生成; ③反应常在有机溶剂中进行。有机物一般在水中的溶解度较小,而在有机溶剂中的溶解度较大。 二、烷烃: (又叫饱和链烃,分子中的原子全部以单键相连,易发生取代反应) 1、基本概念: 烷烃:仅含C—C键和C—H键的饱和链烃。(若C—C连成环状,称为环烷烃。) 通式:C n H2n+2 (n≥1) 2、物理性质递变规律: 烷烃的物理性质随着分子中碳原子数的递增,呈规律性变化,沸点逐渐升高(碳原子数相同时,支链越多,沸点越低);相对密度逐渐增大;常温下的存在状态,也由气态(n≤4)逐渐过渡到液态、固态。 还有,烷烃的密度比水小,不溶于水,易溶于有机溶剂。 说明:沸点的高低与分子间作用--范德华力(包括静电引力、诱导力和色散力)有关。烃的碳原子数目越多,分子间作用力就越大,因而沸点升高。支链增多时,使分子间的距离增大,分子间作用力减弱,因而沸点降低。
脂肪烃(aliphatic hydrocarbons) 具有脂肪族化合物基本属性的碳氢化合物叫做脂肪烃。分子中碳原子间连结成链状的碳架,两端张开而不成环的烃,叫做开链烃,简称链烃。因为脂肪具有这种结构,所以也叫做脂链烃。有些环烃在性质上不同于芳香烃,而十分类似脂链烃,这类环烃叫脂环烃。这样,脂肪烃便成为除芳香烃以外的所有烃的总称。脂链烃和它的衍生物总称为脂肪族化合物,脂环烃及它的衍生物总称脂环族化合物[1]。自然界中的脂肪烃较少,但其衍生物则广泛存在,而且与生命有极密切的关系。如:樟脑常用驱虫剂、麝香常用中草药和冰片。 根据碳原子间键的种类——单键、双键、叁键,可分为烷烃或石蜡烃、烯烃、二烯烃、炔烃。含有双键或三键的叫作不饱和烃。碳链是直的叫作直链烃,有侧链的叫作侧链烃。烷烃的分子通式为C n H2n+2、烯烃为C n H2n、炔烃和二烯烃为C n H2n-2。 脂肪烃的物理性质,例如沸点、熔点、相对密度等,随分子中碳原子数的递增而呈现出有规律的变化,常温下的状态则由气态逐渐变成液态、固态。 主要化学性质为碳原子上的氢原子被其他活泼原子的置换反应、高温下断链、脱氢生成较低碳数的烷烃,烯烃的裂解反应。C6~C8直链烷烃可经脱氢环化生成苯系芳烃的反应。烯烃、二烯烃、炔烃的化学性质活泼,可以进行加成、置换、齐聚、共聚、聚合、氧化等多种反应,工业上最有用的是加成反应及聚合反应。 脂肪烃一般都是石油和天然气的重要成分。C1~C5低碳脂肪烃是石油化工的基本原料,尤其是乙烯、丙烯和C4、C5共轭烯烃,在石油化工中应用最多、最广。 分类方法。 ①饱和脂肪烃分子中无不饱和的键,碳原子间以碳碳单键相连,通式C n H2n+2。 ②不饱和脂肪烃分子中有不饱和键存在。按不饱和键的不同又分为: 烯烃含有碳碳双键通式:有x个碳碳双键,C n H2n+2-2x 炔烃含有碳碳叁键通式:有x个碳碳三键,CnH2n+2-4x
第三章不饱和烃:烯烃和炔烃答案 习题(二)用Z,E标记法命名下列各化合物 答:(1)(E)-2, 3-二氯-2-丁烯 (2)(Z)-2-甲基-1-氟-1-氯-1-丁烯 (3)(Z)-1-氟-1-氯-2-溴-2-碘乙烯 (4)(Z)-3-异丙基-2-己烯 习题(四)完成下列反应式
习题(五)用简便的化学方法鉴别下列各组化合物 答:(1)先用Br2-CCl4溶液,褪色者是(B)和(C),再用稀高锰酸钾溶液,褪色者是(B); (2)使Br2-CCl4或稀高锰酸钾溶液褪色者是(A)和(B),与Ag(NH3)2NO3生成白色沉淀者是(B)。 习题(六)在下列各组化合物中,哪一个比较稳定?为什么? 答:(1)后者比较稳定,两个大基处于碳碳双键异侧,空间效应较小;(2)前者较稳定,它相当于R2C=CHR; (3)第一个较稳定,它相当于R2C=CR2; (4)后者稳定,其角张力较小; (5)环戊烯较稳定,其角张力较小; (6)后者较稳定,其角张力较小; 习题(七)将下列各组活性中间体按稳定性由大到小排列成序 答:(1)(C) > (A)> (B) (2) (B) > (C) > (A) 习题(十一)预测下列反应的主要产物,并说明理由。 答:
习题(十二)写出下列反应物的构造式。 答:(1)CH 2=CH 2 (2)(CH 3)2CHCH=CHCH 3 (3)(CH 3)2C= CH CH 2CH 3 (4)3223CH CH CCH C CH ≡ (5)()CH C CH CHCH C CH ≡=2223 (6)()CH C CH CH ≡423 习题(十五)完成下列转变 答: (1)CH 3CH 2=CH 2 CH 3CH 2 CH 2Br HBr ROOR
第二章烃和卤代烃 第一节脂肪烃(课题1) 【学习目标】 1.了解烷烃、烯烃的结构及物理性质递变规律; 2.掌握烷烃、烯烃的结构特点和主要化学性质; 3.了解1,2-加成和1,4加成。 【活动方案】 活动一.认识脂肪烃的结构、组成和分类 1.阅读下列材料回答: 分子中碳原子间连结成链状的碳架,因为脂肪分子中有这种结构,这样的烃叫脂链烃(也叫开链烃,简称链烃)。有些环烃在性质上不同于芳香烃,而十分类似脂链烃,这类环烃叫脂环烃。这样,脂肪烃便成为除芳香烃以外的所有烃的总称。 ⑴判断下列分子式或结构简式所代表的各种烃中,哪些属于脂肪烃? ⑵根据表格中的要求,写出下列各类脂肪烃的分子组成通式。 活动二.回顾饱和脂肪烃(烷烃)的化学性质 1.回忆甲烷的化学性质,完成下列问题。 ⑴写出乙烷与氯气发生一氯取代反应的化学方程式。 ⑵写出丙烷CH3CH2CH3与Cl2发生一氯取代反应的可能的化学方程式。 ⑶烷烃完全燃烧反应的通式。 2.分析上述化学反应,你认为烷烃的特征反应时什么?该反应的特点有哪些? 活动三.探究不饱和脂肪烃中烯烃的化学性质
1.烯烃的性质与乙烯相似,写出下列反应的化学方程式。 ⑴丙烯CH3CH==CH2与溴的四氯化碳溶液发生加成反应。 练习:写出丙烯与氯化氢发生加成反应后,产物的结构简式 ⑵丙烯在一定条件下发生加聚反应。 ⑶烯烃完全燃烧反应的通式。 3.阅读课本P.30资料卡片---1,2—加成和1,4—加成 ⑴写出1,3-丁二烯(CH2=CH—CH=CH2)与H2发生1,4—加成反应的化学方程式。 ⑵ 1,3-丁二烯与溴发生加成反应时,产物可能有几种?写出这些物质的结构简式。 ⑶ 2-甲基-1,3-丁二烯与溴发生加成反应时,产物可能有几种?写出这些物质的结构简式。 ⑷写出1,3-丁二烯通过1,4-加成反应生成聚-1,3-丁二烯的化学方程式。 活动四.认识脂肪烃的来源及其应用 1.脂肪烃的来源有 2.石油中含有1—50个碳原子的 3.石油通过得到汽油、煤油等;通过得到润滑油、石蜡等烷烃;通过得到轻质油和气态烯烃;而是获得芳香烃的主要途径。 【反馈检测】 完成活动单P35-36