
成都市实验外国语学校2020初三化学中考二模试题和答案
一、选择题(培优题较难)
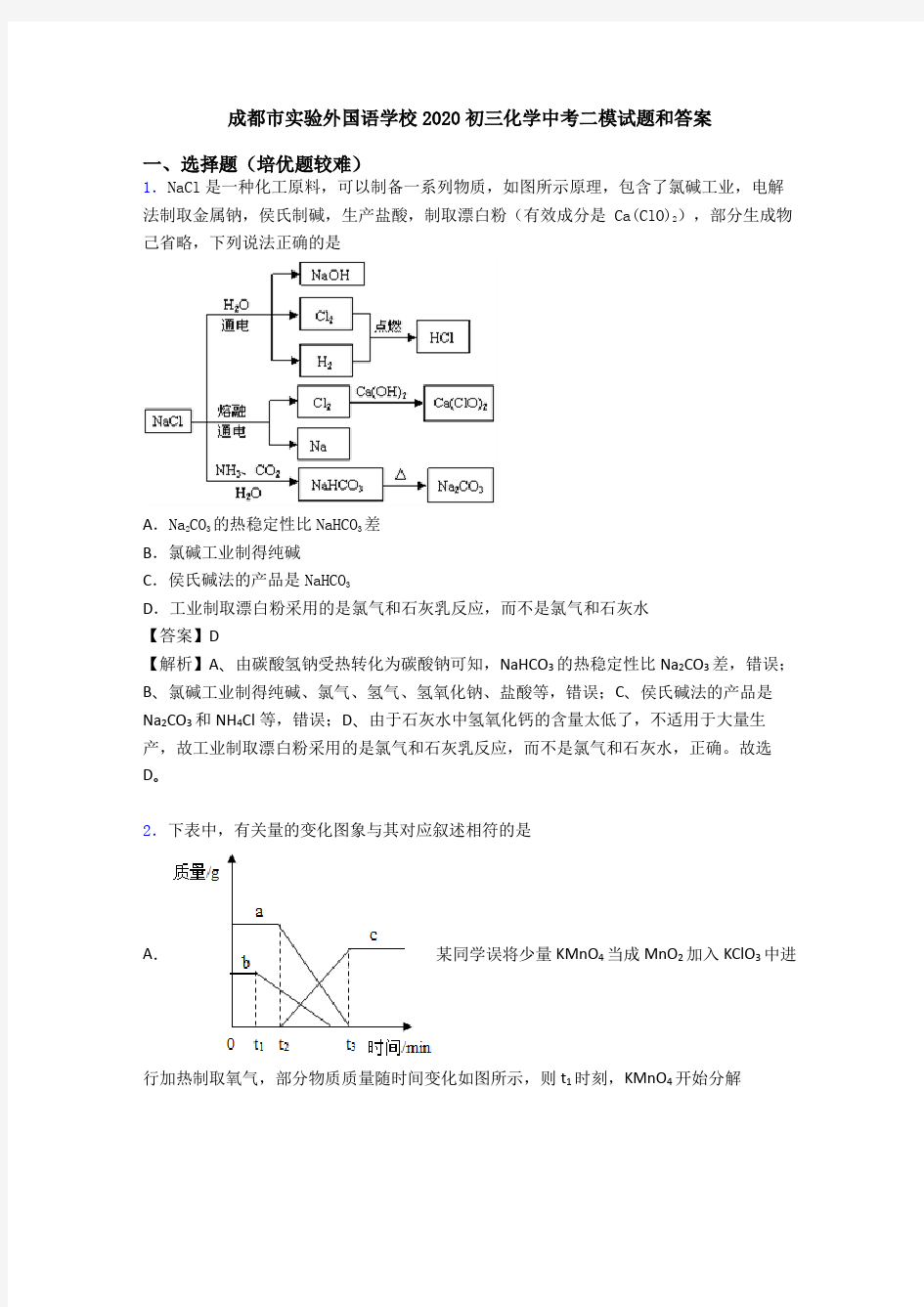
1.NaCl是一种化工原料,可以制备一系列物质,如图所示原理,包含了氯碱工业,电解法制取金属钠,侯氏制碱,生产盐酸,制取漂白粉(有效成分是 Ca(ClO)2),部分生成物己省略,下列说法正确的是
A.Na2CO3的热稳定性比NaHCO3差
B.氯碱工业制得纯碱
C.侯氏碱法的产品是NaHCO3
D.工业制取漂白粉采用的是氯气和石灰乳反应,而不是氯气和石灰水
【答案】D
【解析】A、由碳酸氢钠受热转化为碳酸钠可知,NaHCO3的热稳定性比Na2CO3差,错误;
B、氯碱工业制得纯碱、氯气、氢气、氢氧化钠、盐酸等,错误;
C、侯氏碱法的产品是Na2CO3和NH4Cl等,错误;
D、由于石灰水中氢氧化钙的含量太低了,不适用于大量生产,故工业制取漂白粉采用的是氯气和石灰乳反应,而不是氯气和石灰水,正确。故选D。
2.下表中,有关量的变化图象与其对应叙述相符的是
A.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示,则t1时刻,KMnO4开始分解
B .在一定量硝酸银和硝酸铜的混合溶液中加入铁粉,充分反应,硝酸根质量分数随加入铁粉质量变化如图所示
C .密闭容器中发生化学反应,X 、Y 、Z 的质量随着反应时间的变化如图所示,则该反应的化学方程式一定为3X+Y=4Z
D .稀硫酸和氢氧化钠溶液反应的pH 的变化图象如图所示,图中c 点时,可以加BaCl 2溶液来检验硫酸是否被反应完
【答案】A
【解析】
【详解】
A 、误将少量KMnO 4当成MnO 2加入KClO 3中进行加热,高锰酸钾在加热的条件下分解成锰酸钾、二氧化锰和氧气,然后氯酸钾在二氧化锰的催化下分解为氯化钾和氧气,故b 为高锰酸钾,在t 1时刻,高锰酸钾开始分解,t 2时刻,氯酸钾开始分解,故a 为氯酸钾,c 为氧气,符合题意;
B 、在一定量硝酸银和硝酸铜的混合溶液中加入铁粉,铁粉先和硝酸银反应,
332=Fe Fe+2AgNO NO ()+2Ag ,56份铁生成216份银,固体质量增加,溶液质量减小,硝酸根的质量不变,故硝酸根的质量分数逐渐增大,待硝酸银完全反应后,铁和硝酸铜反应3232=Fe+Cu(NO )Fe(NO )+Cu ,56份铁生成64份铜,固体质量增加,溶液质量减小,硝酸根的质量不变,故硝酸根质量分数逐渐增大,待硝酸铜完全反应后,硝酸根溶质质量分数不变,不符合题意;
C 、由图可知,X 、Y 质量不断减小,则X 、Y 为反应物,Z 的质量逐渐增加,则Z 为生成物,t 1时,该反应恰好完全反应,X 减小量为9,Y 减小量为3,则Z 的增加量为12,X ∶Y ∶Z=3∶1∶4,但是由于不知道X 、Y 、Z 的相对分子质量,无法确定该反应的化学
方程式,不符合题意。
D、稀硫酸与氢氧化钠反应生成硫酸钠和水, c点时,稀硫酸与氢氧化钠恰好完全反应,但是溶液中一直含有硫酸根离子,无论稀硫酸是否完全反应,加入氯化钡都会生成白色沉淀,因此不能用氯化钡来检验硫酸是否完全反应,不符合题意。故选A。
3.某固体混合物由Mg和MgO组成,取该混合物与19. 6%的稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液蒸发82. 2g水后得到固体的质量为24g,则原混合物中氧元素的质量分数为()
A.16%
B.20%
C.25%
D.40%
【答案】C
【解析】
【详解】
镁和稀硫酸反应生成硫酸镁和氢气,氧化镁和稀硫酸反应生成硫酸镁和水,所得溶液蒸发82. 2g水后得到的固体是硫酸镁, 24g硫酸镁中,镁元素的质量为:
24
24g100% 4.8g
120
??=,硫酸根的质量=42g-4.8g-19.2g,参加反应的硫酸溶液中硫酸的
质量=
96
19.2g100%19.6g
98
÷?=,参加反应的硫酸溶液的质量=19.6g19.6%=100g
÷;
反应生成的水的质量=82.2g –(100g-19.6g)=1.8g;生成的水中氧元素的质量
=
16
1.8g100% 1.6g
18
??=,根据质量守恒定律可知,氧化镁中氧元素的质量=反应生成水
中氧元素质量=1.6g。原混合物中氧元素的质量分数=
1.6g
100%25%
1.6g+4.8g
?=。故选
C。
4.A~H是初中常见的物质,已知A~G七种物质均含有同一种元素, D的相对分子质量为100,可用作建筑材料。它们之间的转化关系如图所示,图中“一”表示两端物质间能发生化学反应,“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。下列说法中不正确的是
A.A为一种单质,D为碳酸钙
B.可能涉及四种基本反应类型
C.E、F的物质类别可能相同,也可能不同
D.H的浓溶液具有挥发性
【答案】B
【解析】
【分析】
根据D的相对分子质量为100,可用作建筑材料,可以推断D是碳酸钙;根据C和D可以相互转化,则C为二氧化碳;根据A既可以转化成B,又可以转化成C,A既可能是碳,也可能是氧气,但由于题中A~G七种物质均含有同一种元素,本题中这种元素只能是氧元素才能推出合理结论,因此A是氧气,B是一氧化碳;根据D是碳酸钙,E、F均可以转化为碳酸钙,则E、F都可以是可溶性碳酸盐或一种物质是可溶性碳酸盐,一种物质是氢氧化钙;根据D、E、F都可以和G、H反应,且G可以转化为H,在初中阶段可以推知G、H
都是酸,且G是含氧酸,H不一定是含氧酸,在初中阶段可以推断H是盐酸,则G是稀硫酸。因为稀硫酸和粉末状的碳酸钙能反应生成硫酸钙、水和二氧化碳(在不断搅拌时稀硫酸和块状碳酸钙也是能反应的),稀硫酸和可溶性碳酸盐、氢氧化钙都能反应,而稀硫酸和氯化钡反应能生成盐酸,所以推断G是稀硫酸合理。
【详解】
A、根据题意A~G七种物质均含有同一种元素,分析可知A是氧气,是单质。根据D的相对分子质量为100,可用作建筑材料,D是碳酸钙。选项A正确;
B、根据分析,题中反应可能有化合反应如碳和氧气反应生成二氧化碳,可能有分解反应如碳酸钙高温分解生成氧化钙和二氧化碳,有复分解反应如氢氧化钙和盐酸反应,但不可能发生置换反应,因为氧气转变成二氧化碳、氧气转变成一氧化碳、一氧化碳转变成二氧化碳都不可能是置换反应,选项B不正确;
C、因为E、F都可以是可溶性碳酸盐,也可能一种物质是可溶性碳酸盐,一种物质是氢氧化钙,所以E、F的物质类别可能相同,也可能不同,选项C正确;
D、根据分析可知,H是盐酸,浓盐酸具有挥发性,选项D正确。故选B。
5.某同学将mgMg、A1、Zn、Fe 的混合物放入足量的稀盐酸中,充分反应后,将所得溶液小心蒸干,得到(m+7.1) g不含结晶水的固体,则m的取值范围是
A.2.4≤m≤6.5
B.2.4 C.1.8≤m≤6.5 D.1.8 【答案】D 【解析】 【分析】 【详解】 将mgMg、A1、Zn、Fe 的混合物放入足量的稀盐酸中,充分反应后,将所得溶液小心蒸干,得到(m+7.1) g不含结晶水的固体,该不含结晶水的固体是由金属离子(Mg2+、A13+、 Zn 2+、Fe 2+)和Cl - 组成的。根据质量守恒定律可知:不含结晶水的固体中含有Cl -的质量为(m+7.1) g-mg =7.1g 。则该反应消耗稀盐酸的质量为:7.1g ÷ 35.536.5 =7.3g 。 假设分别为四种金属单质与等量的稀盐酸反应,则 2 23212Mg +2HCl =MgCl +H 2Al +6HCl =2AlCl +3H 24 73542197.3g 7.3g x x ↑↑ 1 22454==737.3g 2197.3g x x 12=2.4g =1.8g x x 2 22234Zn +2HCl =ZnCl +H Fe +2HCl =FeCl +H 65 7356737.3g 7.3g x x ↑↑ 346556==737.3g 737.3g x x 34=6.5g =5.6g x x 由计算可知,若为四种金属单质与等量的稀盐酸反应时,m 最大值为6.5g ,最小值为 1.8g ,而该物质为混合物,故m 的最大值应小于6.5g ,最小值应大于1.8g ,故选D 。 6.不能正确反映对应变化关系的图像是( ) A .在一定量的CuSO 4溶液中逐滴加入NaOH 溶液 B .等质量的Zn 和Mg 分别与足量等体积等质量分数的稀硫酸反应 C .向NaOH 溶液中逐滴加入稀盐酸 D .等质量CaCO 3分别与足量等体积等质量分数的稀盐酸反应 【答案】C 【解析】A. 在一定量的CuSO 4溶液中逐滴加入NaOH 溶液,两者之间反应生成氢氧化铜沉淀和硫酸钠;B. 镁的活动性比锌的强,所以镁先反应完;等质量的Zn 和Mg 分别与足量等体积等质量分数的稀硫酸反应,镁比锌生成氢气多。C. 氢氧化钠溶液呈碱性,pH 大于7,盐酸溶液的pH 小于7,向NaOH 溶液中逐滴加入稀盐酸,溶液的pH 应逐渐减小;D. 等质量CaCO 3分别与足量等体积等质量分数的稀盐酸反应,通常粉末状时,药品和盐酸接触更充分,反应较快;当块状石灰石反应时,速率较慢;但过氧化氢质量相同时,生成物的质量相同。选C 点睛:图像的问题主要是结合化学反应分析图的起点的位置,变化趋势,终点的位置是否 正确 7.下列说法正确的是() A.根据质量守恒定律,2gH2跟8gO2完全反应,可得到10gH2O B.用含Fe2O385%的赤铁矿160t,理论上可生产100t含杂质4. 8%的生铁 C.各取10g镁粉和锌粉,分别与足量的盐酸完全反应,镁粉产生的H2多,说明镁的金属活动性比锌强 D.将l0gCuSO4·5H2O与90gH2O混合,固体完全溶解,可得100g溶质的质量分数为10%的CuSO4溶液 【答案】B 【解析】 【详解】 A、氢气和氧气反应的化学方程式为:,在此反应中氢气、氧气和水的质量关系4:32:36=1:8:9,则1gH2能与8gO2完全反应生成9g水,反应后氢气有剩余,错误; B、160t赤铁矿中含氧化铁的质量为:160t×85%=136t。 设136t氧化铁理论上可以炼出铁的质量为x。 x=95.2t 可炼得含杂质4. 8%生铁的质量为:95.2t÷(1-4.8%)=100,正确; C、金属与酸反应,产生气体的多少与金属的活动性没有关系,错误; D、l0gCuSO4·5H2O中CuSO4的质量为:10g××100%=6.4g。与90gH2O混合,固体完全溶解,可得100g溶质的质量分数为:×100%=6.4%,错误。 故选B。 8.有一包固体粉末X,可能含有碳酸钙、硫酸铜、硫酸亚铁、锌粉,为确定固体粉末的成分,现取X进行下列实验,实验过程及现象如下图所示(不考虑水、稀盐酸的挥发),下列说法中正确的是( ) A.若气体1为纯净物,则溶液2中可能含有三种阳离子 B.若气体1为混合物,则溶液2中可能含有Fe2+ C.若溶液1呈无色,则固体粉末X中不可能含有硫酸铜 D.若溶液2呈浅绿色,则沉淀2不可能是纯净物 【答案】B 【解析】 【分析】 有一包固体粉末X,可能含有碳酸钙、硫酸铜、硫酸亚铁、锌粉。取固体粉末X,加入足量水,过滤,得到溶液1和沉淀1,在沉淀1中加入过量稀盐酸,有沉淀2、溶液2和气体1生成。因为目前所学的除了银离子和稀盐酸产生氯化银沉淀,其他任何物质与稀盐酸反应均无法生成沉淀,根据题意不含银离子,所以沉淀1中包含两种沉淀,为碳酸钙和沉淀2,且可知沉淀2不和稀盐酸反应,结合题意,所以该沉淀2一定是铜,铜的来源是第一步骤硫酸铜和锌反应生成硫酸锌和铜,所以固体粉末X中一定有锌、硫酸铜和碳酸钙。分四种情况讨论:①若固体粉末X只存在锌、硫酸铜和碳酸钙。取固体粉末X,加入足量水,过滤,得到溶液1和沉淀1,溶液1为硫酸锌。a:硫酸铜与锌反应时,硫酸铜过量,沉淀1为碳酸钙和铜。在沉淀1中加入过量稀盐酸,碳酸钙和稀盐酸反应生氯化钙、水、二氧化碳,铜不和稀盐酸反应,所以沉淀2为铜,溶液2为氯化钙,气体1为二氧化碳。符合题意。b:硫酸铜与锌反应时,锌过量,沉淀1为碳酸钙和铜和锌。在沉淀1中加入过量稀盐酸,碳酸钙和稀盐酸反应生氯化钙、水、二氧化碳,铜不和稀盐酸反应,锌和稀盐酸反应生成氯化锌和氢气,所以沉淀2为铜,溶液2为氯化钙和氯化锌,气体1为二氧化碳和氢气。符合题意。②若固体粉末X中存在锌、硫酸铜、碳酸钙和硫酸亚铁,且锌的量只能和硫酸铜反应,锌全部反应完全,无法继续和硫酸亚铁反应,硫酸亚铁存在于溶液1中,即溶液1中含有硫酸锌和硫酸亚铁,其他与①a相同。③若固体粉末X中存在锌、硫酸铜、碳酸钙和硫酸亚铁,且锌与硫酸铜反应后剩余,锌会与硫酸亚铁反应生成硫酸锌和铁。取固体粉末X,加入足量水,过滤,得到溶液1和沉淀1,溶液1为硫酸锌,沉淀1 为碳酸钙和铜、铁。碳酸钙和稀盐酸反应生氯化钙、水、二氧化碳,铜不和稀盐酸反应,铁和稀盐酸反应生成氯化亚铁和氢气,所以气体1包括二氧化碳和氢气两种,溶液2包括氯化钙和氯化亚铁两种。沉淀2为铜。④若固体粉末X中存在锌、硫酸铜、碳酸钙和硫酸亚铁,且锌与硫酸铜反应后剩余,锌会与硫酸亚铁反应生成硫酸锌和铁,反应后锌仍剩余。取固体粉末X,加入足量水,过滤,得到溶液1和沉淀1,溶液1为硫酸锌,沉淀1 为碳酸钙和铜、铁、锌。碳酸钙和稀盐酸反应生氯化钙、水、二氧化碳,铜不和稀盐酸反应,铁和稀盐酸反应生成氯化亚铁和氢气,锌和稀盐酸反应生成氯化锌和氢气,所以气体1包括二氧化碳和氢气两种,溶液2包括氯化钙和氯化亚铁、氯化锌三种。沉淀2为铜。【详解】 A、若气体1为纯净物,根据分析,①的a情况和②两种情况均符合,这两种情况时溶液2中只有氯化钙,只有两种阳离子为钙离子和氢离子,故选项错误; B、若气体1为混合物,则符合①的b情况和③、④,溶液2对应氯化钙、氯化锌;氯化钙和氯化亚铁;氯化钙、氯化铁、氯化锌三种情况,则溶液2中可能含有Fe2+,故选项正确; C、若溶液1呈无色,则固体粉末X中可能含有硫酸铜,因为硫酸铜和锌反应生成硫酸锌和铜,溶液1为硫酸锌溶液,无色,只要保证硫酸铜完全反应即可,故选项错误; D、若溶液2呈浅绿色,则符合③和④两种情况,此时沉淀2均只有铜,为纯净物,故选项错误。故选B。 9.区别生活中常见的物品,其中有两种方法都正确的是( ) A.A B.B C.C D.D 【答案】B 【解析】 A、厕所清洁剂显酸性,能与石灰石的主要成分碳酸钙反应生成二氧化碳,产生冒气泡的现象;厨房洗涤剂显碱性,与石灰石不反应;两种物质溶于水都无明显的放热现象; B、 NH4NO3氮肥和K2SO4钾肥,加Ca(OH)2研磨,硝酸铵会生成氨气,能闻到刺激性气味,硫酸钾不能;硝酸铵溶于水,溶液温度降低,硫酸钾无明显现象; C、苏打是碳酸钠和小苏打是碳酸氢钠,加水,都能溶解;加入稀HCl都能生成二氧化碳气体;D 羊毛织品和尼龙织品,触摸纺织品无明显差异,抽丝灼烧,羊毛会有烧焦羽毛的气味。选B 点睛:鉴别题要做到同一操作下或与同一物质反应时,现象要不同。 10.将金属镁和另一种金属X的混合物共a g,加入Cu(NO3)2、Fe(NO3)2的混合溶液中,充分反应后过滤,得到滤液和滤渣。相关分析错误的是( ) A.若滤渣中含有Fe,则滤渣中也一定含有铜 B.若滤液中有两种溶质,则滤渣中可能有三种金属 C.若滤渣中只有一种金属,则滤液中一定含有两种溶质 D.若滤渣的质量为a g,则金属活动性顺序有可能是Mg>X>Fe>Cu 【答案】C 【解析】 A、镁、铁、铜的金属活动性顺序是Mg>Fe>Cu,金属镁先置换出铜,再置换出铁。若滤渣中含有Fe,则滤渣中也一定含有铜,正确; B、若金属镁的量不足,没有将Fe(NO3)中的铁置换完,则滤液中溶质有硝酸镁和硝酸亚铁,滤渣有铜和铁,由于金属X的活动性不确定,可能位于铁之后,故滤渣中可能有三种金属,正确; C、若滤渣中只有一种金属,则此金属为铜,若镁没有将硝酸铜中的铜置换完,则滤液中含有三种溶质,错误; D、镁与硝酸铜、硝酸亚铁反应,置换出铜、铁,滤渣质量增加。由于加入混合物的质量为ag,且滤渣的质量为a g,那么X必须置换出铜或铜、铁,且相对原子质量比铜、铁要大(如锌),正确。故选C。 11.某碳酸钙和氧化钙组成的混合物中,钙元素的质量分数为50%,将40g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是() A.8.8g B.12g C.15.7g D.20g 【答案】B 【解析】 【详解】 根据质量守恒定律可知,反应前后Ca元素质量不变。若将化学式变形转换为,则。 故选B。 12.下列说法中正确的是( ) 选项事实观点 A某物质分解生成二氧化碳和水该物质由C、H、O元素组成 B酸溶液能使石蕊变红颜色发生改变的变化不一定是化学变化 C碱溶液都显碱性显碱性的溶液不一定是碱 D 氢氧化钠溶液稀释后pH减小,硫 酸溶液稀释后pH变大 溶液稀释后pH都会发生变化 A.A B.B C.C D.D 【答案】C 【解析】 A、某物质分解生成二氧化碳和水,该物质中一定含有C、H、O元素,还可能含有其它元素,错误; B、溶液中颜色发生改变,有新物质生成,一定是化学变化,错误; C、碱溶液都显碱性,显碱性的溶液不一定是碱,如碳酸钠是盐,但显碱性,正确; D、氯化钠溶液稀释后pH不会发生变化,错误。故选C。 13.下列四个图像反映了对应实验过程中相关量的变化,其中正确的是() A.A B.B C.C D.D 【答案】A 【解析】 A向一定质量的氢氧化钠溶液中加入稀硫酸时,不断反应生成硫酸钠,氢氧化钠完全反应,硫酸钠的质量不再改变;B锌和硫酸反应生成硫酸锌和氢气,反应中氢气的质量增加,硫酸完全反应,氢气的质量不再增加;C高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,反应后固体物质的质量减少,但固体中锰元素的质量不变,所以反应中固体中锰元素的质量分数增加,反应结束,不再改变;D二氧化锰是过氧化氢分解的催化剂,反应前后,二氧化锰的质量不变。选A 点睛:图像的问题主要是结合化学反应分析图的起点的位置,变化趋势,终点的位置是否正确 14.A、B、C、为初中化学常见物质,它们之间的转化关系如下图所示(反应条件,部分反物和生成物已略去,“→”表示直接转化关系)。某同学推断正确的是 A.若A为碳酸钙,B为氧化钙,则C一定为水 B.若C为H2O,B为CO2,则A可以为酸、盐、氧化物 C.若A为氧化铁,B为铁,则C可以为FeSO4 D.若A为FeSO4,B为CuSO4,B→C一定发生的是置换反应 【答案】B 【解析】 【分析】 【详解】 A、若A为碳酸钙,碳酸钙可以在高温煅烧条件下生成氧化钙,B可为氧化钙,氧化钙可以与酸反应生成水,碳酸钙可以与酸反应生成水,但是C不一定为水,可以是盐,如氯化钙,硝酸钙等,推断错误,故不符合题意; B、若C为H2O,CO2与碱反应可以生成H2O,则A可以为酸,如碳酸可以转化为二氧化碳和水;可以为盐,如碳酸盐可以直接转化为二氧化碳和水;可以为氧化物,如氧化铁可以与碳单质或酸直接转化为二氧化碳和水。推断正确,故符合题意; C、若A为氧化铁,氧化铁可以被碳、一氧化碳、氢气等置换得到铁单质,B可为铁,铁与稀硫酸反应生成硫酸亚铁,C可以为FeSO4,氧化铁不能直接与酸或其他物质反应生成硫酸亚铁,推断错误,故不符合题意; D、若A为FeSO4,B为CuSO4, FeSO4无法直接转化为CuSO4;B→C可能发生的是置换反应生成盐,如加入锌置换生成硫酸锌。推断错误,故不符合题意; 故选B 15.已知A、B、C、D、E是初中化学中常见的五种物质,均含有同一种元素。其中,A为单质, B和C含有相同的元素。它们在一定条件下的转化关系如图所示(“→”表示物质间的转化关系,反应条件和部分反应物、生成物已省略),根据初中所学知识判断下列说法正确的是() A.A→B的反应一定是化合反应 B.D和E的物质类别可以相同,也可以不同 C.若D是一种白色固体,则B→D的反应属于复分解反应 D.若C为单质, A和B含有相同的元素,其他条件不变。则D→B的反应一定是分解反应【答案】B 【解析】 【详解】 A、A为单质, B和C含有相同的元素,A能生成B和C,故A→B的反应可能是化合反应,也可能是置换反应,如A是碳,B是二氧化碳,C是一氧化碳,故A选项错误; B、当A为碳,B为二氧化碳、C为一氧化碳时,D、E分别可以是碳酸钠和碳酸钙,都属于盐;D、E分别也可以是碳酸钙和碳酸,属于不同类物质,故B选项正确; C、当D为碳酸钙,B为二氧化碳时,B→D的反应不属于复分解反应,故C错误; D、若C为单质, A和B含有相同的元素,则C可能是氧气,A可能是过氧化氢,B可能是水,则D可能是氢氧化钙,氢氧化钙生成水的反应不一定是分解反应,故D选项错误。故选B。 16.A~F都是初中化学中常见的物质,其中A、B、C是氧化物,且A是红棕色粉末,D、F均是单质。它们之间的转化关系如右图所示(“→”表示物质转化的方向;部分反应物、生成物和反应条件未标出)。下列有关说法正确的是 A.反应①~④中一定包含复分解反应 B.做反应①的实验,要先加热A再通入B C.反应④用于湿法冶金,可制取Zn、Cu、Ag D.E可以是酸、盐或有机化合物 【答案】D 【解析】 试题分析∶由题中信息知,A、B、C是氧化物,且A是红棕色粉末,D、F均是单质。故A 是氧化铁,B是一氧化碳,C是二氧化碳,D是铁。故A,B.C.均错误。D正确。 考点∶考查常见物质的性质。 17.著名化学家傅鹰说“化学给人以知识,化学史给人以智慧。”下列有关化学史的说法正确的是() A.阿伏伽德罗等科学家得出结论:分子中原子的重新组合是化学变化的基础 B.拉瓦锡用红磷燃烧的实验证明氧气约占空气总体积的五分之一 C.我国著名实业家侯德榜发明了制取烧碱的“侯氏制碱法” D.波义耳发现了质量守恒定律 【答案】A 【解析】 A.阿伏伽德罗在化学学科中的主要成就,是提出了分子学说,道尔顿提出原子论,阿伏伽德罗提出分子论,都是对物质构成的理论解释,结合二者的理论,有的物质是分子构成的,也可以是原子构成的,在化学变化中,由分子构成的物质,分子中的不同种类和数目的原子将重新组合为新的分子,即在化学变化中,分子变为原子,原子再重新结合生成新的分子.B、拉瓦锡在化学学科中的主要成就,是首次利用天平为化学研究的工具进行定量实验,并首先通过实验得出空气是由氮气和氧气组成的结论,C. 我国著名实业家侯德榜成功地摸索和改进了西方的制碱方法,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法)。D. 波义尔用敞口容器在空气中加热金属,金属与空气中的氧气发生了化学反应,由于有外界的氧气参加反应,可回顾波义尔得出的结论不守恒。而罗蒙诺索夫因为是 在密封玻璃瓶内加热金属,金属虽然也被氧化,但是至于玻璃瓶内的氧气发生了化学反应,故反应前后的质量不变,从而得出了质量守恒定律。选A 点睛:多了解化学通史,熟记科学家们的贡献 18.烧杯中盛有一定质量的氧化镁和氧化铁的固体混合物,向其中加入稀盐酸 100 g ,恰好完全反应,得到该温度下的不饱和溶液 120 g 。再向其中加入足量氢氧化钠溶液,充分反应后过滤,将沉淀洗涤、干燥、称量,其示数为 27.2 g 。则下列相关计算中,不正确的是( )。 A .原固体中金属元素质量为 13.6g B .所用盐酸的溶质质量分数为 29.2% C .最终所得溶液中含有 NaCl 58.5g D .实验中消耗的氢氧化钠质量为 32g 【答案】C 【解析】 【详解】 根据MgO 、Fe 2O 3和酸反应及与碱反应的关系,找出增量,以MgO 为例: - 2 MgO ~2HCl ~2OH ~2NaOH ~2~O ~Mg(OH)NaCl ~405818增量 设所用盐酸的溶质质量分数为x ,氢氧根的质量为y ,实验中消耗的氢氧化钠质量为z ,最终所得溶液中含有NaCl 的质量为m ,则: -2HCl ~2OH ~2NaOH ~2NaCl ~73 348011718100gx y z m (27.2-20)g 增量 x=29.2% y=13.6g z=32g m=46.8g 原固体中金属元素质量为 27.2g-13.6g=13.6g ,故选C 。 19.已知AgNO 3见光易分解,aAgNO 3=bNO 2↑+cO 2↑+ dX (NO 2能与NaOH 反应)。取34 g AgNO 3加热至完全反应,将所得气体依次通过NaOH 溶液、均热的铜网,测得NaOH 溶液增重9.2g ,灼热的铜网增重3.2g 。下列说法不正确的是 A .AgNO 3应保存在棕色瓶中 B .生成X 的质量为21.6g C .X 是银 D .c: d=1: 1 【答案】D 【解析】 【分析】 将所得气体依次通过NaOH 溶液、均热的铜网,测得NaOH 溶液增重9.2g ,灼热的铜网增重3.2g 。说明34 g AgNO 3加热至完全反应,生成二氧化氮9.2g ,氧气3.2g 。根据质量守恒定律可知,生成X 一定含有银元素,它的质量为34g-9.2g-3.2g=21.6g 。34g 硝酸银中银元素 的质量为, 34108 21.6 10814163 g g ? = ++? ,X一定是银。 【详解】 A、AgNO3见光易分解,AgNO3应保存在棕色瓶中,说法正确,不符合题意; B、生成X的质量为21.6g,说法正确,不符合题意; C、X是银,说法正确,不符合题意; D、3.221.6 32108 g g c b =,c:d=1:2,符合题意。 故选D。 20.下图中“—”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,部分反应物、生成物及反应条件未标出。则不可能出现的情况是 A.A B.B C.C D.D 【答案】B 【解析】 A氧化汞受热分解生成汞和氧气;汞与氧气在一定条件下反应生成氧化汞。B、碳和氧气不完全燃烧生成一氧化碳;碳不能通过反应转化成氧气;C碳酸分解生成二氧化碳和水,二氧化碳和水反应生成碳酸;D氯化钡和碳酸钠反应生成碳酸钡沉淀,氯化钡和硫酸反应生成硫酸钡和盐酸。选B 点睛:熟练掌握常见化学方程式,掌握物质间的转化方法。 二、实验题(培优题较难) 21.过氧化钙(CaO2)在生产中具有广泛的应用 (一)过氧化钙的性质与用途 鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_______,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因________。 (二)过氧化钙晶体的制备 (资料)过氧化钙晶体(CaO2·y H2O),常温为白色,能溶于酸,难溶于酒精。制备原理:CaCl2+H2O2+NH3+H2O→CaO2·yH2O↓+NH4Cl,装置如下。 (1)装置A中试管内发生反应的化学方程式为____ (2)B装置的作用是______。 (3)装置C需要控制温度在0℃左右,采用的简单易行的办法是____,控制温度在0℃左右可能的原因主要有: Ⅰ该反应是放热反应,温度低有利于提高CaO2·y H2O产率; Ⅱ______。 (4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·y H2O。 ①洗涤时采用95%的酒精溶液洗涤的优点是______。 ②检验晶体已洗涤干净的试剂为________。 (三)过氧化钙晶体组成的测定 称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水) (1)0—150℃质量不发生改变的原因是__________。 (2)根据图可知y= ____。(写出计算过程) (3)350℃时发生反应的化学方程式为________。 【答案】Ca(OH)2氢氧化钠具有很强的腐蚀性 NH4Cl+Ca(OH)2Δ CaCl2+NH3↑+H2O 防止倒吸 C中放入冰水混合物,保持冰水浴防止双氧水受热分解(或防止氨气挥发)快速晾干硝酸银溶液未达到过氧化钙晶体分解所需要的温度 2 2CaO2高温 2CaO+O2↑ 【解析】 【分析】 【详解】 (一)(1)由题目信息可知,根据质量守恒定律,过氧化钙与水反应生成氢氧化钙和氧气,所以碱是氢氧化钙;过氧化钠与水反应后生成了氢氧化钠,氢氧化钠具有强腐蚀性;(二)(1)氯化铵与氢氧化钙反应生成氯化钙、水和氨气,化学方程式:NH4Cl+Ca (OH)2Δ CaCl2+NH3↑+H2O。 (2)反应生成了氨气,氨气极易溶于水,造成内部压强减小,增加了B起到缓冲作用,避免造成压强减小,液体被倒吸入试管,引起试管炸裂; (3)反应温度为0℃,冰水混合物温度恰好是0℃,所以可以在C中放入冰水混合物,实现温度控制;过氧化氢在高温加热条件下容易分解,同时氨气为气体受热也容易逸出,所以需要控制温度; (4)酒精易挥发,用酒精洗涤可以快速晾干,避免过氧化钙与水接触发生反应;根据氯离子与银离子生成白色沉淀,滴加硝酸银溶液观察是否有沉淀生成; (三)(1)结晶水需要加热到一定温度才可以失去,在0-150℃的范围内,未达到过氧化钙晶体分解所需要的温度,温度不足以失去结晶水,所以质量不变; (2)失去水的质量=10.8g-7.2g=3.6g,剩余过氧化钙质量=7.2g,过氧化钙分子数:水分子 数=7.2g 72 : 3.6g 18 =1:2,所以y=2; (3)过氧化钙受热分解后剩余固体质量为5.6g,减少质量为7.2g-5.6g=1.6g,假设过氧化 钙分解生成氧化钙和氧气,根据质量守恒定律化学方程式为2CaO2高温 2CaO+O2↑,此时 生成氧化钙与氧气质量比=112:32=7:2,而剩余固体质量:减少质量=5.6g:1.6g=7:2, 符合上述推断,所以化学方程式为2CaO2高温 2CaO+O2↑; 22.小红学碱的性质时做了如图两个实验,并把两个实验的滤液都倒入了一个烧杯中,结果烧杯中产生了少量气泡,最终还有白色沉淀生成。回答下列问题: (1)实验①中酚酞溶液的作用___________________。 (2)实验②中滤液的溶质除有氢氧化钠外,还有________________(填化学式)。 (3)烧杯中产生白色沉淀物的化学方程式____________。 (4)小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有: 猜想1:还可能含有CaCl2 猜想2: 还可能含有___________,为了验证猜想1提出方案如下: 实验操作实验现象实验结论 猜想1正确 取烧杯中的少量滤液于试管 中,加入Na2CO3溶液_____________________ 【答案】显示中和反应发生及反应程度Na2CO3CaCl2+Na2CO3 = CaCO3↓+2NaCl Na2CO3 有白色沉淀 【解析】 (1)澄清石灰水解稀盐酸均为无色透明的溶液,实验①中酚酞溶液的作用是显示中和反应发生及反应程度;(2) 把两个实验的滤液都倒入了一个烧杯中,结果烧杯中产生了少量气泡,最终还有白色沉淀生成。证明实验②中滤液的溶质除有氢氧化钠外,还有Na2CO3;(3) 碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,故烧杯中产生白色沉淀物的化学方程式为:CaCl2+Na2CO3 = CaCO3↓+2NaCl;(4)如果氯化钙和碳酸钠恰好完全反应,则溶质为氯化钠;若氯化钙过量,则溶质除了氯化钠以外还有氯化钙;若碳酸钠过量,则溶质除了氯化钠以外还有碳酸钠,故小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有:猜想1:还可能含有CaCl2;猜想2:还可能含有Na2CO3;为了验证猜想1提出方案如下: 实验操作实验现象实验结论 取烧杯中的少量滤液于试管 中,加入Na2CO3溶液 _______有白色沉淀 _____________ 猜想1正确 23.某品牌纯碱中含有少量氯化钠.某化学探究小组为了测定该纯碱的纯度(即碳酸钠的质量分数),组内一同学设计了如下实验: (设计实验方案) 实验装置(如图2所示,固定装置略去); 需要测定的实验数据:纯碱样品的质量;实验前、后装置(包括氢氧化钠固体)的总质量. (1)A装置中反应的化学方程式为;为了保证纯碱样品中的碳酸钠完全反应,其操作是. (2)B装置的作用是;C装置中反应的化学方程式为. (3)补充D装置(简要叙述或画出装置示意图). (交流与表达) (4)有同学认为图2所示实验装置会造成测得纯碱的纯度偏低,原因是. (5)为了克服图2装置的不足,有同学提出,还应增加图1装置与A装置连接(A装置中原双孔橡胶塞换成三孔橡胶塞),在反应前、后用图1装置分两次缓缓鼓入足量空气. ①反应前,断开B、C装置之间的连接,用图1装置鼓入空气的作用是; ②反应后,用图1装置鼓入空气的作用是; ③在A装置中的反应发生时,开关R处于关闭状态,其原因是. (数据处理) (6)称得的纯碱样品质量为10.8g,实验前、后C装置的总质量分别为75.2g和79.6g,纯碱的纯度为%(计算结果保留小数点后一位). (反思与评价) (7)能否用稀盐酸代替稀硫酸?同学们经过讨论认为不能,理由是. (8)改进后的实验装置能减少测定的误差,原因是①反应生成的CO2尽可能被C装置吸收;②. 【答案】(1)Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;逐滴滴入稀硫酸至不再产生气泡为止;(2)除去水蒸气;2NaOH+CO2═Na2CO3+H20;(3)装氢氧化钠固体的球形管;(4)AB 装置中残留反应产生的二氧化碳气体未被C中的氢氧化钠吸收;(5)①用不含二氧化碳的空气排出AB装置中原有的空气;②用不含二氧化碳的空气排出残留在AB装置中反应产生的二氧化碳气体;③避免图1装置吸收反应产生的部分二氧化碳气体;(6)98.1%;(7)稀盐酸会发出氯化氢气体,被C装置吸收,影响实验测定; (8)避免AB装置中原来空气中二氧化碳气体对实验的干扰. 【解析】 【分析】 【详解】 (1)反应物是Na2CO3和H2SO4生成物是Na2SO4、H2O和CO2用观察法配平,二氧化碳后面标上上升符号;因为该反应有气泡产生,没有气泡产生了,说明反应完了; (2)浓硫酸具有吸水性,所以主要是除去二氧化碳中的水蒸气;C装置中反应的反应物是NaOH和CO2生成物是Na2CO3和H20,用观察法配平; (3)D装置是防止空气中的水、二氧化碳进入C装置造成误差,所以用装氢氧化钠固体的球形管就能达到目的; (4)反应结束后在AB装置中会残留反应生成的二氧化碳气体未被C中的氢氧化钠吸收,导致二氧化碳质量减少,结果会偏小; (5)①鼓入的空气经过了氢氧化钠,已经把空气中二氧化碳除去,用不含二氧化碳的空气排出AB装置中原有的空气,由于原有的空气中含有二氧化碳; ②用不含二氧化碳的空气排出残留在AB装置中反应产生的二氧化碳气体,使反应产生的二氧化碳全部被C装置吸收; ③如果不处于关闭状态,生成的二氧化碳会进入图1被图1中氢氧化钠吸收; (6)C装置质量的增加量就是生成二氧化碳的质量,所以生成二氧化碳的质量为:79.6g﹣75.2g=4.4g,设要生成4.4g二氧化碳需要碳酸钠质量为X则: Na CO+H SO=Na SO+H O+CO 23242422 10644 x 4.4g 10644 = x 4.4g X=10.6g,纯碱的纯度为10.6g 10.8g ×100%=98.1%; (7)稀盐酸会挥发出氯化氢气体,被C装置吸收,影响实验测定; (8)改进后装置的优点有:反应生成的CO2尽可能被C装置吸收;避免AB装置中原来空气中二氧化碳气体对实验的干扰. 24.小红、小军、小明三人化学学习小组在实验中,用到了三个分别盛有KCl溶液、KOH 溶液、K2SO4溶液的滴瓶. 小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行了如下探究. (提出问题)该滴瓶中溶质的成分是什么? (提出猜想)通过分析,提出如下猜想: 猜想Ⅰ溶质成分只有:KCl; 猜想Ⅱ溶质成分为:KCl和KOH; 猜想Ⅲ溶质成分为:; 猜想Ⅳ溶质成分为:KCl、KOH和K2SO4。 (实验探究)为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告; (实验反思)小明认为该实验方案并未证明猜想Ⅱ、Ⅲ是否成立,应补充相应实验予以证明,你是否赞 同?(选填“是”或“否”). 【答案】【提出猜想】KCl、K2SO4 【实验探究】(1)BaCl2+K2SO4═BaSO4↓+2KCl (2)酚酞试液酚酞试液变红色 【实验反思】否 【解析】 【提出猜想】 猜想:溶质成分只有KCl;溶质成分为KCl和KOH;溶质成分为:KCl、K2SO4;溶质成分为:KCl、KOH和K2SO4. 最新中考化学二模试题及答案 一、选择题 1.NaCl是重要的资源,其应用与生产如下图所示。下列说法不正确的是 A.应用①操作的主要步骤为:计算、称量、溶解、装瓶、贴标签 B.应用②在制备烧碱的过程中,水参与了反应 C.应用③为提高产率应先通NH3,再通CO2,制备过程中还能得到一种化肥 D.生产中提纯粗盐时可依次加入过量的BaCl2、NaOH、Na2CO3溶液,再过滤、蒸发 2.向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是 A.a点溶液中滴入紫色石蕊试液变红 B.bc段(不含b点)反应的化学方程式为: MgCl2 +2NaOH==Mg(OH)2↓+2NaCl C.整个变化过程中氯离子数目没有改变 D.d点溶液中含有两种溶质 3.下表物质中含有少量杂质,其中除杂方法正确的是 物质杂质除去杂质的方法 A CaCl2溶液HCl滴入碳酸钠溶液 B CO2O2通过灼热的铜网 C NaOH Na2CO3加入稀盐酸至不再产生气泡 D CuO Cu加足量稀盐酸,充分搅拌后再过滤 A.A B.B C.C D.D 4.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是() A.滤渣中一定有银、没有铜和锌B.滤渣中一定有银和锌,可能有铜 C.滤液中一定有硝酸锌、硝酸铜、硝酸银D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 5.下列4个坐标图分别表示4个实验过程中的某些变化,其中正确的是 A.向含有稀硫酸的硫酸铜溶液中加氢氧化钠溶液 B.向一定量的稀盐酸中加入铁粉 C.稀释pH =2的稀硫酸 D.氢氧化钠溶液中滴加盐酸 6.已知FeCl3也可以催化H2O2的分解,现向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,充分反应(忽略水的挥发).下列图象正确的是( ) A.B. C.D. 7.为了达到实验目的,下列方案或结论正确的是 2017年四川省成都实验外国语学校直升选拔数学试卷 一、单项选择题 1.(3分)据调查,某市2016年的房价为9000元/m2,预计2018年将达到11000元/m2,求这两年的年平均增长率,设年平均增长率为x,根据题意,所列方程为() A.9000(1+x)=11000B.9000(1+x)2=11000 C.9000(1﹣x)=11000D.9000(1﹣x)2=11000 2.(3分)关于x的方程ax2﹣(3a+1)x+2(a+1)=0有两个不相等的实根x1、x2,且有x1﹣x1x2+x2=1﹣a,则a的值是() A.1B.﹣1C.1或﹣1D.2 3.(3分)一个几何体由若干个小立方块搭成,它的主视图、左视图和俯视图如图所示,则搭出这个几何体的小立方块的个数是() A.4个B.5个C.6个D.7个 4.(3分)如图,△ABC中,AB⊥BC,AB=3,BC=4,D为△ABC的内心,则△ABD的面积是() A.B.C.D.2 5.(3分)对于任意的﹣1≤x≤1,ax+2a﹣3>0恒成立,则a的取值范围为()A.a>1或a=0B.a>3C.a>3或a=0D.1<a<3 6.(3分)一个平面封闭图形内(含边界)任意两点距离的最大值称为该图形的“直径”,封闭图形的周长与直径之比称为图形的“周率”,下面四个平面图形(依次为正三角形、正方形、正六边形、圆)的周率从左到右依次记为a1,a2,a3,a4,则下列关系中正确的是() A.a4>a2>a1B.a4>a3>a2C.a1>a2>a3D.a2>a3>a4 7.(3分)△ABO顶点坐标分别为A(1,4),B(2,1),O(0,0),如果将△ABO绕点O 按逆时针方向旋转90°,得到△A′B′O,那么线段A′B′的中点坐标是()A.(﹣,)B.(﹣2,)C.(﹣2,2)D.(﹣,2)8.(3分)如图,在四边形ABCD中,AB⊥BC,AB=3,BC=4,CD=5,AD=5,则BD=() A.5B.C.D.8 9.(3分)如图,在△ABC中,D、E分别为BC,AB中点,F在AC上且AF=2FC,AD与EF交于点G,则=() A.3:7B.4:9C.5:11D.6:13 10.(3分)将函数y=3x+b(b为常数)的图象位于x轴下方的部分沿x轴翻折至其上方后,所得的折线是函数y=|3x+b|的图象,若该图象在直线y=3下方的点的横坐标x满足0<x <3,则b的取值范围为() A.b<﹣6或b>﹣3B.b≤﹣6或b≥﹣3C.﹣6<b<﹣3D.﹣6≤b≤﹣3 11.(3分)二次函数y=ax2+bx+c(a≠0)经过原点,当x=﹣1时,﹣2≤y≤1;当x=2时,0≤y≤4,则当x=1时,y的取值范围为() A.﹣≤y≤﹣B.﹣≤y≤3C.﹣≤y≤2D.﹣≤y≤3 成都外国语学校上期期末综合测试 一年级语文试卷 (总分:100分) 第一题:(2分) :1.。2.。 第二题:(60分) (一),。(10分) 火 zh ōn ɡ z ǒu zh īd ǐ 氵 中 li ù s ān di ǎn shu ǐ 辶 上 shu ǐ ji ǎo s īp án ɡ 犭 六 hu ǒ f ǎn qu ǎn p án ɡ 纟 水 sh àn ɡ b ǎo ɡài 宀 (二),,。(5分) 参加 升旗 跳高 商场 冷暖 sh ēn ɡ q í ti ào ɡāo c ān ji ā l ěn ɡ nu ǎn sh ān ɡ ch ǎn ɡ (三),(8分) sh í b ā s ān ɡè d à r én ti ān sh àn ɡ ( ) ( ) ( ) ( ) r ì yu è ch ǐ zi f ēi ni ǎo ɡu ǒ p í ( ) ( ) ( ) ( ) (四)?“√”,“×”。(4分) z òu ér zh ēn z ɑì 做( ) 鹅( ) 真( ) 在( ) xi ɑò w ǎn ɡ d àn d ēn ɡ 校( ) 晚( ) 电( ) 灯( ) (五),“√”。(3分) 公(机 鸡) (河 和)水 电(视 是) (六)按笔顺规则写字,数笔画填空。(4分) 风__________________共( )笔 ; 耳____________________ 共( )笔 (七),,。(12分) 读 兔 竹 机 丢 迷藏 骑 书 左 右 捉 手绢 白 车 飞 桥 跑 河 老 师 衣 服 拔 步 姓 班级___________ 座位 …… … … … … … … … 装 … … …… 订 … … … … 线 … … … … 内 … … … … 不 … … … … 要 … … … … 答 … … … … 题 … … … … … … … … … 江苏省镇江市润州区届中考化学二模试题 说明:1.本试卷共6页,满分100分。考试时间90分钟。 2.考生必须在答题纸上指定区域内作答,在本试卷上和其他位置作答一律无效。 3.相对原子质量:H-1、C-12、N-14、O-16、S-32、Na-23、Mg-24、Cl-35.5、Ca-40、 一、单项选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意) 1.下列属于纯净物的是(▲ ) A.冰红茶 B.液态氮 C.碳素钢 D.大理石 2.下列变化属于化学变化的是(▲ ) A.食物变质 B.海水晒盐 C.矿石粉碎 D.石油分馏 3.下列对化学用语的表述正确的是(▲ ) A.氯化铝——AlCl B.Fe2+——铁离子 C.2个汞原子——2Hg D.纯碱——NaOH 4.下列做法正确的是(▲ ) A.煤气不慎泄露,立即开灯检查 B.甲醛浸泡海鲜,防止腐烂变质 C.禁止使用农药,保护水体资源 D.垃圾分类处理,资源合理利用 5.下列对物质的归类不正确的是(▲ ) 选项归类物质 A 常见碱氨水、烧碱、熟石灰 B 化石燃料煤气、石油、天然气 C 有机化合物甲烷、醋酸、纤维素 D 常见净水物质氯气、明矾、活性炭 6.根据侯氏制碱原理制备少量NaHCO3,下列装置和原理不能达到实验目的的是(▲ ) 甲乙丙丁 A.装置甲:制NH3B.装置乙:制NaHCO3 C.装置丙:分离NaHCO3 D.装置丁:干燥NaHCO3 7.下列实验设计错误的是(▲ ) A .用蒸馏的方法可以使硬水软化 B .用湿润的红色石蕊试纸检验NH 3 C .用灼热的铜网除去N 2中的O 2 D .用100mL 量筒量取5.6 mL 溶液 8.下列排列顺序正确的是 ( ▲ ) 9.下列对实验现象的描述正确的是 ( ▲ ) A .加碘食盐溶液中加入淀粉,溶液变蓝 B .硫粉在空气中燃烧,产生无色无味气体 C .氯化钡溶液中通入二氧化碳,出现白色沉淀 D .鸡蛋清溶液中滴入饱和硫酸铵溶液,出现白色浑浊 10.下图是某反应的微观示意图,下列说法错误的是 ( ▲ ) A .乙和丁为氧化物,一定条件下可相互反应 B .反应生成丙和丁的个数比为1:1 C .甲为有机物,其中C 和N 元素质量比为3:7 D .反应前后原子的种类和个数不变 11.下列化学方程式与实际相符,且书写正确的是 ( ▲ ) A .炼钢的本质:C+O 2 CO 2 B .酸雨形成的原因:CO 2+H 2O =H 2CO 3 C .湿法炼铜:2Fe+3CuSO 4═Fe 2(SO 4)3+3Cu D .电石跟水反应制取乙炔:CaC 2+H 2O =Ca(OH)2+C 2H 2↑ 12.物质性质决定用途。下列说法正确的是 ( ▲ ) A .氧气具有可燃性,可用于炼钢 B .金刚石硬度大,可用于切割玻璃 C .浓硫酸具有吸水性,可用于干燥氨气 D .氢氧化钠具有碱性,可用于治疗胃酸过多 13.下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的的是 ( ▲ ) 选项 物质 目的 主要实验操作 C .人体中元素含量: 由高到低 由大到小 汽水 糖水 肥皂水 A .氮元素的化合价: NH 3 N 2 NaNO 3 由低到高 B .金属的使用年代: D .常见溶液的pH : 由先到后 Al 、Cu 、Fe Ca O C 点燃 催化剂 + + 一定条件 甲 乙 丙 丁 氢原子 碳原子 氮原子 氧原子 2020年成都某实验外国语学校西区招生语文真卷 (满分:100分时间:90分钟) 一、积累与运用。(25分) 1.下列选项中加点字注音有误的一项是( )(2分) A.闷.热(mēn) 羞怯.(qiè)蜷.伏(quán) 畏罪潜.逃(qián) B.呻.吟(shēn)教诲.(huǐ) 感慨.(kǎi) 随声附和.(hè) C.热忱.(chén)虐.待(nüè)惩.戒(chéng) 杞.人忧天(qǐ) D.哺.乳(bǔ) 称.职(chèn)柠.檬(nínɡ) 拈.轻怕重(niān) 2.将下列成语补充完整,并按要求分类。(11分) (1)大义( )然为虎作( ) 道( )岸然天( )海角 应接不( ) 光明( )落盛气( )人心( )意马含赞美意思的词语:(2分)含批评意思的词语:(2分) (2)我还能写出三个含赞美意思的成语:(3分) 3.结合语境选词填空,表述最恰当的一项是( )(3分) 在我们赖以生存的绿色星球上,着几块色彩斑斓的陆地,那是地球上的五大洲:在陆地中间着辽阔的蓝色水域,那是地球的四大洋。这里有生命存在,各种生物活跃在多彩的生态系统中,它们这个星球以绿色的情调和生命的意义。 A.嵌入布满呈现 B.勾勒填充馈赠 C.镶嵌充盈赋予 D.勾画覆盖给予 4.下列各句中,加点的成语使用正确的一项是( )(3分) A.旅游业已成为当地经济发展的支柱产业,这里巧夺天工 ....的鱼然美景闻名天下,每年都吸 引大量游客前来观赏。 B.持续多日强降雨导致部分地区山洪暴发,农田被淹,房屋倒塌。灾情扣人心弦 ....,相关部门正全力以赴组织救灾? C.多年未见的战友意外相逢,一见如故 ....,回忆起出生入死的战斗经历,不禁感慨万千。 D.夕阳像一个巨人被捆缚了手脚,使出浑身解数 ....,憋红了脸,在天边挣扎。 5.下列语句中没有语病的一项是( )(3分) A.5月10日,大约一百名左右的青年志愿者在橘子洲参加了绿色骑行活动。 B.在暑假的户外活动中,同学们要注意安全,防止不要发生意外事故。 C.为了规范义务教育阶段招生行为,长沙市教育局严禁公办学校招收择校生。 D.将建设美丽乡村和打造文化景区相结合,既能改善农村居住环境,又能发扬文化旅游产业。 6.下面的句子,按先后顺序排列最恰当的一项是( )(3分) ①小溪的一边是果园,春天,花香弥漫,蜂飞蝶舞。 ②田野的尽头,连绵的山峰犹如大海里起伏的波涛, ③溪水那么清澈、明净,水里的鱼儿快乐地游来游去。 ④山腰间的公路,像一条银灰色的绸带飘向远方。 ⑤一条小溪从我们村子里流过÷ ⑥小溪的另一边是田野,如今沉甸甸的麦穗,正点着头报告丰收的喜讯: A.④⑤③①⑥② B.⑤③①⑥②④ C.⑤①⑥③②④ D.④⑤①⑥③② 二、根据提示填写诗句。(10分) 一、选择。下面各题均有四个选项,其中只有一个符合题意,选出答案后,将答案填写在答题纸相应的位置上。(共12分。每小题2分) 1.下列词语中加点字的读音完全正确的一项是 A.庇护(bì)巢穴(xué)胆怯(qiè)迫不得已(pǒ) B.翘首(qiào)琐屑(xiè)解剖(pōu)惩恶扬善(chénɡ) C.倔强(jué)呜咽(yè)机械(jiè)刚正不阿(ē) D.堤岸(dī)踱步(duó)谋略(móu)忍俊不禁(jīn) 2.对下列各组词语中两个加点的字解释有误的一项是 A.巧妙绝伦络绎不绝 解释:两个“绝”字意思不同,“巧妙绝伦”的“绝”是“独一无二”的意思,“络绎不绝”的“绝”是“断绝”的意思。 B.锐不可当首当其冲 解释:两个“当”字意思相同,都是“抵挡”的意思。 C.自强不息息息相关 解释:两个“息”字意思不同,“自强不息”的“息”是“停止”的意思,“息息相关”的“息”是“呼吸”的意思。 D.一劳永逸闲情逸致 解释:两个“逸”字意思相同,都是“安乐”“安闲”的意思。 3.下列句子中加点的词语运用不正确的一项是 A.你现在就为几千万年以后才有可能出现的天体变化担心,岂非杞人忧天? B.北京小吃举世闻名,在此谈吃,要谦虚点,切不可班门弄斧,贻笑大方。 C.昨天足球赛中他一人进了两球,今天眼里就没有别人了,真是一叶障目,不见泰山。D.行百里者半九十,最后进入决赛的选手更要认真对待,不可掉以轻心。 4.结合语境,填入横线处最恰当的一项是 知识是形成新创意的素材。但这并不是说,光凭知识就能拥有创造性。发挥创造力的真正关键,在于如何运用知识。创造性的思维,必须有 , ,在此基础上,持之以恒地进行各种尝试。 A.孜孜不倦地汲取知识,并为此而活用知识的态度和意识 B.探求新事物,使自己学识渊博的态度和意识 C.孜孜不倦地汲取知识,使自己学识渊博的态度和意识 D.探求新事物,并为此而活用知识的态度和意识 5. 下列各句没有语病的一项是 A.大量的事实告诉我们,环境灾害是没有国界的。 B.是否多读书,也是提高一个人语文素养的途径之一。(逻辑错误,前后不对应)C.他与其去网上聊天,也不愿和同学们打个招呼。(误用关联词语) D.通过综合性学习,使我们不但增长了知识,而且提高了发现问题和解决问题的能力。6.根据语言环境,填在横线上表达效果最好的一项是 戏曲中最让我动情的是河北梆子,苍凉高亢,嘶喊哭号,大吵大闹,如醉如痴。哦,我的燕赵故乡,你太压抑,又太奔放,你太古老,又太孩子气了。 A.强刺激的河北梆子,是我们土生土长的“滚石乐”。 B.强刺激的河北梆子,是我们土生土长的“滚石乐”吗? C.强刺激的河北梆子,不能说是我们土生土长的“滚石乐”。 D.强刺激的河北梆子,这不就是我们土生土长的“滚石乐”吗? 数学期末检测题 A卷(100分) 一、选择题(共20分,每小题2分) 1、已知两个有理数的积为正数,则这两个有理数的符号为…………() A.都是正数 B.都是负数 C.一正一负 D. 选项.都有可能3.已知-26,则3(x-2y)2-5(x-2y)+6的值是(). A.84 B.144 C.72 D.360 4、若方程x =的解为5,则a等于() ax3 5+ A. 80 B. 4 C. 16 D. 2 5.用小立方块搭成的几何体的一个视图为 ,这一定( ) A.是左视图 B.是主视图 C.是俯视图 D.不是俯视图 6.如图中四个图形折叠后所得正方体与所给正方体的各个面上颜 色一致的是( ) 7.下列四句话中,正确的个数有(). ①过两点有且只有一条直线 ②在同一平面内两条不同的直线有且只有一 个公共点 ③过直线外一点,有且只有一条直线与已知直线平行 ④两条直线同时与第三条直线平行,那么这两条直线平行 A .1 B .2 C .3 D .4 8.已知,⊥,∠:∠2:3,则∠的度数为( ). A .30° B .150° C .30°或150° D .不同于上述答案 9.某种细菌在培养过程中,细菌每半小时分裂一次(由一个分裂为两个),经过两小时,这种细菌由1个可分裂繁殖成( ) A.8个; B.16个; C.4个; D.32个 10.一个口袋内装有大小和形状都相同的一个红球和一个黄球, 那么“从中任意摸出一个球,得到黄球”这个事件是( ) A.必然事件 B.不确定事件; C.不可能事件 D.无法判断是哪类事件 二、填空题(共30分,每小题3分) 1、圆柱的侧面面展开图是 ;圆锥的侧面展开图是 。 2、 的倒数为-8,平方等于9的数为 。 3、_______;a ,02)3(b 2==-++则 如果b a 4.用度、分、秒表示48.26°. 5.∠450 ,∠300 ,则∠0 . 6.代数式 3457 ab c 的系数是,次数是. 7.若-5x 4与2x 25 是同类项,则. 8、当2-时,二次三项式422++mx x 的值等于18,那么当2时,该代数式的 值等于. 9、.我国人均水源占有量为2400立方米,则13亿中国人水源占有总量为立方米.(用科学记数法表示) 10、若4 2=-=+x y x , ,则. 三、计算下列各题(共24分,每小题4分) 1、156(3)3 -+÷-?;; 2、)]4()2[(3032---÷- 科粤版2020年中考化学二模试题及答案 一、选择题(培优题较难) 1.某化学兴趣小组为测定Fe 、Cu 、Ag 三种金属的活动性顺序,选用下列各组试剂,你认为不可行的是 A .Cu 、Ag 、FeSO 4溶液 B .Cu 、FeCl 2溶液,AgNO 3溶液 C .Fe 、Ag 、CuSO 4溶液 D .Fe 、Cu 、稀硫酸,AgNO 3溶液 【答案】A 【解析】根据金属活动顺序进行思考,Fe 、Cu 、Ag 这三种金属的金属活动性由强到弱的顺序为Fe >Cu >Ag .在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱. A 、因为铁的活动性在三种金属中最强,所以Cu ,Ag 都不能和FeSO 4溶液反应,得不出Cu ,Ag 的活动性强弱,所以此方案不可行. B 、Cu ,FeCl 2溶液,AgNO 3溶液这三种物质中,铜与FeCl 2溶液不反应,证明铁的活动性比铜强,铜与AgNO 3溶液能反应,证明铜比银的活动性强,此方案可行. C 、铁可以置换CuSO 4溶液中的铜而出现红色固体,证明铁的活动性比铜强,银和CuSO 4溶液不反应,证明铜比银的活动性强,因此,可以证明三种金属的活动性强弱,此方案可行. D 、Fe ,Cu ,稀硫酸,AgNO 3溶液四种物质中,铁能与稀硫酸反应,也能与AgNO 3溶液反应,证明铁比氢和银的活动性强,铜和稀硫酸不反应,但能与AgNO 3溶液反应,证明铜的活动性比氢弱,比银强,也能得出三种金属的活动性强弱,此方案可行.故选B . 2.向盛有一定质量MgO 和MgCO 3混合物的烧杯中加入142 g 稀盐酸,恰好完全反应,一定温度下,得到150 g 不饱和溶液。下列数据中,与该溶液的溶质质量分数最接近的是 A .5.3% B .5.6% C .12.7% D .13.4% 【答案】C 【解析】 【分析】 【详解】 氧化镁和稀盐酸反应生成氯化镁和水,碳酸镁和稀盐酸反应生成氯化镁、水和二氧化碳; 22MgO 2HCl=MgCl H O 409540 ++溶液增加质量 3222MgCO 2HCl=MgCl H O CO 848444=4044 +-↑++溶液增加质量 可见生成的氯化镁相同时造成的溶液质量增加是相等的,与是氧化镁还是碳酸镁反应无关; 设生成的氯化镁的质量为x ,则 2018—2019学年度九年级二模语文试题 (全卷共140分,考试时间:150分钟) 一积累与运用(20分) 1.古诗文默写。(10分) (1)▲,归雁入胡天。 (2)长风破浪会有时,▲。 (3)▲?曹刘。▲。 (4)无可奈何花落去,▲。 (5)▲,▲,▲。此之谓大丈夫。 (6)《渔家傲·秋思》中用典故表达戍边将士思念家乡却又不甘无功而返的矛盾心理的诗句是▲,▲。 2.下列词语中加点字的字音和字形全都正确的一项是(▲)(3分) A.蜷.曲(ju?n)熟稔.(rěn)祈.愿(qí)惩.恶扬善(ch?ng) B.雏.形(chú)亘.古(ɡènɡ)嗔.怒(chēn)心无旁鹜.(wù) C.回溯.(shuò)戏谑.(xuè)慰藉.(jí)通宵.达旦(xiāo) D.缄.默(jiān)羸.弱(léi)懊.悔(ào)风雪载.途(zài) 3.阅读下面一段文字,回答问题。(4分) 静,是一种气质,也是一种修养。诸葛亮云:“非淡泊无以明志,非宁静无以致远。”心浮气躁,是成不了大气候的。静是要经过(▲)的,古人叫作“习静”。唐人诗云:“山中习静朝观槿,松下清斋折露葵。”“习静”可能是道家的一种功夫,习于安静确实是生活于(▲)的尘世中人所不易做到的。静,不是一味地孤寂,不闻世事。我很欣赏宋儒的诗:“万物静观皆自得,四时佳兴与人同。”惟静,才能观照万物,对于人间生活充满盎然的兴致。静是合乎人道,也是顺乎自然的。 ⑴为文中括号处选择恰当的词语。(2分) 锻炼锻造扰攘繁杂 ⑵文中画线句有语病,请修改。(2分) ▲ 4.下列关于文学常识、文化知识表述不正确 ...的一项是(▲)(3分) A.“铭”是古代刻在器物上用来警诫自己或者称述功德的文字,后来成为一种文体,一般都用韵,如刘禹锡的《陋室铭》。 B.《简·爱》一书讲述了一位孤女在经历各种磨难中不断追求自由与尊严,坚持自我,最终 获得幸福的故事。主人公简·爱是一个性格坚强、独立自主、积极进取的女性形象。 C.《诗经》是我国最早的诗歌总集,也是我国诗歌现实主义传统的源头,它汇集了从西周到春 秋时期的305首诗歌。风、雅、颂、赋、比、兴合称“六义”,是古人对《诗经》艺术经验的总结。 D.“黄发垂髫,并怡然自乐”中的“垂髫”指代儿童,原因是古代儿童未成年时不戴帽子,头 发下垂。同样,“总角”“弱冠”也指代童年。 二阅读(57分) (一)阅读文言文语段,完成5~9题。(17分) 萧相国何者,沛丰人也。以文无害为沛主吏掾。 高祖为布衣时,何数以吏事护高祖。高祖为亭长,常左右之。高祖以吏繇咸阳,吏皆送奉钱三,何独以五。 秦御史监郡者与从事,常辨之。何乃给泗水卒史事,第一。秦御史欲入言征何,何固请,得毋行。 及高祖起为沛公,何常为丞督事。沛公至咸阳,诸将皆争走金帛财物之府分之,何独先入收秦丞相御史律令图书藏之。沛公为汉王,以何为丞相。项王与诸侯屠烧咸阳而去。汉王所以具知天下厄塞,户口多少,强弱之处,民所疾苦者,以何具得秦图书也。何进言韩信,汉王以信为大将军。语在《淮阴侯》事中。 …… 汉五年既杀项羽定天下论功行封。群臣争功,岁余功不决。高祖以萧何功最盛,封为酂侯,所食邑多。功臣皆曰:"臣等身被坚执锐,多者百余战,少者数十合,攻城略地,大小各有差。今萧何未尝有汗马之劳,徒持文墨议论,不战,顾反居臣等上,何也?"高帝曰:"诸君知猎乎?"曰:"知之。""知猎狗乎?"曰:"知之。"高帝曰:"夫猎,追杀兽兔者狗也,而发踪指示兽处者 2015年成都市成都外国语学校自主招生考试数学试卷 (考试时间:120分钟满分:150分) 第Ⅰ卷(选择题,共45分) 一、选择题:每小题3分,共45分. 1.﹣|﹣|的负倒数是() A.B.C.D. 2.计算:(a2b)3的结果是() A.a6b B.a6b3C.a5b3D.a2b3 3.在式子,,,中,x可以取1和2的是() A.B.C.D. 4.如图,H7N9病毒直径为30纳米(1纳米=10﹣9米),用科学记数法表示这个病毒直径的大小,正确的是() A.30×10﹣9米B.3.0×10﹣8米 C.3.0×10﹣10米D.0.3×10﹣9米 5.的平方根是() A.4 B.﹣4 C.2 D.±2 6.如图,AB∥CD,点E在BC上,且CD=CE,∠D=74°,则∠B的度数为() A.68°B.32°C.22°D.16° 7.已知a2﹣5a+1=0,则a+﹣3的值为() A.4 B.3 C.2 D.1 8.在平面直角坐标系中,点P(﹣2,a)与点Q(b,3)关于原点对称,则a+b的值为() A.5 B.﹣5 C.1 D.﹣1 9.下列命题中真命题是() A.有理数都能表示成两个整数之比 B.各边相等的多边形是正多边形 C.等式两边同时乘以(或除以)同一个实数,所得结果仍是等式 D.相等的圆心角所对的弧相等,所对的弦相等 10.已知|a|=2,|b|=3,则|a﹣b|=5的概率为() A.0 B.C.D. 11.某几何体的主视图、左视图和俯视图分别如图所示,则该几何体的体积为() A.3πB.2πC.πD.12 12.某校九年级共有1100名学生参加“二诊”考试,随机抽取50名学生进行总成绩统计,其中有20名学生总成绩达到优秀,估计这次“二诊”考试总成绩达到优秀的人数大约为() A.400 B.420 C.440 D.460 13.若x1,x2是方程x2+2x﹣k=0的两个不相等的实数根,则x12+x22﹣2是() A.正数B.零 C.负数D.不大于零的数 14.已知△ABC的三边长分别为a、b、c,面积为s;△A′B′C′的三边长分别为a′,b′,c′,面积为s′,且a>a′,b>b′,c>c′,则s与s′的大小关系一定是() A.s>s′B.s<s′C.s=s′D.不确定 15.b>a,将一次函数y=ax+b与y=bx+a的图象画在同一个直角坐标系内,则能有一组a、b的取值,使得如下四个图中为正确的是() A.B. C.D. 中考化学二模试题和答案 一、选择题(培优题较难) 1.如图所示的装置可用来测定某气体X的组成。在注射器A中装有0.32g气体X并慢慢通过不含空气并装有足量灼热的氧化铜的玻璃管B,使气体X完全反应。得到以下实验结果:实验前B管重20.32g,实验后B管重20.00g,B管中出现红色粉末。C管中收集到的无色液体是水;注射器D中收集到生成氮气0.28g。下列说法正确的是( ) A.B管中发生的反应为置换反应 B.气体X是氨气(NH3) C.该反应中生成的水与氮气的分子个数比为1:2 D.气体X中氮元素与氢元素的质量之比为7:1 【答案】D 【解析】 【详解】 A、X气体中含有氮元素、氢元素,所以一定不是单质,氧化铜属于化合物,所以B管中反应一定不是置换反应,错误; B、实验前B管重20.32克,实验后B管重20.00克,所以氧化铜中氧元素质量为0.32g,因为氧元素和氢元素结合生成水,所以氢元素质量为:0.04g,收集到生成的氮气0.28克, 气体中氮元素质量为0.28g,所以氮元素与氢元素原子个数比为:0.28g0.04g :=1:2 141 ,所 以气体不是氨气,错误; C、实验前B管重20.32克,实验后B管重20.00克,所以氧化铜中氧元素质量为0.32g,因为氧元素和氢元素结合生成水,所以氢元素质量为:0.04g,所以生成水的质量为: 0.32g+0.04g=0.36g,该反应中生成的水与氮气的分子个数比为0.36g0.28g :=20:1 1828 ,错 误; D、实验前B管重20.32克,实验后B管重20.00克,所以氧化铜中氧元素质量为0.32g,因为氧元素和氢元素结合生成水,所以氢元素质量为:0.04g,收集到生成的氮气0.28克,气体中氮元素质量为0.28g,气体X中氮元素与氢元素的质量比为:0.28g:0.04g=7:1,正确。 故选D。 【点睛】 根据气体与氧化铜反应生成铜、氮气和水来分析X的组成,氮气的质量就是气体中氮元素 成都实验外国语学校 2017年高中自主招生数学真卷(直升卷) 一、选择题 1、根据调查,某市2016年的房价为9000元/平方米,预计2018年的房价将达到11000元/ 平方米,求这两年的平均增长率,设年平均增长率为x ,根据题意,所列方程为 ( ) A.()1100019000=+x B.()11000190002 =+x C.()1100019000=-x D.()11000190002 =-x 2、关于x 的方程()()012132=+++-a x a ax 有两个不相等的实数根1x ,2x ,且a x x x x -=+-12211, 则a 的值是 ( ) A.1 B.-1 C.-1或1 D.2 3、一个几何体由若干个小立方块搭成,它的主视图、左视图、俯视图分别如下,则搭建这个 几何体的小立方块的个数是 ( ) A.4 B.5 C.6 D.7 4、如图,ABC ?中,BC AB ⊥,3=AB ,4=BC ,D 为ABC ?的内心, 则ABD ?的面积是 ( ) A.43 B.23 C.25 D.2 5、对于任意的11≤≤-x ,032>-+a ax 恒成立,则a 的取值范围为 ( ) A.1>a 或0=a B.3>a C.03=>a a 或 D.31<> B.214a a a >> C.321a a a >> D.432a a a >> 2020年中考语文二模试卷 本试卷分为第Ⅰ卷(选择题)、第Ⅱ卷(非选择题)两部分。试卷满分120分。考试时间120分钟。 第Ⅰ卷(共27分) 一、(本大题共11小题,共27分。1~4小题,6~7小题,每题2分;5小题,8~11小题,每题3分) 1.下面各组词语中加点字的读音,完全正确的一项是 A.惆.怅(chóu) 顷.刻(qīnɡ)鲜.为人知(xiǎn) B.畸.形(jī)盘桓.(huán)戛.然而止(ɡá) C.冗.杂(rǒnɡ)告罄.(qìnɡ)忧心忡忡 ..(zhǒnɡ) D.追溯.(sù)绯.红(fēi)风雪载.途(zài) 2.依次填入下面一段文字横线处的词语,最恰当的一项是 危急时刻,人们往往会①自己,反省自己的不足,补齐自身的短板。而在平常时候,人们则容易失去②,习惯于从自身利益的角度去思考问题,判断是非,而不是检视自己有无不足、缺点和失误。当自省机制失去效力,③责人而不自省,只找别人毛病,而不找自己原因,往往会使小纠纷酿成大事故。正所谓:“各自责,天清地宁;各相责,④。” A.①警觉②警醒③凡事④天高地厚 B.①警觉②警醒③凡是④天翻地覆 C.①警醒②警觉③凡事④天翻地覆 D.①警醒②警觉③凡是④天高地厚 3.下面语段中的句子,有语病的一项是 ①为保证避免疫情防控万无一失,做好排查,网格员每天都忙碌在社区里。②工作中,他们还会重点关注独居老人、空巢老人等特殊群体,询问生活物资是否齐全,是否需要帮助采买,体温是否正常等。③网格虽小,却是和老百姓联系最紧密的服务窗口。④为社区居民处理好每一件小事、急事、难事,是社区网格员的工作职责。 A.①句B.②句C.③句D.④句 4.依次填入下面一段文字方框内的标点符号,最恰当的一项是 早在周代,我国就有了图书馆。只不过,那时不叫图书馆,叫 盟府 ,主要保存盟约 图籍、档案等与皇室有关的资料。严格地说,这只是图书馆的雏形 老子堪称中国历史上第一位图书馆馆长,据 史记 记载,老子“姓李氏,名耳,字聃,周守藏室之史也”。这个“守藏室”,就是藏书之所。 A.“”、。《》B.“”,,“” C.《》、,“” D.《》,。《》 5.下面对辛弃疾《破阵子·为陈同甫赋壮词以寄之》一词的赏析,不恰当的一项是 破阵子·为陈同甫赋壮词以寄之 成都外国语学校2015年初升高直升考试 一、选择题(每小题3分,共45分) 1. 5 3--的负倒数是 ( B ) A. 35- B. 35 C. 53- D. 5 3 2. 计算:(a 2b )3的结果是 ( B ) A. a 6b B. a 6b 3 C. a 5b 3 D. a 2b 3 3. 在式子 11-x ,2 1-x ,1-x ,2-x 中,x 可以取1和2的是 ( C ) A. 11-x B. 21-x C. 1-x D. 2-x 4. H7N9病毒直径为30纳米(1纳米=10-9 米),用科学计数法表示这个病毒直径的大小,正确的是( B ) A. 30×10-9米 B. 3.0×10-8米 C. 3.0×10-10米 D. 0.3×10-9米 5. 16的平方根是( D ) A.4 B.-4 C.2 D.2± 6. 如图,AB//CD,点E 在BC 上,CD=CE,∠D=74°,则∠B 的度数为( B ) A. 68° B. 32° C. 22° D. 16° 7. 已知a 2-5a+1=0,则a+a 1-3的值为( C ) A. 4 B. 3 C. 2 D. 1 8. 在平面直角坐标系中,点P (-2,a )与点Q (b,3)关于原点对称,则a+b 的值为( D ) A.5 B.-5 C.1 D.-1 9. 下列命题中真命题是( A ) A. 有理数都能表示成两个整数之比 B. 多边相等的多边形是正方形 C. 等式两边同时乘以同一个实数,所得结果仍是实数 D. 相等的圆心角所对的弧相等,所对的弦相等 10. 已知2a =,3=b ,则5=-b a 的概率为( B ) A. 0 B. 21 C. 31 D. 41 2020-2021学年四川省成都实验外国语学校(西区)八年级(上)入学数学试卷一、选抨题(每小题3分、共30分) 1.(3分)下列计算正确的是() A.a2+a3=a5B.a6÷a3=a2 C.5x﹣3x=2D.(﹣2a2b)3=﹣8a6b3 2.(3分)2015年4月,生物学家发现一种病毒的长度约为0.0000043米,利用科学记数法表示为()A.4.3×106米B.4.3×10﹣5米C.4.3×10﹣6米D.43×107米 3.(3分)随着生活水平的不断提高,汽车越来越普及,在下面的汽车标志图中,不属于轴对称的图形是() A.B.C.D. 4.(3分)计算结果为a2﹣5a﹣6的是() A.(a﹣6)(a+1)B.(a﹣2)(a+3)C.(a+6)(a﹣1)D.(a+2)(a﹣3) 5.(3分)已知三角形的三边长分别为4,5,x,则x不可能是() A.3B.5C.7D.9 6.(3分)如图,在下列条件中,能判断AB∥CD的是() A.∠DAC=∠ACB B.∠DCB+∠ADC=180° C.∠ABD=∠BDC D.∠BAC=∠ADC 7.(3分)下列算式不能用平方差公式计算的是() A.(2x+y)(2y﹣x)B.(3x﹣y)(3x+y) C.(x+1)(﹣x+1)D.(x﹣y)(y+x) 8.(3分)如图,已知∠BAC=∠DAC,那么添加下列一个条件后,仍无法判定△ABC≌△ADC的是() A.CB=CD B.AB=AD C.∠BCA=∠DCA D.∠B=∠D 9.(3分)某学习小组做“用频率估计概率的试验时,统计了某一结果出现的频率,绘制了如图所示折线统计图,则符合这一结果的试验最有可能的是() A.掷一枚正六面体的骰子,出现1点朝上 B.任意写一个整数,它能被2整除 C.不透明袋中装有大小和质地都相同的1个红球和2个黄球,从中随机取一个,取到红球 D.先后两次掷一枚质地均匀的硬币,两次都出现反面 10.(3分)如图,AD是△ABC的角平分线,DF⊥AB,垂足为F,DE=DM,△ADM和△AED的面积分别为58和40,则△EDF的面积为() A.11B.10C.9D.8 二、填空题(本大题共4个小题,每小题4分,共16分) 11.(4分)已知5a=2,5b=3,则52a+b=. 12.(4分)若(2a﹣1)2=4a2+ma+1,则m的值是. 13.(4分)如图,以△ABC的顶点A为圆心,以BC长为半径作弧,再以顶点C为圆心,以AB长为半径作弧,两弧交于点D;连接AD、CD,若∠B=56°,则∠ADC的大小为度. 文言文阅读 【2018 东城二模】 (三)文言文阅读(共8分) 曹刿论战 十年春,齐师伐我。公将战。曹刿请见。其乡人曰:“肉食者谋之,又何间焉?”刿曰:“肉食者鄙,未能远谋。”乃入见。问:“何以战?”公曰:“衣食所安,弗敢专也,必以分人。”对曰:“小惠未徧,民弗从也。”公曰:“牺牲玉帛,弗敢加也,必以信。”对曰:“小信未孚,神弗福也。”公曰:“小大之狱.,虽不能察,必以情。”对曰:“忠之属也。可以一战。战则请从。” 公与之乘,战于长勺。公将鼓之。刿曰:“未可。”齐人三鼓。刿曰:“可矣。”齐师败绩。公将驰之。刿曰:“未可。”下视其辙,登轼而望之,曰:“可矣。”遂逐齐师。 既克,公问其故。对曰:“夫战,勇气也。一鼓作气,再而衰,三而竭。彼竭我盈,故克之。夫大国,难测也,惧有伏焉。吾视其辙乱,望其旗靡,故逐之。” 赵威后问齐使 齐王使使者问赵威后。书未发,威后问使者曰:“岁亦无恙邪?民亦无恙邪?王亦无恙邪?”使者不说,曰:“臣奉使使威后,今不问王而先问岁与民,岂先贱而后尊贵者乎?”威后曰:“不然。苟无岁,何以有民?苟无民,何以有君?故有舍本而问末者耶?” 乃进而问之曰:“齐有处士①曰锺离子,无恙耶?是其为人也,有粮者亦食,无粮者亦食;有衣者亦衣,无衣者亦衣。是助王养其民也,何以至今不业②也?叶阳子③无恙乎?是其为人,哀鳏寡,恤孤独,振困穷,补不足。是助王息其民者也,何以至今不业也?北宫之女婴儿子④无恙耶?彻其环瑱⑤,至老不嫁,以养父母。是皆率民而出于孝情者也,胡为至今不朝⑥也?此二士弗业,一女不朝,何以王.齐国,子万民乎?於陵子仲⑦尚存乎?是其为人也,上不臣⑧于王,下不治其家,中不索交诸侯。此率民而出于无用者,何为至今不杀乎?” (选自《战国策·齐策四》) 注:①处士:有才能而隐居不出来做官的人。钟离:复姓。②业:使之作官而成就功业。用作动词,这里指重用。③叶(shè)阳子:齐国的处士。叶阳为复姓。④北宫:复姓。婴儿子,是其名。⑤彻:通“撤”。环瑱(tiàn):耳环和戴在耳垂上的玉。⑥不朝:不上朝,古代女子得到封号才能上朝,这句是说为什么还没有得到封号呢?⑦於陵子仲:於(wū乌)陵,地名,在今山东省长山县西南;子仲,齐国的隐士。⑧臣:用作动词。臣于王,做王的臣。 11. 下面加点字的意思和用法相同的一项是(1分) A.登轼而.望之今不问王而.先问岁与民 B.何以.战以.养父母 C.公问其故.故.有舍本而问末者耶 D.苟.无岁苟.富贵 12.解释文中加点字的意思(2分) (1)小大之狱.狱: (2)何以王.齐国王: 13.用现代汉语翻译划线句的意思。(2分) 小信未孚,神弗福也 答: 14.请根据两篇文章的内容找出相同的地方,填写表格。(3分) 成都实验外国语学校初升高直升选试题 ————————————————————————————————作者:————————————————————————————————日期: 成都市实验外国语学校2013年初升高直升考试试题 化学 试题说明:1.考试时间:90分钟全卷总分:100分 2.本次考试试卷共2张8页。 3.可能用到的相对原子质量:H-1;C-12;O-16;Na-23;Mg-24; Al-27;Si-28;K-39;Ca-40;S-32;Fe-56;Cu-64;Zn-65; 第Ⅰ卷选择题(共40分) 一、单项选择题(本题有8小题,每题2分,共16分) 1.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也叫可入肺颗粒物,与肺癌、哮喘等疾病的发生密切相关,是灰霾天气的主要原因,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等。2012年2月,国务院同意发布新修订的《环境空气质量标准》,增加了PM2.5监测指标。下列与PM2.5相关的说法 不正确 ...的是(D ) A.大力发展电动车,减少燃油汽车的尾气排放量 B.开发利用各种新能源,减少对化石燃料的依赖 C.其颗粒小,在大气中的停留时间长、输送距离远,因而对人体健康影响更大D.是形成沙尘暴天气的主要因素 2.2008年9月27日,太空第一次留下了“中国人的脚印”。我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证。航天员舱外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能具有的化学性质是( C )A.与CO2反应B.与HCl反应 C.与Fe2O3反应 D.与CuCl2溶液反应 3.下列说法中正确的是(D ) ①质子数相同的粒子一定属于同种元素;②质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子; ③电子数相同的粒子不一定是同一种元素 A.①② B.只有② C.①②③ D.②③ 4.某学生的实验报告中有以下实验数据,其中正确的是( D ) A.温度计上显示的度数为25.68摄氏度 B.用量筒量取5.29 ml盐酸 C.用pH试纸测得溶液的pH是5.4 D.用托盘天平称取2.5g锌 一、语言知识及其运用( 12 分) 1.下列字形和加点字注音全部正确的一项是( )( 2 分) A.勾.当(ɡòu)恻隐忍俊不禁.(jìn)妇儒皆知 B.归省.(xǐnɡ)愧作戛 .然而止 (ɡá)销声匿迹 C.藩.篱(fān)瑟索锲.而不舍(qi è)月明风清 D.枯涸.(h é)技俩顶礼膜.拜(mó) 无可质疑 2.下列句子加点词语使用错误的一项是( )(2 分) A.闻一多先生从唐诗下手,目不窥园,足不下楼,兀.兀.穷.年.,沥尽心血。 B.聂老师对待工作认真负责,在教学上常常吹毛求.疵...。 C.在创造的宇宙里,爱因斯坦是光辉灿烂的明星,这是不.言.而.喻.的。 D.学校开展的“安全教育”活动,让广大师生受益.匪.浅..。 3.下列句子没有语病的一项是( )(2 分) A.变色龙随着周围环境的变化而不断变色,是出于生存的本能。 B.过了一会儿,汽车突然渐渐放慢了速度。 C.《水浒》生动叙述了梁山好汉们从起义到兴盛再到最终失败。 D.父母过于溺爱自己的孩子,这对孩子的成长极为不利 4.下列句子组成语段顺序排列正确的一项是()(2 分) ①说故事的人要针对人性的好恶来安排情节,始终抓住听众的兴趣。 ②如果故事很长,则这种循循善诱、引人入胜的功夫尤其重要。 ③说故事面对的听众则比较复杂,听众的注意力比较难以集中。 ④谈天和说故事是有差异的。⑤谈天是和“谈得来的人交谈” ,无须费许多心机去吸引对方。 A.④⑤①③② B.④⑤③①② C.⑤③②①④ D.⑤④②①③ 5.下面与画线句子表意最相近的一项是()(2 分)语文学习要注重打好基础,就像盖房子,根基不牢,房子肯定盖不高。 A.房子能盖得高吗? B.房子能盖不高最新中考化学二模试题及答案
2017年四川省成都实验外国语学校直升选拔数学试卷
成都外国语学校上学期期末试卷
中考化学二模试题 (2)
2020年成都某实验外国语学校西区招生语文真卷
北京市顺义区中考语文二模试题
成都外国语学校成都外国语学校七年级(上)数学期末(含完整答案)(含完整答案)
科粤版2020年中考化学二模试题及答案
2019中考二模语文试卷及答案
2015年成都市成都外国语学校自主招生考试数学试卷(含解析)
中考化学二模试题和答案
成都实验外国语学校2017年高中自主招生数学 真卷
2020年中考语文二模试卷(部编版,含答案)
成都外国语学校2015年数学直升试卷
2020-2021学年四川省成都实验外国语学校(西区)八年级(上)入学数学试卷
2018年中考语文二模试题分类汇编文言文阅读(1)
成都实验外国语学校初升高直升选试题
2020年最新中考语文模拟试卷及答案