药物泊马度胺(Pomalidomide)合成检索总结报告
一、泊马度胺(Pomalidomide)简介
泊马度胺(Pomalidomide)于2013年2月8日于美国上市。泊马度胺(Pomalidomide)是沙利度胺的衍生物,可调节T细胞并抑制其增殖,发挥免疫调节作用,通过激活自然杀伤细胞,促进肿瘤细胞的凋亡。泊马度胺(Pomalidomide)适应于多发性骨髓瘤。泊马度胺(Pomalidomide)不良反应:胎仔毒性、静脉血栓、血液毒性、过敏反应、头晕、神经病变、有第二原发恶性肿瘤的风险。
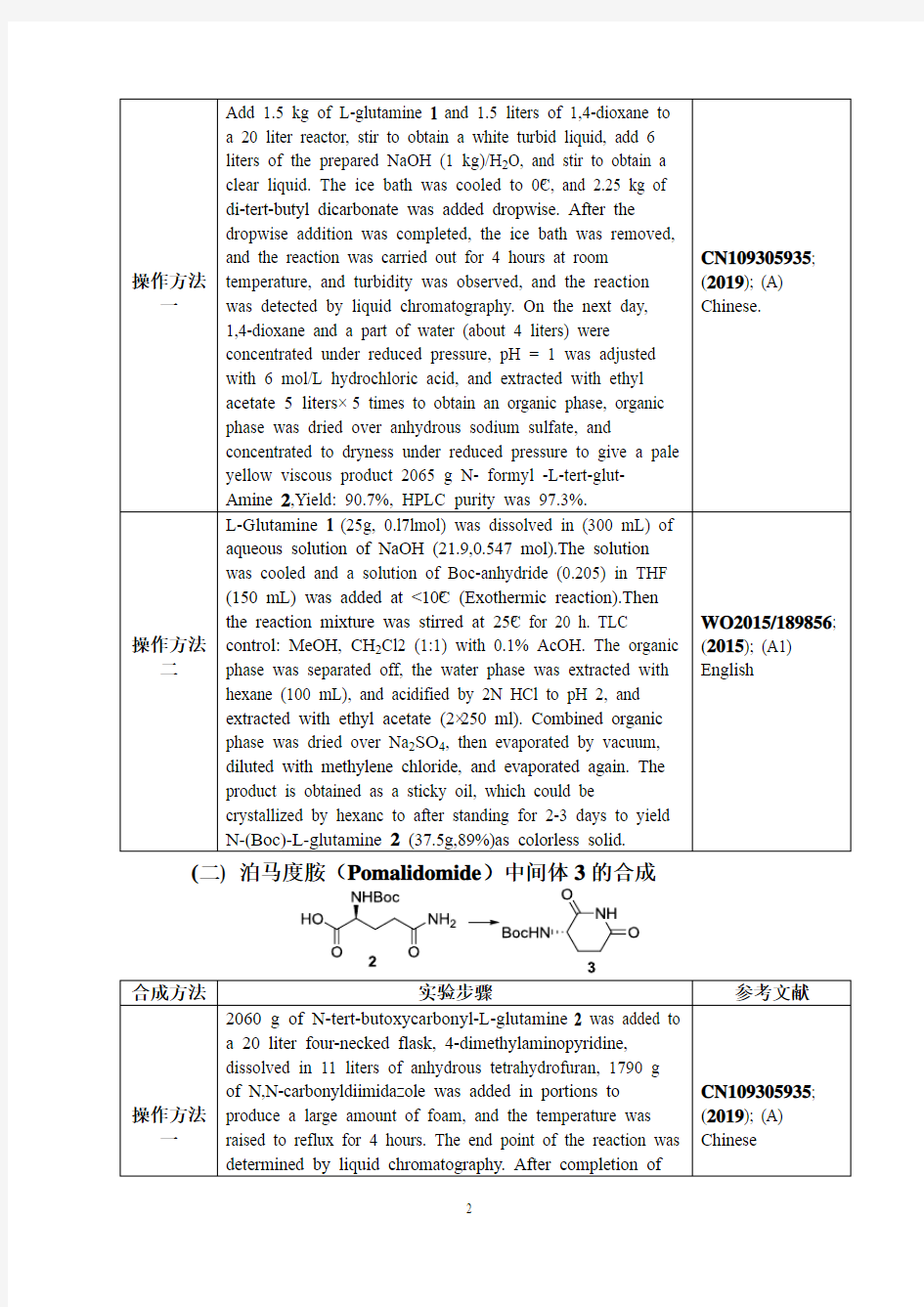
泊马度胺(Pomalidomide)分子结构式如下:
英文名称:Pomalidomide
中文名称:泊马度胺
本文主要对泊马度胺(Pomalidomide)的合成路线、关键中间体的合成方法及实验操作方法进行了文献检索并作出了总结。
二、泊马度胺(Pomalidomide)合成路线
三、泊马度胺(Pomalidomide)合成检索总结报告
(一)泊马度胺(Pomalidomide)中间体2的合成
(
二) 泊马度胺(Pomalidomide )中间体3的合成
糖尿病在发生发展过程中,并发症发病率高达多少? 许多糖尿病患者致死、致残的主要原 因并非糖尿病本身,而是由于糖尿病的并 发症。 糖尿病在发生发展过程中,并发症发病率高达96.15% ,表现复杂,是导致糖尿病患者致死、致残的主 要原因。糖尿病主要并发症有: 感染、低血糖昏迷、糖尿病酮症酸中毒、糖尿病肾病、糖尿病血管病变(包 括糖尿病视网膜病变即微血管病变)、神经病变、糖尿病高渗性昏迷等[1]。 随着人们对糖尿病并发症的发病机制的不断认识,使得糖尿病并发症的治疗途径由以往单一增加胰岛素的降糖作用发展到控制葡萄糖代谢、增加胰岛素受体敏感性、抑制胰岛素抵抗及糖基化终产物的形成、减少氧化应激等方面,不少新型抗糖尿病并发症药物应运而生。现将糖尿病并发症治疗药物及其它正在开发的抗糖尿病新药的最新进展如下。 糖尿病并发症的治疗途径已由单一 向多元转变。不少新型抗糖尿病并发症药 物应运而生。
1 糖尿病并发症治疗药物 1.1 醛糖还原酶抑制剂 糖尿病并发症的成因之一为多元醇代谢活性亢进引起的渗透压异常,即在一些组织,如肾、视网膜、神经和血管中,葡萄糖透入细胞内的过程是非胰岛素依赖性的,由于细胞内外的浓度差而被摄入细胞内的葡萄糖通常代谢为己糖,但如果胞内葡萄糖超过一定数量而形成高血糖时,醛糖还原酶(AR)就会被活化,多元醇通路激活,从而使葡萄糖到山梨醇的转化过程亢进,山梨醇的蓄积便引起渗透压上升,产生组织水肿,发展至基质变化进而发生并发症。另外,AR通过还原性辅酶(NADPH)将葡萄糖转化为山梨醇从而消耗了细胞内贮存的NADPH,使得其他利用NADPH的酶,如谷胱甘肽还原酶、一氧化氮合成酶以及前列腺素过氧化氢酶等的活性受到影响。 由此可知,多元醇通路的激活可通过改变组织渗透压或减少NADPH导致糖尿病并发症的发生,因此,严格控制高血糖时多元醇通路的活性、抑制组织山梨醇的蓄积、减少己糖水平和抑制氧化还原失衡,对控制糖尿病并发症显得非常重要。多项实验表明,AR抑制剂(ARI)可以通过抑制多元醇通路而有效地治疗糖尿病并发症。现时,已有若干ARI进入临床研究阶段(见表1),这些ARI能在实验模型中有效治疗糖尿病并发症。然而,在临床研究中,许多ARI因疗效低、副作用大而被淘汰,正在开发的ARI中较有希望的当属折那司他(Zenarestat)、唑泊司他(Zopolrestat)和AS23201。
头孢呋新(CXM)、红霉素(E)、青霉素(P)、去甲氧万古霉素(NVA)头孢三嗪(CRO)、亚胺培南(IPM)、头孢哌酮(CFP)、头孢唑肟(CZ)、头孢噻肟(CTX)、头孢哌酮/舒巴坦(CFP/SU)、头孢吡肟(FEP)、头孢他啶(CAZ)、阿莫西林(AM)、阿莫西林/舒巴坦AM/SU、复方新诺明(SXT)、阿莫西林/克拉维酸(AM/CA)、庆大霉素(GM)、哌拉西林(PIP)、环丙沙星(CIP)AM 氨节西林/安比西林/氨青霉素AMC 经氨节西林/奥格门丁/克拉维酸 AMx 阿莫西林/轻氨节青霉素 AN 阿米卡星/丁胺卡那霉素/AMK ATM 氨曲南/菌克单/唾肪单酞胺菌素 AZ 阿洛西林/苯咪哩青霉素CAZ 头抱他吮/复达欣/头抱唾甲竣肘 CB 卡比西林/梭节青霉素/CB - - PC CC 克林霉素/氯洁霉素/氯林克霉素 CEC 头抱克罗/CCL /头抱氯氨CF 头抱唾吩/头抱霉素钠/先锋H CFM 头抱克肘/世福素/CFIX CFP 先锋必/头抱氧呱哇/CPZ /头抱呱酮 CIP 环丙沙星/环丙氟呱嚓 CMX 头抱甲肘/头抱氨唾肪哇/倍司特克 CRO 头抱三嗓/CTRX /菌必治CTT 头抱替坦/头抱双硫哇甲氧CTX 头抱噬肪/凯福隆/头抱氨唾肪CXM 头抱吠辛/头抱吠肪/西力欣CZ 头抱哇琳/CEZ /先锋V D 脱氧土霉素/DOXY /强力霉素/多西环素 DP 甲氧苯青霉素/甲氧西林/新青霉素n E 红霉素/EM FOX 头抱西丁/美福仙/CFX FM 吠喃妥因/吠喃坦陡 G 磺胺异嗯哇/512 注:" / ”示前后同药不同名。 英国进口药敏纸片 抗生素英文名全称中文名全称名称缩写浓度产品编号 A Amikacin 阿米卡星(丁胺卡那霉 素) AK 30μg CT0107B Amoxycillin 阿莫西林(羟氨苄青霉 素) AML 2μg CT0060B Amoxycillin 阿莫西林(羟氨苄青霉 素) AML 10μg CT0161B Amoxycillin 阿莫西林(羟氨苄青霉 素) AML 25μg CT0061B Amoxycillin/clavulanic acid 阿莫西林/克拉维酸(棒 酸)(2:1)(澳格门汀) AMC 3μg CT0538B Amoxycillin/clavulanic acid 阿莫西林/克拉维酸(棒 酸)(2:1)(澳格门汀) AMC 30μg CT0223B Ampicillin 氨苄西林AMP 2μg CT0002B Ampicillin 氨苄西林AMP 10μg CT0003B
HIGHLIGHTS OF PRESCRIBING INFORMATION These highlights do not include all the information needed to use POMALYST safely and effectively. See full prescribing information for POMALYST. POMALYST? (pomalidomide) capsules, for oral use Initial US Approval: 2013 WARNING: EMBRYO-FETAL TOXICITY and VENOUS THROMBOEMBOLISM See full prescribing information for complete boxed warning EMBRYO-FETAL TOXICITY ?POMALYST is contraindicated in pregnancy. POMALYST is a thalidomide analogue. Thalidomide is a known human teratogen that causes severe life-threatening birth defects (4, 5.1, 8.1). ?For females of reproductive potential: Exclude pregnancy before start of treatment. Prevent pregnancy during treatment by the use of 2 reliable methods of contraception (5.1, 8.6). POMALYST is available only through a restricted program called POMALYST REMS TM (5.2). VENOUS THROMBOEMBOLISM ?Deep venous thrombosis (DVT) and pulmonary embolism (PE) occur in patients with multiple myeloma treated with POMALYST (5.3). --------------------------RECENT MAJOR CHANGES----------------------------Dosage and Administration (2.3) 03/14 ---------------------------INDICATIONS AND USAGE----------------------------POMALYST is a thalidomide analogue indicated for patients with multiple myeloma who have received at least two prior therapies including lenalidomide and bortezomib and have demonstrated disease progression on or within 60 days of completion of the last therapy. Approval is based on response rate. Clinical benefit, such as improvement in survival or symptoms, has not been verified. -----------------------DOSAGE AND ADMINISTRATION-----------------------4 mg per day taken orally on Days 1-21 of repeated 28-day cycles until disease progression ----------------------DOSAGE FORMS AND STRENGTHS---------------------Capsules: 1 mg, 2 mg, 3 mg, and 4 mg (3) -------------------------------CONTRAINDICATIONS------------------------------?Pregnancy (4) -----------------------WARNINGS AND PRECAUTIONS----------------------- ? Hematologic Toxicity: Neutropenia was the most frequently reported Grade 3/4 adverse event. Monitor patients for hematologic toxicities, especially neutropenia (5.4). -------------------------------ADVERSE REACTIONS------------------------------Most common adverse reactions (≥30%) included fatigue and asthenia, neutropenia, anemia, constipation, nausea, diarrhea, dyspnea, upper-respiratory tract infections, back pain, and pyrexia (6.1). To report SUSPECTED ADVERSE REACTIONS, contact Celgene Corporation at 1-888-423-5436 or FDA at 1-800-FDA-1088 or https://www.doczj.com/doc/9214035715.html,/medwatch. -------------------------- DRUG INTERACTIONS----------------------?Strong CYP1A2 Inhibitors: Avoid the use of strong CYP1A2 inhibitors unless medically necessary (2.3, 7.1, 12.3). --------------------------USE IN SPECIFIC POPULATIONS---------------------?Nursing Mothers: Discontinue drug or nursing taking into consideration importance of drug to mother (8.3). ?Avoid POMALYST in patients with serum creatinine >3.0 mg/dL (8.7). See 17 for PATIENT COUNSELING INFORMATION and Medication Guide. Revised 03/2014 FULL PRESCRIBING INFORMATION CONTENTS* WARNING: EMBRYO-FETAL TOXICITY AND VENOUS THROMBOEMBOLISM 1 INDICATIONS AND USAGE 1.1 M ultiple Myeloma 2 DOSAGE AND ADMINISTRATION 2.1 M ultiple Myeloma 2.2 Dose Adjustments for Toxicities 2.3 Dose Adjustment for Strong CYP1A2 Inhibitors in the Presence of Strong CYP3A4 and P-gp Inhibitors 3 DOSAGE FORMS AND STRENGTHS 4 CONTRAINDICATIONS Pregnancy 5 WARNINGS AND PRECAUTIONS 5.1 E mbryo-Fetal Toxicity 5.2 POMALYST REMS TM Program 5.3 Venous Thromboembolism 5.4 H ematologic Toxicity 5.5 H ypersensitivity Reactions 5.6 Dizziness and Confusional State 5.7 N europathy 5.8 Risk of Second Primary Malignancies 6 ADVERSE REACTIONS 6.1 Clinical Trials Experience in Multiple Myeloma 7 DRUG INTERACTIONS 7.1 Drugs that May Increase Pomalidomide Plasma Concentrations 7.2 Drugs that May Decrease Pomalidomide Plasma Concentrations 8 USE IN SPECIFIC POPULATIONS 8.1 P regnancy 8.3 N ursing Mothers 8.4 P ediatric Use 8.5 G eriatric Use 8.6 Females of Reproductive Potential and Males 8.7 R enal Impairment 8.8 H epatic Impairment 10 OVERDOSAGE 11 DESCRIPTION 12 CLINICAL PHARMACOLOGY 12.1 Mechanism of Action 12.3 Pharmacokinetics 13 NONCLINICAL TOXICOLOGY 13.1 Carcinogenesis, Mutagenesis, Impairment of Fertility 14 CLINICAL STUDIES 14.1 Multiple Myeloma 15 REFERENCES 16 HOW SUPPLIED/STORAGE AND HANDLING 16.1 How Supplied 16.2 Storage 16.3 Handling and Disposal 17 PATIENT COUNSELING INFORMATION *Sections or subsections omitted from the full prescribing information are not listed.
啊阿埃挨哎唉哀皑癌蔼矮艾碍爱隘鞍氨安俺按暗岸胺案肮昂盎凹敖熬翱袄傲奥懊澳芭捌扒叭吧笆八疤巴拔跋靶把耙坝霸罢爸白柏百摆佰败拜稗斑班搬扳般颁板版扮拌伴瓣半办绊邦帮梆榜膀绑棒磅蚌镑傍谤苞胞包褒剥薄雹保堡饱宝抱报暴豹鲍爆杯碑悲卑北辈背贝钡倍狈备惫焙被奔苯本笨崩绷甭泵蹦迸逼鼻比鄙笔彼碧蓖蔽毕毙毖币庇痹闭敝弊必辟壁臂避陛鞭边编贬扁便变卞辨辩辫遍标彪膘表鳖憋别瘪彬斌濒滨宾摈兵冰柄丙秉饼炳病并玻菠播拨钵波博勃搏铂箔伯帛舶脖膊渤泊驳捕卜哺补埠不布步簿部怖擦猜裁材才财睬踩采彩菜蔡餐参蚕残惭惨灿苍舱仓沧藏操糙槽曹草厕策侧册测层蹭插叉茬茶查碴搽察岔差诧拆柴豺搀掺蝉馋谗缠铲产阐颤昌猖场尝常长偿肠厂敞畅唱倡超抄钞朝嘲潮巢吵炒车扯撤掣彻澈郴臣辰尘晨忱沉陈趁衬撑称城橙成呈乘程惩澄诚承逞骋秤吃痴持匙池迟弛驰耻齿侈尺赤翅斥炽充冲虫崇宠抽酬畴踌稠愁筹仇绸瞅丑臭初出橱厨躇锄雏滁除楚础储矗搐触处揣川穿椽传船喘串疮窗幢床闯创吹炊捶锤垂春椿醇唇淳纯蠢戳绰疵茨磁雌辞慈瓷词此刺赐次聪葱囱匆从丛凑粗醋簇促蹿篡窜摧崔催脆瘁粹淬翠村存寸磋撮搓措挫错搭达答瘩打大呆歹傣戴带殆代贷袋待逮怠耽担丹单郸掸胆旦氮但惮淡诞弹蛋当挡党荡档刀捣蹈倒岛祷导到稻悼道盗德得的蹬灯登等瞪凳邓堤低滴迪敌笛狄涤翟嫡抵底地蒂第帝弟递缔颠掂滇碘点典靛垫电佃甸店惦奠淀殿碉叼雕凋刁掉吊钓调跌爹碟蝶迭谍叠丁盯叮钉顶鼎锭定订丢东冬董懂动栋侗恫冻洞兜抖斗陡豆逗痘都督毒犊独读堵睹赌杜镀肚度渡妒端短锻段断缎堆兑队对墩吨蹲敦顿囤钝盾遁掇哆多夺垛躲朵跺舵剁惰堕蛾
峨鹅俄额讹娥恶厄扼遏鄂饿恩而儿耳尔饵洱二贰发罚筏伐乏阀法珐藩帆番翻樊矾钒繁凡烦反返范贩犯饭泛坊芳方肪房防妨仿访纺放菲非啡飞肥匪诽吠肺废沸费芬酚吩氛分纷坟焚汾粉奋份忿愤粪丰封枫蜂峰锋风疯烽逢冯缝讽奉凤佛否夫敷肤孵扶拂辐幅氟符伏俘服浮涪福袱弗甫抚辅俯釜斧脯腑府腐赴副覆赋复傅付阜父腹负富讣附妇缚咐噶嘎该改概钙盖溉干甘杆柑竿肝赶感秆敢赣冈刚钢缸肛纲岗港杠篙皋高膏羔糕搞镐稿告哥歌搁戈鸽胳疙割革葛格蛤阁隔铬个各给根跟耕更庚羹埂耿梗工攻功恭龚供躬公宫弓巩汞拱贡共钩勾沟苟狗垢构购够辜菇咕箍估沽孤姑鼓古蛊骨谷股故顾固雇刮瓜剐寡挂褂乖拐怪棺关官冠观管馆罐惯灌贯光广逛瑰规圭硅归龟闺轨鬼诡癸桂柜跪贵刽辊滚棍锅郭国果裹过哈骸孩海氦亥害骇酣憨邯韩含涵寒函喊罕翰撼捍旱憾悍焊汗汉夯杭航壕嚎豪毫郝好耗号浩呵喝荷菏核禾和何合盒貉阂河涸赫褐鹤贺嘿黑痕很狠恨哼亨横衡恒轰哄烘虹鸿洪宏弘红喉侯猴吼厚候后呼乎忽瑚壶葫胡蝴狐糊湖弧虎唬护互沪户花哗华猾滑画划化话槐徊怀淮坏欢环桓还缓换患唤痪豢焕涣宦幻荒慌黄磺蝗簧皇凰惶煌晃幌恍谎灰挥辉徽恢蛔回毁悔慧卉惠晦贿秽会烩汇讳诲绘荤昏婚魂浑混豁活伙火获或惑霍货祸击圾基机畸稽积箕肌饥迹激讥鸡姬绩缉吉极棘辑籍集及急疾汲即嫉级挤几脊己蓟技冀季伎祭剂悸济寄寂计记既忌际妓继纪嘉枷夹佳家加荚颊贾甲钾假稼价架驾嫁歼监坚尖笺间煎兼肩艰奸缄茧检柬碱碱拣捡简俭剪减荐槛鉴践贱见键箭件健舰剑饯渐溅涧建僵姜将浆江疆蒋桨奖讲匠酱降蕉椒礁焦胶交郊浇骄娇嚼搅铰矫侥脚狡角饺缴绞剿教酵轿较叫窖揭接皆秸街
阿瑞匹坦产品介绍 (来源:武汉楷伦https://www.doczj.com/doc/9214035715.html,/yuanliaoyao/product_2.html) 英文名称:Aprepitant CAS NO. 170729-80-3 [通用名称] aprepitant,阿瑞吡坦 [化学名称] 5一[[(2R,3S)一2一[(1R)一1一[3,5一二(三氟甲基)苯基]乙氧 基]-3_.(4一氟苯基)4一吗啉基-]甲基]一1,2一二氢一3H一1,2,4-三氮唑一3一酮基[性状] 白色或微白色晶体,不溶于水,微溶于乙腈,可溶于乙醇,相对分子质量为534.43。 注册分类:化学药品第3.1类 药理作用 1,本品是美国FDA于2003年批准上市的第一个神经激肽.1(NK-1)受体阻滞剂,通过与NK一1受体(主要存在于中枢神经系统及其外围)结合来阻滞P物质的作用。本品可以通过血脑屏障,占领大脑中的NK一1受体,具有选择性和高亲和性,而对NK.2和NK-3受体亲和性很低。同时本品对其他用于治疗化疗诱发的恶心和呕吐症状的药物的靶点(如多巴胺受体、5 HT受体)亲和作用也很低,其减少恶心、呕吐的效果优于其他药物。 2,本品在与5一羟色胺3(5一HT )受体阻滞剂和地塞米松合用治疗化疗引起的严重致吐症状的标准方 法中,可以改善化疗诱发的急性及延迟性恶心和呕吐的完全反应率。 3,本品血浆蛋白结合率为95%,稳态时其平均表观分布体积(V )为70 L,且可穿过大鼠和家兔的胎盘以及人的血脑屏障。 4,本品在体内可广泛代谢,主要通过CPY3A4,少部分通过CPY1 A2和CPY2C9进行;其代谢部位主要是结构中的吗啉环和侧链。健康受试者服用300 mg单剂量¨C标记的本品72 h后,在血浆中可检测到24%的放射活性,说明本品在血浆中的确存在代谢物,且至少有7种,但基本无药理作用。, 5,本品主要是通过代谢消除,不通过肾脏排泄,其血浆清除率在62—90 mL·min 范围内,半衰期为9~1 3 h。 适应证 预防化疗引起的急性和延迟性恶心、呕吐。 用法与用量 在化疗前1 h口服125 mg,在d2,3早晨服用80 mg。 药物不良反应 本品可与昂丹司琼、地塞米松合用,具有很好的耐受性。不良反应大多数是轻微或中强度的。在有544例患者参加的耐受性评估试验中,服用本品组中不良反应的发生率为69%,而对照组为68%。常见不良反应有厌食、虚弱、疲劳、便秘、腹泻和恶心呕吐等,发生
考核字库(最新版) 注:1、考核对象:实现业务信息化的医护人员,包括医生、护士、辅助检查人员、药剂员、收费员。 2、每月考核从以下文字中提取。考核时,使用拼音及五笔输入法,取消输入法频率记忆功能,单字录入。 3、如有疑问请咨询电脑室。 椹人芒盆渣椒黛蓉苁田棱梅蓝茨肇伸珀薇磁茜蓄瞿薜芨墨鲜楞瓦戟良威雪脲决蛤猪橘蓟景侧杞赭煅本薷洋沉蔻没稻糯穗豉葵杖虎茱茴智樱节藕行留不滑蔓力蛸螵刺榔槟尖首何断续蚕僵虫姜志远野淡斛实茅杷枇羌珠楝艽秦萆酱败火蒿砂台榆熟延佩杭藿淫肉萸芷款贞女鹤菔莱竺脊狗枣绵豆扁浮丝菟钩筋朴厚桃板部槐蛎牡苈葶欢苍仲杜藜蒺知腹淮鸡寄桑壳土郁赤膝苑紫夷旱半葛北根芦茹竹芍浙菖交夜升芥荆蜕蝉荷薄防蒡公蒲炙附蒌玄纸层千梗桔咽聋耳璃玻烧润癖竭静睾观发旦帕塔夏癣百卤柳菜疮痔麝应党芪楂舌仁苡薏木车泽胸苏鲨芝云镁冬门长胞细取提牛斯冰屈缩湿祛固亭隐扰炔雌戊型然芩肤癥聚苓茯枝母经调搽痒虅莪坤胎元腙色上肾保孕道太前夫乐妇阴柏宫性促绒咳颅鹏杏毛诺啡刹班秋庚赛爽肝间法华哚吲雄非英三的群气用外锰品辅隆核介醛腺状嘌别入吸淋五钱檗净洗炉高药计温体茵碘贝角羚藤梨单肌制眼归当恶嘧酞王穿酐右萘产国鲁孟和岛胰脯组重锌精达稳铋吨哌咪巯磺麦明海雾铵噻瑞伏内螺宝伐滴兰盏灯酒心碳益胍果普泌银仑艾汀司倍胡柴波控吡列格潘二球枯依神桂合酶糜开平痹喉羊异铁亚庆岩坦坎铝糠菊香茶杆芽结凝培回勒中宽术枳泮红肽环蜜天待氢给质电脒硫补珍胃健泊泻谷连拜降熊罗特近乃索溴必莫翘小拉奥联四歧菌猴新已生花栀钾碱菪莨山旋啶他腾泡莲浆韦肟瓜维托喷橼枸栓青匹赖石脱蒙麻伪定可尔福酚酰乙对皮陈胆蛇西那苯来妥比巴清热痰敏黄咖琥炎宁儿腥鱼病去葆仙大油络龙狮酮纳服口马泼醋南星沙氟氧左塑硝方复剂悬混干阿酯榈棕止血活金子碟苦膏贴痛消正奇布迪通丁替雷钙乳嚼咀脂磷卵苄羟物解水白蛋脑嗪川丹芎参丸乌草德奈安曲基氨盐松米塞地溶肠酸芬双酊泰醇露甘粉霉疏胺钴甲厘骨接粒颗烯丙林唑味一独糖萄葡苷皂叶七辛呋康昔瓶软立直液射注灵科因卡多释缓利舒美尼素毒抗风破片散分洛克孢头针钠化氯囊胶伤治患啼掉潮供缔磨梦历褐嘶频併躁脏胁渊而见学黏厌听隔竇睫适声钟霰盈吴臭腋刀蛰腘鳞藓苔责浸勾痣黑麟虱真瘩疙痕瘢稍粃丘秕糟廯纯传秃龟瑰玫项浓费预除髓齿龋浅烫癌携己衣顺态育移疥守临引光停镜残块灼催刮排是局检免难件晚念终无幼害汾唾鉄睡冻蛔速癫阶肪争痳振欲疲遗扩求要进旁加蒶同搏养营为疾幽叉类劲减以级返痉贲御簹抑史蔴低拔迟\偏挑官闷隙側窦昏鹅履卒差点诊成程颤癜触购龈贫峽悸偻佝反汁眠轮冠乏量微痘亢乱紊腮眩呼支深碗碎晕抶各如末粗未舟犬歙落棘冈檫疼响弹存搓受绯植割切踇第压挤等唇眉疗退肋钉跖掌身踝咬查缝贯示拇擦处食突浊运统逆盛炽腑窍滞瘀弱亏两摄收随衰犯牙凉秽冒暑厥阳盗汗虚脘泄鸣咯衄音秘便痨胀证喘哮痿肺嗽崩疳跟劳坐骶腰强柱挛髋躯表痤屑寻器瘙搔荨婴腕髂臂趾床腿背痈脸疖疱瘫路迷规鼓渗聍耵疹萎离晶虹巩症斑变胬翼季假眶溢燥泪形眦轻窒缺疣锐褥度绕脐致横持律迫窘巨死颏面臀剧吐呕兆先殖工划自稽惯习老碍障能功绝年更春过少稀月继原赘烂典阔旧滤壁垂样巧庭痫后置剥早会娩常期粘瘤畸巢峡壶流伞娠妊胱膀撕系纤房转段狭有尿输织蜂足窝囯总染感疽漫弥息征综激易空室憩窄绞作慢围周鞘脾茎包肢增积盂瘘肥肛孔疡溃十阻全完张顿嵌斜沟
泊马度胺对多发性骨髓瘤细胞MM1.S凋亡作用及其对Cereblon 表达的调控研究 目的:探讨泊马度胺对人多发性骨髓瘤细胞株MM1.S的增殖、凋亡作用及其对Cereblon表达的影响,进一步探讨其对糖代谢关键酶及关键蛋白AMPK和 p-AMPK的调控。材料与方法:使用不同终浓度的泊马度胺分别作用于MM1.S细胞24、48、72h时CCK-8法检测MM1.S细胞增殖抑制率,Annexin V-FITC/PI双重染色法检测MM1.S细胞凋亡率;实时定量PCR检测CRBN基因表达水平;Western blot 法检测泊马度胺对MM1.S细胞CRBN蛋白、糖代谢关键蛋白AMPK、p-AMPK表达量的影响;ELISA试剂盒检测丙酮酸激酶、乳酸脱氢酶活性及乳酸含量。结果:1、泊马度胺对MM1.S细胞具有增殖抑制作用,其增殖抑制作用呈时间和剂量依赖性(r=0.981,r=0.990)。 作用72 h时,40和80μmol/L组细胞增殖抑制率P<0.001,差异有统计学意义。2、泊马度胺能够诱导MM1.S细胞凋亡。泊马度胺终浓度分别为0、40和80μmol/L培养干预MM1.S细胞72 h,细胞凋亡率分别为:0.003±0.001,8.333±0.260,10.730±0.210,药物浓度越高,凋亡率越高(r=0.952),差异有统计学意义。 3、泊马度胺终浓度分别为0、20、40和80μmol/L培养干预MM1.S细胞72 h,CRBN基因表达量分别为:1.487±0.34,0.478±0.076,0.211±0.054,0.055±0.005。呈剂量依赖性,随着药物浓度增加,CRBN基因表达量下调(P<0.05),差异有统计学意义。 4、与对照组(即0μmol/L组)相比,泊马度胺药物组(40和80μmol/L组)CRBN蛋白表达明显降低,随着泊马度胺药物浓度的增加CRBN蛋白表达量逐渐降低。
11 泊马度胺(Pomalidomide )是新上市的第三代免疫调节剂(Immuno-modulatory drug ,IMiD ),由美国Celgene 公司研发制成,是在第一代IMiD 沙利度胺化学结构基础上修饰合成的药物,较一代、二代IMiD 而言,泊马度胺相对药理更强、毒性更小且患者耐受度更佳,其良好的抗血管新生、抗肿瘤、抗炎症反应效果已在多发性骨髓瘤(Multiple myeloma ,MM )前期临床研究中得到广泛认可[1],且美国食品和药物管理局(FDA )已于2013年2月批准泊马度胺用于已接受两种及以上药物治疗后疾病仍处于进展状态MM 患者临床治疗。近年来,有学者发现,泊马度胺在骨髓纤维化(Myelofibrosis ,MF )、免疫球蛋白轻链型淀粉样变性(Immunoglobulin light-chain amyloidosis ,AL )、小细胞肺癌(Small cell lung cancer ,SCLC )以及其他晚期实体瘤治疗中亦具有一定效果[2] 。本文综述泊马度胺药理作用及临床应用。 1 泊马度胺药理作用 1.1 药理学作用 泊马度胺分子式为C 13H 11N 3O 4,相对分子质量为273.24441,其化学结构式见图1。 图1 泊马度胺化学结构式 Leleu 等[3]发现,泊马度胺可在阻碍MM 细胞与基质细胞黏附介导微环境相互作用同时,直接下调MM 细胞关键功能,发挥抗骨髓瘤效应,还可通过减少TNF-α、IL-6、IL-8、VEGF 表达水平,降低靶细胞存活率。沈静等[4]发现,MM 患者处于明显免疫监视和免疫反应缺陷状态,而意义未明单克隆丙种球蛋白血症(MGUS )进展至MM 便与这一状态有关:转化浆细胞可逃避CD8+T 细胞识别,损伤抗原递呈过程。体外研究结果表明,泊马度胺可支架刺激T 细胞,诱导以干扰素-γ(IFN-γ)、IL-2为代表Th1型细胞因子分泌,促进肿瘤特异性Th1型反应发生与持续[5]。此外,亦有学者将泊马度胺用于人脐动脉移植内皮细胞芽形成抑制实验,发现泊马度胺较来那度胺效果更佳,且缺氧状态下仅对内皮细胞缺氧诱导因子-1α(HIF-1α)表达产生抑制,不影响HIF-2α表达。在此基础上,泊马度胺上调抑癌基因p21(WAF-1)表达、调节CRNB 基因活性作用,也在诱导MM 细胞周期静止、降低MM 细胞对IMiD 耐药性方面发挥了一定作用[6]。1.2 药代动力学 Shah 等[7]以2 mg/d 泊马度胺应用于8例健康男性受试者,试验结果表明,73%泊马度胺经尿液排泄,15%经粪便排泄,其最大血药浓度为13 ng/mL ,药物浓度-时间曲线下面积(AUC )为189ng ·h/mL ,达峰时间为3.0 h ,终末半衰期分别仅为8.9 h 、11.2 h ,故可在机体循环中迅速得到清除,同时,该药血浆蛋白结合率处于12%~44%范围内,无浓度依赖。另一项研究表明,泊马度胺在机体循环中母体化合物成分占70%以上,且排泄前,药物43%经过细胞色素 P450介导羟化、糖脂化,25%被戊二酰亚胺循环水解, 作者简介:杨胜富,本科,主管药师,研究方向:药物临床,Email:doctor6@https://www.doczj.com/doc/9214035715.html,。 泊马度胺药理作用及临床应用 杨胜富 刘宇 龚汉明 (云南省第一人民医院药学部,昆明 650000) [摘 要] 泊马度胺是一种沙利度胺类似物,可增强T 细胞和自然杀伤细胞介导的免疫反应、抑制单核细胞促炎性细胞因子的生成、诱导肿瘤细胞凋亡,在各类恶性肿瘤、免疫性疾病的治疗中受到广泛关注。该药处于临床早期试验阶段,本文对其药理学机制、药代动力学及临床应用进行综述,以期对泊马度胺下一阶段试验的方向及临床应用提供参考。[关键词] 泊马度胺;免疫调节剂;药理作用;临床应用 中图分类号:R614 文献标识码:A 文章编号:2095-5200(2016)02-011-04 DOI:10.11876/mimt201602004
泊马度胺 项目介绍 南京艾德凯腾生物医药有限责任公司2014年01月13日
一、品种基本情况 1、药品名称 通用名:泊马度胺 英文名:Pomalidomide 英文商品名:Pomalyst 结构式为: 2、药理作用及作用机制 Pomalidomide,一种沙利度胺类似物,是一种有抗肿瘤活性.免疫调节剂。在体外细胞学试验,pomalidomide 抑制造血肿瘤细胞增殖和诱导凋亡。此外,pomalidomide 抑制来那度胺-耐药多发性骨髓瘤细胞株的增殖和在来那度胺-敏感和来那度胺-耐药细胞株与地塞米松协同诱导肿瘤细胞凋亡。Pomalidomide增强T 细胞-和天然杀伤(NK)细胞介导的免疫和抑制单核细胞促炎性细胞因子的生成(如,TNF-α和IL-6)。在小鼠肿瘤模型和和体外脐带模型中Pomalidomide 显示抗血管生成活性。 3、制剂的剂型及规格 本品为胶囊,规格:1 mg,2 mg,3 mg和4 mg。 4、拟用于临床的适应症及用法用量 适应症:POMALYST适用为曾接受至少两种既往治疗包括来那度胺和硼替佐米和已证实 末次治疗完成60天或内疾病进展有多发性骨髓瘤患者的治疗。 用量:重复28天疗程在第1-21天每天口服4 mg直至疾病进展 5、品种概述 Pomalyst片于2013年2月8日通过FDA批准,在美国上市。
二、立题背景 美国食品药品管理局(FDA)2月8日批准Pomalyst (pomalidomide)用于其它癌症药物治疗后病情仍有进展的多发性骨髓瘤患者的治疗。 多发性骨髓瘤起因于骨髓中的浆细胞,属血癌的一种,主要影响老年人有。根据美国国家癌症研究所提供的信息,每年大约有21700名美国人被诊断为多发性骨髓瘤,并且会有10710人死于该种疾病。 Pomalyst通过调节人体免疫系统破坏癌细胞,抑制癌细胞的生长。该药物用于先前至少接受过包括来那度胺和硼替佐米在内的两种药物治疗的患者,,患者已对药物没有响应,并在60天的治疗期内病情仍有发展(复发和难以治疗)。 “Pomalyst是包括来那度胺和沙利度胺在内的第三个免疫调节剂类药物,也是过去一年来第二个被批准用于治疗多发性骨髓瘤的药物,”FDA药物评价和研究中心血液和肿瘤产品办公室主任Richard Pazdur医学博士说。“对于多发性骨髓瘤的治疗要通过调整以满足个体患者的要求,今天Pomalyst的获批给对其它药物不起响应的患者提供了另一种治疗选择。” 2012年7月,FDA批准Kyprolis(carfilzomib)用于治疗多发性骨髓瘤。和Kyprolis情况类似,Pomalyst也是通过FDA加速审评程序而获得批准,这样可以使患者早日用到这个比较有希望的药物,同时公司要进行额外的研究以确保该药物的临床收益和安全使用。另外该药物由于其用途是治疗罕有疾病而获得了孤儿药资格。 Pomalyst的安全性和有效性通过221名复发或难治性多发性骨髓瘤患者参与的临床试验进行评价。临床试验的目的是检测使用该药物治疗之后(目标反应率,或ORR),癌症完全或部分消失的患者数量。 结果显示,单纯使用Pomalyst治疗的患者目标反应率为7.4%。但患者对该药物的持续响应时间仍未达到中位值。Pomalyst加低剂量地塞米松治疗的患者目标反应率为29.2%,平均响应时间为7.4个月。 Pomalyst、来那度胺和沙利度胺均由新泽西州Summit的塞尔基因公司上市销售,Kyprolis 由加利福尼亚州南旧金山的奥尼克斯制药公司上市销售。 该药在国内2017年化合物专利到期,晶型专利2024年到期。目前,原研CEL GENE公 司还没有申请该品种的进口,江苏豪森医药已于2013年8月申报3.1类。