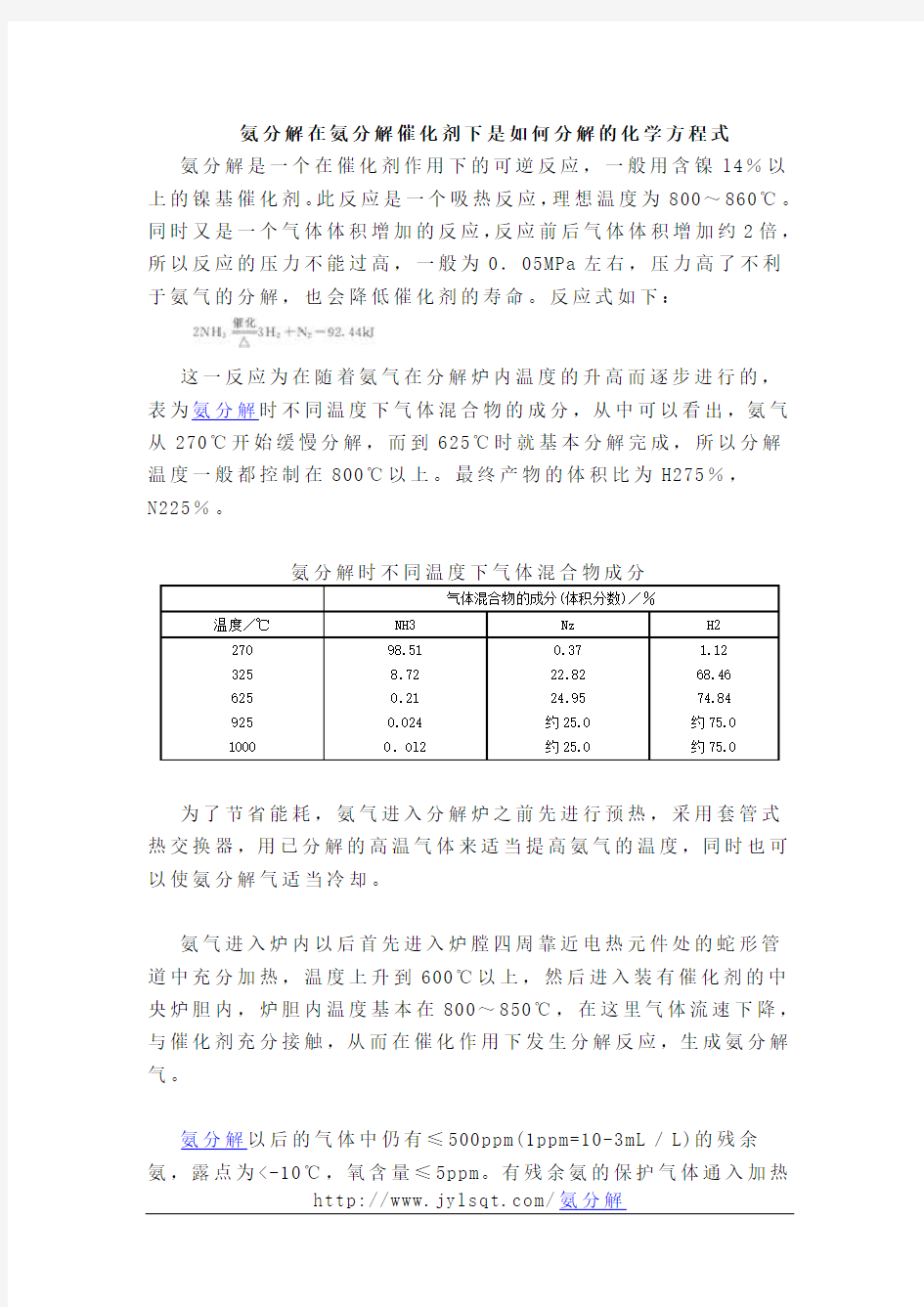

氨分解在氨分解催化剂下是如何分解的化学方程式氨分解是一个在催化剂作用下的可逆反应,一般用含镍l4%以上的镍基催化剂。此反应是一个吸热反应,理想温度为800~860℃。同时又是一个气体体积增加的反应,反应前后气体体积增加约2倍,所以反应的压力不能过高,一般为0.05MPa左右,压力高了不利于氨气的分解,也会降低催化剂的寿命。反应式
如下:
这一反应为在随着氨气在分解炉内温度的升高而逐步进行的,表为氨分解时不同温度下气体混合物的成分,从中可以看出,氨气从270℃开始缓慢分解,而到625℃时就基本分解完成,所以分解温度一般都控制在800℃以上。最终产物的体积比为H275%,
N225%。
氨分解时不同温度下气体混合物成分
气体混合物的成分(体积分数)/%
温度/℃NH3Nz H2
270 325 625 925 1000
98.51
8.72
0.21
0.024
0.Ol2
0.37
22.82
24.95
约25.0
约25.0
1.12
68.46
74.84
约75.0
约75.0
为了节省能耗,氨气进入分解炉之前先进行预热,采用套管式热交换器,用已分解的高温气体来适当提高氨气的温度,同时也可以使氨分解气适当冷却。
氨气进入炉内以后首先进入炉膛四周靠近电热元件处的蛇形管道中充分加热,温度上升到600℃以上,然后进入装有催化剂的中央炉胆内,炉胆内温度基本在800~850℃,在这里气体流速下降,与催化剂充分接触,从而在催化作用下发生分解反应,生成氨分解气。
氨分解以后的气体中仍有≤500ppm(1ppm=10-3mL/L)的残余
氨,露点为<-10℃,氧含量≤5ppm。有残余氨的保护气体通入加热
炉,受热后又会分解,产生微量的原子氮,使辐射管等炉内钢件设
施产生渗氮现象而变脆、开裂,影响设施寿命和产品质量。而且露
点也不符合要求,所以氨分解气必须经纯化后才能使用。
本文由:攻防后备军团编辑https://www.doczj.com/doc/848110975.html,/
2011-6-25
课题2催化剂对过氧化氢分解反应速率的影响 1.完成下列各题空格 ⑴分子或离子间的是发生化学反应的先决条件,但不是每次碰撞都会引发反应。能够引起反应的分子(或离子)间的相互碰撞叫做,能够发生有效碰撞的分子叫做。活化分子具有的能量,因此活化分子所占分数的大小决定的快慢。活化分子的平均能量与所有分子的平均能量的差称为。 ⑵催化剂能使反应的活化能(如图Ea、Ea’分别代表有、无催化剂时正反应的活化能),使得具有平均能量的反应物分子只要吸收较少的能量就能变成,活化分子所占分数增大,可以成千上万倍地加快反应速率。催化剂能增大化学反应速率,但是它改变反应进行的方向,也使那些不可能发生的化学反应得以发生。 ⑶影响过氧化氢分解的因素有溶液的、光、热及遇到大多数。 ⑷分解反应的化学方程式为。 ⑸催化剂对化学反应速率的影响 一般选用MnO2作催化剂,其以及均会影响H2O2分解的速率。通过观察比较H2O2溶液中的快慢程度,或测定H2O2分解放出的O2的体积判断H2O2分解速率的大小。 ⑹保存H2O2溶液时要注意:从安全角度考虑,易分解产生气体的试剂不宜放在密封的中,双氧水通常盛放在干净的中。 2.下列关于催化剂的说法,正确的是() A.催化剂能使不起反应的物质发生反应 B.催化剂在化学反应前后,化学性质和质量都不变 C.催化剂不能改变化学反应速率 D.任何化学反应都需要催化剂 3.能够增加反应物分子中活化分子百分数的是() A.升高温度 B.减小压强 C.增大压强 D.增大浓度 4.亚氯酸盐(如NaClO2)可用作漂白剂,在常温下不见光时可保存一年,但在酸性溶液中因生成亚氯酸而发生分解:5HClO2===4ClO2↑+H++Cl-+2H2O。分解时,刚加入硫酸,反应缓慢,随后突然反应释放出大量ClO,这是因为()
中国工业催化剂分类方法 一.石油炼制催化剂 1.催化裂化催化剂 2.催化重整催化剂 3.加氢裂化催化剂 4.加氢精制催化剂 5.烷基化催化剂 6.异构催化剂 二.无机催化剂 1.脱硫——加氢脱硫、硫回收催化剂 2.转化——天然气转化、炼厂气转化、轻油转化催化剂3.变换——高(中)变、低变、耐硫宽变催化剂 4.甲烷化——合成气甲烷化、城市燃气甲烷化 5.氨合成催化剂 6.氨分解催化剂 7.正、仲氢转化催化剂 8.硫酸制造催化剂 9.硝酸制造催化剂 10.硫回收催化剂 三.有机化工催化剂 1.加氢催化剂 2.脱氢催化剂 3.氧化——气相、液相催化剂 4.氨氧化催化剂 5.氧氯化催化剂 6.CO+H2合成——合成醇、F-T合成催化剂 7.酸催化——水合、脱水、烷基化催化剂 8.烯烃反应——齐聚、聚合、岐化、加成催化剂 四.环境保护催化剂 1.硝酸尾气处理催化剂 2.内燃机排气处理催化剂 3.制氮催化剂 4.纯化——脱痕量氧或氢催化剂 五.其它催化剂 其它催化剂 中国工业催化剂常规分类Classification industrial Catalysts 一、化肥催化剂(Catalysts for fertilizer manufacture) 一)脱毒剂(Purification agent)
1.活性炭脱硫剂(Active carbon desulfurizer) 2.加氢转化脱硫催化剂(Hydrodesulfurization Catalyst) 3.氧化锌脱硫剂(Zinc oxide sulfur absorbent) 4.脱氯剂(Dechlorinate agent) 5.转化吸收脱硫剂(Converted-absoubed desulfurizer) a.氧化铁脱硫剂(Iron ozide desulfurizer) b.铁锰脱硫剂(Iron-Nanganese oxide desulfurizer) c.羰基硫水解催化剂(Carbonyl Sulfide hydrolysis) 6.脱氧剂(Deoxidezer) 7.脱砷剂(Hydrodearsenic Catalyst) 二)转化催化剂(Reforming Catalyst) 1.天然气一段转化催化剂(Nature gas primary reforming catalyst) 2.二段转化催化剂(Secondary reforming catalyst) 3.炼厂气转化催化剂(Refinery gas steam reforming catalyst) 4.轻油转化催化剂(Naphtha steam reforming catalyst) 三)变换催化剂(CO shift catalyst) 1.中温变换催化剂(High temperature CO shift catalyst) 2.低温变换催化剂(Low temperature CO shift catalyst) 3.宽温耐硫变换催化剂(Sulfur tolerant shift catalyst) 四)甲烷化催化剂(Methanation catalyst) 1.甲烷化催化剂(Methanation Catalyst) 2.城市煤气甲烷化催化剂(Town gas methanation Catalyst) 五)氨合成催化剂(Ammonia synthesis Catayst) 1.氨合成催化剂(Ammonia synthesis catalyst) 2.低温氨合成催化剂(Low temperatuer ammonia synthesis catalyst) 3.氨分解催化剂(Ammonia decomposition catalyst) 六)甲醇催化剂(Methanol Catalyst) 1.高压甲醇合成催化剂(High pressure methanol synthesis catalyst) 2.联醇催化剂(Combined methanol synthesis catalyst) 3.低压甲醇合成催化剂(Low pressure methanol synthesis catalyst) 4.燃料甲醇合成催化剂(Fuel methanol synthesis catalyst) 5.低碳混合醇合成催化剂(mixture of lower alcohols synthesis catalyst) 七)制酸催化剂(Acid manufacture catalyst) 1.硫酸生产用钒催化剂(Vanudium catalyst for manufacture of sulfuric acid)2.硝酸生产用铂网催化剂(Platinum ganze catalyst for manufacture 3.非铂氨氧化催化剂(Non-platinum catalyst for ammonia oxidation)4.铂捕集网(platinum catch gamze) 5.硝酸尾气处理催化剂(Treated catalyst for tail gas from nitric acid plant)八)制氮催化剂(Nitrogen manufacture catalyst) 1.一段制氮催化剂(Frist stage catalyst for ammonia combined) 2.二段制氮催化剂(Second stage catalyst for nitrogen manufacture)
过氧化氢分解制氧气不同催化剂的探究 过氧化氢通常被保存在棕色瓶中以避开光照,原因是过氧化氢会自发地(缓慢地)分解成氧气和水。当有二氧化锰催化剂存在时,该分解过程大大加快。除二氧化锰外哪些物质还可以催化分解过氧化氢? 【思考与设计】请你设计实验方案探究 1. 不同催化剂对过氧化氢分解反应速率的影响 2. 同一催化剂存在下,过氧化氢的浓度对分解速率的影响。写出实验的各个步骤和应 注意的安全事项,写一份详细的实验计划。 请老师批准你的实验方案,按计划完成实验并记录实验现象和数据。 【实验材料】锥型瓶、分液漏斗、带刻度的玻璃量气管(或碱式滴定管)、玻璃三通、乳胶 头、导管、秒表、30%的过氧化氢、二氧化锰、0.2mol ·L -1 CuSO 4溶液、0.2mol ·L -1FeSO 4溶液、碘水、肥皂水(或洗发香波) 【实验案例】 1.不同催化剂对过氧化氢分解反应速率的影响 ● 把30%过氧化氢稀释成2%、4%、6%过 氧化氢溶液。 ● 按图综2-2连接装置来测量氧气生成 的体积。 ● 把肥皂水装满玻璃三通,在锥型瓶中加 入催化剂,从分液漏斗向锥型瓶中加入20mL 过氧化氢溶液。 ● 用乳胶头来制造肥皂泡,用秒表测量生 成固定体积(例如20mL )氧气所需要的时间,平均反应速率可以用单位时间内所产生的氧气体积来表示。认真观察实验现象并记录数据。 不同催化剂对同一浓度过氧化氢分解实验的对比表 编号 实 验 实验现象 时间 反应速率 1 20ml 4% 的双氧水+0.1克二氧化锰 2 20ml 4% 的双氧水+1mL 0.2mol ·L -1 CuSO 4溶液 3 20ml 4% 的双氧水+1mL 0.2mol ·L -1 FeSO 4溶液 4 20ml 4% 的双氧水+1mL 碘水 结论 图综2-2过氧化氢分解制氧气不同催化剂的探究
氮化物作为催化剂的研究进展 内容摘要:近年来,被誉为“准铂催化剂”的过渡金属氮化物因其优良的催化活性已受到世界各国学者的广泛关注。大量的研究表明,过渡金属氮化物在氨的合成与分解、加氢精制等许多涉氢反应中都表现出良好的催化活性。过渡金属氮化物的制备方法有高温法和程序升温氮化法, 程序升温氮化法的显著优点是可以制备出高比表面积的金属氮化物。研究人员不仅对金属氮化物催化剂的制备方法进行了大量的研究,并且发现负载型金属氮化物具有负载量低、比表面积大等优点。因此, 金属氮化物的负载化研究正成为目前的研究热点。 关键词:过渡金属、氮化物、催化剂、结构、性能、工业 Nitride as a catalyst research progress Grade: grade 09 Applied Chemistry Specialty Name: Hong Huaiyong number: 122572009003 Abstract:In recent years, known as the" Platinum" transition metal nitride because of its excellent catalytic activity has been subjected to extensive concern of scholars all over the world. A large number of studies show that, transition metal nitride in ammonia synthesis and decomposition, hydrogenation and so many wading hydrogen reaction showed good catalytic activity. Preparation of transition metal nitride has high temperature method and temperature-programmed nitridation, temperature-programmed nitridation method has the advantages of preparation of high specific surface area of the metal nitride. The researchers not only on the metal nitride catalyst preparation method was studied, and found that the load type metal nitride having load low, large specific surface area and other advantages. Therefore, a metal nitride load research is becoming the research hotspot at present. Key word:Transition metal, nitride, catalyst, structure, performance, industry 引言 过渡金属氮化物是元素N插入到过渡金属晶格中所生成的一类金属间充型化合物,它兼具有共价化合物、离子晶体和过渡金属三种物质的性质,从而表现出优良的物理和化学性能。它作为一类具有很高硬度、良好热稳定性和抗腐蚀特性的新型功能材料,已经在各种耐高温、耐磨擦和耐化学腐蚀分机械领域得到应用。而且它在氨合成与分解、加氢脱硫/脱氮(HDS/HDN)、F-T合成等许多涉氢反应都具有优良的催化活性,不逊色于Pt和Rh等贵金属催化剂的性能,被誉为“准铂催化荆”。过渡金属氮化物作为一种有应用前景的新型加氢精制催化剂已引起人们的广泛关注,成为国际催化荆新材料领域的研究热点。本章概述了这一催化新材料的最新研究进展。 1.过渡金属氮化物的结构和电子特征 过渡金属氮化物是一种间充化合物,是由于氮原子填隙似的融进过渡金属的晶格中形成的,它们倾向于形成组成可在一定范围内变动的非计量间隙化合物。其固态化学特征类似于纯金属,具有简单的晶体结构特征。其中的金属原子形成
过氧化氢分解氧气 成员:罗玉洁、何瑾、徐丽、胡艳、骆磊、申林 一、 实验目的 1、掌握实验室用双氧水制备氧气的原理、装置和操作。 2、了解影响双氧水制备氧气反应速率的因素。 3、能认识催化剂在化学反应中的作用及化学反应前后质量的变化。 二、 实验原理 过氧化氢不稳定,在常温下就能缓慢分解放出氧气。但速度较慢,不易察觉。在过氧化氢溶液中加入适量二氧化锰后,能立即有氧气迅速放出。在此反应中,二氧化锰是催化剂,能加速该反应的发生。 过氧化氢 水+氧气→ 二氧化锰 ↑+??→?2222O O H O H 2MnO 三、 实验药品与仪器 实验药品:5%、30%的双氧水、二氧化锰、氧化铜。 仪 器:注射器(20ml )、锥形瓶、导管、软木塞、恒温水浴锅、 集气瓶、橡皮管、钥匙。 四、 实验步骤 1、实验室制备氧气 ①连接仪器,检查装置的气密性; ②在锥形瓶中加入少量二氧化锰粉末,旋紧软木塞,用注射器在双氧水瓶里吸取10ml 5%双氧水,将注水器里的双氧水按需要的量缓慢注入加入装有少量二氧化锰粉末的锥形瓶中; ③等气泡连续均匀冒出时,开始收集; ④等集气瓶中液面下降至瓶口,瓶外有气泡产生时,实验结束。并用带火星的木条进行检验。实验装置如下:
改进装置原因: (1)因锥形瓶中的二氧化锰不易收集。所以将锥形瓶换成试管,便于收集二氧化锰,好做称量,证明二氧化锰作为一种催化 剂时,在反应前后质量不变。 (2)用分液漏斗来控制反应的速率,收集装置采用向下排水法。 (3)通过改变浓度、温度、催化剂来探究对双氧水催化分解氧气速率的影响。 2、探究影响双氧水分解速率的因素 (1)浓度对反应的影响 分别将10ml 5%双氧水溶液与10ml 30%双氧水溶液与等量的MnO2混合于试管中,分别观察实验现象。 (2)温度对反应的影响 分别观察:室温下10ml 30%双氧水溶液,发生装置浸入80℃的水浴加热的10ml 30%双氧水的现象。 (3)催化剂对反应的影响 10mL5%双氧水溶液加入少许氧化铜作为催化剂,10 ml 5%双氧水溶液加入少许二氧化锰作为催化剂。且氧化铜与二氧化锰等量,分别观察实验现象。 五、注意事项 1、在做实验之前,必须检查装置的气密性。气密性检查:用止水夹 关闭,打开分液漏斗活塞,向漏斗中加入水,水面不持续下降,就说明气密性良好。 2、双氧水的浓度不能过大,并且不适宜加多过氧化锰,容易造成反 应太剧烈。 3、刚开始出现气泡时,混有空气,此时不易收集氧气,待气泡增多 时,再进行收集。 六、思考题 1、实验中分液漏斗的作用? 2、二氧化锰在实验中的作用? 3、与高锰酸钾相比,双氧水分解制取氧气有哪些优点? 答:1、分液漏斗可以控制反应物的量,从而控制反应的速率。 2、二氧化锰在该反应中做催化剂,能改变反应的速率,而本身 在反应前后质量和化学性质不变,对于生成物的量是没有影响 的。 3、双氧水分解不需要加热,操作简单方便,且可以通过分液漏 斗控制反应物的量,从而控制反应的速率。
存檔日期:存檔編號: 北京化工大學 研究生課程論文 課程名稱:_____________ 課程代號:_____________ 任課教師:_____________ 完成日期:____年___月___日 專業:_____________ 學號:_____________ 姓名:_____________ 成績:_____________
提高中光催化水分解光催化材料效率的半導體異質結型催化劑CaFe2O4–PbBi2Nb1.9W0.1O9設計 一、設想的描述 1、光催化水分解的目的及應用價值。 氫能已被普遍認為是一種理想、無污染的綠色能源,其燃燒值高且燃燒後唯一的產物是水,對環境不會造成任何污染,因此,氫能開發是解決能源危機和環境問題的理想途徑。在眾多氫能開發的手段和途徑中,通過光催化劑,利用太陽能光催化分解水制氫是最為理想和最有前途的手段之一;而開發高效、廉價的實用光催化劑是實現這一過程的關鍵,也成為當前國際能源材料領域的研究熱點之一。 2、光催化分解水反應機理 像其他的催化反應一樣,光催化水的分解開始當一個半導體催化劑開始吸收比它的帶隙能量強的光子。這些吸收使得處於導帶的電子被激發並且在半導體的價電子帶產生了空穴就像圖1展示的那樣。[1]光電子和空穴氧化和還原水,產生了2:1混合著的氫氣和氧氣通過以下的反應。 氧化反應:H2O + 2h+→2H+ + 1/2O2(1) 還原反應:2H+ + 2e?→H2 (2) 總的反應方程式:H2O →H2 + 1/2O2 (3) 總的反應方程包括四個電子轉移(每生成摩爾氧氣)通常是通過金屬和金屬氧化物助催化劑(在圖中用cat1和cat2表示)附著在半導體表面。這些助催化劑為催化反應提供電子和反應的活性中心。[2]這個反應包括標準Gibbs自由能變化△G=237KJ/mol(1.23eV每轉移一個電子)。實際上,一些超電勢可以加速
冶金工程氨分解气氛制备原理及流程 1.制备原理 将无水氨加热到800~900t°,在催化剂的作用下,很容易分解SH2+N2的气体。其性质为还原性和脱碳性的。 用氨制备的气氛可分为加热分解气氛(吸热式)和燃烧气氛(放热式)两类。燃烧气氛又可分为完全燃烧的和不完全燃烧的两种。 氨分解气氛反应是可逆的,升高温度或降低压力将有利于反应向氨分解方向进行。在600~700t:时氨的分解率达99.88%-99.9596,但分解较缓慢。为了提高反应速度,可采用镍材料(废镍铬电热材料等)做催化剂。 氨分解气氛的制备流程 原料气自氨瓶流入气化器受热气化,在反应罐中借助高温和催化剂的作用进行分解,分解产物自反应罐出来后再返回气化器,利用其余热加热液态氨。冷却后的分解产物经净化,除去残氨和水气,就得到可供使用的分解氨 炉膛密封形式主要有炉体密封和炉罐密封两类。炉体密封,包括炉壳、炉门、电热元件引出孔、热电偶孔、风扇轴孔和推料机械伸出炉外的孔洞等处的密封。电热元件等在可控气氛作用下,需采用抗渗碳性强的材料或加抗渗碳涂料,最好用低压供电,以免元件渗碳或炉壁积碳使元件发生短路而毁坏。中国冶金行业网 采用炉罐(金属或陶瓷罐)隔离密封,密封效果比较好,但会降低传热效果和增加炉罐材料消耗,炉子工作温度也受到限制。还有一种密封形式兼有上述两类密封的特点,即除炉膛密封外,采用辐射管加热器,可防止炉气侵蚀元件和火焰破坏炉内气氛。 放热式可控气氛的原料气可以是液化石油气、煤气或其它气体燃料。原料气与小于理论需要量的空气进行燃烧,部分原料气完全燃烧,部分原料气不完全燃烧。 放热式可控气氛的成分随所用空气过剩系数的大小而不同,可在很宽的范围内变动。气氛氧化性和脱碳性较弱,但产气量也较少氧化性和脱碳性也较强,但产气量较大,成本较低。为提高气氛还原性,常再经净化处理。通过改变空气与燃料的比和净化方法,可在较宽的范围内改变气氛的成分和性质,得到含量不同的气氛,一般又把这类气氛分为淡型、浓型和净化型。这类气氛可能是还原性和增碳性的,也可能是氧化性和脱碳性的,视气氛成分、工件含碳量和工作温度而定。
过氧化氢的催化分解 一、实验目的 1、了解不同催化剂对过氧化氢(H2O2)催化分解速率的影响。 2、认知能催化分解H2O2的不同催化剂。 二、实验原理 过氧化氢催化分解是一级反应:H2O2→H2O+1/2O2.。(凡是反应速度只与反应浓度的一次方成正比的反应称为一级反应。)实验证明,过氧化氢的反应机理为一级反应.化学反应速度取决于反应物的浓度、温度、反应压力、催化剂、搅拌速度等许多因素。许多催化剂如Pt、Ag、Cr、MnO2、FeCl3、CuO、血液、铁丝、炭粉、土豆丝等都能加速H2O2分解。用土豆丝来催化分解H2O2溶液,说明生物体内不断产生的过氧化氢酶,可促使H2O2迅速分解,这种酶广泛存在于动植物组织中。 三、实验仪器与药品 仪器:试管(2个)、具支试管(1个)、锈铁丝、气球、土豆丝、 药品:H2O2溶液, 四、实验步骤 1,过氧化氢溶液的制备 用移液管吸取30℅H2O2溶液5ml,置于50ml容量瓶中,稀释至刻度线,摇匀定容,即得实验用的H2O2溶液。 2,酶催化作用的验证实验 取两只试管,在一支试管中放入切成细条状的土豆丝。分别向两支试管中注入3%的H2O2 5ml,注意观察现象(放入土豆丝的试管中迅速产生大量的气泡,泡沫很快充满试管;用玻璃棒桶开泡沫,)插入带火星的木条,则木条立即复燃,而另一支试管中无明显现象。 3,用抽动法做“催化剂对H2O2分解速度的影响”的实验 ①取一支具支试管,在具支试管中加入10ml浓度30%H2O2溶液,在支管上装上小气球,通过橡皮塞插入一根已生锈的绕成螺旋状的粗铁丝。 ②将螺旋状的锈铁丝向下插入H2O2溶液中是,注意观察现象的变化。(H2O2迅速分解,锈铁丝表面上,有大量气泡产生。气球鼓起;把铁丝向上拉,离开H2O2溶液,则反应不明显。) ③取下塞子,用带火星木条放在试管口,注意观察现象变化。(则木条立即复燃,说明有O2生成。) 五、注意事项 1、实验过程中注意安全 2、玻璃仪器轻拿轻放 六、思考题 1,催化剂对反应速度有何影响? 2,常用催化剂有哪些?
氨分解在氨分解催化剂下是如何分解的化学方程式氨分解是一个在催化剂作用下的可逆反应,一般用含镍l4%以上的镍基催化剂。此反应是一个吸热反应,理想温度为800~860℃。同时又是一个气体体积增加的反应,反应前后气体体积增加约2倍,所以反应的压力不能过高,一般为0.05MPa左右,压力高了不利于氨气的分解,也会降低催化剂的寿命。反应式 如下: 这一反应为在随着氨气在分解炉内温度的升高而逐步进行的,表为氨分解时不同温度下气体混合物的成分,从中可以看出,氨气从270℃开始缓慢分解,而到625℃时就基本分解完成,所以分解温度一般都控制在800℃以上。最终产物的体积比为H275%, N225%。 氨分解时不同温度下气体混合物成分 气体混合物的成分(体积分数)/% 温度/℃NH3Nz H2 270 325 625 925 1000 98.51 8.72 0.21 0.024 0.Ol2 0.37 22.82 24.95 约25.0 约25.0 1.12 68.46 74.84 约75.0 约75.0 为了节省能耗,氨气进入分解炉之前先进行预热,采用套管式热交换器,用已分解的高温气体来适当提高氨气的温度,同时也可以使氨分解气适当冷却。 氨气进入炉内以后首先进入炉膛四周靠近电热元件处的蛇形管道中充分加热,温度上升到600℃以上,然后进入装有催化剂的中央炉胆内,炉胆内温度基本在800~850℃,在这里气体流速下降,与催化剂充分接触,从而在催化作用下发生分解反应,生成氨分解气。 氨分解以后的气体中仍有≤500ppm(1ppm=10-3mL/L)的残余 氨,露点为<-10℃,氧含量≤5ppm。有残余氨的保护气体通入加热
催化剂-应用分析 人们利用催化剂,可以提高化学反应的速度,这被称为催化反应。大多数催化剂都只能加速某一种化学反应,或者某一类化学反应,而不能被用来加速所有的化学反应。催化剂并不会在化学反应中被消耗掉。不管是反应前还是反应后,它们都能够从反应物中被分离出来。不过,它们有可能会在反应的某一个阶段中被消耗,然后在整个反应结束之前又重新产生。 使化学反应加快的催化剂,叫做正催化剂;使化学反应减慢的催化剂,叫做负催化剂。例如,酯和多糖的水解,常用无机酸作正催化剂;二氧化硫氧化为三氧化硫,常用五氧化二钒作正催化剂,这种催化剂是固体,反应物为气体,形成多相的催化作用,因此,五氧化二钒也叫做触媒或接触剂; 催化剂 食用油脂里加入0.01%~0.02%没食子酸正丙酯,就可以有效地防止酸败,在这里,没食子酸正丙酯是一种负催化剂(也叫做缓化剂或抑制剂)。 目前,对催化剂的作用还没有完全弄清楚。在大多数情况下,人们认为催化剂本身和反应物一起参加了化学反应,降低了反应所需要的活化能。有些催化反应是由于形成了很容易分解的“中间产物”,分解时催化剂恢复了原来的化学组成,原反应物就变成了生成物。有些催化反应是由于吸附作用,吸附作用仅能在催化剂表面最活泼的区域(叫做活性中心)进行。活性中心的区域越大或越多,催化剂的活性就越强。反应物里如有杂质,可能使催化剂的活性减弱或失去,这种现象叫做催化剂的中毒。 催化剂对化学反应速率的影响非常大,有的催化剂可以使化学反应速率加快到几百万倍以上。催化剂一般具有选择性,它仅能使某一反应或某一类型的反应加速进行。例如,加热时,甲酸发生分解反应,一半进行脱水,一半进行脱氢: HCOOH=H2O+COHCOOH=H2+CO2 如果用固体Al2O3作催化剂,则只有脱水反应发生;如果用固体ZnO作催化剂,则脱氢反应单独进行。这种现象说明,不同性质的催化剂只能各自加速特定类型的化学反应过程。因此,我们利用催化剂的选择性,可使化学反应主要向某一方向进行。 在催化反应里,人们往往加入催化剂以外的另一物质,以增强催化剂的催化作用,这种物质叫做助催化剂。助催化剂在化学工业上极为重要。例如,在合成氨的铁催化剂里加入少量的铝和钾的氧化物作为助催化剂,可以大大提高催化剂的催化作用。 催化剂在现代化学工业中占有极其重要的地位,现在几乎有半数以上的化工产品,在生产过程里都采用催化剂。例如,合成氨生产采用铁催化剂,硫酸生产采用钒催化剂,乙烯的聚合以及用丁二烯制橡胶等三大合成材料的生产中,都采用不同的催化剂。 酶,是植物、动物和微生物产生的具有催化能力的蛋白质,旧称酵素。生物体的化学反应几乎都在酶的催化作用下进行。酶的催化作用同样具有选择性。例如,淀粉酶催化淀粉水解为糊精和麦芽糖,蛋白酶催化蛋白质水解成肽等。酶在生理学、医学、农业、工业等方面,都有重大意义。目前,酶制剂的应用日益广泛。无论是在初学化学还是在高中化学中,都涉及催化剂问题,许多化学反应都需要催化剂,催化剂不仅是化学的一个十分重要的概念和知识点,目前现代化学工业也正在朝着材料和能源方向发展,这就决定了化学催化剂的作用越来越大,比如工业合成氨是在高温、高压、铁触媒催化条件下进行的,而生物固氮是在常温常压下进行的,有机和生化反应中应用催化剂的更多。目前催化剂已经成为一门学科。因此教学中帮助学生准确把握和理解这个概念是非常重要的。不仅如此,还要运用好这个知识点,培养学生科技创新意识、研究探究能力。 对于催化剂的概念,不同的教材版本有不同的描述,人教版的定义是:在化学反应前后能改变化学反应的速率,但本身的化学性质和物理性质都没有改变的物质,叫这个反应的催化剂。现在沪教版的定义把人教版定义中的“改变”换成“加快”,为此还颇有一番争议。 初中化学课程标准中的要求是:认识催化剂的重要作用。初中学生刚接触化学,只要求简单认识了解一些简单常见的化学现象、常见元素及其物质的性质、用途、实验室制备等方面知识,从新课程标准出发,笔者认为对这个概念的基本要求是:通过实验,让学生自然形成催化剂的概念,在此基础上进一步了解催化剂的应用,而不能引申和拔高。以前使用的人教版的教材是通过氯酸钾受热分解制取氧气的实验引出催化剂概念的。不妨用三个实验对比来说明问题: 实验一:把少量的二氧化锰和氯酸钾混合物放在试管里加热片刻,用带余烬的木条插入管口,木条复燃,说明有氧气产生。 实验二:把少量氯酸钾放在试管里加热片刻,用带余烬的木条插入管口,木条不燃,说明没氧气产生。在加热几分钟,看到氯酸钾融化,有少量气泡,用带余烬的木条插入管口,木条复燃,说明有氧气产生。 实验三:把少量的二氧化锰放在试管里加热片刻,用带余烬的木条插入管口,木条没有复燃,说明没有氧气产生。 以上三个实验说明二氧化锰具有使氯酸钾在较低温度下迅速反应放出氧气的本领。从而引出催化剂的概念:这种在化学反应里能改变其他物质的反应速率,而本身的性质在放入前后都没有变化的物质叫催化剂。沪教版教材在讲催化剂概念时,改用二氧化锰催化双氧水溶液分解来制取氧气的实验,原因是:一是对二氧化锰是不是氯酸钾分解反应的催化剂人们还有争议,因为反应中生成有红色物质;二是二氧化锰催化分解双氧水的反应环保,现象明显。 笔者也曾在初中化学课教学课堂上通过实验、对比、观察、分析、总结、归纳,引出催化剂的概念,但必须把握准确定义要点,就是“改变”或“加快”其他物质的反应速度而自身的质量和性质都没有改变。因为学生是初次认知此概念,笔者认为用“加快”更直观些。课堂上学生会问为什么,我当时用了一个简单的比喻:俗话说无中间人事不成,就像人介绍对象,经媒婆三言两语成了,媒婆有特殊的本能或者说话技巧,至于哪些物质可以做催化剂,它们又是怎样促进反应的,留待以后我们深入学习,有兴趣的同学可以查查资料,老师帮你解决。 在高中教学实践中,在做分组实验时笔者把学生分成五个组:一组做[实验1]和[实验2],二组做
纳米科技 Nanoscience &Nanot echnology No.1 February 2010 第7卷第1期2010年2月 收稿日期:2009-11-16 *基金项目:国家重点基础研究发展规划“973”项目(2005CB221400),国家自然科学基金项目(20473063和20590364) 乙二醇还原Ru/CNTs 的制备及 催化氨分解性能研究* 武小满1,李学峰1,张鸿斌2 (1.许昌学院化学化工学院,河南 许昌 461000) (2.厦门大学化学化工学院固体表面物理化学国家重点实验室,福建厦门 361005) 摘 要:为获得高分散的Ru 负载催化剂,采用乙二醇液相化学还原沉积法制备Ru/CNTs ,TEM 、 XRD 、H 2-TPD 表征,结果表明,乙二醇液相还原法可以制备金属粒径小(2-4nm)而均匀的高分散度的钌修饰CNTs ,其表面存在较高稳态浓度吸附氢。以氨分解制氢作探针反应,实验结果表明,在相同反应条件下,经乙二醇油浴液相还原沉积制备的Ru/CNTs 催化剂上氨转化率约为浸渍法制得相应催化剂上的1.6倍,同时发现钌微晶粒径在3-4nm 范围的Ru/CNTs 对氨分解制氢的催化性能最佳,钌微晶粒径≤2nm 时氨分解转化率明显下降。关键词:钌/碳纳米管;液相化学还原沉积;氨分解制氢 Preparation of Ru/CNTs Nano-material by Polyol Reduction-deposition Method and its Catalytical Performance for Ammonia Decomposition WU Xiao-Man 1,LI Xue-Feng 1,ZHANG Hong-Bin 2 (1.School of Chemistry and Chemical Engineering ,Xuchang University ,Xuchang 461000,China) (2.State Key Laboratory for Physical Chemistry of Solid Surfaces ,College of Chemistry and Chemical Engineering ,Xiamen University ,Xiamen 361005,China) Abstract:With CNTs as substrate,a series of metallic Ru/CNTs were prepared by using glycol reduction -deposition method for gaining Ru -loading catalyst dispersed highly.TEM observations,XRD and H 2-TPD measurements of the produced materials showed that metal Ru nanoparticles were quite uniform in shape and size and well dispersed on the CNTs surface and the Ru/CNTs could adsorb considerably greater amount of hydrogen when using glycol reduction -deposition method,especially by micromaveassisted heating polyol process.The observed NH 3-decomposition conversion over Ru/CNTs catalyst prepared through ethylene glycol reduction-deposition was about 1.6times as high as that of Ru/CNTs catalyst prepared by conventional incipient wetness method under the same reaction condition.The results of the present work demonstrated that NH 3decomposition over the Ru/CNTs catalyst using glycol reduction-deposition method with the Ru x 0-crystallite size at 3~4nm displayed the highest reaction activity;while Ru x 0particle size came down to 2nm and below,the conversion of NH 3decomposition was markedly dropped. Keywords:Ru/carbon nanotubes;glycol reduction-deposition method;NH 3decomposition 中图分类号:O643 文献标识码:A 文章编号:1812-1918(2010)01-0015-06 15
中国工业催化剂常规分类 一、化肥催化剂(Catalysts for fertilizer manufacture) 一)脱毒剂(Purification agent) 1.活性炭脱硫剂(Active carbon desulfurizer) 2.加氢转化脱硫催化剂(Hydrodesulfurization Catalyst) 3.氧化锌脱硫剂(Zinc oxide sulfur absorbent) 4.脱氯剂(Dechlorinate agent) 5.转化吸收脱硫剂(Converted-absoubed desulfurizer) a.氧化铁脱硫剂(Iron ozide desulfurizer) b.铁锰脱硫剂(Iron -Nanganese oxide desulfurizer) c.羰基硫水解催化剂(Carbonyl Sulfide hydrolysis) 6.脱氧剂(Deoxidezer) 7.脱砷剂(Hydrodearsenic Catalyst) 二)转化催化剂(Reforming Catalyst) 1.天然气一段转化催化剂(Nature gas primary reforming catalyst) 2.二段转化催化剂(Secondary reforming catalyst) 3.炼厂气转化催化剂(Refinery gas steam reforming catalyst) 4.轻油转化催化剂(Naphtha steam reforming catalyst) 三)变换催化剂(CO shift catalyst) 1.中温变换催化剂(High temperature CO shift catalyst) 2.低温变换催化剂(Low temperature CO shift catalyst) 3.宽温耐硫变换催化剂(Sulfur tolerant shift catalyst) 四)甲烷化催化剂(Methanation catalyst) 1.甲烷化催化剂(Methanation Catalyst) 2.城市煤气甲烷化催化剂(Town gas methanation Catalyst) 五)氨合成催化剂(Ammonia synthesis Catalyst) 1.氨合成催化剂(Ammonia synthesis catalyst) 2.低温氨合成催化剂(Low temperature ammonia synthesis catalyst) 3.氨分解催化剂(Ammonia decomposition catalyst) 六)甲醇催化剂(Methanol Catalyst) 1.高压甲醇合成催化剂(High pressure methanol synthesis catalyst) 2.联醇催化剂(Combined methanol synthesis catalyst) 3.低压甲醇合成催化剂(Low pressure methanol synthesis catalyst) 4.燃料甲醇合成催化剂(Fuel methanol synthesis catalyst) 5.低碳混合醇合成催化剂(mixture of lower alcohols synthesis catalyst) 七)制酸催化剂(Acid manufacture catalyst) 1.硫酸生产用钒催化剂(Vanadium catalyst for manufacture of sulfuric acid)2.硝酸生产用铂网催化剂(Platinum ganze catalyst for manufacture) 3.非铂氨氧化催化剂(Non-platinum catalyst for ammonia oxidation) 4.铂捕集网(platinum catch gamze) 5.硝酸尾气处理催化剂(Treated catalyst for tail gas from nitric acid plant)八)制氮催化剂(Nitrogen manufacture catalyst) 1.一段制氮催化剂(First stage catalyst for ammonia combined) 2.二段制氮催化剂(Second stage catalyst for nitrogen manufacture)
课题:探究不同催化剂对过氧化氢分解反应速率的影响 【学习目标】 (一)知识与能力: 1.探究不同催化剂对同一反应的催化效果,用比较法通过定性和定量实验, 来寻找实验的最佳方案。认识催化剂、有效碰撞、活化能等理论。 2.提高学生处理实验数据和分析实验结果的能力。 3. 常识性介绍不同催化剂对反应速率影响。 (二)过程与方法: 1.先定量实验,后让学生更深的认识催化剂概念。 2. 要让学生在化学实验的探究中,体会“定量记时比较法”的实际应用 3. 要培养学生把化学知识与日常化工生产中遇到的实际问题联系起来考虑,并由此提出问题,提高学生的抽象概括能力、形成规律性认识的能力。 【学习重点】 建立催化剂的概念,通过定性观察实验现象和定量记时比较分析,认识不同催化剂对过氧化氢分解反应速率的影响 【学习难点】 正确理解催化剂对化学反应速率的影响,定量记时比较法在化学实验中的应用 【学习过程】 知识准备 1、实验目的 比较不同的催化剂对过氧化氢分解速率的影响的差异,从中认识到催化剂的种类、用量及其形状的选择对实验效果的影响。 2、实验原理 (1)反应原理:2H2O2 == 2H2O + O2↑ (2)实验方法:比较法 (3)考虑实验设计依据: a、确定判断依据----相同时间内产生氧气的体积 b、设计反应实验装置----测定相同时间产生氧气的体积 c、排除干扰因素----控制好与实验相关的各项反应条件 3、实验仪器及药品 实验仪器:托盘天平、钥匙、具支试管、导管、橡胶管、水槽、10ml量筒、50ml量筒、计时器、试管 实验试剂:6%H2O2溶液、MnO2、Fe2O3、CuCl2、蒸馏水 【课堂探究】 过氧化氢在一定条件下的分解的化学方程式是: 思考:1、影响H2O2分解速率大小的因素有哪些? 2、常用于H2O2分解的催化剂有哪些? 3、猜测:影响催化剂催化效果的因素可能有哪些呢? 活动探究:探究同质量不同种类催化剂对H2O2分解速率大小的影响。 小组讨论:如何设计实验方案呢?另外,这是一个多变量条件下的实验,在实验设计时应注意什么? 思考:1、可以借助一些什么现象观察到一个反应发生的快慢? 1
催化剂分类 一、化肥催化剂(Catalysts for fertilizer manufacture) 一)脱毒剂(Purification agent) 1.活性炭脱硫剂(Active carbon desulfurizer) 2.加氢转化脱硫催化剂(Hydrodesulfurization Catalyst ) 3.氧化锌脱硫剂(Zinc oxide sulfur absorbent ) 4.脱氯剂(Dechlorinate agent ) 5.转化吸收脱硫剂(Converted-absoubed desulfurizer ) a.氧化铁脱硫剂(Iron ozide desulfurizer) b.铁锰脱硫剂(Iron -Nanganese oxide desulfurizer) c.羰基硫水解催化剂(Carbonyl Sulfide hydrolysis )6.脱氧剂(Deoxidezer ) 7.脱砷剂(Hydrodearsenic Catalyst) 二)转化催化剂(Reforming Catalyst) 1.天然气一段转化催化剂(Nature gas primary reforming catalyst)2.二段转化催化剂(Secondary reforming catalyst) 3.炼厂气转化催化剂(Refinery gas steam reforming catalyst) 4.轻油转化催化剂(Naphtha steam reforming catalyst) 三)变换催化剂(CO shift catalyst) 1.中温变换催化剂(High temperature CO shift catalyst) 2.低温变换催化剂(Low temperature CO shift catalyst) 3.宽温耐硫变换催化剂(Sulfur tolerant shift catalyst ) 四)甲烷化催化剂(Methanation catalyst) 1.甲烷化催化剂(Methanation Catalyst) 2.城市煤气甲烷化催化剂(Town gas methanation Catalyst) 五)氨合成催化剂(Ammonia synthesis Catayst ) 1.氨合成催化剂(Ammonia synthesis catalyst) 2.低温氨合成催化剂(Low temperatuer ammonia synthesis catalyst)3.氨分解催化剂(Ammonia decomposition catalyst) 六)甲醇催化剂(Methanol Catalyst)