
二、医疗器械标签和包装标识内容
注意事项:
1、凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签和包
装标识。简单易用的产品,按照国家食品药品监督管理局的规定,可以省略说明书、标签和包装标识三项中的某一项或者某两项。
2、医疗器械说明书是指由生产企业制作并随产品提供给用户的,能够涵盖该产品安全有效基本
信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。其内容应当真实、完整、准确、科学,并与产品特性相一致。医疗器械企业应当对说明书内容的真实性、完整性负责,不得以任何形式欺骗和误导消费者。
3、医疗器械说明书、标签和包装标识内容应使用语言文字工作委员会公布的规范化汉字,可以
附加其他文种。
4、说明书不得含有下列内容:
①表示功效的断言或者保证:如“疗效最佳”、“保证治愈”、“包治”、“根治”、“即刻见效”“完
全无毒副作用”等;
②绝对化语言和表示:如“最高技术”、“最科学”、“最先进”、“最佳”等。
③说明“治愈率或者有效率的”;
④与其它企业产品的功效和安全性相比较的;
⑤含有“保险公司保险”、“无效退款”等承诺性语言的;
⑥利用任何单位或者个人的名义、形象作证明或者推荐的;
⑦含有使人感到已经患有某种疾病,或者使人误解不使用该医疗器械会患某种疾病或者加重病
情的表述的;
⑧法律、法规规定禁止的其他内容。
三、医疗器械说明书变更要求。
医疗器械注册证书中型号、规格、生产地址、产品标准、产品性能结构及组成、产品适用范围发生变更的,应按照《医疗器械注册管理办法》的规定履行重新注册手续后,变更医疗器械说明书的相关内容。
生产企业变更企业名称、产品名称、商品名称文字性改变、产品型号、规格文字性改变以及产品标准的名称或者代号文字性改变、生产企业注册地址变更和生产地址文字性改变的,应按照《医疗器械注册管理办法》的规定履行变更注册手续后,变更医疗器械说明书的相关内容。
生产企业变更经注册审查的医疗器械说明书的内容,不涉及产品技术性变化的,生产企业应当提交相关文件,办理相应书面告知手续后,变更医疗器械说明书的相关内容。
SYMBOL MEANING CE with number – confirmation of meeting EU requirements manufacturer sterile product; sterilised using steam sterile product; sterilised using ethylene oxide sterile product; sterilised using irradiation sterile product; no information about the type of sterilisation when more than one method can be used non sterile product batch code – the manufacturer’s code use-by-date – indicates the date after which the medical device is not to be used do not re-use – product for single use only do not resterilise do not use if package is damaged keep away from sunlight keep dry temperature limits to which the medical device can be safely exposed product contains natural rubber latex product is latex-free instructions for use attached to the product range of humidity to which the medical device can be safely exposed ,Green dot” means that the manufacturer of the product contributes to the cost of recovery and recycling information about the raw material the given packaging is made of throw away your trash non-pyrogenic product hand wash
《药品包装、标签和说明书管理规定》(暂行)(局 令第23号) 《药品包装、标签和说明书管理规定》(暂行)(局令第23号) -------------------------------------------------------------------------------- 《药品包装、标签和说明书管理规定》(暂行)于2000年3月17日经国家药品监督管理局局务会审议通过,现予发布,自2001年1月1日起执行。 局长:郑筱萸 二○○○年十月十五日 药品包装、标签和说明书管理规定 (暂行) 第一条为加强药品监督管理,规范药品的包装、标签及说明书,以利于药品的运输、 贮藏和使用,保证人民用药安全有效,特制定本规定。 第二条药品包装、标签及说明书必须按照国家药品监督管理局规定的要求印制,其文字及 图案不得加入任何未经审批同意的内容。 第三条药品包装内不得夹带任何未经批准的介绍或宣传产品、企业的文字、音像及其他资 料。 第四条凡在中国境内销售、使用的药品,其包装、标签及说明书所用文字必须以中文 为主并使用国家语言文字工作委员会公布的规范化汉字。 第五条药品的通用名称必须用中文显著标示,如同时有商品名称,则通用名称与商品 名称用字的比例不得小于1:2,通用名称与商品名称之间应有一定空隙,不得连用。 第六条药品商品名称须经国家药品监督管理局批准后方可在药品包装、标签及说明书 上标注。
第七条提供药品信息的标志及文字说明,字迹应清晰易辨,标示清楚醒目,不得有印 字脱落或粘贴不牢等现象,并不得用粘贴、剪切的方式进行修改或补充。 第八条药品的包装分内包装与外包装。 (一)内包装系指直接与药品接触的包装(如安瓿、注射剂瓶、铝箔等)。内包装应能保证药品在生产、运输、贮藏及使用过程中的质量,并便于医疗使用。 药品内包装材料、容器(药包材)的更改,应根据所选用药包材的材质,做稳定性试验,考察药包材与药品的相容性。 (二)外包装系指内包装以外的包装,按由里向外分为中包装和大包装。外包装应根 据药品的特性选用不易破损的包装,以保证药品在运输、贮藏、使用过程中的质量。 第九条药品的标签分为内包装标签与外包装标签。 (一)内包装标签与外包装标签内容不得超出国家药品监督管理局批准的药品说明书所限定的内容;文字表达应与说明书保持一致。 (二)内包装标签可根据其尺寸的大小,尽可能包含药品名称、适应症或者功能主治、用法用量、规格、贮藏、生产日期、生产批号、有效期、生产企业等标示内容,但必须标注药品名称、规格及生产批号。 (三)中包装标签应注明药品名称、主要成分、性状、适应症或者功能主治、用法用量、不良反应、禁忌症、规格、贮藏、生产日期、生产批号、有效期、批准文号、生产企业等内容。 (四)大包装标签应注明药品名称、规格、贮藏、生产日期、生产批号、有效期、批准文号、生产企业以及使用说明书规定以外的必要内容,包括包装数量、运输注意事项或其它标记等。 (五)标签上有效期具体表述形式应为:有效期至×年×月。 (六)由于尺寸原因,中包装标签不能全部注明不良反应、禁忌症、注意事项的,均应注明“详见说明书”字样。 第十条原料药的包装参照本规定第八条第(一)项执行,标签按制剂大包装标签规定 办理。 第十一条药品的每个最小销售单元的包装必须按照规定印有或贴有标签并附有说明 书。 第十二条药品说明书应包含有关药品的安全性、有效性等基本科学信息。 药品的说明书应列有以下内容:药品名称(通用名、英文名、汉语拼音、化学名称、分子式、分子量、结构式(复方制剂、生物制品应注明成分)、性状、药理毒理、药代动力学、
药品说明书和标签管理规定答案 一:名词解释。(10分) 药品的标签:指药品包装上印有或者贴有的内容,分为内标签和外标签。药品内标签指直接接触药品的包装的标签,外标签指内标签以外的其他包装的标签。 二:填空题。(50分,2分/空) 1、药品说明书和标签由国家食品药品监督管理局予以核准 2、药品的标签应当以说明书为依据,其内容不得超出说明书的范 围,不得印有暗示疗效、误导使用和不适当宣传产品的文字和 标识。 3、药品包装必须按照规定印有或者贴有标签,不得夹带其他任何 介绍或者宣传产品、企业的文字、音像及其他资料。 4、药品说明书和标签的文字表述应当科学、规范、准确。非处 方药说明书还应当使用容易理解的文字表述,以便患者自行判 断、选择和使用。 5、药品说明书和标签中的文字应当清晰易辨,标识应当清楚醒目, 不得有印字脱落或者粘贴不牢等现象,不得以粘贴、剪切、涂 改等方式进行修改或者补充。 6、出于保护公众健康和指导正确合理用药的目的,药品生产企业 可以主动提出在药品说明书或者标签上加注警示语,国家食品
药品监督管理局也可以要求药品生产企业在说明书或者标签上加注警示语。 7、药品说明书应当包含药品安全性、有效性的重要科学数据、结 论和信息,用以指导安全、合理使用药品。药品说明书的具体格式、内容和书写要求由国家食品药品监督管理局制定并发布。 8、药品说明书对疾病名称、药学专业名词、药品名称、临床检验 名称和结果的表述,应当采用国家统一颁布或规范的专用词汇,度量衡单位应当符合国家标准的规定。 9、药品生产企业应当主动跟踪药品上市后的安全性、有效性情 况,需要对药品说明书进行修改的,应当及时提出申请。 10、药品说明书核准日期和修改日期应当在说明书中醒目标示。 11、药品商品名称不得与通用名称同行书写,其字体和颜色不得 比通用名称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的二分之一。 12、药品说明书和标签中禁止使用未经注册的商标以及其他未经 国家食品药品监督管理局批准的药品名称。 13、药品标签使用注册商标的,应当印刷在药品标签的边角,含 文字的,其字体以单字面积计不得大于通用名称所用字体的四分之一。 14、醉药品、精神药品、医疗用毒性药品、放射性药品、外用药 品和非处方药品等国家规定有专用标识的,其说明书和标签必须印有规定的标识
医疗器械说明书和标签管理规定 第一条为规范医疗器械说明书和标签,保证医疗器械使用的安全,根据《医疗器械监督管理条例》,制定本规定。 第二条凡在中华人民共和国境内销售、使用的医疗器械,应当按照本规定要求附有说明书和标签。 第三条医疗器械说明书是指由医疗器械注册人或者备案人制作,随产品提供给用户,涵盖该产品安全有效的基本信息,用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 医疗器械标签是指在医疗器械或者其包装上附有的用于识别产品特征和标明安全警示等信息的文字说明及图形、符号。 第四条医疗器械说明书和标签的内容应当科学、真实、完整、准确,并与产品特性相一致。 医疗器械说明书和标签的内容应当与经注册或者备案的相关内容一致。 医疗器械标签的内容应当与说明书有关内容相符合。 第五条医疗器械说明书和标签对疾病名称、专业名词、诊断治疗过程和结果的表述,应当采用国家统一发布或者规范的专用词汇,度量衡单位应当符合国家相关标准的规定。 第六条医疗器械说明书和标签中使用的符号或者识别颜色应当符合国家相关标准的规定;无相关标准规定的,该符号及识别颜色应当在说明书中描述。 第七条医疗器械最小销售单元应当附有说明书。 医疗器械的使用者应当按照说明书使用医疗器械。 第八条医疗器械的产品名称应当使用通用名称,通用名称应当符合国家食品药品监督管理总局制定的医疗器械命名规则。第二类、第三类医疗器械的产品名称应当与医疗器械注册证中的产品名称一致。 产品名称应当清晰地标明在说明书和标签的显著位置。 第九条医疗器械说明书和标签文字内容应当使用中文,中文的使用应当符合国家通用的语言文字规范。医疗器械说明书和标签可以附加其他文种,但应当以中文表述为准。 医疗器械说明书和标签中的文字、符号、表格、数字、图形等应当准确、清晰、规范。
医疗器械标志、标签要求 医疗器械处黄荣建 二〇〇六年三月 一、范围 为医疗器械的安全和有效使用,给使 用者和其他人员规定了用于提供医疗器械 重要信息的标志、标识,主要由下列人员使 用。 ???? 医疗器械制造商 ???? 医疗器械使用者 ???? 负责医疗器械产品上市后监督的人员 ???? 主管部门、检测机构、认证机构等 二、依据 ???? 法律、法规 《医疗器械监督管理条例》 《医疗器械说明书、标签、包装标识》 ???? 国家标准、行业标准 通用标准 专用标准 产品标准 ???? 企业标准(注册产品标准) 标识、标签和使用说明书。 附录A安全要求中“外部标记”。(医用电气产 品) 通用标准 ?GB/T191-2000《包装储运图示标志》
?YY0466-2003《医疗器械用于医疗器械标签、标记和提供信息的符号》 ?YY/T0313-1998《医用高分子制品包装、标志、运输和贮存》?GB9706.1-1995《医用电气设备第一部分:安全通用要求》 ?YY91099-1999《医用X线设备标志、包装、运输和贮存》 专用标准 ?YY0089-1992《病人监护系统专用安全要求》 ?YY0319-2000《医用电气设备第二部分:医疗诊断用磁共振设备安全专用要求》 ?GB9706.X-XXXX《医用电气设备第X部分:XX设备安全专用要求》 ?YY0290.4-1997《人工晶体第4部分:标签和资料》 ?YY/T0486-2004《激光手术专用气管插管标志和提供信息的要求》 产品标准 ?GB8369-2005《一次性使用输血器》 ?GB10152《B型超声诊断设备》 ?YY0460-2003《超声洁牙设备》 医用高分子制品标志 ?单包装或初包装宜有下列标志: —产品名称、型号或规格; —制造厂名称、地址和商标; —生产批号或日期。 ?无菌产品的单包装或初包装还宜有下列标志:
最新版《医疗器械说明书和标签管理规定》 xx年7月30日国家食品药品监督管理总局令第6号公布自xx 年10月1日起施行,下面是为您精心的关于医疗器械说明书和标签管理规定全文内容,仅供大家参考。 第一条为规范医疗器械说明书和标签,保证医疗器械使用的安全,根据《医疗器械监督管理条例》,制定本规定。 第二条凡在 * 境内销售、使用的医疗器械,应当按照本规定要求附有说明书和标签。 第三条医疗器械说明书是指由医疗器械注册人或者备案人制作,随产品提供给用户,涵盖该产品安全有效的基本信息,用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 医疗器械标签是指在医疗器械或者其包装上附有的用于识别产品特征和标明安全警示等信息的文字说明及图形、符号。 第四条医疗器械说明书和标签的内容应当科学、真实、完整、准确,并与产品特性相一致。 医疗器械说明书和标签的内容应当与经注册或者备案的相关内容一致。 医疗器械标签的内容应当与说明书有关内容相符合。 第五条医疗器械说明书和标签对疾病名称、专业名词、诊断治疗过程和结果的表述,应当采用国家统一发布或者规范的专用词汇,度量衡单位应当符合国家相关标准的规定。
第六条医疗器械说明书和标签中使用的符号或者识别颜色应 当符合国家相关标准的规定;无相关标准规定的,该符号及识别颜色应当在说明书中描述。 第七条医疗器械最小销售单元应当附有说明书。 医疗器械的使用者应当按照说明书使用医疗器械。 第八条医疗器械的产品名称应当使用通用名称,通用名称应当符合国家食品药品监督管理总局制定的医疗器械命名规则。第二类、第三类医疗器械的产品名称应当与医疗器械注册证中的产品名称一致。 产品名称应当清晰地标明在说明书和标签的显著位置。 第九条医疗器械说明书和标签文字内容应当使用中文,中文的使用应当符合国家通用的语言文字规范。医疗器械说明书和标签可以附加其他文种,但应当以中文表述为准。 医疗器械说明书和标签中的文字、符号、表格、数字、图形等应当准确、清晰、规范。 第十条医疗器械说明书一般应当包括以下内容: (一)产品名称、型号、规格; (二)注册人或者备案人的名称、住所、 * 及售后服务单位,进口医疗器械还应当载明代理人的名称、住所及 * ; (三)生产企业的名称、住所、生产地址、 * 及生产许可证编号或者生产备案凭证编号,委托生产的还应当标注受托企业的名称、住所、生产地址、生产许可证编号或者生产备案凭证编号;
药品说明书和标签管理规定培训试题及答案 篇一:药品说明书和标签管理规定 试题 部门:__岗位:__姓名:___ 成绩:___ 一 填空题(每空 2 分,共 74 分) 1. 《药品说明书和标签管理规定》 于 2006 年 3 月 10 日经国家食品药品监督 管理局会审通过,现予公布,自 2006 年 6 月 1 日 起施行 2.药品的标签应当以说明书 为依据,其内容不得超出说明书的范围,不得 印有 暗示疗效 、 误导使用 和不适当宣传产品的文字和标识 3.药品生产企业生产供上市销售的最小包装必须附有 说明书 4.药品说明书应当包含药品安全性、有效性的重要科学数据、 结论 和 信 息 ,用以指导安全、合理使用药品。 5.药品说明书 核准 日期和修改日期应当在说明书中项目标示。 6.药品说明书和标签的文字表述 科学 、 规范 、 准确 、以便患者自行判 断、 选择 和使用 7 药品说明书对 疾病名称、 药学专业名词、 药品名称、 临床检验名称和 结 果 的表述, 应采用国家统一颁布或规范的专用词汇, 度量衡单位应当符合 国家 标准 的规定。 8.药品的标签是指药品包装上印有或者帖有的内容,分为内标签和外标签。 药品内标签指 直接接触药品 的包装的标签, 外标签指 内标签 以外的其他包装 的标签。 9.药品的包装尺寸过小无法全部表明上述内容的,至少应当标注药品 通用 名称 、规格、产品批号、有效期 等内容。 10.同一药品生产企业生产的同一药品,分别按 处方药 非 处方 管理的, 两者的包装颜色应当明显区别。 11. 治疗用生物制品有效期的标注自 分装日期 计算, 其他药品有效期的标 注自 生产日期 计算。有效期若标注到日,应当为起算日期对应年月日的 前一 天 ,若标注到月,应当为起算月分对应年月的前一月。 12.药品 商品名称不得与通用名称同行书写, 其字体和颜色 不得 比通用名 称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的 二分 之一 13.药品说明书和标签中禁止使用 未经注册 的商标以及其他未经国家食品
医疗器械说明书和标签管理规定 (国家食品药品监督管理总局局令第6号) 2015年03月31日 第一条为规范医疗器械说明书和标签,保证医疗器械使用的安全,根据《医疗器械监督管理条例》,制定本规定。 第二条凡在中华人民共和国境内销售、使用的医疗器械,应当按照本规定要求附有说明书和标签。 第三条医疗器械说明书是指由医疗器械注册人或者备案人制作,随产品提供给用户,涵盖该产品安全有效的基本信息,用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 医疗器械标签是指在医疗器械或者其包装上附有的用于识别产品特征和标明安全警示等信息的文字说明及图形、符号。 第四条医疗器械说明书和标签的内容应当科学、真实、完整、准确,并与产品特性相一致。 医疗器械说明书和标签的内容应当与经注册或者备案的相关内容一致。 医疗器械标签的内容应当与说明书有关内容相符合。
第五条医疗器械说明书和标签对疾病名称、专业名词、诊断治疗过程和结果的表述,应当采用国家统一发布或者规范的专用词汇,度量衡单位应当符合国家相关标准的规定。 第六条医疗器械说明书和标签中使用的符号或者识别颜色应当符合国家相关标准的规定;无相关标准规定的,该符号及识别颜色应当在说明书中描述。 第七条医疗器械最小销售单元应当附有说明书。 医疗器械的使用者应当按照说明书使用医疗器械。 第八条医疗器械的产品名称应当使用通用名称,通用名称应当符合国家食品药品监督管理总局制定的医疗器械命名规则。第二类、第三类医疗器械的产品名称应当与医疗器械注册证中的产品名称一致。 产品名称应当清晰地标明在说明书和标签的显著位置。 第九条医疗器械说明书和标签文字内容应当使用中文,中文的使用应当符合国家通用的语言文字规范。医疗器械说明书和标签可以附加其他文种,但应当以中文表述为准。 医疗器械说明书和标签中的文字、符号、表格、数字、图形等应当准确、清晰、规范。
医疗器械产品说明以及包装标识详解 医疗器械生产企业对于医疗器械产品的说明书、标签、以及包装标识都不是特别的清楚,所以出现了很多医疗器械厂家的产品标识不够明确,产品使用说明书不易读懂,给经销商和消费者带来了诸多不便,甚至出现法律纠纷。 针对于以上诸多情况,国家食品药品监督管理局于2004年6月18日颁布了《医疗器械说明书、标签和包装标识管理规定》,规定要求:凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签和包装标识。简单易用的产品,按照国家食品药品监督管理局的规定,可以省略说明书、标签和包装标识三项中的某一项或者某两项的,依照其规定。该规定的内容,主要分为六个方面: 一、消费者应该按照医疗器械使用说明书使用医疗器械产品,这就要求医疗器械厂商应该对说明书有个详细的介绍。 二、规定了医疗器械说明书、标签以及包装标识的定义,说明书主要是伴随产品提供给客户,提供客户产品有效信息,并对其使用产品起到指导作用的文件。标签即用于识别产品特性的文字,也可以是图形、符号。包装标识及反应产品的技术特征,同样可以是文字、图形、符号。 三、规定要求,医疗器械使用说明书、标签和包装标识必须包括中文字体,而且数据应该真实、有效与产品特性相一致。 四、规定对医疗器械说明书、标签和包装标识都应该符合国家规定标准,包括对产品的一些技术参数、使用说明等有着详细的说明,此外还规定了内容中不得包含的词语,例如:“疗效最佳”、“保证治愈”、“包治”、“根治”、“即刻见效”、“完全无毒副作用”等表示功效 的断言或者保证的;以及含有“最高技术”、“最科学”、“最先进”、“最佳”
等绝对化语言和表示的都不符合规定。 五、医疗器械说明书中有关注意事项、警示以及提示性内容主要包括: (一)产品使用可能带来的副作用; (二)产品在正确使用过程中出现意外时,对操作者、使用者的保护措施以及应当采取的应急和纠正措施; (三)一次性使用产品应当注明“一次性使用”字样或者符号; (四)已灭菌产品应当注明灭菌方式,注明“已灭菌”字样或者标记,并注明灭菌包装损坏后的处理方法; (五)使用前需要消毒或者灭菌的应当说明消毒或者灭菌的方法; (六)产品需要同其他产品一起安装或者协同操作时,应当注明配合使用的要求; (七)在使用过程中,与其他产品可能产生的相互干扰及其可能出现的危险性; (八)产品使用后需要处理的,应当注明相应的处理方法; (九)根据产品特性,应当提示操作者、使用者注意的其他事项。 六、医疗器械生产企业有违反规定行为的,县级以上食品药品监督管理部门有权给予警告,并要求整改。
2014年6月27日,中国食品药品监督管理局常务会议审议通过了《医疗器械说明书和标签管理规定》,2014年7月30日中国食品药品监督管理总局令第6号发布该规定共有19条,将于2014年10月1日生效。2004年7月8日,国家食品药品监督管理局第10号令发布了《医疗器械说明书,标签和标识管理规定》。包装商标,已被废除。 第一条为了规范医疗器械的使用说明和标签,确保医疗器械的使用安全,本规定是根据《医疗器械监督管理条例》制定的。 第二条在中华人民共和国境内销售和使用的所有医疗器械,均应当有符合本规定要求的说明和标签。 第三条医疗器械规范,是指医疗器械注册人或申报人提供给用户的产品所提供的技术文件,涵盖产品安全有效的基本信息,用于指导正确的安装,调试,操作,使用,维护。和维护。医疗设备标签是指粘贴在医疗设备或其包装上的书面说明,图形和符号,用于识别产品功能并标记安全警告。 第四条医疗器械说明书和标签的内容应当科学,真实,完整,准确,并与产品特性相一致。医疗器械说明书和标签的内容应与注册或备案的有关内容一致。医疗器械标签上的内容应与说明书的有关内容一致。
第五条医疗器械手册,标签中的疾病名称,专业术语,诊治过程和结果的说明,应当采用国家统一发行或标准化的专用词汇,计量单位应当符合国家有关标准的规定。 第六条医疗器械说明书和标签中使用的符号或标识颜色,应当符合国家有关标准的规定;如果没有相关标准,则应在手册中说明符号和标识颜色。 第七条最低销售单位应附有说明。医疗设备的用户应按照说明使用医疗设备。 第八条医疗器械产品名称应使用通用名称,符合中国食品药品监督管理局制定的医疗器械命名规则。第二类和第三类医疗器械的产品名称应与医疗器械注册证书中的产品名称一致。产品名称应在手册和标签中的醒目位置明显标记。 第九条医疗器械说明书和标签的内容应当为中文,中文的使用应当符合国家语言文字标准。医疗器械说明和标签可以用其他语言粘贴,但以中文表达为准。医疗器械说明书和标签中的文字,符号,表格,数字和图形应准确,清晰,规范。
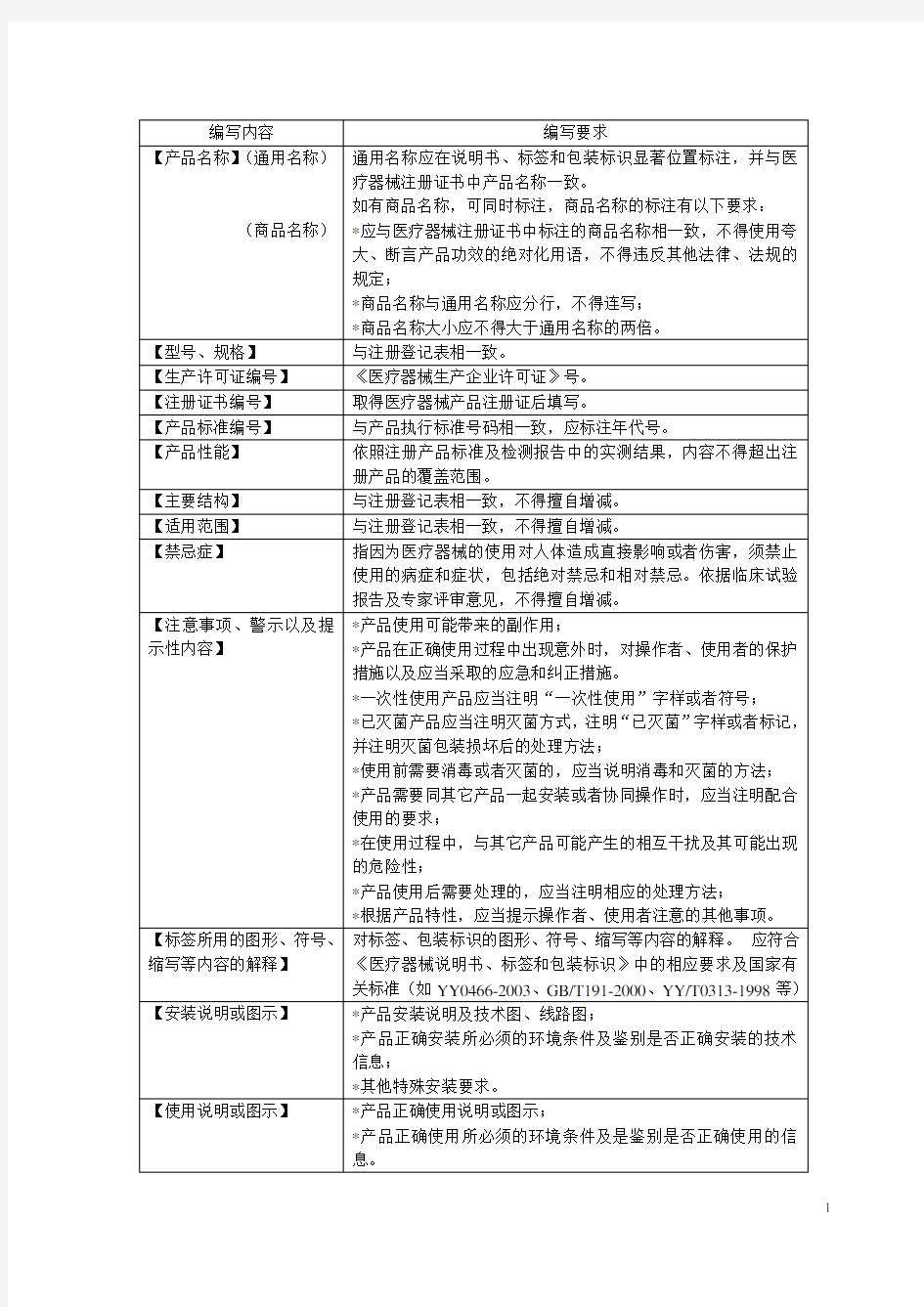
医疗器械说明书、标签和包装标识编写要求示范文本 医疗器械生产企业应按照《医疗器械说明书、标签和包装标识管理规定》的要求正确编写说明书,并承担法律责任。经(食品)药品监督管理部门注册审查的医疗器械说明书的内容不得擅自改动。 医疗器械生产企业须按以下内容和要求依顺序进行编写,否则不予受理。 根据第10号令的基本要求,作此格式仅供参考。
二、医疗器械标签和包装标识内容 注意事项: 1、凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签 和包装标识。简单易用的产品,按照国家食品药品监督管理局的规定,可以省略说明书、标签和包装标识三项中的某一项或者某两项。 2、医疗器械说明书是指由生产企业制作并随产品提供给用户的,能够涵盖该产品安全有效
基本信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。其内容应当真实、完整、准确、科学,并与产品特性相一致。医疗器械企业应当对说明书内容的真实性、完整性负责,不得以任何形式欺骗和误导消费者。 3、医疗器械说明书、标签和包装标识内容应使用语言文字工作委员会公布的规范化汉字, 可以附加其他文种。 4、说明书不得含有下列内容: ①表示功效的断言或者保证:如“疗效最佳”、“保证治愈”、“包治”、“根治”、“即刻见效” “完全无毒副作用”等; ②绝对化语言和表示:如“最高技术”、“最科学”、“最先进”、“最佳”等。 ③说明“治愈率或者有效率的”; ④与其它企业产品的功效和安全性相比较的; ⑤含有“保险公司保险”、“无效退款”等承诺性语言的; ⑥利用任何单位或者个人的名义、形象作证明或者推荐的; ⑦含有使人感到已经患有某种疾病,或者使人误解不使用该医疗器械会患某种疾病或者加 重病情的表述的; ⑧法律、法规规定禁止的其他内容。 三、医疗器械说明书变更要求。 医疗器械注册证书中型号、规格、生产地址、产品标准、产品性能结构及组成、产品适用范围发生变更的,应按照《医疗器械注册管理办法》的规定履行重新注册手续后,变更医疗器械说明书的相关内容。 生产企业变更企业名称、产品名称、商品名称文字性改变、产品型号、规格文字性改变以及产品标准的名称或者代号文字性改变、生产企业注册地址变更和生产地址文字性改变的,应按照《医疗器械注册管理办法》的规定履行变更注册手续后,变更医疗器械说明书的相关内容。 生产企业变更经注册审查的医疗器械说明书的内容,不涉及产品技术性变化的,生产企业应当提交相关文件,办理相应书面告知手续后,变更医疗器械说明书的相关内容。
医疗器械说明书、标签和包装标识管理规定(国家局令第10号)网上培训试题 (各企业将试卷存入本企业培训档案中) 企业名称:__________________________ 答卷人:______________ 成绩:__________ 一、填空题: 1、医疗器械说明书是指由生产企业制作并随产品提供给用户的,能够涵盖该产品安全有效基本信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 2、医疗器械标签是指在医疗器械或者包装上附有的,用于识别产品特征的文字说明及图形、符号。 3、医疗器械包装标识是指在包装上标有的反映医疗器械主要技术特征的文字说明及图形、符号。 二、多项选择题: 1、医疗器械说明书中有关安装的内容应当能够保证操作者、使用者正确安装使用,应当包括(A、B、C): A、产品安装说明及技术图、线路图; B、产品正确安装所必须的环境条件及鉴别是否正确安装的技术信息; C、其他特殊安装要求。 2、医疗器械说明书应当符合国家标准或者行业标准有关要求,一般应当包括以下内容(A、 B、C、D、E、F、G、H、I、十、一): A、产品名称、型号、规格; B、生产企业名称、注册地址、生产地址、联系方式及售后服务单位; C、《医疗器械生产企业许可证》编号(第一类医疗器械除外)、医疗器械注册证书编号; D、产品标准编号; E、产品的性能、主要结构、适用范围; F、禁忌症、注意事项以及其他需要警示或者提示的内容; G、医疗器械标签所用的图形、符号、缩写等内容的解释; H、安装和使用说明或者图示; I、产品维护和保养方法,特殊储存条件、方法; (十)限期使用的产品,应当标明有效期限; (十一)产品标准中规定的应当在说明书中标明的其他内容。 三、判断题: ()1、医疗器械说明书、标签和包装标识的内容应当真实、完整、准确、科学,并与产品 特性相一致。 ()2、医疗器械说明书、标签和包装标识文字内容必须使用中文,不可以附加其他文种。()3、凡在中华人民共和国境内销售、使用的医疗器械应当按照《医疗器械说明书、标签和包装标识管理规定》要求附有说明书、标签和包装标识
国家食品药品监督管理局令 第24号 《药品说明书和标签管理规定》于2006年3月10日经国家食品药品监督管理局局务会审议通过,现予公布,自2006年6月1日起施行。 局长:邵明立 二○○六年三月十五日 药品说明书和标签管理规定 第一章总则 第一条为规范药品说明书和标签的管理,根据《中华人民共和国药品管理法》和《中华人民共和国药品管理法实施条例》制定本规定。 第二条在中华人民共和国境内上市销售的药品,其说明书和标签应当符合本规定的要求。 第三条药品说明书和标签由国家食品药品监督管理局予以核准。 药品的标签应当以说明书为依据,其内容不得超出说明书的范围,不得印有暗示疗效、误导使用和不适当宣传产品的文字和标识。 第四条药品包装必须按照规定印有或者贴有标签,不得夹带其他任何介绍或者宣传产品、企业的文字、音像及其他资料。 药品生产企业生产供上市销售的最小包装必须附有说明书。 第五条药品说明书和标签的文字表述应当科学、规范、准确。非处方药说明书还应当使用容易理解的文字表述,以便患者自行判断、选择和使用。 第六条药品说明书和标签中的文字应当清晰易辨,标识应当清楚醒目,不得有印字脱落或者粘贴不牢等现象,不得以粘贴、剪切、涂改等方式进行修改或者补充。第七条药品说明书和标签应当使用国家语言文字工作委员会公布的规范化汉字,增加其他文字对照的,应当以汉字表述为准。
第八条出于保护公众健康和指导正确合理用药的目的,药品生产企业可以主动提出在药品说明书或者标签上加注警示语,国家食品药品监督管理局也可以要求药品生产企业在说明书或者标签上加注警示语。 第二章药品说明书 第九条药品说明书应当包含药品安全性、有效性的重要科学数据、结论和信息,用以指导安全、合理使用药品。药品说明书的具体格式、内容和书写要求由国家食品药品监督管理局制定并发布。 第十条药品说明书对疾病名称、药学专业名词、药品名称、临床检验名称和结果的表述,应当采用国家统一颁布或规范的专用词汇,度量衡单位应当符合国家标准的规定。 第十一条药品说明书应当列出全部活性成份或者组方中的全部中药药味。注射剂和非处方药还应当列出所用的全部辅料名称。 药品处方中含有可能引起严重不良反应的成份或者辅料的,应当予以说明。 第十二条药品生产企业应当主动跟踪药品上市后的安全性、有效性情况,需要对药品说明书进行修改的,应当及时提出申请。 根据药品不良反应监测、药品再评价结果等信息,国家食品药品监督管理局也可以要求药品生产企业修改药品说明书。 第十三条药品说明书获准修改后,药品生产企业应当将修改的内容立即通知相关药品经营企业、使用单位及其他部门,并按要求及时使用修改后的说明书和标签。第十四条药品说明书应当充分包含药品不良反应信息,详细注明药品不良反应。药品生产企业未根据药品上市后的安全性、有效性情况及时修改说明书或者未将药品不良反应在说明书中充分说明的,由此引起的不良后果由该生产企业承担。 第十五条药品说明书核准日期和修改日期应当在说明书中醒目标示。 第三章药品的标签
附件3 医疗器械说明书、标签和包装标识管理规定 (征求意见稿) 第一条为规范医疗器械说明书、标签和包装标识,保证医疗器械使用的安全,根据《医疗器械监督管理条例》,制定本规定。 第二条凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签和包装标识。说明书、标签和包装标识中的某两项或者三项可以合并。 第三条医疗器械说明书是指由注册申请人/备案人制作并随产品提供给用户的,能够涵盖该产品安全有效基本信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 医疗器械标签是指在医疗器械产品本体或者包装上附有的,用于识别产品特征的文字说明及图形、符号。 医疗器械包装标识是指在包装上(或内)标有的反映医疗器械主要技术特征的文字说明及图形、符号。 第四条医疗器械的使用者应当按照医疗器械说明书使用医疗器械。 第五条医疗器械说明书、标签和包装标识的内容应当真实、完整、准确、科学,并与产品特性相一致。医疗器械标签、包装标识的内容应当与说明书有关内容相符合。 第六条医疗器械说明书、标签和包装标识对疾病名称、专业名词、诊断治疗过程和结果的表述,应当采用国家统一颁布或规范的专用词汇,度量衡单位应当符合国家标准的规定。 第七条医疗器械说明书、标签和包装标识可以用符号的形式表示,使用的符号或识别颜色应符合国家相关标准的规定。若无相关标准,该符号及色彩应于器械附加的说明书中描述。 第八条医疗器械的产品名称应当符合国家相应的标准及国家食品药品监督管理总局制定的医疗器械命名原则。医疗器械的产品名称应当清晰地标明在说明书、标签和包装标识的显著位置,并与医疗器械注册证/备案信息表中的产品名称一致。
《药品说明书和标签管理规定》培训试题 姓名:部门:考核成绩: 一、填空:(每空3分,共90分) 1.药品说明书和标签由()予以核准。 2.药品的标签应当以()为依据,其内容不得超出()的范围,不得印有暗示疗效、误导使用和不适当宣传产品的()和()。 3.药品生产企业生产供上市销售的最小包装必须附有()。 4.药品说明书和标签应当使用国家语言文字工作委员会公布的规范化汉字,增加其他文字对照的,应当以()表述为准。 5.出于保护公众健康和指导正确合理用药的目的,药品生产企业可以主动提出在药品说明书或者标签上加注(),国家食品药品监督管理局也可以要求药品生产企业在说明书或者标签上加注警示语。 6.药品说明书的具体格式、内容和书写要求由()制定并发布。 7.药品说明书()和修改日期应当在说明书中醒目标示。 8.药品的标签是指药品包装上印有或者贴有的(),分为()标签和()标签。 9.药品()指直接接触药品的包装的标签,()指内标签以外的其他包装的标签。 10.包装尺寸过小无法全部标明上述内容的,至少应当标注药品()、()、()、()等内容。 11.有效期若标注到日,应当为起算日期对应年月日的(),若标注到月,应当为起算月份对应年月的()。 12.药品说明书和标签中标注的药品名称必须符合()公布的药品通用名称和商品名称的命名原则,并与药品批准证明文件的相应内容()。 13.药品通用名称应当显著、突出,其字体、字号和颜色必须一致,对于横版标签,必须在()三分之一范围内显著位置标出;对于竖版标签,必须在()三分之一范围内显著位置标出。 14.药品通用名称字体颜色应当使用()或者(),与相应的浅色或者深色背景形成强烈反差; 15.药品标签使用注册商标的,应当印刷在药品标签的边角,含文字的,其字体以单字面积计不得大于通用名称所用字体的()。 16.药品商品名称不得与通用名称同行书写,其字体和颜色不得比通用名称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的()。 17.对贮藏有特殊要求的药品,应当在标签的()位置注明。 二、判断题:(每题1分,共10分) 1.药品包装可以夹带其他任何介绍或者宣传产品、企业的文字、音像及其他资料。() 2.药品说明书和标签的文字表述应当科学、规范、准确。非处方药说明书还应当使用容易理解的文字表述,以便患者自行判断、选择和使用。() 3.药品说明书和标签中的文字应当清晰易辨,标识应当清楚醒目,不得有印字脱落或者粘贴不牢等现象,可以以粘贴、剪切、涂改等方式进行修改或者补充。() 4.药品说明书应当列出全部活性成份或者组方中的全部中药药味。注射剂和非处方药不必列出所用的全部辅料名称。() 5.药品处方中含有可能引起严重不良反应的成份或者辅料的,应当予以说明。() 6.药品说明书获准修改后,药品生产企业应当将修改的内容立即通知相关药品经营企业、使用单位及其他部门,并按要求及时使用修改后的说明书和标签。() 7.药品标签中的有效期应当按照月、日、年的顺序标注。()
医疗废物专用包装物、容器标准 和警示标识规定 第一条根据《医疗废物管理条例》第十六条的规定,制定本标准和规定。 第二条包装袋标准 (一)基本要求 1. 包装袋不得使用聚氯乙烯(PVC )塑料为制造原料; 2. 聚乙烯(PE)包装袋正常使用时不得渗漏、破裂、穿孔; 3 .最大容积为0.1m 3, 大小和形状适中,便于搬运和配合周转箱(桶)盛装; 4. 如果使用线型低密度聚乙烯(LLDPE )或低密度聚乙烯与线型低密度聚乙烯共混(LLDPE+LDPE )为原料,其最小公称厚度应为150 pm ;如果使用中密度或高密度聚乙烯 (MDPE , HDPE ),其最小公称厚度应为80 p m ; 5. 包装袋的颜色为黄色,并有盛装医疗废物类型的文字说明,如盛装感染性废物,应在包装袋上加注“感染性废物” 字样; 6. 包装袋上应印制本规定第五条确定的医疗废物警示标识。 二)技术性能要求
1. 包装袋外观标准符合表一要求。 表1包装袋外观标准 2. 包装袋物理机械性能符合表二要求 表2包装袋物理机械性能 3. 包装袋规格 (1 )推荐采用筒状包装袋:折径x长乂厚(mm ):
LDPE+LLDPE ) 450mm x500mm x0.08mm ( HDPE ;MDPE ) ( 2 )当包装袋容积在0.1m 3范围内,包装袋规格可以根据用户要求确定。 ( 3)当用户有特殊要求,并且包装袋容积超过0.1m 3 时,包装袋厚度应根据试验确定,保证包装袋防渗漏、防破裂、防穿孔,整体物理机械性能不低于表二要求。 第三条利器盒标准 1. 利器盒整体为硬制材料制成,密封,以保证利器盒在正常使用的情况下,盒内盛装的锐利器具不撒漏,利器盒一旦被封口,则无法在不破坏的情况下被再次打开; 2 .利器盒能防刺穿,其盛装的注射器针头、破碎玻璃片等锐利器具不能刺穿利器盒; 3 .满盛装量的利器盒从1.5m 高处垂直跌落至水泥地面,连续3 次,利器盒不会出现破裂、被刺穿等情况; 4. 利器盒易于焚烧, 不得使用聚氯乙烯( PVC )塑料作 为制造原材料; 5 .利器盒整体颜色为黄色,在盒体侧面注明“损伤性废 物”;
闫子轩发表于2007-1-30 13:49 关于《药品说明书和标签管理规定》有关问题解释的通知 国食药监注[2007]49号 各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 《药品说明书和标签管理规定》(局令24号,以下简称《规定》)及其实施公告(国食药监注〔2006〕100号)、《关于进一步规范药品名称管理的通知》(国食药监注〔2006〕99号)发布后,国家局陆续收到一些省局、协会以及企业的来函,要求对其中的部分内容进行解释。经研究,现就有关问题明确如下。 一、药品说明书和标签修改的补充申请 已经批准注册的药品,其说明书和标签的格式、内容不符合《规定》的,均应当根据《关于实施〈药品说明书和标签管理规定〉有关事宜的公告》(以下简称《公告》)的要求提出补充申请。 化学药品、生物制品说明书和标签修改的补充申请按照《药品注册管理办法》关于补充申请的要求执行。国产药品由省级药品监督管
理部门受理和审批并报国家局备案,省级药品监督管理部门审批日期为核准日期。进口药品由国家局受理和备案,备案日期为核准日期。进口分包装药品的说明书和标签应在进口药品说明书和标签同意备 案后,报省级药品监督管理部门审批,其内容除分包装信息外,应当与进口药品的说明书和标签一致。 中药、天然药物说明书和标签修改的补充申请按照《关于印发中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知》(国食药监注〔2006〕283号)执行。 非处方药说明书和标签修改的补充申请按照《药品注册管理办法》的要求执行,进口药品由国家局受理和备案,备案日期为修订日期。 药品生产企业提出补充申请时提交的药品说明书和标签可以是 实样,也可以是设计样稿。 二、药品名称的使用 药品通用名称必须使用黑色或者白色,不得使用其他颜色。浅黑、灰黑、亮白、乳白等黑、白色号均可使用,但要与其背景形成强烈反差。 根据《关于进一步规范药品名称管理的通知》(国食药监注〔2 006〕99号),自2006年6月1日起,属于下列情形的药品可以申请使用商品名称:(一)新化学结构、新活性成份且在保护期、过渡期或者监测期内的药品;(二)在我国具有化合物专利,且该专利在
黑龙江省药监局的说明(ppt): 一、配套文件的主要内容: (2)2006年6月1日前批准注册且2007年6月1日前生产出厂的药品,其说明书和标签符合23号令要求的,可以在药品有效期内销售使用 (4)个别品种因特殊情况如设备技术等原因,其内标签印制通用名称、规格、生产批号和有效期确有困难的,药品生产企业应当向国家食品药品监督管理局提出申请,同意后方可减少标注内容。 二、与23号令相比: 第二十三条有效期的表示方法: 药品标签中的有效期应当按照年、月、日的顺序标注,年份用四位数字表示,月、日用两位数表示。 其具体标注格式为“有效期至XXXX年XX月”或者“有效期至XXXX年XX月XX日”;也可以用数字和其他符号表示为“有效期至XXXX.XX.”或者“有效期至XXXX/XX/XX”等。 预防用生物制品有效期的标注按照国家食品药品监督管理局批准的注册标准执行,治疗用生物制品有效期的标注自分装日期计算,其他药品有效期的标注自生产日期计算。 具体表示方法应当为起算月份对应年月的前一月。 第二十五条 对药品通用名称的书写的要求: 药品通用名称应当显著、突出,其字体、字号和颜色必须一致,并符合以下要求:(一)对于横版标签,必须在上三分之一范围内显著位置标出;对于竖版标签,必须在右三分之一范围内显著位置标出 (二)不得选用草书、篆书等不易识别的字体,不得使用斜体、中空、阴影等形式对字体进行修饰 (三)字体颜色应当使用黑色或者白色,与相应的浅色或者深色背景形成强烈反差 第二十六条 对商品名称的要求有较大变化: 药品商品名称不得与通用名称同行书写,其字体和颜色不得比通用名称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的二分之一。 (四)除因包装尺寸的限制而无法同行书写的,不得分行书写
医疗器械说明书标签与包装标识管理 制度 1
2
国家食品药品监督管理局令 第10号 <医疗器械说明书、标签和包装标识管理规定>于 6月18日经国家食品药品监督管理局局务会审议经过,现予公布。本规定自公布之日起施行。 局长:郑筱萸 二○○四年七月八日 医疗器械说明书、标签和包装标识管理规定 第一条为规范医疗器械说明书、标签和包装标识,保证医疗器械使用的安全,根据<医疗器械监督管理条例>,制定本规定。 第二条凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签和包装标识。简单易用的产 3
品,按照国家食品药品监督管理局的规定,能够省略说明书、标签和包装标识三项中的某一项或者某两项的,依照其规定。 第三条医疗器械的使用者应当按照医疗器械说明书使用医疗器械。 第四条医疗器械说明书是指由生产企业制作并随产品提供给用户的,能够涵盖该产品安全有效基本信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。 医疗器械标签是指在医疗器械或者包装上附有的,用于识别产品特征的文字说明及图形、符号。 医疗器械包装标识是指在包装上标有的反映医疗器械主要技术特征的文字说明及图形、符号。 第五条医疗器械说明书、标签和包装标识的内容应当真实、完整、准确、科学,并与产品特性相一致。 医疗器械标签、包装标识的内容应当与说明书有关内容相符合。 第六条医疗器械说明书、标签和包装标识文字内容必须使用中文,能够附加其它文种。中文的使用应当符合国家通用的语言文字规范。 医疗器械说明书、标签和包装标识的文字、符号、图形、表格、数字、照片、图片等应当准确、清晰、规范。 4