
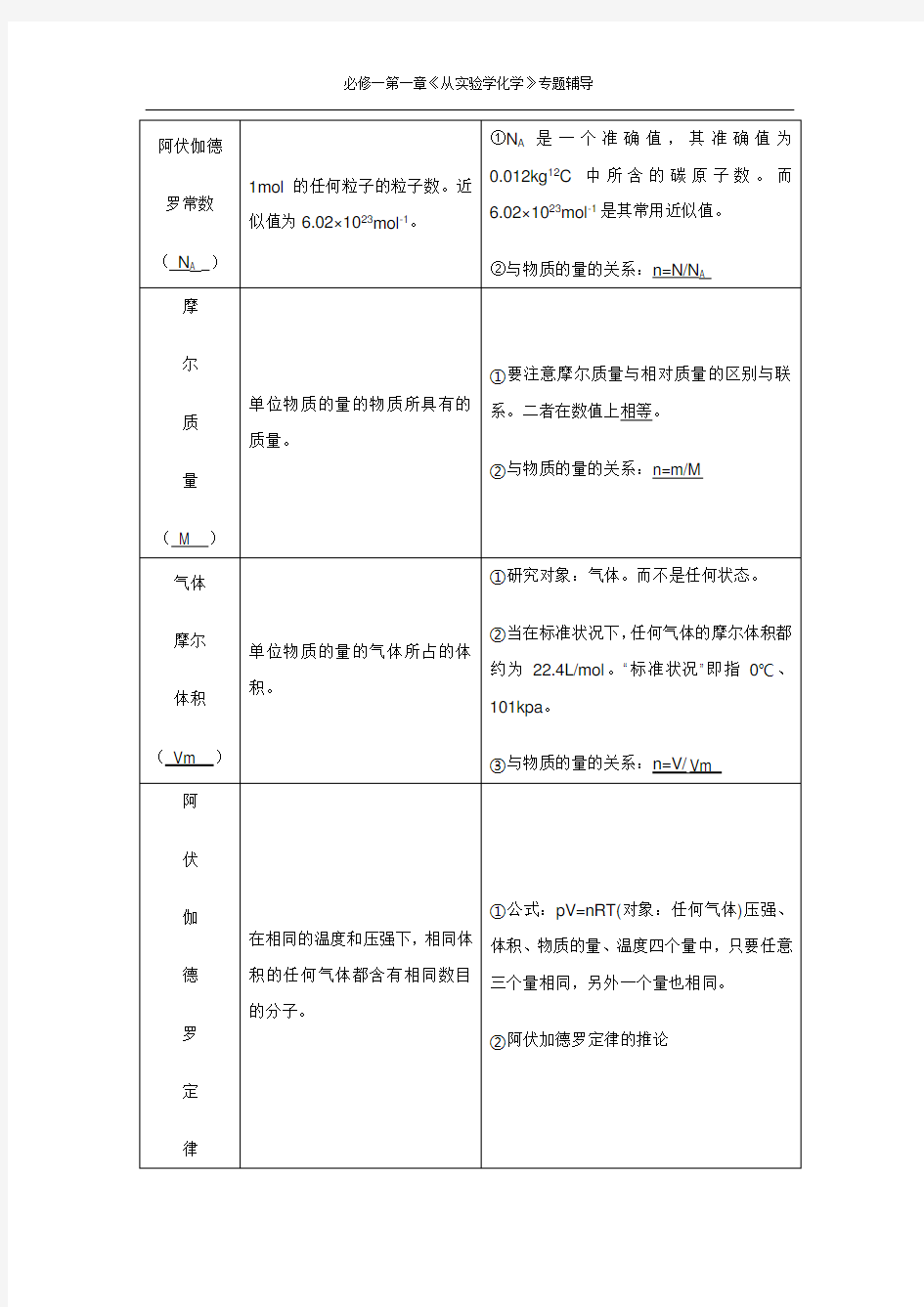
专题一 物质的量
【知识回顾】
一、第一章知识结构框架图:
二、物质的量相关知识点 1、基本概念
【即时练习】
判断正误。(概念理解)
1 1mol大米
2 1mol氧
3 水的摩尔质量等于N A个水分子质量之和。
4 1mol CH4和1mol CO所含分子数目相同。
【答案与解析】
1(X)物质的量是用来描述微观粒子的物理量,不能描述宏观物体。
2(X)使用物质的量一定要指明具体的微粒。例如1mol氧分子(O2)或1mol氧原子(O)。3(X)摩尔质量不等于质量,摩尔质量的单位是g/mol,质量的单位是g。
4(√)1mol的任何粒子的粒子数都相等,为N A个。
2、知识网络:
3、阿伏加德罗定律
1)同温同压下相同体积的任何气体都具有相同的分子数:PV =nRT
说明:
(1)阿伏加德罗定律依然是忽略了气体分子本身的大小 (2)阿伏加德罗定律比气体摩尔体积的应用更为广泛:
① 主要是应用于不同气体之间的比较,也可以同一种气体的比较 ② 被比较的气体既可以是纯净气体又可以是混合气体 2) 阿伏加德罗定律的重要的四个推论
(1)同温同体积时,任何气体的压强之比都等于其物质的量之比,也等于其分子数之比
2
1
2121N N n n P P == (2)同温同压时,任何气体的体积之比都等于其物质的量之比,也等于其分子数之比
2
1
2121N N n n V V == (3)同温同压同体积时,任何气体的质量之比都等于其摩尔质量之比,也就是其式量之比
2
1
21M M m m = (4)同温同压同体积时,任何气体的密度之比都等于其摩尔质量之比,也就是其式量
之比
2
1
2121M M m m ==ρρ
4、分子量的有关计算
(1)标准状况下mgA 气体的体积为V 升,求A 的相对分子质量M=
4
.22V m
(2)标准状况下A 气体的密度为ρg/L ,求A 的相对分子质量ρ4.22=M 使用说明:
① 适用于所有的物质,不受物质状态的限制,也适用于所有的混合物 ② 所有物质:ρm V M =,标准状况下气体ρ4.22=M
③ 某有机物气体在同温同压下对氢气的相对密度为2.69,求该气体的式量。
2
1
21M M D ==
ρρ 使用说明:
A. 相对密度是在同温同压下两种气体的密度之比
B. 既可以用于纯净气体之间的计算,也可以用于混合气体之间
(3)平均相对分子质量
有a mol A 气体,与b mol B 气体混合,则混合气体的平均式量为 M —
总
总n m =
=
i
i
M n %∑=i
i
M V %∑
5、一定物质的量浓度溶液的配制
C 1V 1=C 2V 2
【课堂练习】 相对原子质量:H-1 C-12 O-16 Na-23 P-31 S-32
一、 选择题
1、用1 g NaOH 固体配制成0.5 mol/L NaOH 溶液,所得溶液的体积是 ( ) A .0.5ml
B .5ml
C .50ml
D .500ml
2、设N A 表示阿伏加得德罗常数的数值,下列叙述中正确的是 ( ) A .1 mol NH 3所含有的原子数为N A
B .常温常压下,22 .4 L 氧气所含的原子数为2N A
C .常温常压下,48 g O 3所含的氧原子数为3N A
D.1 L 0.1 mol/LNaCl溶液中所含的Na+为N A
3、设N A表示阿伏加德罗常数,下列说法正确的是()
A.1 mol氦气中有2N A个氦原子
B.14 g氮气中含N A个氮原子
C.2 L 0.3 mol·L-1 Na2SO4溶液中含0.6 N A个Na+
D.18 g水中所含的电子数为8N A
4、科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同
的是
A.原子数B.分子数C.体积 D.物质的量
5、同温同压下,等质量的下列气体所占有的体积最大的是
A.O2B.CH4C.CO2D.SO2
6、在标准状况下,将某X气体VL溶于水中,得到12mol·L-1的溶液500mL,则气体的体积V是()
A.134.4L B.67.2L
C.44.8L D.537.6L
7、体积为V mL,密度为d g·cm-3的溶液,含有相对分子质量为M的溶质mg,其物质的量浓度为c mol·L-1,质量分数为w,下列表达式正确的是()
A.c=(w×1000×d)/M
B.m=V×d×(w/100)
C.w=(c×M)/(1000×d)%
D.c=(1000×m)/(V×M)
8.在一定温度下,已知有关某饱和溶液的一些数据:①溶液的质量,②溶剂的质量,③溶液的体积,④溶质的摩尔质量,⑤溶质的溶解度,⑥溶液的密度,利用下列各组数据计算该
饱和溶液的物质的量浓度,不能
..算出的一组是()
A.④⑤⑥B.①②③④
C.①④⑥D.①③④⑤
9、一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.1000mol·L -1的NaOH溶液中和相同质量的KHC
O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为
2
KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为()
提示:①H2C2O4是二元弱酸
②10[KHC2O4·H2C2O4]+8KMnO4+17H2SO4===8MnSO4+9K2SO4+40CO2↑+32H2O
A.0.008889 B.0.08000
C.0.1200 D.0.2400
10、下列说法正确的是()
A .1mol 物质的质量叫做摩尔质量
B .两个等容容器,一个盛一氧化氮,另一个盛N 2、H 2混合气,同T 、同P 下两容器内气体原子总数一定相同,分子总数和质子总数也相同
C .将98g H 2SO 4溶于500mL 水中所得到的溶液浓度为2mol/L
D .等质量的O 2和O 3中所含的氧原子数相等
11、同温同压下,A 容器中H 2和B 容器中的NH 3所含氢原子数相等,则两个容器的体积比是 ( )
A .3∶2
B .1∶3
C .2∶3
D .1∶2
12、下列叙述中正确的是 ( )
A .镁的原子质量就是镁的相对原子质量
B .一个氧原子的实际质量约等于16
6.02×1023
g
C .水的相对分子质量等于18g
D .二氧化硫的摩尔质量是64g
13、下列说法正确的是 ( )
A .200mL 1mol/L 的Al 2(SO 4)3溶液中,Al 3+和SO 2-4离子总数为6.02×1023
B .标准状况下,22.4L Cl 2和HCl 的混合气体中含分子总数为2×6.02×1023
C .0.1mol 8135Br 原子中含中子数为3.5×6.02×1023
D .30g 甲醛中含共用电子对总数为4×6.02×1023
14、用N A 表示阿伏加德罗常数,下列叙述中正确的是 ( )
A .100mL 0.1mol/L 的稀硫酸中含有硫酸根的个数为0.1N A
B .1mol CH +
3(碳正离子)中含有电子数10N A
C .2.4g 金属镁与足量的盐酸反应,转移电子数为2N A
D .12.4g 白磷中含有磷原子数为0.4N A 15、由14CO 和12CO 组成的混合气体与同温、同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是 ( )
A .混合气体中14CO 与12
CO 的分子数之比为14∶15 B .混合气体中14CO 与12CO 的物质的量之比为1∶1 C .混合气体中14CO 与12CO 的质量之比为14∶15 D .混合气体中14CO 与12CO 的密度之比为1∶1
16、由CO 、H 2和O 2组成的混合气体,在一定条件下恰好完全反应,测得生成物在101kPa 、120℃下对空气的相对密度为1.293,则原混合气体中H 2所占的体积分数为 ( )
A.16
B.23
C.14
D.13
17、若以ω1和ω2分别表示浓度为a mol·L -1和b mol·L -
1氨水的质量分数,且知2a =b ,则下列推断正确的是(氨水的密度比纯水的小) ( )
A .2ω1=ω2
B .2ω2=ω1
C .ω2>2ω1
D .ω1<ω2<2ω1
18有一稀硫酸和稀硝酸的混合酸,其中H 2SO 4和HNO 3的物质的量浓度分别是4mol/L 和2mol/L ,取10mL 此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO 3被还原成NO) ( )
A .0.448L
B .0.672L
C .0.896L
D .0.224L
二、填空题
固定仪器略),其原理与教材中的实验完全相同。回答下列
问题:
⑴左边大试管中要加入几片碎瓷片,其作用是
;
⑵该装置中使用的玻璃导管较长,其作用是;
⑶烧杯中还要盛有的物质是。
2、为除去粗盐中的Ca2+、Mg2+、Fe3+、SO2-4以及泥沙等杂质,某同学设计了一种制备精盐
的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)判断BaCl2已过量的方法是__________________________________。
(2)第④步中,相关的化学方程式是_______________________________________。
(3)配制NaCl溶液时,若出现下列操作,其结果偏高还是偏低?
A.称量时NaCl已潮解()
B.天平的砝码已锈蚀()
C.定容摇匀时,液面下降又加水()
D.定容时俯视刻度线()
3.现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂出去溶液中的NaCl和Na2SO4,
溶液。相应的实验过程可用下图表示:
从而得到纯净的NaNO3
请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X_________,沉淀A________,沉淀
B___________。
⑵上述实验流程中加入过量的Na2CO3的目的是____________________________
______________________________________________________。
⑶按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________,之后若要获得固体NaNO3需进行的实验操作是___________(填操作名称)。
5、已知标准状况下1体积水溶解了560体积氨气,所得氨水的密度为0.9g/cm3,试求该氨水的质量分数和物质的量浓度。
高一数学必修一知识点整理归纳 【集合与函数概念】 一、集合有关概念 1.集合的含义 2.集合的中元素的三个特性: (1)元素的确定性如:世界上的山 (2)元素的互异性如:由HAPPY的字母组成的集合{H,A,P,Y} (3)元素的无序性:如:{a,b,c}和{a,c,b}是表示同一个集合 3.集合的表示:{…}如:{我校的篮球队员},{太平洋,大西洋,印度洋,北冰洋} (1)用拉丁字母表示集合:A={我校的篮球队员},B={1,2,3,4,5} (2)集合的表示方法:列举法与描述法。 注意:常用数集及其记法:https://www.doczj.com/doc/736286513.html, 非负整数集(即自然数集)记作:N 正整数集:N*或N+ 整数集:Z 有理数集:Q 实数集:R 1)列举法:{a,b,c……} 2)描述法:将集合中的元素的公共属性描述出来,写在大括号内表示集合{x?R|x-3>2},{x|x-3>2} 3)语言描述法:例:{不是直角三角形的三角形}
4)Venn图: 4、集合的分类: (1)有限集含有有限个元素的集合 (2)无限集含有无限个元素的集合 (3)空集不含任何元素的集合例:{x|x2=-5} 二、集合间的基本关系 1.“包含”关系—子集 注意:有两种可能(1)A是B的一部分,;(2)A与B是同一集合。 反之:集合A不包含于集合B,或集合B不包含集合A,记作AB或BA 2.“相等”关系:A=B(5≥5,且5≤5,则5=5) 实例:设A={x|x2-1=0}B={-1,1}“元素相同则两集合相等” 即:①任何一个集合是它本身的子集。AíA ②真子集:如果AíB,且A1B那就说集合A是集合B的真子集,记作AB(或BA) ③如果AíB,BíC,那么AíC ④如果AíB同时BíA那么A=B 3.不含任何元素的集合叫做空集,记为Φ 规定:空集是任何集合的子集,空集是任何非空集合的真子集。 4.子集个数: 有n个元素的集合,含有2n个子集,2n-1个真子集,含有2n-1个非空子集,含有2n-1个非空真子集 三、集合的运算 运算类型交集并集补集 定义由所有属于A且属于B的元素所组成的集合,叫做A,B的交集.记作AB(读作‘A交B’),即AB={x|xA,且xB}.
第一章.运动的描述 基础知识点归纳 1.质点(A )(1)没有形状、大小,而具有质量的点。 (2)质点是一个理想化的物理模型,实际并不存在。 (3)一个物体能否看成质点,并不取决于这个物体的大小,而是看在所研究的问题中物体的 形状、大小和物体上各部分运动情况的差异是否为可以忽略的次要因素,要具体问题具体分析。 2.参考系(A )(1)物体相对于其他物体的位置变化,叫做机械运动,简称运动。 (2)在描述一个物体运动时,选来作为标准的(即假定为不动的)另外的物体,叫做参考系。 对参考系应明确以下几点: ①对同一运动物体,选取不同的物体作参考系时,对物体的观察结果往往不同的。 ②在研究实际问题时,选取参考系的基本原则是能对研究对象的运动情况的描述得到尽量的简化,能够使解题显得简捷。 ③因为今后我们主要讨论地面上的物体的运动,所以通常取地面作为参照系 3.路程和位移(A ) (1)位移是表示质点位置变化的物理量。路程是质点运动轨迹的长度。 (2)位移是矢量,可以用以初位置指向末位置的一条有向线段来表示。因此,位移的大小等于物体 的初位置到末位置的直线距离。路程是标量,它是质点运动轨迹的长度。因此其大小与运动路径有关。 (3)一般情况下,运动物体的路程与位移大小是不同的。只有当质点做单一方向的直线运动时,路 程与位移的大小才相等。图1-1中质点轨迹ACB 的长度是路程,AB 是位移S 。 ( 4)在研究机械运动时,位移才是能用来描述位置变化的物理量。路程不能用来表达物体的确切位 置。比如说某人从O 点起走了50m 路,我们就说不出终了位置在何处。 4、速度、平均速度和瞬时速度(A ) (1)表示物体运动快慢的物理量,它等于位移s 跟发生这段位移所用时间t 的比值。即v=s/t 。速度 是矢量,既有大小也有方向,其方向就是物体运动的方向。在国际单位制中,速度的单位是(m/s )米/秒。 (2)平均速度是描述作变速运动物体运动快慢的物理量。一个作变速运动的物体,如果在一段时间t 内的位移为s, 则我们定义v=s/t 为物体在这段时间(或这段位移)上的平均速度。平均速度也是矢量,其方向就是物体在这段时间内的位移的方向。 (3 )瞬时速度是指运动物体在某一时刻(或某一位置)的速度。从物理含义上看,瞬时速度指某一 时刻附近极短时间内的平均速度。瞬时速度的大小叫瞬时速率,简称速率 5、匀速直线运动(A ) (1) 定义:物体在一条直线上运动,如果在相等的时间内位移相等,这种运动叫做匀速直线运动。 根据匀速直线运动的特点,质点在相等时间内通过的位移相等,质点在相等时间内通过的路程相等,质点的运动方向相同,质点在相等时间内的位移大小和路程相等。 (2) 匀速直线运动的x —t 图象和v-t 图象(A ) (1)位移图象(x-t 图象)就是以纵轴表示位移,以横轴表示时间而作出的反映物体运动规律的数学图象,匀速直线运动的位移图线是通过坐标原点的一条直线。 B A B C 图1-1
第1课从内外服联盟到封邦建国 知识结构: 1.夏:出现公共权力,但保留氏族公社特点。 2.商:政治制度是内服与外服制度,具有浓厚的神权色彩。 3.西周: 分封制定义: 目的:巩固周的统治(奴隶主的统治 主体:同姓亲族 宗法制目的:巩固分封制形成的统治秩序,解决贵族之间在权力、财产和土地继承上的矛盾。 核心:嫡长子继承制 内容:确立大宗、小宗体系 作用:利于凝聚宗族,防止内部纷争,强化王权 工具:礼乐制度 第2课中央集权制度的确立 知识结构: 1.统一 (1群雄割据 A.春秋争霸 B.战国变法:秦国商鞅变法。 (2统一:时间:前221年;人物:赢政。 2、中央集权的确立
(1确立: A. “皇帝制”:皇权至上、皇位继承制 B. 三公九卿制:三公是丞相、御史大夫、太尉(中央 C. 郡县制(地方 (2加强皇权的措施:制定官吏选拔和考核制度;制定细苛、严密的法律。 (3影响:打破分封制,奠定大一统王朝制度基础。 第3课中央集权与地方分权的斗争 知识结构: 1. 汉初郡国并行,导致诸候尾大不掉,引发七国之乱。 2. 汉武帝集权措施:建中朝、设刺史、颁布推恩令。 3. 藩镇割据与五代十国:唐朝中后期,地方势力增强,出现藩镇割据局面;唐灭亡后,中国进入五代十国的分裂时期,五代十国是藩镇割据的继续和发展;这一时期,南方经济得到较大发展;后周世宗改革,为北宋结束五代十国分裂局面奠定了基础。 4. 宋加强中央集权 (1措施①收精兵:“三衙”、枢密院、原则; ②削实权:设通判、文臣任州郡长官; ③制钱谷:财赋大部分运往京师; (2影响利:改变藩镇割据分裂局面,加强中央集权; 弊:造成“积贫积弱”的后患。 第4课专制皇权的不断加强
第一单元物质的量(一) 教学目的 1.使学生初步理解摩尔的意义,了解物质的微粒数、物质的质量、摩尔质量之间的关系,了解摩尔质量与式量的联系与区别,并能较熟练地进行摩尔质量的计算。 懂得阿伏加德罗常数的涵义。 2.了解引进摩尔这一单位的重要性和必要性, 3.培养学生演绎推理、归纳推理和运用化学知识进行计算的能力。 教学重难点1.对摩尔概念的内涵的理解; 2.运用摩尔进行有关计算。 教学过程 讲授新课 点燃 引入:问学生反应 C + O2 ===== CO2所表达的意义? 一个碳原子一个氧分子一个二氧化碳分子 -------微观粒子(1)在实验室里,拿一个原子和一个分子反应,容易做到吗? 一般用质量:1克 1克 2克是否容易做到呢? 反应是按比例: 12克 32克 44克 --------宏观质量 (2)怎样知道一定质量的物质里含有多少个微粒? (3)微观粒子和宏观质量之间有什么联系?科学家统一确定了一个新的 物理量-----物质的量,它将微粒与质量联系起来了。 【板】一、物质的量: 【投影】物理量单位符号 长度米 m 质量千克 Kg 时间秒 s 电流安培 A 热力学温度开尔文 K 发光强度坎德拉 cd 物质的量摩尔(mol) n 学生阅读:摩尔的概念。(请看书本第6页最后一节。) 分析讲解:(比喻)一打铅笔---12支;一箱易拉罐可乐---24瓶;一盒粉笔---50支。 为什么要定12克---数值与原子量同阿伏加德罗常数 12克C-12 所含原子数。 学生计算得出NA--- 12/1.997×10-26 6.02×1023 阿伏加德罗常数(精确值)与6.02×1023(近似值)的关系就象π与3.14一样。 引导学生看书:P7(图1-5)1摩尔碳;1摩尔硫;1摩尔P;1摩尔K2Cr2O7的体积。 【提问1】1摩尔金刚石约含碳原子数?1摩尔O2中约含分子数?1摩尔H2O中约含分子数?【板】1、物质的量:表示物质微粒集体的物理量。 2、摩尔(mol):物质的量的单位。简称摩,符号为mol。 3、阿伏加德罗常数:6.02×1023mol-1 (近似值) 【强调】使用摩尔应注意:1摩尔碳原子约含有6.02×1023个碳原子。 每摩尔碳原子含有阿伏加德罗常数个碳原子。 【提问2】1摩尔氯气中含有多少个微粒?个氯分子。 【强调】一般说多少摩尔物质,指的是构成该物质的微粒。
第一章丰富的图形世界知识点总结 本章可分为三大板块 第一大板块常见几何体的性质与分类 1、常见几何体:圆柱、棱柱(长方体、正方体)、棱锥、圆锥、球体。 2、性质:底面的个数与形状、侧面的个数与形状、是否含有曲面。 3、分类依据:底面数(柱体、椎体、球体);是否含有曲面;是否含有顶点等。总结时注意类比与对比。 4、棱体(棱锥)的命名以及N棱柱棱数、面数、顶点数求法(尝试总结N棱锥的棱数、面数、顶点数)。简单逆向思维应用,根据棱数、面数、顶点数判断是何种几何体(注意数学思想之分类讨论)。 第二大板块常见几何体的组成与形成 1、组成:点、线、面。 面与面相交得到线,线与线相交得到点。点动成线,线动成面,面动成体。 能说出常见几何体中侧面与底面相交得到几条线,分别是什么形状。顶点处有几条棱,几个面。 2、形成:面的旋转。常见几何体可以看作哪些平面图形旋转得到。 第三大板块体与面之间的转化关系(体会数学思想之转化化归思想)。 1、展开与折叠: 一般几何体的展开与折叠,展开时注重动手操作到空间想象的转变,折叠时注意结合几何体的性质来判断。 正方体的展开与折叠,对展开图的观察总结,掌握对面、邻面以及有共同顶点的几个面在展开图中的关系,并能利用逆向思维还原。 截面:截面的形成(面截体),截面的本质(面截面所得线围成的平面)。 正方体、圆柱、圆锥等所能得到的截面类型并能通过空间想象做出截面,逆向思维通过截面判断是由什么几何体截得。 2、三视图:主视图(长与高)、左视图(宽与高)、俯视图(长与宽) 会画单独几何体和简单组合体的三视图(长对正、宽相等、高平齐)。简单应用之求组合体面积。 根据数字俯视图画出主视图与俯视图(答案唯一),体会三视图之间的联系。 逆向思维根据三视图还原几何体(理解答案不唯一),从而得到简单应用之根据三视图推测组合体中小方块数目。 本章贯穿的几大思维: 逆向思维 形象思维到抽象思维 转化的思维 学习方法 通过动手操作培养空间想象‘
高中地理必修一知识点总结完整版 第一部分地球的宇宙环境 ★考点1:了解不同级别的天体系统,说明地球在太阳系中的位置。 (1)天体系统的含义:宇宙中的各种天体之间相互吸引、相互绕转,形成天体系统。 (2)天体系统由高到低的层次: (3)地球在太阳系中的位置: 太阳系成员:太阳、行星及卫星、小行星、彗星、流星体、行星际物质;中心天体是太阳。八大行星按距日由近到远依次是水星、金星、地球、火星、木星、土星、天王星、海王星。 ★考点2:知道地球是太阳系中一颗既普通又特殊的行星,理解地球上存在生命的条件。 (1)普通性体现在: ①八大行星绕日公转运动的特征:同向性、共面性、近圆性; ②八大行星根据距日远近、质量、体积等特征分为三类:类地行星(水星、金星、地球、火星)、巨行星(木星、土星)、远日行星(天王星、海王星) (2)特殊性体现在:地球存在生命物质 ★考点3:了解太阳辐射对地球的影响。 (1)太阳直接为地球提供了光、热资源,地球上生物的生长发育离不开太阳。
(2)太阳辐射能维持着地表温度,是促进地球上的大气、水运动和生物活动的主要动力。 (3)为人类生产、生活提供直接和间接的能源。(石油、天然气).太阳辐射影响因素(三个) 我国太阳能资源分布特点及原因 太阳能风能开发条件评价 能源丰富,市场大小距离,资金,技术,政策 新能源的优点:清洁无污染,可再生。缺点:能量密度小,变化大不稳定。 ★考点4:了解太阳活动对地球的影响。 (1)太阳大气层由内至外可以分为光球、色球、日冕层。 (2)太阳活动最主要的类型是黑子和耀斑,分别出现在太阳大气层的光球和色球,其活动的平均周期为11年。 (3)太阳活动对地球的影响主要有: ①影响无线电短波信号,导致通讯衰减或中断。②产生“磁暴”现象,指南针不能正确指示方向。③两极地区高空大气产生极光现象。④地球上许多自然灾害的发生与太阳活动有相关性。 ★考点5:知道地球自转和公转的方向、周期和速度 ★考点6:理解昼夜更替和地方时产生的原因,能够进行简单的区时计算。 (1)昼夜更替现象产生的原因:地球是不透明的球体,因此有昼半球和夜半球之分;地球持续不停地自转,因此昼、夜半球所处部分不停地变化,就有了昼夜更替现象。昼夜更替的周期是1个太阳日。(2)地方时产生的原因:地球自转使得同纬度地区不同地点见到太阳的时刻会有早晚。地方时的确定与经度的对应关系:太阳直射的那条经线地方时为12点,晨线与赤道相交点所在经线的地方时为6点,昏线与赤道相交点所在经线的地方时为18点。同一条经线上的地方时相同,经线(经度)不同地方时不同。经度每隔15°,地方时相差1小时;经度每隔1°,地方时相差4分钟。 (3)时区与区时 时区:为了统一标准,国际上把经度15°划分为一个时区,全球划分为24个时区。
物质的量讲义 (一) 一、概念 1.物质的量 (1)概念:表示物质所含微粒数目多少的物理量 (2)符号:n (3)单位:摩尔(mol) 2.摩尔 (1)概念:摩尔是物质的量的单位,每1mol物质含有阿伏加德罗常数个结构微粒。 (2)符号:mol (3)说明:①必须指明物质微粒的名称,不能是宏观物质名称,例:不能说1摩氢、1摩氧,因这样说指哪种微粒不明确。 ②常见的微观粒子有:分子、原子、离子、电子、质子、中子或它们特定的组合 ③当有些物质的微观粒子只有一种时,可以省略其名称 3.阿伏加德罗常数 (1)含义:实验测定12g12C中碳原子的个数 (2)符号:N A (3)单位:个/mol (4)说明:①N A的基准是12g碳-12中的原子个数 ②12C不仅是摩尔的基准对象,而且还是相对原子质量的基准 ③N A是一个实验值,现阶段常取6.02×1023作计算 ④要注意N A与6.02×1023的区别 4.摩尔质量 (1)概念:单位物质的量的物质的质量 (2)符号:M (3)单位:g·mol-1 (4)说明:①使用范围:A.任何一种微观粒子 B.无论是否纯净 C.无论物质的状态 ②与式量的比较:式量无单位 ③与1mol物质的质量的比较: 5.气体摩尔体积 (1)概念:单位物质的量的气体的体积 V (2)符号: m (3)单位:L·mol-1 (4)标准状况下的气体摩尔体积 ①标准状况:0℃、1atm即1.01×105Pa ②理想气体:A.不计大小但计质量 B.不计分子间的相互作用 ③标准状况下的气体摩尔体积:约22.4L·mol-1 (5)影响物质体积大小的因素: ①构成物质的微粒的大小(物质的本性) ②结构微粒之间距离的大小(温度与压强来共同决定) ③结构微粒的多少(物质的量的大小) 6.物质的量浓度 (1)概念:用单位体积的溶液中溶解溶质的物质的量的多少来表示溶液的浓度 (2)符号:c (3)单位:mol·L-1
第一章有理数 思维路径: 有理数 数轴 运算 (数) (形) 1.有理数: (1)凡能写成)0p q ,p (p q ≠为整数且分数形式的数,都是有理数,整数和分数统称有理数. ▲注意:0即不是正数,也不是负数;-a 不一定是负数,+a 也不一定是正数;π不是有理数; (2)有理数的分类: ① ??? ??????????负分数负整数负有理数零正分数正整数正有理数有理数 ② ???????????????负分数正分数分数负整数零正整数整数有理数 (3)自然数? 0和正整数; a >0 ? a 是正数; a <0 ? a 是负数; a ≥0 ? a 是正数或0 ? a 是非负数;▲ a ≤ 0 ? a 是负数或0 ? a 是非正数. 2.数轴:数轴是规定了原点、正方向、单位长度(数轴的三要素)的一条直线. 3.相反数:
(1)只有符号不同的两个数,我们说其中一个是另一个的相反数;0的相反数还是0; (2)注意: a-b+c 的相反数是-(a-b+c)= -a+b-c ; a-b 的相反数是b-a ; a+b 的相反数是-a-b ; (3)相反数的和为0 ? a+b=0 ? a 、b 互为相反数. (4)相反数的商为-1. (5)相反数的绝对值相等 4.绝对值: (1)正数的绝对值等于它本身,0的绝对值是0,负数的绝对值等于它的相反数; 注意:绝对值的意义是数轴上表示某数的点离开原点的距离; (2) 绝对值可表示为:?????<-=>=) 0a (a )0a (0)0a (a a 或 ???≤-≥=)0()0(a a a a a ; (3) 0a 1a a >?= ; 0a 1a a
第一章集合与函数概念 课时一:集合有关概念 1.集合的含义:集合为一些确定的、不同的东西的全体,人们能意识到这些东 西,并且能判断一个给定的东西是否属于这个整体。 2.一般的研究对象统称为元素,一些元素组成的总体叫集合,简称为集。 3.集合的中元素的三个特性: (1)元素的确定性:集合确定,则一元素是否属于这个集合是确定的:属于或不属于。 例:世界上最高的山、中国古代四大美女、教室里面所有的人…… (2)元素的互异性:一个给定集合中的元素是唯一的,不可重复的。 例:由HAPPY的字母组成的集合{H,A,P,Y} (3)元素的无序性:集合中元素的位置是可以改变的,并且改变位置不影响集合 例:{a,b,c}和{a,c,b}是表示同一个集合 3.集合的表示:{…} 如:{我校的篮球队员},{太平洋,大西洋,印度洋,北冰洋} (1)用大写字母表示集合:A={我校的篮球队员},B={1,2,3,4,5} (2)集合的表示方法:列举法与描述法。 1)列举法:将集合中的元素一一列举出来 {a,b,c……} 2)描述法:将集合中元素的公共属性描述出来,写在大括号内表示集合。 {x R| x-3>2} ,{x| x-3>2} ①语言描述法:例:{不是直角三角形的三角形} ②Venn图:画出一条封闭的曲线,曲线里面表示集合。 4、集合的分类: (1)有限集:含有有限个元素的集合 (2)无限集:含有无限个元素的集合 (3)空集:不含任何元素的集合例:{x|x2=-5} 5、元素与集合的关系: (1)元素在集合里,则元素属于集合,即:a A (2)元素不在集合里,则元素不属于集合,即:a A 注意:常用数集及其记法: 非负整数集(即自然数集)记作:N 正整数集 N*或 N+ 整数集Z 有理数集Q 实数集R
高一化学第一章计算能力题专项训练 一:单项选择: 1、下列溶液中,物质的量浓度为1mol/L 的是() A.将40gNaOH溶于1L水所得的溶液B.将80gSO3溶于水并配成1L的溶液 C.将0.5mol/LNaNO3溶液100ml 加热蒸发掉50g 水的溶液 D.含K+2mol 的K2SO4溶液2L 2、下列条件下,两瓶气体所含原子数一定相等的是()A.同质量,不同密度的N2和CO B.同温度,同体积的H2和N2 C.同体积,同密度的C2H4和C2H6 D.同压强,同体积的N2O和CO2 3、一定量的质量分数为14%的KOH 溶液,若将其蒸发掉50g水后,其溶质质量分数恰好扩大一倍,体积变为62.5ml,则浓缩后溶液的物质的量浓度为() A.2.2mol/L B.4.0mol/L C.5.0mol/L D.6.25mol/L 4、标准状况下的aLHCl(g)溶于1000g 水中,得到的盐酸密度为bg/cm3,则该盐酸的物质的量浓度是() A.a /22.4 mol/L B.ab/22400 mol/L C.ab/(22400+36.5a ) mol/L D.1000ab/(22400+36.5a) mol/L 5、在标准状况下,与12gH2的体积相等的N2的() A.质量为12g B.物质的量为6mol C.体积为22.4L D.物质的量为12mol 6、两个体积相同的容器,一个盛有NO,另一个盛有N2 和O2,在同温、同压下,两容器内的气体一定具有相同的() A.原子总数B.氧原子数C.氮原子数D.质量 7、在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g。此混合气体中C和O 两种原子的物质的量之比() A.3:4 B.4:3 C.2:1 D.1:2 8、20gA 物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD 物质和0.2molE 物质,则E 物质的摩尔质量为() A.100 g/mol B.108 g/mol C.55 g/mol D.96 g/mol 9、实验室里需用480mL0.1 mol/L 的硫酸铜溶液,现选用500mL 容量瓶进行配制,以下操作正
高中语文必修一知识点归纳总结 1、字音:沁(qǐn)园春百舸(gě)峥(zhēng)嵘寥廓(kuò)挥斥方遒(qíu)漫(màn)江携(xié)来浪遏(è)飞舟 2、词义: 峥嵘:本义形容山势高峻突出,引申为不平常。 挥斥方遒:热情奔放,劲头十足。遒,强劲有力。 激扬:激浊扬清,批评坏的,褒扬好的。 3、近义词辨析: 寥廓:(天空)高原空旷。 辽阔:(土地海洋等)辽远广阔。 意气:意志和气概,志趣和性格。也指因主观偏激而产生的情绪,如意气用事。 义气:由于私人关系而甘于承担风险或牺牲自己利益的气概。如讲义气。 遏制:制止,控制(一般只能是一定程度上的效果)。 遏止:用力阻止住。如滚滚洪流,不可遏止。 4、文学常识: 1字音:彷(páng)徨寂寥(liáo)惆怅(chàng)凄婉(wǎn)颓圮(pǐ) 青荇(xǐng)浮藻(zǎo)长篙(gāo)漫溯(sù)斑斓(lán)笙(shēng)箫 2、词义: 彷徨:(心事重重)地走来走去,犹疑不决。
颓圮:坍塌,毁坏。 3、近义词辨析: 沉淀:指沉到溶液底层的难以溶解的物质,比喻凝聚,积累。 积淀:指长时间积累起来的习俗、文化。 彷徨:犹疑不决的走来走去。 倘佯:自由自在地走来走去。 4、文学常识: 徐志摩(1896-1931),笔名云中鹤、南湖,浙江海宁人。诗人、 学者。新月社的主要发起人和主要成员之一。诗集有《志摩的诗》《翡冷翠的一夜》《猛虎集》等,名篇有《再别康桥》《沙扬娜拉》《在病中》等。 一、通假字 1、无能为也已(矣) 2、共其乏困(供) 3、秦伯说,与郑人盟(悦) 4、失其所与,不知(智) 5、何厌之有(餍) 6、若不阙秦(缺) 二、古今异义(古/今) 1、贰于楚也(从属二主、有二心/数词二的大写) 2、以为东道主(东方道路上的主人/泛指主人) 4、今有急而求子(您,多指男子/儿子) 5、越国以鄙远(边远的地方/粗鄙、低下) 6、以烦执事(婉指秦穆公/掌管某事的人) 7、亦去之(离开、距离/到达) 8、微夫人之力(那个人/尊称人的妻子) 三、词类活用 (一)名词作动词
高中必修一到必修五主要语法点 必修一:直接引语和间接引语(宾语从句);现在进行时表将来;定语从句 必修二:定语从句(非限定定从、定从中的介词前提);被动语态(一般将来时、现在完成时及现在进行时的被动语态) 必修三:情态动词;名词性从句(主语从句、宾语从句、表语从句及同位语从句) 必修四:主谓一致;非谓语动词(V-ing) ;构词法 必修 2 第一单元,非限制性定语从句的第二单元一般将来时的主被动第三单元现在完成时的主被动第四单元 现在进行时的主被动第五单元介词+which/whom的用法 必修 3 一二单元情态动词的用法三单元宾语从句和表语从句四单元主语从句 五单元同位语从句 必修4 第一单元主谓一致第二单v-ing作主语和宾语的用法第三单元v-ing作表语,定语和宾语补足语第四单 元v-ing作状语第五单元构词法 必修5 第一单元过去分词作定语和表语第二单元过去分词作宾语补足语第三单元过去分词作状语第四单元 倒装句第五单元省略句 必修一各单元知识点总结 Unit One Friendship 一、重点短语 1.go through 经历,经受get through 通过;完成;接通电话 2. set down 记下,放下 3. a series of 一系列 4 on purpose 有目的的 5. in order to 为了 6. at dusk 傍晚,黄昏时刻 7. face to face 面对面 8. fall in love 爱上 9. join in 参加(某个活动);take part in 参加(活动) join 加入(组织,团队,并成为其中一员) 10. calm down 冷静下来 11. suffer from 遭受 12. be/get tired of…对…感到厌倦 13. be concerned about 关心 14. get on/along well with 与…相处融洽 15. be good at/do well in 擅长于… 16. find it + adj. to do sth. 发现做某事是…
高一化学第一章计算能力题专项训练 一:单项选择: 1 、下列溶液中,物质的量浓度为 1mol/L 的是( ) A. 将40gNaOH 溶于1L 水所得的溶液 B .将80gS θ3 溶于水并配成1L 的溶液 C.将0.5mol∕LNaNO 3溶液IOOmI 加热蒸发掉 50g 水的溶液 D .含 K +2moI 的 K 2SO 4 溶液 2L 2、 下列条件下,两瓶气体所含原子数一定相等的是( ) A. 同质量,不同密度的 N 2和CO B.同温度,同体积的 H 2 和N 2 C.同体积,同密度的 C 2H 4和C 2H 6 D.同压强,同体积的 N 2O 和CO 2 3、 一定量的质量分数为 14% 的 KOH 溶液, 若将其蒸发掉 5Og 水后, 其溶质质量分数恰好扩 大一倍,体积变为 62.5ml ,则浓缩后溶液的物质的量浓度为( ) A. 2.2mol∕L B . 4.Omol∕L C . 5.Omol∕L D . 6.25mol∕L 4、 标准状况下的 aLHCl ( g )溶于1000g 水中,得到的盐酸密度为 bg/cm 3,则该盐酸的物质 的量浓度是( ) A. a /22.4 mol/L B . ab/224OO mol/L D . 1OOOab/(224OO+36.5a) mol/L 5、在标准状况下,与 12gH 2的体积相等的N 2的( ) A. 质量为12g B .物质的量为6mol C .体积为22.4L 的气体一定具有相同的( ) A .原子总数 B ?氧原子数 C 氮原子数 D ?质量 7、在标准状况下,由 CO 和CO 2组成的混合气体13.44L ,质量为20g 。此混合气体中C 和O 两种原子的物质的量之比( ) A . 3:4 B . 4:3 C . 2:1 D . 1:2 8、 2OgA 物质和 14gB 物质恰好完全反应,生成 8.8gC 物质、 3.6gD 物质和 O.2molE 物质, 则 E 物质的摩尔质量为( ) A . 1OO g/mol B . 1O8 g/mol C . 55 g/mol D . 96 g/mol 9、实验室里需用 48OmLO.1 mol/L 的硫酸铜溶液,现选用 5OOmL 容量瓶进行配制,以下操 作正确的是( ) A .称取7.68g 硫酸铜,配成 500mL 溶液 B .称取12.0g 胆矶,配成500mL 溶液 C.称取8.0g 硫酸铜,加入 500mL 水 D .称取12.5g 胆矶,配成500mL 溶液 C . ab/(224OO+36.5a ) mol/L D .物质的量为 12mol 6、两个体积相同的容器,一个盛有 NO ,另一个盛有 N 2和O 2,在同温、同压下,两容器内
高一数学必修1第一章知识点总结 一、集合有关概念 1.集合的含义 2.集合的中元素的三个特性: (1)元素的确定性, (2)元素的互异性, (3)元素的无序性, 3.集合的表示:{ …} 如:{我校的篮球队员},{太平洋,大西洋,印 度洋,北冰洋} (1)用拉丁字母表示集合:A={我校的篮球队员},B={1,2,3,4,5} (2)集合的表示方法:列举法与描述法。 注意:常用数集及其记法: 非负整数集(即自然数集)记作:N 正整数集N*或N+ 整数集Z 有理数集Q 实数集R 1)列举法:{a,b,c……} 2)描述法:将集合中的元素的公共属性描述出来,写在大括号内表示集合的方法。{x∈R| x-3>2} ,{x| x-3>2} 3)语言描述法:例:{不是直角三角形的三角形} 4)Venn图: 4、集合的分类: (1)有限集含有有限个元素的集合 (2)无限集含有无限个元素的集合 (3)空集不含任何元素的集合例:{x|x2=-5} 二、集合间的基本关系 1.“包含”关系—子集 A?有两种可能(1)A是B的一部分,;(2)A与B是注意:B 同一集合。 反之: 集合A不包含于集合B,或集合B不包含集合A,记作A?/B或B?/A 2.“相等”关系:A=B(5≥5,且5≤5,则5=5) 实例:设A={x|x2-1=0} B={-1,1} “元素相同则两集合相等”即:①任何一个集合是它本身的子集。A?A ②真子集:如果A?B,且A≠B那就说集合A是集合B的真子集,记
作A B(或B A) ③如果A?B, B?C ,那么A?C ④如果A?B 同时B?A 那么A=B 3. 不含任何元素的集合叫做空集,记为Φ 规定: 空集是任何集合的子集,空集是任何非空集合的真子集。 有n个元素的集合,含有2n个子集,2n-1个真子集 运算 类型 交集并集补集 定义由所有属于A且属 于B的元素所组成 的集合,叫做A,B的 交集.记作A B (读作‘A交B’), 即A B={x|x∈A, 且x∈B}. 由所有属于集合A或 属于集合B的元素所 组成的集合,叫做A,B 的并集.记作:A B (读作‘A并B’), 即A B ={x|x∈A, 或x∈B}). 设S是一个集合,A是 S的一个子集,由S中 所有不属于A的元素 组成的集合,叫做S中 子集A的补集(或余 集) 记作A C S ,即 C S A=} , |{A x S x x? ∈且 韦恩图示A B 图1 A B 图2 S A
高一语文必修一知识点总结: 第一单元 1 《沁园春》 重要字音:沁(qǐn)园春百舸(gě) 峥(zhēng)嵘寥廓(kuò)挥斥遒(qíu) 漫(màn)江携(xié)来浪遏(è)飞舟 多音字:汗水可汗数字数典忘祖数见不鲜 重要字形:沁香分泌谩骂漫江惆怅为虎作伥苍茫沧桑阻遏碣 重要词义:峥嵘:本义形容山势高峻突出,引申为不平常。 挥斥遒:热情奔放,劲头十足。遒,强劲有力。 激扬:激浊扬清,批评坏的,褒扬好的。 近义词辨析: 寥廓:(天空)高原空旷。辽阔:(土地海洋等)辽远广阔。
意气:意志和气概,志趣和性格。也指因主观偏激而产生的情绪,如意气用事。 义气:由于私人关系而甘于承担风险或牺牲自己利益的气概。如讲义气。 遏制:制止,控制(一般只能是一定程度上的效果)。遏止:用力阻止住。如滚滚洪流,不可遏止。 2.《诗两首》 重要字音:彷(páng)徨寂寥(liáo) 惆怅(chàng)凄婉(wǎn)颓圮(pǐ)青荇(xǐng) 浮藻(zǎo)长篙(gāo) 漫溯(sù)斑斓(lán) 笙(shēng)箫 多音字:看守看见遒劲有劲着迷执著装载记载悄悄悄然重要字形:彷徨惶然惋惜哀婉彷徨牌坊惆怅稠密丝绸追溯朔风挑衅河畔斑斓无耻谰言波澜颓圮祭祀杞人忧天重要词义:彷徨:(心事重重)地走来走去,犹疑不决。颓圮:坍塌,毁坏。 近义词辨析: 沉淀:指沉到溶液底层的难以溶解的物质,比喻凝聚,积累。
积淀:指长时间积累起来的习俗、文化。 彷徨:犹疑不决的走来走去。倘佯:自由自在地走来走去。 3.《大堰河——我的保姆》 【基础知识】 重要字音:青苔(tāi)荆棘(jí)火钵(bō)忸(niǔ)怩麦糟(zāo) 炖(dùn) 肉 团箕(jī) 凌侮(wǔ) 叱(chì)骂 多音字:瓦菲菲薄泥巴拘泥漂泊湖泊青苔舌苔 重要字形:碾碎辗转堤堰揠苗助长偃旗息鼓凌侮陵墓棱角忸怩纽扣枢纽 重要词义:典押:把土地和房屋押给别人,换取一笔,到期还款,收回原物。 天伦:指父子、兄弟等关系。瓦菲:生长在瓦缝中的野草。凌侮:欺凌,侮辱。 近义词辨析:养育:抚养和教育。养活:供给东西使生活。 第二单元(《烛之武退师》《荆轲刺》《鸿门宴》)
第一章 电场基本知识点总结 (一)电荷间的相互作用 1.电荷间有相互作用力,同种电荷互相排斥,异种电荷相互吸引,两电荷间的相互作用力大小相等,方向相反,作用在同一直线上。 2.库仑定律:在真空中两个点电荷间的作用力大小为F= kQ1Q2/r2, 静电力常量k=9.0×109N ·m2/C2。 (二)电场强度 1.定义式:E=F/q ,该式适用于任何电场. E 与 F 、q 无关只取决于电场本身,与密度ρ类似,密度ρ定义为V m =ρ ,而ρ与m 和V 均无关,只与物质本身的性质有关. (1)场强E 与电场线的关系:电场线越密的地方表示场强越大,电场线上每点的切线方向表示该点的场强方向,电场线的方向与场强E 的大小无直接关系。 (2)场强的合成:场强E 是矢量,求合场强时应遵守矢量合成的平行四边形法则。 (3)电场力:F=qE ,F 与q 、E 都有关。 2.决定式 (1)E=kQ/ r2,仅适用于在真空中点电荷Q 形成的电场,E 的大小与Q 成正比, 与r2成反比。 (2)E=U/d ,仅适用于匀强电场。 d 是沿场强方向的距离,或初末两个位置等势面 间的距离。 3.电场强度是矢量,其大小等于F 与q 的比值,反映电场的强弱; 其方向规定为正电荷受力的方向. 4. 电场强度的叠加是矢量的叠加 空间中若存在着几个电荷,它们在P 点都激发电场,则P 点的电场为这几个电荷单独 在P 点产生电场的场强的矢量合. (三)电势能 1.电场力做功的特点:电场力对移动电荷做功与路径无关,只与始末位的电势差有关,Wab=qUab 2.判断电势能变化的方法 (1)根据电场力做功的正负来判断,不管正负电荷,电场力对电荷做正功,该电荷的 电势能一定减少;电场力对电荷做负功,该电荷的电势能一定增加。 (2)根据电势的定义式U=ε/q 来确定。 (3)利用W=q(Ua-Ub)来确定电势的高低 (四)电势与电势差 1.电场中两点间的电势差公式(两个):U AB =W AB /q ;U AB = 2、电场中某点的电势公式: =W A ∞/q = E A (电势能)/ q (五)静电平衡 把金属导体放入电场中时,导体中的电荷重新分布,当感应电荷产生的附加电场E '与原场强E0叠加后合场强E 为零时,即E= E0 +E '=0,金属中的自由电子停止定向移B A ??-A ?A ?
有关物质的量的计算知识点总结 1.物质的量 (1)定义:物质的量是量度一定量粒子的集合体中所含粒子数量的物理量。符号为n ,它是把微观粒子与宏观可称量物质联系起来的一种物理量。是国际单位制中规定的7个基本物理量之一。说明:物质的量是描述物质属性的一个物理量,与质量长度等一样。 (2)物质的量的单位:摩尔,简称摩,符号为mol 适用对象:“摩尔”这个单位不适用于宏观物理,只适用于微观粒子,如,分子、原子、离子、质子、中子、电子等以及他们的特定组合(缔合分子、原子团、官能团等)说明:使用摩尔量度微观粒子时,一定要指明微粒的种类,一般加化学式或微粒符号。如1molS 是正确的,但1mol 氢是错误的。 好多学生不理解物质的量的概念,在授课过程中要注意语言简洁,不用冗余的语言去解释它的概念。 2.阿伏加德罗常数 (1)定义:国际上规定1mol 任何粒子集合体所含的粒子数,称为阿伏加德罗常数,其准确数值与0.012kg 12C 中所含原子数相同,约为6.02×1023。 (2)表示:用符号N A 来表示,同上使用6.02×1023mol -1这个近似值表示,单位mol -1。 (3)物质的量(n )与粒子数(N )、阿伏加德罗常数(N A )之间的关系: A A nN N N N n ==, 3.摩尔质量 (1)定义:单位物质的量的物质所具有的质量,符号M ,常用单位g/mol 或g.mol -1,具体物质的物质的量为常数,不随物质的量的多少而改变。 说明:表示某物质的摩尔质量时,要指明具体粒子种类。如,氮分子(原子)的摩尔质量是正确的,但氮的摩尔质量是错误的。 (2)任何微粒的摩尔质量若以“g/mol ”为单位时,在数值上等于其相对原子(分子)质量,但二者单位不同。 (3)摩尔质量与物质的量之间的关系 物质的质量(m )、物质的量(n )、摩尔质量(M )之间的关系: n m N M m n ==, 4.气体摩尔体积 (1)定义:单位物质的量的气体所占的体积叫作气体摩尔体积。
第一单元 1、揭开货币的神秘面纱 1、商品 ①含义:用于交换的劳动产品 ②基本属性:使用价值(商品能够满足人们某种需要的属性)和价值(凝结在商品中的无差别的人类劳动) 2、货币的含义及本质 ①含义:从商品中分离出来固定充当一般等价物的商品(所以说货币是商品交换发展到一定阶段的产物) ②本质:一般等价物含义:货币具有表现和衡量其他一切商品价值大小的职能 3、货币的职能 (1)基本职能 ①价值尺度原因:货币本身有价值形式:观念上的货币含义:货币充当商品交换媒介的职能 ②流通手段形式:现实的货币商品流通:以货币为媒介的商品交换,公式是W-G-W (2)其他职能:贮藏手段、支付手段、世界货币 4、货币流通规律——流通中实际所需要的货币量受货币流通规律支配 ①其内容是:流通中所需要的货币量同商品的价格总额成正比,与货币的流通次数成反比 ②其公式: 商品价格总额=待售商品数量×商品价格水平 流通中所需要的货币量= 货币流通次数=货币流通次数 5、纸币 ①含义:由国家(或某些地区)发行的、强制使用的价值符号(国家能决定纸币的发行量、纸币的面值,但不能决定纸币的购买力或者纸币代表的价值) ②优点:制作成本低,易于保管、携带和运输,避免磨损减少贵金属的无形流失 ③限度:发行量要以流通中实际所需要的货币量为限度。过多易导致通货膨胀,过少易导致通货紧缩
6、电子货币:用电子计算机进行贮存、转账、购买、支付的 7、货币的发展:金属货币(金银条块——铸币)——纸币——电子货币 二、信用工具和外汇现金结算:用纸币来完成经济往来的收付行为 1、结算方式 转账结算:通过银行转账来完成经济往来的收付行为 现金结算:用纸币来完成经济往来的收付行为 2、常用的信用工具——信用卡、支票 ①信用卡(含义:具有消费、转账结算、存取现金、信用贷款等部分或全部功能的电子支付卡。银行信用卡是商业银行对资信状况良好的客户发行的一种信用凭证。优点:功能多、方便、节省、安全等) ②支票(含义:是活期存款的支付凭证,是出票人委托银行等金融机构见票时无条件支付一定金额给受款人或者持票人的票据。种类:转账支票和现金支票) 3、外汇含义:用外币表示的用于国际间结算的支付手段 4、汇率:又称汇价,是指两种货币之间的兑换比率(如果用100 单位外币可以兑换成更多的人民币,说明外币的汇率升高,外币升值;反之,则说明外币汇率跌落,外币贬值)人民币升值有利于进口,不利于出口。反之,相反。 5、保持人民币币值稳定 ①含义:对内保持物价总水平稳定,对外保持人民币汇率稳定 ②意义:对人民生活安定、国民经济持续快速健康发展,对世界金融的稳定、经济的发展,具有重要意义。 3、影响价格的因素 1、各种因素对商品价格的影响,是通过改变商品的供求关系来实现的。 2、供求影响价格 ①供不应求,价格升高——卖方市场(卖方起主导作用,处于有利地位) ②供过于求,价格降低——买方市场(买方起主导作用,处于有利地位) 3、价值决定价格 ①价值与价格的关系:价值是价格的基础,价格是价值的货币表现(一般情况下,商品价值量与价格成正比)
必修1全册基本内容梳理 从实验学化学 一、化学实验安全 1、(1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。 (2)烫伤宜找医生处理。 (3)浓酸撒在实验台上,先用Na2CO3 (或NaHCO3)中和,后用水冲擦干净。浓酸沾在皮肤上,宜先用干抹布拭去,再用水冲净。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。 (4)浓碱撒在实验台上,先用稀醋酸中和,然后用水冲擦干净。浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。 (5)钠、磷等失火宜用沙土扑盖。 (6)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。 二.混合物的分离和提纯 分离和提纯的方法分离的物质应注意的事项应用举例 过滤用于固液混合的分离一贴、二低、三靠如粗盐的提纯 蒸馏提纯或分离沸点不同的液体混合物防止液体暴沸,温度计水银球的位置,如石油的蒸馏中冷凝管中水的流向如石油的蒸馏 萃取利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂用四氯化碳萃取溴水里的溴、碘 分液分离互不相溶的液体打开上端活塞或使活塞上的凹槽与漏斗上的水孔,使漏斗内外空气相通。打开活塞,使下层液体慢慢流出,及时关闭活塞,上层液体由上端倒出如用四氯化碳萃取溴水里的溴、碘后再分液 蒸发和结晶用来分离和提纯几种可溶性固体的混合物加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液;当蒸发皿中出现较多的固体时,即停止加热分离NaCl和KNO3混合物三、离子检验 离子所加试剂现象离子方程式 Cl-AgNO3、稀HNO3 产生白色沉淀Cl-+Ag+=AgCl↓ SO42- 稀HCl、BaCl2 白色沉淀SO42-+Ba2+=BaSO4↓ 四.除杂 注意事项:为了使杂质除尽,加入的试剂不能是“适量”,而应是“过量”;但过量的试剂必须在后续操作中便于除去。 五、物质的量的单位――摩尔 1.物质的量(n)是表示含有一定数目粒子的集体的物理量。 2.摩尔(mol): 把含有6.02 ×1023个粒子的任何粒子集体计量为1摩尔。 3.阿伏加德罗常数:把6.02 X1023mol-1叫作阿伏加德罗常数。 4.物质的量=物质所含微粒数目/阿伏加德罗常数n =N/NA 5.摩尔质量(M)(1) 定义:单位物质的量的物质所具有的质量叫摩尔质量.(2)单位:g/mol 或g..mol-1(3) 数值:等于该粒子的相对原子质量或相对分子质量. 6.物质的量=物质的质量/摩尔质量( n = m/M ) 六、气体摩尔体积