红外
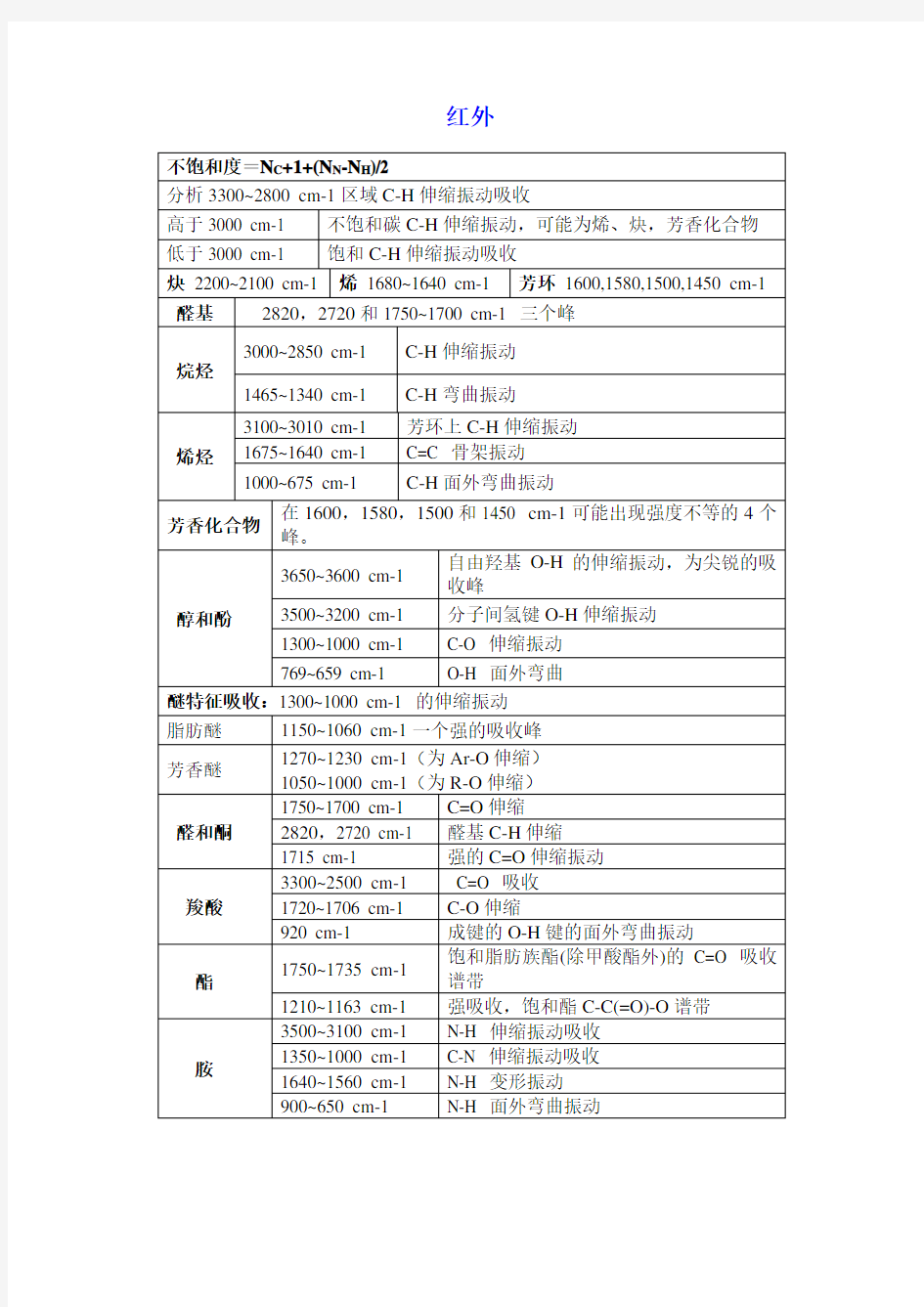
不饱和度=N C+1+(N N-N H)/2
分析3300~2800 cm-1区域C-H伸缩振动吸收
高于3000 cm-1 不饱和碳C-H伸缩振动,可能为烯、炔,芳香化合物低于3000 cm-1 饱和C-H伸缩振动吸收
炔2200~2100 cm-1 烯1680~1640 cm-1 芳环1600,1580,1500,1450 cm-1 醛基2820,2720和1750~1700 cm-1 三个峰
烷烃
3000~2850 cm-1 C-H伸缩振动
1465~1340 cm-1 C-H弯曲振动
烯烃3100~3010 cm-1 芳环上C-H伸缩振动1675~1640 cm-1 C=C 骨架振动
1000~675 cm-1 C-H面外弯曲振动
芳香化合物在1600,1580,1500和1450 cm-1可能出现强度不等的4个峰。
醇和酚3650~3600 cm-1
自由羟基O-H的伸缩振动,为尖锐的吸
收峰
3500~3200 cm-1 分子间氢键O-H伸缩振动
1300~1000 cm-1 C-O 伸缩振动
769~659 cm-1 O-H 面外弯曲
醚特征吸收:1300~1000 cm-1 的伸缩振动
脂肪醚1150~1060 cm-1一个强的吸收峰
芳香醚1270~1230 cm-1(为Ar-O伸缩)1050~1000 cm-1(为R-O伸缩)
醛和酮1750~1700 cm-1 C=O伸缩
2820,2720 cm-1 醛基C-H伸缩1715 cm-1 强的C=O伸缩振动
羧酸3300~2500 cm-1C=O 吸收
1720~1706 cm-1 C-O伸缩
920 cm-1成键的O-H键的面外弯曲振动
酯1750~1735 cm-1
饱和脂肪族酯(除甲酸酯外)的C=O 吸收
谱带
1210~1163 cm-1强吸收,饱和酯C-C(=O)-O谱带
胺3500~3100 cm-1N-H 伸缩振动吸收1350~1000 cm-1C-N 伸缩振动吸收1640~1560 cm-1N-H 变形振动900~650 cm-1N-H 面外弯曲振动
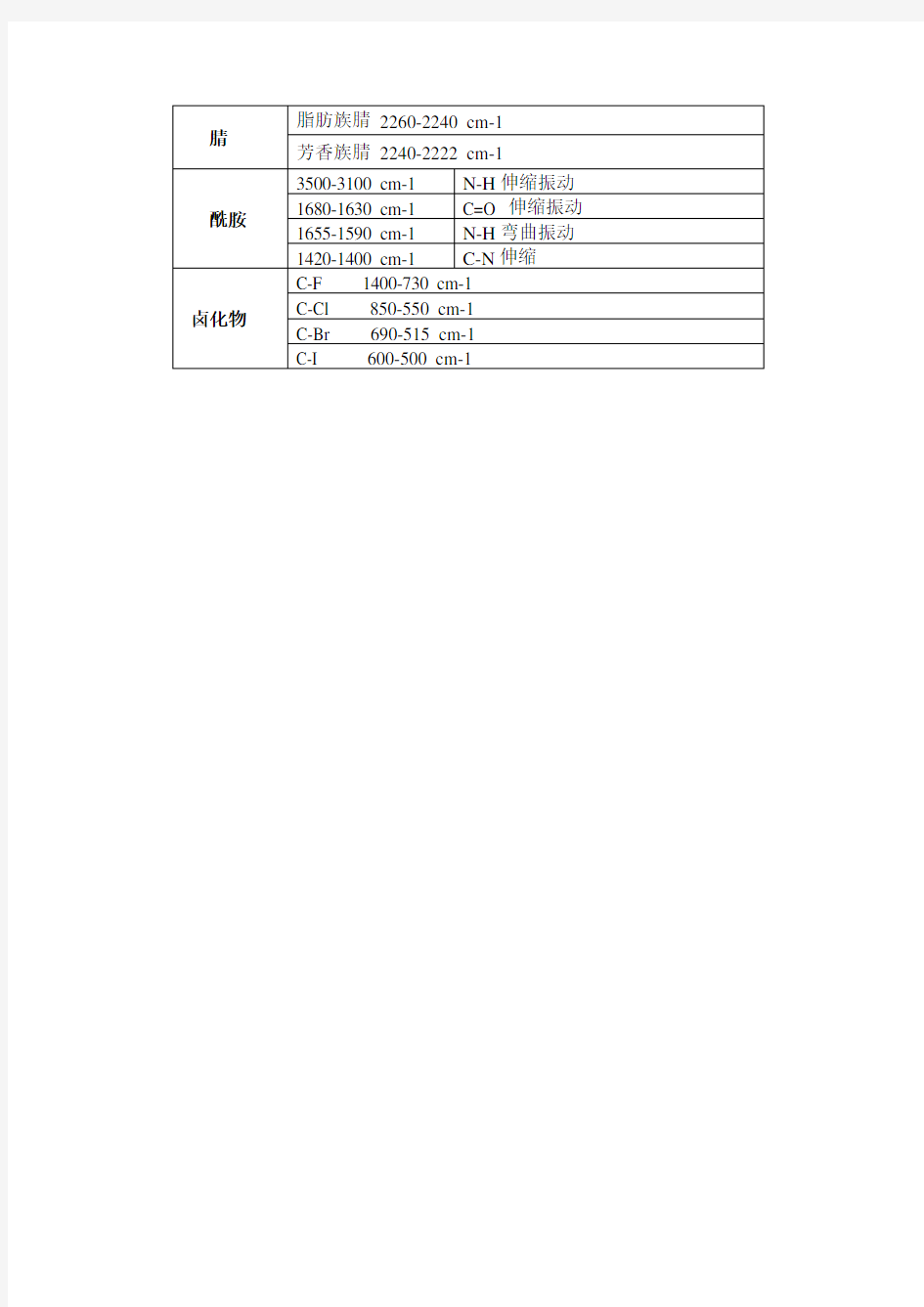
腈脂肪族腈2260-2240 cm-1芳香族腈2240-2222 cm-1
酰胺3500-3100 cm-1 N-H伸缩振动1680-1630 cm-1 C=O 伸缩振动1655-1590 cm-1 N-H弯曲振动1420-1400 cm-1 C-N伸缩
卤化物C-F 1400-730 cm-1 C-Cl 850-550 cm-1 C-Br 690-515 cm-1 C-I 600-500 cm-1
IR波谱解析
名词解析 发色团(chromophoric groups):分子结构中含有π电子的基团称为发色团,它们能产生π→π*和n→π*跃迁从而你呢个在紫外可见光范围内吸收。 助色团(auxochrome):含有非成键n电子的杂原子饱和基团本身不吸收辐射,但当它们与生色团或饱和烃相连时能使该生色团的吸收峰向长波长移动并增强其强度的基团,如羟基、胺基和卤素等。 红移(red shift):由于化合物结构发生改变,如发生共轭作用引入助色团及溶剂改变等,使吸收峰向长波方向移动。 蓝移(blue shift):化合物结构改变时,或受溶剂的影响使吸收峰向短波方向移动。 增色效应(hyperchromic effect):使吸收强度增加的作用。 减色效应(hypochromic effect):使吸收强度减弱的作用。 吸收带:跃迁类型相同的吸收峰。 指纹区(fingerprint region):红外光谱上的低频区通常称指纹区。当分子结构稍有不同时,该区的吸收就有细微的差异,并显示出分子特征,反映化合物结构上的细微结构差异。这种情况就像人的指纹一样,因此称为指纹区。指纹区对于指认结构类似的化合物很有帮助,而且可以作为化合物存在某种基团的旁证。但该区中各种官能团的特征频率不具有鲜明的特征性。 共轭效应 (conjugated effect):又称离域效应,是指由于共轭π键的形成而引起分子性质的改变的效应。 诱导效应(Inductive Effects):一些极性共价键,随着取代基电负性不同,电子云密度发生变化,引起键的振动谱带位移,称为诱导效应。 核磁共振:原子核的磁共振现象,只有当把原子核置于外加磁场中并满足一定外在条件时才能产生。 化学位移:将待测氢核共振峰所在位置与某基准物氢核共振峰所在位置进行比较,其相对距离称为化学位移。 弛豫:通过无辐射的释放能量的途径核由高能态向低能态的过程。 分子离子:有机质谱分析中,化合物分子失去一个电子形成的离子。 基峰:质谱图中表现为最高丰度离子的峰。 自旋偶合:是磁性核与邻近磁性核之间的相互作用。是成键电子间接传递的,不影响磁性核的化学位移。 麦氏重排(McLafferty rearrangement):具有不饱和官能团 C=X(X为O、S、N、C 等)及其γ-H原子结构的化合物,γ-H原子可以通过六元环空间排列的过渡态,向缺电子(C=X+ )的部位转移,发生γ-H的断裂,同时伴随 C=X的β键断裂,这种断裂称为麦氏重排。 自旋偶合:是磁性核与邻近磁性核之间的相互作用。是成键电子间接传递的,不影响磁性核的化学位移。 自旋裂分:因自旋偶合而引起的谱线增多现象称为自旋裂分。 1.紫外光谱的应用 (1).主要用于判断结构中的共轭系统、结构骨架(如香豆素、黄酮等) (2).确定未知化合物是否含有与某一已知化合物相同的共轭体系。 (3).可以确定未知结构中的共轭结构单元。 (4).确定构型或构象 (5).测定互变异构现象 2.分析紫外光谱的几个经验规律 (1).在200~800nm区间无吸收峰,结构无共轭双键。 (2).220~250nm,强吸收(εmax在104~2?104之间),有共轭不饱和键(共轭二烯,α,β-不饱和醛、酮)
波谱解析 (一)紫外光谱 解析UV应用时顾及吸收带的位置,强度和形状三个方面。从吸收带(K带)位置可估计产生该吸收共轭体系的大小;从吸收带的强度有助于K带,B带和R 带的识别;从吸收带的形状可帮助判断产生紫外吸收的基团,如某些芳香化合物,在峰形上可显示一定程度的精细结构。一般紫外吸收光谱都比较简单,大多数化合物只有一、两个吸收带,因此解析较为容易。可粗略归纳为以下几点: ①如果化合物在220~800nm区间无吸收,表明该化合物是脂肪烃、脂环烃或它们的简单衍生物。 ②如果在220~250nm间显示强吸收(ε近10000或更大),表明有R带吸收,即分子结构存在共轭双烯或α,β—不饱和醛、酮。 ③如果在250~290nm间显示中等强度(ε为200~1000)的吸收带,且常显示不同程度精细结构,表明结构中有苯环或某些杂芳环的存在。 ④如果在290nm附近有弱吸收带(ε<100),则表明分子结构中非共轭羰基。 ⑤如果在300nm上有***度吸收,说明该化合物有较大的共轭体系;若***度吸收具有明显的精细结构,说明为稠环芳、稠环杂芳烃或其衍生物。 (二)红外光谱 1. 解析红外光谱的三要素(位置、强度和峰形) 在解析红外光谱时,要同时注意红外吸收峰的位置,强度和峰形。吸收位置是红外吸收最重要的特点,但在鉴定化合物分子结构时,应将吸收峰的位置辅以吸收峰强度和峰形综合分析。每种有机化合物均显示若干吸收峰,对大量红外图谱中各吸收峰强度相互比较,归纳出各种官能团红外吸收强度的变化范围。只有熟悉各官能团红外吸收的位置和强度处于一定范围时,才能准确推断出官能团的存在2 .确定官能团的方法 对于任何有机化合物的红外光谱,均存在红外吸收的伸缩振动和多种弯曲振动。因此,每一个化合物的官能团的红外光谱图在不同区域显示一组相关吸收峰。只有当几处相关吸收峰得到确认时,才能确定该官能团的存在。例1. 甲基(CH3):2960cm-1和2870cm-1为伸缩振动,1460cm-1和1380cm-1为其弯曲振动。 例2. 亚甲基(CH2):2920cm-1和2850cm-1为其伸缩振动,1470cm-1和720cm-1
红外光谱分析 二十世纪初叶,Coblentz 发表了一百多个有机化合物的红外光谱图,给有机化学家提供了鉴别未知化合物的有力手段。到四十年代红外光谱技术得到了广泛的研究和应用。当今红外光谱仪的分辨率越来越高,检测范围扩展到10000-200cm-1,样品量少至微克级。红外光谱提供的某些信息简捷可靠,检测样品中有无羰基及属于哪一类(酸酐、酯、酮或醛)是其他光谱技术难以替代的。因此,对从事有机化合物为研究对象的化学工作者来说,红外光谱学是必需熟悉和掌握的一门重要光谱知识。 一、基本原理 1、基本知识 光是一种电磁波。可根据电磁波的波长范围分成不同类型的光谱,它们各自反映出物质的不同类型的运动形式。表1 列出这些电磁波的波长,其所在区域的光谱名称,以及对应的运动形式。 表1 常用的有机光谱及对应的微观运动
红外光谱研究的内容涉及的是分子运动,因此称之为分子光谱。通常红外光谱系指2-25 μ之间的吸收光谱,常用的为中红外区4000-650cm-1(2.5-15.4 μ) 或4000-400cm-1。 这段波长范围反映出分子中原子间的振动和变角振动,分子在振 动运动的同时还存在转动运动。在红外光谱区实际所测得的图谱是分 子的振动与转动运动的加合表现,即所谓振转光谱。 每一化合物都有其特有的光谱,因此使我们有可能通过红外光谱 对化合物作出鉴别。 红外光谱所用的单位波长μ,波数cm-1。光学中的一个基本公式是λυ= C,式中λ为波长,υ为频率,C 为光速(3 ×1010cm/s) 。设υ为波数,其含义是单位长度(1cm) 中所含的波的个数,并应具有以下关系:波数(cm-1) =104/ 波长( μ)波长和波数都被用于表示红外光谱的吸收位置,即红外光谱图的横坐标。目前倾向于普遍采用波数为单位,而在图谱上方标以对应的 波长值。红外光谱图的纵坐标反映的是吸收强度,一般以透过率(T%) 表示。 2、红外光谱的几种振动形式 主要的基本可以分为两大类:伸缩振动和弯曲振动。 (1)伸缩振动( υ) 沿着键轴方向伸或缩的振动,存在对称与非对称两种类型。它的 吸收频率相对在高波数区。 (2)弯曲振动( δ) 包括面内、面外弯曲振动,变角振动,摇摆振动等。它的吸收频率相对在低波数区。 4000cm -1(高) 400cm -1(低) 3、红外光谱吸收峰主要的几种类型 (1)基频峰:伸缩振动,弯曲振动产生的吸收峰均为基频峰。 (2)倍频峰:出现在基频峰波数二倍处。如基频为900cm-1,倍频为
例1未知物分子式为C 6H 14,其IR 图谱如下,试推其结构。 例 2 未 知 物 分 子 式 为 C 4H 5N , 其 红 外 图谱 如 下 图 例3未知物分子式为C 7H 9N ,其红外图谱如下图所示,试推其结构。 例4未知物分子式为C 8H 8O 2,其红外图谱如下图所示,试推其结构。 1、未知物分子式为 C 14H 12,其 IR 图如下,试推其结构 2.分子式为C 8H 7N ,红外光谱如下,试推其结构。 3.分子式为C 4H 6O 2,红外光谱如下,试推其结构 例2,C 7 H 16 O 3 ,推断其结构:
例3:化合物C 10 H 12 O 2 ,推断结构 例4,化合物C 8 H 8 O 2 ,推断其结构: 例2:C 8 H 14 O 4 1、未知化合物的分子式为C 6H 12O 2,13 C-NMR 谱如下,求其结构 2、未知化合物的分子式为C 8H 8O,13C-NMR 谱如下,求其结构 结构为C6H5C(O)CH3 3、某含氮化合物,质谱显示分子离子峰m/z209,元素分析结果为C:57.4%,H:5.3%,N:6.7%,13 C-NMR 谱如下,推导其结构. 4、未知化合物的分子式为C 8H 18,13 C-NMR 谱如下,求其结构. 结构为(CH 3)3C-CH 2-CH(CH 3)2 5、分子式为C 9 H 10 O ,根据氢谱、碳谱推测其结构
【例题3.1】某未知化合物分子式为C 7H 9N ,碳谱数据如图3-例1所示,同时在氢谱的芳香区有一个明显的单峰,试推导其结构。 【例题3.2】某含氧五元环化合物,分子式为C 5H 10O ,由其碳谱图3-例2推测结构。 【例题3.3】某化合物分子式为C 7H 12O 3,由其氢谱和碳谱图3-例3推断结构 结构未知(C 6 H 12 O ,酮) 解析:100,分子离子峰;85,失去CH 3 (15)的产物;57,丰度最大,稳定结构,失去CO(28)后的产 物
实验二、红外光谱测定固体有机化合物的结构 【实验目的】 1. 掌握有机化合物红外光谱的测定技术和解析方法 2. 熟悉有机化合物红外光谱的样品制备技术及傅立叶红外光谱仪器的构造和工作原理 3. 了解红外光谱仪器性能指标的检查 4. 学会用红外光谱法区分丁二烯的两种几何异构体。 【实验原理】 红外光谱在化学领域中主要用于分子结构的基础研究(测定分子的键长、键角等)以及化学组成的分析(即化合物的定性定量),但其中应用最广泛的还是化合物的结构鉴定,根据红外光谱的峰位、峰强及峰形,判断化合物中可能存在的官能团,从而推断出未知物的结构。有共价键的化合物(包括无机物和有机物)都有其特征的红外光谱,除光学异构体及长链烷烃同系物外,几乎没有两种化合物具有相同的红外吸收光谱,即所谓红外光谱具有“指纹性”,因此红外光谱法用于有机物的结构测定和鉴定是最重要的方法之一。 傅立叶变换红外光谱仪实物图 1:底座;2:样品底座(硅碳钢圆柱);3:压片框架;4:保护外套;5:弹簧; 6:模压杆;7:模压底座;8:模压冲杆 1 2 3 4 5 6 7 8
压片机构造图 区分烯烃顺、反异构体,常常借助于位于1000~650 cm-1 范围的YC-H 谱带。烷基型烯烃的顺式结构出现在730~675cm-1,反式结构出现在~960 cm-1。当取代变化时,顺式结构峰变化大,反式结构峰基本不变,因此在确定异构体时十分有用。除上述谱带外,对于丁烯二酸,位于1710~1580 cm-1范围的光谱特征。 顺丁烯二酸和反丁烯二酸的区别,是分子中两个羧基相对于双键的几何排列不同。顺丁烯二酸分子结构对称性差,加之双键和羰基共轭,在~1600 cm-1出现很强的Vc=c谱带;反丁烯二酸分子结构对称性强,双键位于对称中心,其伸缩振动无红外活性,在光谱中分析不到吸收谱带。另外,顺丁烯二酸只能生成分子间氢键,其羰基谱位于1705cm-1 接近Vc=c 羰基频率的正常值;而反丁烯二酸能生成分子内氢键,其羰基谱带移至1680cm-1.因此,利用这一区间谱带可以很容易地将两种几何异构体区分开来。 【实验仪器和试剂】 仪器:傅立叶变换红外光谱仪,红外专用压片机,压片模具,玛瑙研体。 试剂:阿司匹林,分析纯KBr粉末,苯甲酸,苯甲酸钠,甘氨酸。 【实验步骤】 1、红外光谱仪的性能检查 选择合适的实验测定参数,以空气为背景进行空白测定,然后放聚苯乙烯薄膜于样品光路上,绘制聚苯乙烯薄膜的红外吸收光谱(见图)。 图聚苯乙烯薄膜的红外吸收光谱 规定标准: 按照2010年版中国药典附录31中规定执行。
第一节:概述 1、红外吸收光谱与紫外吸收光谱一样是一种分子吸收光谱。红外光的能量(△E=0.05-1.0ev)较紫外光(△E=1-20ev)低,当红外光照射分子时不足以引起分子中价电子能级的跃迁,而能引起分子振动能级和转动能级的跃迁,故红外吸收光谱又称为分子振动光谱或振转光谱。 2、红外光谱的特点:特征性强、适用范围广。 红外光谱对化合物的鉴定和有机物的结构分析具有鲜明的特征性,构成化合物的原子质量不同、化学键的性质不同、原子的连接次序和空间位置不同都会造成红外光谱的差别。 红外光谱对样品的适用性相当广泛,无论固态、液态或气态都可进行测定。 3、红外光谱波长覆盖区域:0.76 mm ~ 1000mm. 红外光按其波长的不同又划分为三个区段。 (1)近红外:波长在0.76-2.5mm之间(波数12820-4000cm-1) (2)中红外:波长在2.5-25mm(在4000-400 cm-1) 通常所用的红外光谱是在这一段的(2.5-15mm,即4000-660 cm-1)光谱范围,本章内容仅限于中红外光谱。 (3)远红外:波长在25~1000mm(在400-10 cm-1) 转动光谱出现在远红外区。 4、红外光谱图:当物质分子中某个基团的振动频率和红外光的频率一样时,分子就要吸收能量,从原来的振动能级跃迁到能量较高的振动能级,将分子吸收红外光的情况用仪器记录,就得到红外光谱图。 5、红外光谱表示方法: (1)红外光谱图 红外光谱图以透光率T %为纵坐标,表示吸收强度,以波长l ( mm) 或波数s (cm-1)为横坐标,表示吸收峰的位置,现主要以波数作横坐标。波数是频率的一种表示方法(表示每厘米长的光波中波的数目)。通过吸收峰的位置、相对强度及峰的形状提供化合物结构信息,其中以吸收峰的位置最为重要。 (2)将吸收峰以文字形式表示:如下图可表示为,3525cm-1(m),3097cm-1(m),1637cm-1(s)。这种方法指出了吸收峰的归属,带有图谱解析的作用。 第二节各类化合物的红外光谱特征 有机化合物的数目非常大,但组成有机化合物的常见元素只有10种左右,组成有机化合物的结构单元即称为基团的原子组合数目约有几十种。根据上述讨论,基团的振动频率主要取决于组成基团原子质量(即原子种类)和化学键力常数(即化学键的种类)。一般来说,组成分子的各种基团如C-H、C-N 、C=C、C=O 、C-X等都有特定的红外吸收区域(特征吸收峰),根据特征吸收峰可以推断物质的结构。所以,有必要对各类有机化合物的光谱特征加以总结。 一、烷烃 烷烃中只有C-H键组成的C-H,CH2,CH3基团,纯烷烃的吸收峰只有C-H的伸缩、弯曲振动和C-C骨架振动。 1、νC-H 烷烃的C-H伸缩振动频率 一般不超过3000cm-1,甲基和亚甲基的C-H伸缩分别有对称和不对称振动相应出现四个吸收峰,甲基的C-H伸缩振动,对称的出现在2872cm-1,不对称的出现在2962cm-1;亚甲基的对称出现在2853cm-1,不对称的出现在2926 cm-1。一般不对称的吸收强度稍强,在高分辨的红外仪(光栅型),可以在2853-2962 cm-1处,清楚地观察到这四个峰,而在低分辨的仪器中,两两重叠只能看到两个峰。如下图:
总结 当一束具有连续波长的红外光通过物质,物质分子中某个基团的振动频率或转动频率和红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能级跃迁到能量较高的振(转)动能级,分子吸收红外辐射后发生振动和转动能级的跃迁,该处波长的光就被物质吸收。所以,红外红外光谱光谱法实质上是一种根据分子内部原子间的相对振动和分子转动等信息来确定物质分子结构和鉴别化合物的 分析方法。将分子吸收红外光的情况用仪器记录下来,就得到红外光谱图。红外光谱图通常用波长(λ)或波数(σ)为横坐标,表示吸收峰的位置,用透光率(T%)或者吸光度(A)为纵坐标,表示吸收强度。 当外界电磁波照射分子时,如照射的电磁波的能量与分子的两能级差相等,该频率的电磁波就被该分子吸收,从而引起分子对应能级的跃迁,宏观表现为透射光强度变小。电磁波能量与分子两能级差相等为物质产生红外吸收光谱必须满足条件之一,这决定了吸收峰出现的位置。 红外吸收光谱产生的第二个条件是红外光与分子之间有偶合作用,为了满足这个条件,分子振动时其偶极矩必须发生变化。这实际上保证了红外光的能量能传递给分子,这种能量的传递是通过分子振动偶极矩的变化来实现的。并非所有的振动都会产生红外吸收,只有偶极矩发生变化的振动才能引起可观测的红外吸收,这种振动称为红外活性振动;偶极矩等于零的分子振动不能产生红外吸收,称为红外非活性振动。 分子的振动形式可以分为两大类:伸缩振动和弯曲振动。前者是指原子沿键轴方向的往复运动,振动过程中键长发生变化。后者是指原子垂直于化学键方向的振动。通常用不同的符号表示不同的振动形式,例如,伸缩振动可分为对称伸缩振动和反对称伸缩振动,分别用 Vs 和Vas 表示。弯曲振动可分为面内弯曲 振动(δ)和面外弯曲振动(γ)。从理论上来说,每一个基本振动都能吸收与 红外光谱仪其频率相同的红外光,在红外光谱图对应的位置上出现一个吸收峰。实际上有一些振动分子没有偶极矩变化是红外非活性的;另外有一些振动的频率
波谱解析试题1 一、名词解释: 1.发色团 2. 化学位移 二、简答题: 1.红外光谱在结构研究中有何用途? 2.偏共振去偶碳谱在结构研究中具有什么样的意义? 三、化合物可能是A或B,它的紫外吸收λmax 为314nm (lgε=4.2),指出这个化合物是属于哪一种结构。 (A)(B) 四、下面为化合物A、B的红外光谱图,可根据哪些振动吸收峰推断化合物A、B中分别存在哪些官能团? A:
B: 五、归属下列化合物碳谱中的碳信号。(15)
六、某化合物的分子式为C14H14S,其氢谱如下图所示,试推断该化合物的结构式,并写出推导过程。(15分) 七、某化合物分子式为C3H7ON, 结合下面给出的图谱,试推断其结构,并写出简单的推导过程。
波谱解析试题1答案 一、名词解释: 1.发色团:从广义上讲, 分子中能吸收紫外光和(或)可见光的结构系统叫做发色团。因常用的紫外光谱仪的测定围是200~40Onm 的近紫外区, 故在紫外分析中,只有π-π* 和(或)n-π* 跃迁才有意义。故从狭义上讲,凡具有π键电子的基团称为发色团 2. 化学位移:不同类型氢核因所处化学环境不同, 共振峰将分别出现在磁场的不同区域。实际工作中多将待测氢核共振峰所在位置( 以磁场强度或相应的共振频率表示) 与某基准物氢核共振峰所在位置进行比较, 求其相对距离, 称之为化学位移。 二、简答题: 1.红外光谱在结构研究中有何用途? (1)鉴定是否为某已知成分 (2)鉴定未知结构的官能团 (3)其他方面的应用:几何构型的区别;立体构象的确定;分子互变异构与同分异构的确定。 2.偏共振去偶碳谱在结构研究中具有什么样的意义? 当照射1H 核用的电磁辐射偏离所有l H 核的共振频率一定距离时, 测得的13C-NMR(OFR) 谱中将不能完全消除直接相连的氢的偶合影响。此时,13C的信号将分别表现为q (CH3), t (CH2),d(CH),s(C)。据此,可以判断谈的类型。 三、 A: 217(基值)+30(共轭双烯)+5×2(环外双键)+5×4(烷基)=277(nm)
红外 不饱和度=N C+1+(N N-N H)/2 分析3300~2800 cm-1区域C-H伸缩振动吸收 高于3000 cm-1 不饱和碳C-H伸缩振动,可能为烯、炔,芳香化合物低于3000 cm-1 饱和C-H伸缩振动吸收 炔2200~2100 cm-1 烯1680~1640 cm-1 芳环1600,1580,1500,1450 cm-1 醛基2820,2720和1750~1700 cm-1 三个峰 烷烃 3000~2850 cm-1 C-H伸缩振动 1465~1340 cm-1 C-H弯曲振动 烯烃3100~3010 cm-1 芳环上C-H伸缩振动1675~1640 cm-1 C=C 骨架振动 1000~675 cm-1 C-H面外弯曲振动 芳香化合物在1600,1580,1500和1450 cm-1可能出现强度不等的4个峰。 醇和酚3650~3600 cm-1 自由羟基O-H的伸缩振动,为尖锐的吸 收峰 3500~3200 cm-1 分子间氢键O-H伸缩振动 1300~1000 cm-1 C-O 伸缩振动 769~659 cm-1 O-H 面外弯曲 醚特征吸收:1300~1000 cm-1 的伸缩振动 脂肪醚1150~1060 cm-1一个强的吸收峰 芳香醚1270~1230 cm-1(为Ar-O伸缩)1050~1000 cm-1(为R-O伸缩) 醛和酮1750~1700 cm-1 C=O伸缩 2820,2720 cm-1 醛基C-H伸缩1715 cm-1 强的C=O伸缩振动 羧酸3300~2500 cm-1C=O 吸收 1720~1706 cm-1 C-O伸缩 920 cm-1成键的O-H键的面外弯曲振动 酯1750~1735 cm-1 饱和脂肪族酯(除甲酸酯外)的C=O 吸收 谱带 1210~1163 cm-1强吸收,饱和酯C-C(=O)-O谱带 胺3500~3100 cm-1N-H 伸缩振动吸收1350~1000 cm-1C-N 伸缩振动吸收1640~1560 cm-1N-H 变形振动900~650 cm-1N-H 面外弯曲振动
常规样品的红外光谱分析 PB07206298龚智良 实验目的 1.初步掌握两种基本样品制备技术及傅立叶变换光谱仪器的简单操作; 2.通过图谱解析及标准谱图的检索,了解由红外光谱鉴定未知物的一般过程。 实验原理 红外光谱:红外光谱是分子的振动转动光谱,也是一种分子吸收光谱。当样品受到频率连续变化的红外光照射时,分子吸收了某些频率的辐射,并由其振动或转动引起的偶极矩的净变化,产生分子振动和转动能级从基态到激发态的跃迁,使相应于这些区域的光透射强度减弱。记录红外光的百分透射比或波长关系曲线,就得到红外光谱。从分子的特征吸收可以鉴定化合物和分子结构,进行定性和定量分析。红外光谱尤其在物质定性分析中应用广泛,它操作简便,分析速度快,样品用量少且不破坏样品,能提供丰富的结构信息,因此红外光谱法往往是物质定性分析中优先考虑的手段。 能产生红外吸收的分子为红外活性分子,如CO?分子;不能产生红外吸收的分子为非红外活性分子,如O?分子。 中红外区为基本振动区:4000-400cm-1研究应用最多。 红外吸收的波数与相应振动的力常数关系密切。双原子分子的基本频率计算公式为 ??? ??=12? 其中?为约化质量 μ=m??m?
m?+m? 对于多原子分子,其振动可以分解为许多简单的基本振动,即简正振动。一般将振动形式分为两类:伸缩振动和变形振动。 各种振动都具有各自的特征吸收。 仪器结构和测试技术 Fourier变换红外光谱仪(FTIR仪:能够同时测定所有频率的信息,得到光强随时间变化的谱图,称时域图,这样可以大大缩短扫描时间。由于不采用传统的色散元件,其分辨率和波数精度都较好。傅立叶变换红外谱仪主要由光源(硅碳棒、高压汞灯、Michellson干涉仪、检测器、计算机和记录仪组成。测试样品时,由于样品对某些频率的红外光吸收,从而得到不同样品的干涉图。红外光是复合光,检测器接收到的信号是所有频率的干涉图的加合。 对试样的要求:试样应该为纯物质,纯度大于98%,以便于和纯化合物进行比较;样品中不能含游离水;试样的浓度和测试厚度应选择适当,以使大多数吸收峰的透射比处于10%-80%。 制样方法:对于液体样品有液膜法、液体吸收池法;对于固体样品有压片法、糊状法;对于特殊的样品还有薄膜法(包括熔融法和热压成膜法、溶液制膜法;对于气态样品一般都灌注于气体池中进行测试。 除了常规的测试技术外,红外光谱测试还有衰减全发射和偏振红外光谱等特殊的测试技术。 实验步骤、现象及讨论 固体样品制备:使用KBr压片法。用一个玛瑙研钵将少量KBr晶体充分研磨后加入其量5%左右的待测固体样品,混合研磨直至均匀,并使其颗粒大小比所检测的光波长更小(约2μm以下。在一个具有抛光面的金属模具上方一个圆形纸环,用刮勺将研磨好的粉末移至环中,盖上另一块模具,放入油压机中进行压片。KBr压片形成
有机波谱分析习题 第一章电子辐射基础 (一)判断题 1.现代分析化学的任务是测定物质的含量。( ) 2.测定某有机化合物中C、H、O、N元素含量的方法属于定性分析。( ) 3.测定某有机化合物中是否含有羰基属于有机结构分析。( ) 4.利用物质分子吸收光或电磁辐射的性质,建立起来的分析方法属于吸收光谱分析。( ) 5.物质被激发后,利用物质跃迁至低能态或基态时发光的性质建立起来的分析方法属于发射光谱分析。( ) 6.根据Franck-condon原理,在电子能级发生跃迁时,必然伴随振动能级和转动能级的变化。( ) 7.紫外吸收光谱、红外吸收光谱、核磁共振波谱和质谱是有机结构分析的四种主要的有机光波谱分析方法,合称为四大谱。( ) 8.电磁辐射的波长越长,能量越大。( ) 9.有机波谱分析方法和仪器分析方法的灵敏度和准确度都要比化学分析法高得多。( ) 10.一般来讲,分子光谱远比原子光谱复杂,原子光谱通常为线状光谱,而分子光谱为带状光谱。( ) 11.吸收定律偏离线性完全是由于仪器因素引起的。( ) 12.电子能级间隔越小,跃迁时吸收光子的频率越大。( ) 13.分子光谱是由于电子的发射而产生的。( ) 14.分子荧光也叫二次光,都属吸收光谱的范畴。( ) 15.ICP可用于测定F、Cl、Br、C、H、N、O、S等非金属元素。( ) (一)判断题答案 1.×2.×3.√4.√ 5.√ 6.√ 7.√8.×9.×l0.√11.×l2.×13.×l4.×l5.× (二)单选题 1.光或电磁辐射的二象性是指( )。 A.电磁辐射是由电矢量和磁矢量组成;B.电磁辐射具有波动性和电磁性; C.电磁辐射具有微粒性和光电效应;D.电磁辐射具有波动性和微粒性。 2.光量子的能量与电磁辐射的哪一个物理量成正比?( ) A.频率;B.波长;C.周期;D.强度 3.可见光区、紫外光区、红外光区、无线电波四个电磁波区域中,能量最大和最小的区域分别为( )。 A.紫外光区和无线电波区;B.紫外光区和红外光区; C。可见光区和无线电波区;D.可见光区和红外光区。 4.频率为l×107MHz的电磁辐射是处在哪个光区?( ) A.红外光区;B.紫外光区;C.无线电波区;D.可见光区。 5.有机化合物成键电子的能级间隔越小,受激跃迁时吸收电磁辐射的( )。 A.能量越大;B.波数越大;C.波长越长;D.频率越高。 6.分析化学发生第二次变革的年代是( )。 A.20世纪初;B.20世纪20年代;C.20世纪40年代;D.20世纪末。 7.波长为0.0100nm的电磁辐射的能量是多少eV?(已知leV=1.602×10-19J)( ) A.0.124eV:B.12.4eV;C.124eV;D.1.24×105 eV。
GJhO的红外吸收光H 2十2汉4 — 10 解:1?计算不饱和度,为饱和脂肪族类化合物。0 2 2?特征峰及相关峰: u;二2970口打百莒) ' 2874c/w ](s) 笳;J476 结构式中可能含有一个苯环利一个卷键或两个取健.r& 图的240(H210(km 无吸收峰.町否定垒键的存在. 人特征峰及相关峰’ :H 3070(?m~' (ir)300 lt?w~] ( w) t?c_c 1597cm L4 48ft7rw_1.1581c 人级74&湖弋邻位取代) V^3 2954cw_l v^H2847cm~ 1435 cm1 Uc-o-c1288CW _1(ys) v^_o_c1126cnr l(s)J 综匕,结构中存^Ar—COOCH3单尤结构。 不饱利度等于& ■个举环片去4个* 1个羡搭占去I个.还余1个不饱和度?mittra中无t玄y 峰.不存衽「=<、基团"结合苯为邻取代?从怙5減去已知的C JJ IKO J.还#10^1,02.故应还有_个一coocto^Hjo 缥上所述.其结构式町链为= *¥> 1.计算木饱和度,^=2+2X^0-]Q=6 O 「邻位取代萃 按旱峰.分裂峰1581cm 1的存一在,提示GF有可能自接与苯环相连.发生共枫. 北京化工大学北方学院2008——2009学年第二学期 《波谱分析法原理及应用》期末考试试卷评分标准 班级:姓名:学号:分数: 一、解释下列名词(每题5分,共30分) 1、发色基团、助色基团和摩尔吸光系数; 2、红外活性振动和非红外活性振动; 3、自旋-晶格弛豫和自旋-自旋弛豫; 4、化学等价核和磁等价核 5、碳谱的γ-效应和NOE效应; 6、α裂解和i裂解 1、发色基团:能导致化合物在紫外及可见光区产生吸收的基团,不论是否显出颜色都称为发色基团。例如,分子中含有π键的C=C、C≡C、苯环以及C=O等不饱和基团都是发色基团。(1分) 助色基团:本身不会使化合物分子产生颜色或者在紫外及可见光区不产生吸收的一些基团,但这些基团与发色基团相连时却能使发色基团的吸收带波长移向长波,同时使吸收强度增加。通常,助色基团是由含有孤对电子的元素所组成,例如-NH2、-NR2、-OH、-OR等。(2分) 摩尔吸光系数;浓度为1mol/L,光程为1cm时的吸光度。(2分) 2、红外活性振动:瞬间偶极矩变化不为零的振动。(2分) 非红外活性振动;分子在振动过程中不发生瞬间偶极矩的改变。(3分) 3、自旋-晶格弛豫:也叫纵向弛豫。指高能态的核将其能量转移到周围分子而转变成热运动,从而跃回到低能态的过程。(2分) 自旋-自旋弛豫:也叫横向弛豫。这种弛豫是通过相邻的同种核之间的能量交换实现的,发生这种弛豫时,各种能态的核的数目没有改变,核自旋体系的总能量也没有发生变化。(3分) 4.化学等价核:化学位移完全相同的核。(2分) 磁等价核:分子中的一组化学等价核,若它们对组外任何一个核都是以相同的大小偶合,则这一组核为磁等价核。(3分) 5、碳的γ-效应;当取代基处在被观察的碳的γ位,由于电荷相互排斥,被观察的碳周围电子云密度增大,δC向高场移动。(2分) NOE效应:当分子内有在空间位置上互相靠近的两个质子Ha和Hb时,如果用双共振法照射Hb,使干扰场的强度增加到刚使被干扰的谱线达到饱和,则另一个靠近的质子Ha的共振信号就会增加,这种现象称NOE。产生这一现象的原因是由于二个质子空间位置很靠近,相互弛豫较强,当Hb受到照射达饱和时,它要把能量转移给Ha,于是Ha吸收的能量增多,共振信号增大。这一效应的大小与质子之间距离的六次方成反比。当质子间距离超过时,就看不到这一现象。(3分) 6.α裂解:由游离基引发的均裂,是带电荷基团与α碳之间键的断裂。(2分) i裂解:由正电荷(阳离子)引发的碎裂过程,它涉及两个电子的转移,以酮类 的3分) R1+ O C R + 二、简述下列问题(每题5 分,共30分) 1、红外光谱产生必须具备的两个条件 红外光谱分析 红外光谱与分子的结构密切相关,是研究表征分子结构的一种有效手段,与其它方法相比较,红外光谱由于对样品没有任何限制,它是公认的一种重要分析工具。在分子构型和构象研究、化学化工、物理、能源、材料、天文、气象、遥感、环境、地质、生物、医学、药物、农业、食品、法庭鉴定和工业过程控制等多方面的分析测定中都有十分广泛的应用。 红外光谱可以研究分子的结构和化学键,如力常数的测定和分子对称性等,利用红外光谱方法可测定分子的键长和键角,并由此推测分子的立体构型。根据所得的力常数可推知化学键的强弱,由简正频率计算热力学函数等。分子中的某些基团或化学键在不同化合物中所对应的谱带波数基本上是固定的或只在小波段范围内变化,因此许多有机官能团例如甲基、亚甲基、羰基,氰基,羟基,胺基等等在红外光谱中都有特征吸收,通过红外光谱测定,人们就可以判定未知样品中存在哪些有机官能团,这为最终确定未知物的化学结构奠定了基础。 由于分子内和分子间相互作用,有机官能团的特征频率会由于官能团所处的化学环境不同而发生微细变化,这为研究表征分子内、分子间相互作用创造了条件。 分子在低波数区的许多简正振动往往涉及分子中全部原子,不同的分子的振动方式彼此不同,这使得红外光谱具有像指纹一样高度的特征性,称为指纹区。利用这一特点,人们采集了成千上万种已知化合物的红外光谱,并把它们存入计算机中,编成红外光谱标准谱图库,人们只需把测得未知物的红外光谱与标准库中的光谱进行比对,就可以迅速判定未知化合物的成份。 下面将对红外光谱分析的基本原理做一个简单的介绍。 红外吸收光谱是物质的分子吸收了红外辐射后,引起分子的振动-转动能级的跃迁而形成的光谱,因为出现在红外区,所以称之为红外光谱。利用红外光谱进行定性定量分析的方法称之为红外吸收光谱法。 红外辐射是在 1800年由英国的威廉.赫谢(Willian Hersher) 尔发现的。一直到了1903年,才有人研究了纯物质的红外吸收光谱。二次世界大战期间,由于对合成橡胶的迫切需求,红外光谱才引起了化学家的重视和研究,并因此而迅速发展。随着计算机的发展,以及红外光谱仪与其它大型仪器的联用,使得红外光谱在结构分析、化学反应机理研究以及生产实践中发挥着极其重要的作用,是“四大波谱”中应用最多、理论最为成熟的一种方法。 红外光谱法的特点: 1?气态、液态和固态样品均可进行红外光谱测定; 1.红外光谱产生的条件 满足两个条件: (1)辐射应具有能满足物质产 生振动跃迁所需的能量; (2) 辐射与物质间有相互偶合 作用。 偶极矩:μ= q d 偶极子在交变电场中的作用示意图 Δμ≠ 0的分子振动: 不对称分子,如HCl,振动时有偶极矩变化,有红外活性。产生红外吸收光谱。 Δμ= 0的分子振动: 同核双原子分子如N2、O2、Cl2等,振动时偶极矩为零,非红外活性,不能产生红外吸收光谱。 对称多原子分子,如CO2,对称伸缩振动无红外活性,其它振动存在着偶极矩的变化,仍有红外活性,可以观察到红外光谱。 2. 分子振动方程式 (1)经典力学处理 双原子分子化学键的振动类似于简谐振动。 1 =2k v πμ 1212 =m m m m μ+虎克定律: m 1 m 2 k :化学键的力常数,与键能和键长有关, μ:双原子的折合质量 (2) 量子力学处理 双原子分子的振动能:E 振 =(V+1/2)h ν V :振动量子数,且V=0,1,2…,n ;(量子化) ν:化学键的振动频率, ΔE 振 =(V 2+1/2)h ν –(V 1+1/2)h ν = ΔV h ν 分子吸收红外辐射后振动能级由基态跃迁至激发态,能量差为: 1 =2k v πμ ;μπk 21k 越大,μ越小,v 越大,吸收峰将出现在高波数区。 分子吸收红外辐射后振动能级发生跃迁的必要条件之一: h νL = ΔV h ν,式中, νL 红外辐射频率;ν 分子振动频率。 能级跃迁主要是若由基态V = 0 跃迁至第一激发态 V = 1,即,ΔV = 1,所以: h νL = h ν。 , 或:μμπσk k c 130721==由此,νL = ν = 分子振动方程式 (1)首先依据谱图推出化合物碳架类型:根据分子式计算不饱和度,公式: 不饱和度=F+1+(T-O)/2 其中: F:化合价为4价的原子个数(主要是C原子), T:化合价为3价的原子个数(主要是N原子), O:化合价为1价的原子个数(主要是H原子), (2)分析3300~2800cm-1区域C-H伸缩振动吸收;以3000 cm-1为界:高于3000cm-1为不饱和碳C-H伸缩振动吸收,有可能为烯,炔,芳香化合物,而低于3000cm-1一般为饱和C-H伸缩振动吸收; (3)若在稍高于3000cm-1有吸收,则应在2250~1450cm-1频区,分析不饱和碳碳键的伸缩振动吸收特征峰,其中: 炔2200~2100 cm-1 烯1680~1640 cm-1 芳环1600,1580,1500,1450 cm-1 若已确定为烯或芳香化合物,则应进一步解析指纹区,即1000~650cm-1的频区,以确定取代基个数和位置(顺反,邻、间、对); (4)碳骨架类型确定后,再依据其他官能团,如C=O, O-H, C-N 等特征吸收来判定化合物的官能团; (5)解析时应注意把描述各官能团的相关峰联系起来,以准确判定官能团的存在,如2820,2720和1750~1700cm-1的三个峰,说明醛基的存在。 一些常见常用的健值 1.烷烃: C-H伸缩振动(3000-2850cm-1) C-H弯曲振动(1465-1340cm-1) 一般饱和烃C-H伸缩均在3000cm-1以下,接近3000cm-1的频率吸收。 2.烯烃: 烯烃C-H伸缩(3100~3010cm-1) C=C伸缩(1675~1640 cm-1) 烯烃C-H面外弯曲振动(1000~675cm-1)。 3.炔烃: 伸缩振动(2250~2100cm-1) 炔烃C-H伸缩振动(3300cm-1附近)。 4.芳烃: 3100~3000cm-1 芳环上C-H伸缩振动 1600~1450cm-1 C=C 骨架振动 880~680cm-1 C-H面外弯曲振动 芳香化合物重要特征:一般在1600,1580,1500和1450cm-1可能出现强度不等的4个峰。880~680cm-1,C-H面外弯曲振动吸收,依苯环上取代基个数和位置不同而发生变化,在芳香化合物红外谱图分析中,常常用此频区的吸收判别异构体。 5.醇和酚: 主要特征吸收是O-H和C-O的伸缩振动吸收, O-H 自由羟基O-H的伸缩振动:3650~3600cm-1,为尖锐的吸收峰, 红外光谱分析 序言 二十世纪初叶,Coblentz发表了一百多个有机化合物的红外光谱图,给有机化学家提供了鉴别未知化合物的有力手段。到四十年代红外光谱技术得到了广泛的研究和应用。当今红外光谱仪的分辨率越来越高,检测范围扩展到10000-200cm-1,样品量少至微克级。红外光谱提供的某些信息简捷可靠,检测样品中有无羰基及属于哪一类(酸酐、酯、酮或醛)是其他光谱技术难以替代的。因此,对从事有机化合物为研究对象的化学工作者来说,红外光谱学是必需熟悉和掌握的一门重要光谱知识。 一、基本原理 1、基本知识 光是一种电磁波。可根据电磁波的波长范围分成不同类型的光谱,它们各自反映出物质的不同类型的运动形式。表1列出这些电磁波的波长,其所在区域的光谱名称,以及对应的运动形式。 红外光谱研究的内容涉及的是分子运动,因此称之为分子光谱。 通常红外光谱系指2-25μ之间的吸收光谱,常用的为中红外区4000-650cm-1(2.5-15.4μ)或4000-400cm-1。 这段波长范围反映出分子中原子间的振动和变角振动,分子在振动运动的同时还存在转动运动。在红外光谱区实际所测得的图谱是分子的振动与转动运动的加合表现,即所谓振转光谱。 每一化合物都有其特有的光谱,因此使我们有可能通过红外光谱对化合物作出鉴别。 红外光谱所用的单位波长μ,波数cm-1。光学中的一个基本公式是λυ= C,式中λ为波长,υ为频率,C为光速(3×1010cm/s)。设υ为 波数,其含义是单位长度(1cm)中所含的波的个数,并应具有以下关系:波数(cm-1)=104/波长(μ) 波长和波数都被用于表示红外光谱的吸收位置,即红外光谱图的横坐标。目前倾向于普遍采用波数为单位,而在图谱上方标以对应的波长值。红外光谱图的纵坐标反映的是吸收强度,一般以透过率(T%)表示。 2、红外光谱的几种振动形式 主要的基本可以分为两大类:伸缩振动和弯曲振动。 (1)伸缩振动(υ) 沿着键轴方向伸或缩的振动,存在对称与非对称两种类型。它的吸收频率相对在高波数区。 (2)弯曲振动(δ) 包括面内、面外弯曲振动,变角振动,摇摆振动等。它的吸收频率相对在低波数区。 4000cm-1(高) 400cm-1(低)波谱分析答案
红外光谱分析
分析化学_ 波谱分析法1-4讲_82 红外吸收光谱法基本原理_
实用红外光谱解析
红外光谱分析77952