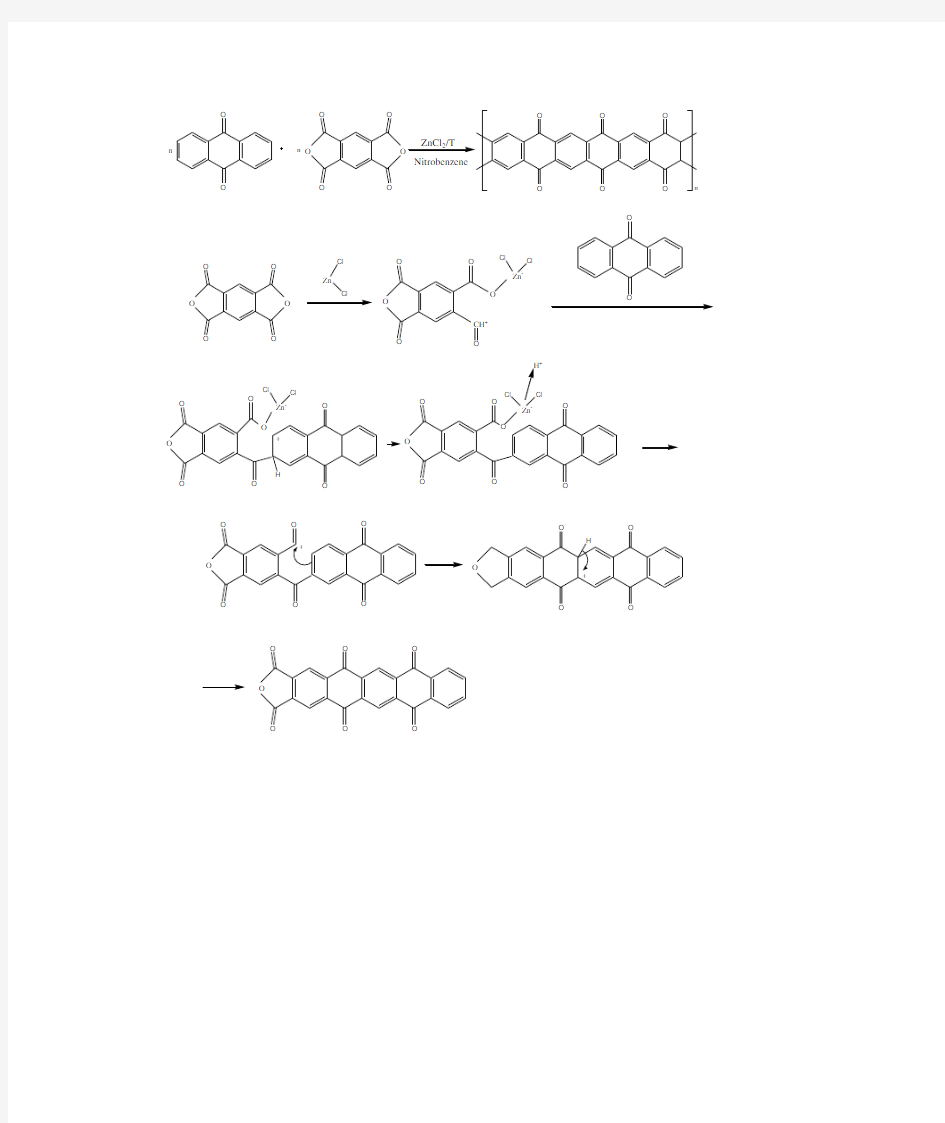
O O n O O O
O n O O O O
Zn
Cl O O O
O CH +O
O Zn -Cl Cl
O O O O O O O Zn
-Cl
Cl
H
+O
O
O
O O O O
O
烷基化反应的机理 石油炼制过程中的烷基化反应是指在酸性催化剂的作用下,烷烃分子与烯烃分子的化学加成反应,在反应过程中烷烃分子中的活泼氢原子的位置被烯烃所取代。由于异构烷烃中叔碳原子上的氢原子比正构烷烃中伯碳原子上的氢原子活泼得多,因此参加烷基化反应的烷烃为异构烷烃,一般特指异丁烷。 烷基化原料是以催化裂化液化气中异丁烷和异丁烯、丁烯-1为主。烷基化常用的酸性催化剂有硫酸、氢氟酸、三氯化铝等,本装置使用的催化剂为硫酸。 正碳离子的概念 在研究各种有机化学反应的时候,人们发现各种有机反应中间产物大体可以分为3种类型:自由基、阳离子、阴离子。烷基化反应属于其中的阳离子反应,即生成了正碳离子。随着人们对烷基化反应机理的不断探索与认识的日渐成熟,人们普遍接收的是正碳离子——链式反应机理。 所谓正碳离子是一个带正电荷的碳原子,它只有6个外层电子,是缺电荷的,其通式可以写为: 围绕正碳离子的取代物可以是氢原子,也可以是甲基基团,其四种形式分别为: 其稳定性从左到右依次增大,也就是说叔碳原子的正碳离子是最稳定的。这里所说的稳定性是相对而言的,总体来说,各种正碳离子都是极不稳定的,很容易进一步参与反应。只有当其与另一对电子成键以后,也就是说,当这个碳原子周围有了8个电子以后,它才能说是真正稳定了。 正碳离子与另一对电子成键的最常见的形式是加合一个负离子。这是正碳离子的最后一步反应,但却开始了另一个正离子的进程。 正碳离子的化学行为 以酸为催化剂的烷基化反应中,酸所提供的氢质子与烯烃的加成反应是产生正碳离子的主要反应。 C H H H CH 3 CH 3 CH 3CH 3 CH 3 CH 3 H H H C C C C
傅-克反应 傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877 年由法国化学家查尔斯傅里德(Friedel C)和美国化学家詹姆斯克拉夫茨(Crafts J)共同发现。该反应主要分为两类:烷基化反应和酰基化反应。 (* ch° gj * Mc, 傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应 傅-克烷基化反应 傅-克烷基化反应在强路易斯酸的催化下使用卤代轻对一个芳环进行烷基化。 假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。总反应式如下: 傅-克烷基化机理 这类反应有个严重缺点:由丁烷基侧链的供电性,反应产物比起原料具有更高的亲核性,丁是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化现象而形成了众多副产物。由丁这类反应是可逆的,还可能出现烷基被其他基团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的问位产物。另外如果氯不是处丁三级碳原子(叔碳原子)上,还有可能发生碳正离子重排反应,而这取决丁碳正离子的稳定性:即三级碳>二级碳>一级碳。空间位阻效应可以被利用丁限制烷基化的数量,比如1, 4-二甲氧基苯的叔丁基化反应。
1,4-二甲氧基苯的叔丁基化 烷基化的底物并不局限丁卤代轻类,傅-克烷基化可以使用任何的碳正离子中问体参与反应,如一些烯轻,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应: 1-氯-2-甲基-2-苯基丙烷的合成 通过烯轻的傅-克烷基化 在这个反应中三氟甲磺酸使被认为在卤离子形成中活化了NBS的供卤素能 力。 傅-克去烷基化反应 傅-克烷基化是一个可逆反应。在逆向傅-克反应或者称之为傅-克去烷基化反应当中烷基可以在质子或者路易斯酸的存在下去除。例如,在用漠乙烷对苯的多 重取代当中,由丁烷基是一个活化基团,原来期待能够得到邻对位取代的产物。然而真正的反应产物是1,3,5-三乙基苯,即所有烷基取代都是问位取代。热力学反应控制使得该反应产生了热力学上更稳定的问位产物。通过化学平衡,问位产 物比起邻对位产物降低了空间位阻。因此反应最终的产物是一系列烷基化与去烷基化共同作用的结果。 1,3,5-三乙基苯的合成 傅-克酰基化反应 傅-克酰基化反应是在强路易斯酸做催化剂条件下,让酰氯与苯环进行酰化的反应。此反应还可以使用埃酸酎作为酰化试剂,反应条件类似丁烷基化反应的条
《药物合成技术》 习题集 适用于制药技术类专业 第一章概论 一、本课程的学习内容和任务是什么?学好本课程对从事药物及其中间体合成工作有何意义? 二、药物合成反应有哪些特点?应如何学习和掌握? 三、什么是化学、区域选择性?举例说明。 四、什么是导向基?具体包括哪些类型?举例说明。 五、药物合成反应有哪些分类方法?所用试剂有哪些分类方法?举例说明。 六、查资料写一篇500字左右的短文,报道药物合成领域的新技术及发展动态? 第二章卤化技术(Halogenation Reaction) 一、简答下列问题 1.何为卤化反应?按反应类型分类,卤化反应可分为哪几种?并举例说明。 2.在药物合成中,为什么常用卤化物作为药物合成的中间体? 3.在较高温度或自由基引发剂存在下,于非极性溶剂中,Br 2 和NBS都可用于烯丙位和苄位的溴取代,试比较它们各自的优缺点。 4.比较X 2 、HX、HOX对双键离子型加成的机理、产物有何异同,为什么? 5.解释卤化氢与烯烃加成反应中,产生马氏规则的原因(用反应机理)。为什么Lewis酸能够催化该反应? 6.解释溴化氢与烯烃加成反应中,产生过氧化效应的原因? 7.在羟基卤置换反应中,卤化剂(HX、SOCl 2、PCl 3 、PCl 5 )各有何特点,它们的 使用范围如何? 二、完成下列反应 三、为下列反应选择合适的试剂和条件,并说明原因。 四、分析讨论 1.试预测下列各烯烃溴化(Br 2/CCl 4 )的活性顺序。
2.在乙胺嘧啶中间体对氯氯苄的制备中,有如下两条路线,各有何特点?试讨论其优缺点。 3.以下是三种制备溴乙烷的方法,其中哪种适合工业生产,哪种适合实验室制备? 4.在氯霉素生产过程中,对-硝基-α-溴代苯乙酮的制备时, (1)反应有无催化剂?若有,属于哪种催化剂? (2)将对硝基苯乙酮与溶于氯苯中,加热至24-25℃,滴加少量溴,当有HBr生成并使反应液变色则可继续加溴,否则需升温至50℃直至反应开始方可继续滴加溴,为什么? (3)反应毕开大真空排净溴化氢,反应过程中溴化氢也不断移走,是不是移得越净越有利于反应?为什么? (4)生产过程中,影响因素有哪些? 第三章烷基化技术 (Hydrocarbylation Reaction ,Alkylation) 一、解释概念及简答 1.常用的烃化剂有哪些?进行甲基化及乙基化时,应选择哪些烃化剂?引入较大烃基时应选用哪些烃化剂? 2.什么叫相转移催化反应?其原理是什么?采用相转移催化技术有什么优点? 3.利用Gabriel反应与Delepine反应制备伯胺时,有什么相同与不同点? 4.什么是羟乙基化反应?在药物合成中有什么特别的意义? 5.进行F-C烃化反应时,芳香族化合物结构、卤代烃对反应有何影响?常用哪些催化剂?如何选择合适的催化剂。 6.若在活性亚甲基上引入两个烃基,应如何选择原料和操作方法?并解释原因。 二、利用Williamson法制混合醚时,应合理选择起始原料及烃化试剂,试设计下列产品的合成方法,并说明原因,掌握其中的规律。 三、完成下列反应 四、为下列反应选择适当的原料、试剂和条件,并说明依据。 五、利用所给的原料,综合所学知识合成下列产品 1.以甲苯、环氧乙烷、二乙胺为主要原料,选择适当的试剂和条件合成局麻药盐酸普鲁卡因。 2.以乙苯为主要原料,选择适当的试剂和条件合成氯霉素中间体对硝基-α-胺基
傅克反应
傅-克反应 傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨(Crafts J)共同发现。该反应主要分为两类:烷基化反应和酰基化反应。 傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应 傅-克烷基化反应 傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。总反应式如下: 傅-克烷基化机理 这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化现象而形成了众多副产物。由于这类反应是可逆的,还可能出现烷基被其他基团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间位产物。另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。空间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化反应。
1,4-二甲氧基苯的叔丁基化 烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应: 1-氯-2-甲基-2-苯基丙烷的合成 曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。 通过烯烃的傅-克烷基化 在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。 傅-克去烷基化反应 傅-克烷基化是一个可逆反应。在逆向傅-克反应或者称之为傅-克去烷基化反应当中烷基可以在质子或者路易斯酸的存在下去除。例如,在用溴乙烷对苯的多重取代当中,由于烷基是一个活化基团,原来期待能够得到邻对位取代的产物。然而真正的反应产物是1,3,5-三乙基苯,即所有烷基取代都是间位取代。热力学反应控制使得该反应产生了热力学上更稳定的间位产物。通过化学平衡,间位产物比起邻对位产物降低了空间位阻。因此反应最终的产物是一系列烷基化与去烷基化共同作用的结果。
2-Methyl-4-ethoxalylcyclopentane-1,3,5-trione. A solution of sodium ethoxide is prepared in a 2-l. three-necked, round-bottomed flask fitted with a mercury-sealed stirrer, a reflux condenser carrying a drying tube, and a stopper by the addition of 69.0 g. (3 moles) of sodium to 950 ml. of absolute ethanol. 69.0g (3mol)钠和950ml无水乙醇在配有干燥回流冷凝管和汞封搅拌器的2L三口圆底烧瓶中制备乙醇钠。The solution is cooled to 0–5° in an ice bath and stirred.溶液在0-5℃下冰浴搅拌。The stopper is replaced by a dropping funnel, and a cold mixture (5–15°) of 108 g. (1.50 moles) of freshly distilled 2-butanone and 482 g. (3.30 moles) of diethyl oxalate(Note 1) is added gradually over a period of 30 minutes.瓶塞用分液漏斗取代,108g(1.5mol)的丁二酮和482g(3.3mol)的乙二酸二乙酯在5-15℃下低温混合,在30分钟内逐步滴加到溶液中。After the addition is complete, the thick, orange-red mixture is allowed to warm with continued stirring to room temperature, heated under reflux for 30 minutes, and cooled again to 0° in an ice bath. 完全加入后,橘红色的粘稠物继续搅拌至室温,加热回流30分钟后在冰浴中冷却至0℃。The mixture is decomposed by stirring with 165 ml. of sulfuric acid (1:1 by volume) added in portions.将165ml浓硫酸(体积比1:1)在搅拌加入,分解混合物。The sodium sulfate formed is filtered by suction and washed with ethanol (150–200 ml.) (Note 2). 硫酸钠抽滤后用乙醇(150–200 ml)洗涤。The washings and filtrate are combined and concentrated by evaporation .合并滤液和洗涤液后蒸发浓缩。The yellowish brown product which accumulates by slow crystallization is collected by filtration, washed with small quantities of ice-cold water, and dried in air.过滤缓慢析出的棕黄色产品用小剂量的冰水洗涤后在空气中干燥。The crude product weighs 140–150 g.粗产品 140-150g。Further evaporative concentration of the mother liquor followed by cooling furnishes an additional 40–50 g. of the keto ester,此外将母液用冷冻蒸发浓缩后又得到40-50g的酮酯。bringing the total yield to 180–200 g. (53–59%)产品总共180-200g(产率53-59%)(Note 2). This crude material (m.p. 120–130°) is used in the next step.粗品(熔点120–130℃)用于下一步中A pure sample can be obtained by crystallization from ethyl acetate after treatment with Norit activated carbon, m.p. 160–162°.纯品是经过活性炭处理后在乙酸乙酯中结晶得到,熔点160–162℃。 The procedure for 2- pyrrolealdehyde 2-吡咯甲醛 In a 3-l. three-necked round-bottomed flask, fitted with a sealed stirrer, a dropping funnel, and a reflux condenser, is placed 80 g. (1.1 moles) of dimethylformamide (Note 1).在配有封闭搅拌器、滴液漏斗和冷凝回流装置的三口圆底烧瓶中放入80g(1.1mol)的二甲基甲酰胺。The flask is immersed in an ice bath, and the internal temperature is maintained at 10–20°, while 169 g.
第一章绪论 1、药物合成反应中反应类型有哪些? ①按有机分子的结构变换方式分:新基团的导入反应;取代基的转化反应;有机分子的骨架。 ②按反应机制分:极性反应(a?亲核试剂、b.亲电试剂);自由基反应;协同反应 2、药物合成反应主要研究对象:化学合成药物 3、化学品的安全使用说明书一一MSDS 4、原子经济性反应:“原子经济性”是指在化学品合成过程中,合成方法和工艺被设计成能把反应过程中使用的所有原料尽可能多的转化到最终产物中。 5、三废:废气、废水、废渣 第二章硝化反应 1、混酸硝化试剂的特点有哪些? ①硝化能力强;②氧化性较纯硝酸小;③对设备的腐蚀性小 2、硝化试剂的活泼中间离子为:硝酰正离子NO?十 3、桑德迈尔反应定义及应用 定义:在氯化亚铜或漠化铜的存在下,重氮基被氮或漠置换的反应;重氮基被氧基置换:将重氮盐与氧化亚铜的配合物在水介质中作用,可以使重氮基被氧基置换,该反应也称Sandmeyer反应。 应用:CuX+Ar-N2X ---------- >Ar-X+N2(X:CI,Br,?CN) 4、常用的重氮化试剂 一般是由盐酸、硫酸、过氯酸和氟硼酸等无机酸与亚硝酸钠作用产生。 5、硝化艮应定义:指向有机分子结构屮引入硝基(一NO?)的反应过程,广义的硝化反应包括生产(C—NO2、N —1\1。2和0—反应。 6、重氮化反应定义:含有伯氨基的有机化合物在无机酸的存在下与亚硝酸钠作用牛成重氮盐的反应。 7、硝化剂:单一硝酸、硝酸和各种质子酸、有机酸、酸酹及各种Lewis酸的混合物。 8、生成硝基烷桂的难易顺序: 卤代怪中卤素被取代的顺序: 9、DMF: DMSO: 10、常用的重氮化试剂有哪些?NaNO2+HCI/H2SO4 第三章卤化反应 1、Ph上取代基对卤化反应的影响 ①催化剂的影响;
傅-克反应,又称傅列德尔-克拉夫茨反应(Friedel –Crafts reaction ),由法国化学家查尔斯?傅列德尔与美国化学家詹姆斯?克拉夫茨于1877年,共同发现,是一类针对芳香族的亲电取代反应。根据取代物的不同,该反应主要分为傅列德尔-克拉夫茨烷基化反应和傅列德尔-克拉夫茨酰基化反应。由于傅-克反应是实现碳碳成键的最有效方式之一,并且是制备各种芳基酮, 杂环芳烃酮等的重要手段, 所以它在医药、农药、染料、香料等工业生产中具有非常广泛的应用。在聚合物合成上与之相关的是一类高性能工程材料,聚(醚)砜和聚(醚)酮。1962年,Dupont 公司的Bonner ,首次采用傅克反应合成了聚醚酮酮(PEKK )。 傅克反应机理如下所示: S O O Cl C O Cl O O AlCl 4 + C O AlCl 3 O -H S O O 聚(醚)砜和聚(醚)酮类聚合物按傅克亲电取代路线合成时,由于所用单体大多来源方便、价格低廉,而且合成反应容易控制,不需要高温和真空条件,反应条件温和,因此聚合物大多成本低,容易得到推广应用。一般反应条件为在无水AlCl 3和N ,N-二甲基甲酰胺(DMF )存在下,于1,2-二氯乙烷(DCE )中进行低温(冰水浴)共缩聚反应。 然而,聚合过程中被带正电荷的亲电试剂进攻的苯环上的5个氢具有相等的活性,尽管由于空间位阻的作用对位的氢最易于脱去,然而其他的氢仍有可能被亲电试剂进攻,这样就必然得到有一定程度支化和交联的聚合物。支化、交联反应一般会降低树脂的性能,导致高温流动性差,冲击强度低,脆性大,后加工困难等。在支化、交联严重时,将得不到具有使用价值的反应产物。
-` 烷基化反应的机理 石油炼制过程中的烷基化反应是指在酸性催化剂的作用下,烷烃分子与烯烃分子的 化学加成反应,在反应过程中烷烃分子中的活泼氢原子的位置被烯烃所取代。由于异构 烷烃中叔碳原子上的氢原子比正构烷烃中伯碳原子上的氢原子活泼得多,因此参加烷基 化反应的烷烃为异构烷烃,一般特指异丁烷。 烷基化原料是以催化裂化液化气中异丁烷和异丁烯、丁烯-1 为主。烷基化常用的酸 性催化剂有硫酸、氢氟酸、三氯化铝等,本装置使用的催化剂为硫酸。 4.1 正碳离子的概念 在研究各种有机化学反应的时候,人们发现各种有机反应中间产物大体可以分为3种类型:自由基、阳离子、阴离子。烷基化反应属于其中的阳离子反应,即生成了正碳 离子。随着人们对烷基化反应机理的不断探索与认识的日渐成熟,人们普遍接收的是正 碳离子——链式反应机理。 所谓正碳离子是一个带正电荷的碳原子,它只有6个外层电子,是缺电荷的,其通式 可以写为: C 围绕正碳离子的取代物可以是氢原子,也可以是甲基基团,其四种形式分别为: H H H CH3 H C H CH3 C H CH3 C CH3CH3 C CH3 其稳定性从左到右依次增大,也就是说叔碳原子的正碳离子是最稳定的。这里所说 的稳定性是相对而言的,总体来说,各种正碳离子都是极不稳定的,很容易进一步参与 反应。只有当其与另一对电子成键以后,也就是说,当这个碳原子周围有了8个电子以后,它才能说是真正稳定了。 正碳离子与另一对电子成键的最常见的形式是加合一个负离子。这是正碳离子的最 后一步反应,但却开始了另一个正离子的进程。 4.2正碳离子的化学行为 以酸为催化剂的烷基化反应中,酸所提供的氢质子与烯烃的加成反应是产生正碳离 子的主要反应。
傅克反应 傅-克反应 傅-克(傅瑞德尔-克拉夫茨)反应:芳香烃在无水AlCl3作用下,环上的氢原子也 能被烷基和酰基所取代。这是一个制备烷基烃和芳香酮的方法,称为Friedel —Crafts 反应,简称傅-克反应。苯环上有强吸电子基(如-NO2 、-SO3H 、-COR) 时,不发生傅-克反应。 a、烷基化反应:卤代烷在AlCl3的作用下生成C+,C+在进攻苯环之前会发 生重排成稳定的C+(三个C以上) 烷基化反应的缺点是副反应的发生 b、硝基化反应:常用的硝基化试剂是酰卤,此外还可以用酸酐。优点是产物 较纯。 一般用Clemmensen还原法可以得到丙苯。 济南盛信达科技有限公司 燕山学院工作室最新招聘信息加入时间:2008-3-13 11:24:44 单位信息 单位名称:济南盛信达科技有限公司单位所在地:山东省济南市高新区 成立时间:单位性质:其他企业 所属行业:制造业 单位简介 济南盛信达科技有限公司,国家重点高新技术企业,具有自营进出口权。为外向型科集研发、外贸、营销于一体.公司几大产品均为国内首创或专利产品。公司先后获得“国省高新技术企业”等荣誉称号。
--------------------------------------------------------------------------- 职位信息 职位名称:其它科研人员类职位招聘时间: 2008-03-13 至 2008-05-20 招聘人数: 2 工作经验: 工作地点:山东省济南市 职位描述:家在济南优先 专业要求:应用化学 ------------------------------------------------------------------------职位名称:企业后勤管理招聘时间: 2008-03-13 至 2008-04-10 招聘人数: 1 工作经验: 工作地点:山东省济南市 职位描述: 专业要求:工商企业管理 ------------------------------------------------------------------------职位名称:企业/业务发展经理招聘时间: 2008-03-13 至 2008-05-01 招聘人数: 2 工作经验: 工作地点:山东省济南市 职位描述:
Friedel-Crafts反应机理 摘要:本文总结了傅-克反应提出以来,化学研究人员对该反应的机理方面的研究,包括动力学研究、中间体结构和性质的。提出傅一克反应机理目前存在的疑问及机理动力学的发展方向。 关键词:傅-克反应;动力学;中间体;反应机理 1、傅-克反应的发现 傅-克反应在整个化学发展史上是最为古老的化学之一[1]。1869年德国化学家Zincke[2]首次报道了在苯环上引入烷基的反应.这个反应的发现来源于一个偶然,当时Zincke想从苄氯和氯乙酸(以苯作为溶剂)出发,在铜粉(或银粉)和密封加热的条件下,通过类似Wurtz反应的方法制各苯丙酸,但他发现在反应过程中有大量的氯化氢产生,同时也生成了二苯甲烷。他意识到这是苄氯和溶剂苯发生反应产生的。为此,在接下来的几年里,他开始研究这类苯环上引入取代基的反应。Zincke的发现引起了化学家们的广泛关注,他们用不同芳烃进行反应,并且得到了相应芳烃的烷基化和酰基化产物.至此,他们一致认为铁、铜、银或锌等金属粉末可以作为此类反应的催化剂,这个反应也因此被命名为Zincke反应。 1877年,Friedel和Crafts[3-4]试图通过Gustavson反应将1,1,1一三氯乙烷(苯作溶剂)在铝粉和碘单质存在条件下转化为1,1,1.三碘乙烷,但出乎意料的是他们再次得到了Zincke反应的产物。经过他们的不断研究,他们又对各种金属卤化物、各种卤代烃以及各种酰卤分别进行了研究,表明Zincke提出的各种金属确实不是此类反应的催化剂,它们的卤代物才是真正意义上的催化剂。至此傅一克反应被正式提出,包括傅一克烷基化反应和傅一克酰基化反应。
烷基化反应 专 题 报 告 班级: 学号: 姓名: 完成日期:
烷基化反应专题报告 前言 随着我国国民经济可持续发展国策的实施,汽车排放尾气对空气的污染问题成为我们关注的焦点,我国石油炼制工业面临的最关键问题就是如何生产符合国家日益严格的环保标准的清洁燃料,以满足国内交通行业和市场的需求。 石油炼制过程中的烷基化反应是指在酸性催化剂的作用下,烷烃分子与烯烃分子的化学加成反应,在反应过程中烷烃分子中活泼氢原子的位置被悉听所取代,由于异构烷烃中叔碳原子上的氢原子比正构烷烃中碳原子上的氢原子活泼的多,因此参加烷基化反应烷烃。反应生成异辛烷(烷基化汽油)的催化反应过程。 烷基化汽油具有以下特点:该种汽油具有辛烷值高(RON95~98) 、敏感性低(RON 与MON 之差一般≤3) 康保性能好;蒸汽压低、燃烧热值高、不含烯烃芳烃硫含量也低。燃烧完全而清洁,不污染环境等优点,是航空汽油和车用汽油的理想调和油。真是由于烷基化的各种优点,使它成为石油加工过程的重要过程之一,越来越受到广泛关注。 烷基化原理及影响因素 一、烷基化原理 碳四烷基化遵循正碳离子反应机理,其过程主要包含四个步骤: 步骤1:叔丁基正碳离子的生成
步骤2:叔丁基正碳离子与丁烯加成生成碳八正碳离子 叔丁基正碳离子与不同的丁烯异构体进行烷基化反应可以生成不同的碳八正碳离子。 TMP+和DMH+分别是三甲基戊烷和二甲基己烷的正碳离子。TMP组分是烷基化油中的理想组分,具有较高的辛烷值(RON 100~109),而DMH的辛烷值较低(RON 55~76),DMH组分的大量存在会降低烷基化油的品质。 步骤3:碳八正碳离子的异构 生成的碳八正碳离子会通过氢转移或甲基转移而生成更稳定的正碳离子。 步骤4:氢转移形成碳八异构烷烃
傅克反应总结材料 傅克反应总结材料 1. 傅克反应的发现: 在这些反应中,以制备芳烃和芳酮是主要的。 2. 傅克反应的反应机理 注意以下三种情形下的反应: A. 烷基正离子的重排(稳定性:叔>仲>伯) 因此反应中都有异构体产物的出现。如: B. 烷基取代不会停留在一取代阶段 于烷基是供电子基团,已取代后芳环上电子云密度增大,使得亲电取代反应更容易进行,所以取代还会继续进行下去,最后可以全部取代。如: 但是有些基团于位阻关系,只能得到已取代的产物。 如果取代基团是酰基,于酰基是吸电子基团,使得芳环电子云密度减小,使得亲电取代反应比较困难,反应一步后会停下来,所以傅克酰化合成芳酮更为有用。 C. 定文问题: 下面的例子将让我们更好的去理解定位问题:
3. 傅克反应的催化剂 路易氏酸,强酸,酸酐,酰氯和一些中性化合物和元素等。 特别需要注意以下及点: A.不同催化剂产生不桶产物: B.不同催化剂产率有很大的差别: C. 氯化物作为催化剂要无水,但是绝对无水活性反而不大,甚至不能进行。有些反应还需要把催化剂暴露在空气中吸水几分钟后,才能催化反应的进行。 4. 傅克反应所用的烷基化剂 A. 常用的是氯化物,活泼性次序RCl>RBr>RI B. 烯类也是很好的烷基化剂,催化剂用BF3和HF效果很好。 C. 醇类也可作为烷基化剂,但是催化剂用BF3和HF效果最好。 5. 酰基取代剂 A. 酰卤 活性顺序为: B. 酸酐也是很好的酰化剂,但是它需要比酰卤多50%的氯化铝。 C. 羧酸也可以直接用作酰化剂,但催化剂不宜用氯化铝,而要用硫酸,磷酸,最好是氟化氢。
6. 芳环 芳环和杂环化合物都能参加F-C反应,其中并环和稠环更易发生反应,杂环中,呋喃类,吡咯类等虽对酸敏感,但在适当情况下也可发生F-C反应。 如环上有供电子基团,可用较若的反应条件。如有吸电子基团,则要用较强的反应条件。 稠环的定位问题: 7. 芳酸的环化 首先要考虑形成环的稳定性,一般是6元环>5元环>7元环 8. 实验操作: 傅克反应总结材料 1. 傅克反应的发现: 在这些反应中,以制备芳烃和芳酮是主要的。 2. 傅克反应的反应机理
第4章烷基化反应 §4-1 C-烷基化反应 一、芳环上的C-烷基化反应 1.烷基化剂:卤代烷,烯烃,醇,醛,酮 2.催化剂:Lewis酸:AlCl3> SbCl5 >FeCl3> BF3> ZnCl2——卤烷,烯烃质子酸:HF > H2SO4> H3PO4——醇,醛,酮,烯烃 3.反应历程:芳香族亲电取代 4.反应特点: (1)连串反应 (2)可逆反应-烷基的转移和岐化 *苯过量
(3)烷基重排 (4)取代苯环再次引入烷基时的位置与反应条件有关温和条件下:亲电取代反应规律 强烈条件下:非规律性产物 5.反应实例: (1)用卤烷的烷基化反应 ——长碳链烷基苯的合成:十二烷基苯 *催化剂:AlCl3 **重排 (2)用烯烃的烷基化反应 *催化剂:AlCl3-HCl, BF3 or 载于硅藻土上的H3PO4 **苯过量 (3)用醇的烷基化反应
(4)用醛酮的烷基化反应 ——制备二芳基或三芳甲烷衍生物 二、活泼亚甲基化合物的烷基化反应——强碱催化 三、炔烃的烷基化反应
§4-2 N-烷基化反应 一、取代型N-烷基化反应 机理: RZ—烷基化剂Z=-OH, -X, -OSO3H 醇:活性弱,强酸(HX, H2SO4, H3PO4)催化,高温(200℃),价廉:甲醇,乙醇,异丙醇,丁醇——活泼胺 卤烷:活性高,价格较高,不可逆反应,生成卤化氢(成盐),加碱(氢氧化钙,氢氧化钠,碳酸钠)中和—引入长碳链烷基,不活泼胺或季胺化 强酸的酯类:(RO)3PO, (RO)2SO2——活性强,价格最高,有毒 脂肪胺>卞胺>芳胺 实例: (1)醇
(2)卤烷 (3)酯 二、加成型N-烷基化反应——亲电加成 烷基化剂:烯烃衍生物—丙稀睛,丙烯酸,丙烯酸酯 ——活性弱,需加催化剂,酸性(HAc,HCl,H2SO4)或碱性(三甲胺,三乙胺) 环氧化物—环氧乙烷,环氧氯乙烷等 ——活性强(酸碱催化开环),爆炸(用量为理论量的30~50%,通N2) 三、缩合还原型N-烷基化反应 烷基化剂——醛酮
烷基化反应的机理 Company number:【0089WT-8898YT-W8CCB-BUUT-202108】
烷基化反应的机理 石油炼制过程中的烷基化反应是指在酸性催化剂的作用下,烷烃分子与烯烃分子的化学加成反应,在反应过程中烷烃分子中的活泼氢原子的位置被烯烃所取代。由于异构烷烃中叔碳原子上的氢原子比正构烷烃中伯碳原子上的氢原子活泼得多,因此参加烷基化反应的烷烃为异构烷烃,一般特指异丁烷。 烷基化原料是以催化裂化液化气中异丁烷和异丁烯、丁烯-1为主。烷基化常用的酸性催化剂有硫酸、氢氟酸、三氯化铝等,本装置使用的催化剂为硫酸。 正碳离子的概念 在研究各种有机化学反应的时候,人们发现各种有机反应中间产物大体可以分为3种类型:自由基、阳离子、阴离子。烷基化反应属于其中的阳离子反应,即生成了正碳离子。随着人们对烷基化反应机理的不断探索与认识的日渐成熟,人们普遍接收的是正碳离子——链式反应机理。 所谓正碳离子是一个带正电荷的碳原子,它只有6个外层电子,是缺电荷的,其通式可以写为: 围绕正碳离子的取代物可以是氢原子,也可以是甲基基团,其四种形式分别为: 其稳定性从左到右依 次增 大,也就是说叔碳原子的正碳离子是最稳定的。这里所说的稳定性是相对而言的,总体来说,各种正碳离子都是极不稳定的,很容易进一步参与反应。只有当其与另一对电子成键以后,也就是说,当这个碳原子周围有了8个电子以后,它才能说是真正稳定了。 正碳离子与另一对电子成键的最常见的形式是加合一个负离子。这是正碳离子的最后一步反应,但却开始了另一个正离子的进程。 正碳离子的化学行为 以酸为催化剂的烷基化反应中,酸所提供的氢质子与烯烃的加成反应是产生正碳离子的主要反应。 如果烯烃与氢质子反应生成的了伯碳原子或仲碳原子上的正碳离子,它们有可能重排或异构化为稳定性相对较高的正碳离子。 如: H H H CH 3 CH 3 CH 3CH 3 CH 3 CH 3 H H H C C C C
傅克反应 摘要:本文总结了傅-克反应提出以来,化学研究人员对该反应的机理方面的研究,包括动力学研究、中间体结构和性质的。提出傅一克反应机理目前存在的疑问及机理动力学的发展方向。 关键词:傅-克反应;动力学;中间体;反应机理 1、傅-克反应的发现 傅-克反应在整个化学发展史上是最为古老的化学之一[1]。1869年德国化学家Zincke[2]首次报道了在苯环上引入烷基的反应.这个反应的发现来源于一个偶然,当时Zincke想从苄氯和氯乙酸(以苯作为溶剂)出发,在铜粉(或银粉)和密封加热的条件下,通过类似Wurtz反应的方法制各苯丙酸,但他发现在反应过程中有大量的氯化氢产生,同时也生成了二苯甲烷。他意识到这是苄氯和溶剂苯发生反应产生的。为此,在接下来的几年里,他开始研究这类苯环上引入取代基的反应。Zincke的发现引起了化学家们的广泛关注,他们用不同芳烃进行反应,并且得到了相应芳烃的烷基化和酰基化产物.至此,他们一致认为铁、铜、银或锌等金属粉末可以作为此类反应的催化剂,这个反应也因此被命名为Zincke反应。 1877年,Friedel和Crafts[3-4]试图通过Gustavson反应将1,1,1一三氯乙烷(苯作溶剂)在铝粉和碘单质存在条件下转化为1,1,1.三碘乙烷,但出乎意料的是他们再次得到了Zincke反应的产物。经过他们的不断研究,他们又对各种金属卤化物、各种卤代烃以及各种酰卤分别进行了研究,表明Zincke提出的各种金属确实不是此类反应的催化剂,它们的卤代物才是真正意义上的催化剂。至此傅一克反应被正式提出,包括傅一克烷基化反应和傅一克酰基化反应。 傅一克反应虽然说是非常古老的化学,但是直到现在其应用依然非常的广泛[5-6]。一直以来,许多化学工作者对傅一克反应机理的研究非常感兴趣,同时也做了许多工作。目前有关该反应机理方面的报道相对较少,直至现在还是没有非常清楚地指明该反应的机理,最主要的是至今仍然没有明确提出该反应实际的反应活性中间体.这未免有些遗憾,但研究者们出色的工作还是给出了大量的信息,为傅一克反应机理的进一步探索做出了巨大贡献。 2、傅-克反应的发展及应用概况 傅-克反应自从被发现以来,大量的论文、书籍或者专利介绍这类反应,它在学术或者工业领域上迅速成为有机合成化学的基础反应。 由于傅一克酰基化反应是实现碳碳成键的最有效方式之一,并且是制备各种芳基酮,杂环芳烃酮等的重要手段,所以它在医药、农药、染料、香料等工业生产中具有非常广泛的应用,因此化学家们对傅一克酰基化反应一直怀有很高的兴趣。一般来讲,傅一克酰基化反应使用的是路易斯酸,如氯化锌、氯化铝、氯化铁、四氯化锡、四氯化钛等或者是很强的质子酸,如氢氟酸、硫酸等.在反应结束以后,这些路易斯酸与产物配位从而以配合物的形式存在,所以在水解后才可以得到目标产物,这就会造成环境的污染[7,8].所以,在过去的几十年里,傅一克酰基化反应一直努力朝着绿色化学的方向发展.通过开发更加有效的催化剂,比如催化量的Ln(OTf)3.使得反应效率得到提高,或者优化反应条件,如微波条件下,离子液体中的傅一克酰基化反应,实现催化剂的回收再利用;抑或是使用石墨作为固体催化剂,以及各种异相催化剂的发展都使得傅一克酰基化反应不断地向前推进。 3.1傅-克烷基化反应 傅-克烷基化反应的反应机理与磺化、硝化类似,首先在催化剂的作用下产
傅克反应机理 Prepared on 24 November 2020
Friedel-Crafts反应机理 摘要:本文总结了傅-克反应提出以来,化学研究人员对该反应的机理方面的研究,包括动力学研究、中间体结构和性质的。提出傅一克反应机理目前存在的疑问及机理动力学的发展方向。 关键词:傅-克反应;动力学;中间体;反应机理 1、傅-克反应的发现 傅-克反应在整个化学发展史上是最为古老的化学之一[1]。1869年德国化学家Zincke[2]首次报道了在苯环上引入烷基的反应.这个反应的发现来源于一个偶然,当时Zincke想从苄氯和氯乙酸(以苯作为溶剂)出发,在铜粉(或银粉)和密封加热的条件下,通过类似Wurtz反应的方法制各苯丙酸,但他发现在反应过程中有大量的氯化氢产生,同时也生成了二苯甲烷。他意识到这是苄氯和溶剂苯发生反应产生的。为此,在接下来的几年里,他开始研究这类苯环上引入取代基的反应。Zincke的发现引起了化学家们的广泛关注,他们用不同芳烃进行反应,并且得到了相应芳烃的烷基化和酰基化产物.至此,他们一致认为铁、铜、银或锌等金属粉末可以作为此类反应的催化剂,这个反应也因此被命名为Zincke反应。 1877年,Friedel和Crafts[3-4]试图通过Gustavson反应将1,1,1一三氯乙烷(苯作溶剂)在铝粉和碘单质存在条件下转化为1,1,1.三碘乙烷,但出乎意料的是他们再次得到了Zincke反应的产物。经过他们的不断研究,他们又对各种金属卤化物、各种卤代烃以及各种酰卤分别进行了研究,表明Zincke提出的各种金属确实不是此类反应的催化剂,它们的卤代物才是真正意
傅克反应总结材料1.傅克反应的发现: 在这些反应中,以制备芳烃和芳酮是主要的。 2.傅克反应的反应机理
注意以下三种情形下的反应: A.烷基正离子的重排(稳定性:叔>仲>伯) 因此反应中都有异构体产物的出现。如: B.烷基取代不会停留在一取代阶段 由于烷基是供电子基团,已取代后芳环上电子云密度增大,使得亲电取代反应更容易进行,所以取代还会继续进行下去,最后可以全部取代。如: 但是有些基团由于位阻关系,只能得到已取代的产物。 如果取代基团是酰基,由于酰基是吸电子基团,使得芳环电子云密度减小,使得亲电取代反应比较困难,反应一步后会停下来,所以傅克酰化合成芳酮更为有用。 C.定文问题:
下面的例子将让我们更好的去理解定位问题: 3.傅克反应的催化剂 路易氏酸,强酸,酸酐,酰氯和一些中性化合物和元素等。 特别需要注意以下及点: A.不同催化剂产生不桶产物: B.不同催化剂产率有很大的差别:
C. 氯化物作为催化剂要无水,但是绝对无水活性反而不大,甚至不能进行。有些反应还需要把催化剂暴露在空气中吸水几分钟后,才能催化反应的进行。 4.傅克反应所用的烷基化剂 A.常用的是氯化物,活泼性次序RCl>RBr>RI B.烯类也是很好的烷基化剂,催化剂用BF3和HF效果很好。 C.醇类也可作为烷基化剂,但是催化剂用BF3和HF效果最好。 5.酰基取代剂 A. 酰卤 活性顺序为: B. 酸酐也是很好的酰化剂,但是它需要比酰卤多50%的氯化铝。 C. 羧酸也可以直接用作酰化剂,但催化剂不宜用氯化铝,而要用硫酸,磷酸,最好是 氟化氢。 6.芳环 芳环和杂环化合物都能参加F-C反应,其中并环和稠环更易发生反应,杂环中,呋喃类,吡咯类等虽对酸敏感,但在适当情况下也可发生F-C反应。
傅-克反应 1 2 傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877 3 年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨4 (Crafts J)共同发现。该反应主要分为两类:烷基化反应和酰基化反应。 5 6 傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应 7 傅-克烷基化反应 8 傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。9 假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,10 碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。总11 反应式如下: 12 13 傅-克烷基化机理 14 这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更15 高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化16 现象而形成了众多副产物。由于这类反应是可逆的,还可能出现烷基被其他基17 团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时18 间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间19 位产物。另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正
20 离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。空21 间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化22 反应。 23 24 1,4-二甲氧基苯的叔丁基化 25 烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中26 间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。 27 如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应: 28 29 1-氯-2-甲基-2-苯基丙烷的合成 30 曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。 31 32 通过烯烃的傅-克烷基化 33 在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。 34 傅-克去烷基化反应 35 傅-克烷基化是一个可逆反应。在逆向傅-克反应或者称之为傅-克去烷基化36 反应当中烷基可以在质子或者路易斯酸的存在下去除。例如,在用溴乙烷对苯37 的多重取代当中,由于烷基是一个活化基团,原来期待能够得到邻对位取代