临检实验室建设标准与要求 一、高通量测序(NGS)实验室简介 1.1NGS实验室又叫高通量测序检测实验室。NGS是下一代测序技术(N EXT G ENERATION S EQUENCING)即高通量测序技术的简称。高通量测序技术是 对传统S ANGER测序(称为一代测序技术)革命性的改变,可同时对几十万到几百万条核酸分子进行序列测定,同时高通量测序使得对一个物种的转录组和基因组进行细致全貌的分析成为可能,也称为深度测序 (D EEP SEQUENCING)。 1.2由于NGS技术对所检测的核酸模板进行大量扩增,容易出现实验室污 染导致检测结果准确性下降;另外NGS技术要求高、影响因素多,实验过程处理不当易导致检测结果准确性下降或检测失败。因此临床基因扩增检验实验室技术验收和规范化管理是NGS技术本身需要,也是在临床上顺利应用该技术前提。 二、NGS实验室临床应用的基本条件 2.1必须拥有符合临检中心相关规定的标准NGS实验室。 2.2检测设备必须符合标准NGS实验室设置要求:高通量测序仪及配套服 务器;高通量测序检测试剂盒;通用电脑;自动分析软件,实验室样本信息管理系统等。 2.3检测人员必须通过专门的技能培训,并获得省级以上卫生计生行政部门 颁发的临床基因扩增检验技术上岗证书。NGS实验室必须建立严格的实验室管理制度、建立标准化操作程序(SOP)、建立系列质量管理文
件等,确保实验室日常运行符合国家卫生部的要求,确保检测结果准确、确保实验室卫生安全,确保实验室长期稳定运行。 2.4NGS临床应用必须在无菌无尘环境下进行操作。 三、NGS实验室建设基本要求 3.1主体结构 主体为彩钢板、铝合金型材。室内所有阴角、阳角均采用铝合金50内圆角铝,从而解决容易污染、积尘、不易清扫等问题。结构牢固,线条简明,美观大方,密封性好。 3.2标准的各区分隔和气压调节 将检测过程分成试剂准备、样本制备、PCR扩增和高通量测序四个独立的实验区。整个区域有一个整体缓冲走廊。每个独立实验区设置有缓冲区,同时各区通过气压调节,使整个检测实验过程中试剂和标本免受气溶胶的污染并降低扩增产物对人员和环境的污染。 可打开缓冲区和PCR扩增区的排风扇往外排气,在实验区的外墙上和各扇门上都安装有风量可调的回风口,空气通过回风口向室内换气。 3.3消毒 在每个实验区和缓冲区顶部以及传送窗内部安装有紫外灯,供消毒用。在各区还设置移动紫外线灯,对实验桌进行局部消毒。 3.4机械连锁不锈钢传递窗
研究标题: 单纯调强放疗与调强放疗联合同期化疗治疗II、III期鼻咽癌的非劣效性II期 临床试验 研究申办方:中山大学附属肿瘤医院 --------------------------------------------------------------------- 研究者姓名:....................... 电话 ................... 地址:.............................................................. ................................................................... __________________________________ 患者姓名:....................... 出生日期:...... 年......月......日 __________________________________ 1.简介 您的医生已经告知您,目前您所患疾病的最主要治疗方法是放疗。您正受邀 参加一项临床研究,其目的是比较单纯调强放疗与调强放疗联合同时期化疗治疗 AJCC分期II、III期鼻咽癌患者的疗效、副反应与生活质量。 目前同时期放化疗是目前Ⅱ~Ⅳb期鼻咽癌的标准治疗方案。在这些确定同 时期化疗地位的临床研究中,放射治疗技术采用的均为二维的常规放疗技术。在 常规放疗技术条件下,同期放化疗确实可以提高局部中晚期的生存,然而同期放 化疗的生存获益主要是通过提高局部控制率实现的。10余年来,调强放射治疗 技术的物理学优势以及鼻咽癌的临床解剖和生物学特点,使得调强放射治疗在鼻 咽癌治疗中得到广泛应用,众多临床实验结果也表明调强放射治疗技术使鼻咽癌 的治疗疗效达到一个新的高度,调强放射治疗技术的应用,削弱了同期放化疗+/- 辅组化疗在局部晚期鼻咽癌中的作用。 并且同时期化疗加重了鼻咽癌患者近期和远期副反应的发生率,如血液毒 性、体重下降及耳毒性等毒副反应。在众多化疗药物中,顺铂是治疗中晚期鼻咽 癌的经典一线药物。但是,由于顺铂引起的胃肠道反应较重,例如剧烈的恶心、 呕吐等,导致部分患者不能耐受化疗;而顺铂直接损害肾实质,治疗时需要水化 和利尿;顺铂的神经毒性和放疗后的远期毒性放射性听神经损伤叠加,严重影响 了患者的生活质量。 因此,根据现有的调强放射治疗结果和同期化疗的疗效,以及常规放射
第七章临床实验室检查 一.单选题 1.下列哪一项无网织红细胞增多 A.溶血性贫血 B.出血性贫血 C.缺铁性贫血 D.再生障碍性贫血 E.感染性贫血 2.下列哪一项属于核右移 A.外周血中性粒细胞增多 B.中性粒细胞五叶核>5% C.外周血杆状核细胞增多 D.外周血三叶核细胞增多 E.出现早、中、晚幼粒细胞 3.不属于血常规检查的项目是 A.红细胞计数 B.白细胞计数 C.血红蛋白测定 D.血小板计数 E.白细胞分类计数 4.下列哪一项属于相对性红细胞增多 A.高原生活 B.剧烈体力劳动 C.大汗淋漓 D.新生儿 E.真性红细胞增多症 5.贫血伴轻度黄疸最可能是 A.脾亢 B.溶血性贫血 C.急性白血病 D.再生障碍性贫血 E.生理性贫血 6.白细胞减少常见于 A.病毒感染 B.化脓菌感染 C.烧伤 D.大出血 E.慢性白血病 7.哪项血象改变是诊断白血病的主要依据 A.白细胞异常增多 B.红细胞减少 C.血红蛋白减少 D.血小板减少 E.大量原始和幼稚型白细胞 8.生理性红细胞和血红蛋白减少见于 A.剧烈活动后 B.妊娠中、晚期 C.新生儿 D.早期高原生活 E.哺乳期 9.外周血中性粒细胞增多见于 A.肺炎球菌性肺炎 B.脾亢 C.伤寒 D.再生障碍性贫血 E.流行性感冒 10.血小板增加可见于 A.溶血性贫血 B.再生障碍性贫血 C.原发性血小板减少性紫癜 D.播散性血管内凝血 E.脾功能亢进 11.外周血中性粒细胞减少见于 A.肺炎球菌性肺炎 B.心绞痛 C.急性心梗 D.急性溶血 E.伤寒 12.嗜酸性粒细胞增多见于 A.肺结核 B.支气管哮喘 C.肺癌 D.上呼吸道病毒感染 E.长期使用糖皮质激素 13.嗜酸性粒细胞减少见于 A.荨麻疹 B.伤寒 C.寄生虫病 D.缺铁性贫血 E.急性大出血 14.下列哪种情况血沉不增快 A.肺结核进展期 B.风湿活动 C.恶性肿瘤 D.心绞痛发作 E.心梗 15.网织红细胞减少见于 A.溶血性贫血 B.脾切除术后 C.正常新生儿 D.再生障碍性贫血 E.失血性贫血 16.血小板增多见于 A.急性白血病 B.脾亢 C.DIC D.巨幼红细胞性贫血 E.急性大出血 17.绝对性红细胞增多见于 A.剧烈呕吐 B.严重腹泻 C.口服利尿剂 D.糖尿病酮症酸中毒 E.慢性肺源性心脏病 18.中性粒细胞胞浆中见粗大的分布不均的蓝黑色颗粒,需考虑 A.阿米巴痢疾 B.疟疾 C.严重化脓性感染 D.白血病 E.晚期活动性结核病
临床常用实验室检查正常值 血液检查 红细胞成年男性(4.0~5.5)×1012/L 女性(3.5~5.5)×1012/L 新生儿(6.0~7.0)×1012/L 血红蛋白成年男性120~160g/L 女性110~150g/L 新生儿170~200g/L 白细胞成人(4~10)×109/L 新生儿(15~20)×109/L 6个月~2岁(11~12)×109/L 白细胞分类N 50~70% E 0.5~5% B0~1% L20~40% M3~8% 血小板(100~300 )×109/L 红细胞比容男0.4~0.5 女0.37~0.48 红细胞平均指数MCV82~92fl MCH27~31pg MCHC320~360g/L 出血时间Duke法 1~3min 凝血时间试管法 4~12min 凝血酶原时间11~13s 网织红细胞0.5%~1.5% 平均1%新生儿2%~6% 红细胞沉降率男0~15mm/h 末女0~20mm/h末 尿液检查 颜色淡黄色 尿量1000~2000ml/24h 平均1500ml/h 比重最大变动范围 1.003~1.030以上 一般变动范围 1.015~1.025 晨尿 1.020左右 尿沉渣检查 红细胞 0~偶见/HP 上皮细胞 0~少量/HP 白细胞<5/HP 透明管型 0~偶见/LP 12小时沉渣计数(Addis计数) 白细胞<1000000 /12h 红细胞<500000/12h 管型<5000/12h 1小时尿细胞计数 白细胞男<7×104/h女<14×104/h
红细胞男<3×104/h女<4×104/h 中段尿培养菌落形成单位(CFU) 杆菌:>105CFU肯定为感染 球菌:>103CFU肯定为感染 尿葡萄糖定性(—)定量斑氏法 0.1~0.9g/d 尿蛋白定性(—)定量<150mg/24h 尿蛋原 稀释试验<1∶20 定量 0~5.9mol/L(0~3.5mg/d) 尿酮体试验定性(—) 尿胆红素试验定性(—) 尿妊娠试验定性乳胶法(—) 粪便检查 颜色:黄褐色量100~300g/日细胞(上皮细胞或白细胞)0~偶见/HP,食物残渣、大量植物细胞、淀粉颗粒、肌纤维等。隐血试验阴性。 血清蛋白测定 总蛋白60~80g /L 白蛋白40~55g/L 球蛋白20~30g/L A/G比值 1.5:1~2.5:1 甲胎蛋白(α-FP,AFP)0~25μg/L (0~25ng/ml)血清C反应蛋白(CRP) 单向免疫扩散法〈8mg/L 尿素氮成人3.2~7.1 mmol/L 儿童1.8~6.5 mmol/L 尿酸119~238μmol/L 肌酐全血88.4~176μmol/L 血清男性53~106μmol/L 女性44~97μmol/L 血糖(空腹) 全血(Folin-吴法)4.4~6.7(80~120 血清(邻甲苯胺法)3.9~6.4 mmol/L(70~110 mg/dl) 血钾(K+)4.1~5.6 mmol/L(4.1~5.6 mEq/L) 血钠(Na+)135~144 mmol/L(135~144 mEq/L) 血钙(Ca2+) 2.2~2.7 mmol/L
一项评价西达本胺联合联合泼尼松、环磷酰胺、依托泊苷及甲氨蝶呤治疗复发或难治性外周T细胞淋巴瘤的多中心、单臂、开放性II期临床试验 知情同意书 受试者姓名: 受试者姓名缩写: 受试者编号: 联系电话: 联系地址:
受试者须知 尊敬的患者:您好! 首先感谢您有意参加本项临床试验。在您同意参加本项临床试验之前,请您仔细阅读这份知情同意书,如果您愿意也可以和您的亲人或朋友商量,或向您的医生或研究人员提出任何您需要了解的问题,直至得到满意的答复。 参加本临床试验是自愿的,如果您同意参加,请您签署此知情同意书,并且保存该份经您和研究者双方签字的知情同意书副本。本临床试验遵循《药物临床试验质量管理规范》和《赫尔辛基宣言》,并获得国家食品药品监督管理局和医院伦理委员会的批准,这将会保证您的权益在本试验中不受侵犯。 签署知情同意书不会改变您的合法权益,仅表示您已经理解了这些信息并愿意参加本试验。 【试验目的和背景】 针对外周T细胞淋巴瘤(PTCL)目前尚无标准的治疗方案,一线治疗包括CHOP 方案(环磷酰胺、阿霉素、长春新碱和强的松四药联合)或CHOP类似方案,虽然可获得较高缓解率,但维持时间短,患者生存获益差。对于难治患者或缓解后再复发的患者,特别是对于因各种原因不能进行自体干细胞移植患者,二线治疗难度更大,因此治疗指南首选临床试验。 西达本胺(Chidamide,爱谱沙)是我国自主研发的亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,为 1.1类新药。在全国多家中心完成的西达本胺片治疗复发或难治性外周T细胞淋巴瘤的II期临床试验结果显示,西达本胺单药有效率为29.1%,常见不良事件为血液学毒性、胃肠道反应、食欲不振等,超过半数患者发生的不良事件为1-2级。这些结果显示,西达本胺安全性较好,主要不良反应为可控的血液毒性,并显示了较好的综合获益,口服给药方便。2014年12月23日国家食品药品监督管理总局(CFDA)批准西达本胺单药治疗复发或难治性PTCL。 本项临床试验的主要目的是在前期相同适应症的单药临床试验基础上,对西达本胺联合泼尼松、环磷酰胺、依托泊苷及甲氨蝶呤治疗复发或难治性PTCL的疗效和安全性进行评价,为西达本胺联合用药的临床应用进一步提供依据。 【试验设计和步骤】 试验将选择合适的患者参加,计划共计入选36例受试者。在入组筛选期间,为了确定您是否适合参加本项临床试验,您的医生将询问并记录您的病史、全身健康状况以及进行相关的检查。您将被要求抽血(约5~8毫升)以及留取尿标本进行血常规、血生化、电解质和尿常规等检查,同时进行皮肤病灶拍照评估、放射学和其他必要的检查,以便了解您的疾病情况是否符合参加本项临床试验的入选标准。 本研究包括联合治疗期和维持治疗期。在联合治疗期,您将接受西达本胺联合泼尼松、环磷酰胺、依托泊苷及甲氨蝶呤的治疗:西达本胺片每次30mg,每周服用2次
儿科常用实验室检查正常参考值 一、小儿各年龄血液细胞成份平均正常值 项目第 1日 第 2~7日 2 周 3 个月 6 个月 1~2 岁 4~5岁8 ~ 1 4 岁 红细胞(×1012) 5. 7~6.4 5.2 ~5.7 4 .2 3 .9 4. 2 4.3 4.44 .5 (×109/mm3) 5. 7~6.4 5.2 ~5.7 4 .2 3 .9 4. 2 4.3 4.44 .5 血红蛋白(g/L)1 86~ 195 163 ~180 1 50 1 11 12 3 1181341 3 9 (g/dl)1 8.6~ 19.5 16. 3~18.0 1 5.0 1 1.1 12 .3 11.813.41 3. 9 红细胞压积(%)5 3 (4) 3 3 4 3737404 1 红细胞平均体积(MCV)(fl) 1 09 (1) 03 8 1 8385919 2 红细胞平均血红蛋白(MCH)(pg) 3 5 (3) 4 2 9 2829303 1 红细胞平均血红蛋白浓度(MCHC)(%) 3 2 (3) 4 3 3 3332333 4 红细胞平均直径(μm)8. 0~8.6 (7) .7 7 .3 … … 7.17.2… … 有核红细胞(/100白细胞) 3 ~10 3~ 10 000000 网织红细胞(占红细胞%)3 0 .3 1 .5 0. 5 0.50.5… …
8 8 5 2 3 6 0二小儿各年龄血小板(BPC)、平均血小板体积(MPV)正常值 分组BPC (×109/L)MPV(fl) G 95%正常范围x±s 0~14天207100~4237.8±0.7 15天~288145~5718.4±1.5 1岁~195119~3209.2±1.4 3岁~17899~32010.0±1.4 7~14岁15181~28511.7±1.8成人13084~20112.2±1.1 三血液生化检查正常值 项目标本 正常值 旧制单位国际单位换算系数
注册指南请仔细阅读本指南,如有疑问,请与我们联系。 一、什么样的临床研究需要注册? 所有在人体进行的研究,包括各种干预措施的疗效和安全性的有对照或无对照试验(如随机对照试验、病例-对照研究、队列研究及非对照研究)、预后研究、病因学研究、和包括各种诊断技术、试剂、设备的诊断性试验,均需注册并公告。 二、中、英文双语注册 在完成中文注册申请表后,必须于两周内完成英文注册申请表。如果两周内不能完成英文版,请与我们联系采用英文翻译服务。在完成中、英文注册资料的上传后15天内可获得注册号,一个月内可在世界卫生组织国际临床试验注册平台检索入口(WHO ICTRP search portal)检索到已注册试验。 未完成英文注册申请表者不算完成注册。 三、注册是否需要费用? 中国临床试验注册中心为非赢利机构,一律免费注册。 四、哪些项目需要收费? 1、只有那些需要我们指导设计的试验才收取一定的服务费用,仅仅用于维持机构运转。参考目前国际注册机构收费标准,任何类型的单个研究设计指导费用均为1500元; 2、翻译服务:500元。 五、伦理审查及其费用 中国临床试验注册中心组建的中国注册临床试验伦理审查委员会由资深各专业临床医学家、临床试验专家、医疗卫生服务用户代表、WHO患者安全保护联盟中国区代表、律师及药物公司代表组成,宗旨是保障受试者权益,审查临床试验的合理性,评估安全性,凡未经其他伦理委员会审查的临床试验均需在中国临床试验注册中心临床试验伦理委员会接受审查。临床试验伦理审查费用标准为每项2000元。 六、申请注册程序 1. 全部注册程序均为在线申报; 2. 首先在中国临床试验注册中心网站上建立申请者账户:点击ChiCTR首页右侧的“用户登陆”区的“注册”; 3. 弹出个人信息注册表,请将你的信息录入此表后点击“注册”,则您的账户就建立起来了;
颅内血管磁共振管壁成像注册登记研究方案 一、研究背景 1. 研究目的与意义 颅内动脉狭窄是缺血性卒中的重要原因。由于缺乏可靠影像学手段及病理学证据,颅内动脉粥样硬化斑块(ICAD)易损性特征一直是研究难点。基于前期高分辨磁共振(HR-MRI)管壁成像研究工作,我们提出:症状性ICAD斑块强化是斑块易损性的重要标志,其强化程度与卒中复发密切相关。我们拟通过建立的颅内动脉狭窄研究队列,采用HR-MRI技术前瞻性比较症状性与无症状ICAD斑块组成、形态结构、强化程度等定量指标,探索①HR-MRI技术在脑卒中病因学诊断,治疗方案决策方面的价值;②建立包含斑块强化特性的ICAD易损斑块评价标准,明确及其在药物治疗效果评估中的价值,为ICAD的个体化治疗提供重要的客观依据。 2. 国内外研究现状 颅内动脉粥样硬化性狭窄是引起脑梗死的重要原因颅内动脉粥样硬化性狭窄发生率存在种族差异[1]。亚洲黄种人及非洲、美洲黑人的颅内动脉狭窄的发生率较美洲白人高。基于我国的两项研究发现年龄超过60岁的正常人群中颅内动脉狭窄发生率为5.9%~6.9%[2, 3]。我国卒中患者中颅内动脉狭窄约占33%~50%,TIA患者中颅内动脉狭窄所占比例更高(>50%)。 症状性ICAD年卒中复发率较无症状ICAD年发生率显著增高。脑梗死后患者存在再卒中风险,而伴有颅内动脉狭窄患者的卒中复发率明显增加。我国国家卒中注册调查的数据显示伴有颅内动脉狭窄1年内卒中复发率随动脉狭窄程度而增加,其1年复发率从3.34%增至7.40%[4]。在WASID研究中症状性ICAD者应用阿司匹林组1年内卒中复发率为19%,而狭窄率≥70%的患者年卒中复发率高达23%;无症状颅内动脉粥样硬化性狭窄发生率为18.9%-27.3%,而其相关卒中年发生率平均3.5%。因此,ICAD导致卒中发生的风险存在显著差异,进一步的危险分层研究对于临床干预决策具有重要指导意义。颅内动脉粥样硬化引起卒中的机制复杂,包括:血栓形成、动脉-动脉栓塞、低灌注、穿支动脉闭塞等。其中血栓形成、动脉-动脉栓塞在卒中事件的发生中占有重要地位。而二者多由于局部斑块
实验室检查结果及正常值 (一)血常规 红细胞(RBC)成年男性:(4.0~5.5)×1012/L 成年女性:(3.5~5.0)×1012/L 新生儿:(6.0~7.0)×1012/L 血红蛋白(Hb)成年男性:120~160g/L 成年女性:1l0~150g/L 新生儿:170~200g/L 白细胞(WBC)成人:(4.0~10.0)×109/L;新生儿:(15.0~20.0)×109/L 中性杆状核粒细胞:1%~5% 中性分叶核粒细胞:50%~70% 嗜酸性粒细胞:0.5%~5% 嗜碱粒性细胞:O%~1% 淋巴细胞:20%~40% 单核细胞:3%~8% 血小板(PLT)(100~300)×109/L (二)尿常规 1.酸碱度(pH)5~8 2.比重(SG)1.015~1.025 3.尿蛋白(Pro)定性定量试验 Pro定性:阴性(neg),Pro定量≤O.15g/24h 4.葡萄糖(Glu)定性:阴性(neg)、糖定量:<2.8mmol/24小时(0.5g/24小时) 5.酮体(Ket)阴性(neg) 6.胆红素(Bil)和尿胆原(Ubg)均为阴性(neg) 7.亚硝酸盐(Nit)阴性(neg) 8.白细胞(Leu)<25/μl 9.红细胞或血红蛋白(潜血试验)(Ery或OB)≤l0/μl 10.尿沉渣镜检白细胞<5/HP(每高倍镜视野)红细胞<3/HP(每高倍镜视野)(三)粪常规 1.颜色黄褐色成型便 2.镜检 (1)白细胞:正常粪便不见或偶见; (2)红细胞:正常粪便无红细胞; (3)细菌:主要为大肠杆菌和肠球菌; (4)虫卵。 3.粪便潜血试验(occult blood test,OBT)正常粪便OBT阴性。 (四)痰液检验 一般性状检查正常人痰液呈无色或灰白色。 化脓性感染时呈黄色;
(一)血常规 红细胞(RBC)成年男性:(~)×1012/L 成年女性:(~)×1012/L 新生儿:(~)×1012/L 血红蛋白(Hb)成年男性:120~160g/L 成年女性:1l0~150g/L 新生儿:170~200g/L 白细胞(WBC)成人:(~)×109/L;新生儿:(~)×109/L 中性杆状核粒细胞:1%~5% 中性分叶核粒细胞:50%~70% 嗜酸性粒细胞:%~5% 嗜碱粒性细胞:O%~1% 淋巴细胞:20%~40% 单核细胞:3%~8% 血小板(PLT)(100~300)×109/L (二)尿常规 1.酸碱度(pH)5~8 2.比重(SG)~ 3.尿蛋白(Pro)定性定量试验Pro定性:阴性(neg),Pro定量≤O.15g/24h 4.葡萄糖(Glu)定性:阴性(neg)、糖定量:</24小时(0.5g/24小时) 5.酮体(Ket)阴性(neg) 6.胆红素(Bil)和尿胆原(Ubg)均为阴性(neg) 7.亚硝酸盐(Nit)阴性(neg) 8.白细胞(Leu)<25/μl 9.红细胞或血红蛋白(潜血试验)(Ery或OB)≤l0/μl 10.尿沉渣镜检白细胞<5/HP(每高倍镜视野)红细胞<3/HP(每高倍镜视野) (三)粪常规 1.颜色黄褐色成型便 2.镜检 (1)白细胞:正常粪便不见或偶见; (2)红细胞:正常粪便无红细胞; (3)细菌:主要为大肠杆菌和肠球菌; (4)虫卵。 3.粪便潜血试验(occult blood test,OBT)正常粪便OBT阴性。 (四)痰液检验 一般性状检查正常人痰液呈无色或灰白色。 化脓性感染时呈黄色; 绿脓杆菌感染时呈黄绿色;
常用化验检查结果的临床意义 Ⅰ血细胞分析 ⑴血红蛋白(Hb):新生儿170~200g/L; 成年:男性120~160g/L女性110~150g /L; 老年(70岁以上):男性94.2~122.2g/L; 女性86.5~111.8g /L ⑵红细胞(RBC):新生儿(6.0~7.0)×10*12/L 男性(4.0~5.5)×10*12/L 女性(3.5~5.0)×10*12/L ⑶白细胞(WBC):成人(4.0~10.0)×10*9/L 新生儿(15.0~20.0)×10*9/L 6个月至2岁(11.0~12.0)×10*9/L ⑷血小板(PLT):(100~300)×10*9/L ⑸网织红细胞计数(RET): 0.5%-1.5% ⑹白细胞分类计数(DC) 百分率绝对值 中性杆状核粒细胞0.01~0.05 (1%~5%)(0.04~0.5)×10*9/L 中性分叶核粒细胞0.50~0.70 (50%~70%)(2.0~7.0)×10*9/L 嗜酸性粒细胞(EOS) 0.005~0.05 (0.5%~5%)(0.02~0.5)×10*9/L 嗜碱性粒细胞(BASO) 0~0.001 (0%~1%)(0~0.1)×10*9/L 淋巴细胞(LYMPH) 0.20~0.40 (20%~40%)(0.8~4.0)×10*9/L
单核细胞(MONO) 0.03~0.08 (3%~8%)0.12~0.8)×10*9/L ⑺血细胞比容(Hct): 男性:0.40~0.50L/L(40~50容积%),平均0.45L/L 女性:0.37~0.48L/L(37~48容积%),平均0.40L/L ⑻平均红细胞体积(MCV):80~100fl ⑼平均红细胞血红蛋白(MCH):27~34pg ⑽平均红细胞血红蛋白浓度(MCHC):320~360g/L(32%~36%) ⑾红细胞体及分布宽度(RDW): <14.5% 红细胞增多见于:(1)严重呕吐、腹泻、大面积烧伤及晚期消化道肿瘤患者。多为脱水血浓缩使血液中的有形成分相对地增多所致。(2)心肺疾病:先天性心脏病、慢性肺脏疾患及慢性一氧化碳中毒等。因缺氧必须借助大量红细胞来维持供氧需要。(3)干细胞疾患:真性红细胞增多症。 红细胞减少见于:(1)急性或慢性失血。(2)红细胞遭受物理、化学或生物因素破坏。(3)缺乏造血因素、造血障碍和造血组织损伤。(4)各种原因的血管内或血管外溶血。 血红蛋白临床意义:贫血、白血病、产后、手术后、大量失血、钩虫病等减少。缺铁性贫血时尤为明显。肺气肿、肺心病、先天性心脏病、严重呕吐、腹泻、出汗过多、大面积烧伤、慢性一氧化碳中毒及真性红细胞增多症等时增高(长期居住高原者生理性增高)。
中国临床试验注册和发表机制及实施说明 Statement for Chinese Clinical Trial Registration and Publishing System 吴泰相1,李幼平1,李静1,钟紫红2,贾万年3,代表中国临床试验注册和发表协作网 Taixiang Wu, Youping Li, Jing Li, Zihong Zhong, Wanlian Jia, on behalf of Chinese Clinical Trial Registration and Publishing Collaboration 执笔人单位: 1.卫生部中国循证医学中心、Chinese Cochrane Centre、循证医学教育部网上合作研究中心、中国临床试验注册中心,四 川大学华西医院 Chinese Evidence-Based Medicine Center Ministry of Health of the People’s Republic of China, Chinese Cochrane Centre, Ministry of Education Virtual Research Center of Evidence-Based Medicine, Chinese Clinical Trial Register, West China Hospital, Sichuan University 2.中国医学科学院协和医科大学 Peking Union Medical College, Chinese Academy of Medical Sciences 3.《解放军医学杂志》编辑部 Editorial Board of Medical Journal of Chinese People’s Liberation Army 2006年4月16~17日在成都召开第四届亚太地区循证医学研讨会期间,中国48家医(药)学期刊和中国临床试验注册中心(Chinese Clinical Trial Register, ChiCTR)、卫生部中国循证医学中心、循证医学教育部网上合作研究中心和Chinese Cochrane Centre的代表经过充分讨论达成共识,决定共同发起创建中国临床试验注册和发表机制,并成立“中国临床试验注册和发表协作网(Chinese Clinical Trial Registration and Publishing Collaboration, ChiCTRPC)”。这种临床医学研究管理新模式的创建和应用,将对提高中国临床试验信息透明度和质量、提高医学研究公信度发挥极其重要的作用。本文介绍其结构特点和运作方式。 1.中国临床试验注册和发表机制的结构特点 中国临床试验注册和发表机制是医(药)学期刊、ChiCTR、技术支撑和教育体系三部分联合协调运行的机制。 1.1 医(药)学期刊是医(药)学科技事业的重要组成部分,是传播和交流医(药)学科技信息的主要载体,反映一个国家医(药)学研究和卫生事业发展水平,承载着为各类医疗卫生决策提供证据的重任,有着其他途径不可替代的重要导向作用[1]。 医(药)学期刊是医(药)学研究结果的主要出口,发表的文献数量占医(药)学文献总量的70%[1]。要实行临床试验注册制度,必须有医(药)学期刊严把出口关,只有完全做到不发表未注册的临床试验,才能保证临床试验注册制度的完全实施。 针对中国医(药)学期刊数量多,医(药)学从业人员数量大,对临床研究知识的掌握和理解程度不一,文章数量巨大质量偏低的特点,ChiCTRPC的成员期刊经讨论决定,从2007年1月1日起优先发表已注册的临床试验,根据各期刊情况,逐步过渡到只发表已注册试验报告。 全国各医(药)学期刊是中国临床试验注册和发表机制中极为重要的环节,是整个机制成功运转的保障。我们希望全国医(药)学期刊积极参与到这件关系到医(药)学研究社会公信度的大事中来,团结一致,共同推动中国临床研究水平的提高。
临床研究方案 放疗同步替吉奥胶囊治疗鼻咽癌 临床研究 研究者放射肿瘤科 医院海军总医院 申办者:海军总医院放射肿瘤科
一:前言 鼻咽癌是我国常见恶性肿瘤之一,在头颈部恶性肿瘤中占首位。发病率有明显的地区分布。据估计,世界上80%的鼻咽癌病例发生在我国。治疗首选放射治疗,放疗后年生存率约为34-53%。 到目前为止,其标准的治疗方案仍为以铂类药物为基础的联合化疗。由于铂类显著的肾毒性、消化道反应、血液学毒性,以及对生活质量的影响,在临床使用上受到限制。 替吉奥为抗代谢药物,有替加氟、吉美嘧啶、奥替拉西钾按1:0.4:1摩尔比组成。吉美嘧啶和奥替拉西钾通过对酶的抑制作用,使替加氟在体内生成5-氟尿嘧啶(5-FU)的有效浓度持续更长的时间,同时减少5-FU胃肠道副反应。适用于头颈部肿瘤及晚期胃癌、胰腺癌、结直肠癌、非小细胞肺癌等患者。临床荟萃分析显示,在晚期胃癌、胰腺癌、结直肠癌、非小细胞肺癌中使用替吉奥可以在提高疗效的同时,还能降低患者的不良反应的发生率。替吉奥联合同步放疗既能使肿瘤细胞的增殖周期发生改变,增加放疗的敏感性,同时不增加患者严重的不良反应发生率。 现进行放疗联合替吉奥胶囊治疗鼻咽癌的临床研究,以探讨该方案的疗效和不良反应。 二:研究目的 ◆主要研究终点:疗效(无进展生存期PFS,总生存期OS) ◆次要研究终点:不良反应(早期,晚期) 三:研究设计 本研究采用单中心、随机、平行对照试验设计,拟纳入病人50例。研究采用随机分组方法:组别1(25例)为替吉奥胶囊同步放化疗,组别2(25例)为氟尿嘧啶+顺铂(PF方案)同步放化疗,在放疗结束后维持化疗3周期治疗结束时评价疗效。任何时间发现病情进展均可停止治疗。
中国临床试验注册中心/中国医学研究信息管理中心 关于推广使用基于互联网的临床研究公共管理平台暨提供数据和安全监测服务的公告 Notification for opening the web-based medical research public management platform ResMan 为了促进临床研究的规范化管理,提高临床试验的质量和公信度,我们于 2010年 3月 1 日起正式开放基于互联网的临床研究公共管理平台(Research Manager, ResMan),供广大临床研究人员、医院科研管理部门、药物研发单位和 CRO 使用。现在,国际医学期刊编辑委员会已开始要求研究者在临床试验投稿时提供其原始数据(individual participants data, IPD)在公共数据库的信息,供编辑、审稿专家和公众共享【1】;共享临床试验原始数据(IPD)已经成为临床试验透明化的重要组成部分。 一、什么是临床试验公共管理平台?临床研究公共管理平台(Research Manager, ResMan)是指将临床试验的管理流程、试验过程中记录的受试者基线资料包括人口学资料、入组时检查的基线数据、试验过程中的实施情况、结果数据等相关资料即“病历记录表(case record form, CRF)”的所有内容,基于互联网在线记录并传送到中央数据库保存管理。每项试验只允许该课题组研究人员进入并实施操作;对基金资助课题,项目管理者、试验申办者或投资者有权浏览实时资料但不能对之做任何更改。由研究者决定是否公开研究结果数据。数据一旦录入并保存,以后对数据所做的任何改动都会自动显示和追踪。研究者决定可公开的资料后,公众可通过“公众浏览”看到,以了解试验的进展情况和试验数据,但不允许看到或不能通过公开资料追索到受试者的任何个人信息。 二、为什么要使用临床研究公共管理平台? 1. 临床试验是研究者和参与者为解决医学领域的科学问题一起共同承担风险,为全社会获得相关医学知识所做出的奉献,因此,让全社会了解研究的细节是对奉献者最大的尊重; 2. 所有临床试验所获得的结果都可能应用于大众,涉及每一位公众的健康,因此,公众有权知道临床试验的所有细节和结果。无论试验结果如何,都应该让公众了解临床试验的细节,这是医学研究伦理的需要; 3. 项目管理机构、试验申办者或投资人可根据需要随时了解临床试验的执行情况和进度; 4. 让公众了解临床试验执行细节和过程可保证临床试验资料的真实性,增加临床试验的公信度; 5. 国际医学期刊编辑委员会要求投稿时需提交在公众可及(public accessible database)的公共数据库查询到原始数据,供医学期刊编辑和审稿专家审核稿件时核查; 6. 便于试验研究者保存和管理试验资料; 7. 可免除使用纸张记录,减少集中录入数据的错误可能性和工作量,提高记录可靠性,利于提高临床试验质量;
实验室检查结果及正常值(一)血常规 红细胞(RBC 成年男性:(4.0?5.5 )X 1012/ L 成年女性:(3.5?5.0 ) X 1012/ L 新生儿:(6.0 ?7.0 )X 1012/L 血红蛋白(Hb)成年男性:120?160g/L 成年女性:1l0?150g/L 新生儿:170?200g/L 白细胞(WBC 成人:(4.0 ?10.0 )X 109/L;新生儿:(15.0 ?20.0 )X 109/L 中性杆状核粒细胞:1%?5% 中性分叶核粒细胞:50%?70%嗜酸性粒细胞:0.5%?5%嗜碱粒性细胞:O%?1%淋巴细胞:20%?40%单核细胞:3%?8% 血小板(PLT (100?300 X 109/L (二尿常规 1.酸碱度(pH 5?8 2.比重(SG 1.015 ?1.025 3.尿蛋白(Pro )定性定量试验Pro定性:阴性(neg) , Pro定量w O.15g/24h 4.葡萄糖(Glu )定性:阴性(neg)、糖定量:<2.8mmol/24小时(0.5g /24小时) 5.酮体(Ket 阴性(neg 6.胆红素(Bil 和尿胆原(Ubg 均为阴性(neg 7.亚硝酸盐(Nit 阴性(neg 8.白细胞(Leu)<25/卩1 9.红细胞或血红蛋白(潜血试验)(Ery或OB w l0 /口1 10.尿沉渣镜检白细胞<5/HP (每高倍镜视野)红细胞<3/HP (每高倍镜视野) (三粪常规 1.颜色黄褐色成型便 2.镜检 (1 白细胞:正常粪便不见或偶见; (2 红细胞:正常粪便无红细胞; (3 细菌:主要为大肠杆菌和肠球菌; (4 虫卵。 3.粪便潜血试验(occult blood test , OBT正常粪便OBT阴性。(四痰液检验 一般性状检查正常人痰液呈无色或灰白色。 化脓性感染时呈黄色;绿脓杆菌感染时呈黄绿色;大叶性肺炎时呈铁锈色;急性左心衰时呈粉红色泡沫样痰;阿米巴肺脓疡时呈咖啡色。呼吸系统有病变时痰可呈粘液性、浆液性、脓性、血性。 (五)电解质 血清钾3.5?5.3mmol/L 血清钠135?145mmo K L 血清氯96?108mmoJ/L
附件 2: XX省临床实验室生物安全检查表 实验室名称:地点: 实验室负责人: 序 标得号 检查内容准检查方法分 分 1生物安全组织管理10 单位有组成合理的生物安全委员会、 1 有成立文件得 单位法人为生物安全的法定责任人 有会议记录得 实验室负责人为生物安全第一责任1有任命文件得 人 现场询问第一责任人的职 责回答完整得 有生物安全手册( SOP)并且现行有2有生物安全手册得 效 安全手册现行有效得有生物安全培训制度2有培训制度文件得
标得号 检查内容准检查方法分 分 有培训记录得 有危害评估体系及规范的危害评估书 面材料,包括检测项目生物因子的危 害程度评估、确定相应的生物安全防 护水平等级等,并且风险评估报告已 得到单位生物安全委员会批准 2人员管理 实验室生物安全第一责任人及实验 室生物安全员(检验科每个专业至 少设一名生物安全员)需持证上岗 实验室从事相关实验活动需接受生物 安全培训,每年至少接受一次培训 培训对象是否全面(应包括实验室管 理人员、技术人员、样本运输人员、 废弃物处置人员、仪器设备维修人员 等)4有评估资料得 内容完整得 有批文得 10 查看上岗证(每一个上岗 证得) 1有培训内容记录得 有培训人员签名得 2每一类型人员已接受培训得 培训内容是否全面(实验室生物安全 2 有每一大类内容得的基本知识、基本操作、应急处置预 案、化学和放射安全、生物危害和传
标得号 检查内容准检查方法分 分 染预防、应急救护等) 建立实验室人员的健康档案 ( 包括体2有健康体检档案得检、接 种、预防服药等 ) 档案全面完整得 3实验室设计20 实验室主入口有门禁系统、门上张贴 3 有门禁系统得 规范的生物危害标志 标志规范得 实验室有人员有准入规定,只有得到 1 有“准入规定”得 授权的人员方可进入 有授权签单得 实验室门为自动关闭的门 ( 有可视窗 2 门符合要求得 且带锁 ) ,所有门保持关闭 门保持关闭状态得 实验室污染区、清洁区分区明确,且 4 实验室分区明确 布局、走向合理 布局、走向符合从清洁区 到缓冲区再到污染区得
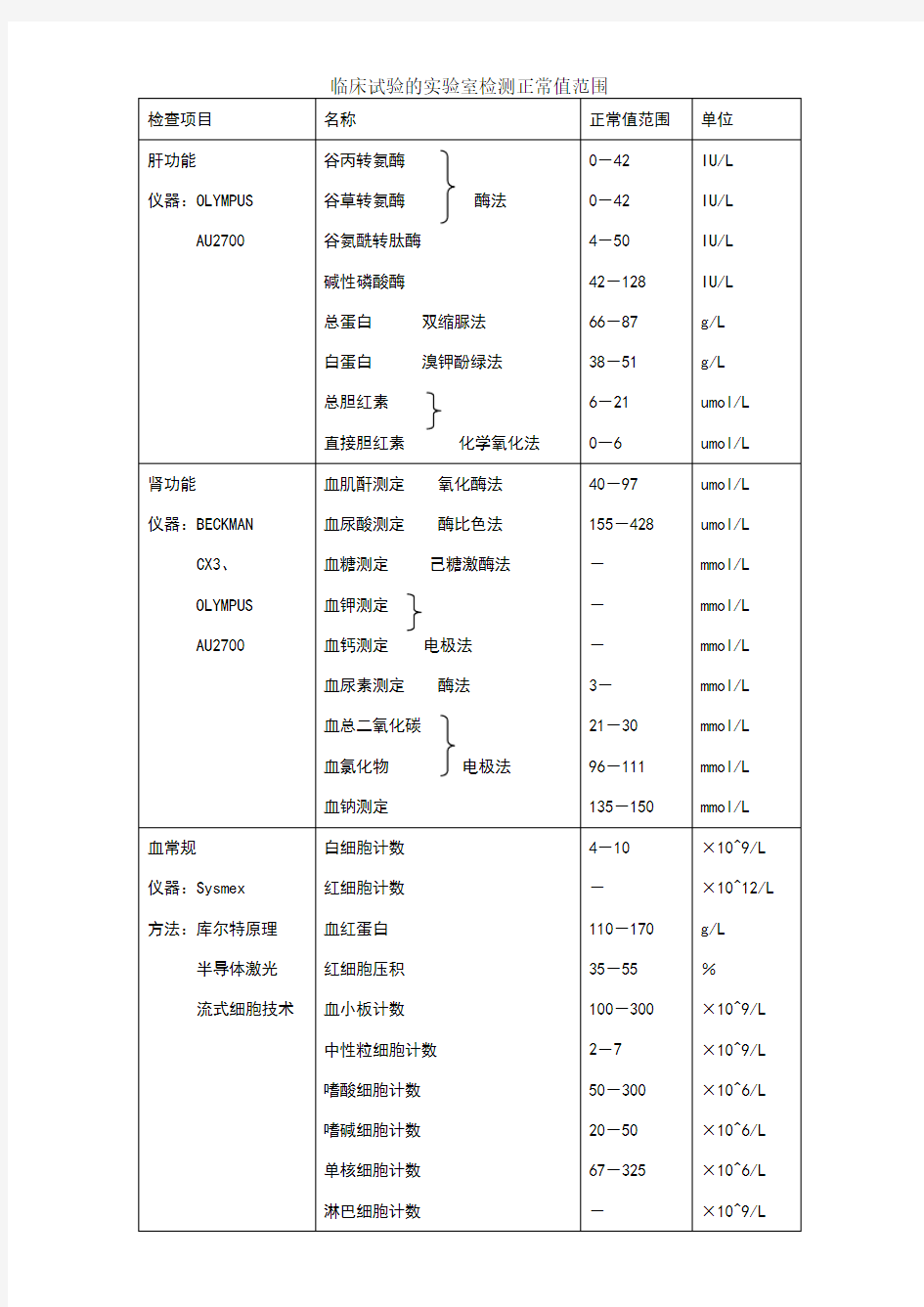
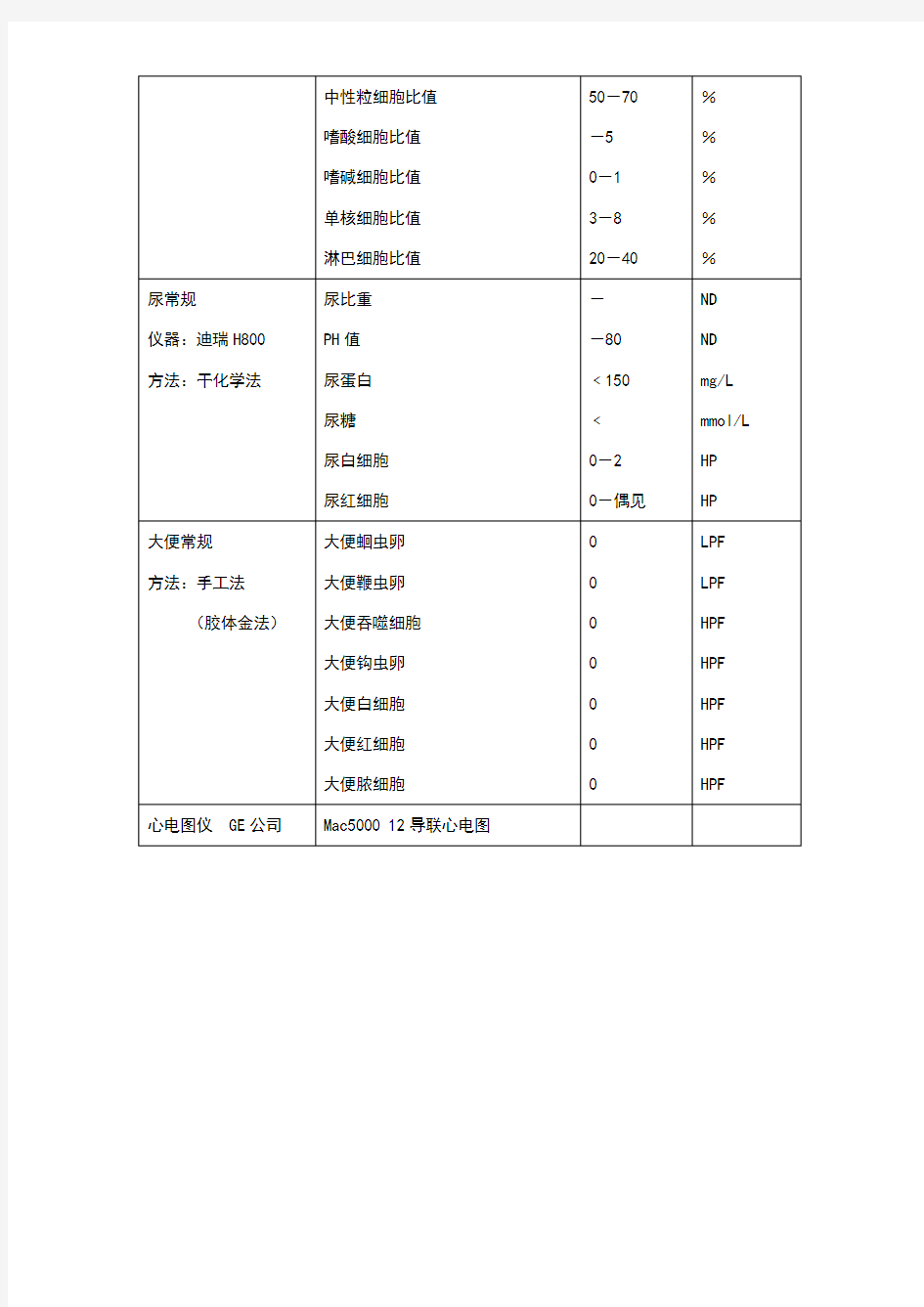
实验室检查正常值大 全
实验室检查结果及正常值 (一)血常规 红细胞(RBC)成年男性:(4.0~5.5)×1012/L成年女性:(3.5~5.0)×1012/L新生儿:(6.0~7.0)×1012/L 血红蛋白(Hb)成年男性:120~160g/L成年女性:1l0~150g/L 新生儿:170~200g/L 白细胞(WBC)成人:(4.0~10.0)×109/L;新生儿:(15.0~20.0)×109/L 中性杆状核粒细胞:1%~5% 中性分叶核粒细胞:50%~70% 嗜酸性粒细胞:0.5%~5% 嗜碱粒性细胞:O%~1% 淋巴细胞:20%~40% 单核细胞:3%~8% 血小板(PLT)(100~300)×109/L (二)尿常规 1.酸碱度(pH)5~8 2.比重(SG)1.015~1.025 3.尿蛋白(Pro)定性定量试验Pro定性:阴性(neg),Pro定量≤O.15g/24h 4.葡萄糖(Glu)定性:阴性(neg)、糖定量:<2.8mmol/24小时(0.5g/24小时) 5.酮体(Ket)阴性(neg)
6.胆红素(Bil)和尿胆原(Ubg)均为阴性(neg) 7.亚硝酸盐(Nit)阴性(neg) 8.白细胞(Leu)<25/μl 9.红细胞或血红蛋白(潜血试验)(Ery或OB)≤l0/μl 10.尿沉渣镜检白细胞<5/HP(每高倍镜视野)红细胞<3/HP(每高倍镜视野)(三)粪常规 1.颜色黄褐色成型便 2.镜检 (1)白细胞:正常粪便不见或偶见; (2)红细胞:正常粪便无红细胞; (3)细菌:主要为大肠杆菌和肠球菌; (4)虫卵。 3.粪便潜血试验(occult blood test,OBT)正常粪便OBT阴性。 (四)痰液检验 一般性状检查正常人痰液呈无色或灰白色。 化脓性感染时呈黄色; 绿脓杆菌感染时呈黄绿色; 大叶性肺炎时呈铁锈色; 急性左心衰时呈粉红色泡沫样痰; 阿米巴肺脓疡时呈咖啡色。 呼吸系统有病变时痰可呈粘液性、浆液性、脓性、血性。
一、常规项目 检验项目英文缩写正常值范围临床意义 红细胞计数 RBC 男(4.4-5.7 ×1012/L 女(3.8-5.1 ×1012/L 新生儿(6-7 ×1012/L 儿童(4.0-5.2 ×1012/L RBC ↑ ,见于真性经细胞增多症,严重脱水、烧伤、休克、肺源性心脏病、先天性心脏病,一氧化碳中毒、剧烈运动、高血压、高原居住等。 RBC ↓ ,各种贫血、白血病,大出血或持续小出血, 重症寄生虫病,妊娠等。 血红蛋白 Hb 、 Hgb 男 120-165g/L 女 110-150g/L 血红蛋白增减的临床意义与红细胞计数基本相同 红细胞压积 PCV 或 HCT 男性 0.39-0.51 女性 0.33-0.46 PCV ↑ 脱水浓缩, 大面积烧伤, 严重呕吐腹泻, 尿崩症等。PCV ↓ 各种贫血,水中毒,妊娠。 红细胞平均体积 MCV 80-100fL MCV 、 MCH 、 MCHC 是三项诊断贫血的筛选指标。平均细胞血红蛋白 MCH 27-32Pg 平均细胞血红蛋白浓度 MCHC 320-360g/L 网织红细胞计数 Ret ·c 成人 0.5%-1.5% Ret ·c ↑ 见于各种增生性贫血。 Ret ·c ↓ 肾脏疾病,分内泌疾病,溶血性贫血再生危象, 再生障碍性贫血等。 血小板计数 PLT BPC (100-300 ×109/L ↑ 增多,急性失血、溶血、真性红细胞增多症、原发性血小板增多、慢性粒细胞白血病、脾切除术后(2月内、急性风湿热、类风湿性关节炎、溃疡性结肠炎、恶性肿瘤、大手术后(2W 内等。
血小板计数 PLT BPC (100-300 ×109/L 减少①遗传性疾病。②获得性疾病,免疫性血小板减少性紫癜、系统性红斑狼疮、各种贫血。 以及脾、肾、肝、心脏疾患。另有阿斯匹林、抗生素药物过敏等。 白细胞计数 WBC 成人(4-10 ×109/L 儿童(5-12 ×109/L 新生儿(15-20 ×109/L 增多:若干种细菌感染所引起的炎症,以及大面积烧伤、尿毒症、传染性单核细胞增多症、传染性淋巴细胞增多症、百日咳、血吸虫病、肺吸虫病、白血病、类白血病、恶性肿瘤、组织坏死、各种过敏、手术后、尤以脾切除后为甚等。 WBC 减少:感冒、麻疹、伤寒、副伤寒、疟疾、斑疹伤寒、回归热、粟粒性 结核、严重感染、败血症、恶性贫血、再生障碍性贫血、阵发性夜间血红蛋白尿症、脾功能亢进、急性粒细胞减少症、肿瘤化疗、射线照射、激素治疗以及多种药物如解热镇痛药、抗生素、抗肿瘤药、抗癫痫病、抗甲状腺药、抗疟药、抗结核药、抗糖尿病药物等。 白细胞计数生理性增多:新生儿、妊娠期、分娩期、月经期、餐后剧烈运动后,冷水浴后、日光浴、紫外线照射、神经过度紧张、恐惧、恶心、呕吐。 白细胞分类计数 WBC 、 DC 中性粒细胞杆状核 1%-5% 分叶核 50%-70% 增多:急性和化脓性感染(疖痈、脓肿、肺炎、阑尾炎、丹毒、败血症、内脏穿孔、猩红热等,各种中毒(酸中毒、尿毒症、铅中毒、汞中毒等,组织损伤、恶性 肿瘤、急性大出血、急性溶血等。 减少:见于伤寒、副伤寒、麻疹、流感等传染病、化疗、放疗。某结血液病(再生障碍性贫血、粒细胞缺乏症、骨髓增殖异常综合症、脾功能亢进、自身免疫性疾病等。 嗜酸性粒细胞 0.5%-5.0% 增多:见于过敏性疾病、皮肤病、寄生虫病、某些血液病、射线照射后,脾切除术后、传染病恢复期等。减少:见于伤寒、副伤寒、应 用糖皮质激素,促肾上腺皮质激素等。