
第22卷 第4期大学化学2007年8 月 手性化合物的命名 王永梅 张文昊 翟玉平 (南开大学材料化学系 天津300071) 摘要 在总结各种手性化合物命名的基础上,加入了硅,氮,磷,硫,砷手性化合物的命名,着重阐述了新型手性分子的命名法则,并配以实例说明。 随着不对称合成的快速发展,手性化合物的结构和类型日渐丰富。手性碳化合物绝对构型的命名已为人们熟知,而新的手性化合物,如平面手性、螺手性的命名成为需要解决的问题。本文在总结前人工作的基础上,较全面地归纳了各种手性化合物的命名。 1 手性化合物的分类 分子存在手性的条件是分子实物和镜像不能重合。 分子结构是整个命名系统的基础,是命名法的根据。按分子结构可以把手性分子分为6类。 1.1 中心手性 图1显示了几种不同的手性中心,以手性中心为特征的分子称为中心手性化合物。特点是中心原子连有4个不同的基团(或孤对电子)。中心原子可以是主族的C,Si,N,P,A s,S,Ge 等,也可是副族的Mn,Cu,B i,Zn 等 。 图1 不同的手性中心 图2 轴手性化合物(丙二烯) 1.2 轴手性 轴手性在结构上可看作中心手性的衍生。分子中的4个 基团分为两对排列在手性轴的两端。当每对中的两个基团都不相同时,分子有手性。这类化合物包括:丙二烯型, 环己烷 图3 平面手性化合物 型,螺环型和联芳型(图2)。 1.3 平面手性 分子中某一平面两侧的结构不对称,这类化合物称为平 面手性化合物。图3分子中苯环所在平面为手性平面。
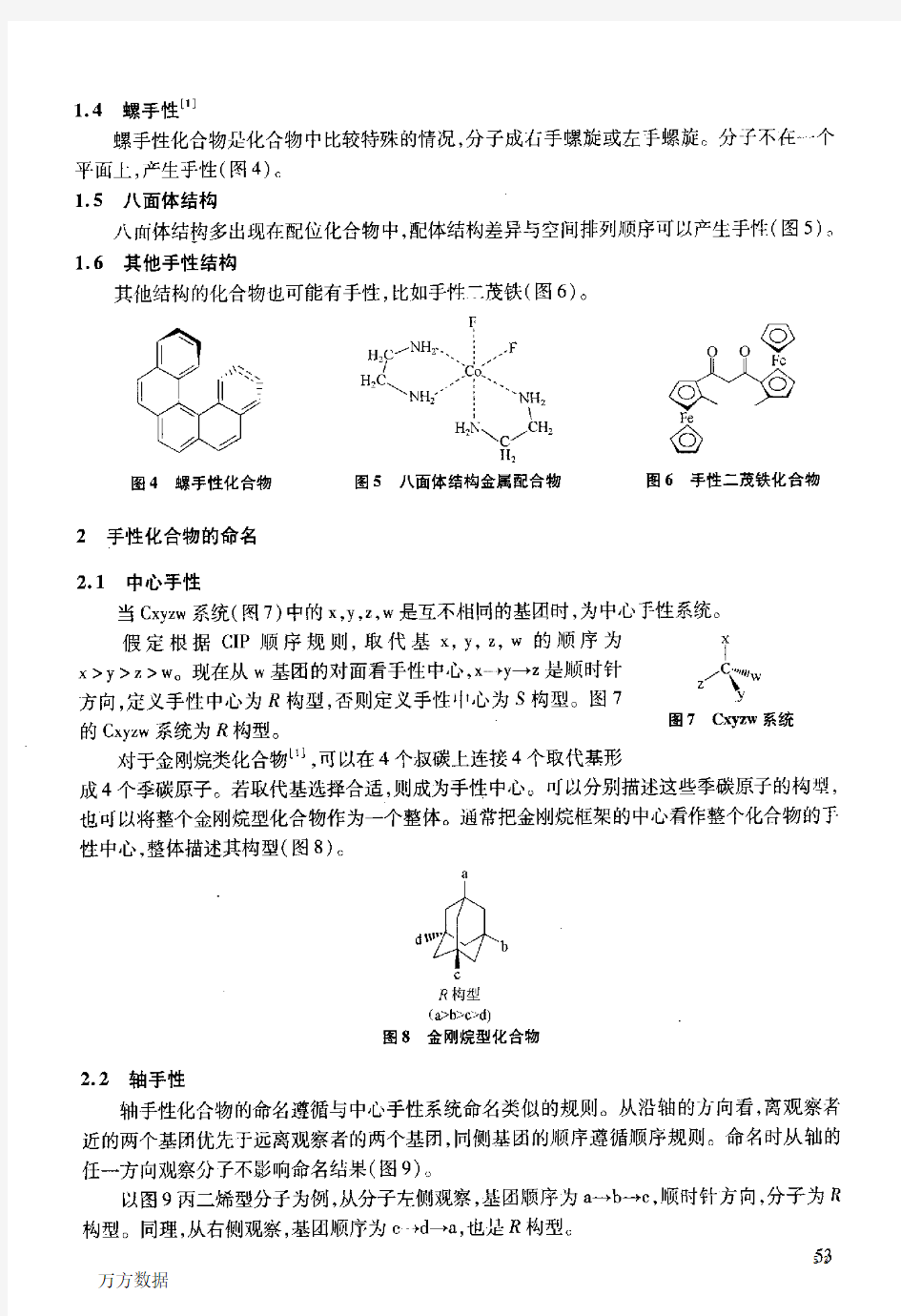
1.4 螺手性[1] 螺手性化合物是化合物中比较特殊的情况,分子成右手螺旋或左手螺旋。分子不在一个平面上,产生手性(图4)。 1.5 八面体结构 八面体结构多出现在配位化合物中,配体结构差异与空间排列顺序可以产生手性(图5)。 1.6 其他手性结构 其他结构的化合物也可能有手性,比如手性二茂铁(图6) 。 图5 八面体结构金属配合物 图4 螺手性化合物 图6 手性二茂铁化合物 2 手性化合物的命名 2.1 中心手性 当Cxyz w 系统(图7)中的x,y,z,w 是互不相同的基团时,为中心手性系统 。 图7 Cxyzw 系统 假定根据C I P 顺序规则,取代基x,y,z,w 的顺序为 x >y >z >w 。现在从w 基团的对面看手性中心,x →y →z 是顺时针 方向,定义手性中心为R 构型,否则定义手性中心为S 构型。图7 的Cxyz w 系统为R 构型。 对于金刚烷类化合物[1],可以在4个叔碳上连接4个取代基形 成4个季碳原子。若取代基选择合适,则成为手性中心。可以分别描述这些季碳原子的构型,也可以将整个金刚烷型化合物作为一个整体。通常把金刚烷框架的中心看作整个化合物的手性中心,整体描述其构型(图8) 。 图8 金刚烷型化合物 2.2 轴手性 轴手性化合物的命名遵循与中心手性系统命名类似的规则。从沿轴的方向看,离观察者近的两个基团优先于远离观察者的两个基团,同侧基团的顺序遵循顺序规则。命名时从轴的任一方向观察分子不影响命名结果(图9)。 以图9丙二烯型分子为例,从分子左侧观察,基团顺序为a →b →c,顺时针方向,分子为R 构型。同理,从右侧观察,基团顺序为c →d →a,也是R 构型。
手性化合物色谱分析方法开发(一) 1、概述 首先,这里所说的手性化合物是指含有一个或多个不对称碳手性中心的对映或者非对映异构体,而不包含氮磷等含有孤电子对的手性中心化合物。不对称性碳原子,需要具有四个不同的取代基,空间上形成不对称四面体,对映异构体之间形成镜面对称,就像人的左右手一样,不能够完全重合,如下图1所示。 Fig.1Diagram for enantiomers 对映异构体具有不同的使偏振光旋转的能力,据此对映异构体可以分为左旋与右旋。在非手性环境下,对映异构体具有相同的化学性质(化学反应特性),相同的物理性质(如溶解度、熔点、沸点、熵焓等)以及同样的色谱保留行为等。但在手性环境中对映异构体之间的某些性质则表现出不同,这也是手性化合物进行拆分的基础。 对映异构体需要对内消旋体与外消旋体进行区分,如下图2所示。左右两个示意化合物结构的相同点在于均具有两个手性中心,不同点则在于左图的两个手性碳原子之间不存在对称平面或轴,而右图则存在对称平面。因此在左图中,1S,2R与1R,2S为外消旋体;右图中1S,2R与1R,2S为内消旋体。
Fig.2Name and distinguish between mesomer and racemate 对于手性化合物的拆分,规模比较大的时候,可使用其他手性试剂(如酒石酸钠)与待拆分的化合物形成非对映异构体,然后根据非对映异构体之间具有不同的物理化学性质,进行相应的分离单元操作。而在分析实验室中,一般是采用色谱法进行拆分,其中包括使用手性固定相法以及在流动相中添加手性流动相形成手性拆分环境的方式。其中手性固定相拆分法包括气相色谱以及液相色谱。 对于气相色谱拆分手性化合物,其拆分选择性主要取决于所使用的手性固定相的种类以及色谱分离的温度。一般气相用于低沸点的手性化合物的拆分,对于有机酸碱等极性手性化合物的拆分,一般需要先进行柱前衍生化处理,使之形成相应的酯或者酰胺。用于气相手性拆分的手性固定相均为环糊精衍生物类,包括β以及γ环糊精,α环糊精比较少;其最高耐受温度不会超过220℃,而且分离温度超过120℃的时候,固定相的手性选择性开始降低;超过200℃的时候,固定相的手性选择性几近与无。 对于液相色谱而言,起主要拆分选择性作用的既包括手性固定相也包括流动相的选择,而且液相色谱可以使用正相洗脱模式,反相洗脱模式,也可以使用极性洗脱以及极性离子洗脱模式;可以等度也可以梯度。最重要的是,色谱柱的类型要比气相色谱手性固定相多的多,其中就包括多糖类衍生物类手性固定相、环糊精及其衍生物类手性固定相、糖蛋白类手性固定相以及大环内酯抗生素类以及冠醚类手性固定相等。此外,液相色谱拆分法可以对样品进行回收而且也可以用于对映异构体的制备,气相色谱法则不能方便的对对映异构体进行制备。
在有机合成中产生手性化合物的方法有4种: 1.使用手性的底物 2.使用手性助剂 3.采用手性试剂 4.使用不对称催化剂 常常需要使用天然产物,如:氨基酸、生物碱、羟基酸、萜、碳水化合物、蛋白质等。 1.使用手性的底物 这种方法局限于比较有限的天然底物 如图,该化合物的硼氢化反应中,由于羟基的作用产生另外新的立体中心(反应从分子的背后发生) 以下两个反应,第一个是由于羧基的控制得到相应的手性产物..另一个则是由于反应中间体烯醇阴离子的构象决定了构型 2.使用手性助剂 如图,在第一步使用LDA去质子化时,为了使得上边的醇锂和下边的烯醇锂相距最远,Z-异构体占优势,在下一步与EtI的反应中得以产生了立体中心。 类似地,用烯醇锆替代烯醇锂(使用LDA,ZrCp2Cl2)确保烯醇的构型,再和醛反应产生不对称中心。 这些反应多数通过手性助剂的金属原子和底物中已有手性的O、N等原子络合,之后再加入其他试剂实现不对称中心的形成。这其中手性唑啉环是一个非常不错的手性助剂,它水解后可以生成一个羧基(潜在官能团) 另外一个试剂是手性的3-烷基哌嗪-2,5-二酮(一个环状二肽,可由两个氨基酸环合生成),如图 在羰基的α位进行不对称烷基化使用的是以下两种试剂A和B(B称为SAMP),如图,对环己酮的反应中采用A得到S异构体而采用B得到R异构体.
在氨基的α位进行不对称烷基化使用的试剂如下二图,用胺和它们作用后再用LDA、MeI甲基化,最后用N2H4脱去助剂得到产物. 还有一些有趣的反应如脯氨酸的α烷基化,涉及到一个立体化学的"存储"问题,经历了一个消失和再产生的过程:: 手性亚砜的作用:分离得到手性亚砜试剂和卤代烷作用后在下一步反应中诱导手性基团的产生,Al/Hg可以方便地除去亚砜基团。 3.采用手性试剂 通过铝锂氢化物与手性二胺或氨基醇作用可以得到一个用于不对称还原的试剂。如图。 利用α-蒎烯和9-BBN作用得到的试剂是一个很好的不对称还原试剂.如图 不对称硼氢化反应也是一个很好的构造立体化学中心的反应。这里需要利用α-蒎烯(图中的反应是针对三取代烯烃的,对于双取代烯烃应采用条件温和的双取代硼烷)
浅谈手性化合物与现代医学 一、手性化合物简介 手性化合物(chiral compounds)是指分子量、分子结构相同,但左右排列相反,如实物与其镜中的映体。人的左右手、结构相同,大姆至小指的次序也相同,但顺序不同,左手是由左向右,右手则是由右向左,所以叫做“手性”。也就是指一对分子。由于它们像人的两只手一样彼此不能重合,又称为手性化合物。判断分子有无手性的可靠方法是看有没有对称面和对称中心。 手性问题与我们的日常生活密切相关。天然存在的手性化合物品种很多,并且通常只含有一种对映体,手性问题还牵涉到农业化学、食品添加剂、饮料、药物、材料、催化剂等诸多领域。它的研究已经成为科学研究和很多高科技新产品开发的热点。在过去20年里,手性研究具有戏剧性的发展,已从过去的少数几个专家的学术研究发展到大面积科学研究的需要,在一些领域并已带来了巨大的经济效益。物质的手性已经变成越来越需要考虑的问题,其对我们的日常生活正在起到越来越重要的作用。 手性化合物主要从天然来源、不对称合成和外消旋体拆分3个方面得到。由天然来源获得手性化合物,原料丰富,价廉易得,生产过程简单,产品的纯度一般都较高,因此很多量大的产品都是从天然物中获得。在药物工业中由于对手性药物的要求不断增加,其大大激发了不对称有机合成的发展,使一些生物技术、生物催化剂也迅速扩展到该领域产生纯的的手性中间体和手性产品。 二、手性药物 由于自然界的生命体存在有手性,因而也就产生了手性药物。手性药物指分子结构中存在手性因素的药物。通常是指由具有药理活性的手性化合物组成的药物,或者是只含有效对映体或是以有效对映体为主的药物。按药效方面的简单划分,手性药物可能存在以下几种不同的情况:①只有一种对映体具有所要求的药理活性,而另一种对映体没有药理作用或活性很小。②一对对映体中的两个化合物具有等同或近乎等同的同一药理活性。③一对对映体具有完全不同的药理活性。 ④一对对映体之间一个有药理活性,另一个不但没有活性,甚至表现出一定的毒副作用。⑤一对对映体之间药理活性相近,但存在个体差异。⑥一对对映体中,一个有活性,另一个却发生拮抗作用。 三、手性药物未来展望 手性制药是医药行业的前沿领域,2001年诺贝尔化学奖就授予在分子不对称催化反应中做出杰出贡献的三位科学家。目前,世界单一对映体手性药物的销售额持续增长。1998年销售额已达到964亿美元。2000年的销售额为1330亿美元,并估计2008年达到2000亿美元。手性药物以其疗效高、毒副作用小、用药量少的优点满足了市场的需求,因而成为未来新药研发的方向。
手性分子的合成方法及研究进展 学号: 班级: 姓名:
摘要:本文主要将手性药物的合成方法分为了两大类,并分别列举了一些方法,其中详细介绍了手性源合成以及酶法获得手性化合物两种方法,并通过对方法的介绍简述了手性化合物的研究进展。 关键词:手性化合物、合成、研究进展 手性是自然界最重要的属性之一,分子手性识别在生命活动中起着极为重要的作用。同一化合物的两个对映体之间不仅具有不同的光学性质和物理化学性质,而且它们具有不同的生物活性,比如在药理上,药物作用包括酶的抑制、膜的传递、受体结合等,均和药物的立体化学有关;手性药物的对映体的生物学活性、毒性、代谢和药物素质完全不同。获得手性化合物的方法,不外乎非生物法和生物法两种。 一、非生物法 非生物催化主要是指采用化学控制等手段来获得手性化合物,它主要包括不对称合成法、手性源合成、选择吸附拆分法、结晶法拆分、化学拆分法、动力学拆分、色谱分离等。下面主要介绍手性源合成: 手性源合成或者手性底物的诱导,该方法被称为第一代手性合成方法,亦称为底物控制法。它是通过底物中原有手性的诱导,在产物中形成新的手性中心。可简略表述为:原料为手性化合物A*,经不对称反应,得到另一手性化合物B*,即手性原料转化为反映产物。 美国Scripps 研究所Wong等曾报道了利用阿拉伯糖来合成L-N-乙酰神经氨酸的方法,该方法便是极其巧妙的利用了手性源合成。 阿拉伯糖是一个醛糖,它开环后的醛基与氨基化合物得到Schiff 碱中间体,硼酸衍生物上的乙烯基以富电子碳原子于Schiff碱上的碳原子发生亲核进攻,得到烯烃衍生物中间体,氨基用酸酐保护,总产率55%, de%为99%。烯烃衍生物中间体与硝酮衍生物进行1,3偶极环加成,得到氮氧五元环化合物,加成过程立体选择性较好,90%的产物是立体控制的。氮氧物五元环化合物经过脱质子化得到西佛碱中间体,水解后即得到L-N-乙酰神经氨酸(如图)。
手性化合物的合成和分离方法研究进展 摘要:手性问题与我们的生活密切相关,它涉及到生命、动植物、药物、食品、香料、农药等诸多领域,本文介绍了手性化合物的一些用途,合成和分离方法及发展方向。手性化合物的制备已成为当前国内外较热门的研究课题之一。本文从非生物法和生物法两个方面较全面地综述了手性化合物的制备方法, 希望为相关研究者提供参考。 关键词:手性化合物;手性药物;制备;生物合成 1.1用途 手性化合物(chiral compounds)是指分子量、分子结构相同,但左右排列相反,如实物与其镜中的映体。人的左右手、结构相同,大姆至小指的次序也相同,但顺序不同,左手是由左向右,右手则是由右向左,所以叫做“手性”。也就是指一对分子。由于它们像人的两只手一样彼此不能重合,又称为手性化合物。判断分子有无手性的可靠方法是看有没有对称面和对称中心[1]。 手性问题与我们的日常生活密切相关。天然存在的手性化合物品种很多,并且通常只含有一种对映体,手性问题还牵涉到农业化学、食品添加剂、饮料、药物、材料、催化剂等诸多领域。它的研究已经成为科学研究和很多高科技新产品开发的热点。在过去20年里,手性研究具有戏剧性的发展,已从过去的少数几个专家的学术研究发展到大面积科学研究的需要,在一些领域并已带来了巨大的经济效益。物质的手性已经变成越来越需要考虑的问题,其对我们的日常生活正在起到越来越重要的作用。 手性化合物主要从天然来源、不对称合成和外消旋体拆分3个方面得到。由天然来源获得手性化合物,原料丰富,价廉易得,生产过程简单,产品的纯度一般都较高,因此很多量大的产品都是从天然物中获得。在药物工业中由于对手性药物的要求不断增加,其大大激发了不对称有机合成的发展,使一些生物技术、生物催化剂也迅速扩展到该领域产生纯的的手性中间体和手性产品[2]。 1.生物制药 在合成中引入生物转化在制药工业中已成为关键技术。如Merck公司开发的酰胺酶抑制剂西司他丁的生产就是一个实例。西司他丁是一种N-取代的(S)-2,2-二甲环丙烷羰酰胺衍生物,它可以从易得原料合成消旋2,2-二甲基环丙羰腈开始,通过不同途径合成。 2.生物农药 拟除虫菊酯类杀虫剂是70年代中期开始大量使用的新型农药,是天然除虫菊酯的模拟物,生物降解性好,对环境影响小。拟除虫菊酯具高效安全杀虫谱广等优点。在世界农药市场占有一定的地位。手性化合物在生物农药方面也有广扩的前景,此杀虫剂占全球杀虫剂市场的20%。 3.香料、添加剂和酶技术 香精香料和其他行业占手性市场总值的4.7%;如人工合成一些甜味剂癸内酯具有强烈的果香香气。 酶技术的一个新方向是美国Altus Biologics的交联酶结晶(cross - linked enzyme
Chirality Direct chiral discrimination in NMR The calculated isotropic component of the proton magnetic shielding polarizability for hydrogen peroxide (H2O2) is shown as a function of dihedral angle (_, as defined in the inset). The two enantiomers are R-HOOH for dihedral angles <180° and S-HOOH for dihedral angles >180°. σ(1)(N) is obtained from finite field calculations at the SCF level. The solid line is to guide the eye, and 1 ppm a.u. = 1.9446 _ 10-18 m/V. Nuclear magnetic resonance (NMR) spectroscopy is an important technique for determining the structure of molecules in solution. NMR can, however, not yet be used to determine the absolute configuration of chiral molecules in a pure liquid, as the chemical shifts and spin-spin coupling constants are identical for the two enantiomers of a chiral molecule. All NMR-based methods for chiral discrimination have therefore required that the chiral solute be in the presence of a chiral reagent or solvent. However, the electric-field perturbed chemical shift tensor, the nuclear magnetic shielding polarizability σ(1)(N), gives rise to three chiral NMR effects in a liquid that could make it possible to discriminate directly between the enantiomers of a chiral molecule: The coherent precession of nu clear spins following application of a π/2 pulse to an optically active liquid will lead to a rotating macroscopic electric polarization [1]; a laser polarized in the plane perpendicular to the field of the magnet may in principle give rise to chiral chemical shifts; and the application of an (oscillating) electric field at right angles to the magnetic field of the spectrometer may
手性化合物 手性化合物是指分子量、分子结构相同,但左右排列相反,如实物与其镜中的映体。人的左右手、结构相同,大姆至小指的次序也相同,但顺序不同,左手是由左向右,右手则是由右向左,所以叫做“手性”。也就是指一对分子。由于它们像人的两只手一样彼此不能重合,又称为手性化合物 什么是手性? 当我们伸出双手,双手手心向上时,可以看出左右手是对称的,但是将双只手叠合,无论如何也不能全部重叠,总有一部分是不能重合在一起的;如果我们将左手置于一面平面镜前,手心对着镜子,可以看到镜子里的左手的像和右手手心对着自己一样,即左手的像和右手可以完全重叠。象这样左手和右手看来如同物与像,但又不能叠合在一起,互相成为“镜像”关系,就称之为“手性”。 有机化合物是含碳的化合物,一个碳原子的最外层上有四个电子,若以单键成键时,可以形成四个共价单键,共价键指向四面体的顶点,当碳原子连接的四个基团各不相同时,与这个碳原子相连接的四个基团有两种空间连接方式,这两种方式如同左右手,互为“镜像”,也是不能完全叠合在一起的,因此,这样的分子叫做“手性分子”。这种构成手性关系的分子之间,把一方叫做另一方的“对映异构体”。许多有机化合物分子都有“对映异构体”,即是具有“手性”。构成生物体的许多有机化合物都有“手性”。如α-氨基酸,在碳连接有一个羧基、一个氨基、一个烃基和一个氢原子(或一个不同于前边的烃基)*,这时你想将其中三个相同颜色的球重叠,但是余下的那个颜色的球总不能重叠。由这些手性氨基酸组成的蛋白质也就与“手性”有密切的关系,因此,生命生理活动中的许多现象与“手性”密不可分。 如何检验物质具有手性? 手性物质具有一特殊性质——旋光性,将纯净的手性物质的晶体,或是将纯净的手性物质配成一定浓度的溶液,用平面偏振光1照射,通过手性物质的偏振光平面会发生一定角度的旋转,这称为旋光性。这种偏振光的平面旋转可左可右,以顺时针方向旋转的对映体,称为右旋分子,用“+”或“d”表示;以逆时针方向旋转的对映体,称为左旋分子,用“-”或“l”;如果将互为对映体的手性物质等物质的量混合后,以偏振光照射,而偏振光不发生旋转,称为外消旋体或外消旋混合物,外消旋体是由于左旋分子和右旋分子发生的偏振光旋转
手性分子绝对构型的确定 手性分子可以分为下面几种类型:中心手性分子,轴手性分子,平面手性分子及螺旋手性分子。 下面用R/S 命名法依次对它们进行命名。 中心手性分子: 如果一个原子连接四个不同的基团,则称这个原子具有手性。常见的有C, N, P, S, Si, As 等原子。 判断方法:先将与手性原子相连的四个原子(团)按次序规则进行排列,然后将次序最小的原子(团)放在距观察者最远的位置,再观察其他3个原子(团)的排列次序,若由大到小的排列次序为顺时针方向,则R 为型,若为逆时针方向,则为S 型. e a 假定原子的优先次序为a >b > d >e b d 为顺时针方向,R 型 b d 为逆时针方向,S 型 轴手性分子:四个基团围绕一根轴排列在平面之外的体系,当每对基团不同时,有可能是不对称的。轴手性分子可分为以下几种类型: 丙二烯型分子:螺环型分子: 环外双键型分子: 联苯型分子: C 3 3 H 3 3 H 3 (远端) 逆时针方向,R 型 顺时针方向,R 型 (近端)逆时针方向,S 型 (近端)逆时针方向,S 型 从左向右看: 从左向右看: (远端) 判断方法:从左向右看,先看到的基团为近端,用实线表示,后看到的基团为远端,用虚线 表示,然后从近端的大基团看到近端的小基团再看到远端的大基团(不看远端的小基团),若为顺时针方向,则为则R 为型,若为逆时针方向,则为S 型. 平面手性分子:平面手性通过对称平面的失对称作用而产生,其手性取决与平面的一边与另
一边的差别,还取决与三个基团的种类。判断方法:第一步是选择手性平面,第二步是确定平面的优先边,这个优先边可以通过按标准的顺序规则在直接连接到平面原子的原子中找到哪一个是最优先的来确定。连接到平面的一套原子中的最优先原子,即先导原子或导向原子标记了平面的优先边(标记为1号),第二优先(标记为2号)给予手性平面直接与1号基团成轴连接的原子,等等,对于1-2-3为顺时针方向,则为R p 为型,若为逆时针方向,则为S p 型. 例如: S p 型R p 型 螺旋手性分子:螺旋性是手性的一个特例,其中分子的形状就像右的或左的螺杆或盘旋扶梯,从旋转轴的上面观察,看到的螺旋是顺时针方向的定为P 构型,而逆时针方向的定为M 构型. 例如: M 型 几个例子: 22 3 从上往下看: 顺时针方向,R 构型 近端 远端 从左向右看: R S 参考文献 《有机结构理论》,图书馆藏书
2018年第26卷 第1期,66~76 合成化学 Chinese Journal of Synthetic Chemistry V o l.26, 2018 No. 1,66-76 ?综合评述? 以联萘酚$binol)为骨架的轴手性化合物 在不对称催化中的研究进展 朱广乾,王鹏! (山东科技大学化学与环境工程学院,山东青岛266590) 摘要:具有C!对称轴的1,r-联二萘酚(B IN0L)具有非手性碳的手性旋光构型,此类分子的独特立体结构决定 了分子兼具刚性和高的立体控制能力,以联萘酚为骨架衍生的一系列新颖的化合物以其优越的手性控制性能和 手性催化剂方面的优良应用而备受关注。本文以有机合成中深具研究前景的不对称催化为切人点,综述了具有 手性联萘酚结构的磷酸化合物、联萘酸金属磷酸盐化合物、联萘酚膦化合物以及相关衍生物在不对称催化反应 中的研究进展。参考文献36篇。 关键词:联萘酚;金属磷酸盐;联萘酚膦配体;不对称催化;综述 中图分类号:0621.3文献标志码:A D O I:10. 15952/j. cnki. cjsc. 1005-1511.2018.01. 17099 P r o g r e s s i n C h i r a l C o m p o u n d s D e r i'^e d f r o m B i n a p h t h o l(B I N O L)S k e l e t o n i n A s y m m e t r i c C a t a l y s i s ZHUGuang-qian,WANG Peng* (College of Chemistry and Environmental Engineering,Shandong University of Science and Technology,Qingdao 266590,China) A b s tra c t: 1,1^-EJinaphthol!^BIN0L)w itli C2symmetry w as chiral optical configuration which has none chiral carbon.The unique spatial structure l eads this type of molecule has high trol a bility.A series of novel chiral compounds derived from B I1N0L structure have provided their supe-rior performance based on stereo control ability and the use of asymmetric cataly introduce the applications of the BIN0L based complexes w itii optical activi chiral phosj^horic acid,binaphthol metal phosj^hate,binaphthol phosj^horus li g ands and related deriva-tives in asymmetric catalytic reactions,were reviewed w it!i 36 references. K e yw o rd s:binaphthol(BIN0L); binaphthol metal phosphate;binaphthol phosphorus ligand;asym-metric catalytic reaction;review 自然界的基本生命现象和相关定律都是由手 性(或称为不对称性)产生的,手性是自然界尤其是生命体的一个基本属性。生命物质如蛋白质、核酸、多糖等都是手性的,这些物质在生命体内均以某特定的单一构型存在,完成相关的催化等特定任务。手性化合物的对映异构体虽然在结构上 很相似,但对生物体而言,许多手性化合物的对映 异构体会表现出不同的特性。因此在进行不对称 收稿日期:2017-05-02;修订日期:2017-12-05 基金项目:国家自然科学基金资助项目(21101099) 作者简介:朱广乾(1993 -),男,汉族,山东章丘人,硕士研究生,主要从事不对称有机合成研究。E-mail: 1015376970@qq.c m 通信联系人:王鹏,副教授,Tel. 0532-********,E-mail:pengwang@https://www.doczj.com/doc/2f14862175.html,
手性化合物的拆分技术研究进展 摘要 本文综述了分离外消旋体的几种主要拆分方法的优缺点及其应用情况。分别有:化学拆分法、膜拆分法、色谱拆分法以及毛细管电泳拆分法。 关键词:手性物;拆分;外消旋体 Technical Progress of Chiral Separation Abstract This article reviews separation methods of chiral which include chemical,membranous,chromatographic and electrophoretic methods. Key words:chiral compounds;chiral separation;raceme 目前获得手性物的主要方法还是通过拆分外消旋体。早期的拆分方法主要有机械拆分,结晶拆分以及手性溶剂结晶拆分。这三种方法都是利用外消旋混合物的两种对应体结晶性能不一样的特点进行分离。已经有较成熟工业应用,但一次性收率较差,在此不做赘述还是本文综述了今年来手性拆分方法中使用较多的化学拆分法、膜拆分、色谱拆分以及毛细管电泳拆分四种拆分技术。 1化学拆分[1] 1.1生成非对映体拆分 此方法是利用外消旋混合物与手性试剂反应后生成有不同性质的非対映体,从而利用生成物的不同物理性质(溶解度、蒸汽压、结晶速率等)将其分离,再将分离后的物质分别还原成之前的対映体。 还可以使用拆分剂家族代替单一拆分剂进行拆分,所谓拆分剂家族是指有类似结构的2~3个手性剂拆分剂。组合拆分提高了产品收率和纯度。 1998年Hulsho F L A等人[2]就使用一定量的(S,S)酒石酸衍生物的拆分剂家族拆分3-(1,4-亚乙基哌啶基)苯甲酸酯和3,4-二笨基四氢吡咯,经过一定处理后,两种対映体的纯度(ee值)分别达到了99%和98%。 如果拆分剂不能和対映体反应,就可以利用拆分剂的空穴与两种対映体之间
手性物质提取分离 手性药物的结晶拆分方法: 手性化合物的拆分是给外消旋混合物制造一个不对称的环境,使两个对映异构体能够分离开来。 从方法学上来讲,可以分为结晶拆分法(物理拆分方法、化学拆分方法)、动力学拆分方法、生物拆分方法(相当部分是生物催化的动力学拆分)及色谱拆分方法。 --手性药物的拆分方法— 1、结晶拆分法 --直接结晶法---在光学活性溶剂中的结晶拆分 --直接结晶法---外消旋体的不对称转化和结晶拆分 --直接结晶法---逆向结晶法逆向结晶法则是在外消旋体的饱和溶液中加入可溶性某一种构型的异构体[如(R)—异构体],添加的(R)—异构体就会吸附到外消旋体溶液中的同种构型异构体结晶体的表面,从而抑制了这种异构体结晶的继续生长,而外消旋体溶液中相反构型的(S)—异构体结晶速度就会加快,从而形成结晶析出。 --直接结晶法---优先结晶法优先结晶方法(preferential crystallization)是在饱和或过饱和的外消旋体溶液中加入一个对映异构体的晶种,使该对映异构体稍稍过量因而造成不对称环境,结晶就会按非稍的过程进行,这样旋光性与该晶种相同的异构体就会从溶液中结晶出来。 --直接结晶法---自发结晶拆分法自发结晶拆分(spontaneous resolution)是指当外消旋体在结晶的过程中,自发的形成聚集体。 --通过形成非对映异构体的结晶法--非对映异构体的形成和拆分原理 --通过形成非对映异构体的结晶法--用于碱拆分的拆分试剂(酸性拆分剂)
2、动力学拆分 --组合拆分拆分原理是采用一组同一结构类型的手性衍生物的拆分剂家族(resolving agent family)代替单一的手性拆分剂进行外消旋化合物的拆分。 --复合拆分方法---形成π电子复合物的拆分(通过形成π电子复合物或π电子转移复合物的拆分方法主要应用十含芳香环化合物的拆分,所用拆分剂是手性的含π电子的酸) --复合拆分方法---金属配合物的拆分方法:有机过渡金属化合物与被拆分物形成非对映异构体的配位物而被分离。 --包合拆分(inclusion resolution)方法--洞穴包合物拆分(拆分剂是手性的环状多元醚(冠醚)和环糊精) 3、色谱分离:气相色谱,液相色谱,薄层色谱、超临界色谱和电泳 -------气相色谱: 按照拆分机制 GC 手性固定相可分为三类:基于氢键的手性固定相;基于配位作用的手性金属配合物固定相;基于包含作用的环糊精衍生物固定相。 -----HPLC柱色谱法分离手性化合物: 直接法:手性固定相CSP拆分:手性流动相CMP拆分 间接法:手性试剂衍生化法CDF 直接法间接法 手性固定相拆分CSP 手性流动相拆分CMP 手性试剂衍生化法 CDF 定义将具有手性识别 作用的配基,通 过稳定的共价键 连接或以物理方 法涂敷于适当的 固相载体上,以 制备出手性固定 相。CMP手性流动相又称手 性添加剂法,这种拆分 法是在流动相中加入 手性试剂,利用手性试 剂与各对映体结合的 稳定常数不同,以及药 物与结合物在固定相 上分配系数的不同来 进行分离。有:配体交 换型手性添加剂、环糊 精添加剂、手性离子对 添加剂。 该法是药物对映体在 分离前与高光学纯度 衍生化试剂( C D A) 反应,形成非对映体, 再进行色谱分离测定。 优点分离时间短, 而手性选择性 和拆分能力此法不需昂贵的手性 柱,亦无须进行柱前衍 生,手性添加剂可视要 可使用已有的非 手性同定相,花费少, 通过选用具有强烈紫