
非肝硬化性门脉高压诊断要点
门静脉高压常见原因是肝硬化,占门静脉高压的80%以上。但目前临床上非肝硬化性门静脉高压日益受到重视,并且,部分此类患者通过适当的治疗,预后较好,因此,有必要提高对该类患者的诊断水平,以减少误诊。
门静脉是肠系膜上静脉和脾静脉汇合而成。肝脏的血供2/3来自门静脉,1/3来自肝动脉,肝脏氧供72%由门静脉提供。门静脉压力通常与血流量(Q)和阻力(R)成正比。正常门静脉血流量为1000~1200ml/min,门静脉压力(PVP)是5~l0mmHg(7~14cmH20)。当PVP≥25mmHg(30cIn H20);肝静脉楔压(WHVP)或PVP高于下腔静脉压(lVC)5mmHg:脾内压≥15lnmHg时,称为门静脉高压。门静脉高压时,肝静脉和门静脉压的梯度增大,由于门静脉内无静脉瓣,当肝窦后压力高于门静脉高压时,血流由向肝性转为离肝性。
此外,肝静脉压力梯度(HVPG)=WHVP—游离肝静脉压(FHVP),正常人在5~6mmHg;尽管临床很少测定HVPG,但其对门静脉高压分类很有意义。
一、发病机理:有关门静脉高压产生的学说很多,最经典的学说主要有前向与后向学说:
1、前向学说(Forward fIow theory)
机体处于高动力循环状态,表观为:全身血管阻力降低:平均动脉压(MAP)降低:血浆容量增加:内脏血流增加;心输出量增加。
导致产生高动力循环状态的原因有:循环中胆酸.胰高糖素、降钙素基因相关肽(CRGP)等扩血管物质增加;血管内皮产生一氧化氮(N0)、前列腺素I2(PG I2)等扩血管物质增加;血管对缩血管物质如去甲肾上腺素等反应性降低。
2、后向学说(Backward fIow theory)
主要因为门静脉系统阻力增加,又因引起血管阻力增加的部位不同将其分为以下三种形式:
①肝前性因门静脉阻塞所致。②肝后性因肝静脉阻塞所致。③肝内性为多因素,最常见有 a.解剖因素如:纤维化、结节形成、肝窦毛细血管化;b.功能因素如:星状细胞(HSC)活化,局部N0合成减低,内皮素—1(ET1)增加等。
二、门脉高压的分类及病因
1、肝前性门脉高压的病因
①肝内血流增加、动一静脉瘘;脾大(非肝脏原因);
②门静脉或脾静脉血栓形成或堵塞。
2、肝内性门脉高压的病因
①急性见于:急性酒精性肝炎/脂肪肝、急性肝衰竭等。
②慢性见于:病毒性,酒精性,砷、氯乙烯、铜盐中毒所致的肝病AIH/PBC/PSC,Wilson病/血色病/α1一抗胰蛋白酶(α1一AT)缺乏,胰腺囊性纤维化,特发性门脉高压,
先天性肝纤维化,血吸虫病(窦前性),结节病,淀粉样病,肝转移癌。
3、肝后性门脉高压的病因
①下腔静脉/肝静脉/肝小静脉的病变:肝静脉血栓形成、下腔静脉血栓形成/蹼性病变、肝窦阻塞综合征(SOS)等。
②心脏疾病如:心肌病、心瓣膜病、缩窄性心包炎等。
三、不同类型门静脉高压性疾病的减少
(一)肝(窦)前性门静脉高压
1、先天性肝纤维化
先天性肝纤传性维化是一组少见的常染色体隐性遗传性疾病,临床以门脉高压和肝功能正常为特点,多合并常染色体隐性遗传性多囊肾或肝内、外胆管发育异常。临床表现差异明显,可表现为门静脉高压及其并发症、复发性胆管炎,或终生无症状尸检偶然发现。
发病年龄依门静脉高压程度及有无合并肾脏疾病成人均可发病,而以10岁以下居多。
根据不同临床表现分为四种类型:门静脉高压型、胆管炎型、门脉高压合并胆管炎型和无症状型。综合国内先天性肝纤维表现为消化道出血的约占44、4%,胆管炎型表现为间断性发热、腹痛、腹胀的约占30.6%,合并型的约占8.3%,与国外文献报道基本一致。
本病区别于常见结节性肝硬化的特点在于:儿童或青少年多见;门静脉高压凸显,表现为肝脾肿大、脾功能亢进,30~70%有消化道出血;肝功能储备良好,少数病例可出现碱性磷酸酶和丙氨酸转氨酶轻度增高,腹水少见,肝性脑病罕见。但是,肝细胞对动脉低血压(缺血、缺氧)敏感,故反复大出血可诱导肝硬化发生,此阶段的临床表现同结节性肝硬化。
此外,先天性肝纤维化常合并其他器官发育异常,特别是婴儿期多囊肾(现统一命名为常染色体隐性遗传性多囊肾)、先天性肝内胆管囊状扩张症或交通性海绵状胆管扩张症(Carolis病),因它们在发病机制、临床表现的共同特征,有学者认为三者属同源疾病。
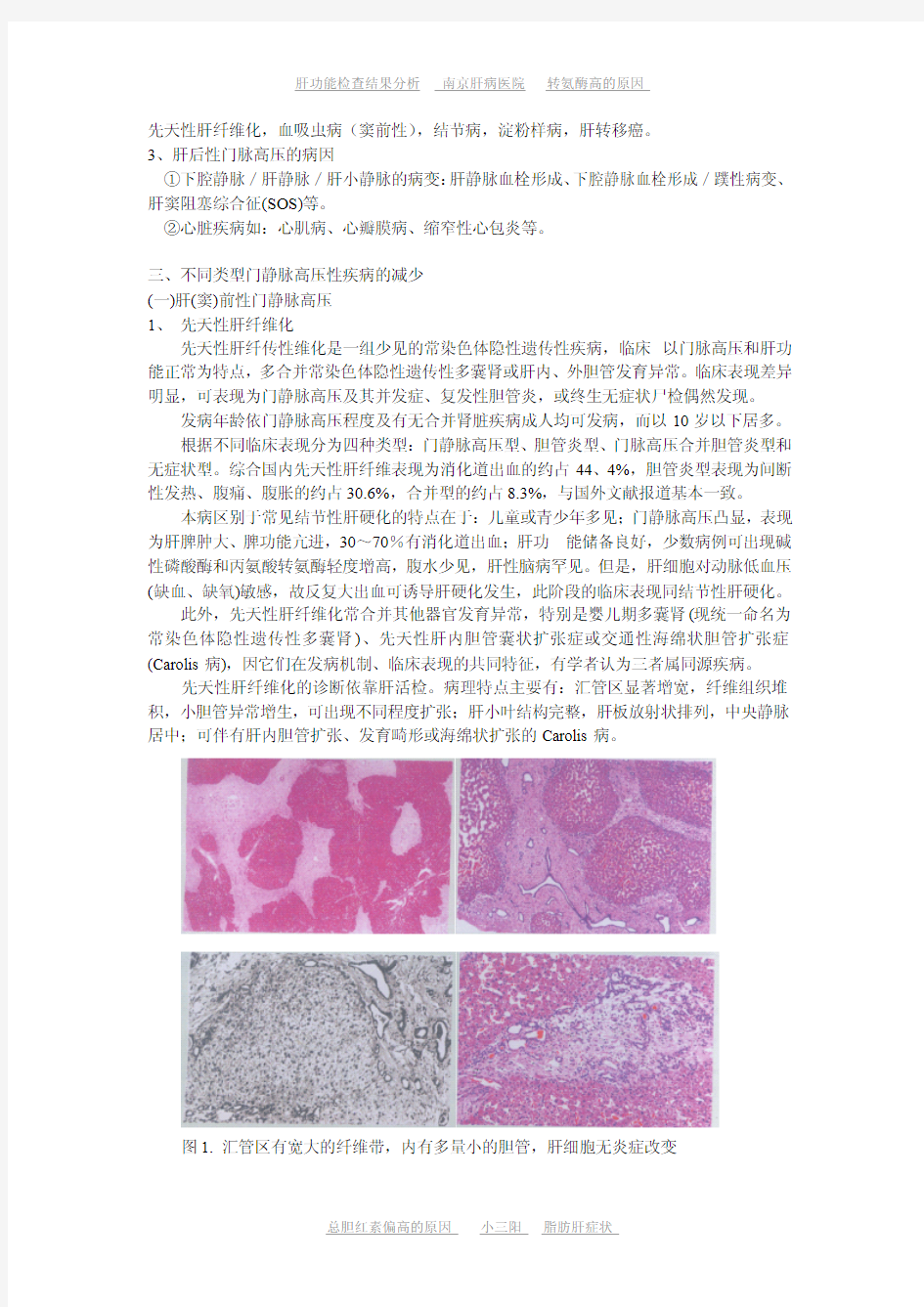
先天性肝纤维化的诊断依靠肝活检。病理特点主要有:汇管区显著增宽,纤维组织堆积,小胆管异常增生,可出现不同程度扩张;肝小叶结构完整,肝板放射状排列,中央静脉居中;可伴有肝内胆管扩张、发育畸形或海绵状扩张的Carolis病。
图1.汇管区有宽大的纤维带,内有多量小的胆管,肝细胞无炎症改变
治疗主要为对症治疗。如能有效控制先天性肝纤维化患者的门静脉高压和感染,通常预后良好。对于已有肝硬化及出现肝衰竭时,原位肝移植是另一有效治疗途径。同时存在肾脏疾病者,必要时可选择肝肾联合移植。
2、特发性门脉高压(IPH)
特发性门静脉高压症(Idiopathic portal hypertension IPH)是由于门静脉主干或分支非特异性炎症引起血管闭塞性纤维化及硬化,临床表理妻鐾大、贫血、门脉高压的一组综合征,除外肝硬化、血液疾病、肝胆系统黪寄生虫病、肝静脉及门静脉阻塞以及先天性肝纤维化等。以日本(34、1%)和印度(25%)高发,在我国较少见,与其他原因所致的肝硬化门脉高压的临床表现相似,容易误诊、漏诊。
对于IPH的命名在不同时期及地区又有不同,l962年印度学者称之为非硬化性门静脉纤维化(NCPF),英国也沿用这一名称;l965年美国称之为肝内门静脉硬化症(HPS),而在日本则称为IPH。IPH病因不明,毒物(砷、铜、氯乙烯原料、6一巯基嘌呤、硫唑嘌呤等免疫抑制剂)、腹腔内感染引起门静脉炎症等均可导致IPH的发生;免疫因素可能在其发病中起重要作用,IPH常与自身免疫现象或自身免疫疾病同时存在。
IPH主要临床表现:脾肿大,贫血,胃、食道静脉曲张,消化道出血,腹水;肝功能正常或轻度异常。肝活检病理组织学改变主要有:汇管区纤维化、硬化,门静脉小支狭窄、闭塞,门静脉分支扩张,门静脉血栓形成,肝实质内纤维化,肝细胞萎缩及肝结节状再生等,均无肝硬化改变。肝门处门静脉可有增厚、狭窄,门脉造影显示门静脉末梢狭窄和稀少。
图3.门静脉壁增厚、狭窄,肝内门静脉硬化或闭锁
由于IPH是由门静脉小分支闭塞等原发病变和血流动力学改变及微循环障碍所引起继
发性病变共同组成,所以不同病例和同一病例的不同区域病变可不相同。在病理诊断中要注意以下几点:①虽然本病具有一定的形态学特点,但是并非特异性改变。所以,结合临床资料,全面分析病变,是十分必要的。②由于肝穿刺标本取材的局限性和IPH病变的不均匀性,要作出正确的病理诊断,标本达到一定量是不可缺少的前提,且标本内必须含足够的汇管区(肝穿刺标本长度至少要2cm以上,最好含11个以上完整的汇管区)。③注意本病与肝硬化的鉴别。首先,不要将被膜下浅层的少数结节,误诊为肝硬化,要注意观察深层改变。其次,不要将肝结节性增生误诊为肝硬化。IPH增生的结节周围是网状塌陷,而不是纤维间隔,这是最主要的鉴别点。
目前IPH尚无统一诊断标准。较多见的诊断建议有以下2种:
(1)Hillaire等的诊断标准,即①有门静脉高压症的表现,如食道静脉曲张,脾功能亢进,腹水或肝静脉压逐步升高;②多普勒超声提示典型的肝静脉和门静脉表现;③肝活检提示没有肝硬化;④排除已知的导致肝硬化的疾病,如慢性病毒性肝炎,酒精性肝病,非酒精性脂肪性肝病,肥胖,血吸虫病,自生免疫性肝炎,或Willson病;⑤排除慢性维生素A摄取异常,职业性接触有毒物质。
(2)日本IPH研究委员会制订的诊断要点:①不明原因的脾大、贫血、脉高压,可除外肝硬化、血液疾病、肝胆系统的寄生虫病、肝静脉及脉阻塞以及肝纤维化等,也就是说,IPH 的临床诊断可通过排除以上相病而确立;②1种以上血液成分减少;③肝功能正常或接近正常;④内X线证实有上消化道静脉曲张;⑤超声、CT或脾脏同位素检查示肝表非肝硬化表现,脾肿大;⑥肝静脉楔压(WHVP)正常或轻度升高,脉压>20mmHg;⑦肝活检显示门静脉纤维化,但无肝硬化。并非必须具备以上每一条标准才能诊断,但是必须确有门静脉高压并且可绝对排除肝硬化和其他原因引起的非肝硬化性门静脉高压才可诊断。
治疗及预后:没有特殊的治疗方法,主要是治疗出血、脾亢等。一般不发生肝硬化,50%患者从有临床表现开始生存期达25年,预后良好。
3、骨髓增生性疾病
骨髓增生性疾病(MLD)包括原发性骨髓纤维化(PMF)、真性红细胞增多症、原发性血小板增多症和慢性粒细胞白血病,常引起门静脉高压。约有3%—12%的门静脉血栓形成(PVT)患者为显性MLD,还有一部分不明原因的PVT患者有潜在的MLD。
PMF是一种造血干细胞克隆性增殖所致的骨髓增殖性肿瘤,表现为不同程度的血细胞减少和/或细胞增多、外周血出现幼红、幼粒细胞、骨髓维化和髓外造血(诊断标准见答疑解难)。约有l7%~25%的骨纤维化患者合并门静脉高压。其产生原因:一是脾脏的髓外造血,导致脾静脉血流量增加,形成高动力循环;其二是形成门静脉或脾静脉血栓。PMF合并门静脉高压常有以下特点:①肝功能基本正常,即使有腹水,患者白蛋白仍正常;②外周血象表现可为白细胞及血小板增高(脾大伴有白细胞及血小板增高是骨髓纤维化与肝硬化脾功能亢进的重要鉴别要点),血红蛋白降低,可见幼稚细胞;③骨髓穿刺及活检有干抽、纤维化及泪滴状细胞。值得注意的是:约有20%的骨髓纤维化可合并肝硬化,而肝炎后肝硬化又可合并骨髓纤维化。这两者与单纯性骨髓纤维化引起门静脉高压的鉴别点主要依靠肝组织病理学、骨髓组织病理学的检查。脾穿刺可发现髓样化生,可见到各阶段的粒细胞、有核红细胞、巨核细胞以及正常的脾淋巴细胞,这也利于鉴别。另外,前两者都会出现肝功能损害的表现也是最基本的临床鉴别指标。
处于纤维化前状态的PMF患者和无症状的纤维化PMF患者生存期较长,所以,治疗大多针对有症状者。目前,PMF的治疗多是姑息的,通常所用药物并不直接针对细胞学和遗传学的根本病因。虽然骨髓纤维化门静脉高压患者有脾大,但不到万不得己临床不选择脾切除,因为脾脏是代偿性造血器官。此外,虽然切脾可以不同程度的改善其门静脉高压、贫
血、血小板减少,可围手术期有25%患者出现出血和血栓,6.7%的患者死亡。脾切除的长期并发症主要包括:白细胞增多、血小板增多和肝肿大加速(可通过术后药物治疗控制)。因此,建议选择安全的对症治疗,如:消化道出血可行曲张静脉内镜下止血、介入治疗或断流术。早期骨髓纤维化可进行化疗,化疗的目的在于纠正白细胞减少、阻止脾脏肿大或减少髓外造血器官的体积,但不能改变PMF的自然病程。故此,一旦有门静脉高压后其化疗的意义不大。异基因干细胞移植是目前唯一具有潜在治愈PMF能力的治疗手段。由于移植本身的高风险,因此,要严格参照其分期及预后(见答疑解难)选择异基因干细胞移植治疗病例。
除PMF外,慢性粒细胞性白血病、真性红细胞增多症、海蓝组织细胞增多症、系统性肥大细胞增多症都可以引起门静脉高压。
(二)肝内(窦性)门脉高压
1、淀粉样变
淀粉样变性(amyloidosis),是淀粉样物质在血管壁及器官、组织细胞外沉积为特征的一种进行性、预后不良性疾病。病变可以局限于一个器官,也可能周身性使多器官、多系统受累。主要侵犯心,肾、肝、脾、胃肠、神经系统、肌肉和皮肤等组织器官。侵及肝脏时,称之为肝淀粉样变性。临床上无特异性症状和体征,其症状决定于原有疾病及淀粉样物质沉积的部位、沉积量以及所受累的器官和系统,继发性、全身性淀粉样变性多数有肝脏受累,常表现为肝大、上腹胀满、纳差,少数可表现为严重肝大(肝重量可达7kg以上)。
图4.刚果红染色可见肝组织中大量红色淀粉样物质沉积
化验检查有ALP、GGT升高,可有轻中度黄疸,转氨酶多正常。淀粉样变性常有凝血障碍,以凝血酶原时间延长为主。
放射性核素硫胶体锝肝扫描可见肝脏对放射性摄取均匀一致地轻度减低,对肝淀粉样变性有辅助诊断价值,并能动态观察疾病的进展及治疗效果。超声显像可见肝内不规则致密回声光团,但无特异性。CT成像显示肝脏密度减低。
活体组织检查是诊断全身性淀粉样变性最主要和最可靠的手段。腹部皮下脂肪组织活检阳性率最高(AL型95%,AA型66%),并且安全易行;直肠活检阳性率占85%;齿龈活检阳性率约为50%。
全身性淀粉样变性患者50%以上肝脏受侵犯,但由此而引起的临床肝病却不常见。对于肝脏明显肿大的淀粉样变性患者由于肝包膜紧张,肝穿刺有引发肝脏破裂或致死性肝出血的危险。因此,对己确诊的全身性淀粉样变性患者,很少有必要进行肝活检来证实肝脏的淀粉样浸润。必要时可在腹腔镜直视下谨慎进行肝活检。
鉴别诊断重点疾病是:原发性胆汁性肝硬化,原发性硬化胆管炎,肝硬化。
目前尚无特异治疗方法。其治疗的目的是防止淀粉样物质的进一步沉积,促进或加速
淀粉样物质的吸收。原发性淀粉样变性治疗常用治疗方案是苯丙氨酸氮芥+泼尼松(MP)方案;继发性淀粉样变性治疗在于控制基础疾病,如:慢性骨髓炎、结核病、类风湿性关节炎等,基本病因的控制淀粉样变性可停止发展甚至消退;对症治疗,如控制继发感染,有效治疗心、肾功能衰竭等。慎用洋地黄;必要时可考虑肾移植。
淀粉样变性患者的预后取决于病因和肾脏受侵犯的程度。中数生存期1年左右,5年生存率约13%,10年生存率仅为1%。血清胆红素增高(>25μmol/L)的患者预后不良,通常在5个月内死亡。常见的死亡原因为继发感染和心、肾功能衰竭。
2、WiIson病
该病在19期《肝病快讯》中做过专题介绍,在此不再赘述。仅提醒容易发生的误诊如下:
(1)急性一一与其他原因急性肝衰竭鉴别,鉴别晕点:胆红素↑,尿铜↑,AKP↓,血清铜蓝蛋白↓,急性溶血,肾功能不全,角膜可见K—F环。此时治疗主要依靠血液滤过、肝移植。
(2)慢性一一与原因不明肝硬化门静脉高压鉴别,鉴别重点:24尿铜↑,血清铜蓝蛋白↓,角膜可见K—F环。此时治疗的重点是驱铜。
图5.角膜K—F环
3、血色病:
血色病为一种罕见的先天性代谢缺陷病,由于过多的铁质沉着在脏器组织所致,引起不同程度的基质细胞破坏、纤维组织增生及脏器功能障碍,临床表现有肝硬化、糖尿病、皮肤色素沉着、内分泌紊乱、心脏和关节病变。
只有当血色病患者体内铁贮积量达25~50g时才出现临床症状,故出现症状的平均年龄为50岁,由于血色病所致的早期临床表现往往被忽视,通常拖延4~5年后才能确立诊断。本病男性多见,且发病年龄较女性早。血色病肝脏肿大的发生先于肝硬化,其肿大程度与铁质沉积程度有关,血色病非肝硬化患者69%有肝肿大,肝硬化者中90%肝肿大,提示铁沉积本身对肝脏病变起主要作用。肝硬化形成后,多出现肝功能不全和门静脉高压及肝硬化其他非特异性表现(性欲减退、闭经、男性乳房发育)。在肝硬化基础上易发生肝癌,血色病肝硬化的癌发生率高于正常人的200倍,主要是原发性肝细胞癌,大部分起源于肝内胆管,肝外癌发生率不高。
病理:最突出的病理变化是各脏器实质细胞内有不等量的含铁色素(含铁血黄素、铁蛋白)及非含铁色素(脂褐素和黑色素)的沉着,并伴有纤维化。
肝含铁量常50~100倍于正常肝含铁量的上限,最明显异常是肝细胞内有含铁血黄素颗粒。主要分布在小管周边,晚期胆管上皮细胞,枯否细胞和巨噬细胞都有铁质沉着,非特
异性的变化有脂肪变性和空泡变性。几乎所有有症状患者都存在肝纤维化或肝硬化,纤维间隔宽窄不一,纤维束起源于门静脉周围,然后延伸,包绕一个或数个小时,其形态变化类似慢性胆管部分梗阻。结节内铁质沉积常是在肝细胞内,而不累及纤维组织,提示结节的形成是纤维组织的包绕,而不是存活干细胞的增生所致。
对临床症状明显的患者诊断不难,如患者有①血清铁增高;②转铁蛋白饱和度增高(达50%~60%时高度怀疑;转铁蛋白饱和度=血清铁/转铁蛋白或总铁结合力);③血清铁蛋白增高,应进一步做活检确诊。
本病应早期诊断、早期治疗。因已有肝硬化的血色病患者,预后差,寿命缩短,并发肝癌的机会高;而肝硬化前期的患者,如能及时将贮存的过多铁排尽,则不影响寿命,且不会发生肝癌。
最根本的有效治疗方法是放血疗法,以去除体内过量的铁(每500ml血含铁约250mg)。静脉放血后,患者全身症状减轻,体重增加,皮肤色素沉着和肝、脾肿大减轻。对心力衰竭患者,可注射铁螯合剂,待心脏功能好转后,再用放血疗法。对于肝硬化腹水、门脉高压、糖尿病和心力衰竭、性功能不全者,应对症治疗。
4、αl一抗胰蛋白酶缺乏症
α1—抗胰蛋白酶缺乏症是血中抗蛋白酶成份α1—抗胰蛋白酶(Q1一AT)缺乏引起的一种先天性代谢性疾病,通过常染色体遗传。多见于儿童,成人少见。
临床特点为新生儿肝炎,婴幼儿和成人的肝硬化,肝癌和肺气肿等。在出生后第一周可有胆汁淤积性黄疸、大便不着色、尿色深。体检可发现肝肿大。生化指标有胆汁淤积的指征,2~4个月时黄疸往往消失,在2岁以后可显现肝硬化。
成年期发病多见于杂合子型α1—AT缺乏性肝病患者,病情发展较缓慢,临床表现各异,大多数成人α1—AT缺乏症患者以突出的门脉高压症为首发表现,患者常死于上消化道出血和/或肝性脑病;常可发生肺气肿。有报道成人杂合子型α1一AT缺乏性肝病患者肝功能衰竭的危险性明显增加。此外,男性肝硬化和肝癌的发病率高于女性。由于α1.AT缺乏导致肝硬化患者,肝脏肿瘤发病率很高,以起源于肝细胞者居多,部源于胆管。
诊断α1一抗胰蛋白酶缺乏症可依靠有家族史、新生儿胆汁淤积,同时伴有肺气肿或反复肺部感染,纸上蛋白电泳发现α1.球蛋白缺乏。可作α1一AT含量测定、Pi表型分析来确诊。肝穿刺活组织检查可见肝细胞充满大小不等球形红色包涵体,PAS染色呈阳性反应;可同时伴有胆汁淤积和肝纤维化病变。
图8.门静脉周围的肝细胞内可见鲜红色的耐淀粉酶的包涵体(高倍镜下)
治疗:目前尚无特效疗法,较有前途的治疗方法是:①肝脏移植对肝损害严重者应行肝移植。由于肝是合成α1一抗胰蛋白酶的惟一场所,因此肝移植不仅能治愈肝病,且能纠正α1一抗胰蛋白酶缺乏。现认为肝移植是治疗Pizz终末期肝硬化的有效方法,应用PiMM 表型的供者肝脏做肝移植,可望提高其存活率及改善病情;②利用遗传工程的方法对患者植入Z基因,以使其产生α1一AT;③基因重组。当然,更好的办法是避免α1一AT缺乏症的发生。父母为Pizz杂合子,其子女有可能出现Pizz表型,在15~17周胎龄时,直接取胎儿脐血作Pizz表型分析,对具有发病危险的胎儿终止妊娠有肯定的价值。
(三)肝后(窦后)性门脉高压
1、Budd-Chiari综合征
巴德一基里亚综合征(Budd-Chiari syndrome,BCS),即肝静脉或下腔静脉肝段阻塞,是临床并不少见的疾病。主要表现为明显肝大、腹痛、腹水,可有轻度黄疸。慢性梗阻者因侧枝循环形成,腹水可不明显。确定诊断主要靠B超(US)、CT、MRI及造影(血管狭窄+扩张才能够诊断)。
依血管受累多少、受累程度和阻塞病变的性质和状态等殊不相同,BCS可分为笔性型、亚急性型和慢性型。在此简要介绍急性型:
急性肝静脉系统血栓形成
约有60%以上的肝静脉血栓形成病例与易栓疾病有关;50%以上有原发性骨髓增殖性疾病;口服避孕药和妊娠常常是促发因素。
临床表现:可有静脉炎综合征表现,如肝窦压力增高、肝窦血液灌注减少,腹痛、发热,肝大且痛,急性门静脉高压,大量腹水。易误为急腹症。可伴功能性肾衰,偶有脑病和肝衰竭,转氨酶升高5倍以上,通常高于20倍,凝血因子水平显著降低,低于50%正常值,通常低于30%正常值,胆红素几天后升高,可因基础血液病或肾衰竭而极度升高。可并发弥漫性血管内凝血(DIC)、多器官功能衰竭(MOSF)、白发性细菌性腹膜炎(SBF)等,多数在数日或数周内可以因循环衰竭(休克)、肝功能衰竭或消化道出血而迅速死亡。腹水、肝肿大和迅速出现的MOSF,是本病的突出表现。
诊断和治疗要点:患者出现急性肝衰竭、肝大、腹水临床表现,超声多普勒、MRI显
像的特征性改变有利于确定诊断。由于CT增强、肝静脉造影等应用的造影剂有损害肾功能导致造影剂肾病的危险,故应避免。而肝活检虽有一定诊断价值,但有引起大出血的风险,故需谨慎使用。
治疗:肝素抗凝、放腹水、扩容、抗感染;局部溶栓及介入治疗;TIPS;肝移植。2、肝窦阻塞综合征(SOS)
本病最初被Bras命名为肝小静脉阻塞性疾病(VOD)。但随后的深入研究发现中央静脉等小静脉阻塞性病变并非VOD的必有表现,进一步的实验研究证明本病发生最早、最为根本性的病理改变是肝窦流出道阻塞而非小静脉阻塞,因此,Deleve等建议将本病更名为肝窦阻塞综合征(SOS),现己被该研究领域的学者普遍认同并采用。
摄入吡咯双烷类生物碱(pyrrolizidine)与骨髓移植是我国引起SOS的两大常见原因,前者存在于土三七、千里光等多种植物药中,对哺乳类动物有肝毒性,而土三七为我国民间常用“伤科药”,故可因外伤等原因过量服用致SOS;骨髓移植后发生SOS与移植预处理方案的大剂量放、化疗损伤肝窦内皮细胞等有关。目前认为肝窦内皮细胞损害所致的肝窦流出道阻塞,进而产生肝内窦性急性门脉高压症是本病的主要发病机制,肝细胞由于淤血、缺氧而发生变性、坏死,造成肝功能损害。中央静脉等小静脉的内皮细胞也可受累而致管壁水肿、纤维化等病变而参与门脉高压(窦后性)的形成与发展。因此,SOS在本质上属于肝微循环障碍性疾病,肝实质细胞的损害主要是继发性改变,此与临床常见的药物性肝炎不同,其原因可能与肝窦内皮细胞较肝实质细胞对前面所述的致SOS物质更为敏感有关。
SOS的临床表现以突出的门脉高压症为特点,急性期的临床表现为依次出现右上腹疼痛、腹胀与黄疸;体征主要肿大伴有触痛、腹水征等。SOS患者的腹水一般为门脉高压,但可继发感染而形成混合性腹水,也可因腹膜小血管自发或穿刺损伤而出现血性腹水。与病毒性肝炎等肝实质疾比,SOS的肝功能损害程度较轻,但继发于骨髓移植者肝损为严重,可能同时存在免疫因素等其他发病机制。与肝硬化和酒精性肝病相类似,本病的转氨酶升高以AST为著,可能与细胞功能不全等有关。其CAl25水平也显著升高,具体机制未明,是否具有临床诊断价值亦有待进一步研究。
SOS患者的超声声像图特点反映了肝内窦(后)性门脉所致的形态学变化与血流动力学改变。Budd—Chiari综合征源性肝淤血等所致的肝后性门脉高压症也常伴有肝肿大,但其3支肝静脉内径均明显扩张。SOS的肝静脉内径变细是肝窦道阻塞的继发性改变,其内膜光滑,管腔通畅,此与肝静窄不同。另外,SOS的肝窦、小静脉病变在肝内分布不尽均匀,因此组织淤血、坏死区可呈补丁状分布,在超声图像上表肝内回声强弱不均匀,易误诊为不均匀脂肪肝、血管瘤甚癌等,应引起重视。MRI在门脉期与延迟期可清楚显示造影阻于门静脉分支末端区肝实质内而未能进入肝叶、段静脉,此影像学表现非常形象地说明了SOS 的病理生理学改变特点,诊断价值。
门脉期见门脉分支末端区肝实质呈不均匀片状强化
图11.SOS患者的肝脏MRI表现
经皮肝穿刺活检仅有部分本病患者存在“小静脉壁增厚及官腔狭窄”等SOS典型病变,其说明肝穿活检对本病的诊断价值有限。出现假阴性结果的可能原因有:①中央静脉等小静脉病变并非SOS的基本病理改变,而光镜下无法观察到肝窦内皮细胞损害致肝窦流出道阻塞的直接征象;②由于SOS的病变分布可呈补丁状,故盲目的经皮肝穿刺活检发现病灶的机会较小。
图12.SOS患者的肝穿刺病理活检:肝窦扩张、淤血,组织条边缘见汇管区静脉壁增厚伴纤维组织增生,管腔狭窄。
图13.SOS患者的肝穿刺病理活检:肝窦扩张、淤血,但中央静脉管腔通畅,管壁无增厚
基于对SOS病理生理改变认识的进展以及经皮肝穿刺活检的局限性,肝内小静脉阻塞的组织学证据已不再是确诊SOS的必备条件。目前临床诊断SOS常用Seattle标准或BaItifnore标准,分别由2个骨髓移植小组于1984年和1987年制订后沿用,它们的准确性分别达89%和95%,显然后者准确性更高。SOS与病毒性肝炎等肝细胞实质性疾病的鉴别点主要是肝功能损害较轻而门脉高压症突出;腹水征呈急剧性、进行性且伴疼痛性肝肿大可与肝硬化腹水相鉴别;超声与MRI有助于本病的诊断与鉴别诊断。病理活检对SOS的诊断价值在于:如能发现肝小静脉壁增厚、纤维化、管腔狭窄甚至闭塞之典型表现,可以确诊为SOS;如仅见肝窦扩张、淤血等但无小静脉改变,则须在结合影像学检查排除心、大血管病变引起的肝淤血后,方可确诊。
预后及治疗:SOS病死率较高,目前尚缺乏特效的内科治疗方法。除积极支持对症处理外,早期诊断并及时给予肝素溶栓治疗对1/3病人有效;但是,此疗法容易引起致命性中枢神经系统出血,并且仅适合于肾、肺功能正常者。去纤苷(Defibrotide)可使轻、中度患者中35%~55%获得完全缓解;对重度无效;应用预防骨髓移植者的SOS发生效果较好。经颈静肝内门体静脉分流术(TIPS)可以降低门脉压力消除腹水;对胆红素和预后无明显影响。肝移植的临床疗效好,因此,对病情严重危及生命者或经上述治疗无效时可考虑肝移植。
附:骨髓移植后肝窦阻塞综合征(SOS)诊断标准:移植后21天内出现下列3项临床症状中的2项或以上:黄疸(血清胆红素>2mg/d或者34、2μmol/L);肝脏肿大伴肝区疼痛;腹水或者体重增加基础体重的2~5%以上。
四、门静脉高压的诊断思路
1、注意病史采集
任何现代化的辅助检查也无法取代详细的病史采集。既往有无肝硬化/慢性肝炎相关的临床表现;有无消化道出血史以及出血的次数、日期、出血量;以往内镜检查结果;过去史中还要注意:酗酒、输血、乙肝、丙肝、腹腔感染、新生儿感染或其它感染、口服避孕药、骨髓增殖性疾病等。
2、重视体格检查
肝细胞衰竭的征象如:神智状况、全身皮肤黏膜有无淤点溺斑、牙龈有无出血等;腹部检查注意腹壁静脉显露的部位、程度、血流方向,脾脏大小,肝脏大小和质地,有无腹水;下肢有无水肿;直肠检查等。尽可能多的发现对诊断有价值的体征。
3、针对性给予辅助检查
根据对其详细病史采集及周密体检,掌握患者病情特征,给予进行有针对性辅助检查。如:实验室检查:生化、免疫、病毒、血液学;上消化道内镜检查;肝活检病理检查;肝脏影像学:肝静脉造影、选择性内脏动脉造影、US/CT/MRI。并且要给辅助科室提供较为详细的临床资料,注意与检验、病理、影像学等科室大夫沟通,这样才能够使得更多的原因不明的门静脉高压患者得到明确诊断。
4、门脉高压的常见原因
(1)肝(窦)前性一脾大、肝功受损不明显多见于:门脉/脾静脉血栓形成/海绵状变性;特发性门脉高压;先天性肝纤维化。
(2)肝(窦)内性一肝功受损明显多见于:各种肝硬化(病毒及非病毒)。
(3)肝(窦)后性一肝大、肝功受损明显多见于:Budd—Chiari综合征;肝静脉系统血栓形成;肝小静脉阻塞性疾病(VOD)。
5、门脉高压伴明显肝功异常者
(1)胆系疾病:如胆道闭锁、家族性淤胆综合征、硬化性胆管炎、特发性新生儿肝炎、长期静脉营养所致的肝硬化。
(2)肝实质疾病:如Wilson病/α1一AT缺乏、自身免疫性肝炎、病毒性肝炎、囊性纤维化、围生期血色病/铁累积性疾病。
(3)肝静脉流出道梗阻:如Budd—Chiari综合征、VOD。
6、门脉高压无明显肝功异常者
(1)先天性肝纤维化;
(2)门静脉梗阻:门脉海绵状变性、门脉先天性异常;
(3)小血管发育异常(Small vessel angiodysplasia,Klatskin’s disease);
(4)脾血管异常。
门静脉高压性脾脏切除的是是非非 作者:王宇, WANG Yu 作者单位:100050,北京市,首都医科大学附属北京友谊医院普通外科 刊名: 中华肝胆外科杂志 英文刊名:CHINESE JOURNAL OF HEPATOBILIARY SURGERY 年,卷(期):2006,12(9) 被引用次数:4次 本文读者也读过(10条) 1.张忠涛.王宇胰腺损伤[期刊论文]-腹部外科2002,15(2) 2.周孝思.张同琳合并肝内胆管结石的胆总管结石是EST的适应证还是禁忌证?[期刊论文]-中国微创外科杂志2007,7(2) 3.王宇门静脉高压症的外科治疗[期刊论文]-中华外科杂志2005,43(19) 4.韩威.李建设.张忠涛.王宇胰腺实性-假乳头状瘤的诊断治疗[期刊论文]-中国医学科学院学报2006,28(4) 5.朱立元.尹耀新急性胰腺炎的治疗[期刊论文]-肝胆外科杂志2001,9(3) 6.姜洪池.陆朝阳巨脾切除的有关技术问题[会议论文]-2005 7.LIU Jun.GONG Hao.ZHANG Zhong-tao.WANG Yu Effect of angiotensin Ⅱ and angiotensin Ⅱ type 1 receptor antagonist on the proliferation,contraction and collagen synthesis in rat hepatic stellate cells[期刊论文]-中华医学杂志(英文版)2008,121(2) 8.王宇.贾继东.WANG Yu.JIA Ji-dong肝肾综合征的发生机制和治疗进展[期刊论文]-肝脏2006,11(1) 9.张忠涛.王宇门体分流手术治疗门静脉高压症[期刊论文]-中国医刊2004,39(2) 10.张忠涛门体分流手术治疗门静脉高压症的历史与现状[期刊论文]-临床外科杂志2004,12(7) 引证文献(4条) 1.阿依甫汗·阿汗.张日新.张金辉.赵晋明.曹峻.邰沁文.季学文.温浩脾大部切除术与脾完全切除术比较治疗肝硬化门脉高压症的系统评价[期刊论文]-中国循证医学杂志 2009(6) 2.潘平生.祝强华.陈丽萍.曹宏勇.彭丽娟PSE联合TACE治疗原发性肝癌伴脾功能亢的临床研究[期刊论文]-中国医学创新 2009(32) 3.沈贵生.朱家胜.朱国民.史有龙.汪天平保脾手术对晚期血吸虫病肝纤维化及相关细胞因子的影响[期刊论文]-中国血吸虫病防治杂志 2009(6) 4.朱俊军.杨业发.张遂亮.潘春华部分脾动脉栓塞术治疗脾功能亢进致血小板减少的疗效观察[期刊论文]-实用医学影像杂志 2008(1) 本文链接:https://www.doczj.com/doc/2814925915.html,/Periodical_zhgdwk200609002.aspx
非肝硬化性门脉高压诊断要点 门静脉高压常见原因是肝硬化,占门静脉高压的80%以上。但目前临床上非肝硬化性门静脉高压日益受到重视,并且,部分此类患者通过适当的治疗,预后较好,因此,有必要提高对该类患者的诊断水平,以减少误诊。 门静脉是肠系膜上静脉和脾静脉汇合而成。肝脏的血供2/3来自门静脉,1/3来自肝动脉,肝脏氧供72%由门静脉提供。门静脉压力通常与血流量(Q)和阻力(R)成正比。正常门静脉血流量为1000~1200ml/min,门静脉压力(PVP)是5~l0mmHg(7~14cmH20)。当PVP≥25mmHg(30cIn H20);肝静脉楔压(WHVP)或PVP高于下腔静脉压(lVC)5mmHg:脾内压≥15lnmHg时,称为门静脉高压。门静脉高压时,肝静脉和门静脉压的梯度增大,由于门静脉内无静脉瓣,当肝窦后压力高于门静脉高压时,血流由向肝性转为离肝性。 此外,肝静脉压力梯度(HVPG)=WHVP—游离肝静脉压(FHVP),正常人在5~6mmHg;尽管临床很少测定HVPG,但其对门静脉高压分类很有意义。 一、发病机理:有关门静脉高压产生的学说很多,最经典的学说主要有前向与后向学说: 1、前向学说(Forward fIow theory) 机体处于高动力循环状态,表观为:全身血管阻力降低:平均动脉压(MAP)降低:血浆容量增加:内脏血流增加;心输出量增加。 导致产生高动力循环状态的原因有:循环中胆酸.胰高糖素、降钙素基因相关肽(CRGP)等扩血管物质增加;血管内皮产生一氧化氮(N0)、前列腺素I2(PG I2)等扩血管物质增加;血管对缩血管物质如去甲肾上腺素等反应性降低。 2、后向学说(Backward fIow theory) 主要因为门静脉系统阻力增加,又因引起血管阻力增加的部位不同将其分为以下三种形式: ①肝前性因门静脉阻塞所致。②肝后性因肝静脉阻塞所致。③肝内性为多因素,最常见有 a.解剖因素如:纤维化、结节形成、肝窦毛细血管化;b.功能因素如:星状细胞(HSC)活化,局部N0合成减低,内皮素—1(ET1)增加等。 二、门脉高压的分类及病因 1、肝前性门脉高压的病因 ①肝内血流增加、动一静脉瘘;脾大(非肝脏原因); ②门静脉或脾静脉血栓形成或堵塞。 2、肝内性门脉高压的病因 ①急性见于:急性酒精性肝炎/脂肪肝、急性肝衰竭等。 ②慢性见于:病毒性,酒精性,砷、氯乙烯、铜盐中毒所致的肝病AIH/PBC/PSC,Wilson病/血色病/α1一抗胰蛋白酶(α1一AT)缺乏,胰腺囊性纤维化,特发性门脉高压,
2015年10月24日在北京召开的「中华医学会感染病学分会年会、中华医学会肝病学分会年会」上,发布了最新一版的「肝硬化门静脉高压食管胃静脉曲张出血的防治指南」,该指南由中华医学会肝病学分会、消化病学分会、内镜分会联合出台,时隔7年,本指南有不少更新,本文将该指南的变化点及要点进行了总结,以供大家参考学习。 本指南的更新点 1.?食管胃静脉曲张破裂出血(EVB)?的诊断:旧版指南建议48小时内进行胃镜检查,而新版指南更新为12-24小时之内行胃镜检查;旧版认为胃镜是诊断EVB的唯一可靠方法,而新版明确了B超、CT、MRI、肝弹性检测等在EVB诊断方面辅助价值。 2.胃镜检查:旧版建议无静脉曲张的代偿期肝硬化患者每2-3年检查1次胃镜,失代偿期肝硬化患者每年检查1次。新版更新为无静脉曲张的代偿期肝硬化患者每2年检查1次胃镜,失代偿期肝硬化患者0.5-1年检查1次胃镜。 3.急性食管胃底静脉曲张出血的治疗 (1)药物治疗新旧指南均推荐短期应用抗菌药物,旧版推荐使用喹诺酮类抗菌药物,对喹诺酮类耐药者可用头孢类抗菌药物,而新版则相反,首选头孢三代,若过敏,则选择喹诺酮类抗菌药物。 (2)旧版推荐H2RA及PPI用于辅助治疗,新版则仅推荐PPI。 (3)新增内容:麻醉插管或ICU可提高急诊内镜治疗食管胃静脉曲张出血的效果和安全性。 4.食管静脉曲张出血一级预防 (1)旧版主要推荐药物治疗应用非选择性β受体阻滞剂,而新版肯定了卡维地洛在食管静脉曲张出血一级预防方面的作用。 (2)旧版对ACEI/ARB及螺内酯等可降低门脉压力的药物,因缺乏证据未作明确推荐,新版明确指出不推荐ACEI/ARB及螺内酯用于一级预防。 (3)新增如何根据LDRf分型选择?治疗时机?的?内容。 (4)明确规定:不推荐内镜下硬化剂治疗用于一级预防;不推荐各种外科手术和TIPS用于一级预防;不推荐EVL联合非选择性β受体阻滞剂同时用于一级预防。 5.食管静脉曲张出血的二级预防 (1)关于二级预防的时机,旧版推荐既往有食管静脉曲张出血史或急性食管胃静脉曲张出血1周后开始,而新版则将时间改为5天后。 (2)明确规定:肝硬化合并顽固性腹水者,无论一级或二级预防均禁用非选择性β受体阻滞剂。 6.新增特殊类型静脉曲张的处理章节,详见下文。 7.待解决的问题方面,新增了对微生态制剂和新的靶点如血管生成抑制剂、抗氧化剂、环氧化酶抑制剂、他汀类药物等进行了展望。 下面为大家奉上本指南的要点。 概述 门静脉高压症引起的?EVB??是最常见的消化系统急症之一,病死率高,近7年来,国内外有关肝硬化门脉高压EVB均有一定进展,本指南旨在帮助临床医生在肝硬化门静脉高压EVB的诊疗和预防工作中做出合理决策。 证据等级分为A、B、C三个级别,推荐等级分为1、2两个级别(表1、2)。 表 1.推荐意见的证据等级?
第十章病理学 第四节门脉性肝硬化 一、教学目标 1. 掌握门脉性肝硬化的病理变化及临床病理联系。 2. 熟悉门脉性肝硬化的并发症、门脉高压症及腹水的形成机制;肝的结构和生理功能。 3. 了解门脉性肝硬化的流行病学特点、病因、实验室检查、诊断方法及其防治。 二、典型案例(请重点看此部分内容,按照病理教学特点,我参照您给的病例做了修改,如 有不恰当处请指出并修改!) (一)病例1:乙型肝炎后肝硬化(临床诊断能这样命名吗?病理诊断应是门脉性肝硬化) 患者,男,43岁,工人。因吃硬食后感到上腹部不适,呕出暗红色液体(还是鲜红色?)数口,出现面色苍白、精神异常伴意识不清而就诊。6年前患者体检发现乙肝表面抗原阳性,肝功能正常,未系统治疗(还是用未正规治疗?)。近半年来患者自觉乏力,胃口差,有时出现牙龈出血和少量鼻出血。近1个月来常感到腹胀,腹部逐渐隆起,尿量减少,双下肢浮肿逐渐加重。患者否认其他病史及家族史。 入院后进行体格检查,体温(T)37.2℃,脉搏(P)98次/分,呼吸(R)25次/分,血压(BP),10.6/8.0 kPa(80/60 mmHg)。肝病面容,贫血貌,全身皮肤及巩膜黄染,颈部、前胸见多个散在蜘蛛痣,双手见肝掌。心率98次/分,律齐,无杂音,听诊双肺呼吸音清,腹部膨隆,腹壁脐周静脉怒张,肝肋下未触及,脾肋下3cm,腹部柔软,无压痛,移动性浊音(+),双下肢凹陷性水肿,全身淋巴结未触及肿大。查体扑翼样震颤(+),肌张力高,腱反射亢进。 实验室检查,血常规:红细胞(RBC)2.4×1012/L,血红蛋白(HGB)82g/L,白细胞(WBC)3.7×109/L,血小板(PLT)75×109/L,白细胞分类示中性粒细胞0.62,淋巴细胞0.35。肝功能试验:丙氨酸氨基转移酶(ALT)85U/L ,天门冬氨酸氨基转移酶(AST)90U/L,血清白蛋白(A)30g/L,血清球蛋白(G)40g/L,血清总胆红素(STB)45μmol/L,结合胆红素(CB)24μmol/L,非结合胆红素(UCB)21μmol/L;血氨105μmol/L。血浆凝血因子测定:凝血酶原时间(PT)22秒。乙型肝炎病毒标志物检测:HBsAg(+),HBsAb(-),HBeAg(+),HBeAb(-),HBcAb(+)。乙型肝炎病毒DNA测定:HBV-DNA 1.8×105/mL。(HBV-DNA <1.00E+03IU/mL,高灵敏HBV-DNA定量检测:1.03E+6IU/mL。)甲胎蛋白26 μgl/L。B超:肝实质弥漫性损伤、肝被膜增厚,肝脏缩小,表面不光滑,呈结节样改变,肝实质回声增强,粗糙不匀称,门脉直径增宽,脾增大,腹腔积液。 入院后嘱患者卧床休息,止血、输血、补液、利尿、抗病毒药拉米夫定等对症支持治疗。第3天再次呕血,量约900mL,患者面色苍白、脉搏微弱、烦躁、昏迷,血压测不到,各种反射消失,经抢救无效死亡。 【尸体解剖】 全身皮肤及巩膜黄染,口、鼻腔内有少量凝血块,颈部、前胸散在蜘蛛痣10余个,腹壁脐周静脉怒张,腹腔内有淡黄色澄清液体约3000mL,双下肢浮肿。 食管下段静脉曲张明显,下段前壁静脉见一破裂口,周边见暗红色凝血块。胃黏膜淤血、
肝硬化门静脉高压症食管、胃底静脉曲张破裂出血诊治专家共识 为规范肝硬化门静脉高压症食管、胃底曲张静脉破裂出血的诊断与治疗,中华医学会外科学分会门静脉高压症学组特组织有关专家编制本共识,旨在为临床诊断和治疗提供一个基本的规范。 门静脉压力的评估 最常用方法是肝静脉压力梯度(hepatic venous pressure gradient,HVPG),重复性和可信性高,正常范围是3-5 mmHg(1 mmHg=0.133 kPa),≥12 mmHg 是形成静脉曲张和(或)出血的阈值。 食管、胃底静脉曲张(gastroesophagealvarices,GOV)出血及预测 静脉曲张最常见的部位见于食管下段2-5 cm处,且易发生破裂出血。近50%门静脉高压症患者可出现食管、胃底静脉曲张,其程度与肝功能损害的严重程度有关。肝功能Child-Pugh 分级A级患者仅40%有静脉曲张,Child-Pugh C级患者则为85%。肝储备功能分级见表1。
HVPG<12 mmHg 时不会形成静脉曲张;HVPG≥12 mmHg 时,易形成静脉曲张。当HVPG≥20 mmHg时则易发生早期再出血(入院第一周复发出血)或不可控制的大出血,而且1年内病死率较高。未经治疗的患者约60%会发生迟发性再出血,多在上次出血后1-2年内发生。 食管、胃底静脉曲张分级与分型 食管静脉曲张分为轻、中、重3级。 轻度(G1):食管静脉曲张呈直线形或略有迂曲,无红色征。 中度(G2):食管静脉曲张呈直线形或略有迂曲,有红色征或食管静脉曲张呈蛇形迂曲隆起但无红色征。
重度(G3):食管静脉曲张呈蛇形迂曲隆起,且有红色征或食管静脉曲张呈串珠状、结节状或瘤样(不论是否有红色征)。 胃底静脉曲张也可分为3型。 1型静脉曲张(GOV1):最常见,表现为连续并沿胃小弯伸展至胃食管交界处以下2~5 cm,这种静脉曲张较直; 2型静脉曲张(GOV2):沿胃底大弯延伸,超过胃食管结合部,通常更长、更迂曲或贲门部呈结节样隆起; 3型静脉曲张(GOV3):既向小弯侧延伸,又向胃底延伸。 孤立胃静脉曲张(IGV)不伴有食管静脉曲张,可分为2型。 1型(IGV1):位于胃底,迂曲交织,呈串珠样、瘤样和结节样等; 2型(IVG2);罕见,常位于胃体、胃窦或者幽门周围。
·1086 ·中国实用外科杂志2015年10月第35卷第10期 指南与共识 文章编号:1005-2208(2015)10-1086-05 DOI:10.7504/CJPS.ISSN1005-2208.2015.10.16 肝硬化门静脉高压症食管、胃底静脉曲张破裂出血 诊治专家共识(2015) 中华医学会外科学分会门静脉高压症学组 中图分类号:R6文献标志码:C 【关键词】肝硬化;门静脉高压症;食管胃底静脉曲张;出血 Keywords liver cirrhosis;portal hypertension;gastroesophageal varices;bleeding 为规范肝硬化门静脉高压症食管、胃底曲张静脉破裂生早期再出血(入院第一周复发出血)或不可控制的大出出血的诊断与治疗,中华医学会外科学分会门静脉高压症血,而且1年内病死率较高。未经治疗的病人约60%会发学组特组织有关专家编制本共识,旨在为临床诊断和治疗生迟发性再出血,多在上次出血后1~2年内发生。 提供一个基本的规范。本共识不是强制性标准,期望帮助无静脉曲张或曲张静脉小的病人每年以8%的速度出临床医师在本共识的指导下针对大多数病人的具体情况现静脉曲张或发展成大的静脉曲张。静脉曲张出血的发 选择最合理的治疗方案。生率为5%~15%。对于出血最重要的预测因子是曲张静本共识反映当前该领域公认的临床经验和最新研究成脉的大小,大的静脉曲张病人出血风险最高(每年15%)。果,今后将不断更新和完善。尽管40%的食管静脉曲张出血可以自行停止,但目前6周 内病死率仍高达20%。胃底静脉曲张比食管静脉曲张少 1 门静脉压力的评估见,仅见于5%~33%的门静脉高压症病人。 目前,临床上评价门静脉压力的最常用方法是肝静脉 3 食管、胃底静脉曲张分级与分型 压力梯度(hepatic venous pressure gradient,HVPG),其具 [1] 有很好的重复性和可信性。HVPG正常范围是3~5 mmHg 按照食管静脉曲张形态及出血危险程度可分为轻、中、 (1 mmHg=0.133 kPa),≥12 mmHg是形成静脉曲张和(或)重3级。轻度(G1):食管静脉曲张呈直线形或略有迂曲,无 出血的阈值。HVPG变化对食管、胃底静脉曲张的进展、破红色征。中度(G2):食管静脉曲张呈直线形或略有迂曲,裂出血风险以及非曲张静脉并发症发生和病人死亡有预有红色征或食管静脉曲张呈蛇形迂曲隆起但无红色征。测价值。重度(G3):食管静脉曲张呈蛇形迂曲隆起,且有红色征或 食管静脉曲张呈串珠状、结节状或瘤样(不论是否有红色2 食管、胃底静脉曲张(gastroesophageal varices, GOV)出征)。 血及预测胃底静脉曲张通常根据其与食管静脉曲张的关系及其静脉曲张最常见的部位见于食管下段2~5 cm处。该在胃内的位置进行分型。胃底静脉曲张是食管静脉曲张 处浅静脉缺乏周围组织的支持,易发生破裂出血。近50%的延伸,可分为3型。1型静脉曲张(GOV1):最常见,表现 门静脉高压症病人可出现食管、胃底静脉曲张,其程度与为连续并沿胃小弯伸展至胃食管交界处以下2~5 cm,这种 肝功能损害的严重程度有关。肝功能Child -Pugh分级 A 静脉曲张较直;2型静脉曲张(GOV2):沿胃底大弯延伸,超 级病人仅40%有静脉曲张,Child-Pugh C级病人则为过胃食管结合部,通常更长、更迂曲或贲门部呈结节样隆85%。肝储备功能分级见表1。在原发性胆汁性肝硬化病起;3型静脉曲张(GOV3):既向小弯侧延伸,又向胃底延人早期,甚至在未形成肝硬化前就可出现食管、胃底静脉伸。 [3] 曲张并发生静脉曲张破裂出血。孤立胃静脉曲张(IGV)不伴有食管静脉曲张,可分为2 HVPG<12 mmHg 时不会形成静脉曲张;HVPG≥12型。1型(IGV1):位于胃底,迂曲交织,呈串珠样、瘤样和结mmHg时,易形成静脉曲张。当HVPG≥20 mmHg时则易节样等;2型(IVG2);罕见,常位于胃体、胃窦或者幽门周
晚期肝硬化易门静脉高压 *导读:门静脉高压即是门静脉压力增高,它一般出现在肝硬化后期。肝硬化给人们带来了严重的影响,不仅令患者的身体承受病痛的折磨,而且还让患者承受巨大的心理压力。…… 门静脉是指肝脏人口处的一支较大的静脉,它是由肠系膜上静脉和脾静脉汇合而形成的,在肝门分成2支进人肝脏。肝脏的血液75%来自门静脉,25%来自肝动脉。主要负责收集食道、胃、肠、胰、胆囊和脾脏的静脉血液。 正常情况下,门静脉压力为0.7-1.5千帕。 时肝内或肝外门静脉血流受阻,均可使门静脉压增高,另外,先天发育不良,畸形或压迫等也使门脉压力增高。这些病变均可造成肝小叶实质性损害,如肝细胞变性坏死、毛细血管网破坏,继以肝内结节及结缔组织、纤维组织增生。久而久之则使肝内血管变形、梗阻、中断,血流淤积。当肝静脉流出道梗阻严重时,肝细胞缺血缺氧,加重了肝细胞的坏死,使肝内阻力增大。在此情况下,门腔静脉只能以增加自己的收缩压力,增定增粗血管来进行代偿。由此则形成门静脉高压。 长期门静脉高压引起一系列并发症,如出现充血性脾肿大,胃肠、腹膜的慢性充血和侧支循环建立等。门静脉高压会导致食管胃底静脉曲张,腹壁及直肠静脉曲张。当食管及胃底静脉曲张达到一定程度,在外界因素作用下,即可破裂,引起上消化道大
出血。表现为大量呕血或柏油样大便;导致直肠静脉破裂出血时则大量便血。 门静脉高压会出现脾脏肿大、腹胀、纳差、腹腔多脏器淤血、脾功能亢进。脾脏肿大和脾功能亢进使红细胞、白细胞和血小板破坏增多,引起贫血和全血象降低,免疫功能低下,机体抵抗力下降。 门静脉高压也是形成腹水、败血症的直接因素 腹水的出现,往往易造成有效循环血量不足、血压下降、电解质紊乱,累及心、脑、肾等多种脏器的功能。这些严重的合并症,时刻危及患者的生命。
2015 年10 月24 日在北京召开的「中华医学会感染病学分会年会、中华医学会肝病学分会年会」上,发布了最新一版的「肝硬化门静脉高压食管胃静脉曲张出血的防治指南」,该指南由中华医学会肝病学分会、消化病学分会、内镜分会联合出台,时隔7 年,本指南有不少更新,本文将该指南的变化点及要点进行了总结,以供大家参考学习。 本指南的更新点 1. 食管胃静脉曲张破裂出血(EVB)的诊断:旧版指南建议 48 小时内进行胃镜检查,而新版指南更新为 12-24 小时之内行胃镜检查;旧版认为胃镜是诊断 EVB 的唯一可靠方法,而新版明确了 B 超、CT、MRI、肝弹性检测等在 EVB 诊断方面辅助价值。 2. 胃镜检查:旧版建议无静脉曲张的代偿期肝硬化患者每 2-3 年检查 1 次胃镜,失代偿期肝硬化患者每年检查 1 次。新版更新为无静脉曲张的代偿期肝硬化患者每 2 年检查 1 次胃镜,失代偿期肝硬化患者 0.5-1 年检查 1 次胃镜。 3. 急性食管胃底静脉曲张出血的治疗
(1)药物治疗新旧指南均推荐短期应用抗菌药物,旧版推荐使用喹诺酮类抗菌药物,对喹诺酮类耐药者可用头孢类抗菌药物,而新版则相反,首选头孢三代,若过敏,则选择喹诺酮类抗菌药物。 (2)旧版推荐 H2RA 及 PPI 用于辅助治疗,新版则仅推荐 PPI。(3)新增内容:麻醉插管或 ICU 可提高急诊内镜治疗食管胃静脉曲张出血的效果和安全性。 4. 食管静脉曲张出血一级预防 (1)旧版主要推荐药物治疗应用非选择性β 受体阻滞剂,而新版肯定了卡维地洛在食管静脉曲张出血一级预防方面的作用。 (2)旧版对 ACEI/ARB 及螺内酯等可降低门脉压力的药物,因缺乏证据未作明确推荐,新版明确指出不推荐 ACEI/ARB 及螺内酯用于一级预防。 (3)新增如何根据 LDRf 分型选择治疗时机的内容。 (4)明确规定:不推荐内镜下硬化剂治疗用于一级预防;不推荐各种外科手术和 TIPS 用于一级预防;不推荐 EVL 联合非选择性β 受体阻滞剂同时用于一级预防。 5. 食管静脉曲张出血的二级预防 (1)关于二级预防的时机,旧版推荐既往有食管静脉曲张出血史或急性食管胃静脉曲张出血 1 周后开始,而新版则将时间改为 5 天后。 (2)明确规定:肝硬化合并顽固性腹水者,无论一级或二级预防均禁用非选择性β受体阻滞剂。
肝硬化门脉高压的发病机制 门静脉高压(portal hypertension,PH)是指由各种原因导致的门静脉系统压力升高所引起的一组临床综合征,其可定义为:门静脉和下腔静脉之间的压力差即门脉压力梯度(portal pressure gradient,PPG)超过正常上限的5mmHg。PPG的正常值范围为1-5 mmHg。在肝硬化患者中,当PPG超过正常值上限5-10 mmHg时,临床症状轻微或并不显著;当PPG超过正常值上限10 mmHg(如出现静脉曲张、腹水)时,患者就会有明显的临床表现。 门静脉高压症基本病理生理特征是门静脉系统血流受阻和(或)血流量增加,门静脉及其属支血管内静力压升高并伴侧支循环形成。在引起PH的所有原因中,第一推动力是门脉血流阻力的增加,随后是门脉流入量的增加。其可用公式表述为: PH=门静脉流入量×流出阻力 肝硬化是引起PH的最常见原因,其次是门静脉血栓形成(portal vein thrombosis,PVT)。在后者当中,门静脉主干阻塞(血栓)是始发原因,因此发病机制更为明确。相较而言,肝硬化PH 的发病机制较为复杂(图1),故本文就肝硬化PH的发病机制作一综述。 图1 PH的发病机制
注:NHs=神经体液系统(neurohumoral system);RAAs=肾素-血管紧张素-醛固酮系统 (reninangiotensin-aldosterone system) 一、肝内阻力增加 在肝硬化中,肝内阻力增加是由肝窦结构改变(窦性纤维化、再生结节)和肝内血管功能性收缩(由窦内皮细胞产生的血管扩张剂减少而导致)共同作用的结果。 1. 肝血管结构紊乱 任何原因引起的慢性肝病都会引起肝窦的病理改变,其主要是由于肝星状细胞(HSC)和窦内皮细胞(SEC)的表型和功能的改变。 正常情况下HSC参与维生素A的代谢和贮存,以及细胞外基质的合成和降解;肝脏损伤后,HSC发生激活,其大量分裂增生并向肝损伤部位迁徙,并合成胶原、纤维连接蛋白和蛋白多糖等细胞外基质,最终致使肝脏发生纤维化,造成肝窦结构改变。 SEC位于肝窦,将肝窦腔与窦周间隙分隔开来。SEC参与了正常肝细胞的物质交换;肝硬化时,SEC 增生活跃,细胞体肿胀,伸入窦腔,细胞变厚,SEC窗孔数量减少或消失,并通过基底膜的沉积导致肝窦内皮毛细血管化。肝窦内皮的毛细血管化可能在肝内阻力增加和纤维化形成早期发挥着作用。 2. 血管内皮功能障碍
《门静脉高压治疗-Baveno VI共识》译文 彭颖1,2,祁兴顺1,郭晓钟1,2 1沈阳军区总医院消化内科,沈阳,110840;2大连医科大学研究生院,大连,110016 第一作者简介:彭颖(1990-),女,在读硕士研究生,主要从事消化系疾病诊治研究。 通讯作者:祁兴顺,电子邮箱:xingshunqi@https://www.doczj.com/doc/2814925915.html, 郭晓钟,电子邮箱:guoxiaozhong1962@https://www.doczj.com/doc/2814925915.html, 关键词:门静脉高压;静脉曲张;肝硬化;Baveno;指南 原文题目为《EXPANDING CONSENSUS IN PORTAL HYPERTENSION Report of the Baveno VI Consensus Workshop: stratifying risk and individualizing care for portal hypertension》杂志2015年6月13日在线发表于《Journal of Hepatology》。 Management of portal hypertension - Baveno VI Consensus: A Chinese-language translation PENG Ying1,2, QI Xingshun1, GUO Xiaozhong1,2 1 Department of Gastroenterology, General Hospital of Shenyang Military Area, Shenyang, 110840, China; 2 Postgraduate College, Dalian Medical University, Dalian, 110016, China. Keywords: portal hypertension; varices; liver cirrhosis; Baveno; guideline Baveno会议的历史 Baveno(音译:巴韦诺)会议旨在定义有关门静脉高压及静脉曲张出血相关重要事件,总结有关门静脉高压的自然病史、诊断和治疗的现有证据,并为执行临床试验以及治疗病患提供循证推荐。该会议由Roberto de Franchis主持。此前的Baveno I、II、IV会议分别于1990、1995、2005年在意大利Baveno召开;Baveno III、V会议分别于2000、2010年在意大利Stresa (音译:斯特雷萨)召开。Baveno VI会议在2015年4月10日-11日召开。参会人员多是
【共识】TIPS治疗肝硬化门静脉高压最新共识发布 中华消化杂志2014-02-14发表评论分享 门静脉高压症是肝硬化发展过程中的重要病理生理环节,也是肝硬化失代偿期的重要临床表现之一。经颈静脉肝内门体静脉分流术(transjugular intrahepaticportosy stemicshunt,TIPS)通过在肝静脉与门静脉之间的肝实质内建立分流道,以微创的方式,从结构上显著降低门静脉阻力,是降低肝硬化患者门静脉压力的关键措施之一。 选择恰当病例,可有效减少食管胃静脉曲张再出血和腹水复发等肝硬化并发症,改善肝硬化患者生活质量,减少或延缓对肝移植的需求。 TIPS应用于临床巳有20余年,在经历了一系列观念、技术、器材和联合药物治疗的探索后,目前该技术的有效性和安全性日渐成熟,患者在生存时间及质量方面明显获益,得到了国内外同行的广泛认可。 近5年来,国内年实施TIPS超过I000例。2013年中华医学会消化病学分会消化介入学组邀请部分国内相关学科专家就TIPS治疗肝硬化门静脉高压达成了如下共识意见,旨在帮助更多的临床医师在肝硬化门静脉高压治疗中合理应用这一微创手术。 一、TIPS适应证 (一)食管胃静脉曲张破裂出血(EGVB) 肝硬化患者食管胃静脉曲张的发生率分别约为30%-70%,在发现有明确的食管胃静脉曲张后的1年内,约30%的患者存在EGVB的风险。 1.急性EGVB:患者6周内的病死率约为20%,对致命性大出血需要给予抢救治疗。在维护气道通畅、血循环稳定的基础上,根据各医院条件考虑: ①补救性TIPS,是药物联合内镜治疗失败的二线方案; ②早期TIPS,即在大量出血后的72h内,将TIPS作为抢救的一线方案。早期TIPS 止血成功率>95%,较药物联合内镜治疗能更加有效地控制致命性大出血及减少再出血,减少重症监护和住院时间,显著提高患者生存率。肝硬化Child-PughC级、但评分<13的患者,可从早期TIPS中获益更多。 2.EGVB二级预防:急性EGVB停止后,患者发生再出血和死亡的风险很大。对于未经治疗的患者,1-2年内平均再出血率为60%,病死率可达33%,因而从急性出血恢复的患者均应接受二级预防措施。
专家视点特发性非硬化性门静脉高压研究进展
————————————————————————————————作者:————————————————————————————————日期:
专家视点:特发性非硬化性门静脉高压研究进展 国际肝病网2014-07-11发表评论分享 作者河南省人民医院尚佳 特发性非硬化性门脉高压(idiopathic portal hypertension,IPH)又称非肝硬化性门脉纤维化、肝结节状再生性增生、肝内窦前性门静脉高压、Banti综合征、非硬化性门脉高压症或肝内门静脉硬化症(HPS),是一组以肝内窦前性门静脉血流阻力增大与门静脉高压为特征的慢性肝脏疾病综合征,主要是由门静脉主干及分支的非特异性炎症而引起的血管闭塞性纤维化及硬化。 IPH在我国少见,在日本(34.1%)和印度(25%)高发,西方国家约为3%~4%。然而,随着人们对IPH的认识逐渐提高以及医疗检测技术的不断发展,IPH的检出率也在逐年增加。 病因 目前认为,多种因素可导致IPH的发生,包括慢性感染、药物及毒物暴露、血栓形成、免疫因素、遗传因素等。最常见的病因是腹腔内感染引起的门静脉炎症,以及毒物、药物(砷、铜、氯乙烯原料及6-巯基嘌呤、硫唑嘌呤等免疫抑制剂)所致。 发病机制 目前,患者发病机制尚不完全明确,常为多种因素作用结果,但多数学者认为免疫因素可能在发病机制中起重要作用。有研究发现IPH常与自身免疫疾病同时存在。通过对此类患者进行遗传基因检测发现,多数患者存在(HLA)-DR3基因遗传性异常,其发病机制有以下两种途径(见图1): 1)感染、药物、血栓等多种诱因作用于肝脏,致使肝内中小静脉分支闭塞,进而导致门静脉血流受阻,从而引起IPH;2)上述因素作用于脾脏,引起脾髓增生致使脾脏增大,脾血流量增加,从而引起IPH。