
水质化验分析方法(常规)
1水质pH值的测定玻璃电极法
水质-pH值的测定一玻璃电极法
1.1范围
1.1.1本方法适用于饮用水、地面水及工业废水pH值的测定。
1.1.2水的颜色、浊度、胶体物质、氧化剂、还原剂及较高含盐量均不干扰测定;但在pH小于1的强酸性溶液中,会有所谓酸误差,可按酸度测定;在pH大于1;的碱性溶液中,因有大量钠离子存在,产生误差,使读数偏低,通常称为钠差。消除钠差的方法,除了使用特制的低钠差电极外,还可以选用与被测溶液的pH值相近似的标准缓冲溶液对仪器进行校
正。温度影响电极的电位和水的电离平衡。须注意调节仪器的补偿装置与溶液的温度一致,并使被测样品与校正仪器用的标准缓冲溶液温度误差在土1C之内。
1.2原理
pH是从操作上定义的(此定义引自GB3100-31C2-82 “量和单位))第151页)?对于溶液X,测出伽伐尼电池参比电极IKC1浓溶液11溶液XIH2IPt的电动势Ex。将未知pH(x) 的溶液x换成标准pH溶液S,同样测出电池的电动势E。,则pH(X) =pH(S)+(Es-Ex)F/(RTInl0)因此,所定义的pH是无量纲的量。pH没有理论上的意义,萁定义为一种实用定义。但是在物质的量浓度小于O.lmol/dm3的稀薄水溶液有限范围,既非强
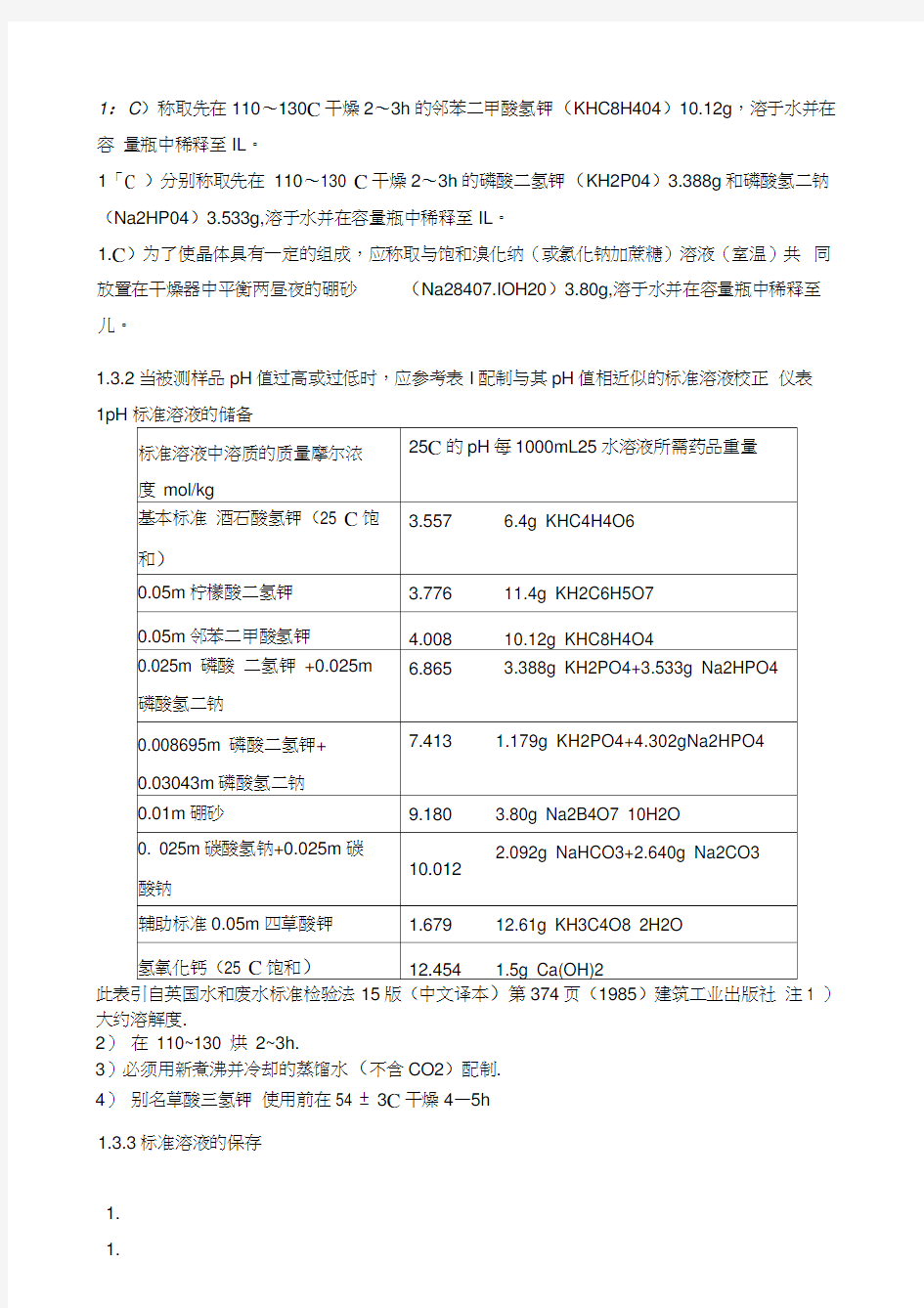
酸性又非强碱性(2 c(H)代表氢离子H十的物质的量浓度,y代表溶液中典型1-1价电解质的活度系数。pH 值由测量电池的电动势而得。该电池通常由饱和甘汞电极为参比电极,玻璃电极为指示电极所组成。在 25C,溶液中每变化1个pH单位,电位差改变为59.16mV,据此在仪器上直接以pH的读数表示。温度差异在仪器上有补偿装置。 1.3试剂 1.3.1标准缓冲溶液(简称标准溶液)的配制方法 1.3.1.1试剂和蒸馏水的质量 1. 1.X106S/CIII的蒸馏水[电导的单位是西门子,Siemens,用符号“ s”表示,1s=1n)],其pH 以6.7?7.3之间为宜。 1. 1:C)称取先在110?130C干燥2?3h的邻苯二甲酸氢钾(KHC8H404)10.12g,溶于水并在容量瓶中稀释至IL。 1「C )分别称取先在110?130 C干燥2?3h的磷酸二氢钾(KH2P04)3.388g和磷酸氢二钠(Na2HP04)3.533g,溶于水并在容量瓶中稀释至IL。 1.C)为了使晶体具有一定的组成,应称取与饱和溴化纳(或氯化钠加蔗糖)溶液(室温)共同放置在干燥器中平衡两昼夜的硼砂(Na28407.IOH20)3.80g,溶于水并在容量瓶中稀释至儿。 1.3.2当被测样品pH值过高或过低时,应参考表I配制与其pH值相近似的标准溶液校正仪表 1pH标准溶液的储备 此表引自英国水和废水标准检验法15版(中文译本)第374页(1985)建筑工业出版社注1 )大约溶解度. 2)在110~130 烘2~3h. 3)必须用新煮沸并冷却的蒸馏水(不含CO2)配制. 4)别名草酸三氢钾使用前在54 ± 3C干燥4—5h 1.3.3标准溶液的保存 1. 1. 1「c冰箱内存放,且用过的标准溶液不允许再倒回去,这样可延长使用期限。 1.3.4标准溶液的pH值随温度变化而稍有差异。一些常用标准溶液的pH(S)值见表2 表2五种标准溶液的pH(S)值 此表引自ilUPAC Manual of Symbols and Terminology for Physicochemical Quantitiesand Units>(1979)第31 页, 这些标准溶液的组成是: A :酒石酸氢钾(25 C饱和1;± B:邻苯二甲酸氢钾,0.05mol/kg; C:磷酸二氢钾,0.025mol/kg; 磷酸氢二钠0.025mol/kg D 磷酸二氢钾0.008695mol/kg 磷酸氢二钠0.03043mol/kg E 硼砂0.01mol/kg 这里溶剂是水 1.3.5样品保存 最好现场测定否则应在采样后把样品保持在0~4并在采样后6h之内进行测定 1.4仪器 1.4.1酸度计或离子浓度计常规检验使用的仪器至少应当精确到0.1pH单位pH范围从0至14如有特殊需要应使用精度更好的仪器 1.4.2玻璃电极与甘汞电极 1.5操作步骤 1.5.1仪器校准操作程序按仪器使用说明书进行先将水样与标准溶液调到同一温度记录测定温度并将仪器温度补偿旋钮调至该温度上用标准溶液校正仪器该标准溶液与水样pH相差 不超过2个pH单位从标准溶液中取出电极彻底冲洗并用滤纸吸干再将电极浸入第二个标准溶液中其pH大约与第一个标准溶液相差3个pH单位如果仪器响应的示值与第二个标准溶液的pH(S)值之差大于0.1pH单位就要检查仪器电极或标准溶液是否存在问题当三者均正常时方可用于测定样品 1.5.2样品测定 测定样品时先用蒸馏水认真冲洗电极再用水样冲洗然后将电极浸入样品中小心 摇动或进行搅拌使其均匀静置待读数稳定时记下pH值 1.6精密度(见表3) 表3 注*根据一个试验室中对pH值在2.21~13.23范围内的生活饮用水轻度中度重度污染的地面水及部分类型工业废水样品进行重复测定的结果而定**根据北京地区19个试验室共使用 10种不同型号的酸度计4种不同型号的电极用本法对pH值在1.41~11.66范围内的7个人工合成水样及1个地面水样的测定结果而定 1.7注意事项 1.7.1玻璃电极在使用前先放入蒸馏水中浸泡24h以上 1.7.2测定pH时玻璃电极的球泡应全部浸入溶液中并使其稍高于甘汞电极的陶瓷芯端 以免搅拌时碰坏 1.7.3必须注意玻璃电极的内电极与球泡之间甘汞电极的内电极和陶瓷芯之间不得有气泡以防断路1.7.4甘汞电极中的饱和氯化钾溶液的液面必须高出汞体在室温下应有少许氯化钾晶体存在 以保证氯化钾溶液的饱和但须注意氯化钾晶体不可过多以防止堵塞与被测溶液的通路 1.7.5测定pH时为减少空气和水样中二氧化碳的溶入或挥发在测水样之前不应提前打开水样瓶1.7.6玻璃电极表面受到污染时需进行处理如果系附着无机盐结垢可用温稀盐酸溶解4对钙镁等难溶性结垢可用EDTA二钠溶液溶解沾有油污时可由丙酮清洗电极按上述方法处理后应在蒸馏水中浸泡一昼夜再使用注意忌用无水乙醇脱水性洗涤剂处理电极 1.8试验报告 试验报告应包括下列内容 a. 取样日期时间和地点 b. 样品的保存方法 c. 测定样品的日期和时间 d. 测定时样品的温度 e. 测定的结果(pH值应取最接近于0.1pH单位如有特殊要求时可根据需要及仪器的精确度确定结果的有效数字位数) f. 其他需说明的情况 1.9参考文献 GB6920-86 2 HZHJS200136水质氨氮的测定电极法 HZ-HJ-S2-0136水质一氦氮的测定一电极法(试行) 2.1范围 本方法可用于测定饮用水、地面水、生活污水及工业废水中氨氮的含量。色度和浊度 对 测定没有影响,水样不必进行预蒸馏。标准溶液和水样的温度应相同,含有溶解物质的总 浓 度也要大致相同。挥发性胺产生正干扰;汞和银因同氨络合力强而有干扰;高浓度溶解离子影响测定。方法的最低检出浓度为0.03mg/L氨氮;测定上限为1400mg/L氨氮。 2.2原理 氨气敏电极为一复合电极,以pH玻璃电极为指示电极,银一氯化银电极为参比电极。此电极对置于盛有O.lmoVL氯化铵内充液的塑料套管中,管端部紧贴指示电极敏感膜处装有疏水半渗透薄膜,使内电解液与外部试液隔开,半透膜与pH玻璃电极间有一层很薄的 膜。当水样中加入强碱溶液将pH提高到11以上,使铵盐转化为氨,生成的氨由于扩散作用通过半透膜(水和其他离子则不能通过),使氯化按电解质波膜层内NH4 ‘ =NH3 +H '反应向左移动,引起氢离子浓度改变,由pH玻璃电极测得其变化。在恒定的离子强度下,测 得的电动势与水样中氨氮浓度的对数呈一定的线性关系。由此,可从测得的电位值确定样品中氦氮的含量。 2.3试剂 所有试剂均用无氨水配制。 2.3.1 铵标准贮备液:CN=I.OOmg/mL。称取3.819氯化铵(NH4C1,在100?105C干燥 2h),溶于水中,移入lOOOmL容量瓶中,稀释至刻度。 2.3.2 100、10、1.0、O.lmg/L的铵标准使用液:参照2.3.1配制或用铵标准贮备液稀释配制。 2.3.3电极内充液:O.lmoVL氯化铵溶液。 2.3.4氢氧化钠(5moVL)-Na2-EDTA(0.5mol/L)混合溶液,贮于聚乙烯瓶中。 2.4仪器 2.4.1离子活度计或带扩展毫伏的pH计。 2.4.2氨气敏电极。 2.4.3电磁搅拌器。 2.5操作步骤 2.5.1仪器和电极的准备 按使用说明书进行,调试仪器。 2.5.2校准曲线的绘制 吸取lO.OOmL浓度为0.1、1.0、10、100、lOOOmg/L的铵标准溶液于25mL小烧杯中,浸入电极后加入l.OmL氢氧化钠-N a2-EDTA溶液,在搅拌下,读取稳定的电位值(在Imin内变化不超过ImV时,即可读取)。在半对数坐标线上绘制E- logc的校准曲线。 2.5.3水样的测定 吸取lO.OOmL水样,以下步骤与校准曲线绘制相同。由测得的电位值,在校准曲线上直接查得水样中的氨氮含量(mg/L), 2.6精密度与准确度 七个实验室分析含14.5 mg/L氨氮的统一分发的加标地面水。实验室内相对标准偏差为 2.0%;实验室间总相对标准偏差为5.2%;相对误差为-1.4%。 注意事项: ⑴绘制校准曲线时,可以根据水样中氨氮含量,自行取舍三或四个标准点。 ⑵实验过程中,应避免由于搅拌器发热而引起被测溶液温度上升,影响电位值的测定。 (3) 当水样酸性较大时应先用碱液调至中性后再加离子强度调节液进行测定 (4) 水样不要加氯化汞保存 (5) 搅拌速度应适当不使形成涡流避免在电极处产生气泡 (6) 水样中盐类含量过高时将影响测定结果必要时应在标准溶液中加入相同量的盐类以消除误差2.7参考文献 水和废水监测分析方法编委会编水和废水监测分析方法第三版pp. 259~260 中国环境科学出版社北京1997 3 HZHJSZ0060水质化学需氧量的测定重铬酸盐法 HZ-HJ-SZ-0060 水质化学需氧量的测定重铬酸盐法 3.1范围 本方法规定了水中化学需氧量的测定方法 本方法适用于各种类型的含COD值大于30mg/L的水样对未经稀释的水样的测定上限为 700mg/L本方法不适用于含氯化物浓度大于1000mg/L(稀释后)的含盐水 3.2定义 在一定条件下经重铬酸钾氧化处理时水样中的溶解性物质和悬浮物所消耗和重铬酸盐相对应的氧的质量浓度 3.3原理 在水样中加入已知量的重铬酸钾溶液并在强酸介质下以银盐作催化剂经沸腾回流后以试亚铁灵为指示剂用硫酸亚铁铵滴定水样中未被还原的重铬酸钾由消耗的硫酸亚铁铵的量换算成消耗氧的质量浓度在酸性重铬酸钾条件下芳烃及吡啶难以被氧化其氧化率较低在硫酸银催化作用下直链脂肪族化合物可有效地被氧化 3.4试剂 除非另有说明实验时所用试剂均为符合国家标准的分析纯试剂试验用水均为蒸馏水或同等纯度的水 3.4.1硫酸银(Ag2SO4)化学纯 3.4.2硫酸汞(HgSO4)化学纯 343 硫酸(H2SO4) ? 1.84g/mL 344硫酸银硫酸试剂向1L硫酸(3.4.3)中加入10g硫酸银(3.4.1)放置1~2天使之溶解并混匀使用前小心摇动 3.4.5重铬酸钾标准溶液 3.4.5.1浓度为c 1/6 K2Cr2O7 = 0.250mol/L的重铬酸钾标准溶液将12.258g在105C干燥2h 后的重铬酸钾溶于水中稀释至1000mL 3.4.5.2浓度为c 1/6 K2Cr2O7 = 0.0250mol/L的重铬酸钾标准溶液将3. 4.5.1条的溶液稀释10 倍而成 3.4.6硫酸亚铁铵标准滴定溶液 3.4.6.1浓度为c [(NH4)2Fe(SO4)2 6H2O] 0.10mol/L的硫酸亚铁铵标准滴定溶液溶解39g硫酸亚铁铵[(NH4)2Fe(SO4)2 6H2O]于水中加入20mL硫酸(3.4.3)待其溶液冷却后稀释至1000mL 3.4.6.2每日临用前必须用重铬酸钾标准溶液(3.准确标定此溶液(3.的浓度取10.00mL重铬 酸钾标准溶液(3.置于锥形瓶中用水稀释至约100mL加入30mL硫酸(3.4.3)混匀冷却后加3 滴(约0.15mL)试亚铁灵指示剂(3.4.7)用硫酸亚铁铵(3.滴定溶液的颜色由黄色经蓝绿色变为红褐色即为终点记录下硫酸亚铁铵的消耗量(mL) 3.4.6.3硫酸亚铁铵标准滴定溶液浓度的计算 c[(NH4)2Fe (SQ) 2。6HO]=10*0.25/V=2.5/V 式中V滴定时消耗硫酸亚铁铵溶液的毫升数 3.4.6.4浓度为C[(NH4)2Fe(SO4)2 6H2O] 0.10mol/L的硫酸亚铁铵标准滴定溶液将3. 4.6.1条的溶液稀释l0倍用重铬酸钾标准溶液(3.标定其滴定步骤及浓度计算分别与3. 4.6.2及 3.4.7邻苯二甲酸氢钾标准溶液c (KC6H5O4) 2.0824 mmol/L称取105时干燥2h的邻苯二甲酸氢钾(HOOCC6H4COOK)0.4251g溶于水并稀释至1000mL混匀以重铬酸钾为氧化剂将邻苯二甲酸氢钾完全氧化的COD值为1.176g氧/ 克(指1g邻苯二甲酸氢钾耗氧1.176g)故该标准溶液的理论COD值为500mg/L 3.4.8 1 10菲绕啉(1 10 phenanathroline monohy drate)指示剂溶液溶解0.7g七水合硫酸亚铁 (FeSO4 7H2O)于50mL的水中加入1.5g 1 10菲绕啉搅动至溶解加水稀释至100mL 3.4.9防爆沸玻璃珠 3.5仪器 常用实验室仪器和下列仪器 3.5.1回流装置带有24号标准磨口的250mL锥形瓶的全玻璃回流装置回流冷凝管长度为 300~500mm若取样量在30mL以上可采用带500mL锥形瓶的全玻璃回流装置 3.5.2加热装置 3.5.3 25mL或50mL酸式滴定管 3.6试样制备 3.6.1采样 水样要采集于玻璃瓶中应尽快分析如不能立即分析时应加入硫酸(3.4.3 )至pH<2置4 °C下保 存但保存时间不多于5天采集水样的体积不得少于100mL 3.6.2试料的准备 将试样充分摇匀取出20.0mL作为试料 3.7操作步骤 3.7.1对于COD值小于50mg/L的水样应采用低浓度的重铬酸钾标准溶液(3.氧化加热回流以后采用低浓度的硫酸亚铁铵标准溶液(3.回滴3.7.2该方法对未经稀释的水样其测定上限为 700mg/L超过此限时必须经稀释后测定 3.7.3对于污染严重的水样可选取所需体积1/10的试料和1/10的试剂放入10 150mm硬质玻璃管中摇匀后用酒精灯加热至沸数分钟观察溶液是否变成蓝绿色如呈蓝绿色应再适当少取试料,重复以上试验直至溶液不变蓝绿色为止从而确定待测水样适当的稀释倍数 3.7.4取试料(3.6.2)于锥形瓶中或取适量试料加水至20.0mL 3.7.5空白试验:按相同步骤以20.0mL水代替试料进行空白试验其余试剂和试料测定(3.7.8)相同记录下空白滴定时消耗硫酸亚铁铵标准溶液的毫升数V1 3.7.6校核试验按测定试料(3.7.8)提供的方法分析20.0mL邻苯二甲酸氢钾标准溶液(3. 4.7)的COD 值用以检验操作技术及试剂纯度该溶液的理论COD值为500mg/L如果校核试验的结 果大于该值的96即可认为实验步骤基本上是适宜的否则必须寻找失败的原因重复实验使之达到要求 3.7.7去干扰试验无机还原性物质如亚硝酸盐硫化物及二价铁盐将使结果增加将其需氧量作为水样COD值的一部分是可以接受的该实验的主要干扰物为氯化物可加入硫酸汞(3. 4.2)部 分地除去经回流后氯离子可与硫酸汞结合成可溶性的氯汞络合物当氯离子含量超过1000mg/L时COD的最低允许值为250mg/L低于此值结果的准确度就不可靠 3.7.8水样的测定于试料(3.7.4)中加入10.0mL重铬酸钾标准溶液(3.和几颗防爆沸玻璃珠(3. 4.9)摇匀将锥形瓶接到回流装置(3. 5.1)冷凝管下端接通冷凝水从冷凝管上端缓慢加入 30mL硫酸银硫酸试剂(3.4.4)以防止低沸点有机物的逸出不断旋动锥形瓶使之混合均匀自溶液开始沸腾起回流两小时冷却后用20~30mL水自冷凝管上端冲洗冷凝管后取下锥形瓶 再用水稀释至140mL左右溶液冷却至室温后加入3滴1 10菲绕啉指示剂溶液(3.4.8)用硫酸 亚铁铵标准滴定溶液(346)滴定溶液的颜色由黄色经蓝绿色变为红褐色即为终点记下硫酸亚 铁铵标准滴定溶液的消耗毫升数V2 3.7.9在特殊情况下需要测定的试料在10.0mL到50.0mL之间试剂的体积或重量要按表1作 相应的调整 表1不同取样量采用的试剂用量 3.8 以mg/L计的水样化学需氧量计算公式如下 COD( mg/L)=c( V1-V2) *8000/V 0 式中c硫酸亚铁铵标准滴定溶液(3.4.6)的浓度mol/L V1--空白试验(3.7.4)所消耗的硫酸亚铁铵标准滴定溶液的体积mL V2--试料测定(3.7.8)所消耗的硫酸亚铁铵标准滴定溶液的体积mL V0--试料的体积mL 8000 1/4O2的摩尔质量以mg/L为单位的换算值测定结果一般保留三位有效数字对COD值小的水样(3.7.1)当计算出COD值小于10mg/L时应表示为COD 10mg/L 3.9精密度 标准溶液测定的精密度 40个不同的实验室测定COD值为500mg/L的邻苯二甲酸氢钾(3.4.7)标准溶液其标准偏差为 20mg/L相对标准偏差为4.0% 4 HZHJS20047水质悬浮物的测定重量法 HZ-HJ-S2-0047 水质一-浮物的测定一-重量法 4.l范围 本方法测定水中悬浮物。 本方法适用于地面水、地下水,也适用于生活污水和工业废水中悬浮物测定。 4.2定义 水质中的悬浮物是指水样通过孔径为0.45i m的滤膜,截留在滤膜上并于103?105C烘干至恒重的固体物质。 4.3试剂 蒸馏水或同等纯度的水。 4.4仪器 4.4.1常用实验室仪器和以下仪器。 4.4.2全玻璃微孔滤膜过滤器。 4.4.3 CN-CA 滤膜、孔径0.45i m.直径60mm。 4.4.4吸滤瓶、真空泵。 4.4.5无齿扁咀镊子。 4.5采样及样品贮存 4.5.1采样 所用聚乙烯瓶或硬质玻璃瓶要用洗涤剂洗净。再依次用自来水和蒸馏水冲洗干净。在采样之前,再用即将采集的水样清洗三次。然后,采集具有代表性的水样500?100 OmL, 盖严瓶塞。 注:漂浮或浸没的不均匀固体物质不属于悬浮物质,应从水样中除去。 4.5.2样品贮存 采集的水样应尽快分析测定。如需放置,应贮存在4C冷藏箱中,但最长不得超过七天。 注:不能加入任何保护剂,以防破坏物质在固、液间的分配平衡。 4.6操作步骤 4.6.1滤膜准备 用扁咀无齿镊子夹取微孔滤膜放于事先恒重的称量瓶里,移入烘箱中于103?105c烘 干半小时后取出置干燥器内冷却至室温,称其重量。反复烘干、冷却、称量,直至两次称量的重量差w 0.2mg。将恒重的微孔滤膜正确的放在滤膜过滤器(4.1)的滤膜托盘上,加盖配 套的漏斗,并用夹子固定好。以蒸馏水湿润滤膜,并不断吸滤。 4.6.2测定 量取充分混合均匀的试样lOOmL抽吸过滤。使水分全部通过滤膜。再以每次IOmL蒸 馏水连续洗涤三次,继续吸滤以除去痕量水分。停止吸滤后,仔细取出载有悬浮物的滤膜 放在原恒重的称量瓶里,移入烘箱中于103?105C下烘干一小时后移入干燥器中,使冷却 到室温,称其重量。反复烘干、冷却、称量,直至两次称量的重量差w 0.4mg为止。 注:滤膜上截留过多的悬浮物可能夹带过多的水份,除延长干燥时间外,还可能造成过滤困难,遇此情况,可酌情少取试样。滤膜上悬浮物过少,则会增大称量误差,影响测定精度,必要时,可增大试样体积。一般以 5 -lOmg悬浮物量做为量取试样体积的实用范 围。 4.7结果计算 悬浮物含量c(mg/L)按下式计算: C= (A-B ) *106/V 式中:C—水中悬浮物浓度,mg/L; A 一悬浮物+滤膜+称量瓶重量,g; B 一滤膜+称量瓶重量,g; V 一试样体积,mL。 4.8参考文献 GB11901-8902 水质化验分析方法(常规) 1水质pH值的测定玻璃电极法 水质-pH值的测定一玻璃电极法 1.1范围 1.1.1本方法适用于饮用水、地面水及工业废水pH值的测定。 1.1.2水的颜色、浊度、胶体物质、氧化剂、还原剂及较高含盐量均不干扰测定;但在pH小于1的强酸性溶液中,会有所谓酸误差,可按酸度测定;在pH大于1;的碱性溶液中,因有大量钠离子存在,产生误差,使读数偏低,通常称为钠差。消除钠差的方法,除了使用特制的低钠差电极外,还可以选用与被测溶液的pH值相近似的标准缓冲溶液对仪器进行校 正。温度影响电极的电位和水的电离平衡。须注意调节仪器的补偿装置与溶液的温度一致,并使被测样品与校正仪器用的标准缓冲溶液温度误差在土1C之内。 1.2原理 pH是从操作上定义的(此定义引自GB3100-31C2-82 “量和单位))第151页)?对于溶液X,测出伽伐尼电池参比电极IKC1浓溶液11溶液XIH2IPt的电动势Ex。将未知pH(x) 的溶液x换成标准pH溶液S,同样测出电池的电动势E。,则pH(X) =pH(S)+(Es-Ex)F/(RTInl0)因此,所定义的pH是无量纲的量。pH没有理论上的意义,萁定义为一种实用定义。但是在物质的量浓度小于O.lmol/dm3的稀薄水溶液有限范围,既非强 酸性又非强碱性(2 污水水质测定—实验常用测定指标 一、生活污水 、SS、PH、氨氮、总氮、总磷、余氯、浊度、VFA等 1.厌氧:COD、BOD 5 2.好氧:COD、BOD 、SS、PH、SV、MLSS、氨氮、总氮、总磷、余氯、浊度、DO等 5 二、工业废水 、浊度、PH、氨氮、硫化物、六价铬、铜、苯胺类、二氧化氯等 1.纺织印染废水: COD、BOD 5 2.制药废水: COD、BOD5、氨氮、硫化物、六价铬、铜、总余氯、苯胺类、总砷、总锌、挥发酚、 甲醛等 3.电镀污水:总铬、六价铬、总镉、总镍、总银、总铅、总汞、总铜、总锌、总铁、COD、PH、 氨氮、总氮、总磷、氟化物、总氰化物等 三、实验常用测定指标 1.COD的测定 a)快速消解分光光度法 HJ/T 399-2007 仪器设备:消解管(锥形瓶)、加热器(微波炉)、分光光度计 b)重铬酸盐法 GB11914-89 仪器设备:回流装置、加热装置、酸式滴定管 c)碘化钾碱性高锰酸钾法 HJ/T132-2003 d)氯气校正法 HJ/T70-2001 的测定 2.BOD 5 a)稀释与接种法HJ 505-2009 仪器设备:滤膜、溶解氧瓶、稀释容器、虹吸管、溶解氧测定仪、冰箱、恒温培养箱 b)微生物传感器快速测定法 HJ/T 86-2002 仪器设备:微生物传感器BOD快速测定仪 c)测压法 具体操作步骤详见OxDirect仪说明书 仪器设备:呼吸法BOD测量仪(OxDirect仪)和生化培养箱 3.氨氮的测定 a)纳氏试剂分光光度法 HJ 535-2009 仪器设备:可见分光光度计、氨氮蒸馏装置 b)水杨酸分光光度计法 HJ536-2009 仪器设备:可见分光光度计、氨氮蒸馏装置 c)电极法 见附件水质氨氮的测定电极法 1 水质自动监测站建设方案 编制单位:榆林兴源电子科技有限公司编制时间:2015年07月 目录 一、水质在线自动监测系统概述 (2) 二、水质在线自动监测系统设计依据 (3) 三、水质在线自动监测系统详述 (4) 3.1 采配水单元 (4) 3.2 预处理单元 (4) 3.3 清洗单元 (6) 3.4系统控制单元 (6) 3.5 数据采集、传输和远程监控 (9) 四、水质在线自动监测仪器 (10) 4.1 五参数分析仪(德国科泽 K100 W系列) (10) 4.2 高锰酸盐指数(德国科泽 K301 COD Mn A) (13) 4.3 氨氮分析仪 (德国科泽K301 NH4 A ) (16) 五、项目预算 (18) 一、水质在线自动监测系统概述 在线水质自动监测系统是以自动监测设备——在线水质分析仪为核心,结合现代的计算机(包括软件)技术、自控技术、网络通讯技术、流体取样术等先进技术手段高度集成的一套完整的自动分析系统。它可以有效地分析来水的各项水质参数,并对水样进行自动留样。同时可利用水质模型功能软件对水质变化趋势进行有效的预测预警,也可以根据实时水质参数之间的关联组合所表现的综合性质,为决策人员提供大量客观详实的有效数据和判断依据。 通常水质在线自动监测系统包括自动分析仪器、取样单元、配水单元、预处理单元、数据采集单元、通讯单元和控制单元;除此以外,还包括清洗除藻、纯水、供电、防雷等辅助单元。水样通过取样设备自动抽取到指定位置,由中控设备控制相应的管路和阀门对水样进行初步的预处理后再进行有针对性的分类处理,合理分配给相应的水质分析设备,分析设备采用符合国家统一颁布的标准方法对水样进行分析测量,并将测量得到的结果传输到数据采集设备,最后由数据采集设备统一发送到远程服务器。在现场,中控设备通常可以对各个系统进行简单的控制,并将测量结果实时显示在中控监视器上。在远程控制中心,一方面通过有功能强大的数据平台,可以把接收来自各站点的监控系统相关信息,汇总得到各种数据报表,并可对数据进行分析处理。先进的数据平台还能结合水质模型功能软件对水质数据进行分析评估以及预测、预警。 本项目监测以下7个常规参数:水温、PH、电导率、DO、浊度、高锰酸盐指数、氨氮。 水环境监测方法标准 标准编号标准名称实施日期 HJ/T338-2007饮用水水源地保护区划分技术规范2007-2-1 HJ/T341-2007水质汞的测定冷原子荧光法(试行)2007-5-1 HJ/T342-2007水质硫酸盐的测定铬酸钡分光光度法(试行)2007-5-1 HJ/T343-2007水质氯化物的测定硝酸汞滴定法(试行)2007-5-1 HJ/T344-2007水质锰的测定甲醛肟分光光度法(试行)2007-5-1 HJ/T345-2007水质铁的测定邻菲啰啉分光光度法(试行)2007-5-1 HJ/T346-2007水质硝酸盐氮的测定紫外分光光度法(试行)2007-5-1 HJ/T347-2007水质粪大肠菌群的测定多管发酵法和滤膜法(试行)2007-5-1 HJ/T191-2005紫外(UV)吸收水质自动在线监测仪技术要求2005-11-1 HJ/T195-2005水质氨氮的测定气相分子吸收光谱法2006-1-1 HJ/T196-2005水质凯氏氮的测定气相分子吸收光谱法2006-1-1 HJ/T197-2005水质亚硝酸盐氮的测定气相分子吸收光谱法2006-1-1 HJ/T198-2005水质硝酸盐氮的测定气相分子吸收光谱法2006-1-1 HJ/T199-2005水质总氮的测定气相分子吸收光谱法2006-1-1 HJ/T200-2005水质硫化物的测定气相分子吸收光谱法2006-1-1 HJ/T164-2004地下水环境监测技术规范2004-12-9 HJ/T132-2003高氯废水化学需氧量的测定碘化钾碱性高锰酸钾法2004-1-1 HJ/T96-2003pH水质自动分析仪技术要求2003-7-1 HJ/T97-2003电导率水质自动分析仪技术要求2003-7-1 HJ/T98-2003浊度水质自动分析仪技术要求2003-7-1 HJ/T99-2003溶解氧(DO)水质自动分析仪技术要求2003-7-1 HJ/T100-2003高锰酸盐指数水质自动分析仪技术要求2003-7-1 HJ/T101-2003氨氮水质自动分析仪技术要求2003-7-1 HJ/T102-2003总氮水质自动分析仪技术要求2003-7-1 HJ/T103-2003总磷水质自动分析仪技术要求2003-7-1 HJ/T104-2003总有机碳(TOC)水质自动分析仪技术要求2003-7-1 HJ/T86-2002水质生化需氧量(BOD)的测定微生物传感器快速测定法2002-7-1 HJ/T91-2002地表水和污水监测技术规范2003-1-1 HJ/T92-2002水污染物排放总量监测技术规范2003-1-1 HJ/T70-2001高氯废水化学需氧量的测定氯气校正法2001-12-1 HJ/T71-2001水质总有机碳的测定燃烧氧化-非分散红外吸收法2002-1-1 中心以化工行业技术需求和科技进步为导向,以资源整合、技术共享为基础,分析测试、技术咨询为载体,致力于搭建产研结合的桥梁。以“专心、专业、专注“为宗旨,致力于实现研究和应用的对接,从而推动化工行业的发展。 水质检测方法汇总 相关检测方法分别如下: 1 【pH值】水质 pH值的测定玻璃电极法GB/T6920-1986 2 -------【溶解氧】水质溶解氧的测定电化学探头法 GB/T11913-1989 碘量法《水和废水监测分析方法》(第四版)国家环保总局2002年 3 【臭和味】文字描述法《水和废水监测分析方法》(第四版)国家环保总局2002年 4 -------【侵蚀性二氧化碳】甲基橙指示剂滴定法《水和废水监测分析方法》(第四版)国家环保总局2002年 5 【酸度】酸度指示剂滴定法《水和废水监测分析方法》(第四版)国家环保总局2002年 6 -------【碱度(总碱度、重碳酸盐和碳酸盐)】酸碱指示剂滴定法《水和废水监测分析方法》(第四版)国家环保总局2002年 7 【色度】水质色度的测定GB/T11903-1989 8 ------【浊度】水质浊度的测定GB/T13200-1991 9 【悬浮物(SS)】水质悬浮物的测定重量法GB/T11901-1989 10------【总可滤残渣】重量法《水和废水监测分析方法》(第四版)国家环保总局2002年 11【总残渣】重量法《水和废水监测分析方法》(第四版)国家环保总局2002 年 12 -----【全盐量(溶解性固体)】水质全盐量的测定重量法 HJ/T51-1999 13【总硬度(钙和镁总量)】水质钙和镁总量的测定 EDTA滴定法 GB/T7477-1987 14 -----【高锰酸盐指数】水质高锰酸盐指数的测定 GB/T11892-1989 15【化学需氧量(COD)】水质化学需氧量的测定重铬酸盐法 GB/T11914—1989 16 ------【生物需氧量】水质生物需氧量的测定稀释与接种法 GB/T7488—1987 17【氨氮】水质铵的测定纳氏试剂比色法 GB/T7479-1987 水杨酸-次氯酸盐光度法《水和废水监测分析方法》(第四版)国家环保总局2002年 18 -----【硝酸盐氮】水质硝酸盐氮的测定酚二磺酸分光光度法》GB/T7480-1987 水质硝酸盐氮的测定紫外分光光度法》HJ/T346-2007 19【亚硝酸盐氮】《水质亚硝酸盐氮的测定分光光度法》GB/T7493-1987 水质在线监测仪器发展现状 水质在线监测仪器作为水质在线自动监测系统的核心,运用现代传感器技术、自动测量技术、自动控制技术等,采用化学法、电化学法、光谱法等分析方法,能对水质参数进行实时连续在线测量和分析。水质在线监测仪器主要监测对象有:化学需氧量(COD)、氨氮、总氮、总有机碳(TOC)、总磷、锑、砷、铜、汞、铬、金属离子、pH值、电导率、浊度、溶解氧等。 1 COD在线监测仪器发展现状 化学需氧量(COD)是指水体中易被强氧化剂氧化的还原性物质所消耗的氧化剂的量,以氧的mg/L来表示,反映了水体中受还原性物质污染的程度,这个指标是为了了解水中的污染物将要消耗多少氧。 1.1 COD在线监测仪器的技术原理 目前COD在线监测仪器的主要技术原理有6种: 1)重铬酸盐法-光度比色法; 2)重铬酸盐法-库仑滴定法; 3)重铬酸盐法-氧化还原滴定法; 4)电化学氧化法-氢氧基及臭氧(混合氧化剂)氧化法; 5)电化学氧化法-臭氧氧化法; 6)紫外吸收法(UV法)。 为便于比较,可将以上6种技术原理归为三类:重铬酸盐法、电化学氧化法和紫外吸收法(UV法)。 1.1.1 重铬酸盐法 1)重铬酸盐法根据测得数值的方法不同分为光度比色法、库仑滴定法、氧化还原滴定法。通常在一定的温度下,在强酸溶液中用一定量的重铬酸钾氧化水样中还原性物质,经过高温消解后,Cr6+被水中还原性物质还原为Cr3+。再使用分光光度计、库仑滴定、氧化还原等方法测得数值,利用该数值与试样中氧化还原物质浓度的关系进行定量分析。 2)该类是国家推荐使用的方法,有测量准确、测量范围广、技术成熟等优点。 3)但该类仪器也存在以下问题:①测量时间相对较长,一旦水质突变,有可能无法及时监测;②通常采用加温或加压的办法提高消解速度,增加了设备的复杂性,易故障;③产生强腐蚀性、含有毒的重金属离子废液,易腐蚀管路,同时会产生二次污染。 1.1.2 电化学氧化法 1)电化学氧化法根据所使用的氧化剂不同分为氢氧基及臭氧(混合氧化剂)氧化法和臭氧氧化法。电化学氧化法采用三电极设计,包括工作电极、辅助电极和参比电极。工作电极(即阳极):该电极头表面镀PbO2,接电源正极,发生的是氧化还原反应。在一定的工作电压下,溶液中的OH-在PbO2的表面放电产生OH 基,具有很强的氧化性。辅助电极(即阴极):该电极也是铂电极,接电源负极,发生的是还原反应。信号电流通过阴、阳两极。参比电极:该电极独立于信号电流以外,自身电位稳定,作为工作电极的电位参照,当水样与电解液定量进入测量池时,有机物被工作电极表面所产生的OH基所氧化,而氧化过程所消耗的电流大小与水样的COD值的大小成线性关系。只要将氧化所消耗的电流信号通过检测、放大与处理就可知与水样浓度相对的COD值。 2)电化学氧化法测量时间较短,运行可靠,OH基通常能将有机物100%氧化,不存在选择性问题,测量范围较广,适用于各种场合的废水。采用该原理的在线监测仪器结构相对简单,由于是链式反应,基本上不消耗电解液。 3)电化学氧化法不属于国标或推荐方法,在应用时,需要将其分析结果与国标方法进行比对试验并进行适当的校正。同时电化学氧化法的在线监测仪器需要添加温度补偿。 1.1.3 紫外吸收法(UV法) 1)UV是Ultraviolet Ray(紫外线)的简称,UV计是应用紫外线吸光度原理,用双波长吸光度测定法测量水中的有机污染物浓度的一种自动在线监测仪器。由于各种有机物对254nm的紫外光大多有吸收,通过测定污水对UV254的吸收程度得到UV吸收值,在通过UV值与COD之间的线性关系式就可以自动换算出所测水样的COD值。同时UV计利用波长为550nm的参比光可以自动校正浊度、电源的波动、元器件老化等因素对测量结果的干扰,从而提高测量精度。 2)UV法不用试剂,不用取样,对样品条件没有任何限制,不需要样品的预处理,因此结构简单,故障率低。适用于市政污水宏观监测、水质变化比较稳定的环境,对水中的一大类芳香族有机物和带双键有机物尤为灵敏,对苯类、苯环 生活饮用水检测标准 生活饮用水卫生标准是从保护人群身体健康和保证人类生活质量出发,对饮用水中与人群健康的各种因素(物理、化学和生物),以法律形式作的量值规定,以及为实现量值所作的有关行为规范的规定,经国家有关部门批准,以一定形式发布的法定卫生标准。 生活饮用水卫生标准可包括两大部分:法定的量的限值,指为保证生活饮用水中各种有害因素不影响人群健康和生活质量的法定的量的限值;法定的行为规范,指为保证生活饮用水各项指标达到法定量的限值,对集中式供水单位生产的各个环节的法定行为规范。 生活饮用水的水质标准: 1.为防止介水传染病的发生和传播,要求生活饮用水不含病原微生物。 2.水中所含化学物质及放射性物质不得对人体健康产生危害,要求水中的化学物质及放射性物质不引起急性和慢性中毒及潜在的远期危害(致癌、致畸、致突变作用)。 3.水的感官性状是人们对饮用水的直观感觉,是评价水质的重要依据。生活饮用水必须确保感官良好,为人民所乐于饮用。 生活饮用水水质标准共35项。其中感官性状和一般化学指标15项,主要为了保证饮用水的感官性状良好;毒理学指标15项、放射指标2项,是为了保证水质对人不产生毒性和潜在危害;细菌学指标3项是为了保证饮用水在流行病学上安全而制定的。 科标能源实验室科提供一些水质检测项目,如下: 色度浑浊度臭和味肉眼可见物PH总硬度(以CaCO3计)铁铝铜锰锌挥发酚类(以苯酚计)阴离子合成洗涤剂硫酸盐氯化物溶解性总固体耗氧量(以O2计)砷镉铬(六价)氰化物铅氟化物汞硝酸盐(以N计)硒四氯化碳三氯甲烷菌落总数总大肠菌群耐热大肠菌群游离余氯总α放射性总β放射性硫化物锑钠钡铍硼镍钼铊银二氯甲烷一氯二溴 水质在线监测系统,通过建立无人值守实时监控的水质自动监测站,可以及时获得连续在线的水质监测数据( 常规五参数、COD、氨氮、重金属、生物毒性等),利用现代信息技术进行数据采集并将有关水质数据传送至环保信息中心,实现环保信息中心对自动监测站的远程监控,有利于全面、科学、真实地反映各监测点的水质情况,及时、准确地掌握水质状况和动态变化趋势。水质在线监测系统由水质在线分析仪、采样系统、辅助参数监测系统等组成。 其中水质在线分析仪是基于紫外全光谱技术的连续在线式水中有机物浓度分析仪,在水质的在线监测方面与传统的COD化学法和现有的紫外单/双波长法相比均具有非常明显的技术优势,同时给用户的使用带来了明显的经济效益,具体表现如下: 与传统的COD化学法在线监测设备想比,在技术上具有结构简单、可靠性高、响应速度快(1秒钟一个数据)实时性高、不存在二次污染等特点,从经济效益上讲水质在线分析仪具有运行费用低、维护周期特别长(一般可达到半年之久)、维护量小等显著特点。 与现有的紫外单/双波长法(利用污水在254nm处的吸光度与污水中COD之间的线性关系测定COD浓度)相比具有测试准确度高、检测范围宽、维护周期特别长(一般可达到半年之久)、维护量小等显著特点。这是因为单波长法仅能对有机污染物组分较为单一的污水或者污水中所含有机污染物组分相对固定的污水进行COD的测定,而对于污染物组分复杂多变的样品由于吸光度与COD之间的相关性较差直接导致测试结果的误差增大。紫外全谱扫描技术则通过污水的紫外光谱数据与有机污染物浓度之间所建立的数学模型来预测水中有机污染物的浓度,由于模型本身的外推能力会使测试准确度随着用户的使用时间增长而愈来愈高。在检测范围上采用专利型在线稀释装置,可以满足在不更换或调整比色皿的 水质化验分析方法(常规) 1水质pH值的测定玻璃电极法 水质-pH值的测定—玻璃电极法 1.l 围 1.1.1 本方法适用于饮用水、地面水及工业废水pH值的测定。 1.1.2水的颜色、浊度、胶体物质、氧化剂、还原剂及较高含盐量均不干扰测定;但在pH小于1的强酸性溶液中,会有所谓酸误差,可按酸度测定;在pH大于1;的碱性溶液中,因有大量钠离子存在,产生误差,使读数偏低,通常称为钠差。消除钠差的方法,除了使用特制的低钠差电极外,还可以选用与被测溶液的pH值相近似的标准缓冲溶液对仪器进行校正。温度影响电极的电位和水的电离平衡。须注意调节仪器的补偿装置与溶液的温度一致,并使被测样品与校正仪器用的标准缓冲溶液温度误差在±1℃之。 1.2 原理 pH是从操作上定义的(此定义引自GB3100-31C2-82“量和单位))第151页).对于溶液X,测出伽伐尼电池参比电极IKC1浓溶液ll溶液XIH2IPt的电动势Ex。将未知pH(x)的溶液x换成标准pH溶液S,同样测出电池的电动势E。,则pH(X) =pH(S)+(Es-Ex)F/(RTlnl0)因此,所定义的pH是无量纲的量。pH没有理论上的意义,萁定义为一种实用定义。但是在物质的量浓度小于O.lmol/dm3的稀薄水溶液有限围,既非强酸性又非强碱性(2 生活饮用水标准检验方法 在各种水体,特别是污染水体中存在有大量的有机物质,适于各种微生物的生长,因此水体是仅次于土壤的第二种微生物天然培养基。水体中的微生物主要来源于土壤,以及人类的动物的排泄物及污染。水体中微生物的数量和种类受各种环境条件的制约。 一般认为,水中微生物以革兰氏阴性杆菌占有较大优势。与其他水体相比,河水及溪水中革兰氏阳性菌相对较多,这是因为陆地微生物冲洗污染的缘故。 《中华人民共和国国家标准生活饮用水标准检验法》提供了水质中细菌总数和总大肠菌群的检测方法。 1、国家标准中,细菌总数是指1ml水样在营养琼脂培养基中,于37℃经24h培养后,所生长的细菌菌落的总数。 对生活饮用水,直接吸取1ml水样于平皿中,加入营养琼脂后混匀,37℃培养24h,进行计数。 对水源水,根据情况对样品进行10倍梯度稀释,选择适宜稀释液1ml,加注平皿,营养琼脂混匀,37℃培养24h,进行计数。 按照规定格式报告每毫升水中细菌总数。 2、国家标准中,利用总大肠菌群作为粪便污染的指标。总大肠菌群是指一群需氧及兼性厌氧的,37℃生长时能使乳糖发酵,在24h内产酸产气的革兰氏阴性无芽胞杆菌。水样中总大肠菌群数的含量,表明水被粪便污染的程度,而且间接地表明有肠道致病菌存在的可能。 国家标准物质提供了多管发酵法及滤膜法检测总大肠菌群的方法。 3、多管发酵法检测总大肠菌群,分为三步:初发酵试验,平板分离,复发酵证实试验。 初发酵试验,采用乳糖蛋白胨培养液37℃培养24h,观察产酸产气情况。对阳性管培养物,接种于品红亚硫酸钠培养基或伊红美蓝培养基,观察菌落特征,并进行革兰氏染色和镜检。对典型和可疑菌落,接种于乳糖蛋白胨培养液,进行复发酵证实试验,并根据标准所附检数表报告结果。 其中,对生活饮用水,初发酵试验接种水样总量300ml,即100ml接种2管,10ml接种10管,采用两个稀释度,12支发酵管。对水源水,初发酵试验接种水样总量55.5ml,即10ml接种5管,1ml接种5管,0.1ml接种10管,共采用三个稀释度,15支发酵管。两种接种方法,所用的检数表是不同的。 4、滤膜法检测总大肠菌群,就是利用微孔滤膜,过滤一定量水样,将水样中含有的细菌截留在滤膜上,然后将滤膜帖放在选择性培养基上(如品红亚硫酸钠培养基),经培养和证实试验后,直接计数滤膜上生长的典型大肠菌群菌落,并计算出每升水样中含有的总大肠菌群数 注意;菌落总数测定中,应选择合适的稀释度进行。生活饮用水,国家标准规定每毫升不得超过100个,因此可以直接吸取1毫升到平板进行培养。 培养时间。与食品中菌落计数不同,测定水中细菌总数,培养时间采用24h。 水质检验方法 一、pH的测定GB/T6904-2008) 1 范围 本标准规定了工业循环冷却水及锅炉用水中pH的测定方法。 本标准适用于循环冷却水及锅炉用水中pH值在0~14范围内的测定,本标准还适用于天然水、污水、除盐水、锅炉给水以及纯水的pH的测定。 2 原理 将规定的指示电极和参比电极浸入同一被测溶液中,成一原电池,其电动势与溶液的pH有关。通过测量原电池的电动势即可得出溶液的pH。 3 试剂和材料 3.1 草酸盐标准缓冲溶液:c[KH3(C2O4)2·2H2O]=0.05 mol/L。 称取12.61 g四草酸钾溶于无二氧化碳的水中,稀释至1000m L.。 3.2酒石酸盐标准缓冲溶液:饱和溶液。 在25℃下,用无二氧化碳的水溶解过量的(约75 g/ L)酒石酸氢钾并剧烈振摇以制备其饱和溶液。 3.3 苯二甲酸盐标准缓冲溶液:c(C6H4CO2HCO2K)=0.05 mol/L。 称取10.24 g预先于(110±5)℃干燥1h的苯二甲酸氢钾,溶于无二氧化碳的水中,稀释至1000m L.。 3.4 磷酸盐标准缓冲溶液:c(KH2PO4)=0.025 mol/L;c(Na2HPO4)=0.025 mol/L。 称取3.39 g磷酸二氢钾和3.53 g磷酸氢二钠溶于无二氧化碳的水中,稀释至1000m L.。磷酸二氢钾和磷酸氢二钠需预先在(120±10)℃干燥2h。 3.4 硼酸盐标准缓冲溶液:c (Na2B4O7·10H2O)=0.01 mol/L. 称取3.80 g十水合四硼酸钠,溶于无二氧化碳的水中,稀释至1000m L.。 3.5 氢氧化钙标准缓冲溶液:饱和溶液。 在25℃时,用无二氧化碳的水制备氢氧化钙的饱和溶液。存放时应防止空气中二氧化碳进入。一旦出现混浊,应弃去重配。 不同温度时个标准缓冲溶液的pH值列于表1 4 仪器、设备 4.1 酸度计:分度值为0.02pH单位。 ZY 环境保护部环境监测仪器质量监督检验中心 作业指导书 HJC-ZY62-2014 铅水质自动在线监测仪技术要求和 检测方法作业指导书 参考《铅水质自动在线监测仪技术要求和检测方法(送审稿)》 自2014年03月01日起实施编写:贺鹏审核:王强批准:杨凯 1、适用范围 本作业指导书规定了铅水质自动在线监测仪的技术要求、性能指标及检测方法。针对应用于不同场合的铅水质自动在线监测仪(以下简称“仪器”),规定了两型仪器的检测范围。 I型仪器的检测范围为:(0.005~0.2)mg/L,??型仪器的检测范围为:(0.2~2)mg/L。 2、规范性引用文件 本作业指导书内容引用了下列文件或其中的条款。凡是不注明日期的引用文件,其有效版本适用于本标准。 GB 4208 外壳防护等级(IP代码) GB/T 13306 标牌 HJ/T 212 污染源在线自动监控(监测)系统数据传输标准 3、术语和定义 下列术语和定义适用于本标准。 3.1 标样核查check with standard solution 仪器测量标准溶液,判定测量结果的准确性。 3.2 定量下限limit of quantification 在满足示值误差要求的前提下仪器能够测定待测物质的最小浓度。 3.3 记忆效应memory effect 仪器完成某一标准溶液或水样测量后对下一个测量结果的影响程度。 3.4 标样加入试验回收率recovery 仪器分别测量加入一定浓度的标准溶液前后的实际水样,计算加入标准浓液后测定值的增加量相对于理论加入量的百分率。 3.5 零点漂移zero drift 在未对仪器进行计划外的人工维护和校准的前提下,按规定周期连续测量浓度值为检 养殖水质检测常用的方法有哪些? 养殖水质检测常用的方法有哪些?众所周知,养殖生产成功的关键在于水,只有管好水,养殖的成功才有保障。保持良好的水质环境,水质检测是至关重要的。水质检测的方法有很多,从传统的经验法到化学法再到目前正在推广的仪器法,经历了漫长的三个阶段。 一、传统经验法 是指养殖人员凭借多年的工作经验,人为地判断水质的各项指标。如鱼类摄食减少,则可能是pH值偏高或偏低,也有可能是氨氮超标;鱼类集中于水面,可能是水中缺氧等。这些人为的判断只是一个粗略的结果,误差是相当大的,而且随着养殖行业的发展,各企业的养殖规模越来越大,养殖的品种也越来越多,养殖的质量要求在不断提高,那么养殖水质的变化就是多样的,造成水质改变的原因更是多样的,例如投喂饲料、投放药物、自然环境、养殖品种数量的变化等因素,都会造成水质改变,单纯依靠人为经验的判断,已根本无法满足需要,有时甚至会带来巨大的损失。因此,这种依靠经验判断水质的土办法虽然运用了很长时间,但随着科学的进步和人们观念的转变,养殖专家的经验依然是各企业的宝贵财富,但作为检测水质的方法,已经逐渐被淘汰了。 二、化学法 在很多人依靠经验判断水质好坏的时候,采用化学方法检测水质还不被广泛利用,这一方法的最大优势就是检测数据准确可靠,但为什么没有推广应用呢?有几个方面的原因:第一,化学方法的检测过程比较复杂,需要较长的时间,要求检测人员具备相当的专业技能,才能准确的检测,如化学滴定法。有的化学检测试纸,如pH试纸,一般只能进行粗略的测量,如观察试纸颜色判断pH值在7~8之间,而无法得到准确的数字;另一方面,试纸容易受到外界环境(如温度、湿度、光照等)的影响,会导致试纸失效,粗略的测量也无法保证了。第二,化学法检测都需要取样测量,而水样采集到实验室时,各项指标都可能已发生变化,因而最终的检测结 水质检测的标准和方法 生活饮用水卫生标准GB5749-85 生活饮用水水质,不应超过下表所规定的限量。 生活饮用水水质标准 项目标准 感官性状和一般化学指标 色色度不超过15度,并不得呈现其他异色 浑浊度度不超过3度,特殊情况不超过5度 嗅和味不得有异臭、异味 肉眼可见物不得含有 PH 6.5-8.5 总硬度以CzCO3,计mg/L 450 铁Femg/L 0.3 锰Mnmg/L 0.1 铜Cumg/L 1.0 锌Znmg/L 1.0 挥发性酚类以苯酚计mg/L 0.002 硫酸盐mg/L 250 氯化物mg/L 250 溶解性总固体mg/L 1000 毒理学指标 氟化物mg/L 1.0 氰化物mg/L 0.05 砷Asmg/L 0.05 硒Semg/L 0.01 汞Hgmg/L 0.001 镉Cdmg/L 0.01 铬六价Cr6+mg/L 0.05 铅Pbmg/L 0.05 银 0.05 硝酸盐以N计mg/L 20 氯仿μg/L 60 四氯化碳*μg/L 3 苯并(a)芘*μg/L 0.01 滴滴滴*μg/L >1.0 六六六*μg/L >5.0 细菌学指标 菌落总数cfu/mL 100 总大肠菌群(MPN/100mL) 3 游离余氯 在与水接触30min后应不低于0.3mg/L。集中式给水除出厂水应符合上述要求外, 管网末梢水不应低于0.05mg/L 放射性指标总σ放射性Bq/L 0.1 总β放射性Bq/L 1.0 检验项目在一般情况下,细菌学指标和感官性状指标列为必检项目,其他指标可根据当地水质情况和需要选定。对水源水、出厂水和部分有代表性的管网末梢水,每月进行一次全分析。 自备给水和农村集中式给水水质检验的采样点数、采样次数和检验项目,可根据具体情况参照上述要求确定。 一水质监测分析方法 1 COD cr 定义:是指水体中易被强氧化剂氧化的还原性物质所消耗氧化剂的量,结果折算成氧的量(以mg/L计)。 意义:测COD是为了了解水中的污染物将要消耗多少氧. 水中的还原性物质:有机物、亚硝酸盐、亚铁盐、硫化物等. 测量原理:在强酸性溶液中,用一定量的K2Cr2O7氧化水样中还原性物质,过量的K2Cr2O7以试亚铁灵作指示剂,用(NH4)2Fe(SO4)2`6H2O 回滴(黄-蓝-红褐色即为终点).根据(NH4)2Fe(SO4)2`6H2O的用量算出水中还原性物质消耗氧的量. 测量过程中一般以Ag2SO4作为催化剂,HgSO4掩蔽CL-干扰. 公式: COD cr(o2,mg/L,)=(V0-V1).C×8×1000/V 2 NH3-N 定义:水容易中的NH3-N是以游离氨或离子氨形式存在的氮. 氮的种类:硝酸盐氮、亚硝酸盐氮、NH3-N、和有机氮. 意义:鱼类对非离子氨比较敏感,为保护淡水水生物,水中非离子<0.02 mg/L. 实验室测量方法:①纳氏试剂光度法②水杨酸-次氯酸盐比色法 3 TN:指水中可溶性及悬浮颗粒中的含氮量 测定方法: 碱性过硫酸钾消解紫外分光光度法 原理:在水样中加过硫酸钾并高温消解,然后在220nm紫外光处测量吸光度,通过吸光度计算TN浓度的方法. 4 TP:P几乎都以各种磷酸盐的形式存在 测定TP的意义:防止水质”富营养化” 检测分析方法:第一步可由氧化剂K2S2O8将水样中不同形态的P转化为磷酸盐;第二步测定正磷酸,从而求的TP含量. 测定方法:K2S2O8-钼蓝法 ①K2S2O8消解 原理:K2S2O8溶液在高压釜内经120℃加热,产生如下反应: K2S2O8+H2O→2KHSO4+?O2 从而将水中存在的有机P、无机P和悬浮P氧化成正磷酸. ②钼蓝分光光度法 方法原理:在酸性条件下,正磷酸盐与钼酸铵、酒石酸锑氧钾反应,生成磷钼杂多酸,被还原剂抗坏血酸还原,则变成蓝色络合物,通常即称磷钼蓝. 保存:由于磷酸盐可能吸附于塑料瓶壁上,故不可用塑料瓶储存,所有 https://www.doczj.com/doc/133740961.html,/search/s_d_%CB%AE%D6%CA%B7%D6%CE%F6%B7%BD%B7%A8%B9%FA%BC %D2%B1%EA%D7%BC%BB%E3%D7%DC_1.htm下载网址 水质分析方法国家标准汇总详细下载目录 水质分析方法国家标准汇总(一) 目录:pH水质自动分析仪技术要求 氨氮水质自动分析仪技术要求 超声波明渠污水流量计 地表水和污水监测技术规范 地下水环境监测技术规范 电导率水质自动分析仪技术要求 高氯废水化学需氧量的测定(碘化钾碱性高锰酸钾法) 高氯废水-化学需氧量的测定(氯气校正法) 高锰酸盐指数水质自动分析仪技术要求 工业废水总硝基化合物的测定(分光光度法) 工业废水总硝基化合物的测定(气相色谱法) 海洋监测规范第一部分:总则 环境甲基汞的测定(气相色谱法) 水质分析方法国家标准汇总(二) 目录:环境中有机污染物遗传毒性检测的样品前处理规范 近岸海域环境功能区划分技术规范 溶解氧(DO)水质自动分析仪技术要求 水和土壤质量有机磷农药的测定(气相色谱法) 水污染物排放总量监测技术规范 水质-1,2-二氯苯、1,4-二氯苯、1,2,4-三氯苯的测定(气相色谱法) 水质-甲基肼的测定(对二甲氨基苯甲醛分光光度法) 水质-pH值的测定(玻璃电极法) 水质-氨氮的测定(气相分子吸收光谱法) 水质-铵的测定(水杨酸分光光度法) 水质-铵的测定(纳氏试剂比色法) 水质-铵的测定(蒸馏和滴定法) 水质-钡的测定(电位滴定法) 水质-钡的测定(原子吸收分光光度法) 水质-苯胺类化合物的测定(N-(1-萘基)乙二胺偶氮分光光度法) 水质-苯并(a)芘的测定(乙酰化滤纸层析荧光分光光度法) 水质-苯系物的测定(气相色谱法) 水质-吡啶的测定(气相色谱法) 水质-丙烯腈的测定(气相色谱法) 水质采样样品的保存和管理技术规定 水质分析方法国家标准汇总(三)(已下载) 目录:水质-采样方案设计技术规定 水污染源在线监测系统的运营管理方法 1、定期进行仪器现场巡查,进行必要的校准、维护、维修、耗材更换工作。以 保障仪器准确可靠运行。 2、负责每天进行一次仪器运行状态检查,如发现问题则在第一时间解决。 3、按仪器运行要求定期对系统进行校准,以保证仪器数据的准确有效。 4、应对在线监测站建立专人负责制,制定操作及维修规程和日常保养制度,建 立日常运行记录和设备台账,建立相应的质量保证体系,并接受环境保护管理部门的台账检查。 5、应每月向有关环境保护管理部门作运营工作报告,陈述站点在线监测系统的 运营情况。 6、安排相对固定的专业人员负责运营维护工作。 7、应备有常用耗材与配件及必要的交通工具,以保障维修及时。 8、接受环保部门的监督、指导、考核,及时汇报重大事故或仪器严重故障的情 况。 一、日常管理 1、质量保证与质量控制制度 1.1操作人员应按国家相关规定,经培训考核合格,持证上岗。 1.2在线监测仪器在有效使用期内应通过检定或校验。应具备运行过程中定期自 动标定和人工标定功能,以保证在线监测系统监测结果的可靠性和准确性。 1.3采用国家级样品,若采用自配标样,应用有证标准样品对自配标样进行验证, 验证结果应在标准值确定度范围内。标样浓度应与被测废水浓度相匹配。每周用国家认可的质控样(或按规定方法配制的标准溶液)对自动分析仪进行一次标样溶液核查,质控样(或标准溶液)测定的相对误差应不大于标准值的±10%,若不符合,应重新绘制校准曲线,并记录结果。 1.4样品的测定值应在校准曲线的浓度范围内。 1.5按照国家规定的监测分析方法进行实际水样比对试验,比对试验时,实验室 质量控制按照有关规定执行,比对试验实验室监测分析方法请见《水污染源在线监测系统运行于考核基数规范(试行)》(HJ/T355-2007)中的表2,比对试验相对误差值应满足HJ/T355-2007表1中规定的性能指标要求。 水质 化学需氧量的测定(GB 11914--89) 1 应用范围 本标准适用于各种类型的含COD 值大于30mg/L 的水样,对未经稀释的水样的测定上限为700mg/L 。 本标准不适用于含氯化物浓度大于1000mg/L 的水样。 2 试剂配制 2.1 蒸馏水或同等纯度的水 2.2 硫酸银(Ag 2SO 4),分析纯 2.3 硫酸汞(HgSO 4),分析纯 2.4 硫酸(H 2SO 4),密度为1.84g/cm 3 2.5 硫酸银—硫酸:向500mL 硫酸中加入5g 硫酸银,放置1-2天使之溶解,并混匀,使用 前小心摇动。 2.6 重铬酸钾标准溶液C (6 1K 2Cr 2O 7)= 0.250mol/L :将12.258g 在105℃干燥2h 后的重铬酸钾溶于水中,稀释至1000mL 。 2.7 硫酸亚铁铵标准滴定溶液C[(NH 4)2Fe(SO 4)2·6H 2O] ≈ 0.10mol/L :溶解39g 硫酸亚铁 铵[(NH 4)2Fe(SO 4)2·6H 2O]于水中,加入20mL 硫酸,待其溶液冷却后稀释至1000mL 。 2.8 邻苯二甲酸氢钾标准溶液500mg/L :称取105℃时干燥2h 的邻苯二甲酸氢钾0.4251g 溶于水,并稀释至1000mL ,混匀。 2.9 1,10—菲啰啉指示剂溶液:溶解0.7g 七水合硫酸亚铁(FeSO 4·7H 2O )于50mL 水中, 加入1.5g 1,10—菲啰啉,搅动至溶解,加水稀释至100mL 。 3 试剂标定 3.1 硫酸亚铁铵标准滴定溶液C[(NH 4)2Fe(SO 4)2·6H 2O] ≈ 0.10mol/L 标定:每日临用前, 必须用重铬酸钾标准溶液准确标定此溶液的浓度。取10mL 重铬酸钾标准溶液置于 250mL 三角烧瓶中,用水稀释至约100mL ,加入30mL 硫酸,混匀,冷却后,加3滴1,10— 菲啰啉指示剂溶液,用硫酸亚铁铵标准滴定溶液滴定至溶液的颜色由黄色经蓝绿色变 为红褐色,即为终点。记录下硫酸亚铁铵的消耗量。 C[(NH 4)2Fe(SO 4)2·6H 2O] = V 50.2 式中:V ------ 滴定时消耗硫酸亚铁铵的毫升数。 3.2 重铬酸钾标准溶液C (6 1K 2Cr 2O 7)= 0.250mol/L 纯度及操作步骤检验:按操作步骤分 总氮 1.方法:碱性过硫酸钾消解紫外分光光度法 总磷 1.方法:钼酸铵分光光度法 化学需氧量(COD) 1.方法: 1.1.重铬酸盐法(重铬酸钾法):---国标 本方法适用于各种类型的含COD 值大于30mg/L 的水样,对未经稀释的水样的测定上限为700mg/L。 本方法不适用于含氯化物浓度大于1000mg/L(稀释后)的含盐水。 1.2. 密封催化消解法: 本方法可以测定地表水生活污水工业废水(包括高盐废水)的化学需氧量水样。因其 化学需氧量值有高有低,因此在消解时应选择不同浓度的重铬酸钾消解液进行消解。请参考下表选择消解液: 1.3. 催化快速法: 本方法适用于焦化,造纸,石化,化工,印染,皮毛,制革,酿造,试剂,冶金,木材,加工,日化,助剂,制药,化肥及食品加工等多种工业废水中化学需氧量的测定。 当使用30mm光程比色皿时不经稀释的废水COD值测定范围为60~1000 mg/L。 氯离子浓度高于900mg/L干扰测定。故在消化水样前加入硫酸汞,使其与氯形成络合物以消除干扰。氯离子高于900mg/L的水样,应先做定量稀释,使Cl-含量降至900mg/L以下再行测定。 五日生化需氧量(BOD5) 1.方法:稀释与接种法: 本方法适用于BOD5 大于或等于2mg/L 并且不超过6000mg/L 的水样。BOD5大于 6000mg/L 的水样仍可用本方法,但由于稀释会造成误差,有必要要求对测定结果做慎重的说明。 溶解氧(DO) 1.方法: 1.1.碘量法: 碘量法是测定水中溶解氧的基准方法。在没有干扰的情况下,此方法适用于各种溶解氧浓度大于0.2mg/L 和小于氧的饱和浓度两倍(约20mg/L)的水样。易氧化的有机物,如丹宁酸,腐植酸和木质素等会对测定产生干扰。可氧化的硫的化合物,如硫化物硫脲,也如同易于消耗氧的呼吸系统那样产生干扰。当含有这类物质时宜采用电化学探头法。 水质总碱度检测方法 1.目的 本方法规定了用酸式滴定法测定工厂生产用水及生活饮用水的总碱度。 2.范围 适用于工厂所有生产用水及生活饮用水。 3.原理 碱度是水介质与氢离子反应的定量能力,通过用强酸标准溶液将一定体积的水样滴定至pH 值为所测得的碱度称为总碱度.测定结果用相当于碳酸钙的质量浓度,mg/L 为单位表示。 5.试剂 5.1. L 甲基橙指示剂:称取甲基橙溶于,70℃的纯水中冷却定容至100ml 。此试剂贮 存于棕色玻璃瓶中,有效期3个月 5.2. L 盐酸标准溶液:吸取盐酸(ρ20=mL ),稀释至1000mL 。此试剂贮存于玻璃瓶 中,有效期2个月。按下述方法标定: 5.3. 称取在2500 C 烘箱中烘干过的无水碳酸钠~克于250mL 锥形瓶中,加50mL 纯水溶解,加4滴甲基橙指示剂,用配制的盐酸溶液滴定至溶液由黄色突变为橙色。同时做空白试验。 计算公式:c(HCl)= 0()0.05299 m V V -? 式中:c(HCl)—盐酸标准溶液的浓度,mol/L ; m —碳酸钠的质量,g ; V —滴定碳酸钠所消耗盐酸标准溶液的体积,mL ; Vo —空白试验消耗盐酸标准溶液的体积,mL 。 —与盐酸标准溶液[c(HCl)=L]相当的以克表示的碳酸钠的质量。 6.仪器 6.1. 酸式滴定管 6.2. 移液管 6.3. 250mL 锥形瓶 7.操作规程 7.1. 吸取水样于250mL 锥形瓶中,加4滴甲基橙指示剂,用盐酸标准溶液滴定至试 液由黄色突变为橙色。 8.计算公式: ρ(CaCO3)= 1()50.041000c HCl V V ??? 式中:ρ(CaCO3) —水样的总碱度,mg/L ; c(HCl)—盐酸标准溶液的的浓度,mol/L ; V 1—滴定水样消耗标准盐酸溶液的体积,mL ; V —所取水样的体积,mL ; —与氢氧化钠标准溶液[c(NaOH)=L]相当的以克表示的总碱度(CaCO3) 的质量。水质检测方法
实验室水质检测方法汇总
河流断面水质自动监测站方案(常规参数)20150707
水质检测标准、检测方法
水质检测方法汇总
水质在线监测仪器发展现状(DOC)
生活饮用水检测标准
水质在线监测系统
水质检测方法
生活饮用水标准检验方法
水质检验方法
(完整word版)铅水质自动在线监测仪技术要求和检测方法作业指导书
养殖水质检测常用的方法有哪些
水质检测的标准和方法
水质在线检测教程
水质分析方法国家标准汇总
水质在线自动监测管理汇总
水质检测方法总结(1)
常用水质检测方法
水质总碱度检测方法