
分液漏斗的分类及试用方法(附萃取操作) 一、分液漏斗分为:球形分液漏斗(如图1a)、梨形分液漏斗(如图1b)、梨形刻度分液漏斗(如图1c)(一般:上面的塞子称为活塞,下面颈脖子上的塞子称为旋塞) 图1a 图1b
图1c 二、分液漏斗用于气体发生器中控制加液,也常用于互不相溶的几种液体的分离。 梨形分液漏斗多用于分液操作使用,球形分液漏斗多用于滴加反应液使用。 三、使用注意事项 1、球形分液漏斗的使用注意事项: 1) 使用前玻璃活塞应涂薄层凡士林,但不可大多,以免阻塞流液孔。使用时, 左手虎口顶住漏斗球,用姆指食指转动活塞控制加液。此时玻璃活塞的小槽要与漏斗口侧面小孔对齐相通,才便加液顺利进行。 2) 作加液器时,漏斗下端不能浸入液面下。 3) 无论选用何种形状的分液漏斗,加入全部液体的总体积不得超过其容量的 3/4。 2、梨形分液漏斗的使用注意事项: ①检查分液漏斗是否漏水; ②混合液体倒入分液漏斗,将分液漏斗置于铁圈上静置
③打开分液漏斗活塞,再打开旋塞,使下层液体(水)从分液漏斗下端放出,待油水界面与旋塞上口相切即可关闭旋塞; ④把上层液体(油)从分液漏斗上口倒出。 注意:若用梨形分液漏斗进行萃取操作:振荡时,活塞的小槽应与漏斗口侧面小孔错位封闭塞紧。分液时,下层液体从漏斗颈流出,上层液体要从漏斗口倾出。 注意:分液漏斗洗干净后把塞子拿出来,不要插在分液漏斗里面,尤其是要进烘箱前;长期不用分液漏斗时,应在活塞面加夹一纸条防止粘连。并用一橡筋套住活塞,以免失落。 四、安装 盛有液体的分液漏斗,应妥善放置,否则玻塞及活塞易脱落,倾洒液体,造成不应有的损失。正确的支架方法通常有两种:一种是将其放在用石棉绳或塑料膜缠扎好的铁环上,铁环则牢固地被固定在铁支台的适当高度(见图2);另一种是在漏斗颈上配一塞子,然后用单爪夹牢固地将其夹住并固定在铁支台的适当高度(见图3)。但不论如何放置,从漏斗口接受放出液体的容器内壁都应贴紧漏斗颈
萃取的方法及注意事项 萃取是从溶液或固体混合物中,用溶剂把所需物质抽提出来的操作。它也可以用来洗去混合物中的少量杂质,因此萃取也是提纯物质的一种方法。 一、对溶液进行萃取 对溶液中的某一成分进行萃取时,萃取溶剂与溶液中原来的溶剂必须是不互溶的。所选用的溶剂还必须对所提取的物质溶解度大,而对其它杂质溶解度较小。萃取溶剂多数为有机溶剂,被萃取的溶液一般都是水溶液。 1.用分液漏斗进行萃取。 分液漏斗是实验室中最常用的萃取仪器。 操作方法: (1)选取大小合适的分液漏斗。所用分液漏斗的容积应为被萃取溶液与萃取溶剂二者体积总和的1.5倍。 给漏斗的活塞涂油,塞好。将分液漏斗安放在漏斗架或铁架台的铁圈上。 (2)将溶液与萃取溶剂从漏斗口注入,塞好漏斗口上的塞子(塞子不能涂油,塞好后应再旋紧一下,以防漏液)。 (3)取下分液漏斗,用右手手掌顶住塞子,手指可捉住漏斗口颈或本身,左手握住漏斗的活塞,使大拇指和食指捏住活塞柄,中指垫在塞座下边,做好旋转活塞的准备。振摇漏斗如图5-37所示。振摇 时,漏斗稍倾斜,漏斗口向下,振摇1~2分钟.可 打开活塞,将蒸汽放出。如此反复操作直至发生 的气体很微弱(即放出的气体压力很少)时,再 剧烈振摇2~3分钟,然后将漏斗放回漏斗架,静置。 (4)待漏斗内液体分成上下两层后,打开塞子,再慢慢旋开活塞将下层液体放出。这种将两种互不相溶的液体进行分离的操作叫分液。分液时,一定要尽可能分离干净。有时在两液界面之间会出现一些絮状物,也应将其放出。然后将上层液从漏斗口倒出。切不可从活塞处放出,以免被残留在漏斗颈上的第一种液体玷污。 (5)重复萃取操作3~5次,直至确定最后一次加入的萃取溶剂里已无所需萃取的物质时为止。
有机化学实验二萃取和洗涤 实验目的: 1、学习萃取法的基本原理和方法; 2、学习分液漏斗的使用方法。 实验原理: 萃取和洗涤是利用物质在不同溶剂中的溶解度不同来进行分离的操作。萃取和洗涤在原理上是一样的,只是目的不同。从混合物中抽取的物质,如果是我们需要的,这种操作叫做萃取或提取;如果是我们不要的,这种操作叫做洗涤。 萃取是利用物质在两种不互溶(或微溶)溶剂中溶解度或分配比的不同 来达到分离、提取或纯化目的的一种操作。 实验仪器及药品: 仪器:分液漏斗、试管 药品:0.01%I2—CCl4溶液、1%KI—H2O溶液 实验操作步骤:(本次实验为间歇多次萃取操作) 一、多次萃取操作步骤及注意事项 1、选择容积较液体体积大一倍以上的分液漏斗,把活塞擦干,在活塞上 均匀涂上一层润滑脂,使润滑脂均匀分布,看上去透明即可。 2、检查分液漏斗的顶塞与活塞处是否渗漏(用水检验),确认不漏水时方可使用。 3、将被萃取液和萃取剂依次从上口倒入漏斗中,塞紧顶塞(顶塞不能涂润滑脂)。 4、取下分液漏斗,并前后振荡,然后再将漏斗放回铁圈中静置。
5、待两层液体完全分开后,打开顶塞,再将下层液体自活塞放出至接受瓶: 6、将所有的萃取液合并,加入过量的干燥剂干燥。 7、然后蒸去溶剂,根据化合物的性质利用蒸馏、重结晶等方法纯化。 本次实验成败关键: 1、分液漏斗的使用方法正确(包括振摇、“放气”、静置、分液等操作) 2、准确判断萃取液与被萃取液的上下层关系 安全事项:CCl4蒸气对人体有伤害,请注意安全。 萃取实验:(用KI—H2O溶液从I2—CCl4溶液中萃取I2) 1、一次萃取 (1)准确量取10ml0.01%的I2—CCl4溶液,放入分液漏斗中,再加入40ml1%KI—H2O溶液进行萃取操作,分去KI—H2O溶液层,取I2—CCl4层3ml于编号为1的试管中备用。 (2)准确量取10ml0.01%的I2—CCl4溶液,放入分液漏斗中,再加入20ml1%KI—H2O溶液进行萃取操作,分去KI—H2O溶液层,取I2—CCl4层3ml于编号为2的试管中备用。 2、多次萃取 取10ml0.01%的I2—CCl4溶液分别每次用20ml1%KI—H2O溶液进行二次萃取操作,分离后,取经二次萃取后的I2—CCl4层3ml于编号为3的试管中备用。 3、完成下列工作 (1)将盛有3ml0.01%的I2—CCl4溶液的试管(编号为4)分别与编号为1、2、3的试管的颜色进行比较,写出结果。 (2)通过比较总结所用萃取剂量、萃取次数与萃取效应的关系。
一、固相萃取基本原理与操作 1、固相萃取吸附剂与目标化合物之间的作用机理 固相萃取主要通过目标物与吸附剂之间的以下作用力来保留/吸附的1)疏水作用力:如C18、C8、Silica、苯基柱等 2)离子交换作用:SAX, SCX,COOH、NH2等 3)物理吸附:Florsil、Alumina等 2、p H值对固相萃取的影响 pH值可以改变目标物/吸附剂的离子化或质子化程度。对于强阳/阴离子交换柱来讲,因为吸附剂本身是完全离子化的状态,目标物必须完全离子化才可以保证其被吸附剂完全吸附保留。而目标物的离子化程度则与pH值有关。如对于弱碱性化合物来讲,其pH值必须小于其pKa值两个单位才可以保证目标物完全离子化,而对于弱酸性化合物,其pH值必须大于其pKa值两个单位才能保证其完全离子化。对于弱阴/阳离子交换柱来讲,必须要保证吸附剂完全离子化才保证目标物的完全吸附,而溶液的pH值必须满足一定的条件才能保证其完全离子化。 3、固相萃取操作步骤及注意事项 针对填料保留机理的不同(填料保留目标化合物或保留杂质),操作稍
有不同。 1)填料保留目标化合物 固相萃取操作一般有四步(见图1): ? 活化---- 除去小柱内的杂质并创造一定的溶剂环境。(注意整个过程不要使小柱干涸) ? 上样---- 将样品用一定的溶剂溶解,转移入柱并使组分保留在柱上。(注意流速不要过快,以1ml/min为宜,最大不超过5ml/min) ? 淋洗---- 最大程度除去干扰物。(建议此过程结束后把小柱完全抽干) ? 洗脱---- 用小体积的溶剂将被测物质洗脱下来并收集。(注意流速不要过快,以1ml/min为宜) 如下图1:
1、有机溶剂。乙醚是最常用的有机溶剂,因为可方便地用旋转蒸发仪将其除去。乙酸乙酯也是很好的溶剂,但是它相对比较难被除去。应该尽量避免使用二氯甲烷,因为二氯甲烷比水重,容易形成难以处理的乳状液和复杂的物质 2、选择分液漏斗的大小。通常选用125mL或250mL的分液漏斗,较大量的反应(1~10g)可以用500mL或1L的分液漏斗。请记住:分液漏斗中要装得下溶剂及洗涤液,两者在漏斗中必须能完全混合。 3、用所选择的有机溶剂稀释初始反应混合物并移入选择好的分液漏斗。大量的原料需要大量的溶剂。常规反应(50~500mg产品)可用25~100mL溶剂来稀释。 4、洗涤有机层以除去杂质。洗涤相的体积通常是有机相体积的1/10~1/2。最好重复洗涤2--3次。酸洗(通常用10%HCl)可以除去胺,碱洗(通常用饱和NaHCO3或10%NaOH)可以除去酸性杂质。大多数情况下,当杂质既非酸性又非碱性时,可用蒸馏水洗涤,以除去各种无机杂质。(注意:在摇动分液漏斗中的混合液体时,记住要经常排气,排气时使分液漏斗上沿口朝下,然后上举,在防护罩后面打开活塞。这样可以释放在摇动液体时产生的气体压力。此外,在分液漏斗中放出液体之前,记住首先应打开盖子。) 5、反向萃取回收损失的产品。如果你的产物有水溶性(含有几个极性基团),你可能需要用乙醚或乙酸乙酯反向萃取水层,以避免过多产物流失在水相中。可以使用TLC检测是否所有产物已经从水相中被萃取出。 6、在结束阶段进行盐洗(饱和NaCl溶液)此操作有利于干扰乳化,并且可以除去溶于有机相中的水,起到“干燥”有机层的作用。 7、干燥有机层。将有机溶液和水相分离之后,在有机相中加入干燥剂以除去微量的水。通常用高效快速的MgSO4,但MgSO4有轻微的酸性;或用Na2SO4,它的干燥速度稍慢,效率较低,但Na2SO4为中性。这些化合物可以和残留在有机溶液中的水结合,作用后形成团块。加入的干燥剂要适量,只要有一些干燥剂不再结块,说明可以不用再加入干燥剂了。8、在干燥有机相时,可以准备抽滤装置。选择合适的抽滤瓶和布氏漏斗,剪好两张和布氏漏斗一样大小的干净滤纸(一般垫两张,防止抽破,滤纸一般比漏斗口径稍微小一点为最好)。用叠好的滤纸和布氏漏斗将溶液抽滤到抽滤瓶中(注意布氏漏斗抽滤口朝向以及倒吸等情况)。 9、将抽滤瓶中的液体倒入圆底烧瓶中脱溶。为了防止在旋转蒸发时爆沸,溶液量不要超过圆底烧瓶容量的一半。 10 、旋转蒸发浓缩溶液。然后将产物溶解在少量溶剂中,并将其转入一个稍小的已知重量的圆底烧瓶中。 11、再次旋转蒸发浓缩溶液。通过浓缩、加入二氯甲烷,然后重复几次操作,高沸点的溶剂可被有效地除去。 12、用真空泵除去残留的溶剂。对于非挥发性的化合物,可以用真空泵高效地除去残留的溶剂。这儿有一个加快此过程的窍门:排空圆底烧瓶,充入氮气,重复此过程,然后用真空泵抽30分钟。如果你的产物是挥发性的(低分子量和/或低沸点),应该用旋转蒸发仪而不是真空泵抽至样品恒重。
萃取、反萃取岗位操作规程 一、本岗位的职责范围 1、严格按照岗位规定的工艺参数及技术指标进行操作,以高度责任感保质保量完成生产任务。 2、做到“三勤”即勤观察,勤检查、勤总结、掌握生产规律,作好流量平衡稳定生产。 3、按照设备维护规程和单体设备操作方法作好设备的 操作维护,保养和正常运行处理设备的一般故障,遇到岗位工不能处理的问题时,及时向有关领导(班长或值班长)汇报,以求及时正确处理。 4、做好前后岗位的联系,为下道工序创造良好的条件,紧密协作,共同完成生产任务。 5、搞好岗位范围内的清洁卫生,防止跑、冒、滴、漏,做好安全文明生产。 6、严格遵守劳动纪律和各项规章制度,上班时不得擅自脱岗,睡岗、干私活;不开玩笑,不打闹,养成良好的工作作风 三、本岗位工艺参数及技术指标 1、萃取: A:有机相组成体积比 85%溶剂油+10%P204+5%TBP,重量比:100:12.2:6.1 B:萃原液酸度PH=2.0—2.5 C:流比O/A 1/2—1.5
D:接触相比O/A1.2—1.5 E:接触时间7min F:分层时间:7—10 min G:段数: 7段 H:温度:常温 (2)反萃取 A:反萃取剂:2.8—3.0N B:流比O/A10—15/1 C:接触相比O/A 2/1 D:接触时间:10 min E:段数: 5段 F:温度:17—20℃ (3)再生 A:再生剂:4—5.5N硫酸 B:接触相比1/2 C:温度:40—45℃ D:接触时间:10 min E:段数: 2段 F:分层时间:10 min 四、萃取、反萃取、再生、洗涤开停车顺序: 萃取开车顺序 (一)1、接到开车通知后,做开车前检查。取样分析原液含钒量。 2、检查各阀门是否关闭、管道是否完好。 3、检查回流闸板是否放在最低位置。 (二)、逐级开启萃取、反萃取、再生、洗涤搅拌(1~7),调整接比,防止转相,打开萃取槽余水出口阀门、捕收池余水出口阀门。通知上下工序。。
实验五萃取和洗涤 计划学时:3学时 实验目的: 1、学习萃取法的基本原理和方法; 2、学习分液漏斗的使用方法。 实验原理: 萃取和洗涤是利用物质在不同溶剂中的溶解度不同来进行分离的操作。萃取和洗涤在原理上是一样的,只是目的不同。从混合物中抽取的物质,如果是我们需要的,这种操作叫做萃取或提取;如果是我们不要的,这种操作叫做洗涤。 萃取是利用物质在两种不互溶(或微溶)溶剂中溶解度或分配比的不同来达到分离、提取或纯化目的的一种操作。 将含有机化合物的水溶液用有机溶剂萃取时,有机化合物就在两液相间进行分配。在一定温度下,此有机化合物在有机相中和在水相中的浓度之比为一常数,此即所谓“分配定律”。 假如一物质在两液相A和B中的浓度分别为c A和c B,则在一定温度条件下,c A∕c B=K,K是一常数,成为“分配系数”,它可以近似地看作为此物质在两溶剂中溶解度之比。 设在Vml的水中溶解W o g的有机物,每次用Sml与水不互溶的有机溶剂(有机物在此溶剂中一般比在水中的溶解度大)重复萃取: 第一次萃取: 设V=被萃取溶液的体积(ml),近似看作与A的体积相等(因溶质量不多,可忽略) W o=被萃取溶液中溶质的总含量(g) S=萃取时所用溶剂B的体积(ml) W1=第一次萃取后溶质在溶剂A中的剩余量(g) W2=第二次萃取后溶质在溶剂A中的剩余量(g)
W n =经过n 次萃取后溶质在溶剂A 中的剩余量(g ) 故W o -W 1=第一次萃取后溶质在溶剂B 中的含量(g ) 故W 1-W 2=第二次萃取后溶质在溶剂B 中的含量(g ) 则: 具体实例见P.100-101。 另外一类萃取原理是利用萃取剂能与被萃取物质起化学反应。这种萃取通常用于从化合物中移去少量杂质或分离混合物。常用的这类萃取剂如5%氢氧化钠水溶液,5%或10%的碳酸钠、碳酸氢钠水溶液,稀盐酸、稀硫酸及浓硫酸等。碱性的萃取剂可以从有机相中移出有机酸,或从溶于有机溶剂的有机化合物中除去酸性杂质(使酸性杂质形成钠盐溶于水中);稀盐酸及稀硫酸可从混合物中萃取出有机碱性物质或用于除去碱性杂质;浓硫酸可应用于从饱和烃中除去不饱和烃,从卤代烷中除去醇及醚等。 实验仪器及药品: 仪器:分液漏斗、试管 药品:0.01%I 2—CCl 4溶液、1%KI —H 2O 溶液 实验操作步骤:(本次实验为间歇多次萃取操作) 一、多次萃取操作步骤及注意事项(边示范边讲解) 1、选择容积较液体体积大一倍以上的分液漏斗,把活塞擦干,在活塞上 KV KV + S 当用一定量的溶剂萃取时,总是希望在水中的剩余量越少越好。因为上式中恒小于1,所以n 越大,Wn 就越小,也就是说把溶剂分成几份作多次萃取比用全部量 的溶剂作一次萃取为好。 W 1/V W o W S =K 经整理得:W 1=KV KV + S W o 同理:W 2/V W S =K 经整理得:W 2=KV KV + S W 1W 1W o 经过n 次后的剩余量:Wn=W o n 2
萃取车间操作规程 一、开机前准备工作 1、进入车间前劳保用品要穿戴整齐。 2、检查萃取室内取暖设备运行是否正常。观看并记录温度是否达到25℃以上。 3、检查车间卫生情况,如若地面设备肮脏、工具摆放不整齐,要立刻打扫整理。设备是否溢漏,若溢漏,则即刻通知主任派人修理。 4、对各个储罐体积和水表数据进行登记,并检查再生剂、反萃剂和高压液是否充足。 5、查看上班操作记录和化验结果以便本班进行调整,填写本班操作记录,调整各段变频器参数。 二、开机 1、测水相和有机相进口流速并进行调整;检查每个阀门的开关情况。 2、观察萃取段、洗涤段、反萃段各段有机相多少来决定先开哪一段。为达各段平衡,有机相多的先开。 3、再生、萃取和反萃段先开机器转速控制变频器,调整变频器参数然后立刻打开水相泵开关,观察每个离心萃取器的水相出口,水相流到出口并且每个出口都不夹带有机相后立刻打开有机相开关(再生萃取段大概需要5-10分钟,反萃段需要10-15分钟。以观测为准)。切记:反萃段开机前和有机相流到出口后需要调整该段水相出口开关。 4、洗涤段先开机器转速控制变频器,然后立刻打开有机相开关,观察该段的水相出口,水相出口流量明显变小后立刻打开该段有机相开关(大概需要3-5分钟,以观测为准)。 三、运行 1、各段有机相打开后要不断观察各个离心萃取器的运行状况。 2、运行过程中,观察各个泵的运转情况,是否有阻塞、漏液和杂音;管道是否漏液。检查离心萃取器转速是否正常,是否有杂音发热停止等情况发生;油相和水相分离情况是否完好,是否有堵塞情况发生 3、运行过程中,观察各个聚结器中的油水界面,大概每隔三个半小时把聚集器里的水放一次。反后有机相聚结器中排出的水现在倒掉,以后会倒进反萃剂储槽重新利用;洗后有机相聚结器中排出的水倒进隔壁负载洗水储槽;负载有机相聚结器中排放出的水倒入隔壁高压液储槽。 4、观察再余液、萃余液、负载洗水、高反液储槽中的有机相是否超过100升如超过则将之返回有机相储槽。 四、试剂的配置 1、试剂添加量: 一釜再生剂:25kgNaOH + 50kgNa2CO3 + 493L纯水=0.5m3 反萃剂:3mol/L NH4HCO3 + 1mol/L氨水 2、配反萃剂和再生剂时要先检查配制釜的放料开关是否关闭,然后往配置釜
萃取 也称液—液萃取。指溶于水相的溶质与有机溶剂接触后,经过物理或化学作用,部分或几乎全部转移到有机相的过程。它是一种分离技术,主要用于物质的分离和提纯。这种分离方法具有装置简单、操作容易的特点,既能用来分离、提纯大量的物质,更适合于微量或痕量物质的分离、富集,是分析化学经常使用的分离技术,也广泛用于原子能、冶金、电子、环境保护、生物化学和医药等领域。 萃取 萃取是有机化学实验室中用来提纯和纯化化合物的手段之一。通过萃取,能从固体或液体混合物中提取出所需要的化合物。这里介绍常用的液-液萃取。 基本原理: 利用化合物在两种互不相溶(或微溶)的溶剂中溶解度或分配系数的不同,使化合物从一种溶剂内转移到另外一种溶剂中。经过反复多次萃取,将绝大部分的化合物提取出来。 分配定律是萃取方法理论的主要依据,物质对不同的溶剂有着不同的溶解度。同时,在两种互不相溶的溶剂中,加入某种可溶性的物质时,它能分别溶解于两种溶剂中,实验证明,在一定温度下,该化合物与此两种溶剂不发生分解、电解、缔合和溶剂化等作用时,此化合物在两液层中之比是一个定值。不论所加物质的量是多少,都是如此。用公式表示 。 C A /C B =K C A .C B 分别表示一种化合物在两种互不相溶地溶剂中的摩尔浓度。K是一个常数,称为 “分配系数”。 有机化合物在有机溶剂中一般比在水中溶解度大。用有机溶剂提取溶解于水的化合物是萃取的典型实例。在萃取时,若在水溶液中加入一定量的电解质(如氯化钠),利用“盐析效应”以降低有机物和萃取溶剂在水溶液中的溶解度,常可提高萃取效果。
要把所需要的化合物从溶液中完全萃取出来,通常萃取一次是不够的,必须重复萃取数次。利用分配定律的关系,可以算出经过萃取后化合物的剩余量。 设:V为原溶液的体积 w 为萃取前化合物的总量 w 1 为萃取一次后化合物的剩余量 w 2 为萃取二次后化合物的剩余量 w 3 为萃取n次后化合物的剩余量 S为萃取溶液的体积 经一次萃取,原溶液中该化合物的浓度为w 1 /V;而萃取溶剂中该化合物的浓度为 (w 0-w 1 )/S;两者之比等于K,即: w1/V =K w1=w0 KV (w0-w1)/S KV+S 同理,经二次萃取后,则有 w2/V =K 即 (w1-w2)/S w2=w1KV =w0 KV KV+S KV+S 因此,经n次提取后: w n=w0( KV ) KV+S 当用一定量溶剂时,希望在水中的剩余量越少越好。而上式KV/(KV+S)总是小于1,所以n越大,w n 就越小。也就是说把溶剂分成数次作多次萃取比用全部量的溶剂作一次萃取为好。但应该注意,上面的公式适用于几乎和水不相溶地溶剂,例如苯,四氯化碳等。而与水有少量互溶地溶剂乙醚等,上面公式只是近似的。但还是可以定性地指出预期的结果。
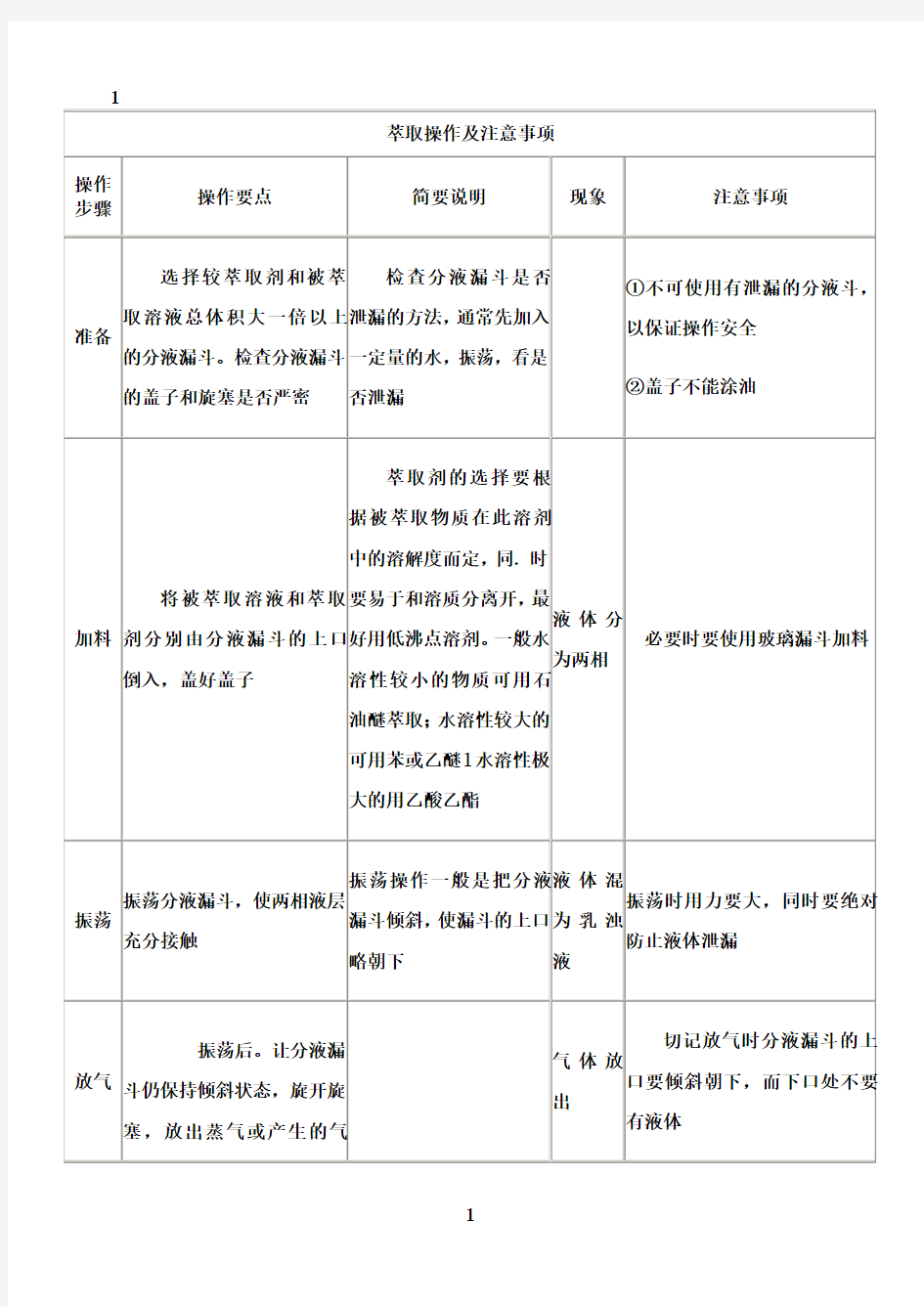
萃取操作及注意事项 操作 步骤 操作要点简要说明现象注意事项 准备 选择较萃取剂和被萃 取溶液总体积大一倍以 上的分液漏斗。检查分 液漏斗的盖子和旋塞是 否严密 检查分液漏斗是否泄 漏的方法,通常先加入 一定量的水,振荡,看 是否泄漏 ①不可使用有泄漏的分液斗,以 保证操作安全 ②盖子不能涂油 加料将被萃取溶液和萃取剂 分别由分液漏斗的上口 倒入,盖好盖子 萃取剂的选择要根据萃 取物质在此溶剂中的溶 解度而定,同时要易于 和溶质分离开,最好用 低沸点溶剂。一般水溶 性较小的物质可用石油 醚萃取;水溶性较大的 可用苯或乙醚l水溶性 极大的用乙酸乙酯 液体分 为两相 必要时要使用玻璃漏斗加料 振荡振荡分液漏斗,使两相 液层充分接触 振荡操作一般是把分液 漏斗倾斜,使漏斗的上 口略朝下 液体混为 乳浊液 振荡时用力要大,同时要绝对防止 液体泄漏 振荡后。让分液漏斗仍气体放出切记放气时分液漏斗的上口要倾
放气保持倾斜状态,旋开旋 塞,放出蒸气或产生的 气体,使内外压力平衡 斜朝下,而下口处不要有液体 重复 振荡再振荡和放气数次 操作和现象均与振荡和放气相同 静置将分液漏斗放在铁环 中,静置 静置的目的是使不稳定 的乳浊液分层。一般情 况须静置10min左右,较 难分层者须更长时间静 置 液体分为 清晰的两 层 在萃取时。特别是当溶液呈碱性 时,常常会产生乳化现象,影响分 离。破坏乳化的方法有: ①较长时间静置, ②轻轻地旋摇漏斗,加速分层 ⑧若因两种溶剂(水与有机溶 剂)部分互溶而发生乳化,可以加 入少量电解质(如氯化钠),利用盐 析作用加以破坏I若因两相密度差 小发生乳化,也可以加入电解质, 以增大水相的密度 ④若因溶液呈碱性而产生乳化, 常可加入少量的稀盐酸或采用过 滤等方法消除.根据不同情况,还 可以加入乙醇、磺化蓖麻油等消除 乳化 分离液体分成清晰的两层 后,就可进行分离。分 离液层时,下层液体应 经旋塞放出,上层液体 如果上层液体也从旋塞 放出,则漏斗旋塞下面 颈都所附着的残液就会 把上层液体沾污 液体分为 两部分