
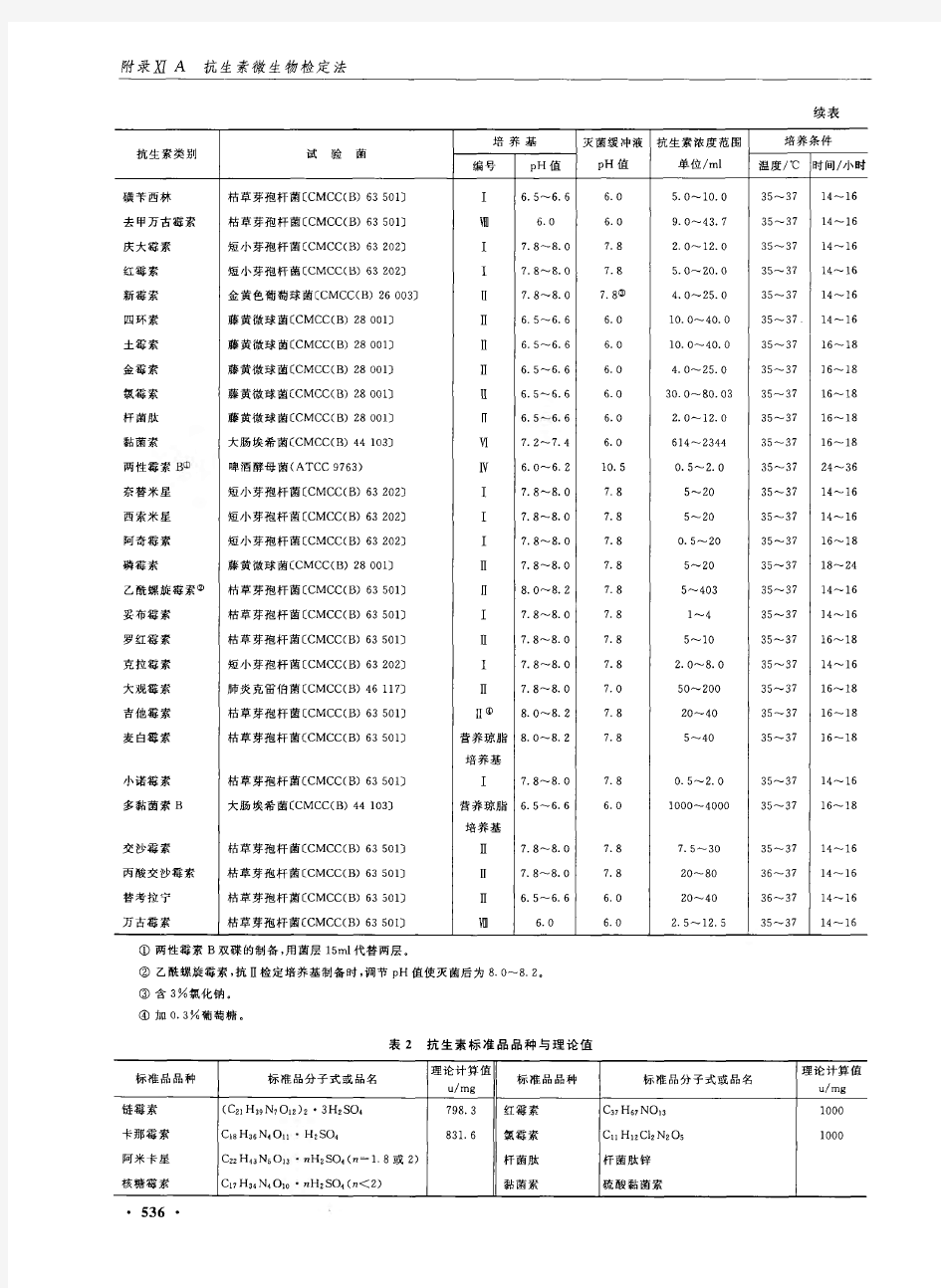
发布日 20070423 期 栏目 化药药物评价>>化药质量控制 标题 抗生素微生物检定方法学验证中的常见问题分析 作者 审评三部 部门 正文容 审评三部审评五室英 摘要:本文对抗生素微生物检定法中的管碟法在方法学验证中的常见问题如线性与围中溶液 浓度与直径的关系、精密度的测定方法等进行了分析,归纳其错误的问题,给出了正确的操作方法。 关键词:抗生素微生物检定法多组分抗生素方法学验证 抗生素微生物检定法是国际上通用的、经典的抗生素测定方法。自20世纪40年代建立至今,在各国药典中被普遍采用。虽然伴随着HPLC等化学分析技术的发展,一些抗生素品种的效价已被化学分析法所取代,但由于①微生物检定法可直观、特异地反映出抗生素品种的抗菌活性; ②多组分抗生素由于结构与不同活性组分生物活性的差异,化学测定结果难以准确表征组分组 成、含量和生物活性间的关系;③许多抗生素品种由于各种原因如无特征紫外吸收等,目前没有适当的化学分析方法表征其活性,故抗生素微生物检定法目前在各国药典中仍占有重要的地位,且短期化学分析法不可能完全取代微生物检定法。中国药典2005年版仍采用抗生素微生物检定法中的管碟法测定其效价,目前申报已有国家标准的该类制剂较多,在质量研究中存在诸多问题,现就常见的问题加以分析,希望对注册申请人有所帮助。 一、方法的建立 1、供试品与标准品的同质性抗生素微生物检定法的原理以供试品与标准品同质为前提,方
法建立前,首先应确定供试品与标准品是否同质,包括化学结构、所含组分及组分比例的一致性,对于制剂还要考虑辅料的影响是否造成供试品与标准品不同质。 2、培养基、试验菌、缓冲液和培养条件的选择 可参照中国药典建立,在此不再赘述。 3、检定方法的确定 可采用一剂量法(标准曲线法)、二剂量法及三剂量法等。一般确定线性与围采用一剂量法(标准曲线法),常规含量测定采用二剂量法,标准品标定采用三剂量法。 4、抗生素溶液的稳定性 选定的品种可参照中国药典现行版附录抗生素微生物检定法的品种,若溶剂和缓冲液与其不同,应考察抗生素储备溶液和测定溶液在室温、40℃和不同pH值缓冲液中,以及放置不同时间的稳定性,以确定抗生素储备溶液和测定溶液的存放时间和条 件。 二、方法的验证 验证的目的是证明采用的方法适合于检测的要求。 验证容有:准确度、精密度(包括重复性、中间精密度)、专属性、适用性和线性。 在申报资料中常见的错误有:线性测定不符合抗生素微生物检定法一剂量中心浓度等比测定的原理;精密度的测定方法不正确;无专属性试验。下面就方法验证的容与常见的错误加以简述。 1、专属性考察杂质、辅料等对测定结果准确性的影响,可通过以下试验验证: (1) 用辅料等替代抗生素进行试验,应不产生抑菌作用。 (2) 采用回收率试验进行验证,至少有9对以上数据,并进行显著性检验。
抗生素生物毒性及对环境的影响 毛瑞祥,张贝贝,武文权,乔鑫 指导老师:张纪亮 概要:在过去三年来,受关注的化学污染物已几乎完全侧重于传统的“优先”的污染物,特别是急性毒性/致癌性农药和能在环境中持续留存的工业中间体。然而,这个范围的化学物质只是较大的“整体”的风险评估中的一部分。另一类不同的生物活性化学物质抗生素被收到相对较少的关注,不过他们确实潜在的环境污染物,这类化学物质包括抗生素和个人护理产品中的活性成分,人类和兽医用药,不仅包括处方药和生物制品,也包括诊断剂,食品,香料,防晒剂,及许多其他类似物。这些化合物及其活性代谢产物可以不断地被运送到水生环境。本次调查研究试图综合抗生素环境起源,分布和发生方面的文献,以影响和促进其在环境科学界的更集中讨论。关键词:毒性残留环境处理抗生素促进更集中讨论 The biological toxicity of antibiotics and its effect on Environment Mao Rui-xiang , Zhang Bei-bei , Wu Wen-quan , Qiao xin Supervisor:Zhang Ji-liang Abstract:During the last three decades, the impact of chemical pollution has focused almost exclusively on the conventional "priority" pollutants, especially those acutely toxic/carcinogenic pesticides and industrial intermediates displaying persistence in the environment. This spectrum of chemicals, however, is only one piece of the larger puzzle in "holistic" risk assessment. Another diverse group of bioactive chemicals receiving comparatively little attention as potential environmental pollutants includes the pharmaceuticals and active ingredients in personal care products (in this review collectively termed PPCPs), both human and veterinary, including not just prescription drugs and biologics, but also diagnostic agents, "nutraceuticals," fragrances, sun-screen agents, and numerous others. These compounds and their bioactive metabolites can be continually introduced to the aquatic environment as complex mixtures via a number of routes but primarily by both untreated and treated sewage.This review attempts to synthesize the literature on environmental origin, distribution/occurrence, and effects and to catalyze a more focused discussion in the environmental science community. Keywords:Toxic residues Environment treatment antibiotic more focused discussion 内容 抗生素是一类广泛应用于防治人类、禽畜及水产养殖中各种细菌感染疾病的化合物。近年来,抗生素的种类、产量与用量不断增加,加上药品管理的混乱和药物的滥用问题非常严重,从而导致了人体以及环境中细菌耐药性的不断增强。国际环境科学界乃至公众已开始广泛关注河流、湖泊等水环境中药物污染及其潜在的危害性。 抗生素是指由细菌、霉菌或其它微生物在生活过程中所产生的具有抗病原体或其它活性的一类物质,广泛用于人体医药卫生和畜禽养殖疾病的预防和控制. 据统计,我国兽用抗生素平均年使用量约为6 000 t[1],按
QCA/QC-SOP-006 1.主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2.引用标准 《中国药典》2010年版二部。 3.术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生 素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4.操作技术(仪器与用具) 4.1操作室:光线明亮,操作间分a.一般操作间b半无菌操作间。室温控制20-25℃。注 意抗生素的污染。 4.2双蝶:内径90mm高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁液 中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4钢管:内径6.0±0.1mm高7.8±0.1mm或8.0±0.1mm,10.0±0.1mm.重量差异不超±0.05g. 用后置1:1000苯扎溴铵溶液内浸泡2h以上,再灭菌洗涤,先用水洗,超声波30min或 用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW冲洗3次150-160℃干热灭菌2小时 备用. 4.5钢管放置器 4.6恒温培养箱:隔水式为宜35-37℃ 4.7灭菌刻度吸管:用于吸取菌液及培养基(5ml、20ml),用后立即置5%石碳酸或1:1000 苯扎溴铵溶液中消毒后再常规洗涤.150-160℃干热灭菌2小时备用. 4.8玻璃容器:滴定管、移液管、刻度吸管、容量瓶.符合一等品规定用前用清洁液浸泡, 水 洗、PW冲3次
环境因素对微生物生长的影响 ?一、温度的影响 ?1.高温的影响一般来说无芽孢的细菌在水中加热到100℃迅速死亡。?(一)高温杀菌的机理 ?提问:? 1)蛋白质、核酸变性2)细胞膜溶解细胞膜中的脂类在高温作用下溶解,“失血过多”(二)影响高温杀菌的因素 ?细菌的种类、含水量、芽孢有无、以及湿热或干热 1)细菌种类 2)含水量 ?细菌细胞含水量高的更容易被杀死。 分子层次现象——蛋白质的凝固温度与含水量有关,含水量越高,蛋白质凝固温度越低,反之亦然。3)芽孢 4)湿热与干热 湿热—水蒸汽(121℃ 20~30min) 干热—热空气(160~170℃ 2h灭菌) ?提问:?湿热灭菌温度低时间短?保水(热空气蒸发蛋白质水分); ?蒸汽冷凝放热; ?凝水热传导能力强于空气;2.适宜温度 ?提问:为什么会存在适宜温度? ?酶的活性 ?根据细菌适宜温度的不同,可将细菌分为四大类,
?嗜冷菌、嗜中温菌、嗜热菌、嗜超热菌。 ?废水中的细菌一般都是嗜中温菌,最适温度多在30℃左右,嗜冷菌和嗜热菌占少数。 3.低温 ?低温——细胞结冻~最适温度下限 ?进入休眠状态 ?提问:? 酶活性降低,导致代谢、遗传普遍停滞;?膜细胞流动性变差。?一旦获得适宜温度,即可恢复活性 ?提问:细胞内外冻结易导致死亡,原因何在? ?冰渣导致细胞膜破裂,失“血”过多 ?嗜中温菌(耐冷喜温)一般在5℃以下处于休眠状态,因此通常实验室用冰箱的4℃冷藏温度保藏细菌,或甘油、石蜡冷冻保存菌种 ?低温下冷藏的食物变质 ———嗜冷细菌(或霉菌)的最适宜温度在5~15℃之间。 提问:嗜冷细菌的秘密武器是什么??—具备低温活性酶 —细胞质膜含有大量的不饱和脂肪酸,在低温下能保持半流动性,使之能有效地集中必需的营养物质。二、p H的影响 ?大多数细菌最适环境p H为6~8,可生存的p H范围在4~10之间。 ?研究表明细胞内部由于细胞膜的屏蔽作用、磷酸盐缓冲及细菌能动的调节,p H一般都保持中性,环境的p H难以影响细胞内的p H变化。 ?提问:外界的pH变化如何对细菌产生影响? 1.影响细胞膜蛋白及胞外水解酶的活性 ?从而影响营养物的正常吸收与转运 2.影响营养物的解离与吸收 ?主要影响一些极性营养物如脂肪酸、氨基酸
抗生素的生物效价测定法 测定抗生素效价的方法比较多,一般可以分为物理学方法、化学方法、生物学方法、和两种方法配合等四大类,可根据具体情况选择使用。 生物学方法以抗生素的杀菌力作为衡量效价的标准,其原理恰好和临床应用于的要求一致这是它的优点;又其灵敏度较高,需用检品的量较小,也是其它方法所不及的。 抗生素的生物效价测定法,常用的有稀释法、比浊法和扩散法(或称渗透法)。 稀释法这一方法是用培养基将检品抗生素稀释到各种浓度,并依次分装到一系列的容器内,再加入等量“试验菌种”菌种菌液,并放在37 ℃保温箱内培养一定时间,观察何种稀释度适能抑制细菌的生长,该稀释度即为测定终点(或以细菌生长所引起的PH改变及溶血现象等生化反应作为测定终点),再与同样处理的标准抗生素的终点作比较,即可求得检品的效价。这种方法可以使用液体培养基,也可以使用固体培养基。所用的材料及培养基都必须严格无菌,并要注意无菌操作。由于测定终点是以有无细菌生长来判断的,因此所得结果公是一个范围。 比浊法原理及操作大致与稀释法相同。比浊法也是将不同量的检品及标准品分别加入培养基中,观察其对“试验菌种”的效应——即细菌生长所引起的混浊。这一方法和稀释法的区别有二:a.比浊法的稀释间隔的密度比较近,准确度高一些;b.比浊法不以细菌有无生长的区分为终点,而是将标准品浓度和细菌生长所引起的混浊度求得一定的比例,再由检品的细菌生长混浊度推算检品的效价。这一方法易受杂质的影响,并且不适用于有色或混浊的检品。 扩散法使用固体培养基,在培养基凝固以前将“试验菌种”混合进去,在这样备妥的培养表面,可以用种种设计使检品液或含有抗生素的物质与有菌种的培养基接触。经过培育后,由于抗生素向培养基中扩散,凡抑菌浓度所能达到之下细菌不能生长因而形成透明的抑菌范围,此种范围一般都呈圆形,称为“抑菌圈”。扩散法有几种,或中一种叫管碟扩散法(筒称管碟法)为国际上常用的方法,在我国也作为法定的抗生素检定法。 下面我们将详细地讨论管碟法的原理和实验方法。 一、管碟法测定的设计原理及计算方法 管碟法所用的管子系用瓷、铝或玻璃制成,较好的用不锈钢制成,它是内径为6+0.1毫米、外径为8+0.1毫米、高10+0.1毫米的圆筒形管子,管子的重量尽可能相等。 摊布固体培养基的容器可用双碟,亦可用平底下班盘。管子放在混有菌种的固体培养基上时,可用人工放臵,也可用特定的管子放臵器放臵。
微生物综合性实验设计报告化学抑杀菌剂的效果评价
微生物综合性实验设计报告 化学抑杀菌剂的效果评价 一、所选化学试剂的主要性质 试剂性状药理应用备注 头孢霉素白色或类白色的 结晶性粉末;微 臭。在水中略溶, 在乙醇、氯仿、乙 醚中几乎不溶。 1%水溶液pH为 3.5~6。在碱性物 质存在时,游离酸 容易溶解。对金黄色葡萄 球菌、肺炎链球 菌、大肠杆菌、 流感嗜血杆菌 等有抗菌作用。 抑制细胞壁合 成 其游离酸供口服, 用于呼吸道、泌尿 道、皮肤和软组织 等部位的敏感菌感 染,注射剂也用于 败血症和骨感染。 对青霉素过敏或有过敏 体质者及肾功能不全者 慎用。对头孢类抗生素 过敏者禁用;注射剂刺 激性较低,适宜于肌注 应用;可致菌群失调、 维生素缺乏、二重感染 等副作用。干燥、阴凉 处,避免受热。 红霉素白色或类白色的 结晶或粉末;无 臭,味苦;微有引 湿性。在甲醇、乙 醇或丙酮中易溶, 在水中极微溶解。抗菌谱与青霉 素近似,对葡萄 球菌、螺旋杆菌 等有较强的抑 制作用。对支原 体、放线菌、立 克次氏体、衣原 体有抑制作用。 金黄色葡萄球 菌对本品易耐 药。抑制蛋白质 合成 抗菌谱与青霉素相 似,且对支原体, 衣原体,立克次体 等及军团菌有抗菌 作用。 在酸中不稳定,能被胃 酸破坏,抗菌活性随pH 值的升高而增强。与万 古霉素、青霉素、及碳 酸氢钠等混用可产生浑 浊、沉淀或降效。主要 对革兰氏阳性菌具有抗 菌性。细菌的聚核糖体 结合而抑制肽链的延 伸; 磺胺类 复方磺胺甲噁唑白色结晶性粉末, 无臭,味微苦。几 乎不溶于水,溶于 稀盐酸、氢氧化钠 试液或氨试液中。 熔点为 167-171℃。 抗菌谱与SD 相似,但抗菌作 用较强。磺胺药 在体内的代谢 产物乙酰化物 的溶解度低 敏感菌所致肠炎, 支气管炎,中耳炎, 尿路感染等 交叉过敏对一种磺胺 药过敏的患者对其它磺 胺药可能过敏。 穿心莲清热、祛湿、利胆。用于肝胆湿热引起的口苦、肋痛;急性胆囊炎、胆管炎。 黄连素黄连素是一种重要的生物碱,它具有显著的抑菌作用。黄连素能对抗病原微生物,对多种细菌如痢疾杆菌、结核杆菌、肺炎球菌等都有抑制作用,其中对痢疾杆菌作 用最强,常用来治疗细菌性胃肠炎、痢疾等消化道疾病。临床主要用于治疗细菌性 痢疾和肠胃炎,它无抗药性和副作用。 二、所用菌种主要特点
抗生素微生物测定法操作规程 1.目的:建立抗生素微生物测定操作规程,便于操作者正确进行抗生素效价测定。2.适用范围:适用于抗生素的效价测定。 3.责任人:QC质量检验员 4.正文: 4.1 仪器设备与试液: 4.1.1 仪器设备 4.1.1.1 操作室:应在抗生素检定室中进行。 4.1.1.2 超净工作台:(用于菌种的接种或传代) 4.1.1.3 恒温培养箱:隔板上可备有带孔的玻璃板并垫平。 4.1.1.4 电热鼓风干燥箱 4.1.1.5 电热压力蒸汽灭菌器 4.1.1.6 电热恒温水浴锅 4.1.1.7 天平:分析天平,感量0.1mg 4.1.1.8 游标卡尺:精度0.05mm,长度125mm。 4.1.1.9 双碟:为硬质玻璃培养平皿,内径90mm,高16~17mm,碟底厚薄均匀水平,无气泡。 4.1.1.10 陶瓦盖:内径约130mm,外径108mm,平坦,吸水性强。 4.1.1.11 钢管:内径(6.0±0.1)mm 或(7.8±0.1),高(10.0±0.1)mm,每套钢管重量差异不超过±0.05g,内外壁及两端面光滑平坦,管壁厚薄一致。 4.1.1.12 钢管放置器:置于半无菌操作间内,应保持清洁,防止抗生素污染。可定期按钢管放置器操作规程进行消毒。 4.1.1.13 毛细滴管:用玻璃管拉制,管口光滑。 4.1.1.14 称量瓶:25ml、50ml、100ml、200ml、250ml 4.1.1.15 刻度吸管:1ml、2ml、5ml、10ml、20ml 4.1.1.16 移液管2ml、5ml、10ml、20ml 4.1.1.17 其他玻璃仪器 4.1.2 试液: 41.2.1 缓冲液、磷酸盐缓冲液(pH 6.0)、磷酸盐缓冲液(pH 7.8) 4.1.2.2 生理盐水 4.1.2.3 0.1%新洁尔灭 4.1.2.4 5%石炭酸 4.1.2.5 75%乙醇溶液(配制酒精棉球用) 4.1.2.6 3%煤酚皂溶液
兽药抗生素对植物及土壤微生物影响的研究进展 兽药抗生素对植物及土壤微生物影响的研究进展 摘要:基于国内外相关研究,本文概述了兽药抗生素对植物毒理效应和对土壤微生物的干扰作用等相关研究成果,有助于了解抗生素污染对生物安全和粮食生产带来的潜在威胁。 关键词:兽药抗生素;植物;土壤微生物;效应 中图分类号:S859.79 文献标识码:A 文章编号:1674-0432(2013)-01-0173-1 1 兽药市场抗生素销售情况 21世纪以来,随着科技和医疗水平的提高,大量抗生素被广泛投入于人和动物疾病的治疗及预防,这在保障人类健康和促进畜牧业发展方面起了重要作用。据调查,欧盟国家使用的兽药主要是抗生素和杀寄生虫类药物,兽药类抗生素约占所有兽药用量的70%以上。我国是抗生素的生产大国,2003年仅青霉素的产量就达28000t,占世界总产量的60%;土霉素产量为10000t,占世界总产量的65%;多西环素的产量也为世界第一。 2 禽畜抗生素在土壤中的残留状况 兽药抗生素来源畜牧养殖、水产养殖、宠物的排泄物及使用中的损失。研究表明,兽类抗生素药物只有15%可被吸收利用,大约85%未被代谢而以排泄物的形式直接排放至环境中。土壤中抗生素残留水平差异较大,一般在ug/kg和mg/kg等级。Hamscher等研究发现四环素和氯四环素浓度随着土层深度的增加有增加趋势; Martínez-Carballo等研究表明氯四环素在土壤中有较长持久性,在土壤中残留的水平大约为44.1ug/kg~32.3mg/kg。 3 抗生素对作物毒理研究现状 3.1 形态方面 抗生素对于植物的影响,一定程度上取决于植物对于抗生素的吸收,但是不同种类的抗生素在吸收量上有很大的区别。低浓度的土霉素胁迫对拟南芥幼苗的根长和株高显著抑制,但对其幼苗的侧根数量
微生物制药的研究进展 姓名:李青嵘 班级:生工102 学号:1014200044
摘要 本文通过对历史文献的检索,从微生物生产维生素,微生物生产多价不饱和脂肪酸,微生物生产抗生素,微生物生产抗癌物质,微生物生产医用酶制剂等五个方面综述了微生物制药的研究进展。 关键词:微生物,制药,发酵工程 1.前言 随着生物技术的迅猛发展,在医药领域的许多方面取得了巨大的进展.,其中采用微生物制药,具有生产工艺简单,生产成本低廉,产品产量高,产品纯度高,可大规模工业化生产等优势,同样得到了巨大的发展。从传统工艺,如利用发酵工程生产抗生素、酶制剂以及B-胡萝卜素等;到现今的利用转基因技术生产干扰素、胰岛素、生长因子等几十种新药和疫苗。本文着重综述了微生物的发酵工程在医药研究和生产中应用的最近进展,主要包括生产维生素、多价不饱和脂肪酸、抗生素、抗癌物质医用酶制剂等五个方面。 2.研究内容 2.1.微生物生产维生素 维生素是六大生命要素之一, 为整个生命活动所必需。β-胡萝卜素、VC、VE是目前应用最为广泛,效果最为显著的三种维生素,它们的作用分别是:β-胡萝卜素是强力抗氧化剂, 有抑制癌细胞增殖和提高机体免疫力等作用。V C 和V E 均是抗氧化剂, 前者可阻止、破坏自由基形成,还具有激活免疫系统细胞的活力,刺激机体产生干扰素以抵御外来侵染因子。至于VE可产生抗体,增强机体免疫力。目前,上述的“三素”以实现了微生物工业化生产。 目前,β-胡萝卜素主要是由三孢布拉霉菌生产,在1998年,陈涛等[1]已经针对三孢布拉霉菌的特点,优化发酵工艺,在3M3的发酵罐中发酵120h,生产的β-胡萝卜素产量已达到1146.5mg/L。虽然,传统的工艺生产β-胡萝卜素的产量高,生产周期比较短,但是传统的工艺复杂,成本过高,不利于大规模工业化生产。故,目前许多课题组专注于开发新的生产β-胡萝卜素的菌种或改进传统工艺。据近年所发表的期刊文献,目前,采用红酵母发酵生产β-胡萝卜素是一种工艺简单,成本低廉的方法,虽然在产量方面较传统方法的低很多,但是该方法仍具有很大的发展潜力。何海燕等[2]采用粘红酵母R3-35摇瓶发酵84h,生产的β-胡萝
抗生素效价测定操作规 程
1. 主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2. 引用标准 《中国药典》2010年版二部。 3. 术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4. 操作技术(仪器与用具) 4.1 操作室:光线明亮,操作间分 a.一般操作间b 半无菌操作间。室温控制20-25℃。注意抗生素的污染。 4.2 双蝶:内径90mm 高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁 液中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3 陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4 钢管:内径 6.0±0.1mm 高7.8±0.1mm 或8.0±0.1mm,10.0±0.1mm.重量差异不超 ±0.05g.用后置1:1000苯扎溴铵溶液内浸泡2h 以上,再灭菌洗涤,先用水洗,超声波30min 或用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW 冲洗3次150-160℃干热灭菌2小时备用. 4.5 钢管放置器 4.6 恒温培养箱:隔水式为宜35-37℃ 4.7 灭菌刻度吸管:用于吸取菌液及培养基(5ml 、20ml ),用后立即置5%石碳酸或 QCA/QC-SOP-006 山东良福制药有限公司 起草人 日 期 抗生素效价测定操作规程 审核人 日 期 批准人 日 期 第五版 实施日期 总页数 共5页
抗生素微生物检定管碟法在中国药典中的应用及操作要点 录入时间:2010-11-18 10:29:10 来源:青岛海博 抗生素微生物检定法可分为:(1)稀释法;(2)比浊法;(3)琼脂扩散法(管碟法和打孔法)。各国药典通常采用后两种方法测定抗生素的效价。 管碟法:利用抗生素在摊布特定试验菌的固体培养基内成球面形扩散,形成含一定浓度抗生素球形区,抑制了试验菌的繁殖而呈现出透明的抑菌圈。 此法系根据抗生素在一定浓度范围内,对数剂量与抑菌圈直径(面积)呈直线关系而设计,通过检测抗生素对微生物的抑制作用,比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。 原理:利用抗生素在固体培养基中的平面扩散作用,依据量反应平行线原理并采用交叉实验设计方法,在相同实验条件下通过比较标准品(已知效价)和供试品两者对所接种试验菌产生的抑菌圈(直径或面积)大小,来测定供试品效价的一种方法。 管碟法的操作步骤: 1、预试验:确定最佳的试验条件:调整试验菌的浓度、使用量、抗生素终浓度、培养基等,使抑菌圈的大小符合规定:一剂量法中心点的抑菌圈直径应在16~17.5mm,二剂量法高剂量浓度标准品溶液所致的抑菌圈直径在18~22mm,三剂量法中间剂量浓度标准品溶液所致的抑菌圈直径在15~18mm。 2、试验准备:双碟、钢管、毛细滴管、吸管的清洗及灭菌;容量瓶、定量吸管的清洗;培养基、缓冲液的准备、半无菌间的紫外消毒等。 3、双碟的制备:每只双碟加底层培养基约20ml,待培养基凝固后,将双碟放入35~37℃培养箱中,待用。 4、供试品、标准品溶液的制备:估计供试品的效价,根据试验要求设计供试品、标准品溶液稀释步骤,平行制备供试品、标准品相关剂量的溶液。 5、菌层的制备:注意菌层培养基温度;根据预试验确定加入菌层培养基的菌液量,注意制备菌层的速度和平整度。 6、滴加抗生素溶液:注意标准品、供试品高、低剂量溶液滴加顺序,保证滴加速度和加量的均匀一致。 7、双碟的培养:根据培养温度的要求在培养箱中进行培养,培养箱中水平碟放的双碟数以不超过三层
实验九紫外线对微生物生长的影响 抗生素对微生物生长的最低抑制浓度的测定及硫化氢产生实验 杨明轩生物111 1102040128 一、实验目的 1、了解并掌握紫外线和抗生素杀灭微生物细胞的原理。 2、学习和掌握应用紫外线杀菌的实验操作步骤。 3、学习并掌握采用液体培养技术测定药剂对微生物的最低抑制浓度的方法。 4、通过了解不同细菌对含能产硫化氢半固体培养基的分解利用情况,结合实验八的结果,认识微生物代谢类型多样性。 二、实验原理 紫外线是杀菌效率较强的物理因素。其原理是,紫外线可以直接作用于细胞内的DNA分子,使同一DNA 链上相邻的嘧啶形成胸腺嘧啶二聚体,因而导致双链DNA结构发生变化,使DNA的正常复制受到影响,最终导致细胞死亡。紫外线的杀菌效果与照射剂量呈正相关,即紫外灯的功率、照射时间和照射物品距紫外灯的距离等因素都会影响杀菌效果。虽然紫外线具有很好的杀菌效果,但其穿透能力不强,一层黑纸即可阻挡紫外线的通过,因此紫外线常用于室内空气灭菌或器皿的表面灭菌。本实验采用平板法验证紫外线的杀菌作用和不同微生物对紫外线的耐受性。 很多化学药剂都能够抑制微生物的生长。最低抑制浓度(MIC)是指药物抑制微生物生长的最低浓度,由于微生物对药物的耐受性不同,因此最低抑制浓度是有差异的。可以通过液体稀释法来测定最低抑制浓度。将一定培养液中加入不同浓度的药剂,配制成一定浓度梯度,再将制备好的菌悬液按一定体积接种,置一定温度培养后,可通过肉眼或分光光度计测定浊度,以不能生长菌株的试管内药剂的浓度为MIC。 三、实验材料 1、菌种:大肠杆菌(Escherichia coli)、金黄色葡萄球菌(Staphylococcus aureus)、 枯草芽孢杆菌(Bacillus subtilis)、普通变形杆菌(Proteus vulgaris)、 2、培养基:牛肉膏蛋白胨培养基、LB培养基、产硫化氢半固体穿刺培养基; 3、试剂:无菌水、10μg/μl链霉素; 5、仪器:无菌培养皿、无菌试管、刮铲、灭菌黑纸、。 四、实验方法 (1)紫外线对微生物生长的影响 1、将供试菌株接种于LB斜面,置37℃培养过夜。 2、将5ml无菌水分别注入菌种管内,混匀制成均匀的菌悬液,37℃振荡培养过夜。 3、取事先制备的LB平板3个,分别以0.1ml菌悬液涂布一个平板,并做好标记。 4、取一灭菌的剪成五角星形状的黑纸放置在培养皿中央,将培养皿放于紫外灯箱内,打开皿盖,开紫外灯照射15min,盖好培养皿盖后将培养皿取出,注意将培养皿立即倒置于37℃温箱中培养过夜。 5、观察结果平纪录。 (2)抗生素对微生物生长的最低抑制浓度的测定 1、取活化好的菌种斜面,分别挑取一环接种于液体培养基中,在37℃下培养6~8h,作为测试液。 2、按下表配制不同链霉素浓度的培养基并按照顺序加样(每个试管3个重复),全班留一个只含培养基,不接菌也不用药的,做对照。 3、将试管置于37℃温箱培养12~24h,取出试管,充分震荡,用肉眼观察每个试管浊度,用“+”或“-”表示生长与否。也可用分光光度计检测浊度。
实验三抗生素效价的生物测定 一、实验目的 1.熟悉抗生素效价测定的原理 2.掌握培养基的配制、灭菌 3、掌握接种技术 二、实验原理 抗生素的医疗价值决定于它的抗菌特性,因此利用它们各自的抗菌活性来测定其效价有着特殊的意义。效价的测定法有:液体稀释法,比浊法和扩散法等。本实验采用国际上最为常用的杯碟扩散法来定量测定洁霉素的效价。测定时,将规格完全一致的不锈钢小管(即牛津小杯)置于含敏感菌的琼脂平板上,并在牛津小杯中加入己知浓度的标准青霉素溶液和未知浓度的青霉素发酵液。于是,抗生素就自牛津小杯处向平板四周扩散,在抑菌浓度所达范围内敏感菌的生长被抑制而出现抑菌圈。在一定的范围内,抗生素浓度的对数值与抑菌圈直径呈线性关系。因此,只要将被测样品与标准样品抑菌圈直径进行比较,就可在标准曲线上查得未知样品的抗生素效价。 三、材料和器皿 1 菌种:大肠杆菌(E.coli)。 2培养基:牛肉膏蛋白胨琼脂培养基(作生物测定用时,平板应分上下两层,上层须另加25%葡萄糖)。 牛肉膏蛋白胨琼脂培养基配方: 牛肉膏3g 蛋白胨10g Nacl 5g 琼脂15-20g 1000ml 水pH 7.4-7.6 3试剂 (1)l%pH6磷酸缓冲液:K2HPO4 0.2g(或K2HPO4·3H20 0.253g)KH2P040.8g,蒸馏水100ml。 (2)25% 葡萄糖溶液100ml。 (3)苄青霉素钠盐:1667U/mg(1U即1国际单位,等于0.6ug)。 4其他:牛津小杯(不锈钢小管,内径6土0.lmm,外径8土0.lmm,高10土0.1mm),培养皿(直径90mm,深20mm;大小一致,皿底平坦),试管、滴管、移液管(5ml)、移液枪(1ml)、枪头、镊子、涂布棒等。 四、方法和步骤 1标准曲线的测绘 (1)倒底层培养基:取无菌培养皿5套,每皿移入20ml牛肉膏蛋白陈底层琼脂培养基,置水平待凝,备用。
抗生素微生物检定法 --------2017 1 简述 抗生素微生物检定法系在适宜条件下,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效价)的方法。依试验设计原理不同,可分为稀释法、比浊法和琼脂扩散法。后二者被列为抗生素微生物检定的国际通用方法。《中国药典》也采用这两种方法。 抗生素微生物检定管碟测定法系琼脂扩散法,是利用抗生素在摊布特定试验菌的固体培养基内成球面形扩散,形成含一定浓度抗生素球形区,抑制了试验菌的繁殖而呈现出透明的抑菌圈。此法系根据抗生素在一定浓度范围内,对数剂量与抑菌圈直径(面积)呈直线关系而设计,通过检测抗生素对微生物的抑制作用,比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。 抗生素微生物比浊法是将一定量的抗生素加至接种有试验菌的液体培养基内,混匀后,经培养,测量培养基的浊度。此法系根据抗生素在一定的浓度范围内,其浓度或浓度的数学转换值与试验菌生长产生的浊度(浊度与细菌数量、细菌群体质量及细菌细胞容积的增加之间存在直接关系)之间存在线性关系而设计,通过测定培养后细菌浊度值的大小,比较标准品与供试品对试验菌生长抑制的程度,计算出供试品的效价。 抗生素效价以“单位(u)”或“微克(μg)”表示。 抗生素管碟测定法 2 仪器与用具 2.1 操作室光线明亮,操作室应分为两部分,彼此分开,其中一部分为一般操作室,一部分为半无菌操作室。半无菌操作室应设有紫外线灭菌灯,并附设空气净化(空气净化级别为100级~10000级)及空调设备,控制室温在20~25℃之间,达到无菌或半无菌状态。操作台应稳固,台面用玻璃板,并用水平仪调节至水平。注意操作,避免室内抗生素污染。 2.2 双碟内径约90mm , 高16~17mm硬质玻璃或塑料培养平皿,碟底厚薄均匀,水平透明,无色斑气泡。
·综 述· 抗生素对微生物作用的研究* 孙延忠1,2,曾洪梅1**,李国庆2 (1.中国农业科学院植物保护研究所,北京 100094;2.华中农业大学植物保护系,湖北武汉 430070) 摘 要 抗生素能干扰微生物细胞新陈代谢的某个或几个环节(包括代谢物或酶系统),使它不能以正常的代谢途径维持和延续生命活动。分别从抗生素抑制细胞壁合成、影响细胞膜功能、抑制蛋白质合成、影响能量代谢、干扰核酸合成5方面综述了抗生素对微生物的作用。 关键词 抗生素;微生物 中图分类号 Q939.92 文献标识码 A 文章编号 1005-7021(2003)03-0044-04 抗生素(antibiotics)是生物,包括微生物、植物和动物在内,在其生命活动过程中所产生的(或由其它方法获得的),能在低微浓度下有选择地抑制或影响它种生物功能的有机物质[1]。自从青霉素被发现并应用于临床,人们就开始探索抗生素是怎样作用于微生物的。研究表明,有的抗生素能阻断能量供应系统;有的能干扰微生物代谢中间物的合成或聚合过程,引起微生物形态结构的变化,改变遗传信息,从而产生抑制作用。根据抗生素干扰代谢过程的不同,可将抗生素对微生物的作用分为5大类型[1,2]:①抑制细胞壁合成;②影响细胞膜功能;③抑制细胞蛋白质合成;④作用于能量代谢系统;⑤干扰核酸合成。本文主要从以下几方面综述抗生素对微生物的作用。 1 干扰细胞壁的合成 细胞壁的主要作用是保护微生物免受周围环境的机械损伤和渗透压改变的影响。抗生素能抑制微生物细胞壁的合成,使细胞壁变薄或失去完整性,造成细胞膜暴露,最后由于渗透压差导致原生质渗漏[1]。这类抗生素主要引起细菌溶菌及真菌菌丝芽管和菌丝尖端出现膨大。青霉素(Peni-cillin)、多氧霉素(Polyo xin)和尼可霉素(Nikkomycin)等是作用于细胞壁的抗生素,它们都能抑制细胞壁的合成。 青霉素对细胞壁的抑制作用是发生在细胞壁合成后期的转肽过程,主要是抑制肽聚糖复合物的交叉连接,使坚韧的细胞壁无法合成[3](图1)。Park观察到被青霉素抑制的葡萄球菌累积了尿核苷,并能引起细菌形态结构的变化,提出青霉素是细菌细胞壁合成的特异抑制剂的观点[3]。细菌细胞膜上存在青霉素结合蛋白(penicillin binding protein,PBP),该蛋白具有转肽酶和羧肽酶活性,能与青霉素特异性结合而使酶失活,使转肽酶不能催化肽聚糖链间的交联,从而抑制细胞壁的合成[4],结果无壁的细胞在膨压作用下破裂死亡,即出现溶菌现象。青霉素的作用并不限于转肽酶,它对某些细菌的D-丙氨酸羧肽酶以及其它酶也有抑制作用[5]。与青霉素作用类似的还有头孢菌素C类[4](Cephalosporin C),万古霉素(Van-comycin)[6]等 。 图1 青霉素抑制细菌细胞壁的合成 多氧霉素D(Poly oxin D)是作用于真菌细胞壁合成的抗生素(图2)。多氧霉素是由可可链霉菌(Streptomyces cacaoi)产生的一组嘧啶核苷类抗生素,对病原真菌有很强的抑制作用。高浓度的多氧霉素D能抑制敏感真菌分生孢子的萌发,低浓度的多氧霉素D虽不能抑制分生孢子萌发,但能引起分生孢子的芽管或菌丝顶端出现膨大,从而抑制菌丝的进一步生长。实验结果表明,多氧霉素D抑制14C-葡萄糖胺掺入粗糙脉孢菌的几 收稿日期:2002-07-18 作者简介:孙延忠 男,硕士研究生。现从事农用抗生素作用机制的研究。 *国家“九五”科技攻关项目(96-C01-02-02);北京市科技合同项目(H0120100010119)资助 **通讯作者44微生物学杂志2003年5月第23卷第3期 J O URNAL OF M IC R OBIOLOGY M ay2003Vol.23No.3
抗生素微生物检定管碟法 抗生素微生物检定法可分为:(1)稀释法;(2)比浊法;(3)琼脂扩散法(管碟法和打孔法)。各国药典通常采用后两种方法测定抗生素的效价。 管碟法:利用抗生素在摊布特定试验菌的固体培养基内成球面形扩散,形成含一定浓度抗生素球形区,抑制了试验菌的繁殖而呈现出透明的抑菌圈。 此法系根据抗生素在一定浓度范围内,对数剂量与抑菌圈直径(面积)呈直线关系而设计,通过检测抗生素对微生物的抑制作用,比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。 原理:利用抗生素在固体培养基中的平面扩散作用,依据量反应平行线原理并采用交叉实验设计方法,在相同实验条件下通过比较标准品(已知效价)和供试品两者对所接种试验菌产生的抑菌圈(直径或面积)大小,来测定供试品效价的一种方法。 管碟法的操作步骤: 1、预试验:确定最佳的试验条件:调整试验菌的浓度、使用量、抗生素终浓度、培养基等,使抑菌圈的大小符合规定:一剂量法中心点的抑菌圈直径应在16~17.5mm,二剂量法高剂量浓度标准品溶液所致的抑菌圈直径在18~22mm,三剂量法中间剂量浓度标准品溶液所致的抑菌圈直径在15~18mm。 2、试验准备:双碟、钢管、毛细滴管、吸管的清洗及灭菌;容量瓶、定量吸管的清洗;培养基、缓冲液的准备、半无菌间的紫外消毒等。 3、双碟的制备:每只双碟加底层培养基约20ml,待培养基凝固后,将双碟放入35~37℃培养箱中,待用。 4、供试品、标准品溶液的制备:估计供试品的效价,根据试验要求设计供试品、标准品溶液稀释步骤,平行制备供试品、标准品相关剂量的溶液。 5、菌层的制备:注意菌层培养基温度;根据预试验确定加入菌层培养基的菌液量,注意制备菌层的速度和平整度。 6、滴加抗生素溶液:注意标准品、供试品高、低剂量溶液滴加顺序,保证滴加速度和加量的均匀一致。 7、双碟的培养:根据培养温度的要求在培养箱中进行培养,培养箱中水平碟放的双碟数以不超过三层为宜。 8、抑菌圈的测量:抑菌圈测量仪的使用,每组试验双碟应在相同的测量参数下进行测量。手工测量:游标卡尺 9、结果的可靠性检验及效价测定:抑菌圈测量仪提供计算结果或手工计算结果。 操作要点 第一步一般应制成500或1000单位/毫升的溶液,以后逐步稀释至供试浓度的溶液,稀释步骤应为3~4步。 溶解:对于需用乙醇溶解的样品,由于溶解样品时所用乙醇量较大,加灭菌水后溶液放热,因此需充分摇匀后加灭菌水至接近容量瓶刻度,待冷至室温后再稀释至刻度。 标准品溶液与供试品溶液浓度的比值D应控制在±5%以内,以保证两者浓度的偏差在一定范围内。 试验菌的菌龄对抑菌圈有一定影响。故检定时应保持菌种及菌液的新鲜。 一般菌种一月转种一次,冰箱冷藏保存。对易变异的菌株,如藤黄微球菌等在制备菌悬液前进行单菌分离;其他菌株可半年分离一次。 试验菌传代最好不超过5次,以防止菌种老化变异。芽孢杆菌培养物用灭菌水洗下后,应在65℃加热30分钟,使菌体的菌龄一致,用革兰氏染色,应有芽孢85%以上。 加入菌悬液的体积,一般不少于0.3ml,并且不大于上层培养基体积的2%。如果加入菌悬液的体积过小,则在同次实验中,不同次加入菌悬液的体积相差较大,造成实验误差;如果加入菌悬液的体积过大,则会使上层培养基变稀,并且因菌悬液的温度较低,加至培养基中可能造成培养基结块,影响测定结果。对于
QCA/QC-SOP-??? 1.主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2.引用标准 《中国药典》2010年版二部。 3.术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生 素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4.操作技术(仪器与用具) 4.1操作室:光线明亮,操作间分a.一般操作间b半无菌操作间。室温控制20-25℃。注 意抗生素的污染。 4.2双蝶:内径90mm高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁液 中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4钢管:内径6.0±0.1mm高7.8±0.1mm或8.0±0.1mm,10.0±0.1mm.重量差异不超±0.05g. 用后置1:1000苯扎溴铵溶液内浸泡2h以上,再灭菌洗涤,先用水洗,超声波30min或 用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW冲洗3次150-160℃干热灭菌2小时备用. 4.5钢管放置器 4.6恒温培养箱:隔水式为宜35-37℃ 4.7灭菌刻度吸管:用于吸取菌液及培养基(5ml、20ml),用后立即置5%石碳酸或1:1000 苯扎溴铵溶液中消毒后再常规洗涤.150-160℃干热灭菌2小时备用. 4.8玻璃容器:滴定管、移液管、刻度吸管、容量瓶.符合一等品规定用前用清洁液浸泡, 水 洗、PW冲3次
抗生素微生物检定标准操作规程 1 简述 抗生素微生物检定法系在适宜条件下,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效价)的方法。依试验设计原理不同,可分为稀释法、比浊法和琼脂扩散法。后二者被列为抗生素微生物检定的国际通用方法。中国药典也采用这两种方法。 抗生素微生物检定管碟测定法系琼脂扩散法,是利用抗生素在摊布特定试验菌的固体培养基内成球面形扩散,形成含一定浓度抗生素球形区,抑制了试验菌的繁殖而呈现出透明的抑菌圈。此法系根据抗生素在一定浓度范围内,对数剂量与抑菌圈直径(面积)呈直线关系而设计,通过检测抗生素对微生物的抑制作用,比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。 抗生素微生物比浊法是将一定量的抗生素加至接种有试验菌的液体培养基内,混均后,经培养,测量培养基浊度。此法系根据抗生素在一定的浓度范围内,其浓度或浓度的数学转换值与试验菌生长产生的浊度(浊度与细菌群体质量及细菌细胞容积的增加之间存在直接关系)之间存在线性关系而设计,通过测定培养后细菌浊度值的大小,比较标准品与供试品对试验菌生长抑制的程度,计算出供试品的效价。 抗生素效价以“单位(u)”或“微克(μg)”表示。 抗生素管碟测定法 2 仪器与用具 2.1 操作室光线明亮,操作室应分为两部分,彼此分开,其中一部分为一般操作室,一部分为半无菌操作室。半无菌操作室应设有紫外线灭菌灯,并附设空气净化(空气净化级别为100级~10,000级)
及空调设备,控制室温在20~25℃之间,达到无菌或半无菌状态。操作台应稳固,台面用玻璃板,并用水平仪调节至水平。注意操作,避免室内抗生素污染。 2.2 双碟内径约90mm,高16~17mm硬质玻璃或塑料培养平皿,碟底厚薄均匀,水平透明,无色斑气泡。 碟底平度检查,可将双碟放在水平台上,下垫一张白纸,碟内加水2~3ml,再滴加蓝墨水,观察蓝色深浅是否一致。 用过的双碟经高压灭菌倒出培养基后,置清洗液中浸泡过夜,冲洗,沥干,至150℃~160℃干热灭菌2小时或高压121℃蒸气灭菌30分钟,备用。 2.3 陶瓦盖内径约103mm,外径108mm,平坦,吸水性强,应定期清洗、干燥或干热灭菌。 2.4 钢管内径(6.0±0.1)mm,高(10.0±0.1)mm;外径(8.0±0.1)mm或(7.8±0.1)mm,每套钢管重量差异不超过±0.05g,内外壁及两端面光洁平坦,管壁厚薄一致。每次使用后应置1:1000新洁尔溶液内,浸泡2小时以上,灭菌后再洗涤,先用水洗涤,超声波超声30分钟或用沾有去污粉的纱布条串擦内外壁,水冲洗,沥干,再用蒸馏水冲洗3次后,置带盖的容器内,在150℃~160℃干热灭菌2小时,备用。 2.5 钢管放置器有6孔和4孔两种。放置于无菌或半无菌室的操作平台上,钢管下落时应垂直平稳、位置正确。双碟升降平稳。应保持清洁,防止抗生素污染。可定期用75%乙醇棉擦拭落管筒及储管杯。置钢管的玻璃管应定期干烤灭菌。 2.6 恒温培养箱以隔水式为宜,温度平稳,波动小。设置漂移温度为35~37℃或24~26℃,依各品种要求而定,箱内网状隔板上放置带孔的玻璃板并调整水平。 2.7 灭菌刻度吸管用于吸取菌液及培养基。使用后应立即置5%石