格氏碱中甜菜碱的测定方法 (1)
- 格式:docx
- 大小:22.10 KB
- 文档页数:6
离子色谱测定甜菜碱中的羟基乙酸、一氯乙酸和二氯乙酸甜菜碱可用作营养成分预防一些慢性病[1],也可用作饲料添加剂[2]。
天然甜菜碱已不能满足市场需求;合成甜菜碱因其价格优势市场需求越来越大,但合成甜菜碱中含有羟基乙酸(GL)、一氯乙酸(MCA)和二氯乙酸(DCA)[3]。
这些杂质可能对人体和动物造成危害[4]。
本论文拟建立一种简单快速和具有实用价值的分析方法用于甜菜碱中上述三种主要杂质成分的检测。
实验所用色谱仪为瑞士万通850离子色谱仪,配抑制电导检测器。
色谱柱为瑞士万通Metrohm A supp5 阴离子交换柱(4 mm i.d.×150 mm);流动相为2 mmol/L Na2CO3+2 mmol/L NaHCO3混合水溶液,流动相流速为0.7 mL/min;柱温为30℃;进样量为20 μl。
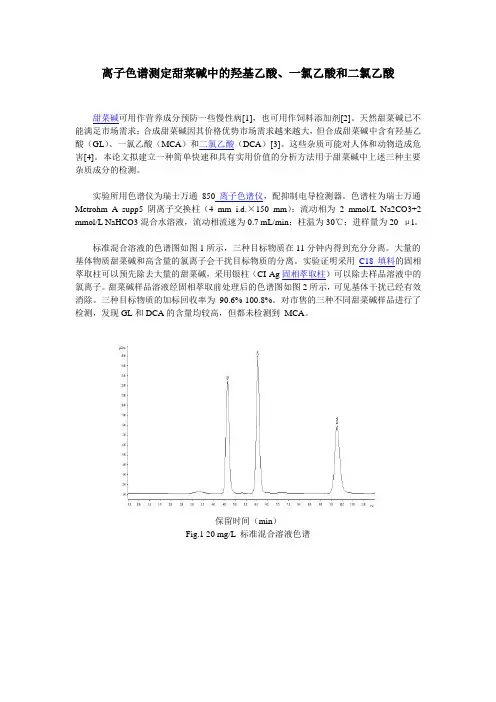
标准混合溶液的色谱图如图1所示,三种目标物质在11分钟内得到充分分离。
大量的基体物质甜菜碱和高含量的氯离子会干扰目标物质的分离。
实验证明采用C18填料的固相萃取柱可以预先除去大量的甜菜碱,采用银柱(CI-Ag固相萃取柱)可以除去样品溶液中的氯离子。
甜菜碱样品溶液经固相萃取前处理后的色谱图如图2所示,可见基体干扰已经有效消除。
三种目标物质的加标回收率为90.6%-100.8%。
对市售的三种不同甜菜碱样品进行了检测,发现GL和DCA的含量均较高,但都未检测到MCA。
保留时间(min)Fig.1 20 mg/L 标准混合溶液色谱保留时间(min)Fig.2 经样品前处理后的甜菜碱样品色谱图参考文献[1] S.A. Craig, Am J Clin Nutr 80 (2004) 539.[2] C.S. Kasper, M.R. White, P.B. Brown, Aquaculture 205 (2002) 119.[3] H.E.Bellis, Process for making aqueous betaine solutions:US, 5696287 [P]. 1997-12-09.[4] P.N. Fitzsimmons, A.D. Hoffman, G.J. Lien, D.E. Hammermeister, J.W. Nichols Aquatic Toxicology, 94 (2009) 186.。

重量法测定甜菜碱和甜菜碱预混剂中甜菜碱含量
胡彩虹;刘波静
【期刊名称】《中国饲料》
【年(卷),期】2002(000)004
【摘要】甜菜碱及其盐酸盐的结构式分别为(CH3)3N+CH2COO-和
(CH3)3NCH2COO@HCl,分子量分别为117 11和153 61.在日粮中添加甜菜碱,能代替蛋氨酸、氯化胆碱,促进生长,提高饲料转化效率;提高胴体瘦肉率,改善肉品品质和风味.市场上销售的甜菜碱有三种:甜菜碱、甜菜碱盐酸盐和甜菜碱预混剂,产品质量参差不齐.目前甜菜碱含量的测定,是执行农业部发布的"甜菜碱盐酸盐产品质量标准"([农牧函1998]13号),该方法是利用甜菜碱为季胺碱的特性,用高氯酸进行滴定.我们在前人研究基础上,建立了重量法测定甜菜碱和甜菜碱预混剂中甜菜碱含量的方法.
【总页数】2页(P27-28)
【作者】胡彩虹;刘波静
【作者单位】浙江大学饲料所;浙江大学饲料所
【正文语种】中文
【中图分类】S816
【相关文献】
1.化学法测定合成甜菜碱中甜菜碱含量 [J], 杨官娥;郑晓敏;杨正平;刘玉明;魏文珑
2.离子色谱法测定甜菜糖蜜中甜菜碱含量的研究 [J], 张玮;李会荣;刘婕
3.比色法测定甜菜碱和甜菜碱预混剂中甜菜碱的含量 [J], 胡彩虹;夏枚生
4.亲水性液相色谱串联质谱法测定红甜菜中甜菜碱含量 [J], 周芹;吴玉梅
5.干旱和NaCl胁迫下梭梭幼苗中甜菜碱含量和甜菜碱醛脱氢酶活性的变化(简报) [J], 陈鹏;潘晓玲
因版权原因,仅展示原文概要,查看原文内容请购买。

中国化工贸易化学合成法制备甜菜碱刘 悦1 闫 皙2(1.河北科技大学化学与制药工程学院,河北石家庄 050018;2.石家庄科英化工技术有限公司,河北石家庄 050018)1课题研究的国内进展及现状甜菜碱最初是甜菜制糖时留下的废液中提取而来的,新鲜甜菜中含甜菜碱,制糖废液中约含3%,糖蜜中含8%。
甜菜碱原为制糖过程中的一个副产品,其产品及产地有很大局限性,使用上也没有得到更加广泛的推广。
长期以来,人们对甜菜碱的研究主要集中在如何从甜菜中提取的工艺研究,规模比较有限,直到十九世纪七十年代,芬兰的CALTER公司才对其进行了专门研究,该公司通过天然提取法制得的天然无水甜菜碱产品质量好,并流入我国市场。
此后,许多国家都对甜菜碱进行了研究,取得了一定进展。
1.1 关于合成方法的研究1999年,苏天铎等人以氯乙酸、氢氧化钠和三甲胺为原料合成 甜菜碱,其方法是:以室温为起始反应温度反应0.5 h,然后分别于50℃~55℃和80℃~85℃反应1 h,以强酸性阳离子交换树脂为反应液分离提纯物质。
其收率超过97%,产品纯度达到98.5%。
该法具有操作简便、反应时间短、反应条件温和、产品纯度高等优点,但离子交换法工艺繁琐,不利于工业推广。
2008年,杨昆等人以三甲胺及一氯乙酸、氢氧化钾为原料合成甜菜碱:利用实验确定合适的反应温度、时间及配比等优化条件,得到的反应液去除水溶剂后加适量乙醇趁热过滤,除去氯化钾,然后,将滤液冷却结晶,抽滤,干燥,得到甜菜碱,产率可达93.4%,纯度达99.33%.该工艺用氢氧化钾代替氢氧化钠,反应过程中生成的副产物氯化钾较氯化钠容易分离,有利于提高产品纯度,但氢氧化钾成本较氢氧化钠要高,会增加其生产成本。
1.2 对甜菜碱分离方法的研究崔国辉利用离子交换法使甜菜碱得到提纯:将反应液利用阳离子强酸性树脂,吸附甜菜碱,杂质用纯水冲走,然后用氨水解析出甜菜碱,甜菜碱溶液减压浓缩后,降温到30℃析出晶体,过滤得到甜菜碱,母液回收套用,得到的甜菜碱再经过真空干燥,得到含量99%以上的甜菜碱。


新版鸡精、鸡粉中谷氨酸钠的测定
作业指导书
O P E R A T I N G I N S T R U C T I O N S
鸡精、鸡粉中谷氨酸钠的测定
编号:XZJY050-00-2019
版本:第一版第0次修改
编制:审核:批准:
实施日期:2019.01.01
一、编制目的
为规范本中心鸡精、鸡粉调味料中谷氨酸钠的检验方法,特编制本指导书。
二、适用范围
鸡精调味料、鸡粉调味料中谷氨酸钠的测定。
三、编制依据
SB/T 10415-2007 《鸡粉调味料》
AB/T 10371-2003 《鸡精调味料》
四、实验原理
利用氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,用氢氧化钠标准溶液滴定后定量,以酸度计测定终点。
五、试剂和材料
5.1试剂
5.1.1 甲醛(36%):应不含有聚合物
5.1.2 氢氧化钠标准滴定溶液[c(NaOH)=0.050mol/L]。
5.2仪器
5.2.1 酸度计
5.2.2 磁力搅拌器
5.2.3 25mL 碱式滴定管
六、实验方法
准确称取均匀样品3g~4g,用适量水溶解,移入100mL容量瓶中,加水至刻度,混匀后吸取10.00mL,置于200mL 的烧杯中,加60mL 水,开动磁力搅拌器,用氢氧化钠标准滴定溶液(0.05mol/L)滴定至酸度计指示pH8.2。
加入10.0mL 甲醛溶液,混匀,再用氢氧化钠标准滴定溶液
1。

HPLC测定甜菜糖蜜中甜菜碱含量谷艾素;刘其波【摘要】目的:建立甜菜碱的高效液相色谱测定法,用于甜菜糖蜜中提取甜菜碱的生产工艺。
方法:采用SCX阳离子交换柱(250mm×4.6mm,5μm),柱温40℃,0.003mol/L磷酸二氢钾溶液为流动相,流速1.0mL/min。
结果:甜菜碱在0~0.290mg/mL质量浓度范围内线性关系良好(r=0.999 9),加标回收率在96.90%~99.56%。
结论:所建方法适用于甜菜糖蜜中提取甜菜碱生产工艺中质量控制。
【期刊名称】《生物化工》【年(卷),期】2017(000)005【总页数】3页(P50-52)【关键词】高效液相色谱;甜菜糖蜜;甜菜碱【作者】谷艾素;刘其波【作者单位】河北玉星生物工程股份有限公司;河北省宁晋县农业局【正文语种】中文【中图分类】O657.72甜菜碱[1](betaine)是一种季铵型生物碱,化学名称为N,N,N-三甲基甘氨酸内盐,其分子内有3个有效甲基,使其成为高效甲基供体。
其化学结构与氨基酸、胆碱相似具有多种生物学功能,参与氨基酸和脂肪的代谢,调节渗透压,具有促进生长等功效,广泛应用于饲料和食品添加剂、发酵行业、日化等领域[2-6]。
甜菜糖蜜是提取天然甜菜碱的主要原料,因此需要对生产过程中提取的甜菜碱进行定量检测,对生产进行指导和控制以保证生产工艺的合理性。
甜菜碱检测方法很多,包括碘量法、核磁共振法[7-8]、质谱法[9-13]、比色法[14-15]、离子色谱直接诱导法等,但这些方法存在很大的缺陷,如灵敏度低、仪器昂贵、操作繁琐等。
本实验拟建立高效液相色谱法(HPLC)检测甜菜糖蜜中甜菜碱的方法,结果表明,方法准确、可靠,解决了灵敏度低和成本高的问题。
甜菜糖蜜、磷酸二氢钾(分析纯)、甜菜碱(对照品)。
岛津LC-10AT vp 型高效液相色谱仪。
对照品溶液:准确称取甜菜碱对照品0.058g,置于100mL容量瓶中,加纯化水溶解并定容至刻度,制备成0.580mg/mL的储备液,甜菜碱标准对照品溶液由此稀释得到。
甜菜碱的制备*孙国建(天津市化学试剂研究所 天津 300240)摘要:本文以一氯乙酸和三甲胺为原料制甜菜碱。
该方法具有操作简单,原料低廉,应用效果显著等特点。
关键词:饲料添加剂;甜菜碱;制备中图分类号:TQ226.26 文献标识码:B 文章编号:1008-1267(2000)02-0018-01 甜菜碱是一种高效的甲级供体,可以在饲料中替代部分蛋氨酸和氯化胆碱,有利于防止因氯化胆碱的氧化反应而破坏饲料中的维生素类。
甜菜碱在生物体内又是一种最有效的渗透溶解剂,有重要的物质代谢作用,同时可以改善饲料的适口性,对水产动物的嗅觉和味觉具有较好的诱惑力,从而提高其采食率,降低饵料系数,促进其生长。
甜菜碱的制备有两种方式,一是由甜菜糖蜜中提取。
二是由一氯乙酸同三甲胺反应而得。
目前市场上销售的产品均为甜菜糖蜜的提取物,因为价格偏高而不利于产品的推广应用,而我们选择了人工合成的方法,使得产品成本下降,有利于其在饲料生产中的广泛应用,具有较重要的社会及经济效益。
1 实验方法将94.5g一氯乙酸溶于200ml水中,加入192.5ml4M氢氧化钠,搅拌升温至35℃,缓慢滴加295ml三甲胺水溶液(含三甲胺59g),滴加完毕后,反应2h,升温至60℃,通入压缩空气维持搅拌2h,再升温至80℃维持2h,冷却至室温,加水稀释至4L,通过装有大孔径离子交换树脂交换柱,得到甜菜碱溶液,减压浓缩,得到黄色晶体,干燥,得产品100g,收率85%,产品含量97%。
2 结果与讨论2.1 反应条件的选择反应时间的长短,对于产品的收率影响较大。
如反应时间较短,则反应不完全,降低产品的收率。
反应温度,无论是加料温度还是反应温度均不可太高。
如果温度过高则会造成三甲胺的流失,从而降低产品的收率。
三甲胺的投料量对于产品的影响不大。
另外,浓缩时需用减压浓缩,而不能直接浓缩,防止溶液过热,造成分解,影响产品的收率及外观,实验结果见表1。
表1 实验结果加料温度(℃)反应温度(℃)反应时间(h)收率(%) 135502842353528533535171435351.579550502762.2 应用效果本产品由天津市饲料科学研究所在鱼饲料中添加0.5%,进行生产性网箱实验,实验证明,鱼体增重率可提高30%左右,节约饲料达25%。


实验六-1 十二烷基二甲基甜菜碱的合成一、实验目的1. 掌握甜菜碱型两性离子表面活性剂的合成原理和合成方法。
2. 了解甜菜碱型两性离子表面活性剂的性质和用途。
3. 学习熔点的测定方法。
二、实验原理十二烷基二甲基甜菜碱是用N,N-二甲基十二烷胺和氯乙酸钠反应合成的,反应方程式为:三、主要仪器和药品电动搅拌器、熔点仪、电热套、四口烧瓶(250ml)、球形冷凝管、玻璃漏斗、温度计;N,N-二甲基-十二烷胺、氯乙酸钠、乙醇、盐酸、乙醚四、实验内容将四口烧瓶、温度计、电动搅拌器、冷凝管组装好,称取10.7gN,N-二甲基十二烷胺,放入四口烧瓶中,再称取5.8g氯乙酸钠和30ml质量分数50%的乙醇溶液,倒入四口烧瓶中,在水浴中加热至60~80℃,并在此温度下回流至反应液变成透明为止。
冷却反应液,在搅拌下滴加浓盐酸,直至出现乳状液不再消失为止,放置过夜。
第二天,十二烷基二甲基甜菜碱盐酸盐结晶析出,过滤。
每次用10ml质量分数为50%乙醇溶液洗涤两次,粗产品用乙醚:乙醇=2:1溶液重结晶,得精制的十二烷基甜菜碱。
用熔点仪测其熔点。
五、注意事项1. 玻璃仪器必须干燥。
2. 滴加浓盐酸至乳状液不再消失即可,不要太多。
3. 洗涤滤波时,溶剂要按规定量加,不能太多。
六、思考题1. 两性表面活性剂有哪几类?它在工业和日化方面有哪些用途?2. 甜菜碱型与氨基酸型两性表面活性剂其性质的最大差别是什么?实验六-2 洗发香波的制备一、实验目的1. 掌握配制洗发香波的工艺。
2. 了解洗发香波中各组分的作用和配方原理。
二、实验原理1. 主要性质和分类洗发香波(shampoo)是洗发用发化妆洗涤用品,是一种以表面活性剂为主要加香产品。
它不但有很好的洗涤作用,而且有良好的化妆效果。
在洗发过程中不但去油垢、去头屑,不损伤头发、不刺激头皮、不脱脂,而且洗后头发光亮、美观、柔软、易梳理。
洗发香波在液体洗涤剂中产量居第三位。
其种类很多,所以其配方和配制工艺也是多种多样的。

枸杞子中甜菜碱含量测定方法的建立和提取方法的优化作者:黄钰馨马玲李苗郑国保马小荣来源:《中国药房》2020年第14期中圖分类号 R927.2 文献标志码 A 文章编号 1001-0408(2020)14-1700-04DOI 10.6039/j.issn.1001-0408.2020.14.07摘要目的:建立枸杞子中甜菜碱的含量测定方法,并优化其提取方法。
方法:采用高效液相色谱法测定枸杞子中甜菜碱的含量,色谱柱为Waters Spherisorb NH2,流动相为乙腈-0.01 mol/L磷酸二氢钾水溶液(75 ∶ 25,V/V),流速为0.7 mL/min,检测波长为195 nm,柱温为30 ℃,进样量为10 μL。
以甜菜碱含量为指标,在单因素试验的基础上,采用L9(34)正交试验设计对枸杞子中甜菜碱超声提取的甲醇体积分数、提取时间、料液比进行筛选并进行验证。
测定10批枸杞子中甜菜碱的含量,并与2015年版《中国药典》收录的薄层色谱法测定结果进行比较。
结果:甜菜碱检测质量浓度的线性范围为2.035~2 035.04 μg/mL(R 2=0.999 3);检测限、定量限分别为0.410、2.051 μg/mL,平均加样回收率为97.41%~98.86%(RSD为0.8%~1.4%,n=3),精密度、重复性、稳定性(24 h)试验的RSD均不大于1.2%。
最优提取方法为料液比1 ∶ 30(g/mL)投料、甲醇超声提取45 min。
3次验证试验所得提取液中甜菜碱的平均含量为2.30%(RSD=0.43%, n=3)。
10批枸杞子中甜菜碱的含量为1.91%~2.55%,与薄层色谱法的测定结果(1.88%~2.60%)无明显差异(相对误差为-1.92%~2.7%)。
结论:成功建立了枸杞子中甜菜碱的含量测定方法,并优化了其提取工艺。
关键词枸杞子;甜菜碱;高效液相色谱法;含量测定;提取方法Establishment of the Content Determination Method of Betaine in Lycium barbarum and Optimization of the Extraction MethodHUANG Yuxin1,MA Ling1,LI Miao2,ZHENG Guobao2,MA Xiaorong1(1. Ningxia Hui Autonomous Region Institute of Drug Control, Yinchuan 750002, China; 2. Agricultural Biotechnology Research Center of Ningxia Academy of Agricultural and Forestry Sciences,Yinchuan 750002, China)ABSTRACT OBJECTIVE: To establish the content determination method of betaine in Lycium barbarum, and to optimize the extraction method. METHODS:HPLC method was used to determine the content of betaine in L. barbarum. The determination was performed on Waters Spherisorb NH2 column with mobile phase consisted of acetonitrile-0.01 mol/L monopotassiun phosphate aqueous solution (75 ∶ 25, V/V) at the flow rate was 0.7 mL/min. The detection wavelength was 195 nm, and column temperature was 30 ℃. The sample size was 10 μL. Using the content of betaine as index, on the basis of single factor tests, L9(34) orthogonal test design were used to select the methanol volume fraction, extraction time and solid-liquid ratio of betaine in L. barbarum by ultrasonic extraction. The contents of betaine in 10 batches L. barbarum were determined, and compared with the results of TLC included in 2015 edition of Chinese Pharmacopeia. RESULTS: The linear range of betaine was 2.035-2 035.04 μg/mL(R2=0.999 3). The limits of detection and quantification were 0.410 μg/mL and 2.051 μg/mL, respectively. The average recovery were 97.41%-98.86% (RSDs were 0.8%-1.4%, n=3). RSDs of precision,reproducibility and stability (24 h) tests were not higher than 1.2%. The optimal extraction method included solid-liquid ration of 1 ∶ 30 (g/mL), ultrasonic extraction with methanol for 45 min. The average content of betaine in the extract from the three validation tests was 2.30%(RSD=0.43%, n=3). The contents of betaine in 10 batches L. barbarum were 1.91%-2.55%,which was no significantly different from the results of TLC (1.88%-2.60%)(RE were -1.92%-2.79%). CONCLUSIONS: The content determination method of betaine in L. barbarum was established successfully, and the extraction process was optinized.KEYWORDS Lycium barbarum; Betaine; HPLC; Content determination; Extraction method枸杞子为茄科植物宁夏枸杞(Lycium barbarum L.)的干燥成熟果实[1],是我国传统中药材,具有治疗糖尿病[2]、保护视网膜[3]、抗氧化[4]等作用。
xx碱中甜菜碱的测定方法
1、原理
凯氏法测定试样中的含氮量,即在催化剂作用下,用硫酸破坏有机物,使含氮物转化成硫酸铵。
加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数
8.396,计算出甜菜碱含量。
2、试剂
2.1硫酸(GB 625):
xx,含量为98%,无氮。
2.2混合催化剂:
0.4g硫酸铜,5个结晶水(GB 665),6g硫酸钾(HG 3—920)或硫酸钠(HG 3—908),均为化学纯,磨碎混匀。
2.3氢氧化钠(GB 629):
xx,40%水溶液(m/V)。
2.4硼酸(GB 628):
xx,2%水溶液(m/V)。
2.5混合指示剂:
甲基红(HG 3—958)
0.1%乙醇溶液,溴甲酚绿(HG 3—1220)
0.5%乙醇溶液,两溶液等体积混合,在阴凉处保存期为三个月。
2.6盐酸标准溶液:
邻苯二甲酸氢钾法标定,按GB 601制备。
2.6.1盐酸标准溶液:
c(HCl)=
0.1mol/L。
8.3mL盐酸(GB 622,分析纯),注入1 000mL蒸馏水中。
2.6.2盐酸标准溶液:
c(HCl)=
0.02mol/L。
1.67mL盐酸(GB 622,分析纯),注入1 000mL蒸馏水中。
2.7蔗糖(HG 3—1001):
分析纯。
2.8硫酸铵(GB 1396):
分析纯,干燥。
2.9硼酸吸收液:1%硼酸水溶液1 000mL,加入
0.1%溴甲酚绿乙醇溶液10mL,
0.1%甲基红乙醇溶液7mL,4%氢氧化钠水溶液
0.5mL,混合,置阴凉处保存期为一个月(全自动程序用)。
3、仪器设备
3.1实验室用样品粉碎机或研钵。
3.2分样筛:
xx
0.45mm(40目)。
3.3分析天平:
感量
0.0001g。
3.4消煮炉或电炉。
3.5滴定管:
酸式,
10、25mL。
3.6xx烧瓶:250mL。
3.7xx蒸馏装置:
半微量水蒸气蒸馏式。
3.8锥形瓶:
150、250mL。
3.9容量瓶:100mL。
3.10消煮管:250mL。
3.11定氮仪:
以xx原理制造的各类型半自动。
4、试样的选取和制备
选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器中,防止试样成分的变化。
5分析步骤
5.1.1试样的消煮
称取试样
0.5~1g(含氮量5~80mg)准确至
0.0002g,放入xx烧瓶中,加入
6.4g混合催化剂,与试样混合均匀,再加入12mL硫酸和2粒玻璃珠,将凯氏烧瓶置于电炉上加热,开始小火,待样品焦化,泡沫消失后,再加强火力(360~410℃)直至呈透明的蓝绿色,然后再继续加热1~2h。
5.1.2氨的蒸馏:
将试样消煮液冷却,加入20mL蒸馏水,转入100mL容量瓶中,冷却后用水稀释至刻度,摇匀,做为试样分解液。
将半微量蒸馏装置的冷凝管末端浸入装有20mL硼酸吸收液和2滴混合指示剂的锥形瓶内。
蒸汽发生器的水中应加入甲基红指示剂数滴,硫酸数滴,在蒸馏过程中保持此液为橙红色,否则需补加硫酸。
准确移取试样分解液10~20mL注入蒸馏装置的反应室中,用少量蒸馏水冲洗进样入口,塞好入口玻璃塞,再加10mL氢氧化钠溶液,小心提起玻璃塞使之流入反应室,将玻璃塞塞好,且在入口处加水密封,防止漏气。
蒸馏4min降下锥形瓶使冷凝管末端离开吸收液面,再蒸馏1min,用蒸馏水冲洗冷凝管末端,洗液均流入锥形瓶内,然后停止蒸馏。
5.1.
2.3蒸馏步骤的检验
精确称取
0.2g硫酸铵,代替试样,按
5.1.2步骤进行操作,测得硫酸铵含氮量为
21.19±
0.2%,否则应检查加碱、蒸馏和滴定各步骤是否正确。
5.1.3滴定用5.1.
2.1或
5.1.
2.2xx蒸馏后的吸收液立即用
0.1mol/L或
0.02mol/L(
4.6.2)盐酸标准溶液滴定,溶液由蓝绿色变成灰红色为终点。
6、空白测定
称取蔗糖
0.5g,代替试样,按第5章进行空白测定,消耗
0.1mol/L盐酸标准溶液的体积不得超过
0.2mL。
消耗
0.02mol/L盐酸标准溶液体积不得超过
0.3mL。
7、分析结果的表述
7.1计算见下式:
粗蛋白质(%)=(V2-V1)·c×
0.0140×
8.396/(m×V'/V)×100
式中:
V2──滴定试样时所需标准酸溶液体积,mL;
V1──滴定空白时所需标准酸溶液体积,mL;
c──盐酸标准溶液浓度,mol/L;
m──试样质量,g;
V──试样分解液总体积,mL;
V──试样分解液蒸馏用体积,mL;
0.0140──与
1.00mL盐酸标准溶液〔c(HCl)=
1.000mol/L〕相当的、以克表示的氮的质量。
8.396──氮换算成甜菜碱的平均系数(甜菜碱中含氮量为
11.91%,则系数换算为)。
7.2重复性
每个试样取两个平行样进行测定,以其算术平均值为结果。
允许相对偏差为1%。