胃息肉的分型
- 格式:doc
- 大小:28.50 KB
- 文档页数:5

肠息肉NICE分型是一种判断肠息肉的情况的分型,根据肠息肉表面颜色、血管形态、腺管开口三方面来区分,可分为3型。
1、NICE1型:周围黏膜色泽相似或略淡,表面没有血管或只有单独的条状血管,腺管口可出现呈黑点或白点状腺管或无法显示,考虑为增生性息肉或无蒂锯齿状腺瘤或息肉;
2、NICE2型:周围黏膜相比呈棕色,在表面可见棕色血管,腺管口呈白色椭圆形、管状或树枝状结构,提示为腺瘤;
3、NICE3型:相比周围黏膜呈深棕色,出现血管明显的扭曲或缺失,腺管口不规则或缺失,考虑为深层黏膜下浸润癌。

息肉分型标准ip息肉是指人体某一部位突出出来的肿块或肉质增生物。
它通常不会引起明显的症状,但有时会导致出血、感染以及不适感。
根据特定的分类标准,医生可以将息肉分为不同的类型。
这些分型标准可以帮助医生确定正确的治疗方法,并评估患者的病情。
1.结构性息肉:结构性息肉通常是指直肠或结肠内突出的肿块。
这些息肉可以分为以下几种类型:-腺瘤性息肉:这是最常见的结构性息肉类型。
腺瘤性息肉通常是良性的,但也可能是癌前病变。
根据其形态和组织学特征,腺瘤性息肉又可以进一步分为腺瘤性息肉、高级腺瘤性息肉和恶性腺瘤性息肉。
-高尔基森恶性息肉:这是一种罕见且具有一定恶性潜力的结构性息肉。
高尔基森恶性息肉通常表现为大型、具有恶性特征的息肉。
-炎症性息肉:这种类型的结构性息肉通常是由炎症或感染引起的。
它们通常是临时的,一旦炎症或感染得到控制,炎症性息肉就会消失。
2.非结构性息肉:非结构性息肉是指其他部位的突出肿块,不限于结肠或直肠。
这些息肉可能由以下几种原因引起:-舌唇瘤:这是一种常见的口腔内非结构性息肉,通常位于舌尖或唇部,由于长期刺激或摩擦引起。
-鼻息肉:这是一种位于鼻腔内的非结构性息肉,通常是由于长期鼻窦炎或鼻粘膜炎症引起的,常伴有鼻塞、嗅觉减退等症状。
-子宫息肉:这是一种生长在子宫内腔的非结构性肿块。
子宫息肉通常是由于子宫内膜增生引起的,可导致异常阴道出血或月经不调。
这些分类标准有助于医生了解息肉的类型,从而确定适当的治疗方法。
对于结构性息肉,腺瘤性息肉是最常见的类型,它通常是良性的,但在某些情况下可能发展成恶性肿瘤。
因此,及早检测和切除腺瘤性息肉对于预防结直肠癌的发生至关重要。
治疗结构性息肉的方法通常包括内窥镜下切除、手术切除以及消化道息肉切除术。
非结构性息肉的治疗方法则取决于它们的位置和恶性潜力。
总之,息肉的分型标准对于指导医生了解和治疗息肉非常重要。
通过了解不同类型的息肉特征,医生可以为患者提供更合适的治疗方案,并在需要时进行进一步的检查和评估。

消化内镜诊断标准分级消化内镜诊断标准分级一、反流性食管炎反流性食管炎分为四个级别:Ⅰa级:正常或有轻微炎症,没有明显的糜烂或溃疡。
Ⅰb级:有少量糜烂或溃疡,但没有融合。
Ⅱ级:有多处糜烂或溃疡,且有融合,但不超过食管周长的75%。
Ⅲ级:糜烂或溃疡广泛,融合超过食管周长的75%。
二、慢性胃炎慢性胃炎分为三种类型:慢性萎缩性胃炎慢性非萎缩性胃炎特殊类型胃炎它们的内镜下表现如下:慢性萎缩性胃炎:黏膜红白相间,白相为主,皱襞变平甚至消失,部分黏膜血管显露,可伴有黏膜颗粒或结节状等表现。
慢性非萎缩性胃炎:黏膜红斑,黏膜出血点或斑块,黏膜粗糙伴或不伴水肿,及充血渗出等基本表现。
特殊类型胃炎的内镜诊断必须结合病因和病理。
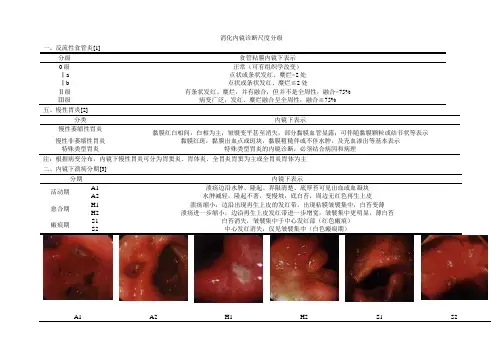
三、内镜下溃疡分期内镜下溃疡分为四个阶段:A1活动期A2愈合期H1瘢痕期H2瘢痕期它们的内镜下表现如下:A1:溃疡边缘水肿、隆起、界限清楚、底厚苔可见出血或血凝块。
A2:水肿减轻,隆起不着,变慢坡,底白苔,周边无红色再生上皮。
H1:溃疡缩小,边缘出现再生上皮的发红带,出现粘膜皱襞集中,白苔变薄。
H2:溃疡进一步缩小,边缘再生上皮发红带进一步增宽,皱襞集中更明显,薄白苔白苔消失,皱襞集中于中心发红部(红色瘢痕)。
S1:中心发红消失,仅见皱襞集中(白色瘢痕期)。
四、胃息肉分类胃息肉分为四个级别:Ⅰ级Ⅱ级Ⅲ级Ⅳ级五、早期食管、胃癌分型早期食管、胃癌分为五个类型:0-Ⅰ型Ⅰ型Ⅱ型Ⅲ型它们的内镜下表现如下:0-Ⅰ型:缓慢坡,界限不清。
Ⅰ型:隆起起始部清楚无细颈。
Ⅱ型:隆起起始部见有细颈但无蒂。
Ⅲ型:明显之蒂。
六、食管、胃进展期胃癌食管、胃进展期胃癌分为五个类型:BorrmannⅠ型BorrmannⅡ型BorrmannⅢ型BorrmannⅣ型BorrmannⅤ型以上都是内镜下消化系统疾病的诊断标准分级,可以帮助医生准确诊断和治疗。

肠息肉nice分型标准
肠息肉的分型标准主要使用了一种称为"NICE"的系统。
这种系统将肠息肉分为以下四类:
1. N型(NICE型):这是最常见的类型,即典型的刺样肿瘤型息肉。
这类息肉通常有典型的息肉形态,并与肠壁相连。
2. I型(Inverted型):这种类型的息肉很少见,呈葡萄糖浆状或扁平状,其肿瘤细胞形态与肠黏膜表面相反,即肿瘤细胞向下增生。
3. C型(Cap型):这种类型的息肉呈圆顶状或扁平状,类似于典型息肉,但其形态不规则,可有凹陷或溃破。
4. E型(Equivalent型):这是一种比较特殊的类型,形态和组织学上与I型和C型息肉相似,但其在肠道内不呈息肉状,而是以弥漫、平坦的方式出现。
NICE分型系统的目的是为医生提供一种标准化的分类方法,以帮助了解肠息肉的病理特征、临床表现和治疗选择。
然而,这个分型系统仍然需要更多的研究来确定其在临床实践中的准确性和应用性。
消化内镜诊断尺度分级一、反流性食管炎[1]分级食管粘膜内镜下表示0级正常(可有组织学改变)Ⅰa点状或条状发红、糜烂<2处Ⅰb点状或条状发红、糜烂≧2处Ⅱ级有条状发红、糜烂,并有融合,但并不是全周性,融合<75%Ⅲ级病变广泛,发红、糜烂融合呈全周性,融合≧75%五、慢性胃炎[2]分类内镜下表示慢性萎缩性胃炎黏膜红白相间,白相为主,皱襞变平甚至消失,部分黏膜血管显露;可伴随黏膜颗粒或结节状等表示慢性非萎缩性胃炎黏膜红斑,黏膜出血点或斑块,黏膜粗糙伴或不伴水肿,及充血渗出等基本表示特殊类型胃炎特殊类型胃炎的内镜诊断,必须结合病因和病理注:根据病变分布,内镜下慢性胃炎可分为胃窦炎、胃体炎、全胃炎胃窦为主或全胃炎胃体为主二、内镜下溃疡分期[3]分期内镜下表示活动期A1溃疡边沿水肿、隆起、界限清楚、底厚苔可见出血或血凝块A2水肿减轻,隆起不著,变慢坡,底白苔,周边无红色再生上皮愈合期H1溃疡缩小,边沿出现再生上皮的发红带,出现粘膜皱襞集中,白苔变薄H2溃疡进一步缩小,边沿再生上皮发红带进一步增宽,皱襞集中更明显,薄白苔瘢痕期S1白苔消失,皱襞集中于中心发红部(红色瘢痕)S2中心发红消失,仅见皱襞集中(白色瘢痕期)A1 A2 H1 H2 S1 S2三、消化性溃疡出血的诊断尺度[4]Forrest分级内镜下表示ⅠⅠa喷射性Ⅰb溃疡底部或周边渗血ⅡⅡa溃疡底血管显露,无活动出血Ⅱb溃疡覆盖血凝块,无活动出血Ⅱc溃疡底呈黑色ⅢⅢ溃疡底清洁ⅠaⅠbⅡaⅡb ⅡcⅢ四、胃息肉分类[5]分级内镜下表示Ⅰ缓慢坡,界限不清Ⅱ隆起起始部清楚无细颈Ⅲ隆起起始部见有细颈但无蒂Ⅳ明显之蒂七、早期食管、胃癌分型[6]分型胃镜下表示0-ⅠⅠ隆起型(息肉型),病变向胃腔内突出,呈息肉状0-Ⅱ平坦隆起及凹陷均欠显著。
此型又可分一下三个亚型Ⅱa表浅隆起型,病灶轻度隆起Ⅱb概况平坦型,病灶凹陷和隆起均不显著Ⅱc浅凹陷型,病灶轻微凹陷,相当于糜烂0-ⅢⅢ深凹陷型,病灶凹陷较显著八、食管、胃进展期胃癌[7]分级内镜下表示BorrmannⅠ型隆起型。

消化内镜诊断标准分级一、反流性食管炎中国消化内镜学会分级标准分级食管粘膜内镜下表现0级正常(可有组织学改变)Ⅰa级点状或条状发红、糜烂<2处,无融合Ⅰb级点状或条状发红、糜烂≧2处,无融合Ⅱ级有条状发红、糜烂,并有融合,但并非全周性,融合<75%Ⅲ级病变广泛,发红、糜烂融合呈全周性,融合≧75%洛杉矶分级标准分级食管粘膜内镜下表现A级一个或一个以上粘膜破损,长径不超过5mm,病灶互相不融合B级一个或一个以上粘膜破损,长径超过5 mm,病灶互相不融合C级粘膜破损有融合,但不超过75%的食管周径D级粘膜破损融合,超过75%的食管周径必须注明:各病变部位(食管上、中、下段) 和长度;若有狭窄注明狭窄直径和长度;Barrett 食管应注明其长度、有无食管裂孔疝。
......感谢聆听二、食管静脉曲张(EV)分级分级EV形态及直径(D)轻度直径小于3mm,直行或轻度迂曲,位于食管下段血管直径3~6 mm,迂曲、隆起或串珠状或结节状,不超过食管中下段中度重试血管直径大于6 mm,阻塞部分管腔,可达食管上段三、慢性胃炎分类内镜下表现慢性萎缩性胃炎黏膜红白相间,白相为主,皱襞变平甚至消失,部分黏膜血管显露;可伴有黏膜颗粒或结节状等表现慢性非萎缩性胃炎黏膜红斑,黏膜出血点或斑块,黏膜粗糙伴或不伴水肿,及充血渗出等基本表现特殊类型胃炎特殊类型胃炎的内镜诊断,必须结合病因和病理注:根据病变分布,内镜下慢性胃炎可分为胃窦炎、胃体炎、全胃炎胃窦为主或全胃炎胃体为主四、内镜下溃疡分期分期内镜下表现活动期A1 溃疡边缘水肿、隆起、界限清楚、底厚苔可见出血或血凝块A2 水肿减轻,隆起不著,变慢坡,底白苔,周边无红色再生上皮愈合期H1 溃疡缩小,边缘出现再生上皮的发红带,出现粘膜皱襞集中,白苔变薄H2 溃疡进一步缩小,边缘再生上皮发红带进一步增宽,皱襞集中更明显,薄白苔瘢痕期S1 白苔消失,皱襞集中于中心发红部(红色瘢痕)S2 中心发红消失,仅见皱襞集中(白色瘢痕期)A1 A2 H1 H2 S1 S2五、消化性溃疡出血的诊断标准Forrest分级内镜下表现再出血风险% ⅠⅠa 喷射性出血55%Ⅰb 溃疡底部或周边活动性渗血55%ⅡⅡa 溃疡底血管显露,无活动出血43%Ⅱb 溃疡覆盖血凝块,无活动出血22%Ⅱc 黑色基底10% ⅢⅢ基底洁净5% 推荐对Forrest分级I a一Ⅱb的出血病变行内镜下止血治疗六、胃息肉分类分级内镜下表现Ⅰ缓慢坡,界限不清Ⅱ隆起起始部清楚无细颈Ⅲ隆起起始部见有细颈但无蒂Ⅳ明显之蒂七、早期食管、胃癌分型[6]分型胃镜下表现0-ⅠⅠ隆起型(息肉型),病变向胃腔内突出,呈息肉状0-Ⅱ平坦隆起及凹陷均欠显著。

什么是腺瘤胃息肉关于《什么是腺瘤胃息肉》,是我们特意为大家整理的,希望对大家有所帮助。
胃是身体中非常关键的身体器官,无论是进餐還是消化吸收都是历经胃,所以说每个人都应当有一个身心健康的胃里。
殊不知胃也是较为敏感的,假如大伙儿在平常不留意医护得话非常容易引起一些胃里病症,像胃息肉就非常普遍,今日要为大伙儿详细介绍什么叫囊腺瘤胃息肉。
囊腺瘤胃息肉的发病症状有什么呢!1、增生性息肉此型囊肿约占胃息肉的75%~90%,是炎症性粘膜增生产生的囊肿样物,并不是真实的肿瘤。
囊肿较小,一般直徑低于1.5cm,正圆形或橄榄型,有蒂或无蒂,表层光洁,可伴随糜乱。
组织学上由此可见增生的胃小凹上皮细胞和增生的原有层腺管,上皮细胞分裂优良,核分裂象罕见,原有层见炎症性体细胞侵润,一部分囊肿伴随肠化生。
极少数增生性息肉可产生异形增生或囊腺瘤性灶而造成恶化,但其病变率一般不超过1%~2%。
2、腺瘤性息肉系来自胃粘膜上皮细胞的良好胃肿瘤,约占胃息肉的10%~25%。
一般容积很大,呈球型或半球型,大部分无蒂,表层光洁,极少数呈平扁状、条形或分呈分。
组织学上关键由表层上皮细胞、小凹上皮细胞和腺管增生产生。
上皮细胞分裂不成熟,核分裂象多见,可分成管形、绒毛状及复合型囊腺瘤,常伴随显著肠化生和异形增生。
囊肿质间为松散结缔组织,有小量网织红细胞侵润。
粘膜肌层无显著增生,肌肉组织无分散化状况。
本型囊肿病变率高,达到30%~58.3%,特别是在瘤体直徑超过2cm、绒毛状腺瘤、异形增生Ⅲ度者恶化率高些。
由此可见引起瘤胃囊肿的原因是许多的,绝大多数全是良好的,可是在病发前期的情况下不可以立即医治得话,病况便会恶变。
什么叫囊腺瘤胃息肉,期待上边的详细介绍能造成您的高度重视,大伙儿在平常一定要留意医护胃里身心健康,培养规律性的饮食搭配和生活方式,不暴食暴饮。


增生性胃息肉怎么治疗胃息肉是比较常见的疾病,是由于胃粘膜发生病变,最后出现胃息肉。
胃息肉严重影响患者的生活和工作,令患者陷入无限的折磨之中,每个患者朋友们都希望自己能够早日康复,恢复正常的生活,那么,究竟增生性胃息肉怎么治疗呢?感兴趣的朋友们,可以来看看下文是怎么介绍的。
胃息肉(gastric polyp)是指胃黏膜局限性良性隆起病变。
本病属消化内科,早期或无并发症时多无症状。
出现症状时常表现为上腹隐痛、腹胀、不适,少数可出现恶心、呕吐、胃酸,厌食,消化不良,体重下降,腹泻。
胃里的息肉主要指由胃粘膜上皮和/或间质成分增生所引起的息肉状病变。
正常胃粘膜由于粘膜周围萎缩,出现腔内息肉状改变。
增生性改变时,肥厚的粘膜也可出现息肉状改变。
增生性改变既可出现局灶性或弥漫性息肉状改变。
胃窦息肉即长于胃窦处的胃息肉。
病例术者遇一例60岁女性患多发性胃息肉,息肉生长于胃体及胃底部,最大息肉1。
5cm,最小息肉0。
5cm,都为广基型,息肉色鲜红,突出于胃腔内。
经胃镜直视下导入激光切除,术后原胃部不适症状全消失,术后至今身体健康,无任何不适症状,饮食良好。
文献报道胃息肉比结肠息肉发病少见,且多发生于40岁以上男性,常在慢性胃炎时合并形成,单个息肉占绝大多数。
症状1、胃部疼痛不适:部分患者感觉胃部疼痛不适,但绝大多数胃息肉是在消化道内镜检查中偶然发现的,临床症状并不明显。
2、消化道出血:临床上只有很少一部份胃息肉的病人出现消化道出血[1] ,常常见于比较大的增生性或者腺瘤样的息肉,这些症状也常常缺乏特异性。
3、失血、贫血:也有病人因息肉而长时期慢性失血,出现贫血、营养不良等症状。
4、恶心、呕吐:靠近幽门生长的较大的息肉还可以引起幽门的梗阻,表现为剧烈的恶心,呕吐,腹痛等症状。
小凹上皮、固有胃腺、黏膜固有层的胃黏膜各组成部分的全部或一部分呈“非异型性”增殖。
增生为其基本表现,占胃息肉的85%-95%。
炎症性黏膜缺损的修复过程中出现小凹上皮的过度性再生而形成,也称为再生性息肉或炎症性息肉。

·短篇论著·基金项目:江苏省卫生健康委科研项目(LGY2018016)作者单位:214000 江苏无锡,江南大学附属医院消化内科 (王锦、薛育政),肾内科(包能)通信作者:薛育政,胃息肉的病理类型特征及采用无痛胃镜治疗的效果王 锦 包 能 薛育政【摘要】 目的 探讨不同病理类型胃息肉的分布、幽门螺杆菌(Hp )感染率、内镜下背景黏膜特征及采用无痛胃镜治疗的效果。
方法 选择2020年10月至2022年10月江南大学附属医院消化内科收治的309例胃息肉患者作为研究对象,所有患者均接受无痛胃镜下胃息肉电凝切除术治疗。
统计并分析309例患者胃息肉的病理类型、分布位置、Hp 感染率、内镜下背景黏膜特征,以及采用无痛胃镜治疗的效果。
结果 309例胃息肉患者的病理类型主要为胃底腺息肉(51.13%)和增生性息肉(38.51%)。
胃底腺息肉主要分布于胃体(48.10%)、胃底(30.38%)及多部位分布(20.25%),增生性息肉主要分布于胃窦(36.13%)、胃体(25.21%)和胃底(20.17%),炎症性息肉主要分布于胃窦(44.44%)。
增生性息肉、腺瘤性息肉和炎症性息肉患者的Hp 感染阳性检出率分别为73.95%、72.73%和72.22%,均显著高于胃底腺息肉患者(43.67%),差异均有统计学意义(P 均<0.05)。
胃底腺息肉患者中背景黏膜表现为慢性萎缩性胃炎者的占比(8.86%)分别低于增生性息肉患者(26.05%)和腺瘤性息肉患者(72.73%),差异均有统计学意义(P 均<0.05);腺瘤性息肉患者中背景黏膜表现为慢性萎缩性胃炎者的占比高于炎症性息肉患者,差异有统计学意义(P <0.05)。
309例胃息肉患者均采用无痛胃镜下电凝切除术治疗,其中302例达到彻底切除息肉的目的,7例有息肉残留,息肉的彻底切除率为97.73%。
结论 不同病理类型胃息肉的好发部位存在差异,增生性息肉、炎症性息肉和腺瘤性息肉患者的Hp 感染率均较高,增生性息肉和腺瘤性息肉患者发生慢性萎缩性胃炎的风险均较高。

曾斌芳治疗胃息肉中医临床经验总结胃息肉是消化系统多发病,易复发,部分息肉易发生癌变,西医目前以内镜下手术治疗为主,虽疗效确切,但复发率高。
曾斌芳教授经多年中医临床研究和经验总结,认为胃息肉的基本病机乃脾胃虚弱,脾胃气虚、正气不足贯穿疾病始终,也是其易复发的重要原因,据此提出健脾益气活血、理气化痰祛湿、扶正与祛邪并重的治疗措施,并创立经验方——益气散结汤,获得较好的临床疗效。
但对直径>0.5 cm的胃息肉,仍建议先行胃镜下治疗再行中药治疗,可缩短中药疗程,减轻患者身心负担,避免患者因不能长期口服中药致中断治疗而影响疗效。
Abstract:Gastric polyps are frequently occurring diseases of the digestive system,which are easy to recur. Some of the polyps are prone to canceration. Western medicine is currently under endoscope surgery. Although the curative effect is exact,the recurrence rate is high. Professor ZENG Bin-fang,after years of clinical research and experience,concludes that the basic pathogenesis of gastric polyps is deficiency of spleen and stomach,spleen qi deficiency and qi deficiency through the disease,and they are also important reasons for its recurrence. Accordingly,invigorating the spleen,invigorating qi and activating blood circulation,regulating qi and reducing phlegm dampness,and strengthening the body resistance to eliminate pathogenic factors are proposed to treat gastric polyps. In addition,the Yiqi Sanjie Decoction was created,with good clinical efficacy. But for gastric polyps of d> 0.5 cm,it is still recommended to take gastroscopic treatment before taking TCM treatment,which can shorten the course of TCM,relieve the physical and mental burden of patients,and prevent patients from interrupting treatment because they can not take TCM for a long time,to affect the curative efficacy.Keywords:experience of famous doctors;ZENG Bin-fang;gastric polyps;TCM treatment胃息肉是指胃黏膜表层上皮或黏膜下组织形成的局限性向腔内突起的良性隆起性病灶,是消化系统常见病,少数易发生癌变。
手术禁食禁水时间不能过八个小时吗
文章导读
胃息肉会拖慢胃黏膜的进展,导致胃粘膜出现慢性疾病,胃息肉患者不得不做手术治疗,但是刚刚做完手术的患者,需要进食6-8个小时,一直等到肠道中有气体排出才能正常进食,因为只有这样才能保证吃下去的食物可以完全消耗,如果不能消耗会流到身体的其他部位,这样会让患者承受二次痛苦。
胃息肉是指胃黏膜局限性良性隆起性病变,一般无临床表现。
部分患者可以出现上腹部不适、隐痛、烧心、反酸、恶心、不思饮食、慢性腹泻等。
胃息肉的病理分型有炎症性息肉、增生性息肉和腺瘤性息肉。
腺瘤性息肉癌变率较高,所以临床上发现息肉,先做活检病理确定息肉类型,若为腺瘤性息肉,多主张内镜下切除息肉治疗。
那么息肉切除后饮食上应该注意哪些方面呢?
胃息肉术后饮食的注意事项为:
1. 禁食:术后禁食6-8小时,或更长时间,似息肉的大小、创面大小而定。
然后先进食流质饮食,在过渡到半流食、软食、普食。
2. 流食:患者如果没有不适反应,次日可以给予流质饮食,每次50~100ml,间隔2小时可以给予一次。
3. 第三日,可以给予全量流质或半流食。
饮食原则为无刺激性食物,少量多餐,每次100~200ml,每日6-7餐。
食物应该选择不过甜、不过酸的食物,如鸡蛋汤、蔬菜汤、藕粉、小米汤等。
息肉的分型向来比较多和杂,现总结一下,大致可分为三大类:
(一)胃息肉的分型 规范和比较统一的息肉的分型基本状况
息肉分型目前用较多二字来反映是客观的,应用上难以统一来形容是
现实的。总体上的分型有:按大体形态学或组织学、病理、病生、病
变性质等。目前国内外较多的是Morson的组织分类,即:肿瘤性、
错构瘤性、炎症性和化生性四类。根据息肉数目多少分为多个与单发。
根据有蒂或无蒂分为有蒂型、亚蒂型(广基型)按山田和中村的分类,
以胃息肉为例,山田将胃内隆起性病变按其形态的不同,不论其性质
将其分为四型,I型:隆起的起势部较平滑而无明确的境界;Ⅱ型:
隆起的起势部有明确的境界;Ⅲ型:隆起的起势部略小,形成亚蒂;
Ⅳ型:隆起的起势部有明显的蒂部。中村按息肉的形态和组织学改变
的不同将其分为Ⅲ型:Ⅰ型最多,一般直径不超过2cm,有蒂多数,
也有无蒂,表面比较光滑,呈颗粒状、乳头状或绒毛状,色泽与周围
粘膜相同,也可呈暗红,多见胃窦部,此型与腺瘤性息肉相当。Ⅱ型:
多见胃窦部与胃体交界处,息肉顶部常发红,凹陷,是由于反复的粘
膜缺损,再生修复而形成,合并早期胃癌最多,组织学改变与Ⅰ型不
同;Ⅲ型:呈平盘状隆起,形态与Ⅱa早期胃癌相似,此型相当于Ⅱa
亚型异型上皮灶。同时尚有与结肠息肉相类似的由肠上皮而来的乳头
腺瘤,癌变率较高,中村认为可列入Ⅳ型。山田和中村的分类分型无
论在国内外、过去和现在一直被人们应用,说明了该分类分型的科学
性、实用性。使诊断能较准确地反映疾病的部位、性质、病程,对指
导诊断治疗用药及其它有效合理的手段选择、制订治疗方案和预后估
计具有十分重要意义。
(二) 胃息肉的分型习惯性和随意性的息肉分型状态 无论在
临床和各种病案及有关各种报告上还是各种学术期刊上,只要注意观
察均可见各种各样的术语表述其分类型。这一问题不是术语表达问
题,更不是应用方法问题,而是概念问题,我们认为概念不能混淆,
矫正和统一是必行的。
(三)胃息肉的分型根据经验分型息肉分类分型 无论何种方法
并不重要,重要的是能客观地反映疾病、为能解除疾病提供根据,本
着这一原则,有人认为前人较多分类分型虽能反映疾病,但对指导临
床运用内镜诊断和治疗息肉有较大的缺陷。息肉的大小已被较多学者
认为是有无恶变的依据之一,息肉发病部位均在管腔,而管腔解剖直
径较小而恒定,除此息肉在现代无论是诊断还是治疗多采用内镜这个
工具,而内镜的管腔外径又小于脏器解剖内径,鉴于上述情况,用大、
小型、特大型息肉分型,0.5cm以内为微型,0.5~2.0cm为小型,2.0~
3.0cm为大型,3.0~5.0cm为特大型,不仅能反映息肉的良恶性的可
能性,同时判断内镜切除的可能性及难度,以及内镜管腔直径的限制,
息肉大小有否内镜治疗适应征,均有必要,故将其分为小型、大型和
特大型。
胃息肉的临床分型
胃息肉按临床分类,最常采用Mings分类法分为再生性胃息肉及
肿瘤性胃息肉两大类。
第一类为再生性胃息肉——即为增生息性肉,发病较常见,其比
例约76%~90%。分布于胃内的部位不定,多数倾向于发生在胃炎
的部位。多发性占多数,直径平均1cm,其表面光滑呈分叶状。息肉
由指状细长的嵴和高分化类似于幽门腺上皮被复的扩张腺窝组成。不
规则的腺窝呈分支形和囊样变。增生的上皮细胞较大,深染色、单层,
核位于基底部,但分裂象少见。胞浆可分泌粘液,PAS阳性。间质为
粘膜肌向粘膜表面呈放射状生出的平滑肌束及胶原纤维组成,有时息
肉有大量血管瘤样的血管及浆细胞等炎症细胞浸润。上皮细胞的异型
性及肠化生不典型。主要是增生再生的结果,恶变者很少。
第二类为胃腺瘤。此病为真性肿瘤性腺瘤,包括腺瘤性息肉和乳
头状及绒毛状腺瘤。与结肠腺瘤的组织学和生物学相似。胃腺瘤比胃
癌远为少见,约占所有息肉的25%。发生于胃部的粘膜上皮,大都
由增生的胃粘液腺构成。
胃肠息肉是常见的消化道疾病之一。
可因疼痛、大便出血、粘液便等就诊而被检出。
大部分患者不一定出现症状,而是在做诊断性检查或体检时被发
现的。
息肉在显微镜下的组织学特点可分为4类:
肿瘤性息肉、错构瘤性息肉、炎症性息肉和增生性息肉。
炎症息肉与肠道的炎症反应有关,生长十分缓慢,基本上不会癌
变。
腺瘤型息肉分为腺管状腺瘤、绒毛状腺瘤、绒毛腺管状腺瘤。
研究表明,腺瘤性息肉癌变率约为5%-40%,其中绒毛状腺瘤癌
变率最高,息肉越大,癌变的机会也越大。
随着内窥镜检查的普及,越来越多的胃息肉被临床发现。
胃镜诊断中采用的各种术语成为困扰胃息肉患者的问题。
为此,在这里将胃息肉的分型问题做一归纳。
胃镜的分型总体上有:组织学;病理;病生;病变性质及病变大
小等。
考虑到内窥镜治疗的问题,以及病变大小与恶变的线性关系。
息肉的大小也成为界定息肉的重要指标。
按照大小,息肉可分为:
0.5cm以内为微型;
0.5~2.0cm为小型;
2.0~3.0cm为大型;
3.0~5.0cm为特大型。
癌前病变是一个病理学专业术语,指某些具有明显癌变危险的病变,
如不及时治疗就可能转变为癌。胃癌癌前病变的研究对于胃癌的早期
发现有重要意义,它不仅可以从癌前病变的研究了解胃癌的发生过程
以及环境因素,对这种病变的随诊可以及时发现早期胃癌。那么,什
么是胃癌的癌前病变呢?
作为胃癌的癌前病变自然是胃黏膜上皮细胞的病变,如我们所知的各
种癌前疾病:慢性萎缩性胃炎、胃溃疡、胃息肉等,虽然都是一些不
同的疾病,但他们发生胃癌的基础都是胃黏膜上皮细胞。多数学者认
为胃癌癌前病变主要是胃黏膜上皮异型增生。胃黏膜的肠上皮化生作
为慢性萎缩性胃炎的主要病变组成,是否为癌前病变,尚难定论,但
它与胃癌发生有密切关系,这已是广泛的共识。
当前属于癌前病变范围的一些术语很多,如异型增生、不典型增生、
上皮内非浸润性肿瘤等,在使用上很混乱。尽管在2000年出版的
WHO肿瘤分类中已明确将胃黏膜的癌前病变根据细胞的异型和结
构的紊乱程度分为低级别及高级别上皮内瘤变两级,但在实施过程中
仍出现诊断的不统一,因此有关专家又先后召开了两次国际会议,专
门探讨胃黏膜上皮内瘤变及早期癌的分类及诊断标准,最后在第二次
的维也纳国际会议上取得了较为一致的意见,即把胃黏膜从反应性增
生到浸润性癌的系列变化分为反应性增生、不能确定的上皮内瘤变
(即难以区分是反应性增生还是异型增生)、低级别上皮内瘤变、高级
别上皮内瘤变及浸润性癌五大类,将过去在诊断中最易出现分歧的重
度异型增生、原位癌甚至可疑浸润性癌均明确地归属于高级别上皮内
瘤变,统称高级别上皮内瘤变。
目前,低级别上皮内瘤变的处理缺乏统一的指导原则,大多数学者建
议对其进行密切的定期内镜随访而无须特殊处理。由于高级别上皮内
瘤变与浸润性癌关系十分密切,因此一旦明确诊断最好进行手术切
除。