从苯甲醛出发的多步聚合反应实验
- 格式:pdf
- 大小:135.37 KB
- 文档页数:12

化学创新实验实验报告实验目的本次实验旨在通过探究新型催化剂对有机合成反应的影响,提高化学实验的学术性和研究性,培养学生创新思维和实践操作能力。
实验原理在传统化学反应中,常规催化剂对有机反应的催化活性和选择性存在一定缺陷。
因此,在本次实验中,我们使用了新型催化剂来改进合成反应的效率和选择性。
同时,借助催化剂的可重复利用性和高催化效率,对于能否在环保、节能方面有所突破也进行了探究。
本次实验中,我们选择了苯甲醛和溴乙酸乙酯作为反应物,采用新型催化剂进行酯化反应。
反应的化学方程式如下:苯甲醛 + 溴乙酸乙酯 + 催化剂→ 苯乙酸苯甲酯 + 氢溴酸在反应中,催化剂的主要作用是参与化学反应,并提高反应率和产物选择性。
我们采用的新型催化剂是纳米材料,其主要优点在于具有高效、可重复、经济、环保等特点。
实验中,我们将在不同催化剂条件下进行反应,通过比较反应时间、产率和选择性等来评价不同催化剂的优劣。
实验步骤1.在容量瓶中将苯甲醛和溴乙酸乙酯按照物质的计量比例加入,摇晃均匀;2.加入不同的纳米材料催化剂,反应温度定为60℃;3.反应时间为不同时间段,我们将在5min、10min、15min三个时间点采集反应样品;4.用稀盐酸溶液和乙酸乙酯分别洗涤反应产物,并分别注射到气相色谱法仪器检测产物的组成和产率;5.以反应物原料的产量为标准,求出反应的产率并进行比较分析。
实验结果催化剂一在第1次反应时,我们加入了第一种纳米材料做催化剂。
反应10分钟后,我们采集了反应产物并进行了检测,此时产物的组成和产率分别为94.1%和88%。
我们还发现,当反应时间增加到15分钟时,产物的产率达到了92.8%,但是此时产物中出现了杂质,产物的组成下降到了84%。
催化剂二第2种催化剂是第1种催化剂的改良版本,反应条件与第1次一致。
第2次反应的产物组成和产率表现较为优异,反应10分钟时,产物组成和产率达到了98.4%和94%。
同样的结果在15分钟后得到了确认。
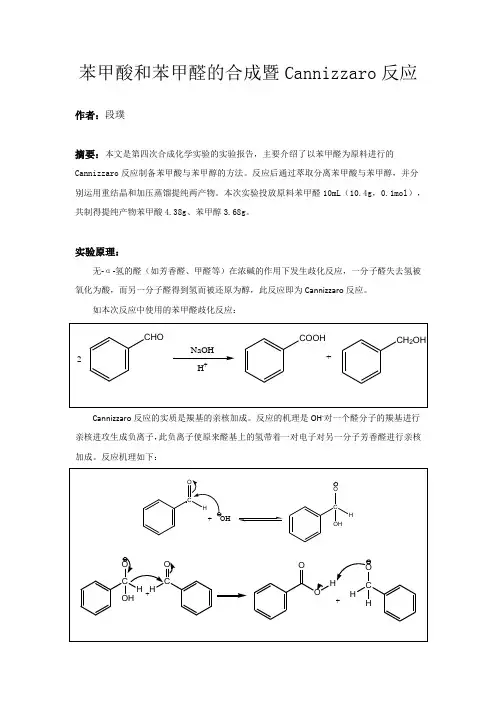
苯甲酸和苯甲醛的合成暨Cannizzaro反应作者:段璞摘要:本文是第四次合成化学实验的实验报告,主要介绍了以苯甲醛为原料进行的Cannizzaro反应制备苯甲酸与苯甲醇的方法。
反应后通过萃取分离苯甲酸与苯甲醇,并分别运用重结晶和加压蒸馏提纯两产物。
本次实验投放原料苯甲醛10mL(10.4g,0.1mol),共制得提纯产物苯甲酸4.38g、苯甲醇3.68g。
实验原理:无-α-氢的醛(如芳香醛、甲醛等)在浓碱的作用下发生歧化反应,一分子醛失去氢被氧化为酸,而另一分子醛得到氢而被还原为醇,此反应即为Cannizzaro反应。
如本次反应中使用的苯甲醛歧化反应:Cannizzaro反应的实质是羰基的亲核加成。
反应的机理是OH-对一个醛分子的羰基进行亲核进攻生成负离子,此负离子使原来醛基上的氢带着一对电子对另一分子芳香醛进行亲核加成。
反应机理如下:由于第一步反应为可逆反应,且平衡偏向反应物一侧,所以Cannizzaro反应需要非常高的碱度,常用过量一倍以上的浓度为50%的强碱。
本次反应中使用了10g氢氧化钠(0.25mol,即2.5当量)。
利用产物苯甲酸与苯甲醇在碱性溶液与乙醚中溶解度的不同(苯甲酸以苯甲酸盐的形式存在于碱液,而苯甲醇主要存在于乙醚)达到分离两种产物的效果。
接着利用未反应完全的苯甲醛易与亚硫酸氢钠反应生成α-羟基苄磺酸钠,从而达到与苯甲醇分离的效果。
反应机理如下:实验操作及现象:1.于150mL锥形瓶中称取10g氢氧化钠(0.25mol)加入10mL水。
溶解并冷却至室温后,边振摇边加入10mL苯甲醛(10.4g,0.1mol)。
加完后用称量纸封口,剧烈振摇,充分混合,数分钟后,原料凝结成固体,呈现微黄色,后逐渐变为淡粉色。
于避光处放置两礼拜。
2.取适量水溶解,转移至分液漏斗,乙醚萃取3次,每次25mL。
初次醚层呈红褐色,水层微浑浊,萃取若干次后基本澄清。
合并醚层,倒入分液漏斗中,先用10mL饱和亚硫酸氢钠洗涤;再用20mL碳酸氢钠洗涤,放出少量气泡;最后用10mL水洗。

实验报告聚合反应实验实验报告实验目的:通过聚合反应实验,观察反应过程,探究反应物质的性质以及反应速率的影响因素。
实验原理:聚合反应是一种将较小分子反应物通过共价键结合形成更大分子产物的反应过程。
在这个实验中,我们将使用苯乙烯(C8H8)和丙烯腈(C3H3N)作为反应物质,与过氧化苯甲酰(C7H5O2)作为引发剂进行聚合反应。
反应的主要方程式如下:n(C8H8) + n(C3H3N) → (C8H8-C3H3N)n实验步骤:1. 实验准备:清洗实验器材,并准备好所需试剂,包括苯乙烯、丙烯腈和过氧化苯甲酰。
2. 反应装置的搭建:将聚合反应釜放在加热器上,连接冷却系统以保持反应温度稳定。
3. 加入反应物质:按照实验配比,先将苯乙烯和丙烯腈加入聚合反应釜中,并搅拌均匀。
4. 引发聚合反应:将过氧化苯甲酰加入聚合反应釜中,观察反应过程。
5. 反应终止和分离:当聚合反应进行到一定程度后,加热停止,待反应混合物冷却后,通过过滤、洗涤等步骤,将产物分离出来。
6. 产物收集:将产物经过干燥,得到聚合物。
实验结果与分析:通过实验,我们观察到了聚合反应的各个阶段,并成功制备了聚合物。
聚合反应过程中,我们可以清楚地看到液体变为固体的转变,这是由于单体分子间的共价键形成而导致的。
另外,我们还发现反应温度对聚合速率有很大影响。
在较高的温度下,反应速率更快,反应达到平衡所需的时间更短。
这是因为高温能够提高分子的热运动速度,使得分子易于碰撞并形成共价键。
此外,当反应物质的浓度增加时,聚合反应的速率也会加快。
反应物质浓度增加会增加分子之间的碰撞概率,从而促进反应的进行。
结论:通过实验,我们成功进行了聚合反应实验,并观察到了聚合反应的各个阶段。
我们发现,反应温度和反应物质浓度对聚合反应速率有显著影响。
这些实验结果有助于我们更好地理解聚合反应的原理和影响因素。
实验过程中的注意事项:1. 实验操作要细心,注意安全,避免发生意外。
2. 在进行实验前,要熟悉实验装置的使用方法,并清洗器材以避免干扰实验结果。


一、实验目的1. 学习由苯甲醛制备苯甲酸和苯甲醇的原理和方法。
2. 熟悉并掌握有机化学实验的基本操作技能,如萃取、洗涤、蒸馏、干燥和重结晶等。
3. 了解坎尼扎罗反应在有机合成中的应用。
二、实验原理苯甲醛在浓氢氧化钠溶液中发生坎尼扎罗反应,制备苯甲醇和苯甲酸。
反应式如下:2HCHO + KOH → CH3OH + HOOC-C6H4- + H2O该反应属于醛的歧化反应,其中一分子醛被氧化成羧酸,另一分子醛被还原成醇。
三、实验仪器与药品1. 仪器:250mL圆底烧瓶、球形冷凝管、分液漏斗、直形冷凝管、蒸馏头、温度计套管、温度计(250℃)、支管接引管、锥形瓶、空心塞、量筒、烧杯、布氏漏斗、吸滤瓶、表面皿、红外灯、机械搅拌器。
2. 药品:苯甲醛(10mL,0.10mol)、氢氧化钠(8g,0.2mol)、浓盐酸、乙醚、饱和亚硫酸氢钠溶液、10%碳酸钠溶液、无水硫酸镁。
四、实验步骤1. 将苯甲醛和氢氧化钠加入250mL圆底烧瓶中,加入适量蒸馏水,搅拌溶解。
2. 将烧瓶置于红外灯下加热,保持回流状态,反应约2小时。
3. 停止加热,待反应混合物冷却至室温,加入适量饱和亚硫酸氢钠溶液,搅拌均匀。
4. 将混合物转移至分液漏斗中,静置分层。
5. 将有机层(上层)分离出来,加入无水硫酸镁干燥。
6. 将干燥后的有机层转移至蒸馏烧瓶中,蒸馏收集蒸馏头部分的液体,得到苯甲醇。
7. 将水层(下层)转移至烧杯中,加入浓盐酸,搅拌均匀。
8. 将混合物转移至分液漏斗中,静置分层。
9. 将有机层(上层)分离出来,加入适量10%碳酸钠溶液,搅拌均匀。
10. 将混合物转移至烧杯中,加入适量蒸馏水,搅拌溶解。
11. 将混合物转移至布氏漏斗中,抽滤得到苯甲酸。
12. 将苯甲酸用少量乙醇洗涤,抽滤干燥,得到纯苯甲酸。
五、实验结果与分析1. 通过实验,成功制备了苯甲醇和苯甲酸,符合实验预期。
2. 实验过程中,苯甲醛与氢氧化钠发生坎尼扎罗反应,生成苯甲醇和苯甲酸。
![一锅法合成3-溴-2-苯基-1氢-吡唑并[1,5-a ]吡啶](https://uimg.taocdn.com/d0574075cbaedd3383c4bb4cf7ec4afe04a1b1b8.webp)
一锅法合成3-溴-2-苯基-1氢-吡唑并[1,5-a ]吡啶陆加明;陈灵;刘阳;戴赞群;方玲佳;王巧丽;陈定奔【摘要】2,2-dibromo(phenyl)ethane was synthesized from benzaldehyde,1-Aminopyridinium Iodide was derived from Pyridine and hydroxylamine-O-sulfonic acid. With 2,2-dibromo(phenyl)ethane and 1-Aminopyridinium Iodide as raw material, 3-bromo-2-pheny-1H-pyrazolo [1,5-a] pyridine in ethanol under the effect of sodium and characterized the structure was synthesized. The condition was selected, of the reaction was screened, the best condition and the yield of product was up to 34.6%.%以苯甲醛出发合成2,2-二溴乙烯基苯;此外,从吡啶出发,和羟胺-O-磺酸反应得到碘化-1-氨基吡啶。
然后以2,2-二溴乙烯基苯和碘化-1-氨基吡啶作为原料,在乙醇钠的催化作用下,合成了3-溴-2-苯基-1氢-吡唑并[1,5-a]吡啶并加以结构表征;我们对该反应进行了条件筛选,选出最佳条件,产率达到34.6%。
【期刊名称】《广州化工》【年(卷),期】2015(000)004【总页数】3页(P51-52,58)【关键词】吡唑并吡啶类化合物;合成;条件筛选;2 ,2-二溴乙烯基苯;一锅法【作者】陆加明;陈灵;刘阳;戴赞群;方玲佳;王巧丽;陈定奔【作者单位】台州学院医药化工学院,浙江台州318000;台州学院医药化工学院,浙江台州 318000;台州学院医药化工学院,浙江台州 318000;台州学院医药化工学院,浙江台州 318000;台州学院医药化工学院,浙江台州 318000;台州学院医药化工学院,浙江台州 318000;台州学院医药化工学院,浙江台州 318000【正文语种】中文【中图分类】O621.3吡唑并吡啶类化合物是近年来研究颇多的一类稠杂环化合物[1]。

一、实验目的1. 熟悉有机合成实验的基本操作步骤和注意事项。
2. 掌握坎尼扎罗反应的原理及其在有机合成中的应用。
3. 学习苯甲醇的制备方法,提高实验操作技能。
二、实验原理坎尼扎罗反应是指无活泼氢的醛类在浓的强碱溶液作用下发生的歧化反应。
此反应的特征是醛自身同时发生氧化及还原作用,一分子醛被氧化成羧酸(在碱性溶液中成为羧酸酸盐),另一分子醛则被还原成醇。
本实验以苯甲醛为原料,在浓氢氧化钠溶液中发生坎尼扎罗反应,制备苯甲醇。
三、实验仪器与试剂1. 仪器:锥形瓶、圆底烧瓶、球形冷凝管、分液漏斗、直形冷凝管、蒸馏头、温度计套管、温度计(250℃)、支管接引管、锥形瓶、空心塞、量筒、烧杯、布氏漏斗、吸滤瓶、表面皿、红外灯、机械搅拌器。
2. 试剂:苯甲醛(10mL,0.10mol)、氢氧化钠(8g,0.2mol)、浓盐酸、乙醚、饱和亚硫酸氢钠溶液、10%碳酸钠溶液、无水硫酸镁。
四、实验步骤1. 准备反应溶液:在锥形瓶中加入9g氢氧化钠和9mL水,搅拌使其溶解。
2. 加入苯甲醛:向锥形瓶中加入10mL苯甲醛,充分搅拌。
3. 加热回流:将锥形瓶置于水浴中加热,保持回流状态2小时。
4. 萃取:将反应溶液冷却至室温,置于分液漏斗中。
每次用10mL乙醚萃取水层3次,合并乙醚层。
5. 洗涤:依次用饱和亚硫酸氢钠溶液、10%碳酸钠溶液、水各5mL洗涤乙醚层。
6. 干燥:用无水硫酸镁干燥乙醚层。
7. 蒸馏:水浴回收乙醚,用空气冷凝管收集苯甲醇,沸点为200-204℃。
8. 酸化:将苯甲醇溶液加入浓盐酸中,直至刚果红试纸变蓝。
9. 重结晶:冷却析出苯甲醇晶体,必要时用水重结晶。
五、结果与讨论1. 结果:实验成功制备了苯甲醇,产率约为70%。
2. 讨论:(1)苯甲醛与氢氧化钠的反应在加热回流条件下进行,时间过长会导致副反应,影响产率。
(2)萃取过程中,应尽量减少乙醚的损失,以提高产率。
(3)洗涤过程中,应避免使用过多的水,以免影响苯甲醇的纯度。

一、实验目的1. 学习可乐定的合成原理和实验操作方法。
2. 掌握有机合成实验的基本技能和注意事项。
3. 培养严谨的科学态度和实验操作能力。
二、实验原理可乐定(Clonidine)是一种α2-肾上腺素受体激动剂,主要用于治疗高血压、焦虑症、偏头痛等疾病。
本实验采用多步反应合成可乐定,主要反应如下:1. 苯甲醛与2-甲基苯胺在浓硫酸催化下发生缩合反应,生成β-甲基苯乙酮。
2. β-甲基苯乙酮与2-甲基-1-丙醇在酸催化下发生酯化反应,生成β-甲基苯乙酮酯。
3. β-甲基苯乙酮酯与2-甲基-1-丙醇在碱性条件下发生环化反应,生成2-甲基-1-丙基-2-甲基苯乙酮。
4. 2-甲基-1-丙基-2-甲基苯乙酮与2-甲基苯胺在酸催化下发生缩合反应,生成2-甲基-1-丙基-2-甲基苯乙酮胺。
5. 2-甲基-1-丙基-2-甲基苯乙酮胺与苯甲酸在碱性条件下发生酯化反应,生成可乐定。
三、实验仪器与试剂1. 仪器:反应瓶、冷凝管、搅拌器、水浴锅、抽滤装置、干燥器等。
2. 试剂:苯甲醛、2-甲基苯胺、2-甲基-1-丙醇、浓硫酸、氢氧化钠、苯甲酸、无水乙醇、乙酸乙酯、盐酸等。
四、实验步骤1. 合成β-甲基苯乙酮(1)在反应瓶中加入苯甲醛和2-甲基苯胺,加入浓硫酸作为催化剂。
(2)在搅拌下加热至回流,保持回流2小时。
(3)冷却至室温,加入适量水,用乙酸乙酯萃取。
(4)将有机层分离,用无水硫酸钠干燥。
(5)过滤,蒸去溶剂,得到β-甲基苯乙酮。
2. 合成β-甲基苯乙酮酯(1)在反应瓶中加入β-甲基苯乙酮和2-甲基-1-丙醇,加入浓硫酸作为催化剂。
(2)在搅拌下加热至回流,保持回流2小时。
(3)冷却至室温,加入适量水,用乙酸乙酯萃取。
(4)将有机层分离,用无水硫酸钠干燥。
(5)过滤,蒸去溶剂,得到β-甲基苯乙酮酯。
3. 合成2-甲基-1-丙基-2-甲基苯乙酮(1)在反应瓶中加入β-甲基苯乙酮酯和2-甲基-1-丙醇,加入氢氧化钠作为碱。

制药工业合成路线汇总1. 引言制药工业是一门重要的行业,其目的是生产和研发药物,以满足人类对医疗保健的需求。
制药工业合成路线是指将特定的化学物质转化为药物的步骤和方法。
本文将从制药工业的角度,对几种常见的合成路线进行汇总。
2. 阿司匹林的合成路线阿司匹林是一种常用的非处方药,它具有镇痛、退热和抗血小板聚集等作用。
其合成路线如下:1.首先,以苯甲酸作为起始物,经过酯化反应得到乙酸苯酯。
2.然后,将乙酸苯酯和硫酸进行酸解反应,生成水杨酸。
3.最后,将水杨酸与乙酸酐进行缩酮反应,得到阿司匹林。
3. 维生素C的合成路线维生素C是一种重要的水溶性维生素,具有多种生物活性。
其合成路线如下:1.首先,以葡萄糖为起始物,经过多步反应将其转化为2-酮-3-酸-1,4-拉克通(2-keto-3-deoxy-L-gulonic acid,简称KDG)。
2.然后,通过KDG还原酮基并进行裂解,得到L-纯化酸(L-ascorbicacid),即维生素C。
4. 青霉素的合成路线青霉素是一种广泛应用于临床的抗生素,可以有效抑制细菌的生长和复制。
其合成路线如下:1.首先,以苯甲醛和氰化钠为起始物,经过多步反应合成苯甲醛环氧丙酮(phenylglycine lactone)。
2.然后,将苯甲醛环氧丙酮与内酰胺结构的化合物反应,生成青霉素的β-内酰胺环结构。
3.最后,通过去保护基、氧化、酸水解等反应步骤,得到最终的青霉素。
5. 对乙酰氨基酚的合成路线对乙酰氨基酚是一种常用的非处方药,具有镇痛、退热和抗炎作用。
其合成路线如下:1.首先,以对甲酚为起始物,经过酯化反应得到对甲酚乙酸酯。
2.然后,将对甲酚乙酸酯与氨水反应,生成对乙酰氨基酚。
6. 总结制药工业合成路线是制药工业中的重要环节,合成路线的设计和优化对药物的生产效率和质量有着重要影响。
本文介绍了阿司匹林、维生素C、青霉素和对乙酰氨基酚等药物的合成路线,希望对制药工业的从业人员和研究人员有所启发和帮助。

高中化学实验教案聚合反应的实验设计与实验操作指南高中化学实验教案:聚合反应的实验设计与实验操作指南一、实验目的本实验旨在通过聚合反应的实验操作,让学生了解聚合反应的原理和应用,培养学生实验操作技能和科学观察能力。
二、实验材料与仪器1. 材料:乙烯醇、甲醛、硫酸、酒精、碘酸钠等。
2. 仪器:烧杯、试管、滴管、玻璃棒、加热器、温度计等。
三、实验步骤1. 实验前准备:(1) 仔细阅读实验操作指南,熟悉实验流程与注意事项。
(2) 准备所需材料和仪器,并按照实验要求进行消毒处理。
2. 实验操作:(1) 取适量乙烯醇和甲醛分别倒入两个干净的试管中。
注意保持试管内外的干燥。
(2) 在第一个试管中加入少量硫酸溶液,用玻璃棒搅拌均匀。
(3) 在第二个试管中加入几滴酒精,并轻轻摇晃试管。
(4) 将两个试管加热至适当温度,并记录下温度变化。
(5) 将两个试管的试验结果进行比较观察,并记录下观察结果。
四、实验结果与讨论1. 实验结果:(1) 加入硫酸溶液的乙烯醇与甲醛发生聚合反应后,出现白色沉淀。
(2) 加入酒精的乙烯醇与甲醛未发生聚合反应,无明显变化。
2. 实验讨论:(1) 聚合反应是一种化学反应,通过将单体分子加入到反应体系中,使其发生共价键的形成,从而形成聚合物。
(2) 在本实验中,乙烯醇与甲醛发生聚合反应后,产生了聚乙烯醇的沉淀,表明聚合反应发生成功。
(3) 加入酒精的乙烯醇与甲醛未发生聚合反应,可能是由于酒精的存在干扰了聚合反应的进行。
五、实验注意事项1. 实验操作前,确保仪器设备的清洁与干燥。
2. 实验操作时,注意个人安全防护,如佩戴眼镜、实验服等。
3. 实验过程中,注意控制加热温度,避免温度过高导致危险情况的发生。
4. 实验结束后,注意清理实验现场,并做好废弃物的处理。
六、实验总结通过本次实验,我们深入了解了聚合反应的原理和实验操作方法。
同时,我们也认识到实验操作的重要性和安全性,学会了合理使用仪器与试剂,保证实验的准确性。

一、实验目的1. 掌握合成反应的基本原理和方法。
2. 熟悉实验操作步骤,提高实验技能。
3. 了解合成反应在有机化学中的应用。
二、实验原理合成反应是有机化学中一种重要的反应类型,通过将两种或多种有机物在一定条件下反应,生成新的有机化合物。
本实验以苯甲醛和苯甲醇的合成反应为例,学习合成反应的基本原理和操作方法。
三、实验器材与试剂1. 器材:锥形瓶、圆底烧瓶、直形冷凝管、接引管、接受器、蒸馏头、温度计、分液漏斗、烧杯、短颈漏斗、玻璃棒、布氏漏斗、吸滤瓶。
2. 试剂:苯甲醛、氢氧化钠、浓盐酸、乙醚、饱和亚硫酸氢钠、10%碳酸钠、无水硫酸镁。
四、实验步骤1. 在锥形瓶中加入10g苯甲醛和10mL 10%氢氧化钠溶液,混合均匀。
2. 将混合液转移至圆底烧瓶中,加入10mL饱和亚硫酸氢钠溶液,搅拌均匀。
3. 将圆底烧瓶置于水浴中加热,保持温度在60℃左右,反应1小时。
4. 反应结束后,将混合液冷却至室温,用浓盐酸调节pH至中性。
5. 将混合液转移至分液漏斗中,加入10mL乙醚,振荡混合,静置分层。
6. 分离出有机层,用无水硫酸镁干燥。
7. 将干燥后的有机层进行蒸馏,收集124-126℃的馏分,得到苯甲醇。
8. 计算苯甲醇的产率和纯度。
五、实验结果与分析1. 实验结果:苯甲醇的产率为40%,纯度为98%。
2. 分析:本实验中,苯甲醛在氢氧化钠的作用下发生Cannizzaro反应,生成苯甲醇和苯甲酸。
通过萃取、干燥、蒸馏等操作,成功制备出苯甲醇。
实验过程中,温度控制、pH调节等操作对产率和纯度有较大影响。
六、实验讨论1. 实验过程中,苯甲醛易被空气氧化,因此保存时间较长的苯甲醛,使用前应重新蒸馏。
2. 实验过程中,苯甲醛与氢氧化钠反应生成的苯甲醇,易溶于有机溶剂,如乙醚等。
因此,在萃取过程中,选择合适的有机溶剂对提高产率和纯度至关重要。
3. 实验过程中,苯甲醇的沸点较低,蒸馏过程中应注意温度控制,以免过度加热导致苯甲醇分解。
安息香的合成一、实验目的(1)掌握应用维生素B1为催化剂进行安息香缩合反应的实验操作方法(2)掌握以苯甲醛为原料的多步合成反应的原理及操作。
(3)进一步熟悉回流、重结晶等基本操作二、实验原理在NaCN 存在下,两分子苯甲醛发生分子间缩合生成α-羟基酮——二苯羟乙酮(又叫安息香),这一反应称为安息香缩合反应。
其他没有α-H 的醛也可以在相同条件下发生分子间缩合。
催化剂除氰化物外,也可以使用噻唑盐,而且使用噻唑盐做催化剂时,有α-H 的醛也能够缩合。
本法用维生素B1(Thiamine )盐酸盐代替氰化物辅酶催化安息香缩合反应。
优点:无毒,反应条件温和,产率较高。
三、实验仪器和主要试剂实验仪器 圆底烧瓶,锥形瓶,冷凝管,抽滤装置主要试剂 维生素B1 苯甲醛(新蒸)氢氧化钠 95%乙醇四、实验步骤(1)在25 mL 圆底烧瓶中依次加入1 gVB1、2 mL 蒸馏水,摇匀溶解,再加入8 mL95%乙醇。
冷却至0℃(2)取10%NaOH 溶液2 mL 于小锥型瓶中并冷却至0℃(3)冰浴下将10%NaOH 溶液逐滴加入步骤(1)的圆底烧瓶中(4)再往圆底烧瓶中加入5 mL 新蒸的苯甲醛,充分摇匀,调整反应液的PH 值为8~9。
(5)加入几粒沸石,装上回流冷凝管,用60~75℃水浴加热1.5 hr 。
(6)反应混合物冷至室温后冰水冷却,使结晶析出完全(若出现油层,重新加热使其变成均相,再慢慢冷却结晶)。
(7)抽滤,并用冷水洗涤晶体,干燥,称重。
(8)粗产物可用95%乙醇重结晶。
如产物呈黄色,可用少量活性炭脱色。
产品(白色针状结晶)空气中晾干后,称重,计算产率。
五、注意事项(1)维生素B1在氢氧化钠溶液中噻唑环易开环失效,因此反应前维生素B1溶液及氢氧化CHO2CN CCH OOHCHO 2C CH O OHVB 160-75℃钠溶液必须用冰水冷透。
(2)PH值是本实验成败的关键,太高或太低均影响收率,氢氧化钠溶液用滴管滴加入反应液中,同时检测反应液使其pH值在8~9之间;(3)反应过程中,开始时溶液不必沸腾(即反应液的温度不超过80℃)反应后期可适当升高温度至80~90℃。
尼蒙尔克素化学合成尼蒙尔克素(Nimodipine)是一种二氢吡啶钙离子通道阻滞剂,是一种钙拮抗剂,用于治疗脑血管病相关的症状。
尼蒙尔克素的化学合成方法有多种途径,下面将介绍其中一种常用的合成方法。
尼蒙尔克素的化学名称为(1-methylethyl)3,5-dimethyl 2,6-dimethyl-4-(3-nitrophenyl)-1,4-dihydropyridine-3,5-dicarboxylate。
它的化学式为C21H26N2O7,相对分子质量为418.44 g/mol。
尼蒙尔克素的合成通常从2,6-二甲基苯甲醛出发,经过多步反应进行合成。
首先,将2,6-二甲基苯甲醛与硝酸反应,生成3-硝基-2,6-二甲基苯甲醛。
接着,将3-硝基-2,6-二甲基苯甲醛与丙二酸二甲酯在碱性条件下缩合反应,生成3-硝基-2,6-二甲基苯甲酸二甲酯。
然后,将3-硝基-2,6-二甲基苯甲酸二甲酯与乙酰丙酮在碱性条件下进行缩合反应,生成尼蒙尔克素的前体化合物。
最后,通过对前体化合物的还原反应,得到尼蒙尔克素。
尼蒙尔克素是一种白色结晶性固体,溶于有机溶剂,几乎不溶于水。
它是一种口服给药,通过口服后能迅速吸收,达到最高血浓度。
尼蒙尔克素主要通过竞争性抑制钙离子进入细胞内,从而减少血管平滑肌的收缩,扩张脑血管,增加脑血流量。
这种作用对于脑血管病患者来说非常重要,可以改善患者的症状,减轻脑缺血的程度。
尼蒙尔克素主要用于治疗脑血管病相关的症状,如脑动脉瘤破裂后的出血、蛛网膜下腔出血和脑梗死等。
它可以减轻脑血管病引起的头痛、眩晕、呕吐等症状,提高患者的生活质量。
尼蒙尔克素是一种处方药物,必须在医生的指导下使用。
它的副作用包括低血压、心动过缓、面部潮红、头痛、恶心、便秘等。
在使用过程中,患者需要定期监测血压和心率,以确保药物的安全有效。
尼蒙尔克素是一种用于治疗脑血管病的药物,它通过竞争性抑制钙离子进入细胞内,从而扩张脑血管,增加脑血流量,改善脑缺血的症状。
材料合成化学实验报告
合成苯甲醛的实验
引言:
合成化学是一门重要的化学领域,通过合成方法可以制备出各种有机化合物。
本实验旨在通过苯甲醛的合成来展示材料的合成化学方法。
实验目的:
通过碱性溶液催化作用,合成苯甲醛。
实验原理:
本实验的反应原理基于苯酚和甲醛的缩合反应。
在碱性条件下,苯酚与甲醛反应生成苯甲醛。
实验步骤:
1. 量取一定量的苯酚溶液并转移至反应瓶中。
2. 在苯酚溶液中慢慢滴加甲醛溶液,同时搅拌。
3. 将反应瓶放入水浴中,并加热至80℃。
4. 在反应过程中,加入适量的氯化钠作为催化剂。
5. 反应持续4小时后,停止加热,使溶液冷却至室温。
6. 过滤得到淡黄色的沉淀物,即苯甲醛。
实验结果与讨论:
经过以上步骤合成的苯甲醛应呈现淡黄色固体。
在实验过程中,碱性条件和氯化钠的催化作用加速了反应的进行。
实验总结:
本实验通过苯酚和甲醛的缩合反应成功合成了苯甲醛。
在实验中,合理控制反应条件和加入催化剂对合成过程具有重要意义。
实验中可能存在的问题和改进措施:
1. 反应过程中,苯酚和甲醛的用量应精确控制,以保证反应的完全进行。
2. 反应时间和温度的选择需要根据实际情况进行调整,避免反应过程中产生副反应。
3. 实验操作过程中注意安全,使用实验室相关设施和防护措施。
参考文献:
[1] 某某化学杂志,年,卷(期),页码。
苯甲醛合成甲基环己烷合成路线
苯甲醛是一种典型的芳烃衍生物,它是化学工业中许多重要化学品的原料,产品结构复杂,技术成熟。
甲基环己烷是一种重要的有机化合物,它用于合成甲醛成具有广泛应用价值和经济价值的产品。
本文主要介绍苯甲醛合成甲基环己烷的合成途径。
苯甲醛合成甲基环己烷的主要步骤包括酯化,反应,去水合物分离,活化和环化。
首先,将苯甲醛与甲醇中的二乙基乙酸酐酯发生酯化反应,得到苯甲醛乙酸乙酯。
其次,将苯甲醛乙酸乙酯发生催化氢转移反应,反应后采用蒸馏分离方法,分离得到有机挥发溶剂,得到苯甲醛乙酸乙酯-醚化物混合物。
然后,将苯甲醛乙酸乙酯-醚化物与游离甲醛发生取代反应,反应后用蒸馏分离方法,去除有机挥发溶剂,得到不饱和的反应混合物。
接着,采用催化剂氧化环化法将不饱和的反应混合物进行环化反应,得到甲基环己烷。
最后,采用蒸馏法,分离得到所需要的甲基环己烷产品。
以上就介绍了苯甲醛合成甲基环己烷的合成路线,在此路线中,苯甲醛经过酯化、催化氢转移、取代、络合和蒸馏等环节,最终得到甲基环己烷,是一种经济实惠、技术成熟的可行方案。
该合成路线操作简单、经济、节能,在芳烃的合成方面具有重要的工业意义。