六价铬的测定实验方案
- 格式:doc
- 大小:61.00 KB
- 文档页数:3

六价铬的测定实验报告
实验报告:六价铬的测定
实验目的:
1. 学习测定六价铬的方法和原理
2. 掌握吸收光谱法对六价铬的测定
实验原理:
当六价铬溶液中添加一定量的酸性二氧化钾时,会生成黄色的
二氧化铬络合物,吸收峰位在400nm左右。
吸收光谱法是通过比
较未知浓度样品的吸光度和标准品吸光度之间的差异,来确定浓度。
实验步骤:
1. 准备样品和标准品,分别用去离子水稀释到50mL的量级;
2. 在样品中加入0.2M硫酸,使其pH值维持在1左右;
3. 加入2 mL 5%酸性二氧化钾溶液,使其转化成黄色的络合物;
4. 在400nm波长处测定吸光度,并记录下来。
实验结果:
样品吸光度为0.987,标准品吸光度为1.234,由此可得未知样品六价铬浓度为1.54mg/L(标准品六价铬浓度为2mg/L)。
实验讨论:
1. 在实验过程中,要严格控制样品的酸度,否则六价铬会转化为三价铬或四价铬,影响浓度的准确性。
2. 吸收光谱法对样品要求较高,可能会受到杂质的干扰,需使用较高纯度的试剂。
结论:
本实验通过吸收光谱法成功测定了六价铬的浓度为1.54mg/L。
此方法简便、准确,可用于工业废水等样品的六价铬测定。
参考文献:
1. 关于重金属离子剧毒的探究[J]. 化学杂志,2005,22(4):10-13.
2. 谢振玉.化学分析实验[M].南京: 南京大学出版社,2014.。


水中六价铬测定实验报告一、实验目的本实验旨在测定水样中六价铬的含量,了解水样的污染程度,为环境保护和水质监测提供科学依据。
二、实验原理在酸性溶液中,六价铬与二苯碳酰二肼反应生成紫红色络合物,其颜色的深浅与六价铬的含量成正比。
通过分光光度计在特定波长下测定吸光度,从而确定六价铬的浓度。
三、实验仪器与试剂1、仪器分光光度计比色皿移液管(1mL、5mL、10mL)容量瓶(50mL、100mL)玻璃棒烧杯(50mL、100mL)电子天平漏斗2、试剂六价铬标准储备液(100mg/L)二苯碳酰二肼溶液(显色剂)硫酸溶液(1+1)磷酸溶液(1+1)四、实验步骤1、标准曲线的绘制分别吸取 000mL、020mL、050mL、100mL、200mL、400mL 六价铬标准储备液于 50mL 容量瓶中,用水稀释至标线。
向各容量瓶中加入 05mL 硫酸溶液(1+1)和 05mL 磷酸溶液(1+1),摇匀。
再加入 2mL 二苯碳酰二肼溶液,摇匀。
静置 5 10 分钟后,在分光光度计上,于 540nm 波长处,用 1cm 比色皿,以水作参比,测定吸光度。
以六价铬的浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2、水样的预处理若水样浑浊或有颜色,需进行预处理。
取适量水样于烧杯中,加入硫酸和硝酸混合液,加热消解至溶液澄清,冷却后转移至容量瓶中。
3、水样的测定吸取适量预处理后的水样于 50mL 容量瓶中,按照标准曲线绘制的步骤进行操作,测定吸光度。
五、实验数据及处理1、标准曲线数据|六价铬浓度(mg/L)| 000 | 040 | 100 | 200 | 400 |800 |||||||||吸光度| 0000 | 0085 | 0210 | 0420 | 0840 | 1680 |根据以上数据,绘制标准曲线,得到回归方程:y = 021x + 0002 (其中 y 为吸光度,x 为六价铬浓度)2、水样测定数据|水样编号|吸光度||||| 1 | 0250 || 2 | 0380 || 3 | 0180 |将吸光度代入回归方程,计算水样中六价铬的浓度:水样 1 中六价铬浓度:(0250 0002)÷ 021 = 1186mg/L水样 2 中六价铬浓度:(0380 0002)÷ 021 = 1795mg/L水样 3 中六价铬浓度:(0180 0002)÷ 021 = 0852mg/L六、实验结果分析1、本次实验测定的水样中,六价铬的浓度在不同水样之间存在差异。


水质六价铬的测定方法
水质六价铬的测定方法
一、准备试剂
1.1钨氧化物滴定液:将1.1g的碳酸钴和
2.2g的钨酸钠溶于1000ml水,加入3ml的37%硫酸铵,调至pH2.2,加入少量稳定剂(锰酸钠0.1g,氯化钙0.05g),充分搅拌至溶解,再溶于1000ml水冲洗蒸馏水,即成钨氧化物滴定液。
2.1钨氧化物稀释液:将10ml的钨氧化物滴定液稀释至1000ml,加磷酸10ml,加
0.1g的钠硫酸溶液50ml,再加氯化钠调至稀释液的pH约为7.0~7.5。
3.1复碱液:将1.14g的氢碳水合物(用氢氧化钠调至pH12.7)溶解在1000ml水,
即成复碱液。
4.1标样:用氢氧化钠调至pH12.7,充分搅拌至溶解。
5.1蒸馏水:利用实验室设备进行蒸馏取得清水,可用于溶液清洗,试剂配置。
二、操作流程
1.取150ml试样,在样品加氯化钠调至PH6.0~7.0。
2.取50ml试样,加入5ml复碱液,充分搅拌,再加入5ml的5%酒石酸溶液,加电极,调至1.7V,稳定时间1min,滴加0.6ml钨氧化物滴定液,再滴加1.4ml钨氧化物稀释液
测量电位后转化成六价铬的浓度。
3.取150ml试样,采用适当的标样和标准溶液,用同样的方法进行测定,计算出结果。
三、结果判定
根据测定得出的结果转换成六价铬浓度,以mg/L为单位表示,根据浓度值判断水质
中六价铬的情况:
1.≤0.1mg/L,六价铬含量符合国家规定;
2.0.1>至1mg/L,六价铬数量升高,应采取相应的措施改善水质;
3.>1mg/L,六价铬数量超标,极易危及人体健康,应采取积极措施降低六价铬含量。

六价铬的测定实验六六价铬的测定⼀、实验⽬的(1)学会六价铬的⽔样采集保存、预处理及测定⽅法。
(2)学会各种标准溶液的配制⽅法和标定⽅法。
⼆、概述铬(Cr )的化合物常见的价态有三价和六价。
在⽔体中,六价铬⼀般以-24CrO 、HCrO -4⼆种阴⼦形式存在,受⽔中pH 值、有机物、氧化还原物质、温度及硬度等条件影响,三价铬和六价铬的化合物可以互相转化。
铬是⽣物体所必需的微量元素之⼀。
铬的毒性与其存在价态有关,通常认为六价铬的毒性⽐三价铬⾼100倍,六价铬更易为⼈体吸收⽽且在体内蓄积。
但即使是六价铬,不同化合物的毒性也不相同。
当⽔中六价铬浓度为1mg/L 时,⽔呈淡黄⾊并有涩味,三价铬浓度为1mg/L 时,⽔的浊度明显增加,三价铬化合物对鱼的毒性⽐六价铬⼤。
铬的⼯业来源主要是含铬矿⽯的加⼯、⾦属表⾯处理、⽪⾰鞣制、印染等⾏业。
三、⽔样保存⽔样应⽤瓶壁光洁的玻璃瓶采集。
如测总铬⽔样采集后,加⼊硝酸调节pH<2;如测六价铬,⽔样采集后,加NaOH 使pH 为8~9;均应尽快测定,如放置不得超过24h 。
四、⼲扰及清除含铁量⼤于1mg/L ⽔样显黄⾊,六价钼和汞也和显⾊剂反应⽣成有⾊化合物,但在本⽅法的显⾊酸度下反应不灵敏。
钼和汞达200mg/L 不⼲扰测定。
钒有⼲扰,其含量⾼于4mg/L 即⼲扰测定。
但钒与显⾊剂反应后10min ,可⾃⾏褪⾊。
氧化性及还原性物质,如:ClO —、Fe 2+、SO 32-、S 2O 32-等,以及⽔样有⾊或混浊时,对测定均有⼲扰,须进⾏预处理。
五、⽅法的选择铬的测定可采⽤⼆苯碳酰⼆胼分光光度法、原⼦吸收分光光度法和滴定法。
清洁的⽔样可直接⽤⼆苯碳酰⼆肼分光光度法测六价铬。
如测总铬,⽤⾼锰酸钾将三价铬氧化成六价铬,再⽤⼆苯碳酰⼆肼分光光度法测定。
六、测定⽅法(⼆苯碳酰⼆肼分光光度法)1. 实验原理在酸性溶液中,六价铬离⼦与⼆苯碳酰⼆肼反应,⽣成紫红⾊络合物,其最⼤吸收波长为540nm ,吸光度与浓度的关系符合⽐尔定律。

六价铬的测定方法六价铬是一种常见的金属元素,它广泛应用于工业和生活中。
然而,由于六价铬具有强烈的毒性和致癌性,它的浓度需要进行监测和控制,以确保环境和人体健康的安全。
本文将介绍几种常用的六价铬测定方法。
一、草酸还原法草酸还原法是一种常用且简单的六价铬测定方法。
该方法通过将六价铬还原为三价铬,然后使用指示剂进行滴定测定。
具体步骤如下:1. 取适量的样品,并将其转化为六价铬酸盐的形式。
2. 将草酸加入样品中,将六价铬还原为三价铬。
3. 添加适量的指示剂,并进行滴定,直至指示剂的颜色发生转变。
4. 计算样品中六价铬的浓度。
二、硫氧化法硫氧化法是一种常用的六价铬测定方法,它利用硫酸氧化六价铬为可滴定的二价铬。
具体步骤如下:1. 取适量的样品,并将其转化为六价铬酸盐的形式。
2. 加入硫酸,在高温下将六价铬氧化为二价铬。
3. 添加适量的指示剂,并进行滴定,直至指示剂的颜色发生转变。
4. 计算样品中六价铬的浓度。
三、电化学法电化学法是一种准确且高灵敏度的六价铬测定方法。
该方法通过电化学传感器测定样品中六价铬的浓度。
具体步骤如下:1. 准备一个具有特定电极的电化学传感器。
2. 将样品溶液放置在电化学传感器中。
3. 通过施加电势,观察电化学传感器中反应的电流。
4. 根据电流的变化,推断样品中六价铬的浓度。
四、光谱法光谱法是一种精确且无损的六价铬测定方法。
该方法利用光谱分析技术测定样品中六价铬的吸收或发射光谱。
具体步骤如下:1. 准备一个光谱分析仪器,如紫外-可见光谱仪或荧光光谱仪。
2. 将样品溶液放置在光谱仪器中。
3. 测量样品在特定波长处的吸收或发射光谱。
4. 根据光谱图形的特征,推断样品中六价铬的浓度。
以上是几种常用的六价铬测定方法,每种方法都有其优点和适用范围。
在实际应用中,可以根据需要选择合适的方法进行测定。
六价铬的监测和控制对于保护环境和人体健康具有重要意义,因此准确测定六价铬的浓度是非常重要的。
希望本文介绍的测定方法对读者有所帮助。

六价铬测定实验报告六价铬测定实验报告引言:六价铬是一种常见的有害物质,它广泛存在于工业废水、电镀废液等环境中。
由于其对人体健康的危害性,准确测定六价铬的含量对环境保护和人体健康至关重要。
本实验旨在通过一种简便、准确的方法,测定样品中六价铬的含量。
实验原理:本实验采用邻苯二胺与六价铬在酸性条件下反应生成紫色络合物的原理。
邻苯二胺与六价铬生成的络合物具有较强的紫色吸收峰,可以通过紫外可见分光光度计测定其吸光度,从而计算出六价铬的含量。
实验步骤:1. 样品制备:取适量待测样品,如废水、废液等,通过过滤或沉淀去除杂质,得到清澈的溶液。
2. 酸化处理:将样品溶液转移到酸洗瓶中,加入适量的硫酸进行酸化处理。
酸化可以使六价铬完全转化为三价铬,提高测定的准确性。
3. 邻苯二胺溶液的制备:取适量的邻苯二胺,加入足够的去离子水溶解,制备成一定浓度的邻苯二胺溶液。
4. 反应:将酸化后的样品溶液与邻苯二胺溶液混合,充分摇匀,使其反应平衡。
5. 测定吸光度:将反应后的溶液转移到紫外可见分光光度计比色皿中,设置波长为520nm,测定吸光度值。
6. 绘制标准曲线:准备一系列不同浓度的六价铬标准溶液,按照相同的方法测定吸光度值,绘制六价铬浓度与吸光度的标准曲线。
7. 计算样品中六价铬的含量:根据样品的吸光度值,利用标准曲线的拟合方程计算出六价铬的浓度。
实验结果与讨论:通过上述实验步骤,我们成功测定了样品中六价铬的含量。
在标准曲线的基础上,我们可以根据样品的吸光度值得出相应的浓度。
实验结果显示,样品中六价铬的含量为X mg/L。
本实验采用了邻苯二胺与六价铬络合物的测定方法,该方法简便、准确,并且具有较高的灵敏度。
然而,在实际应用中,我们还需要注意一些潜在的干扰因素。
例如,样品中可能存在其他金属离子,它们可能与邻苯二胺发生竞争反应,导致测定结果的偏差。
因此,在实际应用中,我们需要对样品进行前处理,去除干扰物质,以提高测定的准确性。

六价铬检测方法
六价铬定性检测方法(电镀层)
1.试样的准备:测试前样品表面不能有任何污染物、指印或其它外来的污点。
如果
表面涂有薄油则在测试前需要在室温下(不高于35℃)用清洁剂、软布或合适的溶剂去除。
高于35℃时试样不能强制干燥。
不能用碱性溶剂处理样品因为碱金属易引起铬酸盐涂层的脱落。
2.如果样品表面有聚合物涂层,可以用细砂纸如800号的SiC砂红轻轻摩擦去除
之,但不能将样品表面的铬酸盐涂层也同时摩擦。
当然也可用其它更有效的方法去除。
3.将0.4克1,5二苯卡巴肼溶解于由20毫升丙酮和20毫升乙醇(96%)组成
的混合液中,然后加入20毫升75%的正磷酸溶液和20毫升去离子水。
该溶液应在使用前的8小时以内制备。
4.向样品表面滴加1到5滴测试液。
如果含有六价铬几分钟内会出现红到紫罗兰
的颜色。
好久以后出现的颜色不要考虑,因为这时样品正在变干。
5.为了便于比较,也可用类似的方法测试样品的基体部分。
把样品表面的所有涂
层去除掉,比如用砂纸或锉摩擦,或用酸溶解涂层,样品的基体就暴露出来了。
以上1~5的操作均是在EDX已确认有铬存的情况下而进行,若EDX确认更本无铬盐存在则亦无六价铬的存在,故无需进行此项测试。
如果实验显示样品中含有六价铬,而需进一步定量检测则需用比色计或分光光度计进行“比色法定量测定六价铬”.。
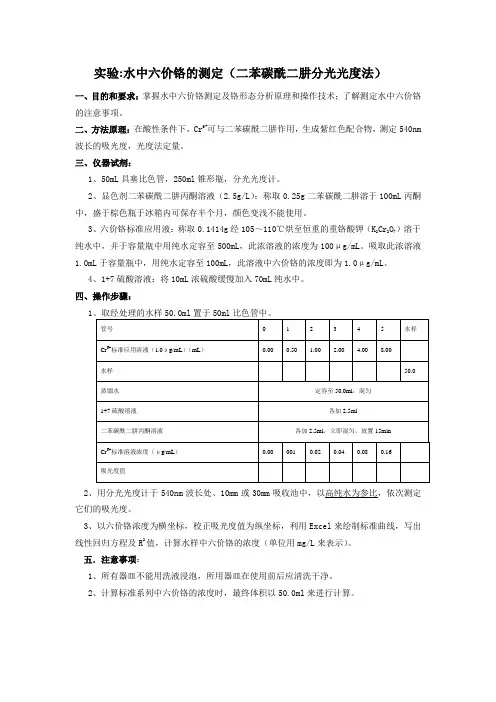
实验:水中六价铬的测定(二苯碳酰二肼分光光度法)
一、目的和要求:掌握水中六价铬测定及铬形态分析原理和操作技术;了解测定水中六价铬的注意事项。
二、方法原理:在酸性条件下,Cr6+可与二苯碳酰二肼作用,生成紫红色配合物,测定540nm 波长的吸光度,光度法定量。
三、仪器试剂:
1、50mL具塞比色管,250ml锥形瓶,分光光度计。
2、显色剂二苯碳酰二肼丙酮溶液(2.5g/L):称取0.25g二苯碳酰二肼溶于100mL丙酮中,盛于棕色瓶于冰箱内可保存半个月,颜色变浅不能使用。
3、六价铬标准应用液:称取0.1414g经105~110℃烘至恒重的重铬酸钾(K2Cr2O7)溶于纯水中,并于容量瓶中用纯水定容至500mL,此浓溶液的浓度为100μg/mL。
吸取此浓溶液1.0mL于容量瓶中,用纯水定容至100mL,此溶液中六价铬的浓度即为1.0μg/mL。
4、1+7硫酸溶液:将10mL浓硫酸缓慢加入70mL纯水中。
四、操作步骤:
1
2、用分光光度计于540nm波长处、10mm或30mm吸收池中,以高纯水为参比,依次测定它们的吸光度。
3、以六价铬浓度为横坐标,校正吸光度值为纵坐标,利用Excel来绘制标准曲线,写出线性回归方程及R2值,计算水样中六价铬的浓度(单位用mg/L来表示)。
五.注意事项:
1、所有器皿不能用洗液浸泡,所用器皿在使用前后应清洗干净。
2、计算标准系列中六价铬的浓度时,最终体积以50.0ml来进行计算。

六价铬的测定方法一、试剂理化性质≤1.1、试剂名称:六价铬;1.2、英文名称:Chromium;1.3、CAS号:13765-19-8;1.4、分子式:Cr6+;二、实验原理由于六价铬的实验原理比较复杂,我们采用了清洁化学等技术进行实验,以生成Cr6+以及其它价铬盐,例如Cr3+,Cr2 O3等。
清洁化学方法分为二个步骤:首先是敏化,即清洗原样品,使Cr6+释放出来;其次是识别,即做出溶剂消除栽培,为便于后续测定步骤作准备。
三、实验方法3.1、准备样品采样时选择土壤或生物样品,收集到足够数量的样品后,均匀混合后,在实验室中进行一定量的研磨,然后用筛子筛细,使之变成粉末状,放在容器中,备用。
3.2、敏化将粉末样品放入无水甲醇(CH3OH)中,在水浴恒温器的控温条件下,加热至90℃,2h后放入冷却剂,过夜后用毛细管蒸馏,除去CH3OH;此时即可得到Cr6+溶液样品。
3.3、识别用酸性溶液(HCl或H2SO4)将Cr6+溶液样品中的Cr3+及其它价铬盐析出,用萃取剂(乙醇系溶剂)萃取Cr6+,便于后续的测定。
3.4、测定六价铬的测定方法多种多样,总的来说,可以基本上分为以下几类:(1)电感耦合等离子体原子发射光谱法;(2)紫外-可见吸收光谱法;(5)高效液相色谱法;(6)原子吸收光谱法。
以上是六价铬测定的几种常见方法,还有一种叫波谱技术,也会用到,这几种方法各有优劣,也就是看实验需求的情况而定的。
四、安全注意事项1.在进行六价铬的测定实验前,请确保操作室的洁净程度,以使得试剂及产物不会污染样品。
2.在实验室中使用萃取剂(乙醇系溶剂)请注意安全,在使用毛细管时要当心,以免出现意外状况。
3.在进行敏化步骤时,加热时应当控制好温度,以免造成烧伤或者其它事故发生。
4.结束实验后,余下试剂及样品应当存放至显微镜温柜中,注意防止潮湿及高温环境,以便确保洁净实验结果的准确性。
六价铬的测定实验方案一、实验依据依据GB7467—87、HJ609-2011六价铬水质自动在线监测仪技术要求二、实验方法在酸性溶液中,六价铬与二苯碳酰二肼反应生成紫红色化合物,于波长540nm进行分光光度测定。
国标中采用光程30mm或10mm比色皿进行测试,我们则采用比色管代替三、实验过程1.试剂配置1.1 丙酮。
1. 2 硫酸1. 2.1 1+1硫酸溶液。
将硫酸(H2SO4=1.84g/ml,优级纯)缓缓加人到同休积的水中,混匀。
1.3 磷酸: 1+1磷酸溶液。
将磷酸(H3P04 =1.69g/m1,优级纯)与水等体积混合。
1.4 氢氧化钠:4g/L氢氧化钠溶液。
将氢氧化钠(NaOH) 1g溶于水并稀释至250ml.1.5 氢氧化锌共沉淀剂1. 5.1 硫酸锌: 8% (m/ V)硫酸锌溶液。
称取硫酸锌(ZnS047 H2O) 8g,溶于looml水中。
1. 5.2 氧氧化钠:2% (m/V)溶液。
称取2 .4 9氢氧化钠,溶于120m1水中。
用时将 3 .5.1和3.5.2两溶液混合。
1.6 高锰酸钾:40g/ L 溶液。
称取高锰酸钾(KMnO4)4g,在加热和搅拌下溶于水,最后稀释至100ml.1.7. 铬标准贮备液。
称取于110。
C,干燥2h的重铬酸钾(K2Cr2O7,,优级纯)0.2829士0.00 01g,用水溶解后,移人1000ml容量瓶中,用水稀释至标线,摇匀。
此溶液lml含0.l0mg六价铬。
1.8 铬标准溶液。
吸取5 .00 mI 铬标准贮备液(1.7)置于500ml容量瓶中,用水稀释至标线,摇匀。
此溶液1m l含1.00ug六价铬。
使用当天配制此溶液。
1.9 铬标准溶液。
吸取25. 00m1 铬标准贮备液(1.7)置于500m】容量瓶中,用水稀释至标线,摇匀。
此溶液1m l含5.00ug六价铬。
使用当天配制此溶液。
1.10 尿素:200g/ L尿素溶液。
将尿素〔(NH2)2CO)20g溶于水并稀释至100m l .1.1 1 亚硝酸钠:20g/ L溶液。
六价铬的测定实验报告六价铬的测定实验报告引言:六价铬是一种常见的有害物质,它广泛存在于工业废水、大气污染物和土壤中。
由于其对人体健康和环境造成的危害,准确测定六价铬的含量对于环境保护和健康监测至关重要。
本实验旨在通过一种简单而有效的方法,测定水样中六价铬的浓度。
实验步骤:1. 样品制备:收集不同来源的水样,如自来水、河水、地下水等,并过滤掉悬浮物。
2. 标准曲线制备:准备一系列不同浓度的六价铬标准溶液。
取适量的六价铬标准溶液,分别加入不同的量的蒸馏水,制备出一系列浓度递增的标准溶液。
3. 反应体系构建:取一定量的水样,加入硫酸和硝酸,使水样中的六价铬还原为三价铬。
然后加入硫氰酸钾,与三价铬形成深红色络合物。
4. 分光光度计测定:将反应后的溶液转移到光度计比色皿中,使用分光光度计在特定波长下测定溶液的吸光度。
5. 建立标准曲线:测定标准溶液的吸光度,并记录下吸光度与浓度的关系,建立标准曲线。
6. 测定样品中的六价铬浓度:使用同样的方法,测定样品中的六价铬的吸光度,并通过标准曲线计算出样品中的六价铬浓度。
结果与讨论:通过实验测定,我们得到了一系列标准曲线的吸光度与浓度的关系。
利用这个标准曲线,我们可以计算出样品中的六价铬浓度。
在实验中,我们还发现了一些问题。
首先,水样中可能存在其他物质干扰,这些物质可能会影响六价铬的测定结果。
因此,在进行测定时,需要对样品进行预处理,以去除或减少这些干扰物质的影响。
其次,实验中使用的方法可能存在一定的误差,因此需要进行多次测定,取平均值来提高结果的准确性。
此外,实验过程中的仪器校准和操作技巧也对结果的准确性有一定影响。
六价铬的测定方法有很多种,如电化学法、光谱法、原子吸收光谱法等。
每种方法都有其优缺点,选择合适的测定方法需要综合考虑实验条件、样品性质和测定精度等因素。
结论:通过本实验,我们成功地测定了水样中六价铬的浓度。
在实际应用中,这个方法可以用于监测环境中的六价铬污染,及时采取措施保护环境和人体健康。
水质中六价铬的测定实验报告实验名称:水质中六价铬的测定实验实验目的:熟悉分光光度法测定水中六价铬的方法,掌握实验操作技能,提高实验操作能力。
实验原理:分光光度法是利用物质分子吸收特定波长的能量,从而测量物质浓度的一种分析方法。
分光光度法广泛应用于色度分析、无机分析和有机分析等领域。
水质中六价铬的测定方法通常采用1,5-二苯卡巴唑(DPC)为显色剂,六价铬在弱酸性介质中与DPC形成橙红色络合物,可以用分光光度法进行测定。
实验步骤:1. 根据实验室提供的标准六价铬溶液,制备一系列不同浓度的六价铬标准溶液(0.1μg/mL,0.5μg/mL,1μg/mL,2μg/mL,4μg/mL)。
2. 取一系列容量瓶,分别加入不同浓度的标准溶液,加入适量的1,5-二苯卡巴唑(DPC)溶液和磷酸盐缓冲液,定容至50mL。
3. 选取一种浓度的标准溶液作为校准曲线,使用分光光度计在400-600nm范围内测定标准溶液的吸光度,并制作校准曲线。
4. 用同样的方法测定待测样品的吸光度,并根据校准曲线计算出待测样品中六价铬的浓度。
实验结果:校准曲线如下所示:浓度(μg/mL)吸光度(A)0.1 0.1140.5 0.5801 1.1102 2.2704 4.389使用上述校准曲线测定了一组待测样品的吸光度,结果如下所示:样品编号吸光度(A)六价铬浓度(μg/mL)1 0.252 0.292 0.642 0.663 1.236 1.12结论:本实验通过分光光度法测定了水质中六价铬的浓度,并掌握了实验操作技能。
实验结果表明,待测样品中六价铬浓度分别为0.29μg/mL、0.66μg/mL和1.12μg/mL。
六价铬的测定方法测定六价铬的方法六价铬常见于工业外排废水和土壤中,是一种有害污染物。
为了保护环境和人类健康,我们需要测定六价铬的含量。
本文将介绍两种测定六价铬的方法。
方法一:硫酸钠还原法该方法利用硫酸钠还原六价铬为三价铬,然后利用二苯基卡宾作为指示剂,采用氨水-硫脲法测定三价铬的含量。
实验步骤:1.取适量待测样品,加入适量浓硝酸,加热至样品完全溶解,转移至250 mL 锥形瓶中。
2.加入2 g 硫酸钠和1 g 二苯基卡宾,试管盖好。
3.放入100 mL 密闭容器中,在水浴中恒温还原4 h。
4.取出,冷却,加入25 mL 准确氨水和25 mL 准确浓盐酸,振摇混合。
5.用氨水调整pH 值到6-9,加入3 g硫脲,振摇混合,使硫脲充分溶解。
6.立即定容至250 mL 振摇混合,放置10 min。
7.用紫外分光光度计测定样品透过率,按照指定曲线计算出三价铬的含量。
方法二:碘化钾-汞化钾法该方法利用碘化钾和汞化钾氧化六价铬成为四氧化三铬,然后用光度法测定四氧化三铬的含量。
实验步骤:1.取适量待测样品,转移至250 mL 锥形瓶中。
2.加入碘化钾-汞化钾试剂,试管盖好。
3.振摇混合,静置10 min。
4.用光度计测定样品透过率,按照指定曲线计算出六价铬的含量。
注意事项:1.硫酸钠还原法中,硫酸钠的用量应当控制得当,不宜过量,否则可能影响测定结果。
2.碘化钾-汞化钾法中,碘化钾和汞化钾应当按照一定比例混合,过量反应可能影响测定结果。
另外,汞化钾是有毒物质,操作时需注意安全。
结语:以上两种测定六价铬的方法各有优缺点,实验者应当根据实际需要进行选择。
在操作过程中,应当注意安全,避免给环境和人体带来损害。
工业废水中六价铬的测定实验报告
1.掌握测定工业废水中六价铬的方法及原理;
2.了解操作方法及注意事项。
实验仪器:
1.分光光度计
2.取样瓶
3.量筒、滴定管、移液管等。
实验原理:
在酸性条件下,铬酸盐离子转化为铬(III)离子,然后与酚酞指示剂生成氧化钴酸盐颜色,根据吸收波长(535nm处)与标准曲线,测定六价铬浓度。
实验步骤:
1.取工业废水样品5ml,加入硫酸约1ml,装入取样瓶中,配制成约0.2mol/L
的硫酸介质,并用去离子水定容至50ml,充分混合。
2.在分光光度计中,设置基准波长为535nm,空白比色池中放入去离子水,调为零吸光度。
3.在色谱池中加入1ml酚酞指示剂溶液(0.1g/L),再加入2-3滴硫酸(约0.5ml),加入经调试的废水样品溶液至刻度线,充分搅拌混合后即可测定吸光度。
4.以铬标准品制备出不同浓度的标准溶液,进行光谱扫描,建立Cal表示,根据工业废水对比,测定六价铬质量浓度。
实验结果:
测得工业废水中六价铬的质量浓度为0.032mg/L。
实验结论:
通过本次实验,我们学习了测定工业废水中六价铬的方法及原理,并对实验步骤进行了深入了解。
通过实验的数据计算,可以判断工业废水中六价铬的浓度是否符合国家排放标准。
六价铬的测定实验方案
一、实验依据
依据GB7467—87、HJ609-2011六价铬水质自动在线监测仪技术要求
二、实验方法
在酸性溶液中,六价铬与二苯碳酰二肼反应生成紫红色化合物,于波长540nm进行分光光度测定。
国标中采用光程30mm或10mm比色皿进行测试,我们则采用比色管代替
三、实验过程
1.试剂配置
1.1 丙酮。
1. 2 硫酸
1. 2.1 1+1硫酸溶液。
将硫酸(H2SO4=1.84g/ml,优级纯)缓缓加人到同休积的水中,混匀。
1.3 磷酸: 1+1磷酸溶液。
将磷酸(H3P04 =1.69g/m1,优级纯)与水等体积混合。
1.4 氢氧化钠:4g/L氢氧化钠溶液。
将氢氧化钠(NaOH) 1g溶于水并稀释至250ml.
1.5 氢氧化锌共沉淀剂
1. 5.1 硫酸锌: 8% (m/ V)硫酸锌溶液。
称取硫酸锌(ZnS047 H2O) 8g,溶于looml水中。
1. 5.2 氧氧化钠:2% (m/V)溶液。
称取2 .4 9氢氧化钠,溶于120m1水中。
用时将 3 .5.1和3.5.2两溶液混合。
1.6 高锰酸钾:40g/ L 溶液。
称取高锰酸钾(KMnO4)4g,在加热和搅拌下溶于水,最后稀释至100ml.
1.7. 铬标准贮备液。
称取于110。
C,干燥2h的重铬酸钾(K2Cr2O7,,优级纯)0.2829士0.00 01g,用水溶解后,移人1000ml容量瓶中,用水稀释至标线,摇匀。
此溶液lml含0.l0mg六价铬。
1.8 铬标准溶液。
吸取5 .00 mI 铬标准贮备液(1.7)置于500ml容量瓶中,用水稀释至标线,摇匀。
此溶液1m l含1.00ug六价铬。
使用当天配制此溶液。
1.9 铬标准溶液。
吸取25. 00m1 铬标准贮备液(1.7)置于500m】容量瓶中,用水稀释至标线,摇匀。
此溶液1m l含5.00ug六价铬。
使用当天配制此溶液。
1.10 尿素:200g/ L尿素溶液。
将尿素〔(NH2)2CO)20g溶于水并稀释至100m l .
1.1 1 亚硝酸钠:20g/ L溶液。
将亚硝酸钠(NaNO2)2g溶于水并稀释至100m1.
1.1 2 显色剂(I)。
称取二苯碳酞二肼(C13H14N4O)0 .2g,溶于50m1 丙酮(1.1)中,加水稀释至l00ml,摇匀,贮于棕色瓶,置冰箱中。
色变深后,不能使用。
1.1 3 显色剂(II)。
称取二苯碳酸二肼2g,溶于50ml丙酮(1.1)中,加水稀释至l00ml,摇匀。
贮于棕色瓶,
置冰箱中。
色变深后,不能使用。
注: 显色剂(I)也可按下法配制称取4.0g苯二甲酸配(C6H4O),加到80ml乙醉中,搅拌溶解(必要时可用水浴微温),加人0.5g二苯碳酸二肼,用乙醇稀释至100m1。
此溶液于暗处可保存六个月。
使用时要注意加人显色剂后立即摇匀,以免六价铬被还原。
2.仪器
选用华夏科创的多参数仪器代替分光光度计,采用其中540nm的灯进行测试
3.采样与样品
实验室样品应该用玻璃瓶采集。
采集时,加人氢氧化钠,调节样品pH值约为8。
并在采集后尽快测定,如放置,不要超过24h。
四、实验步骤
1 样品的预处理
1.1 .1 样品中不含悬浮物,是低色度的清洁地面水可直接测定。
1.1 .2 色度校正:如样品有色但不太深时,按6.3步骤另取一份试样,以2m l丙酮(1.1)代替显色剂,其他步骤同1.3.试份测得的吸光度扣除此色度校正吸光度后,再行计算。
1.1 .3 锌盐沉淀分离法:对混浊、色度较深的样品可用此法前处理。
取适量样品(含六价铬少于100ug)于150m1烧杯中,加水至50mI。
滴加氢氧化钠溶液(1.4),调节溶液pH值为7~8。
在不断搅拌下,滴加氢氧化锌共沉淀剂(3.5)至溶液pH值为8~9。
将此溶液转移粟100 m l容量瓶中50.0m 1滤液供测定。
注: 当样品经锌盐沉淀分离法前处理后仍含有机物干扰测定时,可用酸性高锰酸钾氧化法破坏有机物后再测定。
即取50.0ml 滤液于150m1锥形瓶中,加人几粒玻璃珠.加人0.5m1硫酸溶液(1.2.1),0.5mI磷酸溶液(1 .3)摇匀。
加人2滴高锰酸钾溶液(1.6),如紫红色消褪,则应添加高锰酸钾溶液保持紫红色。
加热煮沸袋溶液体积约剩20ml. 取下稍冷,用定量中速滤纸过滤,用水洗涤数次。
合并滤液和洗液至50m1比色管中。
加人1m l尿素溶液( 1. 10 ).摇匀.用滴管滴加亚硝酸钠溶液(1.11),每加一滴充分摇匀,至高锰酸钾的紫红色刚好褪去。
稍停片刻,待溶液内气泡逸尽。
转移至50ml比色管中,用水稀释至标线,供测定用。
1.1.4 二价铁、亚硫酸盐、硫代硫酸盐等还原性物质的消除:取适量样品(含六价铭少于50ug)于50ml比色管中,用水稀释至标线,加人4m1显色剂(II) (1.13),混匀,放置5 min后,加人1m1硫酸溶液(1.2)摇匀。
5一10min后,在540nm波长处,用10或30mm光程的比色皿,以水做参比,测定吸光度。
扣除空白试验测得的吸光度后,从校准曲线查得六价铬含量。
用同法做校准曲线。
1.1.5 次氯酸盐等氧化性物质的消除:取适量样品,(含六价铬少于50ug)于50m1比色管中,用水稀释至标线,加人0.5m1硫酸溶液(1.2)、0.5 m1磷酸溶液(1.3), 1.0ml尿素溶液(1.10),摇匀,逐滴加入1 ml亚硝酸钠溶液(1.11),边加边摇,以除去由过量的亚硝酸钠与尿素反应生成的气泡,待气泡除尽后,以下步骤同1.3(免去加硫酸溶液和磷酸溶液)。
2.空白试验
按同试徉完全相同的处理步骤进行空白试验,仅用50ml水代替试样。
3.测定
取适量(含六价铬少于50ug)无色透明试份,置于50m1 比色管中,用水稀释至标线。
加人0,5m1硫酸溶液(1.2)和0.5ml磷酸溶液(1.3),摇匀。
加人2 ml显色剂(I)(1.12),摇匀,5~l0min 后,在540nm波长处,用10或30mm的比色皿,以水做参比,测定吸光度,扣除空白试验测得的吸光度后,从校准曲线上在得六价铭含量。
注: 如经锌盐沉淀分离、高锰酸钾氧化法处理的样品,可直接加入显色剂测定。
4.校准
向一系列50m1 比色管中分别加人0、0.20、0.50、1.00、2.00、4 .00、6 .00、8 .00和
10.0m1铬标准溶液(1.8或1.9)(如经锌盐沉淀分离法前处理,则应加倍吸取),用水稀释至标线。
然后按照测定试样的步骤(1.1和1.3)进行处理。
从测得的吸光度减去空白试验的吸光度后,绘制以六价铬的量对吸光度的曲线。
5.结果的表示
计算方法
六价铬含量c( mg/L)按下式计算:
式中: m —由校准曲线查得的试份含六价铬量,ug
V —试份的体积,ml
六价铬含量低于0.1mg/L ,结果以三位小数表示;六价铬含量高于0.lmg/L ,结果以
二位有效数字表示。
6.步骤流程图
试剂配置
样品采集
空白前处理 和样品一致 样品前处理
色度校正
1.1.2 锌盐沉淀分离法1.13
二价铁、亚硫酸盐、硫代硫酸盐等还原性物质的消除1.1.4
次氯酸盐等氧化性物质的消除1.1.5
空白测试
曲线校准
比色管中分别加人0、
0.20、0.50、1.00、2.00、
4 .00、6 .00、8 .00和
10.0m1铬标准溶液
加入显色剂 样品测试
加入显色剂
测得结果 测试完成。