体外诊断试剂行业发展概述
- 格式:pdf
- 大小:362.61 KB
- 文档页数:4


体外诊断试剂研究报告体外诊断试剂是指在体外(体诊断)对人体进行检测的试剂,包括血液、尿液、唾液、体液等的检测。
本研究报告主要对体外诊断试剂的发展状况、应用领域和未来趋势进行了深入分析。
体外诊断试剂是近年来医疗领域的热门研究方向之一。
据统计,全球体外诊断试剂市场规模呈逐年增长趋势。
其中,血液检测试剂是体外诊断试剂市场的主要组成部分,其市场规模最大。
尿液、唾液等其他体液检测试剂也存在一定的市场需求。
体外诊断试剂市场的增长主要受益于人口老龄化以及慢性疾病的增多。
体外诊断试剂的应用领域广泛,涵盖了临床生化分析、微生物学检测、分子诊断和免疫学检测等多个方面。
在临床生化分析方面,例如血糖试剂和血脂试剂被广泛应用于糖尿病和高血脂等疾病的检测。
微生物学检测方面,体外诊断试剂可用于快速检测细菌和病毒感染,如流感病毒试剂和细菌培养试剂。
分子诊断方面,例如PCR试剂和基因芯片试剂可以对遗传性疾病进行检测。
免疫学检测方面,购买荧光染色试剂请输入可能用于肿瘤标志物的检测。
未来,体外诊断试剂市场有望继续保持增长态势。
首先,随着人口老龄化加剧以及慢性疾病的高发,对体外诊断试剂的需求将持续增加。
其次,随着生物技术和纳米技术的不断进步,体外诊断试剂的研发水平也将提高,将越来越多的新试剂投入市场。
此外,大数据和人工智能等新兴技术的应用也将进一步推动体外诊断试剂的发展。
例如,利用大数据分析可以实现个性化诊断和治疗,提高体外诊断试剂的准确性和效率。
综上所述,体外诊断试剂是一个具有广阔市场前景的领域。
随着医疗技术的不断发展,体外诊断试剂的研究和应用将逐渐取得更多突破,为人类健康事业做出更大的贡献。

体外诊断试剂专业知识体外诊断试剂专业知识一、体外诊断试剂的发展历程20世纪50年代,体外诊断试剂的发展可以追溯到英国军医凯瑟琳泰勒布朗(Katherine T. Blount)利用妊娠试纸进行妊娠诊断,及美国医学家弗兰克布兰德(FrankBrad)和莱恩斯科特(LaneScott)发明的心肌酶信号检测系统,这两项技术的发明,标志着体外诊断试剂的出现,并开创了体外诊断试剂的发展历史。
二、体外诊断试剂的分类体外诊断试剂可以根据检测对象的不同分为两大类:病原体诊断试剂和生物标志物诊断试剂。
1、病原体诊断试剂病原体诊断试剂是指用于检测病原体(如病毒、细菌、真菌等)的试剂。
它们包括血清学试剂、细菌培养试剂、血凝素试剂、PCR试剂和抗原特异性试剂等。
2、生物标志物诊断试剂生物标志物诊断试剂是指用于检测生物体内特定物质和反应的试剂。
它们包括抗体检测试剂、激酶检测试剂、细胞因子检测试剂、代谢物检测试剂、蛋白质检测试剂等。
三、体外诊断试剂的检测原理1、血清学试剂血清学试剂是检测血清中抗原和抗体的试剂,其检测原理是通过血清中抗原与抗体之间的特异性结合,从而检测出病毒及其他病原体的存在,以此作为诊断病毒性疾病的依据。
2、细菌培养试剂细菌培养试剂是检测细菌的试剂,其检测原理是将样本放置在营养培养基上,细菌在这种营养基上可以生长、繁殖,当生长足够时,可使用适当的染色技术检测到细菌的存在,以此作为诊断细菌性疾病的依据。
3、抗体检测试剂抗体检测试剂是检测抗体的试剂,其检测原理是将待检样本与抗原反应,当抗原与抗体结合时,可以检测出抗体的存在,以此作为诊断疾病的依据。
四、体外诊断试剂的应用1、临床诊断体外诊断试剂可以用于临床诊断,常见的检测项目有病毒感染性疾病、性病、肝炎、肾病等;2、流行病学研究体外诊断试剂还可以用于流行病学研究,常见的检测项目有流行性感冒、流行性腮腺炎等;3、毒物检测体外诊断试剂也可以用于毒物检测,常见的检测项目有酒精、毒品等。
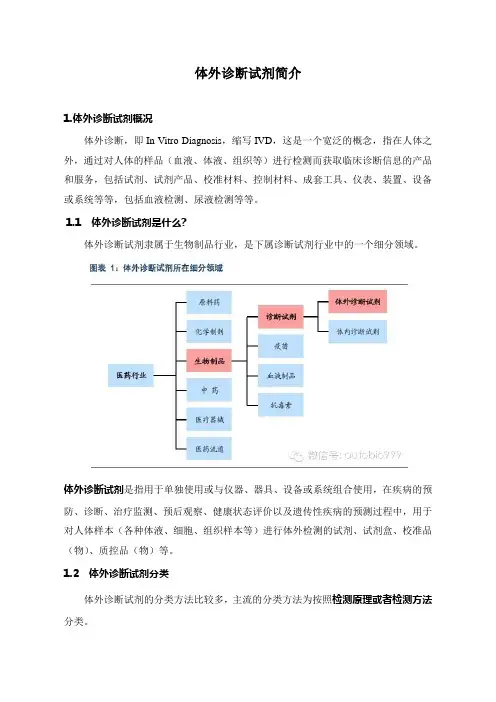
体外诊断试剂简介1.体外诊断试剂概况体外诊断,即In Vitro Diagnosis,缩写IVD,这是一个宽泛的概念,指在人体之外,通过对人体的样品(血液、体液、组织等)进行检测而获取临床诊断信息的产品和服务,包括试剂、试剂产品、校准材料、控制材料、成套工具、仪表、装置、设备或系统等等,包括血液检测、尿液检测等等。
1.1 体外诊断试剂是什么?体外诊断试剂隶属于生物制品行业,是下属诊断试剂行业中的一个细分领域。
体外诊断试剂是指用于单独使用或与仪器、器具、设备或系统组合使用,在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中,用于对人体样本(各种体液、细胞、组织样本等)进行体外检测的试剂、试剂盒、校准品(物)、质控品(物)等。
1.2 体外诊断试剂分类体外诊断试剂的分类方法比较多,主流的分类方法为按照检测原理或者检测方法分类。
根据检测原理或者检测方法,体外诊断试剂可以分为:生化诊断试剂、免疫诊断试剂、分子诊断试剂、微生物诊断试剂、尿液诊断试剂、凝血类诊断试剂、血液学和流式细胞诊断试剂等。
生化、免疫和分子诊断试剂为我国诊断试剂主要的三大类品种。
免疫诊断在原理上是利用抗原抗体的特异性结合,但是检测端的方法就比较多了,检测方式多样化,比如利用放射性元素的放射性而准确测量抗原抗体结合的放射免疫(放免)、利用氯金酸在特定环境下通过静电作用与蛋白质大分子结合的胶体金技术、利用活性酶作为标记物的酶联免疫(酶免)、利用镧系元素(稀土元素)螯合物荧光寿命长的特定进行检测的时间分辨荧光法(TRFIA)和利用化学发光原理和免疫反应原理相结合的化学发光检测(CLIA)。
放免由于对环境污染较大,现在逐渐被其他免疫诊断方法所替代,目前酶免是免疫诊断中比较主流的方法。
核酸诊断是目前分子诊断中的主要部分,另一种是生物芯片技术。
分子诊断的检测目标直接是决定生命性状的遗传物质和表现形式,包括DNA、RNA和蛋白质。

ivd行业发展历程
IVD行业(体外诊断行业)发展历程可以追溯至20世纪初,以下是该行业的主要发展里程碑和阶段:
1. 20世纪初至20世纪50年代:这个时期主要是对传统的血液检测和尿液检测进行改进和发展。
医生和实验室技术人员开始使用一些基本的离心机、显微镜和试剂盒来进行血液和尿液分析,以进行基本的疾病诊断和监测。
2. 20世纪60年代至70年代:随着科学技术的进步,体外诊断技术得到了显著改进和发展。
在这个时期,单一物质的检测开始普及,例如血糖和血液中的特定蛋白质。
化学分析仪器、免疫测定技术和DNA检测方法的引入,使得诊断和监测更为精确和快速。
3. 20世纪80年代至90年代:该行业在这个时期取得了显著的技术突破和市场扩展。
大规模制造和商业化的自动化分析系统开始普及,简化了诊断过程并提高了诊断效率。
同时,免疫测定技术和分子生物学技术的进步,推动了更多新的诊断指标和方法的发展。
4. 21世纪初至今:随着基因组学和蛋白质组学等新型技术的快速发展,体外诊断技术得到了更大的革命性变革。
高通量筛查技术、基于微流控和纳米技术的检测方法开始应用于诊断和筛查领域。
个性化医疗的发展也促进了该行业的产品创新和市场增长。
总的来说,体外诊断行业经历了从传统的手工操作到自动化分析,再到高科技和个性化医疗的发展。
随着科技的不断进步,IVD行业在提高诊断效率和准确性方面发挥着越来越重要的作用。

一、体外诊断的定义及细分1.1.体外诊断定义体外诊断(In Vitro Diagnostics,IVD)是指在人体之外,通过对人体样本(血液、体液、组织等)进行检测获取临床诊断信息,进而判断机体功能和机体疾病的诊断方法。
除了某些特殊情形需要体内诊断以外,目前临床诊断信息的80%来自体外诊断。
体外诊断包括产品和服务,其中体外诊断试剂作为国家药监系统监管产品,由《体外诊断试剂注册管理办法》做出解释:按医疗器械管理的体外诊断试剂,包括可单独使用或与仪器、器具、设备或系统组合使用,在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中,用于对⼈体样本(各种体液、细胞、组织样本等)进⾏体外检测的试剂、试剂盒、校准品(物)、质控品(物)等。
1.2.体外诊断分类按照不同的检测原理或方法,体外诊断可分为生化诊断、免疫诊断、分子诊断、微生物诊断、尿液诊断、凝血类诊断、血液学和流式细胞诊断等,我国目前体外诊断的主要方法是生化诊断、免疫诊断和分子诊断。
下图为各分类体外诊断原料组成。
图表1:体外诊断分类简介数据来源:solarzoom、智银资本1.3.体外诊断试剂原料定义与分类体外诊断试剂原料指用于生化、免疫或分子诊断等试剂的反应体系原料,主要指核心反应体系。
上游诊断试剂原材料质量的好坏直接决定了体外诊断产品的质量,其中核心反应体系原材料如抗原、抗体、诊断酶是体外诊断质量控制最为重要的战略节点。
按照性质不同,体外诊断试剂原料可分为抗原、抗体、酶与辅酶、底物及标准品等类别。
图表2:体外诊断试剂原料的分类数据来源:IVD资讯网、头豹研究院、智银资本抗原与抗体、酶及辅酶是体外诊断试剂发挥诊断功能的重要组成成分,影响体外诊断试剂各项性能水平(如灵敏度、稳定性),是体外诊断试剂成本构成主要的部分,合计占据体外诊断原料市场75%以上的市场份额。
其他原料是除上述发生核心反应的活性物质外的原料,包括微球、磁珠、膜、引物、探针及其他化学及生物制品等。

体外诊断行业简介及分类⏹体外诊断产业定义:体外诊断产业(In Vitro Diagnosis,简写为IVD),从广义上讲,是指在人体之外,通过对人体的样品(血液、体液、组织等)进行检测而获取临床诊断信息的产品和服务。
从狭义上讲,体外诊断产业主要指体外诊断相关产品,包括体外诊断试剂及体外诊断仪器。
⏹体外诊断仪器主要有生化分析仪、血液分析仪、酶标仪、化学发光免疫分析仪、尿液分析仪、尿沉渣分析仪、实时荧光定量PCR仪等;体外诊断试剂则不仅包括进行体外检测直接使用的试剂,还包括相应的校准品、质控品、对照品等。
体外诊断仪器与相应的体外诊断试剂共同组成体外诊断系统。
⏹体外诊断产品分类:按检验原理或检验方法的不同,临床体外诊断主要分为血液学诊断、生化诊断、免疫诊断、分子诊断、尿液诊断、尿沉渣诊断、微生物诊断、凝血诊断等,其中血液、生化、免疫、尿液、尿沉渣诊断等临床最为常见。
体外诊断产品分类类别应用领域检验仪器主要特点血液学诊断红细胞、白细胞、血小板数量血液分析仪临床应用最普遍的诊断领域生化诊断糖类、脂类、蛋白类、无机元素类、肝功能、肾功能等生化分析仪医院常规检测项目,试剂消耗量大免疫诊断传染性疾病、性病、肿瘤、孕检、药物检测、血型鉴定等酶标仪灵敏度低,特异性差,但是成本低,中小医院仍有应用化学发光分析仪灵敏度高、特异性强,可定量分析,免疫分析技术发展方向胶体金快速诊断试剂快速方便,适合门急诊及家庭使用分子诊断传染病、性病、遗传病、肿瘤等实时荧光定量PCR仪灵敏度高、特异性强,诊断窗口期短,可进行定量检测尿液诊断尿液PH值、尿蛋白、尿糖等尿液分析仪医院常规检验项目尿沉渣诊断尿液红细胞、白细胞、上皮细胞等尿沉渣分析仪医院常规检验项目微生物诊断细菌类别检验微生物培养仪、鉴定仪外企近似垄断国内市场凝血诊断血栓与止血功能检验血凝仪希森美康近似垄断国内市场。

根据产品风险程度的高低,体外诊断试剂依次分为第三类、第二类、第一类产品。
(一)第三类产品:1.与致病性病原体抗原、抗体以及核酸等检测相关的试剂;2.与血型、组织配型相关的试剂;3.与人类基因检测相关的试剂;4.与遗传性疾病相关的试剂;5.与麻醉药品、精神药品、医疗用毒性药品检测相关的试剂;6.与治疗药物作用靶点检测相关的试剂;7.与肿瘤标志物检测相关的试剂;8.与变态反应(过敏原)相关的试剂。
(二)第二类产品:除已明确为第三类、第一类的产品,其他为第二类产品,主要包括:1.用于蛋白质检测的试剂;2.用于糖类检测的试剂;3.用于激素检测的试剂;4..用于酶类检测的试剂;5.用于酯类检测的试剂;6.用于维生素检测的试剂;7.用于无机离子检测的试剂;8.用于药物及药物代谢物检测的试剂;9.用于自身抗体检测的试剂;10.用于微生物鉴别或药敏试验的试剂;11.用于其他生理、生化或免疫功能指标检测的试剂。
(三)第一类产品:1.微生物培养基(不用于微生物鉴别和药敏试验);2.样本处理用产品,如溶血剂、稀释液、染色液等。
体外诊断试剂发展史体外诊断试剂行业的发展状况与上个世纪90年代初,家电产业的发展极为类似:一方面市场很大,另一方面,进口试剂及诊断仪器的垄断优势正在被民族产品打破和制约。
”这是对中国体外诊断试剂发展现状的总结。
中国体外诊断试剂产业发展总体表现出一种发展中大国的特点,那就是市场大,市场潜力更大。
中国有18000多家医院、300多个血站,同时,数以千计的体检中心以及数以百计的独立实验室正如雨后春笋般异军突起,一些独立的医学检验实验室也方兴未艾,这为体外诊断试剂的发展提供了广阔的市场空间。
中国人口占世界总人口的22%,但体外诊断试剂份额却只占全世界的2%,而且,近年来,各种新技术、新方法的兴起和融合,又促进了体外诊断试剂的开发应用和更新换代。
与此同时,随着人民群众收入的增加和生活标准的提高,人们对健康和医疗品质又有了更高的需求。

体外诊断试剂竞争分析报告.doc 体外诊断试剂竞争分析报告简介体外诊断试剂是一种用于检测人体样本的化学试剂。
随着医疗科技的发展,体外诊断试剂市场竞争日益激烈。
本文旨在对当前体外诊断试剂市场的竞争情况进行分析,为相关企业制定市场策略提供参考。
市场概述体外诊断试剂市场呈现出快速增长的趋势。
根据市场研究机构的数据显示,全球体外诊断试剂市场在2020年达到了1000亿美元的规模,预计在未来几年内将保持稳定增长。
市场的增长主要受益于人口老龄化趋势的影响以及对早期疾病诊断的需求增加。
市场竞争分析1.主要竞争对手当前体外诊断试剂市场上存在着众多主要竞争对手,包括但不限于___诊断、___医疗、___等。
这些公司不仅在产品研发和制造方面具备雄厚实力,还拥有广泛的销售渠道和客户群体。
2.产品差异化策略为了在激烈的竞争中脱颖而出,企业采取了多种产品差异化策略。
例如,一些企业注重研发高精度、高灵敏度的试剂,以满足医疗诊断的需求;另一些企业则专注于开发便携式试剂盒,方便用户在家中自行进行检测。
3.市场份额分析根据市场调研数据,目前市场上的体外诊断试剂部分竞争对手分布如下:___诊断:占据市场份额的25%___医疗:占据市场份额的20%___:占据市场份额的15%其他竞争对手:占据市场份额的40%市场趋势分析1.技术创新驱动体外诊断试剂市场正处于技术快速创新的阶段。
不断推出更加高效、准确的试剂是企业在市场上保持竞争力的重要手段。
例如,一些企业正在积极研发新型样本采集和分析方法,以进一步提高诊断的准确性和速度。
2.经济发展影响随着全球经济的发展,人们对健康需求的增加也在推动体外诊断试剂市场的增长。
尤其是新兴经济体的崛起带来了巨大的市场机会。
市场前景展望体外诊断试剂市场在未来几年内有望继续保持稳定增长。
随着技术的进步和人们对健康的关注度提高,市场需求将进一步增加。
同时,市场竞争也将变得更加激烈,企业需要持续关注市场动态,加强产品研发和市场营销,才能在竞争中保持优势。

中国体外诊断行业(IVD)简介什么是中国IVD?“IVD”是英文in vitro diagnostic products的缩写,中文译为体外诊断产品。
在国际上,IVD作为医疗器械的一个独立分支,拥有其特有的界定和法规监管体系,特别是美国食品药品监督管理局(FDA)与欧盟(EC)。
IVD主要包括用于体外诊断的仪器、试剂或系统。
但在中国情况却不同,IVD未被独立区分与界定,即没有IVD的概念。
而国际上通常的IVD 概念所包括的产品被打散,分别从属于医疗器械(Medical Devices,MD)、体外诊断试剂(IVD Reagents) 以及药品中。
在中国,除用于血源筛查与采用放射性核素标记被界定归属药品管理的体外诊断试剂,其它全部IVD产品均隶属于医疗器械(MD)。
医疗器械的定义在中国国务院2000年276号文《医疗器械监督管理条例》规定。
医疗器械是指单独或者组合使用于人体的仪器、设备、器具、材料或者其他物品,包括所需要的软件;其用于人体体表及体内的作用不是用药理学、免疫学或者代谢的手段获得,但是可能有这些手段参与并起一定的辅助作用;其使用旨在达到下列预期目的:(一)对疾病的预防、诊断、治疗、监护、缓解;(二)对损伤或者残疾的诊断、治疗、监护、缓解、补偿;(三)对解剖或者生理过程的研究、替代、调节;(四)妊娠控制。
并且规定对医疗器械实行分类管理。
根据风险以及采取的措施分为三级,由低到高为:第一类是指,通过常规管理足以保证其安全性、有效性的医疗器械。
第二类是指,对其安全性、有效性应当加以控制的医疗器械。
第三类是指,植入人体;用于支持、维持生命;对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。
但是依据实际需要,又将IVD试剂单独界定、独立管理。
并于2007年4至5月出台了从质量管理、生产、产品注册到经营的一系列法规与规则。
对体外诊断试剂的定义在2007年6月1日起实施的《体外诊断试剂注册管理办法(试行)》中有明确规定,即体外诊断试剂是指按医疗器械管理的体外诊断试剂,包括可单独使用或与仪器、器具、设备或系统组合使用,在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中,用于对人体样本(各种体液、细胞、组织样本等)进行体外检测的试剂、试剂盒、校准品(物)、质控品(物)等。
照 201 2年第29卷第1期 体外诊断试剂行业发展概述 谷威 ,潘峰 ,周飞。 (1.赤峰市疾病预防控制中心,赤峰024000;2.汕头金石粉针剂有限公司,汕头515041; 3.东南大学生物科学与医学工程学院,南京210096)
[关键词]体外诊断试剂;生化诊断试剂;免疫诊断试剂;分子诊断试剂;行业发展 [中图分类号]R446 [文献标识码]A [文章编号]2095—3593(2012)01.0098 04
随着科学技术的快速发展,尤其是现代生物技 术、单克隆抗体技术、微电子处理器、光化学等方面的 重要突破,体外诊断试剂行业先后经历了化学、酶、免 疫测定和探针技术四次技术革命,每一次技术革命都 使体外诊断试剂跨上了一个新的台阶,不仅灵敏度、特 异性有了极大提高,而且应用范围迅速扩大,操作门槛 逐步降低,商业价值也日趋重要。体外诊断试剂现已 发展成为拥有数百亿美元国际市场的朝阳产业。 我国检验医学的发展曾远远落后于世界先进水 平,极大地阻碍了我国体外诊断试剂的产业化发展。 建国后至70年代,我国的检验试剂基本由医院检验科 人员根据需要自行配制。20世纪70年代后,一些国 外先进设备和技术的引进,使得我国体外诊断试剂产 业化的雏形基本形成,但此时试剂往往由实验室制备, 没有统一的标准,也没有成型的生产和销售组织过程。 20世纪80年代以后,随着国家的改革开放,大量 国外先进技术进入中国,体外诊断试剂迅速步入产业 化进程,并涌现出一大批生产厂家。到20世纪90年 代初期,我国体外生化诊断试剂的生产厂家超过了100 家,体外免疫诊断试剂厂家超过了300家,但由于厂家 产品质量参差不齐,市场秩序较为混乱,国家从1993 年开始对体外诊断试剂行业开展整顿,取缔无生产资 质的厂家,吊销质量不合格厂家的生产文号。经过政 府管理和市场淘汰后,我国体外诊断试剂市场逐渐进 入快速健康发展阶段,行业集中度也有所提高l1J。 1体外诊断试剂定义及分类 体外诊断试剂是在疾病的预防、诊断、治疗监测、 预后观察、健康状态评价以及遗传性疾病的预测过程 中,用于对人体样本(各种体液、细胞、组织样本等)进 行体外检测的试剂、试剂盒、校准品、质控品等。 体外诊断试剂按检测原理分类,主要有生化诊断 试剂、免疫诊断试剂、分子诊断试剂、微生物诊断试 剂、尿液诊断试剂、凝血类诊断试剂、血液学和流式细 作者简介谷威,男,硕士,检验师,从事流感及手足【_=I病的疫情监测工作。 98· 胞诊断试剂等。其中生化、免疫、分子诊断试剂为我国 诊断试剂主要的三大类品种。 生化诊断试剂是通过各种生物化学反应或免疫反 应测定体内生化指标的试剂,主要用于配合手工、半自 动、全自动生化分析仪等仪器进行检测,测定酶类、糖 类、脂类、蛋白和非蛋白氮类、无机元素类、肝功能等指 标。 免疫诊断试剂是通过抗原与抗体相结合的特异性 反应进行测定的试剂,从结果判断的方法学上又可分 为放射免疫、胶体金、酶联免疫、时问分辨荧光、化学发 光等试剂,主要应用于传染性疾病、内分泌、肿瘤、药物 检测、血型鉴定等。 分子诊断试剂主要是对与疾病相关的蛋白质和各 种免疫活性分子以及编码这些分子的基因进行测定的 试剂,主要用于肝炎、性病、肺感染性疾病、优生优育、 遗传病基因、肿瘤等检测。分子诊断试剂主要有临床 己经使用的核酸扩增技术(PCR)产品和当前国内外正 在大力研究开发的基因芯片、蛋白芯片类产品I1]。 2体外诊断试剂产业链介绍 2.1上游原料主要依赖进口 体外诊断试剂的上游为生物化学原料,包括诊断 酶、抗原、抗体等活性生物制品以及高纯度氯化钠、碳 酸钠、谷氨酸、柠檬酸等精细化学品。诊断酶、抗原、抗 体为主要原料。其中酶类体外生化诊断试剂成本中诊 断酶约占60%。我国诊断酶几乎全部依靠进口,国内 仅少数厂家生产个别产品,且规模较小。由于我国在 主要生物化学原料方面的制备技术尚未完全成熟,体 外生化诊断试剂原料将在较长时间内维持依赖进口的 格局 ”。 2.2下游需求呈现刚性 体外诊断试剂的消费需求来自医学临床检验、血 液筛查、海关检测和食品安全检测等,其中医学检测是 体外诊断试剂最主要的消费领域,包括医院检验科、 体检中心、独立医学实验室、防疫站等。根据卫生部 2012,Vo1.29,No.1 趋势研究 Trend Study
62010年中国卫生统计年鉴》口],2009年我国卫生机构 总数为916 571家,其中医院数量为20 291家,这些 卫生机构是我国体外诊断试剂的主要用户。除了疾病 诊疗外,健康体检也需要大量使用诊断试剂产品。根 据教育部的统计,2010年我国高等教育毕结业人数 约1 393万人,招生人数约1 088万人,这些人员的毕 业体检、入学体检和求职应聘体检等需要约2 000万人 份的诊断试剂。血制品厂商和血站是体外诊断试剂的 另一个主要消费终端,根据中国输血协会的统计,我国 每年献血约900万人次,采血量约l 000万袋,这些血 液均须进行多项检测。随着生活水平的提高,人们对 健康的重视程度不断加强,对医疗保健的支出也相应 增加,体外诊断试剂作为不可重复使用的医疗消费品, 其市场需求具有持续性、抗经济周期能力强等特点。 3市场需求状况 3.1市场需求现状 目前全球体外诊断需求市场主要分布在北美、欧 洲、日本等发达经济体国家;中国、印度、巴西等新兴经 济体国家由于人口基数大、经济增速高,近几年医疗保 障投入和人均医疗消费支出持续增长,由此带动体外 诊断市场需求。根据Kalorama Information的市场报 告,2008年北美、欧盟、日本三者合计占全球体外诊断 市场份额超过80%,中国、印度、拉美、东欧等合计占比 约10%,市场分布不均衡,也体现出体外诊断作为新兴 产业,在广大发展中国家有良好的发展空间口]。 3.2市场需求发展趋势 我国体外诊断试剂行业现己具备一定的市场规模 和基础,正从产业导入期步入成长期,市场发展前景良 好。根据预测,2008 ̄2012年,中国体外诊断市场规 模增速将显著高于全球平均水平,年复合增长率将保 持在16%左右。 2010年我国体外诊断市场规模为20.7亿美元f约 合136.8亿元),其中体外诊断仪器市场规模为5.7亿 美元(约合37.8亿元),体外诊断试剂市场规模为15.0 亿美元(约合99亿元)。中国人口占世界的1/5,但体 外诊断市场份额仅为全球的3%,且中国体外诊断产品 人均年使用量仅为1.5美元,而发达国家人均使用量 达到25~30美元,因此中国体外诊断市场增长空间 广阔,预计未来数年将保持15%~20%的增速。预测 2012年我国体外诊断试剂市场规模将超过133亿元, 2015年将在目前的市场规模上实现翻番,达到208亿 元,具有广阔的市场成长空间。 3.3主要品种发展趋势 目前我国体外诊断试剂市场主要由生化诊断试 剂、免疫诊断试剂、分子诊断试剂、血液学诊断试剂等 部分构成,其中免疫诊断试剂市场份额达到33%;生 化诊断份额为27%;血液学和流式细胞为15%,分子 诊断为5%,其它还包括尿液和凝血类诊断试剂等。 生化诊断试剂主要应用于医院的常规检测项目, 也是医疗检测的基本组成部分,在免疫诊断试剂规模 逐步扩大的同时,生化诊断试剂凭借成本低、速度快的 优势,仍将保持较大的市场份额,其未来发展主要体 现在两个方面:一是原有检测项目上将着眼于产品质 量的持续提高,二是技术进步带来的新检测项目的持 续开发。随着县级医院全自动生化分析仪和基层医院 半自动生化分析仪的普及,预计未来几年,我国生化诊 断试剂市场将呈现超过行业平均增长速度的高速增 长[4l0 免疫诊断试剂在诊断试剂盒中品种最多,主要有 放射免疫、胶体金、酶联免疫、时问分辨荧光、化学发光 试剂等。放射免疫试剂由于对环境污染较大,目前在 国际市场上己被淘汰,国内还有少量使用。酶联免疫 试剂具有成本低、可大规模操作等特点,是目前免疫诊 断试剂中的主流。化学发光试剂灵敏度高、特异性强, 可用于半定量和定量分析,是免疫试剂的重要发展方 向之一,主要用于其他方法目前较难测定的一些项目, 随着研发生产技术的成熟和成本的降低,最终可能替 代酶联免疫试剂,成为市场的主流。胶体金是目前最 快速方便的免疫学检测技术之一,特别适合于医院的 急诊化验室、监护病房、门诊即时检验,以及家庭、社区 医疗、医师诊断和事故现场等医院外的即时检验、大批 量时间紧的检测和大面积普查等,发展潜力巨大。 分子诊断试剂主要有临床己经使用的PCR产 品和当前国内外正在大力研究开发的基因芯片产品。 PCR产品灵敏度高、特异性强、诊断窗口期短,可进行 定性、定量检测,可用于肝炎、性病、肺感染性疾病、优 生优育、遗传病基因、肿瘤等的检测。基因芯片是分子 生物学、微电子、计算机等多学科结合的结晶,但成本 高、开发难度大,目前产品种类很少,一股用于科研和 药物筛选等用途。 根据Kalorama Information的预测,在总体市场 规模快速增长的同时,我国诊断试剂主要品种的市场 需求也将迅速增长。2008~2012年,我国体外诊断试 剂市场主要由生化、免疫和分子诊断试剂构成,且三大 品种增长迅速,其中分子诊断试剂增速最高,年复合 增长率可达20%,其次为免疫诊断试剂,年复合增长率 为18%,生化和其他诊断试剂的年复合增长率也将达 到15%。 201 2年第29卷第1期 4行业竞争格局 4.1国际竞争格局 经过多年发展,全球体外诊断已成为拥有数百亿 美元庞大市场容量的朝阳行业,产业发展成熟,市场 集中度较高,并聚集了一批著名跨国企业集团,包括罗 氏、西门子、雅培、贝克曼、Becton Dickinson fBD)、强 生、生物梅里埃、伯乐等。这些企业集团下属体外诊断 业务年销售收入均在10亿美元以上,产品线丰富,不 仅包括各类体外诊断试剂,还包括各类诊断仪器以及 与之相关的医疗技术服务。 4.2国内竞争格局 体外诊断试剂行业在我国属于新兴产业,与欧美 国家相比起步晚,产业化发展相对滞后。目前我国体 外诊断试剂生产企业约300~400家,其中规模以上 企业近200家,但年销售收入过亿元的企业仅约20 家,企业普遍规模小、品种少。 近几年我国体外诊断试剂行业已从导入期步入发 展期,市场需求快速增长,国内企业抓住机遇,凭借产 品性价比高和更为贴近本土市场的优势,不断抢占份 额,致使原以进口产品为主导的市场格局被逐渐打破。 随着研发投入的加大和产品质量水平的提升,我国体 外诊断试剂行业现己涌现一批实力较强的本土企业, 集中在生化、免疫、分子诊断三大领域,并在某些产品 领域逐渐具备与国际巨头竞争的实力。 总体而言,国内企业市场割据竞争的格局较为明 显,实力较强的综合性企业还较少,行业排名靠前的 企业主要是在某一领域具备竞争优势。目前国内各领 域领先企业正积极进行多元化发展,一是依托原有优 势纷纷进入生化、免疫、分子诊断试剂等多个领域,以 丰富试剂产品种类;二是开展上游核心原料以及配套 诊断仪器的自主研发生产,以增强市场竞争实力;三 是开始积极开拓国外市场,尤其是亚非拉等发展中国 家市场。随着国内领先企业技术研发实力的提升和经 营规模的壮大,预期行业市场集中度将进一步提高, 同时国内领先企业与国外企业在高端市场的竞争能力 也将快速提升。 4.3行业内主要领域及代表企业 4.3.1生化诊断试剂我国生化诊断试剂市场起步最 早,发展较成熟。McEvoy&Farmer《中国临床诊 断市场(2ol11》指出,目前我国生化诊断试剂市场 约三分之二的份额已由国产品牌占据,主要企业有 利德曼、中生北控、北京九强、科华生物、四川I迈克 等。经过多年发展,我国在生化诊断试剂领域的自 1 00· 主创新能力和竞争实力显著提升,整体技术水平已 基本达到国际同期水平,试剂品种已较为齐全,生 化分析仪的生产厂商也逐渐增多,并涌现出一些具 备与国际巨头竞争的企业。随着国内企业技术水平 及其产品质量的进一步提升,未来生化诊断试剂市 场的国产化替代趋势将进一步加强,同时国内企业 与国外企业在高端市场的竞争也将进一步加剧。 4.3.2免疫诊断试剂我国免疫诊断试剂发展初期以放 射免疫试剂作为起步,但由于其对环境污染较大,国 内目前仅少量中小厂商生产销售,现市场主要应用品 种为酶联免疫、化学发光、时间分辨荧光和胶体金试剂, 其中酶联免疫和化学发光是应用主流【5】。 《中国临床诊断市场f20l1)》指出,目前我国免疫 诊断试剂市场60%以上的份额仍由国外品牌占据,主 要企业为罗氏、西门子、雅培等,国内产品主要集中在 酶联免疫试剂,主要企业有北京万泰、科华生物等。目 前国产酶联免疫试剂主要集中在肝炎及性病的临床诊 断上,特别是乙肝就占60%以上,生产厂家较多,竞 争较为激烈【6J。 化学发光是近l0多年发展起来的免疫诊断技术, 在欧美等发达国家已进入成熟期,并已成为免疫检测 的主流方法。化学发光试剂技术门槛较高,使用时须 与相应的封闭式化学发光仪配套,在我国尚处于发展 初期,现市场主要为进口品牌占据,国内主要企业有深 圳新产业和北京倍爱康。 4.3.3分子诊断试剂我国分子诊断市场起步最晚但技 术起点较高,且由于市场容量基数相对较小,近年来 增长速度最快。分子诊断试剂综合了多种高精尖技术, 进入门槛较高,目前临床应用产品主要是核酸扩增技 术(PCR)试剂系列。分子诊断市场目前以国内企业为 主,主要企业包括达安基因、深圳匹基、科华生物、复 星医药等,由于专利原因国外也只有少数几家企业生 产该类产品,如罗氏、雅培等公司有部分产品进入中国 市场t7]。 4.4行业利润水平及其变动趋势 体外诊断试剂行业属于高技术行业,整体利润水 平较高,企业综合毛利率一般在55%以上,新产品上 市后2~3年即可收回投资,特别是具有技术垄断优 势的新产品,利润回报更高。此外,行业具有规模经 济特征,大批量品种盈利能力强,小批量品种往往亏 损。目前我国体外诊断试剂市场集中度不高,行业内 还存在大量中小型规模企业,随着国家对行业准入和 产品质量要求的进一步提升以及国外领先企业对我国