儿童嗜血细胞综合征
- 格式:ppt
- 大小:681.00 KB
- 文档页数:34





嗜血细胞综合症亦称嗜血细胞性淋巴细胞增生症 (hemophagocytic lymphohistioicytosissyndromeHPLS),属于组织细胞增生症Ⅱ型,包括家族性和继发性2类.家族性嗜血细胞综合症(FHLH)是一种少见的常染色体阳性遗传病,患儿出生时正常,多于6月一1岁突然高热、黄疸、出血、肝脾肿大,少数有惊厥.中约50%有阳性家族史,临床呈致死性经过,未经治疗者中位数生存期为2个月,系l0号染色体基因缺陷所致,通常2岁以下者考虑FHLH.继发性HPS可分为感染相关性和肿瘤相关性.既往认为感染相关性主要为病毒感染,如巨细胞病毒、单纯疱疹病毒、水痘一带状疱疹病毒、流感病毒、人类细小病毒 B19,目前认识到本病也可由肠道革兰氏阴性杆菌、流感嗜血杆菌、肺炎球菌、葡萄球菌、布氏杆菌、真菌及杜氏利什曼原虫等所.肿瘤相关性继发于患血液系统或非血液系统恶性疾病的病人,由于恶性疾病本身及化疗、放疗所致免疫抑制状态引起对感染易感增高所致.另外系统性红斑狼疮及先天免疫缺陷患儿也可并发此病.HPS最显著的病理特征是良性组织细胞增加并伴嗜血现象,多见于淋巴结的淋巴窦和髓索、肝窦、门静脉、脾脏的红髓和骨髓.在急性期,该病与白血病、恶性组织细胞增生症、传染性单核细胞增生症等病相似,且并非所有病例第一次骨穿即能发现嗜血细胞,有时需多部位穿刺才能确诊.HPS的治疗及预后决定于疾病类型.目前治疗主要为(1)丙球或肾上腺皮质激素或大剂量甲强冲击,(2)抑制T细胞活化的特异性抑制剂cytA或联用粒细胞集落刺激因子,(3)为减少或抑制淋巴因子的供应原可用化疗,(4)化疗后造血干细胞移植或血浆置换.1994年国际组织细胞协会建议应用HIM一94方案:化疗加免疫疗法(足叶乙甙+糖皮质激素+cytA)+MTX鞘注.丙球的疗效仍有争议.我们在以后的工作中应提高对该病的认识,减少误诊,并进一步观察该病的疗效.--------------------------------------------------------------------------------噬血细胞综合征(hemophagocyticsyndrome,HPS)亦称噬血细胞性淋巴组织细胞增生症(hemophagocyticlymphohistocytosis),又称噬血细胞性网状细胞增生症 (hemophagocyticreticulosis),于1979年首先由Risdall等报告.其特征是发热,肝脾肿大,全血细胞减少.本综合征分为两大类,一类为原发性或家族性,另一类为继发性,后者可由感染及肿瘤所致.原发性HPS,或称家族性HPS,为常染色体隐性遗传病,其发病和病情加剧常与感染有关;继发性HPS分为感染相关性HPS(infection-associatedhemophagocyticsyndrome,IAHS),此型多与病毒感染有关,由病毒引起者称病毒相关性HPS(virus-associatedhemophagocyticsyndrome,VAHS); 由肿瘤引起者称肿瘤相关性HPS(malignancy-associatedhemophagnocyticsyndrome,MAHS).1.家族性噬血细胞综合征(familialhemophagocyticsyndrome)1.1发病年龄一般早期发病,70%发生于1岁以内,甚至可在生前发病,出生时即有临床表现.多数在婴幼儿期发病,但也有迟至8岁发病者.成年发病亦不能排除家族性HPS.在同一家族中,其发病年龄相似.1.2症状体征,症状多样,早期多为发热、肝、脾肿大,有的有皮疹、淋巴结肿大和神经症状.发热持续,亦可自行退热; 肝脾肿大明显,且呈进行性;皮疹无特征性,常为一过性,往往出皮疹时伴高热;约有一半病人有淋巴结肿大,有的有巨大淋巴结.中枢神经系统的症状一般在病程晚期出现,但也可发生在早期,表现为兴奋性增高、前囟饱胀、颈强直、肌张力增强或降低、抽搐等.亦可有第VI或第VII对颅神经麻痹、共济失调偏瘫或全瘫、失明、意识障碍、颅内压增高等.肺部的症状多为肺部淋巴细胞及巨噬细胞浸润所致,但难与感染鉴别.1.3实验室检查血象:多为全血细胞减少,以血小板减少为明显,白细胞减少的程度较轻;观察血小板的变化,可作为本病活动性的一个指征.病情缓解时,首先可见到血小板上升;而在病情恶化时,亦首先见到血小板下降.骨髓象:骨髓在疾病早期的表现为中等度的增生性骨髓象,噬血现象不明显,常表现为反应性组织细胞增生,无恶性细胞浸润,应连续多次检查骨髓,以便发现吞噬现象.该病的极期除组织细胞增多外,有多少不等的吞噬性组织细胞,主要吞噬红细胞,也可吞噬血小板及有核细胞.晚期骨髓增生度降低,这很难与细胞毒性药物所致的骨髓抑制鉴别.有的病例其骨髓可见大的颗粒状淋巴细胞,胞体延长如马尾或松粒状,这可能是HPS的一种特殊类型的淋巴细胞.高细胞因子血症:在家族性HPS及继发性HPS的活动期常见下列因子增多:IL-l受体拮抗因子、可溶性IL-2受体(sIL-2)、γ-干扰素(IFN-γ)、肿瘤坏死因子(TNF)等.血脂:可见甘油3酯增多,可在疾病的早期出现,脂蛋白电泳常见极低密度脂蛋白胆固醇及低密度脂蛋白胆固醇升高,高密度脂蛋白胆固醇降低.当病情缓解时,脂蛋白胆固醇可恢复正常.肝功能:转氨酶及胆红素可增高,其改变的程度与肝受累的程度一致.在全身感染时,可有低钠血症、低白蛋白血症及血清铁蛋白增多.凝血象:在疾病活动时,常有凝血异常,特别是在疾病活动期,有低纤维蛋白原血症,部分凝血活酶时间延长,在有肝受损时,其凝血酶原时间可延长.脑脊液:中等量的细胞增多(5-50×106/L),主要为淋巴细胞,可能有单核细胞,但很少有噬血细胞,蛋白增多,但有的即使有脑炎的临床表现,其脑脊液亦可能正常.免疫学检查:家族性HPS常有自然杀伤细胞及T细胞活性降低.影像检查:部分病人胸片可见间质性肺浸润,晚期病人头颅CT或MRI检查可发现异常,其改变为陈旧性或活动性感染,脱髓鞘,出血,萎缩或(及)水肿.有时亦可通过CT检查发现脑部钙化.1.4病理主要的发现是在单核-巨噬细胞系统发现良性的淋巴组织细胞浸润,组织细胞呈吞噬现象,吞噬最多的是红细胞,有时也吞噬血小板和白细胞.受累器官为脾、淋巴结、骨髓和脑.脊髓;此外,还可见于甲状腺、肺、心.肠、肾和胰腺.1.5诊断诊断标准为:①发热超过1周,热峰≥38.5℃;②肝脾肿大伴全血细胞减少,累及≥2个细胞系,骨髓增生减少或增生异常及肝功能异常,血乳酸脱氢酶(LDH)≥1000U/L或≥正常均值+3S,及凝血功能障碍,血纤维蛋白原≤1.5g/L,伴血病铁蛋白≥1000ng/mL或≥正常+3s;④噬血细胞占骨髓有核细胞≥2%,或(和)累及骨髓、肝、脾.淋巴结及中枢神经系统的组织学改变.有些不典型病例不符合上述标准,如主要为脑膜受累及新生儿期发病者,发热则不明显;而血细胞减少,高脂血症及低纤维蛋白原血症的表现也取决于内脏受累的严重程度,有些病人上述表现可能晚期才出现.起病时,有不少病人可以无脾大,甚至没有噬血细胞现象.1.6鉴别诊断最容易混淆的是家族性HPS与继发性HPS,特别是与病毒相关性HPS的鉴别,因为病毒感染不但与病毒相关性HPS有关,在家族性HPS患者,也常有病毒感染,而且家族性HPS也常由病毒感染而诱发.家族性HPS为常染色体隐性遗传病,常问不到家族史,更增加了诊断的难度.一般认为,在2岁前发病者多提示为家族性HPS,而8岁后发病者,则多考虑为继发性HPS.在2~8岁之间发病者,则要根据临床表现来判断,如果还难肯定,则应按家族性HPS处理.其次要与恶性组织细胞病(恶组)相鉴别,2者在骨髓片上很难鉴别,但HPS要比恶组常见得多.但如临床上呈暴发经过、严重肝功能损害、骨髓中组织细胞恶性程度高,特别是肝、脾或其他器官发现异常组织细胞浸润,则先考虑为恶组为宜;否则应诊断为HPS.1.7治疗a.化学疗法:常用的化疗药物有细胞毒性药物,如长青花碱或长春新碱与肾上腺皮质激素联用,亦可应用反复的血浆置换,或 VP16或VM26与肾上腺皮质激素合用.有的应用VP16、肾上腺皮质激素,鞘内注射氨甲煤呤(MTX)及头颅照射治疗取得良好效果.有的主张在缓解时,应用上述药物小剂量维持治疗.b.免疫治疗:有人用环胞菌素A治疗家族性HPS取得满意效果,同样,用抗胸腺细胞球蛋白(ATG)亦可诱导缓解.c.造血干细胞移植:尽管上述化疗可使病情缓解,有的可缓解9年,但仍不能根治家族性HPS.Fisher 等(1986)首先报告用骨髓移植治愈家族性HSP患者,在2000年上海举行的国际小儿血液肿瘤学术研讨会上,日本学者Imashukn报告5例由 EBV所致的HPS,应用造血干细胞移植,随后用环胞菌素A加VP16,大大改善了本病的预后.d.治疗方案:国际组织细胞协会 1994年提出一个治疗家族性HPS的方案(HLH94):地塞米松每日10mg/m2与VP16每周150mg/m2,连用3周,第4周起减量,第9周起VP16每2周用药1次,并加用环胞菌素A每日5~6mg/kg口服,共用1年.有神经症状者,前8周每2周鞘内注射MTX1次.如果是家族性HPS,争取做异基因造血干细胞移植.如果为非家族性HPS,则在8周治疗后根据病情停止治疗.1.8预后不经治疗的家族性HPS患者存活期约2个月,而在应用化疗后则大大改善了预后.有的患者经化疗后存活9年以上,但只有异基因造血干细胞移植才能治愈家族性HPS.2继发性噬血细胞综合征(secondaryhemoPhagocyticsyndrome)2.1感染相关性噬血细胞综合征(IAHS)严重感染引起的强烈免疫反应,淋巴组织细胞增生伴吞噬血细胞现象,本病常发生于免疫缺陷者,由病毒感染所致者称病毒相关性HPS(VAH),但其它微生物感染,如细菌、真菌、立克次体、原虫等感染也可引起HPS.其临床表现除有HPS的共同表现(如前所述)外,还有感染的证据.骨髓检查有淋巴组织细胞增生,并有吞噬红细胞、血小板和有核细胞现象.2.l.l预后有人对198例小儿感染相关性HPS进行了追踪.其中103例(52%)死于全血细胞减少、器官衰竭或弥漫性血管内凝血(DIC).3岁以下6例有3例死亡,而3岁以上的病例76例仅有29例死亡.l岁以下患病者,其预后极差,29例只有9例存活.由细菌引起者预后较好,EB病毒所致者预后最差,99例EB 病毒所致者,死亡72例,其它病毒所致者,其病死率亦在 50%左右.2.1.2治疗应用免疫抑制剂治疗,多用肾上腺皮质激素及(或)VP16,取得较好的效果.特别是对EB病毒所致者,VP16及环胞菌素A的效果最好,因为VP16可抑制病毒的核抗原合成,环胞菌素A可减轻高细胞因子血症.至于静脉丙种球蛋白的应用,却有不同意见. 有人主张应用,有人则反对应用.治疗本病的目的是抑制其难于控制的淋巴细胞和巨噬细胞活性.如能发现病原微生物,则应及时应用有效的抗微生物治疗.如果是在应用免疫抑制剂时发生的HPS,则应停用免疫抑制剂.威胁生命的表现是难于控制的高热、进行性全血细胞减少、DIC 及多器官功能衰竭,这些都是应用免疫抑制剂的指征.其治疗方案与家族性HPS 相同.2.2肿瘤相关性噬血细胞综合征(malignancy- associatedhemophagocyticsyndrome,MAHS)本病分为两大类:一类是急性淋巴细胞白血病(急淋)相关的HPS,急淋在治疗前或治疗中可能合并有感染或没有感染伴发的HPS.除急淋外,纵隔的精原细胞瘤(mediactinalgermcelltum)也常发生继发性 HPS.第2类是淋巴瘤相关的HPS(lymphoma-associatedhemophagocytic,syndrome,LAllS),淋巴瘤常为亚临床型,没有淋巴瘤的表现,故往往误诊为感染相关性HPS,特别容易误诊为EB 病毒相关性淋巴瘤.治疗:治疗方案决定于疾病的类型,如HPS发生于治疗前的免疫缺陷患者,则治疗主要是抗感染及抗肿瘤;如果HPS发生于化疗后,而肿瘤已缓解则应停止抗肿瘤治疗,同时抗感染,加用肾上腺皮质激素及VP16;对进展迅速的MAHS则应针对细胞因子所致的损害进行治疗,可用前述HLH94方案.--------------------------------------------------------------------------------谢谢拉,不知道应该如何与恶性组织细胞增生症鉴别呢?--------------------------------------------------------------------------------自己查阅文献及一些资料,总结了几点,请同道指正:一.诊断标准1.发热超过1周,热峰≥38.5℃;2.肝脾肿大伴全血细胞减少,累及≥2个细胞系,骨髓增生减少或增生异常及肝功能异常,血乳酸脱氢酶(LDH)≥1000U/L或≥正常均值+3S,及凝血功能障碍,血纤维蛋白原≤1.5g/L,伴血病铁蛋白≥1000ng/mL或≥正常+3s;3.噬血细胞占骨髓有核细胞≥2%,或(和)累及骨髓、肝、脾.淋巴结及中枢神经系统的组织学改变.2.与恶组鉴别1.病因:多数HPS患者经细菌培养、血清免疫学、组织病理学等检查可找到原发病;MH常为病因不明.2.对治疗的反应:HPS经针对原发病进行治疗往往有效,多数患者随原发病好转而恢复;MH患者病情进展快,预后差,抗生素、抗病毒、激素治疗无效,绝大多数患者在数月内死亡.3.骨髓特点:HPS患者骨髓组织细胞增生以Hem为主,异常组织细胞不见或偶见,多核巨组织细胞不见;MH半数以上患者伴有Hem及单核样或淋巴样组织细胞增生,但常见有幼稚多形态的异常组织细胞,多核巨组织细胞虽亦有较大诊断价值,但检出率较低.MH由于病变分布具有高度局灶性和不规则性,对伴Hem增生疑为HPS的患者,如病因不明,应在病程不同阶段多部位多次骨髓穿刺或行病变组织活检,以提高异常组织细胞检出率4.NAP积分对细菌相关性HPS与MH的鉴别有一定参考意义,多数BHPS患者NAP积分增高,而MH患者NAP积分常降低甚至为0.回复时间:2008-5-8 19:00:57投诉•网友回复区•••月月红天••嗜血细胞综合征可分为原发生和反应性,潜在疾患可为感染、肿瘤、免疫介导性疾病等,由于噬血细胞增多,加速了血细胞的破坏.帮你在网上当了2个诊断标准1发热;2肝脾肿大;3血细胞减少(外周血2或血3系细胞减少),其中血红蛋白<90g/L,血小板<100x109/L,中性粒细胞<1.Ox109/L;4高甘油3醋血症和/或低纤维蛋白原血症;5骨髓、脾或淋巴结可见噬血细胞但无恶性表现.I)发热超过1周,热峰>38.5C;(2)肝脾大伴全血细胞减少,累计>2个细胞系; (3)骨髓增生减少或增生异常,嗜血细胞占骨髓有核细胞>2%;(4)肝功能异常,血乳酸脱氢酶>1000U/L或>正常均值+3s现在好像这个病打的有点滥了,找不出病因,看到几个吞噬细胞就是感染性嗜血细胞综合症是一种与急性病毒感染有关的良性噬血组织细胞增生症,多发于儿童,其特点为单核-巨噬细胞增生活跃,并有明显的吞噬红细胞现象.患者多有明显高热,肝、脾和淋巴结肿大,原发病治疗好后多可自愈.患者有贫血现象,白细胞明显减少,分类可见淋巴细胞明显增高,易见异淋.血小板常减低.骨髓多增生活跃,粒系统所占比例降低,中性粒细胞可见毒性变.幼红系统增生多正常,淋巴系统比例亦未见明显改变,可见异淋.单核巨噬系统增生活跃,常>10%,巨噬细胞大小为20~40微米,或更大,胞浆丰富,吞噬多个成熟红细胞,或幼红细胞或血小板等.巨核细胞大致正常.回复时间:2008-5-8 18:49:17投诉••psxfcsz••1发热;2肝脾肿大;3血细胞减少(外周血2 或血3系细胞减少),其中血红蛋白<90g/L,血小板<100x109/L,中性粒细胞<1.Ox109/L;4高甘油3醋血症和 /或低纤维蛋白原血症;5骨髓、脾或淋巴结可见噬血细胞但无恶性表现.。


(一)发热原因待查:根据患儿发热病史大于14天,伴肝脾增大,血象三系进行性下降,故考虑发热原因待查, 分析如下:1.噬血细胞综合征:根据患儿发热时间长,伴肝脾增大,血象三系进行性下降,谷丙转氨酶、谷草转氨酶、乳酸托氢酶、甘油三酯升高,纤维蛋白原降低,骨髓象可见吞噬细胞及分类不明细胞,故考虑本病可能性大。
噬血细胞综合征可分为家族遗传性噬血细胞综合征及后天获得性噬血细胞综合征,后者多为感染相关或肿瘤相关,患儿支原体抗体阳性,EBV-CA-IgG弱阳性,NA-lgG阳性,骨髓象可见分类不明细胞,目前感染相关或肿瘤相关噬血细胞综合征均不能除外。
入院后复查骨穿及其他检查协诊。
2.败血症:本病可以引起长期发热,肝脾肿大,应注意本病,但本患儿感染中毒症状不重,血象三系进行性下降,目前诊断依据不足,可以进一步做血培养协诊诊断。
3.传染性单核细胞增多症:EB病毒感染可以引起发热,多伴有肝脾,淋巴结肿大,皮疹,血象不高,淋巴分类为主, 外周血可以见到异形淋巴细胞。
木患儿发热,肝脾肿大血象不高,淋巴分类为主故应考虑本病,但其EBV未提示近期感染,进一步行EB四项及滴度以协诊。
4.肺结核:临床表现为长期不规则的低热,轻咳,食欲不振,盗汗,乏力,消瘦等。
本患儿长期发热, 消瘦,卡疤阴性,抗炎治疗效果不佳,应考虑本病,但其无结核接触史,无盗汗,乏力等结核感染中毒症状,胸片无典型肺结核表现,故考虑可能性不大,进一步做PPD及肺CT协助诊断。
(二)支气管炎患儿有咳嗽、有痰,双肺呼吸音粗,未及啰音,胸片示两肺纹理增多,模糊毛糙,右下肺为著,未见具体片影,故诊断支气管炎成立。
结合其年龄、血象考虑病毒感染可能性大,患儿支原体抗体阳性,亦需注意支原体感染。
入院后完善病原检查以协诊。
1.积极完善相关检查:血尿便常规,生化全项心肌酶,骨穿,头颅及胸腹部CT协诊有无占位。
2.抗感染治疗:其支原体抗体阳性,予舒美特10mg∕Kg.d,实予0.2g日1次静点抗感染。

噬血细胞综合征治疗进展噬血细胞综合征(HLH)是一种罕见的炎症性疾病,特征为异常活跃的免疫系统导致过度的炎症反应。
它可以是遗传性的(常见于儿童)或是获得性的(常见于成年人),并且可由感染、肿瘤、自身免疫疾病等因素引起。
传统的HLH治疗方法主要包括糖皮质激素和化疗药物,如顺铂、蒽环类等,并且需要进行造血干细胞移植。
由于HLH病因复杂,疾病进展迅速且病情严重,常规治疗方法存在一定的限制和不足。
近年来,随着对HLH发病机制的进一步了解和治疗技术的进步,新的治疗方法被提出并取得了一定的进展。
以下将针对这些新的治疗方法进行介绍。
1. 靶向治疗:针对HLH发病机制中的关键分子进行干预是一种新的治疗策略。
使用干扰素伽玛(IFN-γ)治疗HLH可以抑制过度激活的免疫系统,减轻炎症反应。
抗炎细胞因子IL-1β抑制剂(如阿那帕塞塞)也被应用于HLH治疗中。
这些药物能够抑制过度激活的免疫细胞,并具有降低炎症水平的作用。
2. 免疫调节治疗:免疫调节治疗通过调节免疫系统的功能来改善HLH患者的病情。
免疫调节治疗的一个重要方向是免疫抑制剂的应用。
环孢素A(CsA)和他克莫司(Tac)是常用的免疫抑制剂,它们可以抑制T细胞的激活和增殖,从而减轻HLH患者的炎症反应。
3. 基因治疗:基因治疗是一种治疗方法,通过改造患者的基因来修复HLH病因所在的基因缺陷。
目前,基因治疗在治疗遗传性HLH方面取得了一定的进展。
逆转录酶病毒媒介的基因敲除技术可以矫正患者HLH相关基因的突变,从而修复异常的免疫功能。
4. 细胞治疗:细胞治疗是一种新兴的HLH治疗方法,通过植入患者体内的免疫细胞来增强免疫功能。
来自供者的造血干细胞移植已被广泛应用于HLH的治疗中。
使用CAR-T细胞疗法也被探索用于HLH的治疗。
CAR-T细胞通过植入经过工程化的T细胞来识别和攻击HLH病因所在的细胞。
随着对HLH治疗机制的深入研究,新的治疗方法不断涌现并且取得了显著的疗效。
噬血细胞综合征噬血细胞综合征(hemophagocytic syndrome,HPS),是一组骨髓、脾脏、淋巴结等造血组织中良性、反应性增生的组织细胞吞噬自身血细胞而引发的一系列临床病症。
临床表现为持续高热,肝、脾、淋巴结大,外周血细胞减少,肝功能异常,凝血功能障碍等。
1979年首先由Risdull等报告,多发于儿童。
可由感染病毒,或是因为用药不当,以及体内有肿瘤(对于小孩来说肿瘤几率低)等诱发,由于婴幼儿自身抵抗能力弱,调节不当,致使单核巨噬细胞增生而且对自身血细胞发生攻击并消除,使得婴儿贫血导致死亡。
嗜血细胞综合征 - 分类原发性HPS,或称家族性HPS,为常染色体隐性遗传病,其发病和病情加剧常与感染有关.继发性HPS分为感染相关性HPS(infection—associatedhemophagocytic syndrome,IAHS),此型多与病毒感染有关,由病毒引起者称病毒相关性HPS (virus-associated hemophagocyticsyndrome,VAHS);由肿瘤引起者称肿瘤相关性HPS(malignancy-associated hemophagnocytic syndrome,MAHS)。
嗜血细胞综合征 - 流行病学本病以儿童多见,男性多于女性。
儿童原发性HLH(FHL)的年发病率约为0.12/1O 万,80%的患者在2岁以前发病.继发性HPS在任何年龄均可发病.所以,一般认为2岁前发病者提示的原发性可能性大,8岁后发病者则提示继发性的可能性大,2-8岁发病者则根据临床表现进行判断.在日本和亚洲国家发病率较高。
本病来势凶险,东方患者的死亡率约为45%。
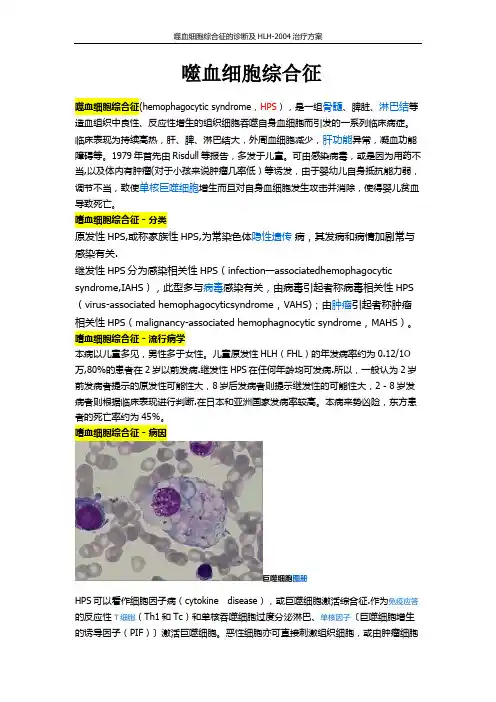
嗜血细胞综合征 - 病因巨噬细胞图册HPS可以看作细胞因子病(cytokine disease),或巨噬细胞激活综合征.作为免疫应答的反应性T细胞(Th1和Tc)和单核吞噬细胞过度分泌淋巴、单核因子〔巨噬细胞增生的诱导因子(PIF)〕激活巨噬细胞。


附件4儿童噬血细胞综合征诊疗规范(2019版)一、概述噬血细胞性淋巴组织细胞增生症(hemophagocytic lymphohistiocytosis,HLH),又称噬血细胞综合征,是一组由于细胞因子风暴引起的淋巴细胞、巨噬细胞增生和活化,伴随吞噬血细胞现象的一类综合征。
依据病因又分为原发性HLH(primary HLH,pHLH)和继发性HLH(secondary HLH, sHLH)两种类型。
pHLH为常染色体或X连锁隐性遗传,伴有相关基因异常;sHLH可继发于各种病毒(如EBV)、细菌、寄生虫所引起的感染、风湿免疫性疾病、代谢性疾病及肿瘤等。
二、适用范围满足2004年国际组织细胞协会制定的诊断标准的HLH患儿。
三、诊断(一)临床表现1.发热:最常见,间断或持续发热,体温常>38.5℃,热型不定,可呈波动性或迁延性,也可自行消退。
2.肝、脾、淋巴结肿大:往往显著并呈进行性发展,脾肿大更有临床意义,部分患者伴有黄疸。
3.皮疹:多样,可为全身斑丘疹、红斑、水肿、麻疹样皮疹、脂膜炎等。
4.中枢神经系统受累:多见于pHLH、EBV-HLH等,有报道73%家族性HLH(Familial HLH,FHL)在确诊时有CNS受累,临床主要表现为抽搐、易激惹、嗜睡、昏迷、活动障碍、颅神经损伤及智力障碍等。
5.贫血、出血:出血包括皮肤黏膜、穿刺部位以及消化道、肺、中枢等内脏出血。
贫血则由出血以及细胞因子抑制骨髓造血所致。
6.呼吸系统:可表现为咳嗽、气促、呼吸困难,听诊可闻及湿啰音,严重时可出现浆膜腔积液。
(二)实验室检查1.血常规:可有一系至三系减低,以血小板减少和贫血最多见。
2.骨髓象:早期噬血细胞并不常见,与临床表现的严重程度不相平行,仅表现为反应性组织细胞增生,无恶性细胞浸润,晚期噬血现象阳性率高。
骨髓内未发现噬血细胞不能排除HLH,应密切结合临床。
3.肝功能:可表现有低白蛋白血症,血清转氨酶不同程度升高或胆红素升高,与肝脏受累程度一致。
噬血细胞综合征的诊断方法有多少?
一、概述
某同事邻居家的儿子今年五岁,有一天突然出现了眼皮红肿的状态,整个人都提不起精神,并且颈部淋巴处有些红肿,赶紧送进医院检查。
医生说他的,血小板量很少,白细胞明显减少,病人可能很严重,就赶忙去了较大的医院治疗,治疗期间发生了高烧不退的症状,最后确诊得知嗜血细胞综合症。
但是大家对视觉细胞综合症完全不了解,并不知道这种病症是什么,这是一种极其罕见的病症,是否能够痊愈呢?又该如何获得治疗?如何查看自己是不是患上了这样的病症?
二、步骤/方法:
1、噬血细胞综合征是一种恶性的疾病,一般情况下发病率很低,会出现发热脾气大的症状,并且在骨髓生长的都会发现嗜血的症状,早期多为发热,肝脾肿大的症状,较为难于治愈,并且会出现输血感染的,器官衰竭一类的死因。
2、在检查时需要对血常规检查,会出现血红细胞减少,血小板减少明显。
也可以对骨髓做检查,会发现嗜血的症状,通过影像学的检查会出现出血萎缩和水肿的症状,并且一般会伴随着凝血功能的障碍。
3、这种病症一般以男性儿童较多,发病率特别低。
80%的患者会在两岁前发病,一般是原发性的可能性较大,八岁以后发病的话则可
能是继发性的。
死亡率大概达到45%以上,因此患病后应当及时去获得专业的治疗。
三、注意事项:
嗜血细胞综合症治疗较困难,如果出现了失败或者疾病复发的话,可以使用骨髓移植术来治疗,建议尽早进行骨髓移植术,才能更好的,减缓病情获得康复。
噬血细胞综合征治疗进展
噬血细胞综合征(HLH)是一种罕见但严重的免疫系统疾病,特点是细胞因子风暴引起的慢性炎症反应,导致系统性器官衰竭。
这种疾病常常发生在儿童和年轻人身上,但也可以发生在成年人身上。
在过去的几十年里,我们对HLH的认识和治疗取得了重大进展,从而使患者的预后得到了显著改善。
目前,HLH的治疗主要分为两个方面:疾病活动期的治疗和疾病缓解期的维持治疗。
在疾病活动期,使用糖皮质激素和免疫调节药物(如环孢素、偶氮脲)是常见的治疗手段。
这些药物可以抑制细胞因子的产生和释放,从而减轻炎症反应。
对于疾病活动期较为严重的患者,常常需要进行干细胞移植以重建免疫系统。
在疾病缓解期,维持治疗的目标是控制疾病的复发并维持免疫系统的正常功能。
为了达到这个目标,常常使用长期的免疫抑制剂,如环孢素、偶氮脲或其他免疫抑制剂。
一些研究还发现,某些基因治疗和细胞治疗技术可以用于治疗HLH,例如基因修饰T细胞疗法和Chimeric Antigen Receptor T-cell(CAR-T)疗法。
HLH的早期诊断和治疗也是关键。
随着我们对HLH的认识不断深入,人们更加重视早期诊断和治疗的重要性。
一些研究表明,早期高剂量的糖皮质激素治疗可能有助于阻止疾病的进展,并改善患者的预后。
对于怀疑患有HLH的患者,及早进行详细的检查和诊断非常重要。
HLH的治疗进展令人鼓舞。
通过细胞因子抑制、干细胞移植、免疫抑制剂和免疫治疗等多种治疗手段的综合应用,患者的预后得到了明显的改善。
我们仍然需要更多的研究来进一步深入了解HLH的发病机制和治疗方法,以进一步提高患者的生存率和生活质量。