石墨基本知识.ppt
- 格式:ppt
- 大小:4.64 MB
- 文档页数:48
1.石墨烯(Graphene)的结构石墨烯是一种由碳原子以sp²杂化轨道组成六角型呈蜂巢状晶格的平面薄膜,是一种只有一个原子层厚度的二维材料。
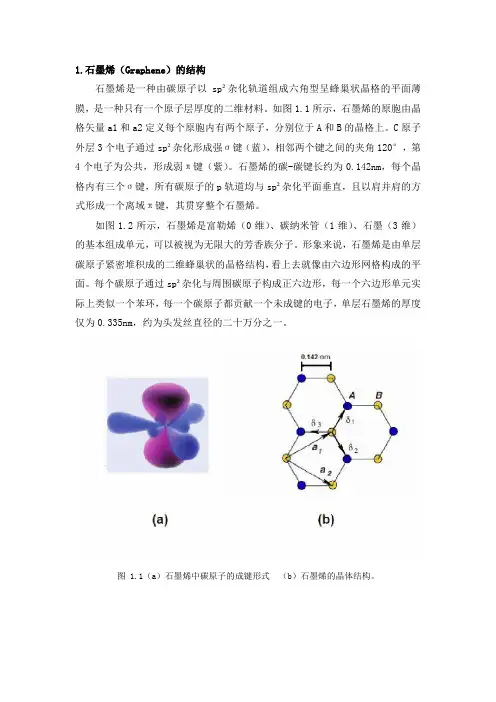
如图1.1所示,石墨烯的原胞由晶格矢量a1和a2定义每个原胞内有两个原子,分别位于A和B的晶格上。
C原子外层3个电子通过sp²杂化形成强σ键(蓝),相邻两个键之间的夹角120°,第4个电子为公共,形成弱π键(紫)。
石墨烯的碳-碳键长约为0.142nm,每个晶格内有三个σ键,所有碳原子的p轨道均与sp²杂化平面垂直,且以肩并肩的方式形成一个离域π键,其贯穿整个石墨烯。
如图1.2所示,石墨烯是富勒烯(0维)、碳纳米管(1维)、石墨(3维)的基本组成单元,可以被视为无限大的芳香族分子。
形象来说,石墨烯是由单层碳原子紧密堆积成的二维蜂巢状的晶格结构,看上去就像由六边形网格构成的平面。
每个碳原子通过sp²杂化与周围碳原子构成正六边形,每一个六边形单元实际上类似一个苯环,每一个碳原子都贡献一个未成键的电子,单层石墨烯的厚度仅为0.335nm,约为头发丝直径的二十万分之一。
图 1.1(a)石墨烯中碳原子的成键形式(b)石墨烯的晶体结构。
图1.2石墨烯原子结构图及它形成富勒烯、碳纳米管和石墨示意图石墨烯按照层数划分,大致可分为单层、双层和少数层石墨烯。
前两类具有相似的电子谱,均为零带隙结构半导体(价带和导带相较于一点的半金属),具有空穴和电子两种形式的载流子。
双层石墨烯又可分为对称双层和不对称双层石墨烯,前者的价带和导带微接触,并没有改变其零带隙结构;而对于后者,其两片石墨烯之间会产生明显的带隙,但是通过设计双栅结构,能使其晶体管呈示出明显的关态。
单层石墨烯(Graphene):指由一层以苯环结构(即六角形蜂巢结构)周期性紧密堆积的碳原子构成的一种二维碳材料。
双层石墨烯(Bilayer or double-layer graphene):指由两层以苯环结构(即六角形蜂巢结构)周期性紧密堆积的碳原子以不同堆垛方式(包括AB堆垛,AA堆垛,AA‘堆垛等)堆垛构成的一种二维碳材料。


课题1 金刚石、石墨和C60知识梳理(1)同一种元素可以组成不同的单质金刚石、石墨和C60都是由碳元素组成的单质,但由于碳原子的排列方式不同,因此它们的_________有很大差异。
(2)金刚石、石墨和C60的物理性质和用途金刚石石墨C60物理性质外观无色透明正八面体形状的固体深灰色细鳞片状固体形似足球,这种足球状的碳分子很稳定光泽加工雕琢后有夺目光泽有金属光泽硬度最硬(天然存在)很软导电性不导电优良的导电性用途刻刀、钻石、钻头铅笔芯、电极、润滑剂制备新材料、制作新器件等(3)木炭、活性炭的吸附性木炭、活性炭、炭黑、焦炭等物质都是由石墨的微小晶体和少量杂质构成的。
由于木炭和活性炭都具有疏松多孔的结构,因此它们都具有较强的_________能力,可以吸附毒气、色素以及有异味的物质等。
据此,木炭和活性炭在制糖工业、食品工业、防毒面具制作等方面有重要的应用。
(4)物质的结构、性质、用途之间的关系物质的结构决定性质,性质决定用途。
其关系可简单表示为:物质的组成结构物质的性质物质的用途答案:(1)物理性质(3)吸附(1)稳定性常温下,碳受日光照射或跟空气、水分接触,都________发生变化。
但是随着温度的升高,碳的活动性大大增强,在高温下,碳能够跟很多物质起反应。
(2)可燃性氧气充足时:C+O2点燃CO2氧气不足时:2C+O2点燃2CO,用煤生炉子,燃烧不旺时就会发生这一反应。
(3)还原性a.与非金属氧化物反应,如:C+CO2高温2CO,煤炉中经常发生这一反应。
b.与金属氧化物反应,如与氧化铜、氧化铁、氧化铝等的反应。
木炭还原氧化铜的反应原理:C+2CuO 高温2Cu+CO2↑现象:黑色粉末变成________固体,放出的气体能_________。
装置:用高锰酸钾制氧气的装置c.碳的还原性的应用:单质碳的还原性可用于冶金工业,例如用焦炭炼铁。
答案:(1)不容易(3)红色使澄清石灰水变浑浊含氧化合物里的氧________叫做还原反应。

WORD整理版1.石墨烯( Graphene)的结构石墨烯是一种由碳原子以sp2杂化轨道组成六角型呈蜂巢状晶格的平面薄膜,是一种只有一个原子层厚度的二维材料。
如图 1.1 所示,石墨烯的原胞由晶格矢量 a1和 a2定义每个原胞内有两个原子,分别位于 A 和 B 的晶格上。
C原子外层 3 个电子通过sp2杂化形成强σ 键(蓝),相邻两个键之间的夹角120°,第4 个电子为公共,形成弱π键(紫)。
石墨烯的碳 - 碳键长约为 0.142nm,每个晶格内有三个σ键,所有碳原子的p轨道均与sp2杂化平面垂直,且以肩并肩的方式形成一个离域π 键,其贯穿整个石墨烯。
如图 1.2 所示,石墨烯是富勒烯(0 维)、碳纳米管( 1 维)、石墨(3 维)的基本组成单元,可以被视为无限大的芳香族分子。
形象来说,石墨烯是由单层碳原子紧密堆积成的二维蜂巢状的晶格结构,看上去就像由六边形网格构成的平面。
每个碳原子通过 sp2杂化与周围碳原子构成正六边形,每一个六边形单元实际上类似一个苯环,每一个碳原子都贡献一个未成键的电子,单层石墨烯的厚度仅为 0.335nm,约为头发丝直径的二十万分之一。
图 1.1 ( a)石墨烯中碳原子的成键形式(b)石墨烯的晶体结构。
专业学习参考资料WORD整理版图 1.2 石墨烯原子结构图及它形成富勒烯、碳纳米管和石墨示意图石墨烯按照层数划分,大致可分为单层、双层和少数层石墨烯。
前两类具有相似的电子谱,均为零带隙结构半导体(价带和导带相较于一点的半金属),具有空穴和电子两种形式的载流子。
双层石墨烯又可分为对称双层和不对称双层石墨烯,前者的价带和导带微接触,并没有改变其零带隙结构;而对于后者,其两片石墨烯之间会产生明显的带隙,但是通过设计双栅结构,能使其晶体管呈示出明显的关态。
单层石墨烯(Graphene):指由一层以苯环结构(即六角形蜂巢结构)周期性紧密堆积的碳原子构成的一种二维碳材料。

初三化学金刚石、石墨和C60(基础) 知识讲解一、初中化学金刚石石墨和C60选择题1.下表是元素周期表的部分,其中碳元素部分信息缺失,下列有关该元素认识错误的是A.该元素对应原子的质子数为6B.该元素属于金属元素C.该元素可以组成多种单质D.该元素化学性质与最外层电子数密切相关2.石墨烯是一种由碳原子组成的六角型呈蜂巢晶格的二维碳纳米材料,碳纳米管主要是由呈六边形排列的碳原子构成数层到数十层的同轴圆管,它们的微观结构如图所示。
下列说法正确的是()A.碳元素只能组成碳纳米管和石墨烯两种单质B.碳纳米管不与其他物质发生反应C.构成石墨烯的原子间有一定间隔D.构成碳纳米管的原子不再运动3.下列有关碳及其化合物的说法正确的是()A.C60表示一个C60分子B.H2CO3中C的化合价为+2价C.一氧化碳可冶炼金属,因其具有氧化性D.金刚石和石墨的物理性质有很大差异是因为构成它们的原子大小不同4.下列关于空气及其成分的说法错误的是A.氮气、氩气可以作焊接金属的保护气B.任何物质都能在氧气中燃烧C.煤燃烧排放的SO2、NO2等是产生酸雨的主要成分D.二氧化碳可做大棚温室的气体肥料5.化学反应C+H2O 高温H2+CO中的还原剂是A.C B.H2O C.H2D.CO 6.下列有关碳单质的说法错误的是( )A.金刚石、石墨充分燃烧的产物都是二氧化碳B.金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同C.书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼D.金刚石和石墨都是硬度最大的物质7.在“一带一路”伟大战略实施中,代表中国智造的高铁走在了前列.高铁动车与电路连接的石墨电刷没有用到石墨的性质是( )A.稳定性B.滑腻感C.还原性D.导电性8.金刚石和石墨物理性质有很大差异的原因是A.原子排列方式不同B.原子大小不同C.原子种类不同D.原子数目不同9.有关金刚石、石墨、C60的下列说法中,错误的是A.金刚石、石墨、C60都具有还原性B.石墨有导电性,可制作电极C.C60是由碳原子构成D.金刚石与石墨物理性质不同的原因是碳原子的排列方式不同10.下列对一些事实的微观解释,其中错误的是 ( )选项事实解释A金刚石坚硬而石墨质地很软碳原子的结构不同B 冬天戴眼镜进入室内,眼镜片出现水雾眼镜温度低,分子运动减慢,水蒸气液化C水电解产生氢气和氧气化学变化中分子是可以再分的D刑侦人员牵着警犬寻找犯罪分子下落分子不断运动且同种分子性质相同A.A B.B C.C D.D11.2009年12月7日~18日世界气候大会在丹麦首都哥本哈根召开,商讨2012至2020年全球温室气体减排协议。

关于碳和石墨材料简介前述:工业材料分为金属材料和非金属材料。
金属材料具有以下5个特点:1):是结晶体2):是电的良导体3):是热的良导体4):具有延展性5):研磨后能全反射光线其中不能满足任何一个条件的就属于非金属材料石墨材料不具有上述第四点,因而属于非金属材料。
石墨材料是具有金属材料特性及陶瓷特性的一种特殊材料,是一种非常重要的工业材料。
石墨材料根据成型方法可分为:1):各向异性石墨2):各向同性石墨在这里主要阐述除制钢、电机用碳刷等各向异性石墨材料外,被广泛用于冶金、机械、电机、核能、电加工、半导体、及宇宙开发上的各向同性----等方性石墨的性质、制造方法和用途。
一: 碳、石墨及相关延伸产品:1: 碳* 碳是自然界分布最普遍的元素之一,也是构成地球上一切生命体最重要的元素。
以碳元素为主要构成的有机高分子材料,包括塑料、橡胶和纤维等,已发展成为材料学三个主要学科方向之一。
而以碳元素本身,通过不同结构、组合,也形成一个独特的无机非金属材料世界。
* 碳原子间不仅能够以sp3杂化轨道形成单键,还能以sp2及sp杂化轨道形成稳定的双键和叁键,因此,除了自然界存在多种同素异形体的碳材料外,科学家们通过实验还合成了许许多多结构和性质完全不同的碳材料,如人们熟悉的金刚石和石墨,以及近年来发现的卡宾(Carbyne)、C60为代表的富勒烯以及碳纳米粉体、管材、线材等。
这些新型碳材料的特性几乎可涵盖地球上所有物质的性质甚至相对立的两种性质,如从最硬到极软、全吸光-全透光、绝缘体-半导体-高导体、绝热-良导热、高铁磁体、高临界温度的超导体等。
* 碳,大量存在于各种物体中,是一种具有多种多样性质的重要物质,也算是有机化合物,是生物体的基本组成成分,到目前为止,在已确认的超过100万以上的化合物中,90%以上都含有碳的成分。
* 碳在结晶构造上有2种同素异形体:1):石墨(六方晶体),2):金刚石(正方晶体),都用”C”来表示起原子符号。

石墨管的选择石墨炉法需要根据待测元素及样品选择适合的石墨管,现在普遍使用的石墨管有三种:普通石墨管、热解石墨管和平台石墨管。
普通石墨管用普通石墨制作的,应用最为广泛。
由于石墨具有多孔的特性,液体样品在石墨管壁会有一定的渗透。
热解石墨管是在普通石墨管的表面用CVD 方法进行热解,而具有金属般光泽的表面,样品在管壁渗透较少。
平台石墨管中装有一个盛样品的平盘(平台),图1 峰形比较(左:热解石墨管和普通石墨管的比较 右:平台石墨管和热解石墨管的比较)1.何时使用普通石墨管普通石墨管可用于测定各种元素,特别是原子化温度低的元素。
这些元素有Cd , Pb , Na , K , Zn 和Mg 等。
也适用于检测灵敏度要求低的分析或高浓度样品的分析,例如:测定Al 、Fe 和Cu 时,用热解石墨管可以测到1 ppb ,用普通石墨管可以测到100 ppb 。
图2显示了用普通石墨管和热解石墨管测定铜(Cu )的工作曲线,普通石墨管的测定点是20、40和60 ppb ,用热解石墨管的测定点是2、4和 6 ppb ,显示的吸收相似。
2.何时使用热解涂层石墨管通常,热解石墨管分析易和石墨管的主要组分碳结合的元素(易形成碳化物的元素)。
典型元素如Ni 、Ca 、Ti 、Si 、V 和Mo 。
在普通石墨管中,样品容易渗透到石墨中,造成待测元素与碳之间有较大的接触面积。
在热解石墨管中,由于接触面积小,抑制了碳化物的形成,从而提高了灵敏度。
比较峰形可以看到,热解石墨管得到的峰教尖锐,而普通石墨管得到的峰形宽。
图1 是用热解石墨管分析Cu 的实例。
在例中可以看到,测定结果容易受样品中酸浓度和样品在石墨管中的分布状况影响,热解石墨管分析的重现性不如普通石墨管。
酸浓度对灵敏度的影响如图3所示。
与平台石墨管和普通石墨管比较,酸度变化对热解管灵敏度的影响大。
3.何时使用平台石墨管平台石墨管的特点是将样品溶液注射到平台上,如图4所示方式加热。

金刚石、石墨和C60【要点梳理】要点一、碳的单质1.同一种元素可以组成不同的单质:金刚石、石墨和C60都是由碳元素组成的单质,但是由于碳原子排列方式不同,即结构不同,因此它们的性质存在着差异。
金刚石的结构石墨的结构 C60的结构2.金刚石、石墨和C60的比较:(高清课堂《金刚石、石墨和C60》)名称金刚石石墨C60外观无色透明、正八面体形状的固体,仔细琢磨后有璀璨夺目的光泽深灰色不透明的细鳞片状的固体,有金属光泽C60分子形状似足球导电性几乎不导电良好几乎不导电硬度天然存在的最硬的物质质软(最软的矿物之一)质脆导热性良好良好很差用途钻头、刻刀、装饰品等电极、铅笔芯、润滑剂等制备新材料、超导材料等3.木炭、活性炭的吸附性:木炭、活性炭、焦炭、炭黑等物质都是由石墨的微小晶粒和少量杂质构成的,所以从严格的意义上来说它们还不是碳的单质(被称为无定形碳)。
由于木炭和活性炭均具有疏松多孔的结构,因此它们具有较强的吸附能力,可以吸附毒气、色素以及有异味的物质等。
木炭和活性炭有吸附性,所以它们在制糖工业、食品工业、防毒面具制作等方面有重要的应用。
【要点诠释】1.金刚石和石墨在一定条件下可以相互转化,这个转化过程发生了化学变化。
2.物质的组成和结构决定物质的性质,物质的性质决定物质的用途。
3.由于木炭疏松多孔,有很大的表面积,因此它具有吸附性,活性炭的吸附性比木炭更强。
吸附作用是将气体或溶液里的微小粒子吸附在固体表面,没有生成新物质,属于物理变化。
4.“碳”和“炭”的区别:“碳”是元素的名称,是核电荷数为6的一类原子的总称。
比如碳元素、碳单质、含碳化合物、一氧化碳等,这儿不能用“炭”。
而“炭”指的是具体物质,它表示由碳元素组成的某种单质——木炭、活性炭、焦炭等。
一般在未指明具体单质时,习惯上用碳,如“炽热的碳”、“当碳燃烧时”。
要点二、碳的化学性质1.稳定性:在常温下,碳的化学性质不活泼。
在高温下,碳能够与很多物质起反应。