有机化学反应机理画法剖析
- 格式:doc
- 大小:1.41 MB
- 文档页数:15


化学高三第六节课有机化学反应机制的解析有机化学是化学的一个重要分支,研究的是含碳的化合物的性质、结构和反应规律。
在高三化学课程中,有机化学反应机制的解析是一个重要的内容。
本文将对高三化学第六节课有机化学反应机制的解析进行探讨。
一、酯化反应的机理解析酯化反应是有机化学中常见的一类反应。
它是通过酸催化或碱催化作用,将醇与羧酸酯化形成酯的过程。
酯化反应的机理可以分为酸催化和碱催化两种情况。
在酸催化的情况下,反应机理如下:1. 酸质子(H^+)与羧酸中的羟基氧原子发生质子化作用,生成活化的酸中间体。
2. 醇中的氢氧阴离子(OH^-)与活化的酸中间体中的酸质子发生质子交换作用,生成酯和水。
在碱催化的情况下,反应机理如下:1. 碱(OH^-)与羧酸发生质子交换作用,生成羧酸根离子。
2. 醇中的氢氧阴离子(OH^-)与羧酸根离子发生质子交换作用,生成酯和水。
二、还原反应的机理解析还原反应是有机化学中常见的一类反应。
它是将有机化合物中的含氧官能团还原为相应的氢氧化物或氢化物的过程。
还原反应的机理可以分为羰基还原和酮碳还原两种情况。
在羰基还原的情况下,反应机理如下:1. 还原剂(通常为金属碱金属或金属铝)提供氢原子,与羰基中的氧原子发生氢质子化作用,生成碳正离子中间体。
2. 配体与碳正离子中间体发生配位作用,生成酯或醇的产物。
在酮碳还原的情况下,反应机理如下:1. 还原剂提供氢原子,与酮中的氧原子发生氢质子化作用,生成碳正离子中间体。
2. 配体与碳正离子中间体发生配位作用,生成醇的产物。
三、环构化反应的机理解析环构化反应是有机化学中常见的一类反应。
它是通过重新排列碳骨架的方式,形成新的环状化合物的过程。
环构化反应的机理可以分为阳离子环构化和自由基环构化两种情况。
在阳离子环构化的情况下,反应机理如下:1. 亲核试剂(例如,碱氧化剂)与环外的角质阳离子或舒展阳离子发生亲核取代作用,生成环内的新的角质阳离子。
2. 亲核试剂与新生成的角质阳离子发生质子交换作用,形成新的碳正离子。
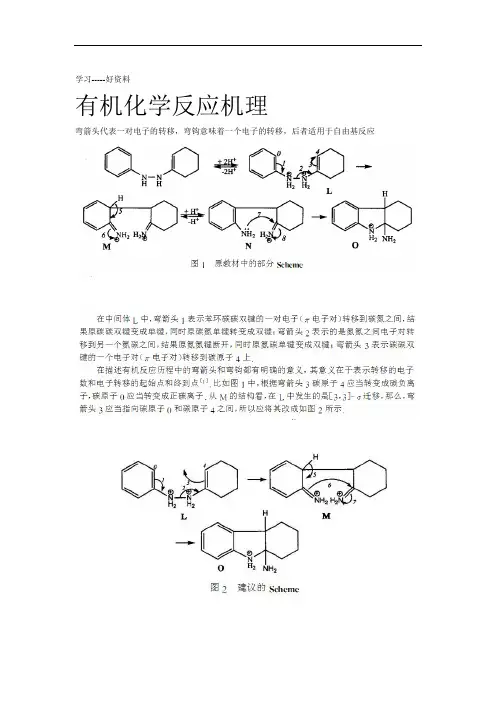
学习-----好资料有机化学反应机理弯箭头代表一对电子的转移,弯钩意味着一个电子的转移,后者适用于自由基反应更多精品文档.学习-----好资料更多精品文档.好资料学习-----1 有机反应机理入门 1.1 画路易斯结构式键应准确无误,然后用氢原子完成其余的化学键。
先画出分子的骨架,环和pi 对于有机分子,骨架有时以简化形式给出。
62个;硼、铝和镓画出孤对电子,使每个原子核外满足充满电子的结构:氢个。
最后结构式中的每个原子总的成键电子数可以通过数其核个;其它原子8 )。
外的成键电子获得(包括共享电子提示:画路易斯结构式可参考以下结构特征:氢原子永远在构的外围,因为它只能成一个共价键;(1)碳、氮和氧有特定的键合模式。
(2)代表氢、烷基、芳基或它们的组合,这种变化并不影响成键R在以下的示例中模式。
pi也可以是sigma键与键。
4这4个键可以都是sigma键,①中性的碳原子为 )。
如双键和三键键的组合( 个键。
带有单个正电荷或负电荷的碳有3 ②)氮烯除外有3个键和一对未成对电子。
( ③中性的氮原子键,带有一个正电荷。
正电荷的氮成④ 4更多精品文档.学习-----好资料对未成键电子。
2⑤负电荷的氮成键,带有一个负电荷和2 对孤对电子。
⑥中性的氧原子成2键,带有2 带正电荷的氧成3键,带有1对孤对电子。
⑦轨道,可d(3) 有时磷原子和硫原子可有10个成键电子,这是因为磷和硫具有个电子。
以扩展而容纳10 Lewis结构式是价键理论的重要内容,也是学习反应机理的基础。
1.2 电负性或部分)的分子与带有负电荷(多数有机反应依赖于带有正电荷(或部分正电荷部分电荷的产生依赖于)的分子的相互作用而发生。
在中性有机分子中,负电荷电负性的差异。
年确定。
其数值越大,表明其吸电1960Linus 电负性的数值最初由Pauling在子能力越强,所以氟是吸电子能力最强的元素,见表:成键后,电负性大的元素的原子拥有部分负电荷,而且,双键结构的部分电荷电子受原子核的束缚小,pi比单键结构的部分电荷密度更大,这是因为双键上的更易于流动。

有机化学反应机理的解析方法概述有机化学反应机理的解析是有机化学研究中的重要环节。
了解有机化学反应的机理有助于预测和控制反应的结果,提高合成的效率和选择性。
本文将介绍几种常用的方法和策略来解析有机化学反应的机理。
1. 实验方法实验方法是解析有机化学反应机理的基础。
通过实验,可以观察和记录反应的各个阶段,推导出反应机理的可能路径。
常用的实验方法包括核磁共振(NMR)和质谱(MS)等技术。
这些技术可以提供反应物、产物和中间体的结构信息,从而揭示反应的机理。
2. 系统性变化法系统性变化法是一种常用的解析有机化学反应机理的策略。
通过改变反应条件、反应物结构和配体等因素,可以观察到反应结果的变化,推测出可能的反应途径和中间体。
这种方法可以帮助确定反应中的关键步骤和控制因素。
3. 理论计算方法理论计算方法是一种重要的解析有机化学反应机理的手段。
通过计算化学方法,如密度泛函理论(DFT)和分子动力学模拟,可以模拟和预测反应物、中间体和过渡态的结构、能量和反应路径。
这些计算结果可以提供有机化学反应机理的理论依据。
4. 文献研究文献研究也是解析有机化学反应机理的重要手段。
通过查阅相关的文献资料,可以了解已经报道的反应机理和相关研究成果。
这可以为解析新的有机化学反应机理提供参考和启发。
总结解析有机化学反应机理是一项复杂而重要的工作。
实验方法、系统性变化法、理论计算方法和文献研究是解析有机化学反应机理的常用方法和策略。
通过综合运用这些方法,可以揭示反应的机理和路径,为有机化学研究和合成提供指导和帮助。
参考文献:1. Smith, G. M. Organic Reaction Mechanisms. Royal Society of Chemistry, 2015.2. Carey, F. A., & Sundberg, R. J. Advanced Organic Chemistry. Springer, 2007.3. March, J. Advanced Organic Chemistry: Reactions, Mechanisms, and Structure. Wiley, 2007.。


有机化学反应机理解析有机化学是研究碳元素化合物的科学,它涉及了大量的反应和机理。
了解有机化学反应的机理对于有机化学的学习和应用非常重要。
本文将对有机化学反应机理进行解析,希望能够帮助读者更好地理解有机化学反应。
一、酯水解反应的机理酯水解反应是有机化学中常见的一种反应,它是酯与水反应生成醇和羧酸的过程。
这个反应的机理可以分为两步:首先是酯的酯键被水攻击,生成酯中间体;然后是中间体被水继续攻击,生成醇和羧酸。
具体来说,酯的酯键被水攻击时,酯中间体的形成是通过亲核进攻的机制进行的。
水中的氢氧根离子(OH-)是亲核试剂,它攻击酯的羰基碳,将酯中间体形成。
然后,中间体再次被水攻击,生成醇和羧酸。
二、醇的氧化反应的机理醇的氧化反应是有机化学中常见的一种反应,它是醇与氧化剂反应生成醛或酮的过程。
这个反应的机理可以分为两步:首先是醇失去氢原子,生成醛或酮中间体;然后是中间体被氧化剂进一步氧化,生成醛或酮。
具体来说,醇失去氢原子的过程是通过氧化剂的作用进行的。
氧化剂可以是氧气、过氧化氢等。
醇中的氢原子被氧化剂夺取后,生成醛或酮中间体。
然后,中间体再次被氧化剂氧化,生成醛或酮。
三、芳香化反应的机理芳香化反应是有机化学中常见的一种反应,它是烯烃或炔烃与芳香化试剂反应生成芳香化产物的过程。
这个反应的机理可以分为两步:首先是烯烃或炔烃与芳香化试剂发生电子亲和反应,生成芳香化中间体;然后是中间体发生质子化或亲核取代反应,生成芳香化产物。
具体来说,烯烃或炔烃与芳香化试剂发生电子亲和反应时,烯烃或炔烃中的π电子与芳香化试剂中的空位轨道发生相互作用,形成芳香化中间体。
然后,中间体可以发生质子化反应,即失去一个质子,生成芳香化产物。
或者中间体可以发生亲核取代反应,即被亲核试剂攻击,生成芳香化产物。
四、酮的加成反应的机理酮的加成反应是有机化学中常见的一种反应,它是酮与亲核试剂反应生成加成产物的过程。
这个反应的机理可以分为两步:首先是酮的羰基碳被亲核试剂攻击,生成酮中间体;然后是中间体发生质子化或亲核取代反应,生成加成产物。

有机化学反应机理解析有机化学反应的机理研究是化学领域中的重要领域之一,其主要内容是研究反应中电子的迁移和化学键的形成和断裂。
有机化学反应机理解析是深入探究反应机理的过程,它不仅可以用于对反应的解释,还可以为反应的设计与控制提供指导。
有机化学反应机理解析的方法主要包括实验和理论计算两种方式。
实验方法是通过分析反应物和产物的结构、反应条件和反应动力学特性等多个角度来揭示反应机理。
理论计算方法则是通过分子建模、计算化学和量子化学等手段,以理论预测为基础,结合实验验证来推断反应机理,并提供反应路径和反应中间体的结构性质等重要信息。
实验方法实验方法是研究有机化学反应机理的经典方法。
其主要通过实验手段来探究反应过程中的分子间相互作用、复合物的形成和断裂过程、过渡态的形态和识别过渡态等关键步骤,确立反应机理。
对于一般的有机化学反应,实验方法可以采用以下步骤:(1)研究反应动力学:反应动力学研究是研究反应机理的重要手段,其可以通过监测反应物消耗和产物生成的速率变化来探明反应的速率常数和反应机理。
(2)利用同位素标记法:同位素标记法是通过标记反应物或产物的一种方式,标记成为异位素的反应物会在反应中发生一系列的过程,从而揭示反应机理。
例如利用放射性标记法研究化学反应,可以通过对标记物的辐射测定来定量反应过程中中间体的形成和消失,为揭示反应机理提供重要的实验数据。
(3)利用电化学技术:电化学技术是一种重要的实验手段,它可以利用电解法控制反应速率,探析反应中离子和电子的行为,从而揭示反应机理。
例如利用电化学技术可以研究氧化还原反应中电子传递的机制,以及酸碱催化反应的机制。
理论计算方法理论计算方法是揭示有机化学反应机理的重要工具之一,其通过计算机程序分析反应物、中间体、过渡态等模型的几何构型和电子结构,在理论水平上推导反应机理并表明反应路径,对实验方法产生补充。
目前,常用的理论计算方法包括密度泛函理论(DFT)、分子力场(MM)和量子化学等。
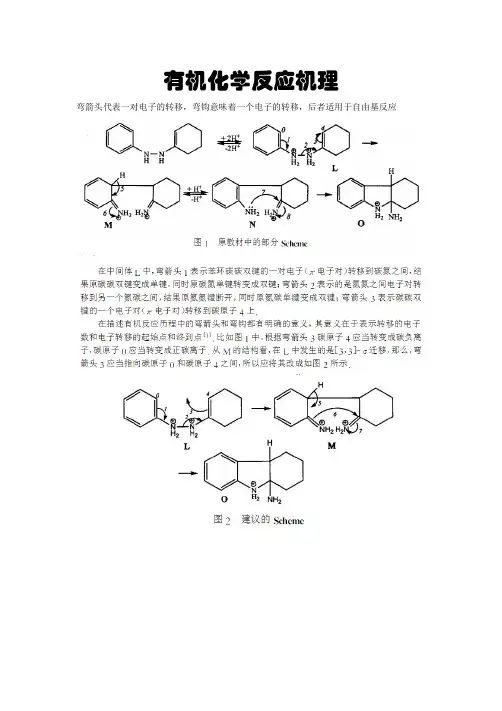
有机化学反应机理弯箭头代表一对电子的转移,弯钩意味着一个电子的转移,后者适用于自由基反应1 有机反应机理入门1.1 画路易斯结构式先画出分子的骨架,环和pi键应准确无误,然后用氢原子完成其余的化学键。
对于有机分子,骨架有时以简化形式给出。
画出孤对电子,使每个原子核外满足充满电子的结构:氢2个;硼、铝和镓6个;其它原子8个。
最后结构式中的每个原子总的成键电子数可以通过数其核外的成键电子获得(包括共享电子)。
提示:画路易斯结构式可参考以下结构特征:(1)氢原子永远在构的外围,因为它只能成一个共价键;(2) 碳、氮和氧有特定的键合模式。
在以下的示例中R代表氢、烷基、芳基或它们的组合,这种变化并不影响成键模式。
①中性的碳原子为4键。
这4个键可以都是sigma键,也可以是sigma键与pi 键的组合(如双键和三键)。
②带有单个正电荷或负电荷的碳有3个键。
③中性的氮原子(氮烯除外)有3个键和一对未成对电子。
④正电荷的氮成4键,带有一个正电荷。
⑤负电荷的氮成2键,带有一个负电荷和2对未成键电子.⑥中性的氧原子成2键,带有2对孤对电子.⑦带正电荷的氧成3键,带有1对孤对电子。
(3)有时磷原子和硫原子可有10个成键电子,这是因为磷和硫具有d轨道,可以扩展而容纳10个电子。
Lewis结构式是价键理论的重要内容,也是学习反应机理的基础。
1。
2 电负性多数有机反应依赖于带有正电荷(或部分正电荷)的分子与带有负电荷(或部分负电荷)的分子的相互作用而发生。
在中性有机分子中,部分电荷的产生依赖于电负性的差异.电负性的数值最初由Linus Pauling在1960年确定。
其数值越大,表明其吸电子能力越强,所以氟是吸电子能力最强的元素,见表:成键后,电负性大的元素的原子拥有部分负电荷,而且,双键结构的部分电荷比单键结构的部分电荷密度更大,这是因为双键上的pi电子受原子核的束缚小,更易于流动.电负性是很基础的知识,但很有用,很重要.通过电负性,可以解释为什么硼烷加成到烷基取代的不对称烯烃上不服从Markovnikov规则,为什么含活泼氢的羰基化合物去质子后主要以烯醇式存在.。



一、Arbuzow反应(重排)亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R'I >R'Br >R'Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzow反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理一般认为是按 S N2 进行的分子内重排反应:反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger 反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
有机化学反应机理总结(较全)有机化学反应机理总结 (完整版)本文总结了几种常见的有机化学反应的机理,并提供了相关的示意图。
以期帮助读者更好地理解有机化学反应的机理和反应过程。
1. 反应类型1: 取代反应取代反应是有机化学中最基本的反应类型之一。
它涉及到一个分子或它的一部分被另一个原子或基团取代的过程。
以下是一个典型的取代反应的机理示意图:机理步骤:1. 亲核试剂与底物发生反应,亲核试剂攻击底物的部分阳离子或电子不足的原子。
2. 形成一个中间体,中间体中的某个基团离开。
3. 离开基团被亲核试剂取代,形成最终产物。
2. 反应类型2: 加成反应加成反应发生在两个分子之间,它们在反应中结合形成一个新的分子。
加成反应的机理示意图如下所示:机理步骤:1. 两个反应物中的亲核试剂和电荷不足的物种发生相互作用。
2. 形成一个键合物中间体。
3. 中间体通过质子转移或亲核试剂攻击等步骤,产生最终产物。
3. 反应类型3: 消除反应消除反应是一种从底物中除去一些原子或基团的反应,生成了双键或环。
以下是消除反应的机理示意图:机理步骤:1. 底物中的一个基团被移除,形成一个中间体。
2. 中间体中的某个原子或基团与另一个原子或基团形成新的共价键。
3. 生成最终产物。
以上是几种常见有机化学反应的机理总结。
希望本文能对读者理解有机化学反应的机理和反应过程有所帮助。
参考文献:请注意,以上内容仅供参考,具体反应机理可能会因具体情况而有所不同。
有机化学反应机理弯箭头代表一对电子的转移,弯钩意味着一个电子的转移,后者适用于自由基反应1 有机反应机理入门1.1 画路易斯结构式先画出分子的骨架,环和pi键应准确无误,然后用氢原子完成其余的化学键。
对于有机分子,骨架有时以简化形式给出。
画出孤对电子,使每个原子核外满足充满电子的结构:氢2个;硼、铝和镓6个;其它原子8个。
最后结构式中的每个原子总的成键电子数可以通过数其核外的成键电子获得(包括共享电子)。
提示:画路易斯结构式可参考以下结构特征:ﻫ(1) 氢原子永远在构的外围,因为它只能成一个共价键;(2) 碳、氮和氧有特定的键合模式。
ﻫ在以下的示例中R代表氢、烷基、芳基或它们的组合,这种变化并不影响成键模式。
①中性的碳原子为4键。
这4个键可以都是sigma键,也可以是sigma键与pi键的组合(如双键和三键)。
ﻫ②带有单个正电荷或负电荷的碳有3个键。
③中性的氮原子(氮烯除外)有3个键和一对未成对电子。
ﻫ④正电荷的氮成4键,带有一个正电荷。
⑤负电荷的氮成2键,带有一个负电荷和2对未成键电子。
⑥中性的氧原子成2键,带有2对孤对电子。
⑦带正电荷的氧成3键,带有1对孤对电子。
(3) 有时磷原子和硫原子可有10个成键电子,这是因为磷和硫具有d轨道,可以扩展而容纳10个电子。
Lewis结构式是价键理论的重要内容,也是学习反应机理的基础。
1.2 电负性多数有机反应依赖于带有正电荷(或部分正电荷)的分子与带有负电荷(或部分负电荷)的分子的相互作用而发生。
在中性有机分子中,部分电荷的产生依赖于电负性的差异。
ﻫ电负性的数值最初由LinusPauling在1960年确定。
其数值越大,表明其吸电子能力越强,所以氟是吸电子能力最强的元素,见表:成键后,电负性大的元素的原子拥有部分负电荷,而且,双键结构的部分电荷比单键结构的部分电荷密度更大,这是因为双键上的pi电子受原子核的束缚小,更易于流动。
电负性是很基础的知识,但很有用,很重要。
通过电负性,可以解释为什么硼烷加成到烷基取代的不对称烯烃上不服从Markovnikov规则,为什么含活泼氢的羰基化合物去质子后主要以烯醇式存在...1.3共振结构ﻫ当分子中成键电子的分布不能用一个路易斯结构充分表达时,可由若干个仅仅在电子的位置上有差别的路易斯结构的组合来表达。
这种仅仅在电子的位置上有差别的路易斯结构称为共振结构。
共振结构表达了分子中电子的离域。
画共振结构ﻫ对于给定的分子或中间体,画共振结构的简单方法是先画出一个路易斯结构,然后用箭头表示电子的流动,画出一个仅仅是电子分布不同的结构。
这种电子流动只是形式上的,而分子中并没有真正的流动发生。
实际的分子就是这些共振结构的某些特征的杂化体。
所以,共振结构并不代表分子或中间体的实际结构,而只是一种帮助我们预测实际分子中电子分布的形式结构。
例如:提示:化学家常用以下几种箭头:①双向箭头用来联结共振结构:ﻫﻫ②两个单箭头表示平衡:ﻫﻫ③弯箭头表示一对电子沿箭头方向从起点流动到终点:ﻫ④半弯箭头表示一个电子沿箭头方向从起点流动到终点:共振结构的规则①所有参与离域的电子都是pi电子或孤对电子,因为它们很容易进入p轨道。
②每个参加离域的电子一定要与其它电子有一定程度的交盖。
这意味着如果轨道之间是90o定向的,将不会交盖,最好的交盖发生在0度定向的情况下。
③每个共振结构必须要有相同的pi电子数。
双键计2个;三键计2个,因为三键中只有一个pi键可与相邻的pi体系交盖;pi体系带有电荷时,负电荷计2个,正电荷计0个。
④每个结构中必须具有相同数目的成对pi电子。
ﻫ以下两个结构不是共振结构,第一个结构中有两对pi电子:一对pi键电子和一对负离子的孤对电子;在第二个结构中没有成对的pi电子而只有未成对电子(图中点所示)。
ﻫ⑤所有的共振结构必须具有一致的几何构型,否则它们就不能代表相同的分子。
例如以下结构(杜瓦苯)就不是苯的共振结构,因为它不是平面构型,而且少2个pi电子。
由于几何构型是同杂化状态联系在一起的,这意味这所有的共振结构中的原子的杂化状态不能变。
⑥依赖电荷分离的共振结构能量很高,对共振结构的贡献较不依赖电荷分离的共振结构小。
ﻫ⑦通常,负电荷集中在电负性大的原子上,正电荷集中在电负性小的原子上,这样的结构对共振结构贡献大。
ﻫ所以说含活泼氢的羰基化合物去质子产物主要以烯醇式为主,称其为碳负离子有失严密。
单个共振结构并不代表真正存在的化学实体,重要性在于可以帮助阐明化学物种(分子、中间体、过渡态等)的电子分布;一般而言,共振结构越多,其化学物种就越稳定,据此可以解释为什么在芳环的亲电取代中硝基钝化芳环,并成为第二类定位基。
1.4 互变异构体与平衡互变异构体是那些仅在单、双键及小原子(通常为氢)的安排上不同的异构体。
适当条件下,上述异构体可通过简单的机理达到平衡。
ﻫ平衡存在于正、逆反应速率相等的过程中。
ﻫﻫ提示:以下因素可帮助区分共振结构与互变异构体:ﻫ①互变异构体是容易互相转化的异构体。
它们仅在单、双键及氢的安排上不同。
互变异构体间的平衡用一对半箭头表示。
ﻫ②不同的共振结构代表不同的sigma键模式,而不是不同的化学物种。
共振结构用双箭头联结。
ﻫ③对于给定的化合物,所有的共振结构都有一致的sigma键键合模式和一致的几何构型。
而在互变异构体中,sigma键模式则不同。
ﻫ1.5酸和碱(1) 布朗斯太德(Bronsted)酸和碱ﻫ布朗斯太德酸是质子供体;而布朗斯太德碱是质子受体:ﻫﻫ如果上述反应可逆,反过来定义也一样:ﻫ(2) 路易斯(Lewis)酸和碱路易斯酸是孤对电子或pi电子的受体,是缺电子体。
换言之,路易斯酸上的原子由于与一个或多个电负性较大的原子相连而具有正电荷或部分正电荷。
ﻫ路易斯碱是孤对电子或pi电子的供体。
具有负电荷的路易斯碱的碱性较没有负电荷的路易斯碱的碱性强。
ﻫ因此,有机反应也被认为是路易斯酸碱之间的反应:ﻫ1.6 亲核试剂与亲电试剂亲核试剂是寻找缺电子中心的反应物种。
它们含有带有负电荷或部分负电荷的原子(亲核性原子)。
缺电子中心称为亲电试剂,这些缺电子中心通常带有正电荷或部分正电荷,但缺电子物种也可以是中性分子。
ﻫ提示:一些基本概念①共价键断裂时,如果原来由两个原子共享的电子保留在一个碎片上,这种方式称为共价键的异裂。
尽管异裂过程常常与离子中间体有关,但也有例外。
ﻫ②对多数反应而言,称其中的一个反应物为底物而另一个为进攻试剂常常比较方便。
为新键提供碳原子的分子常被指定为底物。
而形成碳碳键时,则需要主观指定哪个是底物哪个是进攻试剂。
③在异裂反应过程中,进攻试剂有时带给底物一对电子,有时从底物带走一对电子。
带来一对电子的称为亲核试剂,这样的反应称为亲核反应;带走一对电子的称为亲电试剂,这样的反应称为亲电反应。
④对于底物分子被异裂切断的反应,其断裂的一部分通常称为离去基团。
带着一对电子离去的称为离核基团,而留下一对电子的离去基团称为离电基团。
这些概念看来枯燥,但若能熟练运用,对于讨论问题十分方便。
1.7 反应机理的表达反应机理应一步一步地给出反应过程中化学键(电子)重新组合、安排的过程。
ﻫ这些机理并没有真正的实体存在,只是为了表达反应是如何发生的一种尝试。
尽管实验可以证明某些机理合理而另一些不合逻辑,但对多数反应而言,并没有证据支持其机理。
因此,在遵从公认的准则的情况下,我们可以任意地描述一个反应的机理。
1.7.1 配平方程式从有机化学的观点来看,只要碳和电荷平衡,就可以认为一个反应方程式已经配平了。
不必配平反应过程中的无机物。
1.7.2用弯箭头表示电子的流动ﻫ在表达机理时,旧键的断裂和新键的形成一般用弯箭头表示。
这些箭头是表达反应过程中电子的重新分布的方便的工具。
这些说明电子重新分布的箭头是从电子云密度高的位点画向缺电子(电子云密度低)的位点。
ﻫ也就是从负电荷或部分负电荷(孤对电子)的位点画向正电荷或部分正电荷的位点(偶极矩的正极点)。
换言之,是从亲核试剂(路易斯碱)画向亲电试剂(路易斯酸)。
而且一般只是一些在非常反应中才会出现两个箭头从同一原子同出(或同入)的情况。
例酰氯和氨生成酰胺的反应机理:附:弯箭头简史ﻫ弯箭头的发明者被认为是Robert Robinson (1886-1975),1947年Nobel化学奖得主。
ﻫﻫThe first use ofcurly arrows to represent the movement of electrons is in a paper entitledAn Explanation of the Property of InducedPolarityofAtoms and anInterpretation of the Theory o fPartial Valences on anElectronic Basis, by William Ogi lvy Kermack and Robert Robinson, published in The Journalof the Chemical Society, 1922, 121: 427.酸、碱介质中的反应机理ﻫ对于酸性介质中进行的反应,首先在反应物中找到碱性最强的原子,然后使其质子化,再给这个正离子寻找合适的反应。
对于碱性介质中的反应,先在反应物中找到酸性最强的质子,去质子后得到一个负离子,再给这个负离子寻找合适的反应。
如果这个负离子有合适的离去集团,就可以发生消除反应。
如果形成的负离子是良好的亲核试剂,就寻找亲电物种使之反应。
例Claisen缩合的反应机理:1.7.3 化学反应的推动力化学反应可以由焓减、熵增或这两个过程联合推动。
由少数分子生成多数分子的反应是熵增推动的;而生成更稳定分子的过程则主要是焓减推动的。
考虑一个化学反应的机理时,应提出这样的问题:反应为什么这样进行?什么因素有助于反应进行?(1) 离去基团对于亲核取代反应,离去基团的性质常常成为该反应能否发生的关键。
一般而言,离去基团的离去能力与其碱性的强弱相反。
例如水(H2O)是比羟基(OH-)更好的离去基团;碘离子(I-)是比氟离子(F-)更好的离去基团。
离去基团能力:如果反应涉及到差的离去基团,要使反应发生,常常需要很强的亲核试剂。
(2) 生成稳定的小分子生成稳定的小分子既是焓减过程也是熵增过程,因此成为化学反应的很好的推动力。
这些稳定的小分子包括:氮、二氧化碳、一氧化碳、水、二氧化硫和无机盐等。
例在四苯基环戊二烯酮和顺丁烯二酸酐的反应中,生成一氧化碳成为反应的推动力:1.7.4反应原料与产物间的结构关系:标号法给反应原料和生成物的原子标号,可以帮助我们确定产物分子中原子与原料分子中原子之间的关系,并由此了解反应是如何进行的。