天然气酸性气体的脱除
- 格式:doc
- 大小:48.00 KB
- 文档页数:16


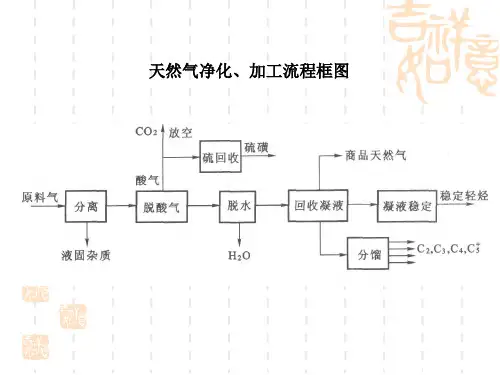

天然气脱酸脱碳工艺流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!天然气脱酸脱碳工艺流程。
1. 进气预处理。
天然气通过除尘器去除粉尘颗粒。
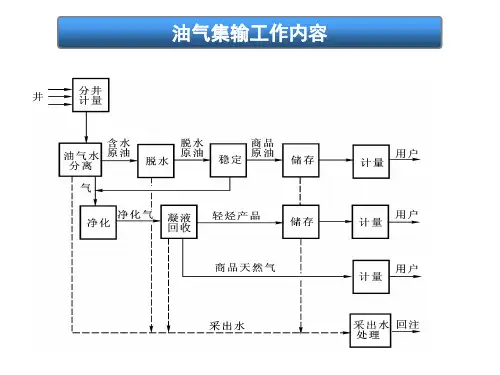

MDEA又称为N-甲基二乙醇胺,MDEA法脱碳技术是利用活化MDEA水溶液在高压常温将天然气或合成气中的二氧化碳(CO2)吸收,并在降压和升温的情况下,二氧化碳(CO2)又从溶液中解吸出来,同时溶液得到再生。
我公司除了在国内建设MDEA法脱碳装置外,也成功登陆海外市场,在印度尼西亚也建设了类似装置。
典型装置中国海洋石油公司(CNOOC)天然气MDEA法脱除二氧化碳装置印尼石油公司提供了天然气MDEA法脱碳装置MDEA脱除酸性气体技术主要应用于以下几个领域:1.天然气脱除二氧化碳(CO2),配套管输天然气或LNG净化装置2.天然气脱除硫化氢(H2S),配套管输天然气或LNG净化装置3.天然气选择性脱除硫化氢(H2S),配套管输天然气4.变换气脱除二氧化碳(CO2),配套合成氨、甲醇或者深冷分离装置5.合成气脱除二氧化碳(CO2),配套合成氨、甲醇或者深冷分离装置6.煤气脱除二氧化碳(CO2)和硫化氢(H2S),配套合成氨、甲醇或者深冷分离装置7.食品级二氧化碳(CO2)生产,达到国际饮料行业标准装置特点装置规模:处理天然气或变换气1000~500,000m3/h脱碳精度:二氧化碳(CO2)含量为10PPM~3%脱硫精度:硫化氢(H2S)含量为0.1~20mg/m3工作压力:适宜的压力为0.5~15MPa适用领域:天然气处理与加工、甲醇原料净化、合成氨原料净化等技术特点1.MDEA脱除酸性气体的流程可以采用贫液一段吸收和贫液半贫液两段吸收,贫液一段吸收的流程投资省、电耗低、热耗高;贫液半贫液二段吸收的投资大、电耗高、热耗低,根据脱除不同规模的二氧化碳,采用不同的流程。
2.MDEA溶液对天然气的溶解度低于天然气在纯水中的溶解度,因此,MDEA脱除酸性气体的过程中,天然气的损失很低。
3.MDEA溶液兼有物理吸收和化学吸收的特点,溶剂对二氧化碳的负载量大。
4.MDEA稳定性较好,在使用过程中很少发生降解的现象,它对碳钢设备几乎无腐蚀。

民营科技2018年第6期科技创新天然气预处理过程中的脱酸与脱水工艺初探魏建岗(陕西延长石油天然气有限责任公司,陕西延川717200)天然气的预处理,指的是天然气在液化前脱除其中含有的CO2,H2S、游离水及其他杂质,防止对液化体统造成腐蚀以及在低温条件下冻堵输气管线。
其不同于常规的天然气净化,天然气净化只是除去天然气中含有的酸性气体和水分,标准为H2S≤6mg/m3,CO2≤3%,远不及天然气预处理的标准严格,天然气的预处理标准要求CO2<50ppm,H2S<4ppm,H2O<1ppm。
1天然气脱酸工艺技术1.1可再生溶剂脱酸工艺。
油气田生产的天然气一般含有相当一部分酸性气体,酸性气体不仅会腐蚀设备,燃烧后还会污染环境。
可再生溶剂脱酸的原理是利用溶剂与被处理的天然气充分混合,天然气中的二氧化碳、硫化氢被溶剂吸收,然后通过热再生去除,溶液冷却后再次投入使用,如此反复循环,达到脱酸目的。
谈一下三种脱酸的方法:1)化学吸收法。
化学吸收法是天然气脱酸工艺技术中较为常用的方法,主要利用氨醇类溶液对天然气进行脱酸,其优势在于比物理溶剂更能适应低压,此外由于其对烃类的溶解度小,不会造成天然气中烃类物质的损失和浪费。
2)物理吸收法。
利用物理吸收法进行天然气脱酸时,溶剂用量不会随着天然气中酸性气体含量发生变化。
其有如下优势:能够处理分压力较高的天然气,通过减压、闪蒸技术将酸性气体从原料气中分离出来,此外处理量较大,稳定性也较好。
其缺点也显而易见,一是价格昂贵;二是会吸收一部分重烃,影响天然气的热值。
3)联合吸收法。
顾名思义,就是化学吸收法与物理吸收法有机融合来进行天然气脱酸的方法。
将化学溶剂与物理溶剂按一定比例混合在一起,混合液同时具备化学溶剂与物理溶剂的优良特性,以达到两种方法取长补短、优势互补的目的。
1.2其他天然气脱酸工艺。
1)低温分离工艺。
这种工艺技术适用于二氧化碳驱所产生的伴生气脱酸,依据对产品的不同要求可以采用不同的流程。
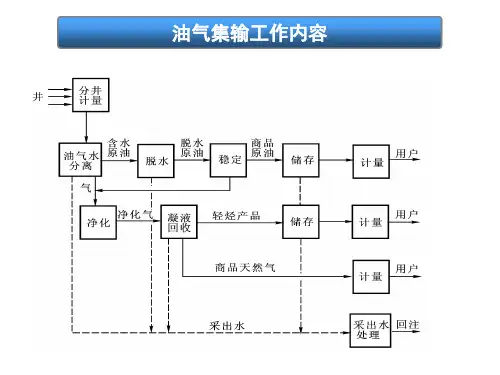


天然气酸性气体的脱除第一节概述在天然气中含有的硫化氢(H2S)、二氧化碳(CO2)和有机硫化合物,统称为酸性气体。
在天然气中的有机硫化合物主要有二硫化碳(CS2)、羰基硫(COS)、硫醇(RSH)、硫醚(RSR`)及二硫醚(RSSR`)等。
天然气中酸性气体的存在,具有相当大的危害。
硫化氢是一种具有臭鸡蛋的刺激性恶臭味的无色气体,有毒,它可以麻痹人的中枢神经系统,经常与硫化氢接触能引起慢性中毒;硫化氢具有强烈的还原性,易受热分解,在有氧存在时易腐蚀金属;易被吸附于催化剂的活性中心使催化剂“中毒”;在有水存在时能形成氢硫酸对金属有较强的腐蚀;H2S还会产生氢脆腐蚀。
二氧化碳在有水存在时,会对金属形成较强的腐蚀;同时CO2含量过高,会降低天然气的热值。
有机硫大多无色有毒,低级有机硫比空气轻,易挥发。
有机硫中毒能引起恶心、呕吐、血压下降,甚至心脏衰竭、呼吸麻痹而死亡。
因此,在化工生产中对酸气性组分是有严格要求的,必须严格控制天然气中酸性组分的含量。
从天然气中脱除酸性组分的工艺过程称为脱硫、脱碳,习惯上统称为天然气脱硫。
第二节天然气酸性组分脱除的方法天然气酸性组分的脱除,其目的是按不同用途把天然气中的酸性气体脱除到要求的范围内。
目前,国内外报道过的脱硫方法有近百种(1)。
就其过程的物态特征而言,可分为干法和湿法两大类;在习惯上将采用溶液或溶剂作脱硫剂的方法统称为湿法,将采用固体作脱硫剂的脱硫方法统称为干法。
就其作用机理而言,可分为化学溶剂吸收法、物理溶剂吸收法、物理—化学吸收法、直接氧化法、固体吸收/吸附法及膜分离法等。
一、化学溶剂吸收法化学溶剂吸收法又称化学吸收法,是以可逆化学反应为基础,以碱性溶液为吸收溶剂(化学溶剂),在低温高压下,溶剂与原料气中的酸性组分(主要是H2S和CO2)反应生成某种化合物,在升高温度、降低压力的条件下该化合物又能分解放出酸气并使溶剂得以再生。
这类方法中最具有代表性是醇胺法和碱性盐溶液法。
醇胺法是一种较为成熟的方法,在上世纪三十年代已开始工业生产,常用化学吸收剂有:单乙醇胺(MEA)、二乙醇胺(DEA)、二异丙醇胺(DIPA)、甲基二乙醇胺(MDEA)等。
碱性盐溶液法主要有改良热钾碱法(Catacarb 法、Benfield法)、氨基酸盐法(Alkacid)等(1)。
醇胺类化合物分子中至少含有一个羟基和一个胺基。
羟基的作用是降低化合物的蒸汽压,并增加在水中的溶解度;而胺基则使溶液呈碱性,促进溶液对酸性组分的吸收。
醇胺根据其氮原子上所连接的有机机团的数目可分为伯胺(如MEA)、仲胺(如DEA)、叔胺(如MDEA)三类,它们与H2S、CO2的反应如表4-1所示:表4-1 醇胺吸收H2S和CO2的主要反应从上表中可以看出,醇胺和H2S和CO2的主要反应均为可逆放热反应。
因此,在吸收塔内,酸性组分压力较高,且温度较低时,反应平衡向右移动,原料气中的酸性组分被脱除;在再生塔内,酸性组分压力较低,且温度较高时,反应平衡向左移动,溶液释放出酸性组分,实现溶液再生。
一般说来,醇胺法脱除酸性组分的流程基本形式是相同的,如图4-1所示。
只是根据不同的实际情况会进行适当的调整。
在整个脱除过程中,原料气由下而上与溶液逆流接触通过吸收塔。
从吸收塔流出的富含酸性组分的富液首先在闪蒸塔内闪蒸至中压,除去溶液中溶解的烃类,然后通过贫富液换热器将贫液中的热量回收后进入再生塔进行再生,再生合格的贫液通过贫富液换热器和贫液冷却器将贫液温度降下来后,再通过循环泵加压后进入吸收塔完成循环。
再生出来的酸性组分经过冷却将水分分离出来后,进入硫磺回收系统,水分则回到再生塔顶部,以保持溶液中水组分的平衡和降低溶剂的蒸发损失。
溶液中闪蒸出来的烃类进入燃料气系统。
图4-1醇胺法脱硫的典型工艺流程二、物理溶剂吸收法物理溶剂吸收法又叫物理吸收法,主要是利用有机化合物对天然气中的酸性组分进行物理吸收而将它们从原料气脱除。
物理吸收法遵循享利定律:Ci=KiPi。
Ci——某气体i在某溶剂中饱和溶液的浓度;Pi——某气体i的分压;Ki——溶解常数,与气体和溶剂的性质有关;与温度有关,通常随温度升高而减小。
从享利定律可知,溶剂的酸气负荷正比于气相中酸性组分的分压。
吸收了酸性组分的的富液在压力下降时,会放出所吸收的酸性组分。
因此,吸收操作应在高压低温下进行,而解吸应在高温低压下进行。
物理溶剂吸收法的优点主要有:溶剂吸收能力强,适宜于处理酸气分压高的原料气;溶剂不易变质,无腐蚀,对设施、装置无苛刻要求;还能脱除有机硫等。
物理溶剂吸收法不宜用于重烃含量高的原料气。
且多数方法由于受溶剂溶解平衡的影响,再生程度受到一定限制,净化度比不上化学吸收法。
物理溶剂吸收法的流程一般较简单,主要设备有吸收塔、闪蒸塔和循环泵。
溶液通常靠多级闪蒸进行再生,不需要蒸汽和其它热源。
当净化度要求较高时,则需采用汽提或真空闪蒸真空解吸、惰性吹脱和加热溶剂等较为复杂的方法进行再生。
目前已应用于工业的有主要有以下四种(2):即弗卢尔(Flour)法使用的碳酸丙烯酯,普里索尔(Purisol)法使用的N—甲基吡咯烷酮(NMP),埃斯塔索文(Estasolven)法使用的磷酸三丁酯(TBP)和赛勒克梭(Selexol)法使用的聚二醇二四醚。
三、物理—化学吸收法物理—化学吸收法使用化学溶剂和物理溶剂的混合液,兼有化学吸收和物理吸收两类方法的特点。
物理—化学吸收法不仅有良好的选择性,还能脱除有机硫和溶液的硫负荷均较高的特点。
迄今为止,工业上应用最广泛的物理—化学吸收法是砜胺法也称为萨菲诺(Sulfinol)法,此法所采用的物理溶剂为环丁砜,而化学溶剂则是一乙醇胺(MEA)、二异丙醇胺(DIPA)或甲基二乙醇胺(MDEA)等,溶液中还含有一定量的水。
其余还有Optisol、Amisol、Selefining、UcarsolLE等(3)。
下面以砜胺法为例简要介绍物理—化学吸收法。
(一)溶液组成如上所述,砜胺法溶液由环丁砜、醇胺和水组成。
醇胺主要是指MEA、DGA、DIPA、MDEA 等,但工业化后最常用的主要有DIPA(Sulfinol-D法)和MDEA(Sulfinol-M法),主要原因是它们对设备的腐蚀轻微,不易变质和发泡,且可以兼顾到一定选择性。
溶液的组成一般控制在环丁砜45%、DIPA40%、水15%。
溶液中水的存在不仅是醇胺与CO2反应所必须的,同时可以降低溶液的粘度,改善换热器传热效率,减少溶液对烃类的吸收量,改善再生效果。
不过含水量过高又会导致溶液的酸气负荷下降,热容升高和净化气露点升高等缺点。
因此,溶液中的水含量不应低于10%,不能高于25%。
(二)基本原理砜胺法溶液中的环丁砜和水对酸性组分的吸收属于物理吸收,环丁砜吸收酸性组分能力强,在相同条件下吸收H2S的能力是水的7倍,对CO2的吸收能力为水的两倍(见表4-2),它们基本上服从享利定律。
环丁砜化学名是二氧化四氢噻吩,对水、酸、碱、氧稳定,在220℃以下有很好的热稳定性。
环丁砜溶于水,不易挥发、无毒不易燃。
其结构式为:H2C——CH2H2CCH2SOO砜胺法溶液中醇胺对酸性组分的吸收属于化学吸收。
其化学反应在表4-1中已有表述。
砜胺溶液的吸收平衡曲线是物理吸收与化学吸收作用的总和。
如图4-2(4)所示,在H2S分压低时,平衡吸收量随分压的变化不明显,表明化学吸收起主导作用,随着H2S分压升高,物理吸收作用迅速增大,环丁砜的物理吸收作用增大。
图4-2 H2S在溶剂中平衡溶解度(三)砜胺法的主要优点1、酸气负荷高砜胺法的流程与醇胺法基本相同,与醇胺溶液比较,砜胺溶液用环丁砜代替醇胺溶液中一部分水,环丁砜是H2S的良好吸收剂,在其它条件相同时,H2S在环丁砜中的溶解度比在水中的溶解度大得多,所以砜胺溶液比醇胺溶液有较高的酸气负荷。
2、消耗指标低由于砜胺溶液的酸气负荷高,所以相应的溶液循环量就低,一般约为MEA法的50~70%;溶液的比热也比醇胺溶液低(环丁砜的比热为水比热的1/3),砜胺液再生比醇胺液容易,耗热少,因此,砜胺法比醇胺法的水、电、蒸汽等消耗指标低得多。
3、净化度高与单纯的物理吸收和化学吸收法相比较,由于砜胺法兼有物理和化学两种脱硫溶剂的特长,其脱硫效率比较高,从长期的操作经验看,可以达到H2S含量低于6mg/Nm3,而且还能脱除相当数量的有机硫化物。
4、溶剂损失量小由于环丁砜的化学性质稳定,蒸汽压低,再生时蒸发损耗少。
5、对设备腐蚀较轻微由于Sulfinol-D或Sulfinol-M中胺液都比较稳定,降解产物少;环丁砜本身也很稳定,减少了溶液中的水含量,就减少了酸性组分对金属的酸性腐蚀。
四、直接氧化法这类方法以氧化—还原反应为基础,借助溶液中氧载体的催化作用,把被碱性溶液吸收的H2S直接氧化为单质硫,然后通过鼓入空气,使吸收剂再生,从而使脱硫与硫回收合为一体。
与醇胺法脱硫相比,氧化还原法的优点可归纳如下:1、净化度高,净化气中H2S含量可低于5mg/Nm3;2、脱硫的同时直接生成元素硫,基本上无二次污染;3、多数方法可以选择脱除H2S而基本上不脱除CO2;4、操作温度为常温,操作压力高压或常压均可。
直接氧化法在焦炉气、水煤气、合成气、克劳斯装置尾气处理方面有广泛应用,近年来在天然气脱硫领域内也正在推广。
但由于这类方法吸收溶剂的硫容量(单位质量或体积溶液能够吸收硫的质量),故主要是应用在小型单井脱硫或移动撬装装置方面。
以所使用的氧载体分类,直接氧化法主要有铁法,钒法及其他方法。
铁法的氧载体大多使用三价铁,目前国内获工业应用的有EDTA络合铁法,FD法及HEDP-NTA络合铁法等(5)。
钒法的氧载体是五价钒,获工业应用的主要有Stretford法,Sulfolin及Unisulf法等。
五、固体吸收、吸附法固体吸收、吸附法是指使H2S被固体物质吸收或吸附,然后再用空气或减压解吸,使吸收、吸附剂再生的方法。
固体吸收法主要有固体氧化铁法,吸附法主要有分子筛法。
这两类脱硫方法仅适用于H2S含量较低或流量很小的天然气脱硫。
固体吸收法主要指以固体脱硫剂(主要成分为活性氧化铁)吸收天然气中的H2S,它们与H2S发生如下反应:Fe2O3+3H2S→Fe2S3+3H2OFe3O4+4H2S→3FeS+4H2O+SFeS+S→FeS2脱硫剂吸收H2S饱和后,可在水蒸气存在下以空气使之再生,其反应为:2Fe2O3+3O2+6H2O→4Fe(OH)3+6S2Fe(OH)3→Fe2O3+3H2O目前,最常见的固体吸收法主要有海绵铁法,SulfaTreat法等。
固体吸附法是利用天然气中不同组分在吸附剂表面吸附性能的差异,可选择地除去酸性组分的一类方法,常用的固体吸附剂主要有活性炭、分子筛等。