AF的治疗
- 格式:ppt
- 大小:4.07 MB
- 文档页数:63

中华医学科技奖形式审查结果公布年份2018推荐奖种医学科学技术奖项目名称精准干预心脏自主神经(CANS)治疗房颤(AF)推荐单位推荐单位:上海市医学会推荐意见:该项目组在国家自然科学基金、国家国际科技合作专项和上海市科委重点项目的资助下,依托上海健康医学院奉贤中心医院中心实验室和心血管病研究所,针对AF 临床治疗效果与高发病趋势不匹配、发病机制复杂不明、缺乏精准干预CANS治疗AF的策略和路径等科学问题,主要成果包括:(1)犬“CANS介导AF”模型方法学数据库建设;(2)CANS因果AF”动物模型制作和机制研究;(3)量化靶向干预CANS 治疗AF”三个内容的研究。
研究研究成果为行业内系统地开展“CANS介导AF”相关机制的研究、制定干预CANS的措施、研发“CANS因果AF”动物模型,奠定了扎实的基础。
所研发的“CANS因果AF”动物模型,确证CANS张力异常是独立和上游触发AF的因素,为临床CANS触发的AF的机制和干预策略的研究,提供科学可靠的动物模型。
研究同时提出了,持续2小时和1000bpm快频率AF(量化)需要干预交感神经,以及治疗“CANS触发AF”,应当靶向RAN和AVN-FP‘主控区’的精准干预CANS 治疗AF的创新理论。
鉴于本项应用基础研究的创新内容,产生了良好的社会效应。
同意推荐该项目申报2018年中华医学科技奖。
项目简介心房颤动(AF)是临床常见的心律失常,具有较高的致残和病死率。
心脏自主神经(CANS) 功能紊乱在AF的发生和发展中起着重要的作用,然而CANS触发和维持AF 的机制尚未阐明,并且干预CANS治疗AF尚未未取得实质性的突破。
基于研究基础并查阅文献,我们发现当前研究CANS与AF相关机制的动物模型,不能诠释“CANS 上游触发AF”的机制,也不能准确回答哪类AF需要干预CANS科学问题。
其次临床治疗AF的PVI+GPs消融术,没有量化CANS活动进行精准靶向干预,可能会过度干预CANS致新的CANS失衡产生。

心房纤颤公主岭市中心医院内三科盛香艳AF是一种十分常见的心律失常,仅次于慢性心律失常和早搏,而居第3位,这种房性心律失常对患者造成很多危害。
因此对我们临床医生来说,正确地诊断和治疗房颤非常重要。
一、发病机制1、心脏协调中心失常学说,最初认为心脏各部协调一致的活动依赖于间隔协调中心的控制。
Koonecker依据此学说用穿刺间隔的方法破坏协调中心制造房颤的模型,但Porrer与Menillion观察到与心脏间隔分离开来的心肌既可颤动也可自发复律。
——故不支持协调中心失常单说。
2、单中心和多中心异位冲动学说支持此学说的证据有:○1某些af继发于房早、房速。
○2af常见于洋地黄中毒,甲亢、肺部疾病,交感N↑,发热等。
○3af常见于心房肌受牵拉,细胞内钙超载和心力衰竭等易于诱发房颤的条件。
○4局部注射乌更碱可产生房颤,但消融后可消除af。
○5单一点快速心房起搏,使心房组织不能保持1:1夺获,可模拟出房颤的心电。
○6用计算机等时标测技术研究af有时可见af激动顺序局灶激动模式。
3、多折反学说Af发生和维持的电生理基础是有效不应期缩短。
心房超速起搏表明,心房肌波长在9.7~12.3cm—超速起搏骤停出现2~3个连发性早搏;心房波长在7.8~9.7cm者超速起搏诱发房扑反应;心房波长<7.8cm,超速起搏才能诱发af,可见短波长才能在心房内建立子波拆反,此与af心房肌有效不定期缩短相一致。
心房内有4~6个以上的子波折返才表现出af—心房越大越容易af。
Ⅲ类抗心律失常药,延长有效不应期。
治疗afIC类抗心律失常药,减慢房内传导,延长折反波长4、af的心房肌重构,所谓的电重构即在快速心率或其他病理条件影响下,发生电生理特性的改变。
Af时心房肌有效不应期的缩短,即是电重构的基本表现。
给狗心房 800次/min 30min 就可产生af叶持续时间越长,招致af、引起af、越不容易复律。
5、自主N介导的af,心肌电活动的稳定性在于迷走N与交感N活动的平衡。

干预自主神经系统治疗心房颤动的进展(完整版)心房颤动(Atrial fibrillation,AF)是最常见的快速性心律失常之一。
按照2016 ESC/EACTS房颤管理指南,在2010年,估计世界范围内AF 的男性和女性分别为2 090万和1 260万人,在发达国家中发病率和患病率更高[1-2]。
到2030年,预期在欧洲有1 400 ~1 700万名AF患者,每年新诊断12 ~21.5万名AF患者[2-4]。
AF随着年龄增加发病率逐渐增高,随着老龄化时代的来临,AF的发病率和危害也日益加重。
目前治疗AF的主要方式为手术消融和药物治疗,王等[5]人将402例AF患者分为消融组和抗心律失常药物组,进行随访得出结论:消融组治疗有效率为83.2%,药物组治疗有效率为50.2%,虽然消融组有效率高于药物组,但仍有较高的复发率,如何更加有效的治疗AF,增加成功率降低复发率也越来越引起临床医生的重视。
AF的发生机制复杂,研究发现AF的发生与遗传因素、心脏自主神经系统(Cardiac Autonomic Nervous System,CANS)的激活和肾素-血管紧张素-醛固酮系统的激活等有关。
而越来越多的证据显示自主神经系统(Autonomic Nervous System,ANS)活动在AF的发生和维持中都起着重要作用,通过干预ANS(包括神经丛消融、肾去神经化治疗、经皮神经刺激、运动训练等)可能提高AF治疗的成功率并降低AF复发率。
本文拟对CANS及解剖、引起AF的机制及干预自主神经治疗AF的进展进行综述。
1 与CANS相关的解剖交感神经纤维主要来源于沿颈部和胸部脊髓的主要自主神经节。
这些自主神经节包括颈上神经节(与C1-3相通)、星状(颈胸)神经节(与C7-8至T1-2连通)和胸神经节(低至第七胸神经节)。
星状神经节是心脏交感神经支配的主要来源,星状神经节与多个胸内神经和结构以及皮肤相连(图1)。
这些神经节容纳大多数节后交感神经元的细胞体,其神经轴突形成上、中、下心脏神经并终止于心脏表面。

体表ECG信号分析技术在AF信号分析过程中的价值心房颤动(Atrail fibrillation,简称房颤)是临床最常见的持续性心律失常。
目前,AF的治疗,如:速率和节律控制,通常都是基于试错法,主要是因为还没有找到预测AF状态和对药物反应情况的有效测试方法,导致现有的治疗策略都未能把AF的各种机制和模式考虑在内[1],其效果均存在无法预料的不确定性。
从体表心电图对房颤信号的时频相关特征进行分析,能及时提供反映患者心房活动动态行为的信息。
本文首先简单分析了STFSA技术宅房颤机制研究与临床应用中的争议后,尝试使用体表心电图频谱分析技术,探讨其在预测药物治疗房颤中的价值。
房颤是最常见的心律失常疾病之一,几乎见于所有的器质性心脏病,在非器质性心脏病亦可发生。
可引起严重的并发症,如心力衰竭和动脉栓塞,心脏病患者中,有心房颤动的患者死亡率是其他患者的两倍。
据统计,中国房颤患者约为800万,60岁以上是高发人群,而且随着老龄化进程的加快,房颤患者人数还会增长[2]。
一、STFSA技术用于AF信号分析中的不足通常房颤由局部快速激动触发,这些局部区域中常见者包括肺静脉,上腔静脉。
近年来,人们开始研究其诱发和维持的机制,主要有触发学说、折返学说、多波子学说和主导转子学说等。
这些理论希望研究能够对AF做出定量分析和引导AF治疗的有效指标和方法[3]。
近年来,针对房颤节律下心房心电信号的研究成为最近的热点。
其中时空频谱分析(spatio-temporal frequency spectral analysis,STFSA)技术为房颤机制的研究提供了重要手段,同时对临床治疗也具有重要的指导价值。
尽管STFSA 技术已经较广泛应用于房颤机制研究和临床应用,但是目前仍存在一定的争议,主要变现在以下几个方面:1采样位点和时间的差异。
不同的研究中心信息采样时间和位点并不一致,这使得分析结果往往存在差异,并不一样。
2心室波常被删除。

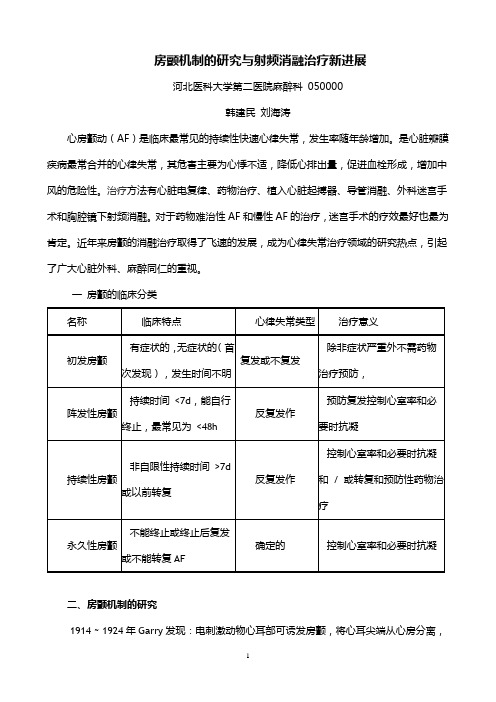
房颤机制的研究与射频消融治疗新进展河北医科大学第二医院麻醉科050000韩建民刘海涛心房颤动(AF)是临床最常见的持续性快速心律失常,发生率随年龄增加。
是心脏瓣膜疾病最常合并的心律失常,其危害主要为心悸不适,降低心排出量,促进血栓形成,增加中风的危险性。
治疗方法有心脏电复律、药物治疗、植入心脏起搏器、导管消融、外科迷宫手术和胸腔镜下射频消融。
对于药物难治性AF和慢性AF的治疗,迷宫手术的疗效最好也最为肯定。
近年来房颤的消融治疗取得了飞速的发展,成为心律失常治疗领域的研究热点,引起了广大心脏外科、麻醉同仁的重视。
一房颤的临床分类二、房颤机制的研究1914 ~ 1924年Garry发现:电刺激动物心耳部可诱发房颤,将心耳尖端从心房分离,离去心耳组织则不颤动,未被离去的心房组织颤动。
提出了房颤是由一系列飘忽不定、高度复杂的环形运动组成。
1947 年Scher 提出了房颤局灶机制假说:心房的局灶发放高频电激动可导致房颤。
当兔心房局部注射乌头碱后可诱发房颤,切除注射乌头碱的部位心房后房颤终止。
1955 年Nahum 和Hoff通过刺激犬的胆碱能神经能够诱发房颤或房性早搏。
为房颤的去迷走神经治疗的提供理论基础。
1959 年Moe 和Abildskov通过犬迷走神经介导的房颤模型研究,提出了“ 多发子波折返” 假说:房颤的维持有赖于心房内一定数量(至少3~5 个)折返子波的同时存在,折返环路与心房解剖无关,由心房局部的有效不应期和可兴奋性决定。
这些折返子波之间可以发生碰撞、湮灭、分裂、融合等多种作用方式,导致折返子波的数量、折返环的大小、速度等改变。
较好解释房颤的多种电生理特性。
1982 年Allessie 等在犬心通过灌注乙酰胆碱和快速心房起搏诱发出持续性房颤,并在心内膜密集标测;结果证实了M oe 和Abildskov的多发性子波折返学说。
1992年,Schuessler研究结果显示,心房内存在着的周长很短的“8”字形密闭的功能性折返环,这种周长很短的折返环可使折返环周围心房肌组织产生颤动样传导从而导致房颤。
・专家论坛・胺碘酮应用指南解读蒋文平 杨向军中图分类号 R541.7 R972.+2 文献标识码 A 文章编号 1007-2659(2005)01-0016-03作者单位:苏州大学附属第一医院心内科(江苏苏州215006) 胺碘酮(a m i odar one,AM )1962年在比利时合成,早年作为冠状动脉扩张剂,用于心绞痛治疗,但它能延长QT 间期,具抗心律失常作用。
上世纪70年代初Rosenbau m 等将其作为抗心律失常药物(AAD ),开始在欧洲和南美应用,直到1985年美国F DA 才批准用于危及生命的室性心律失常治疗。
心房颤动(AF )心房扑动(AF L )也是共识的适应证。
1 为何要制订A M 的应用指南胺碘酮作为AAD 应用已30余年,为何现在要制订应用指南呢?AM 现在是全球应用最广的AAD,到1998年它的处方已占了抗心律失常药物处方的24.1%,其中欧洲和北美分别占34.8%、32.8%,拉丁美洲占73.8%,亚洲国家较少。
它心脏副作用很小,抗心律失常范围广,但心外副作用较多,因此必需规范它的使用方法和适应证。
在2000年[1]、2003年[2]分别有两个应用指南问世。
我国应用胺碘酮也已25年余,也积累了自己的一些经验,在应用上也有一些共识,因此在2004年我们参阅国外的经验,制订了我国AM 的应用指南[3]。
2 AM 的药代动力学要正确地应用AM ,必需对其药代动力学有所了解,AM 是含碘苯呋喃衍生物,200mg 的AM 含碘量74.7mg,它是高度脂溶性,吸收后广泛分布于脂肪、肌肉、皮肤、内脏等各种组织,因此它的清除半衰期极长(平均60天以上),口服要达到体内平衡也需很长时间,因此为缩短起效时间,必需给较大负荷量。
一般在体内取得平衡,摄入量与排出量取得相等需数周或一月以上。
负荷量越大,起效越快,因此口服AM 负荷量一般在二周内10g 左右,维持量200~400mg/d 。