G6一些硅酸盐矿物的讲义晶体化学式计算
- 格式:ppt
- 大小:839.00 KB
- 文档页数:65

矿物晶体化学式计算方法矿物晶体化学式计算方法一、有关晶体化学式的几个基本问题1.化学通式与晶体化学式化学通式(chemical formula)是指简单意义上的、用以表达矿物化学成分的分子式,又可简单地称为矿物化学式、矿物分子式。
晶体化学式(crystal-chemical formula)是指能够反映矿物中各元素结构位置的化学分子式,即能反映矿物的晶体化学特征。
举例:(1)钾长石的化学通式为:KAlSi3O8或K2O⋅Al2O3⋅6SiO2,而其晶体化学式则必须表示为K[AlSi3O8];(2)磁铁矿的化学式可以写为:Fe3O4,但其晶体化学式为:FeO⋅Fe2O3。
(3)具Al2SiO5化学式的三种同质多像矿物:红柱石、蓝晶石和夕线石具有不同的晶体化学式:2. 矿物中的水自然界中的矿物很多是含水的,这些水在矿物中可以三种不同的形式存在:吸附水、结晶水和结构水。
层间水等。
由于H3O+与K+大小相近,白云母KAl2[AlSi3O10](OH)2在风化过程中K+易被H3O+置换形成水云母(K, H3O+)Al2[AlSi3O10](OH)2。
由于结晶水和结构水要占据一定的矿物晶格位置,所以在计算矿物晶体化学式要考虑它们的数量。
3. 定比原理定比是指组成矿物化学成分中的原子、离子、分子之间的重量百分比是整数比,即恒定值。
举例:(1) 某产地的磁铁矿的化学分析结果为:FeO=31.25%,Fe2O3=68.75%,已知它们的分子量分别为:71.85和159.70。
因此,FeO和Fe2O3的分子比为:FeO:Fe2O3=(31.25/71.85):68.75/159.70)=1.01:1因此,磁铁矿的化学式可写为:FeO Fe2O3或Fe3O4。
(2) 某金绿宝石的化学成分为BeO=19.8%,Al2O3=80.2%,它们的分子量分别为25和102,因此两者之间的分子比为:BeO:Al2O3=(19.8/25) 80.2/102)=1:1金绿宝石的化学式可简写为BeO Al2O3或BeAl2O4。

------------------------------------------------------------精品文档-------------------------------------------------------- 成岩成矿矿物学––矿物晶体化学式计算方法矿物晶体化学式计算方法一、有关晶体化学式的几个基本问题1.化学通式与晶体化学式化学通式(chemical formula)是指简单意义上的、用以表达矿物化学成分的分子式,又可简单地称为矿物化学式、矿物分子式。
晶体化学式(crystal-chemical formula)是指能够反映矿物中各元素结构位置的化学分子式,即能反映矿物的晶体化学特征。
举例:(1)钾长石的化学通式为:KAlSiO或KO?AlO?6SiO,而其晶体化学式则282332必须表示为K[AlSiO];83(2)磁铁矿的化学式可以写为:FeO,但其晶体化学式为:FeO?FeO。
3432(3)具AlSiO化学式的三种同质多像矿物:红柱石、蓝晶石和夕线石具有不同的晶52体化学式:2. 矿物中的水自然界中的矿物很多是含水的,这些水在矿物中可以三种不同的形式存在:吸附水、结晶水和结构水。
吸附水:吸附水以机械吸附方式成中性水分子状态存在于矿物表面或其内部。
吸附水不参加矿物晶格,可以是薄膜水、毛细管水、胶体水等。
当温度高于110?C 时则逸散,它可以呈气态、液态和固态存在于矿物中。
吸附水不写入矿物分子式。
结晶水:结晶是成中性水分子参加矿物晶格并占据一定构造位置。
常作为配位体围绕某一离子形成络阴离子。
结晶水的数量与矿物的其它组份呈简单比例。
如石膏:Ca[SO] ?2HO。
24++-+等离子形式参加H、OHH(或称化合水):常以OO表示,结构水呈H、结构水32-+离子少见,O最常见。
H矿物晶格。
占据一定构造位置,具有一定比例。
通常以OH3+++与HO + HO。
结构水如沸石水、层间水等。


总结硅酸盐类矿物的晶体化学特点与物理性质之间的关系及亚类的划分总结硅酸盐类矿物的晶体化学特点与物理性质之间的关系及亚类的划分由于中心原子Si是四面体的结构,这种稳定的结构使得硅酸盐有稳定的化学性质,从而其硬度大、耐火,可用于制造耐火材料、玻璃、陶瓷、水泥等。
化学成分和晶体化学特征在硅酸盐矿物的晶体结构中,硅氧配位四面体[SiO4]4-是它们的基本构造单元。
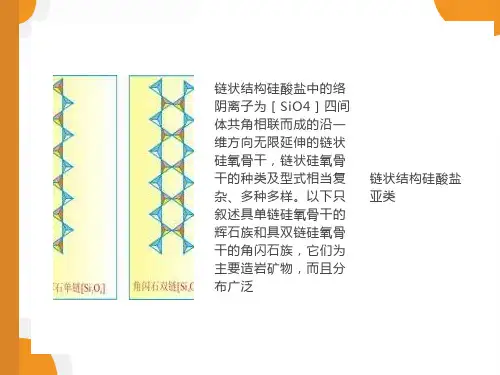
硅氧四面体在结构中可以孤立地存在,也可以以其角顶相互连接,即每一硅氧四面体可与一个、两个、三个甚至四个硅氧四面体相连,从而形成多种复杂的络阴离子。
根据硅氧四面体在晶体结构中的连接方式,主要有下列5中类型的络阴离子: 1、岛状络阴离子 2、环状络阴离子 3、链状络阴离子 4、层状络阴离子 5、架状络阴离子化学成分和晶体化学特征在硅酸盐矿物的晶体结构中,硅氧配位四面体[SiO4]4-是它们的基本构造单元。
硅氧四面体在结构中可以孤立地存在,也可以以其角顶相互连接,即每一硅氧四面体可与一个、两个、三个甚至四个硅氧四面体相连,从而形成多种复杂的络阴离子。
根据硅氧四面体在晶体结构中的连接方式,主要有下列5中类型的络阴离子: 1、岛状络阴离子 2、环状络阴离子 3、链状络阴离子 4、层状络阴离子 5、架状络阴离子请总结硅酸盐类矿物的晶体化学特点与物理性质之间的关系及亚类的划分。
求高人啊啊这本上面有,讲的挺好。
《无机化学》第四版,高等教育出版社,面向21世纪课程教材,北京师范大学无机化学教研室、华中师范大学无机化学教研室、南京师范大学无机化学教研室编(吴国庆主编)。
简述氧化物类矿物化学组成、晶体化学、形态、物理性质等特点由两种元素组成,其中一种是氧元素的化合物是氧化物。
不同氧化物的晶体类型,形态及物理性质不同,例如二氧化硅是原子晶体,质地坚硬,硬度大,熔点高,表面有光泽。
而二氧化碳是分子晶体,无色无味,密度比空气大,微溶于水。
二氧化钠是离子晶体,为白色块状晶体,硬密度较小,熔点较底,暴露在空气中易潮解。




矿物晶体化学式计算⽅法矿物晶体化学式计算⽅法⼀、有关晶体化学式的⼏个基本问题1.化学通式与晶体化学式化学通式(chemical formula)是指简单意义上的、⽤以表达矿物化学成分的分⼦式,⼜可简单地称为矿物化学式、矿物分⼦式。
晶体化学式(crystal-chemical formula)是指能够反映矿物中各元素结构位置的化学分⼦式,即能反映矿物的晶体化学特征。
举例:(1)钾长⽯的化学通式为:KAlSi3O8或K2O?Al2O3?6SiO2,⽽其晶体化学式则必须表⽰为K[AlSi3O8];(2)磁铁矿的化学式可以写为:Fe3O4,但其晶体化学式为:FeO?Fe2O3。
(3)具Al2SiO5化学式的三种同质多像矿物:红柱⽯、蓝晶⽯和⼣线⽯具有不同的晶体化学式:2. 矿物中的⽔⾃然界中的矿物很多是含⽔的,这些⽔在矿物中可以三种不同的形式存在:吸附⽔、结晶⽔和结构⽔。
吸附⽔:吸附⽔以机械吸附⽅式成中性⽔分⼦状态存在于矿物表⾯或其部。
吸附⽔不参加矿物晶格,可以是薄膜⽔、⽑细管⽔、胶体⽔等。
当温度⾼于110?C时则逸散,它可以呈⽓态、液态和固态存在于矿物中。
吸附⽔不写⼊矿物分⼦式。
结晶⽔:结晶是成中性⽔分⼦参加矿物晶格并占据⼀定构造位置。
常作为配位体围绕某⼀离⼦形成络阴离⼦。
结晶⽔的数量与矿物的其它组份呈简单⽐例。
如⽯膏:Ca[SO4] ?2H2O。
结构⽔(或称化合⽔):常以H2O+表⽰,结构⽔呈H+、OH-、H3O+等离⼦形式参加矿物晶格。
占据⼀定构造位置,具有⼀定⽐例。
通常以OH-最常见。
H3O+离⼦少见,也最不稳定,易分解:H3O+→H++ H2O。
结构⽔如沸⽯⽔、层间⽔等。
由于H3O+与K+⼤⼩相近,⽩云母KAl2[AlSi3O10](OH)2在风化过程中K+易被H3O+置换形成⽔云母(K, H3O+)Al2[AlSi3O10] (OH)2。
由于结晶⽔和结构⽔要占据⼀定的矿物晶格位置,所以在计算矿物晶体化学式要考虑它们的数量。

矿物晶体化学式计算方法一、有关晶体化学式的几个基本问题1. 化学通式与晶体化学式化学通式(chemical formula)是指简单意义上的、用以表达矿物化学成分的分子式,又可简单地称为矿物化学式、矿物分子式。
晶体化学式(crystal-chemical formula)是指能够反映矿物中各元素结构位置的化学分子式,即能反映矿物的晶体化学特征。
举例:(1)钾长石的化学通式为:KAlSi3O8或K2O⋅Al2O3⋅6SiO2,而其晶体化学式则必须表示为K[AlSi3O8];(2)磁铁矿的化学式可以写为:Fe3O4,但其晶体化学式为:FeO⋅Fe2O3。
(3)具Al2SiO5化学式的三种同质多像矿物:红柱石、蓝晶石和夕线石具有不同的晶体化学式:红柱石:Al V Al VI OSiO4蓝晶石:Al2VI OSiO4矽线石:Al VI SiAl IV O5此外,还要指出的是,晶体化学式是最简化学式的Z倍(Z为单位晶胞分子数)。
如:金红石TiO2,其Z=2,因此,金红石的晶体化学式应该为:Ti2O4,锐钛矿的Z=4,它的晶体化学式为Ti4O8,板钛矿的Z=8,它的晶体化学式为Ti8O16。
2. 矿物中的水自然界中的矿物很多是含水的,这些水在矿物中可以三种不同的形式存在:吸附水、结晶水和结构水。
吸附水:吸附水以机械吸附方式成中性水分子状态存在于矿物表面或其内部。
吸附水不参加矿物晶格,可以是薄膜水、毛细管水、胶体水等。
当温度高于110︒C时则逸散,它可以呈气态、液态和固态存在于矿物中。
吸附水不写入矿物分子式。
结晶水:结晶是成中性水分子参加矿物晶格并占据一定构造位置。
常作为配位体围绕某一离子形成络阴离子。
结晶水的数量与矿物的其它组份呈简单比例。
如石膏:Ca[SO4] ⋅2H2O。
结构水(或称化合水):常以H2O+表示,结构水呈H+、OH-、H3O+等离子形式参加矿物晶格。
占据一定构造位置,具有一定比例。
通常以OH-最常见。
矿物晶体化学式计算方法一、有关晶体化学式的几个基本问题1.化学通式与晶体化学式化学通式(chemical formula)是指简单意义上的、用以表达矿物化学成分的分子式,又可简单地称为矿物化学式、矿物分子式。
晶体化学式(crystal-chemical formula)是指能够反映矿物中各元素结构位置的化学分子式,即能反映矿物的晶体化学特征。
举例:(1)钾长石的化学通式为:KAlSi3O8或K2O⋅Al2O3⋅6SiO2,而其晶体化学式则必须表示为K[AlSi3O8];(2)磁铁矿的化学式可以写为:Fe3O4,但其晶体化学式为:FeO⋅Fe2O3。
(3)具Al2SiO5化学式的三种同质多像矿物:红柱石、蓝晶石和夕线石具有不同的晶体化学式:2. 矿物中的水自然界中的矿物很多是含水的,这些水在矿物中可以三种不同的形式存在:吸附水、结晶水和结构水。
吸附水:吸附水以机械吸附方式成中性水分子状态存在于矿物表面或其内部。
吸附水不参加矿物晶格,可以是薄膜水、毛细管水、胶体水等。
当温度高于110︒C时则逸散,它可以呈气态、液态和固态存在于矿物中。
吸附水不写入矿物分子式。
结晶水:结晶是成中性水分子参加矿物晶格并占据一定构造位置。
常作为配位体围绕某一离子形成络阴离子。
结晶水的数量与矿物的其它组份呈简单比例。
如石膏:Ca[SO4] ⋅2H2O。
结构水(或称化合水):常以H2O+表示,结构水呈H+、OH-、H3O+等离子形式参加矿物晶格。
占据一定构造位置,具有一定比例。
通常以OH-最常见。
H3O+离子少见,也最不稳定,易分解:H3O+→ H+ + H2O。
结构水如沸石水、层间水等。
由于H3O+与K+大小相近,白云母KAl2[AlSi3O10](OH)2在风化过程中K+易被H3O+置换形成水云母(K,H3O+)Al2[AlSi3O10](OH)2。
由于结晶水和结构水要占据一定的矿物晶格位置,所以在计算矿物晶体化学式要考虑它们的数量。