高考化学二轮复习课件:专题7化学反应与能量变化
- 格式:ppt
- 大小:3.47 MB
- 文档页数:27




2014高三二轮专题复习七 化学反应中的能量变化【考情分析】一、考纲要求1.理解化学反应中的能量变化与化学键变化的关系;2.理解吸热反应、放热反应与反应物及生成物能量的关系;3.了解化学反应中能量变化的实质,知道化学能与热能的转化是化学反应中能量转化的主要形式。
4.认识能源是人类生存和发展的重要基础,知道节约能源、提高能量利用效率的实际意义。
5.了解焓变与反应热涵义。
明确ΔH = H (反应产物)-H (反应物)。
6.理解盖斯定律,并能运用盖斯定律进行有关反应焓变的简单计算。
7.以上各部分知识与技能的综合应用。
二、命题趋向依据新课程化学实验的学习目标和学习内容,近几年的主要题型有(1)热化学方程式的书写及正误判断;(2)反应热的计算;(3)比较反应热的大小;(4)反应热与能源的综合考查。
由于能源问题已成为社会热点,因此有关能源的试题将成为今后命题的热点;对于燃烧热和中和热的概念及计算仍将是高考考查的重点,主要在选择题、填充题、实验题中体现,重点考查学生灵活运用知识、接受新知识的能力。
新课标关注能源、提高能量利用效率,今年又是各地降低能耗,走可持续发展的一年,估计与实际相联系节约能源的试题可出现。
新课标明确了焓变与反应热的关系,极有可能出现运用盖斯定律进行有关反应焓变的简单计算。
考试大纲对反应热的要求是:掌握热化学方程式的含义;了解化学反应中的能量变化、吸热反应、放热反应、反应热、燃烧热、中和热;理解盖斯定律的含义,掌握有关反应热的简单计算;初步认识使用化石燃料的利弊,新能源的开发,燃料充分燃烧的条件。
学习中应以“热化学方程式”为突破口,通过对热化学方程式的书写及正误判断充分理解其含义,同时触类旁通,不断掌握反应热的计算技巧,学会应用盖斯定律。
化学反应中的能量变化在高考中经常涉及的内容有:书写热化学方程式、判断热化学方程式的正误及反应热的大小比较等等。
中和热实验的测定是高中阶段比较重要的一个定量实验。
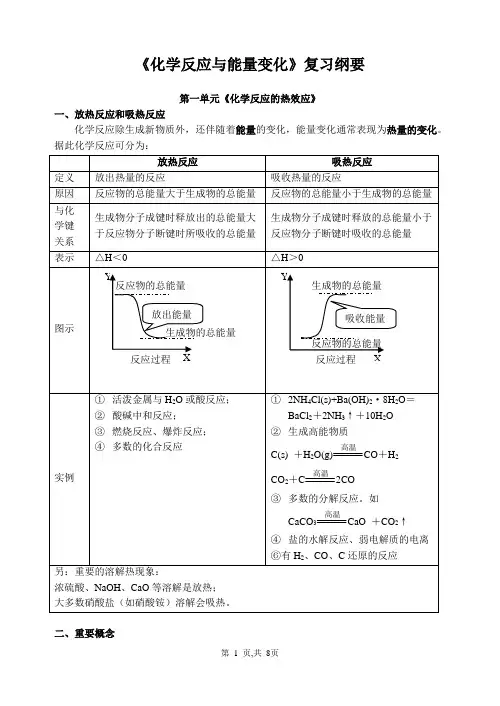
《化学反应与能量变化》复习纲要第一单元《化学反应的热效应》一、放热反应和吸热反应化学反应除生成新物质外,还伴随着能量的变化,能量变化通常表现为热量的变化。
据此化学反应可分为:二、重要概念1、反应热:当化学反应的反应物和产物的温度相同,反应中所放出或吸收的热量称为反应热。
2、焓:物质内部所具有的能量。
焓是物质的一种固有性质。
在一定条件下,一定量的物质具有确定的焓值,但目前人们无法求得,只能判断其相对值。
3、焓变:指反应产物的总焓与反应物的总焓之差。
焓变:△H =H 产物-H 反应物。
单位:kJ ·mol -1。
焓变与反应热的关系:在等压条件下,如果反应中物质的能量变化全部转化为热能的形式,没有其他形式的能量转化,这时的前后焓变即为反应热。
否则,焓变就可能还包含其他形式的能量转化,如光、电、波等。
一般说:反应热=焓变=△H4、燃烧热:25℃,101KPa 时,1mol 物质完全燃烧生成稳定化合物时所放出的热量叫做燃烧热。
一般:C→CO 2(g ),H→H 2O (l ),S→SO 2(g ),N→N 2(g )*苏教版中“标准燃烧热”:指25℃,101KPa 下,1mol 物质完全燃烧生成稳定化合物时的反应热。
或在标准态下,298K 时,1mol 物质完全燃烧的焓变,称为该物质的标准燃烧焓..... 另:写燃烧反应的热化学方程式时,一般可燃物都以1mol 为系数,其他可以是分数。
5、中和热:在稀溶液中,强酸和强碱中和反应,生成1mol H 2O 时的反应热。
注意:①强酸和强碱中和热:H +(aq)+OH -(aq)=H 2O(l);△H =-57.3kJ/mol :。
②弱酸弱碱的中和反应,放出的热会低于57.3 kJ/mol 。
③浓酸、浓碱反应,会受到稀释溶解放热的影响 三、热化学方程式1、定义:能够表示反应热的化学方程式。
2、书写注意:a.标明物质的聚集状态。
如s 、l 、g 、aq 等。





