有机化学反应规律总结(非常齐全)
- 格式:pdf
- 大小:500.99 KB
- 文档页数:5

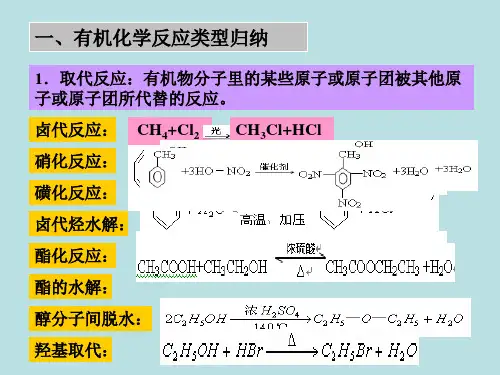
高中化学一轮复习:有机化学知识点总结1、有机反应类型(1)取代反应:有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应。
特征:一般有光照条件;一上一下,交换位置(2)加成反应:有机物分子中双键/叁键上的碳原子与其他原子直接结合生成新的化合物分子的反应。
特征:双键变单键(叁键变双键),原子加两边(3)加聚反应:含碳碳双键或是叁键的相对分子质量小的化合物,在一定条件下,互相结合成相对分子质量大的高分子的反应,简称加聚反应。
特征:双键,小分子变大分子(4)氧化反应:有机物燃烧;醇或醛的催化氧化。
特征:点燃;Cu /Ag 催化(5)酯化反应:醇跟羧酸生成酯和水的反应,也属于取代反应。
2、烃类:仅含碳和氢两种元素的有机物称为碳氢化合物 分为:烷烃、烯烃和炔烃(1)烷烃:碳原子之间都以碳碳单键结合成链状,碳原子剩余的价键全部跟氢原子结合而达到饱和的烃。
如:甲烷(CH 4)、乙烷(C 2H 6)、丙烷(C 3H 8)、丁烷(C 4H 10)等,烷烃通式为:C n H 2n+2(n≥1) 分子式(碳原子数)不同的烷烃互为同系物;分子式相同、结构不同的烷烃互为同分异构体。
(2)烷烃的物理性质a. 随着分子里含碳原子数的增加,熔点、沸点逐渐升高,相对密度逐渐增大;b. 碳原子数等于或小于4的烷烃,在常温常压下都是气体;其他烷烃在常温常压下都是液体或固体;c. 烷烃的相对密度小于水的密度;d. 一般不溶于水,而易溶于有机溶剂,液态烷烃本身就是良好的有机溶剂。
(3)烷烃的化学性质稳定,跟酸、碱及氧化物都不发生反应,也难与其他物质化合;但在特定的条件下能发生下列反应:a. 能燃烧:C n H 2n+2 +3n 12+O 2 −−−→点燃nCO 2 + (n+1)H 2O b. 易与卤素单质X 2取代:C n H 2n+2 + Cl 2 −−−→光照C n H 2n+1Cl + HCl有机物主要化学性质甲烷(1)燃烧(点燃时要验纯)(淡蓝色火焰,无黑烟,甲烷含碳量低)(2)取代反应(与氯气)CH4 + Cl2CH3Cl + HCl CH3Cl + Cl2CH2Cl2 + HClCH2Cl2 + Cl2 CHCl3 + HCl CHCl3 + Cl2CCl4 + HCl现象:黄绿色逐渐消失,试管内壁有油状液滴产生,试管内上升一段水柱。

有机化学基础知识点整理有机合成反应的分类和机理有机化学是研究碳元素及其化合物的科学,是化学的重要分支之一。
在有机化学中,有机合成是一项关键的技术,用于合成复杂的有机分子。
有机合成反应是有机化学中最基本、最重要的内容之一,它通过不同的化学反应方式将简单的有机化合物转化为复杂、有用的有机分子。
一、有机合成反应的分类1. 加成反应:加成反应是指两个或多个分子的化学键被断裂,并形成新的键。
常见的加成反应有羰基化合物的加成反应、烯烃的加成反应等,这些反应能够构建碳碳键和碳氧键。
2. 消除反应:消除反应是指一个分子中的两个官能团结合并成为一个新的官能团,并且释放出一些小分子(如水或卤素)。
典型的消除反应有醇的脱水反应、酮或醇与酸脱水等。
3. 置换反应:置换反应是指原有分子中的一个官能团被另一个官能团所取代。
最常见的例子就是芳香族化合物的取代反应,通过氯代烷和芳香环之间的反应来实现。
4. 氧化还原反应:氧化还原反应是指反应中发生氧化和还原的过程,也是有机合成中最常用的反应之一。
在氧化还原反应中,电子转移导致了化学键的形成或断裂,它可以将一个官能团转化为另一个官能团。
例如,醛可以通过氧化反应转化为羧酸。
5. 缩合反应:缩合反应是指两个或多个分子之间的化合物反应,生成一个更大分子的过程。
例如,胺和酮缩合反应可以生成相应的醛。
二、有机合成反应的机理1. 加成反应机理:加成反应一般经历亲核试剂(nucleophile)攻击电子不足的位点,形成共价键,断裂旧键。
以酮和亲核试剂为例,亲核试剂攻击酮羰基碳上的δ+空穴,使酮羰基碳上的键断裂形成负离子中间体,之后再与亲核试剂发生亲核加成反应生成产物。
2. 消除反应机理:消除反应通常需要考虑酸碱性质和受限杂原子(如O、N等原子)对反应的影响。
脱水反应机理中,醇中的-OH基质子化生成强酸,然后酸催化下分子内的-ОН离子和酸质子反应,释放出水分子,从而形成双键。
3. 置换反应机理:典型的置换反应是芳香族化合物的取代反应。
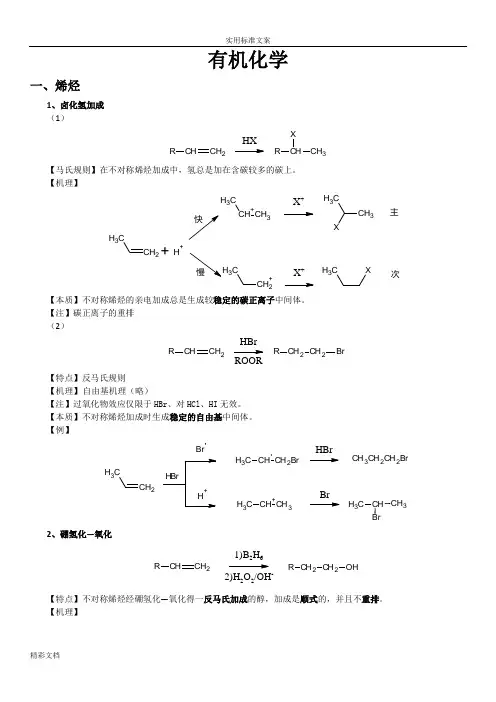
有机化学一、烯烃1、卤化氢加成 (1)CHCH 2RHXCH CH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3CH +CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】2CH33H323H32CH CH2CH32CH CH=CH(CH3CH2CH2)3-H3CH2CH2C22CH3CH2OCH2CH2CH33CH2CH2C2CH2CH3+O H-OHB-OCH2CH2CH3CH2CH2CH3H3CH2CH2B OCH2CH2CH3CH2CH2CH32CH2CH3HOO-B(OCH2CH2CH3)3B(OCH2CH2CH3)3+3NaOH3NaOH3HOCH2CH2CH33+Na3BO32【例】CH31)BH32)H2O2/OH-CH3HHOH3、X2加成C CBr/CClC CBrBr【机理】CCC CBrBrCBr+C CBrOH2+-H+C CBrOH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化1)稀冷高锰酸钾氧化成邻二醇。

高中化学有机(yǒujī)反响(fǎnxiǎng)总结(zǒngjié)高中化学有机(yǒujī)反响(fǎnxiǎng)总结1、取代反响:有机物分子里的某些原子或原子团被其他原子或原子团所取代的反响。
⑴硝化反响:苯分子里的氢原子被NO2所取代的反响。
⑵磺化反响:苯分子里的氢原子被硫酸分子里的磺酸基〔SO3H〕所取代的反响。
⑶酯化反响:酸和醇起作用生成酯和水的反响。
⑷水解反响:一般指有机化合物在一定条件下跟水作用生成两种或多种物质的化学反响。
〔其中皂化反响也属于水解反响。
皂化反响:油脂在有碱存在的条件下水解,生成高级脂肪酸钠和甘油的反响。
〕水解反响包括卤代烃水解、酯水解、糖水解、|白质水解。
另:缩聚反响也属于取代反响。
2、加成反响:有机物分子中双键〔叁键〕两端的碳原子与其他原子或原子团所直接结合生成新的化合物的反响。
⑴油脂的氢化反响属于加成反响。
油脂的氢化:液态油在催化剂〔如Ni〕存在并加热、加压的条件下,跟氢气起加成反响,提高油脂的饱和度的反响,也叫油脂的硬化。
⑵水化反响:在有机化学中指分子中不饱和键〔双键或叁键〕或羰基在催化剂存在或不存在下和水分子化合的反响。
3、消去反响:有机化合物在一定条件下,从一个分子中脱去一个小分子〔如H2O、HBr等〕,而生成不饱和〔含双键和叁键〕化合物的反响。
4、聚合反响:由相对分子质量小的化合物分子结合成相对分子质量较大的高分子化合物的反响。
⑴加聚反响:由不饱和的相对分子质量小的化合物分子结合成相对分子质量较大的高分子化合物的反响。
这样的聚合反响同时也是加成反响,所以叫加聚反响。
⑵缩聚反响:由相对分子质量小的化合物分子结合成相对分子质量较大的高分子化合物,同时生成小分子〔如H2O、NH3、H某等分子〕的反响。
5、氧化反响:在有机反响中,通常把有机物分子中参加氧原子或失去氢原子的反响叫氧化反响。
6、复原反响:在有机反响中,通常把有机物分子中参加氢原子或失去氧原子的反响叫氧化反响。
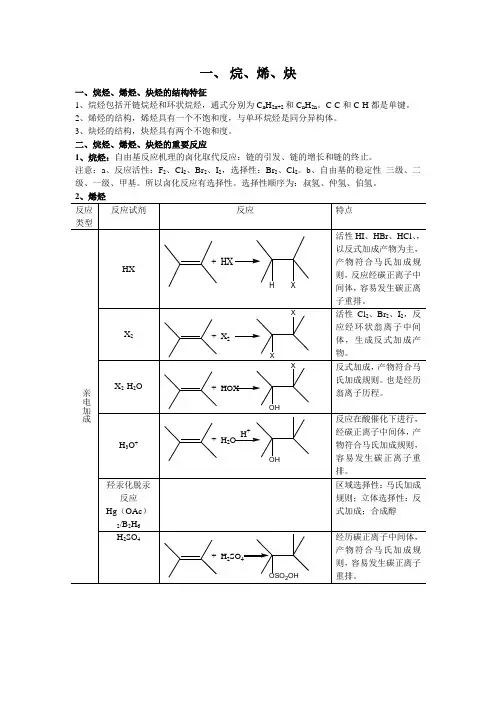
一、烷、烯、炔一、烷烃、烯烃、炔烃的结构特征1、烷烃包括开链烷烃和环状烷烃,通式分别为C n H2n+2和C n H2n。
C-C和C-H都是单键。
2、烯烃的结构,烯烃具有一个不饱和度,与单环烷烃是同分异构体。
3、炔烃的结构,炔烃具有两个不饱和度。
二、烷烃、烯烃、炔烃的重要反应1、烷烃:自由基反应机理的卤化取代反应:链的引发、链的增长和链的终止。
注意:a、反应活性:F2、Cl2、Br2、I2,选择性:Br2、Cl2。
b、自由基的稳定性三级、二级、一级、甲基。
所以卤化反应有选择性。
选择性顺序为:叔氢、仲氢、伯氢。
(1)、与X2和HX可发生1,2-和1,4-加成,后者又称为共轭加成。
1,2-加成是速率控制的反应,1,4-加成是平衡控制的反应。
(2)、D-A反应特点:反应是经环状过渡态进行的协同成环反应,具有立体选择性。
而且是反应是可逆的。
在较高温度下,产物经逆反应生成共轭二烯烃和相应的不饱和亲二烯烃。
富电子的共轭二烯和缺电子的亲二烯体有利于正常的D-A反应的进行。
当烯烃双键上连有吸电子的取代基时是有利于反应的进行。
而且在反应完成时,主要生成内型加成产物。
二、芳烃与芳香杂环化合物一、苯的结构、休克尔规则与芳香性1、苯的结构2、休克尔规则与芳香性(1)芳香性的特点a、具有较大的C/H比b、键长趋于平均化c、具有特殊的稳定性的d、难加成e、易取代f、难氧化(2)非苯系芳香性体系要满足休克尔规则要点:a、单环的化合物具有共轭的离域体系b、共平面或近似于平面c、共轭的π电子数符合4n+2规则,n值必须为整数。
3、具有一个杂原子的五元环、六元环芳香杂环呋喃、吡咯、噻吩和吡啶。
一般说来,杂原子与碳原子的电负性愈接近,其相应的五元芳香的杂环的芳香性愈强。
其共轭能力也愈大。
二、芳环上的取代反应1、苯环上的亲电取代反应芳环上的亲电取代反应主要包括卤化、磺化、消化和付-克反应。
反应通式可表示为:2、苯环上的亲核取代反应由于在芳环中π电子云密度相对较大,亲核试剂难于向芳环进攻,发生相应的亲核取代反应。

2025年有机化学反应规律知识点总结有机化学作为化学领域的重要分支,其反应规律复杂多样且充满魅力。
随着科学技术的不断进步和研究的深入,到 2025 年,我们对有机化学反应规律的认识也更加全面和深入。
以下将对一些重要的有机化学反应规律进行总结。
一、加成反应加成反应是有机化学中常见的反应类型之一,它是指两个或多个分子结合生成一个较大分子的反应。
1、烯烃的加成烯烃是含有碳碳双键的烃类化合物。
在加成反应中,烯烃的双键容易被打开,与其他分子发生加成。
例如,与氢气的加成可以生成烷烃;与卤素单质的加成可以生成卤代烃。
以乙烯与氢气的加成反应为例:CH₂=CH₂+ H₂ → CH₃CH₃,这个反应需要在催化剂的作用下进行,如镍。
2、炔烃的加成炔烃含有碳碳三键,其加成反应与烯烃类似,但相对较为复杂。
例如,与氢气加成可以分步进行,最终生成烷烃。
3、醛和酮的加成醛和酮中的羰基(C=O)可以与氢气、氢氰酸等发生加成反应。
例如,醛与氢气加成生成醇:CH₃CHO + H₂ → CH₃CH₂OH 。
二、取代反应取代反应是指有机物分子中的某些原子或原子团被其他原子或原子团所替代的反应。
1、烷烃的卤代反应烷烃在光照条件下可以与卤素单质发生取代反应,生成卤代烃。
例如,甲烷与氯气的反应:CH₄+ Cl₂ → CH₃Cl + HCl ,反应逐步进行,可以生成一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳等多种产物。
2、苯环上的取代反应苯环具有特殊的稳定性,但在一定条件下也能发生取代反应。
例如,苯与溴在催化剂作用下发生溴代反应生成溴苯。
3、醇的取代反应醇分子中的羟基可以被卤素原子取代,如醇与氢卤酸的反应。
三、消去反应消去反应是指在一定条件下,有机物分子脱去小分子(如 H₂O、HX 等)生成不饱和化合物的反应。
1、醇的消去反应醇在浓硫酸、加热的条件下可以发生消去反应生成烯烃。
例如,乙醇消去生成乙烯:CH₃CH₂OH → CH₂=CH₂+ H₂O 。

化学有机反应顺口溜化学是自然的一种,在分子、原子层次上研究物质的组成、性质、结构与变化规律;创造新物质的科学。
以下是小编为你整理的关于化学有机反应,欢迎大家阅读。
化学有机反应顺口溜有机化学并不难,记准通式是关键。
只含碳氢称为烃,结构成链或成环。
双键为烯叁键炔,单键相连便是烷。
脂肪族的排成链,芳香族的带苯环。
异构共有分子式,通式通用同系间。
烯烃加成烷取代,衍生物看官能团。
羟醛羧基连烃基,称为醇醛及羧酸。
羰基醚键和氨基,衍生物是酮醚胺。
苯带羟基称苯酚,萘是双苯相并联。
去氢加氧叫氧化,去氧加氢叫还原。
醇类氧化变酮醛,醛类氧化变羧酸。
羧酸都比碳酸强,碳酸强于石炭酸。
光照卤代在侧链,催化卤代在苯环。
烃的卤代衍生物,卤素能被羟基换。
消去一个水分子,生成烯和氢卤酸。
钾钠能换醇中氢,银镜反应可辩醛。
氢氧化铜多元醇,溶液混合呈绛蓝。
醇加羧酸生成酯,酯类水解变醇酸。
苯酚遇溴沉淀白,淀粉遇碘色变蓝。
氨基酸兼酸碱性,甲酸是酸又像醛。
聚合单体变链节,断裂派键相串联。
千变万化多趣味,无限风光任登攀。
化学有机反应顺口溜拓展一化合价实质要记准,金正非负单质零;氢一氧二应记住,正负总价和为零;许多元素有变价,条件不同价不同。
化学有机反应顺口溜拓展二钾钠铵硝都能溶,盐酸不溶只有银:硫酸不溶只有钡,微溶还有钙和银;碳酸大多都不溶,溶铵钾钠微溶银;碱类大多都不溶,只溶铵钠钾和钡,石灰水儿属微溶。
化学有机反应顺口溜拓展三钾钠银氢正一价,钙镁钡锌正二价;铝是正三氧负二,氯负一价最常见;硫有负二正四六,正二正三铁可变;正一二铜二四碳,单质零价永不变;其它元素有变价,先死后活来计算。

有机化学重要的反应整理重要的反应1.能使溴水( Br 2/H 2O)褪色的物质( 1)有机物① 通过加成反应使之褪色:含有、— C≡ C—的不饱和化合物② 通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③ 通过氧化反应使之褪色:含有— CHO (醛基)的有机物(有水参加反应)注意:纯净的只含有— CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④ 通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯( 2)无机物① 通过与碱发生歧化反应3Br 2 + 6OH -== 5Br -+ BrO 3- +3H2O 或 Br 2 + 2OH -== Br - +BrO - + H2O② 与还原性物质发生氧化还原反应,如2- 2 -、 I-2+ H2S、 S、 SO2、 SO3、Fe2.能使酸性高锰酸钾溶液KMnO4/H+ 褪色的物质1)有机物:含有、— C≡C—、— OH(较慢)、— CHO 的物质苯环相连的侧链碳上有氢原子的苯的同系物(但苯不反应)2)无机物:与还原性物质发生氧化还原反应,如2-、 SO2、 SO32---2+ H2S、S、 Br、 I、 Fe3.与 Na 反应的有机物:含有—OH、— COOH 的有机物与 NaOH 反应的有机物:常温下,易与含有酚羟基、— COOH 的有机物反应...加热时,能与卤代烃、酯反应(取代反应)与 Na2CO3反应的有机物:含有酚羟基的有机物反应生成酚钠和NaHCO3;.含有— COOH 的有机物反应生成羧酸钠,并放出CO2气体;含有— SO3H 的有机物反应生成磺酸钠并放出CO2气体。
与 NaHCO 3反应的有机物:含有— COOH 、— SO3H 的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
4.既能与强酸,又能与强碱反应的物质( 1) 2Al + 6H + == 2 Al 3+ + 3H 2↑2Al + 2OH - + 2H 2O == 2 AlO 2-+ 3H2↑+3+O Al 2O3 + 2OH-== 2 AlO 2-+ H O( 2) Al O + 6H == 2 Al+ 3H22( 3) Al(OH) 3 + 3H + == Al 3+ + 3H2O Al(OH) 3 + OH - == AlO 2-+2 H2O( 4)弱酸的酸式盐,如NaHCO 3、NaHS 等等NaHCO 3 + HCl == NaCl + CO 2↑ + H2O NaHCO 3 + NaOH == Na 2CO3 + H 2ONaHS + HCl == NaCl + H 2S↑NaHS + NaOH == Na 2S + H2O(5)弱酸弱碱盐,如 CH3COONH 4、 (NH 4 )2S 等等2CH 3COONH 4 + H 2SO4 == (NH 4)2SO4 + 2CH 3COOHCH 3COONH 4 + NaOH == CH 3 COONa + NH 3↑ + H 2O(NH 4)2S + H 2SO4 == (NH 4) 2SO4 + H 2S↑(NH 4)2S +2NaOH == Na 2S + 2NH 3↑ + 2H 2O( 6)氨基酸,如甘氨酸等H 2NCH 2COOH + HCl→ HOOCCH 2NH 3ClH 2NCH 2COOH + NaOH→H2NCH 2COONa + H 2O( 7)蛋白质分子中的肽链的链端或支链上仍有呈酸性的—COOH 和呈碱性的— NH 2,故蛋白质仍能与碱和酸反应。

有机化学反应机理总结有机化学反应机理是有机化学研究的重要内容之一,它揭示了有机化合物在反应过程中的分子结构变化和反应速率规律。
通过对有机反应机理的研究,我们可以更好地理解和预测有机化学反应的发生过程,为有机合成化学和药物设计提供理论依据。
下面我们将对常见的有机化学反应机理进行总结和归纳。
1. 加成反应。
加成反应是有机化学中最基本的反应类型之一,它是指两个或多个单体分子中的双键或三键断裂,然后原子或原子团以共价键的方式结合形成新的分子。
加成反应可分为电子亲和性和电子排斥性两种机理。
电子亲和性加成反应是指亲电试剂攻击双键或三键,形成中间离子,最后被亲核试剂攻击生成产物。
电子排斥性加成反应是指亲核试剂攻击双键或三键,生成中间离子,然后被亲电试剂攻击生成产物。
2. 消除反应。
消除反应是有机化学中另一种重要的反应类型,它是指有机分子中的两个邻近原子或原子团通过共价键的方式脱离分子,生成双键或三键。
消除反应可分为β-消除、α-消除和γ-消除等不同机理,其中最常见的是β-消除反应。
β-消除反应是指邻位原子或原子团与相邻的氢原子脱离,生成双键或三键。
3. 取代反应。
取代反应是有机化学中最常见的反应类型之一,它是指有机分子中的一个原子或原子团被另一个原子或原子团取代。
取代反应可分为亲核取代和亲电取代两种机理。
亲核取代是指亲核试剂攻击有机分子中的一个原子或原子团,将其取代生成新的产物。
亲电取代是指亲电试剂攻击有机分子中的一个原子或原子团,将其取代生成新的产物。
4. 加成-消除反应。
加成-消除反应是一种复合反应类型,它是指有机分子中的双键或三键发生加成反应生成中间产物,然后再发生消除反应生成最终产物。
加成-消除反应的机理比较复杂,通常需要通过实验数据和理论计算来揭示其反应过程和产物结构。
总的来说,有机化学反应机理的研究对于我们理解和掌握有机反应规律具有重要意义。
通过深入学习和掌握有机反应机理,我们可以更好地设计和优化有机合成路线,提高有机合成的效率和选择性,为新药物的研发和合成提供理论指导。

有机化学反应总结有机化学是一门研究有机化合物的结构、性质和合成方法的学科。
有机化学反应是有机化学中的核心内容,能够将一个有机化合物转化为另一个有机化合物,通过不同的反应路径,可以得到多种不同的产物。
在这篇文章中,我们将对常见的有机化学反应进行总结和探讨。
一、取代反应取代反应是有机化学中最基本的反应类型之一。
它是指一个原子、基团或官能团与另一个原子、基团或官能团发生替换的过程。
常见的取代反应有酯酸酯化反应、醇酸酯化反应、SN1和SN2取代反应等。
例如,酯酸酯化反应是一种以酸为催化剂的酯化反应。
在此反应中,醇和酸酐经过酸催化可以生成酯和水。
这种反应在有机合成中非常重要,常用于酯类的制备。
二、加成反应加成反应是指两个或多个分子发生直接结合形成一个新的分子。
这种反应通常涉及双键或三键的断裂,生成新的化学键。
常见的加成反应有烯烃加成反应、炔烃加成反应等。
例如,烯烃的加成反应是指一个或多个亲电试剂通过与烯烃的共轭体系发生反应,形成新的化学键。
这种反应是有机合成中的重要工具,可以合成多种有机化合物,如醇、醚、酮等。
三、消除反应消除反应是指一个分子中的两个官能团(常为两个邻接碳原子上的官能团)发生消除反应,生成一个新的分子和一个小分子。
常见的消除反应有脱水反应、脱氢反应等。
例如,脱水反应是指从一个有机化合物中去除一个水分子的反应。
这种反应常常利用酸、碱或热作为催化剂,可以合成醚、烯烃等化合物。
四、重排反应重排反应是指在化学反应中,有机化合物的官能团或它所连接的碳原子的连接方式发生改变,从而得到结构不同的产物。
重排反应可以通过原子间的改变或分子内的改组实现。
常见的重排反应有烷基迁移反应、脱羧反应等。
重排反应在有机化学中具有重要的意义,不仅可以提供快速合成目标产物的途径,还可以帮助研究人员预测和解释有机化合物的行为。
五、氧化还原反应氧化还原反应是指化学反应中电子的转移。
氧化是指物质失去电子,而还原是指物质获得电子。
有机反应类型及反应规律1.取代反应(1)取代反应指的是有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应。
(2)烃的卤代、芳香烃的硝化或磺化、卤代烃的水解、醇分子间的脱水反应、醇与氢卤酸的反应、酚的卤代、酯化反应、酯的水解和醇解以及蛋白质的水解等都属于取代反应。
(3)在有机合成中,利用卤代烷的取代反应,将卤原子转化为羟基、氨基等官能团,从而制得用途广泛的醇、胺等有机物。
卤代(1)概念:卤代通常是烃或烃的衍生物中的氢被卤素单质中的卤原子取代的反应。
(2)烃或烃的衍生物的卤代(芳香烃及其衍生物除外): ①条件:通常是光照;②特点:分步进行,产物复杂; 如甲烷的氯代反应:第一步:CH 4+Cl 2==CH 3Cl+HCl ;第二步:CH 3Cl+Cl 2==CH 2Cl 2+HCl ;第三步:CH 2Cl+Cl 2==CHCl 3+HCl ;第四步:CHCl 3+Cl 2==CCl 4+HCl ;(3)芳香烃及芳香烃的衍生物的卤代:①苯卤代条件:如苯与Br 2取代反应,须用液溴(与溴水不反应,只发生萃取的物理变化),且使用Fe 或FeBr 3作催化剂:;②取代苯的卤代:因取代基使苯上与取代及相邻或相对的氢原子变得较为活泼,故只需用溶液即可。
如:光光光光;③芳香烃的衍生物侧链上的卤代:与烃的卤代相似,光照即可。
芳香烃的硝化与磺化(1)硝化反应:;(2)磺化反应:;卤代烃的水解(1)概念:卤代烃分子中的卤原子可以被其他多种原子团(-OH、NH2等)取代,卤代烃遇碱的水溶液发生的反应即为水解反应;(2)条件:氢氧化钠水溶液(注意与卤代听的消去反应的条件区别);(3)实例:分布反应:CH3CH2Br+H2O CH3CH2OH+HBr;HBr+NaOH=NaBr+H2O;总反应:CH3CH2Br+NaOH CH3CH2OH+NaBr;醇分子间脱水成醚(以乙醇为例)(1)条件:浓硫酸作催化剂,140℃;(2)2CH3CH2OH C2H5—O—C2H5+H2O;醇与氢卤酸反应(1)条件:浓的氢溴酸,加热;(2)CH3CH2OH+HBr CH3CH2Br+H2O;酯化反应(1)概念:酸与醇作用生成酯和水的反应;(2)拓展:酚与无机含氧酸同样能发生酯化反应;(3)酯化反应规律:①一元醇与一元羧酸之间的酯化反应:CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O;②多元羧酸与一元醇之间的酯化反应:HOOC-COOH+2CH3CH2OH C2H5COO-COOC2H5+2H2O;③一元羧酸与多元醇之间的酯化反应:2CHCOOH+ +2H2O;④多元羧酸与多元醇之间的酯化反应:a. HOOCCOOCH2CH 2OH+H 2O ;b. +2H2O ;c n +n +(2n-1)H 2O ; ⑤羟基酸自身的酯化反应:a. +H 2O ;b. +H 2O ;c. +(n-1)H 2O 。
高中有机化学反应类型归纳总结★取代反应烷:CH4+Cl2→(光)CH3Cl+HCl苯:苯+Br2→(Fe)苯-Br+HBr(液溴)苯+HO-NO2→(浓H2SO4;△)苯-NO2+H2O(硝化反应)甲苯:苯-CH3+3HO-NO2→(浓H2SO4;△)三硝基甲苯(TNT)+3H2O苯-CH3+Cl2→(光)苯-CH2Cl+HCl醇:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑卤代烃:CH3CH2Br+NaOH→(△)CH3CH2OH+NaBr(水解反应) 另有酯化,硫化,水解等★加成反应烯:CH2=CH2+Br2→CH2BrCH2Br CH2=CH2+H2O→(催化剂;△)CH3CH2OHCH2=CH2+H2→(Ni)CH3CH3炔:CH≡CH+2Br2→CHBr2CHBr2苯:苯+3H2→(Ni)C6H6(环已烷)苯+3Cl2→C6H6Cl6(六六六)醛:CH3CHO+H2→(Ni;△)CH3CH2OH(加氢还原)另有加聚★消去反应卤代烃:CH3CH2Br+NaOH→(醇;△)CH2=CH2↑+NaBr+N2O醇:CH3CH2OH→(浓H2SO4;△)CH2=CH2↑+H2O (乙醇为170℃,其它醇不用记) ★水解反应(取代反应)卤代烃:CH3CH2Br+H2O→(NaOH)CH3CH2OH+HBr酯:CH3COOC2H5+H2O(可逆;稀H2SO4;△)CH3COOH+C2H5OH另有多糖二糖蛋白质的水解★氧化反应1 燃烧:CxHyOz+(x+y/4-z/2)O2→(点燃)xCO2+y/2H2O (有机物燃烧通式)2 催化反应醇:2CH3CH2OH+O2→(Cu;△)2CH3CHO+2H2OCH3CH2OH+CuO→(△)CH3CHO+H2O+Cu醛:2CH3CHO+O2→(催化剂;△)2CH3CHO烯:2CH2=CH2+O2→(催化剂)2CH3CHO烷:2CH3CH2CH2CH3+5O2→(催化剂)4CH3COOH+2H2O3 被酸性KMnO4氧化烯炔苯的同系物(与苯环相连的C上要有H)醇醛4 与新制Cu(OH)2反应醛:CH3CHO+2Cu(OH)2→(△)CH3COOH+Cu2O↓+2H2O5 银镜反应(1)甲醛甲醛过量时:HCHO+2[Ag(NH3)2]OH→(△)HCOONH4+2Ag↓+3NH3+H2O 银氨溶液过量:HCHO+4[Ag(NH3)2]OH→(△)(NH4)2CO3+4Ag↓+6NH3↑+2H2O (2)乙醛CH3CHO+2[Ag(nh3)2]OH→(△)CH3COONH4+2Ag↓+3NH3+H2O 另有HCOOR(甲酸盐甲酯某酯)葡萄糖麦芽糖果糖★还原反应1 加H2加成:醛:CH3CHO+H2→(Ni;△)CH3CH2OH另有烯炔等★特征反应1 显色反应酚+Fe3+→紫色淀粉+I2→蓝色蛋白质(含苯环)+浓HNO3→黄色2 生H2醇:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑酚:2苯-OH+2Na→2苯-ONa+H2↑酸:2CH3COOH+Zn→(CH3COO)2Zn+h2↑3 需水浴加热的反应(1) 苯→硝基苯(硝化反应):苯+HO-NO2→(浓H2SO4)苯-NO2+H2O(55℃~65℃)(2)银镜反应(3)乙酸乙酯水解(70℃~80℃)(4)纤维素水解(5)酚醛树脂的制备。
有机反应规则总结1 Arbuzov亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R'I >R'Br >R'Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚磷酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R'X 的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理一般认为是按 S N2 进行的分子内重排反应:反应实例2 Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例3 Baeyer----Villiger 反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定不高于100℃的条件下反应,均可用水浴加热,优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有:(1)、实验室制乙烯(170℃)(2)、蒸馏(3)、固体溶解度的测定(4)、乙酸乙酯的水解(70-80℃)(5)、中和热的测定(6)制硝基苯(50-60℃)〔说明〕:(1)凡需要准确控制温度者均需用温度计。
(2)注意温度计水银球的位置。
3.能与Na反应的有机物有:醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有:(1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物(2)含有羟基的化合物如醇和酚类物质(3)含有醛基的化合物(4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)6.能使溴水褪色的物质有:(1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成)(2)苯酚等酚类物质(取代)(3)含醛基物质(氧化)(4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应)(5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化)(6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。
)7.密度比水大且难溶于水的液体有机物有:溴乙烷、溴苯、硝基苯、四氯化碳等。
8、密度比水小且难溶于水的液体有机物有:烃、大多数酯、一氯烷烃。
密度比水小且易溶与水的: 含碳原子少的醇,醛,羧酸9.能发生水解反应的物质有卤代烃、酯(油脂)、二糖、多糖、蛋白质(肽)、盐。
10.不溶于水的有机物有:烃、卤代烃、酯、淀粉、纤维素11.常温下为气体的有机物有:分子中含有碳原子数小于或等于4的烃(新戊烷例外)、一氯甲烷、甲醛。
有机化学必备规律汇总A.有机合础成与推断基础知识网络:1.不饱和键数目的确定:①一分子有机物加成H2(或Br2)含有一个双键;②加成两个分子H2(或Br2)含有一个参键或两个双键;③加成三分子H2含有三个双键或一个苯环。
④一个双键相当于一个环。
2、符合一定碳氢比(物质的量比)的有机物:C:H=1:1的有乙炔、苯、苯乙烯、苯酚等。
C:H=1:2的有甲醛、乙酸、甲酸甲酯、葡萄糖、果糖、单烯烃。
3、有特殊性的有机物归纳:①含氢量最高的有机物是:CH4;②一定质量的有机物燃烧,消耗量最大的是:CH4;③完全燃烧时生成等物质的量的CO2和H2O的是:环烷烃、饱和一元醛、酸、酯(通式符号C n H2n O x的物质,X=0,1,2,……)④使FeCl3溶液显特殊颜色的是:酚类化合物;⑤能水解的是:酯、卤代烃、糖类(单糖除外)、肽类(包括蛋白质);⑥含有羟基的是:醇、酚、羧酸(能发生酯化反应,有些可与Na作用生成H2);⑦能与NaHCO3作用成CO2的是:羧酸类;⑧能与NaOH发生反应的是:羧酸和酚类。
4、重要的有机反应规律:①双键的加成和加聚:双键任意断裂其一,加上其它原子或原子团或断开键相互连成链。
②醇的消去反应:总是消去与羟基所在碳原子相邻的碳原子上的氢原子上,若没有相邻的碳原子(如CH3OH)或相邻的碳原子上没有氢原子【如(CH3)3CCH2OH】的醇不能发生反应。
③醇的催化反应:和羟基相连的碳原子上若有二个或三个氢原子,被氧化成醛;若有一个氢原子被氧化成酮;若没有氢原子,一般不会被氧化。
④酯的生成和水解及肽键的生成和水解:酯化反应规律:酸脱羟基(-COOH上的-OH)醇(-OH上的H)脱氢;酯水解反应与酯化反应恰好为逆反应;肽键的脱水缩合:酸脱羟基(-COOH上的-OH)氨基(-NH2上的H)脱氢;肽键水解与肽键的生成恰好为逆反应⑤有机物成环反应:a二元醇脱水,b羟基的分子内或分子间的酯化,c氨基的脱水。
有机化学反应条件总结
(分子间脱水)
苯硝化(水
二糖及多糖
(取代)
酯水解(彻
化,生成醛脱去与羟基相连接碳原子上的氢和羟基中的氢
反应,烷烃
苯环侧链卤
反应,苯环被取代
不饱和烃加
举例
苯酚的取代
醛的氧化反
烯烃炔烃与
苯酚与浓溴、;醇
有机化学官能团的引入总结
卤代烃水解
烷烃芳香烃
烯烃炔烃与
烯烃炔烃与
取
—OH +NaOH +H 2O
—ONa
有机化学规律性知识性总结
举例
2CH 3CH 2OH+2Na→2CH 3CH2ONa+H 2↑
、甲
甲酸盐、
HCHO + 4Ag(NH 3)2OH 4Ag↓+ (NH 4)2CO 3 + 6NH 3 +
2H 2O
注:甲醛(相当于两个醛基) (葡萄糖、
麦芽糖等)
CH 2OH-(CHOH)4- CHO+2Ag(NH 3)2OH
CH 2OH-(CHOH)4-COONH 4+2Ag↓+3NH 3↑+H 2O
OH
官能团转化示意图
有机合成
我们说有机合成就是通过有机反应构建目标分子的骨架,并引入或转化所需的官能团。
所以说有机合成的重点就是如何重新构建骨架和引入及转变官能团,在这个过程中逆合成分析法是一个非常实用和有效的方法,即从产物的特征(包括碳链结构,官能团类型,空间结构等)出发,去分析得到该产物的上一步物质的特征,然后依次类推,并和最初给出的反应物相结合,推出合成过程中的中间产物,最终解决有机合成题。
(1)官能团的引入: 1)引入羟基(-OH )
①醇羟基的引入:a.烯烃与水加成;b.醛(酮)与氢气加成;c.卤代烃碱性水解;d.酯的水解等。
②酚羟基的引入:酚钠盐过渡中通入CO2,
的碱性水解等。
③羧羟基的引入:醛氧化为酸(被新制Cu(OH)2悬浊液或银氨溶液氧化)、酯的水解等。
2)引入卤原子:a.烃与X 2取代;b.不饱和烃与HX 或X 2加成;c.醇与HX 取代等。
3)引入双键:a.某些醇或卤代烃的消去引入C=C ;b.醇的氧化引入C=0等。
(2)官能团的消除
1)通过加成消除不饱和键。
2)通过消去、氧化或酯化等消除羟基(-OH ) 3)通过加成或氧化等消除醛基(-CHO ) 4)通过取代或消去和消除卤素原子。
(3)官能团间的衍变
卤代烃
R —X
醇 R —OH 醛 R —CHO
羧酸 RCOOH
酯RCOOR ’
水解 水解 酯化
氧化 还原
氧化
酯化 水解
不饱和烃
加
成 消
去
消去
加成
根据合成需要(有时题目信息中会明示某些衍变途径),可进行有机物的官能团衍变,以使中间物向产物递进。
常见的有三种方式:
①利用官能团的衍生关系进行衍变,如伯醇[]
−→−O 醛[]
−→−O 羧酸;
②通过某种化学途径使一个官能团变为两个, 如
CH 3CH 2OH
O
H 2-−−→−消去CH 2=CH 22
Cl +−−→−加成Cl —CH 2—CH 2—Cl −−→
−水解HO —CH 2—CH 2—OH; (4)有机高分子的合成
从有机高分子的结构特点也可以找到解题线索,如根据题中给出的高分子化合物的结构特点,可以判断出合成该高分子化合物的单体特征,然后采用逆推法,从单体出发进一步向上推演,查找单体中相应官能团和碳链结构的来源途径,并和题中的其他已知因素结合理解和推演,最终可以顺利解题。
以丙烯为例,看官能团之间的转化:
上述转化中,包含了双键、卤代烃、醇、醛、羧酸、酯高分子化合物等形式的关系,领会这些关系,基本可以把常见的有机合成问题解决。