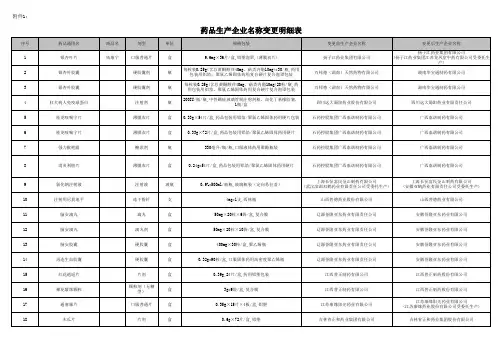
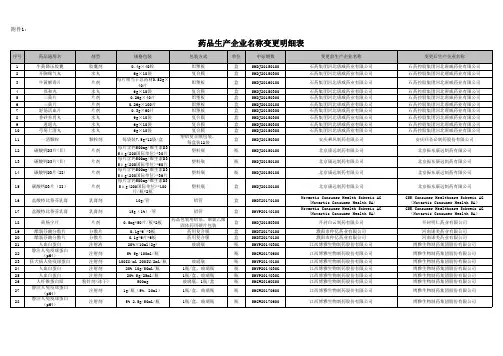
药品生产企业名称变更明细表
- 格式:pdf
- 大小:259.17 KB
- 文档页数:5


变更《药品生产许可证》一、行政许可的内容变更《药品生产许可证》登记事项和许可事项。
《药品生产许可证》登记事项为:企业名称、注册地址、法定代表人、企业类型。
《药品生产许可证》许可事项为:企业负责人、生产地址、生产范围。
二、行政许可依据(一)《中华人民共和国药品管理法实施条例》(二)《药品生产监督管理办法》(国家食品药品监督管理局令第14号)(三)《关于加强药品生产许可证管理的通知》(苏食药监安〔2004〕401号)三、申请范围持有《药品生产许可证》的药品生产企业申请变更《药品生产许可证》登记事项和许可事项。
四、申请材料申请人应提交《药品生产许可证》正副本,并按要求报送电子文档及以下相关材料,所有材料用A4纸制作,文字材料和表格用电脑打印,并按照下列顺序排列。
(一)变更企业名称的,应提交:1、企业申请报告、变更申请表;2、原《药品生产许可证》和《企业法人营业执照》正副本复印件;3、企业名称变更预核登记核准通知书;4、申报单位对申报资料的真实性作的保证声明。
(二)变更注册地址的,应提交:1、企业申请报告、变更申请表;2、原《药品生产许可证》和《企业法人营业执照》正副本复印件;3、登记事项变更后新核发的《企业法人营业执照》复印件;4、申报单位对申报资料的真实性作的保证声明。
(三)变更企业类型的,如果是有限责任公司变更的应提交:1、企业申请报告、变更申请表;2、原《药品生产许可证》和《企业法人营业执照》正副本复印件;3、登记事项变更后新核发的《企业法人营业执照》复印件;4、董事会决议和产权(股权)转让协议书;5、申报单位对申报资料的真实性作的保证声明。
如果是国有企业改制的应提交:1、企业申请报告、变更申请表;2、原《药品生产许可证》和《企业法人营业执照》正副本复印件;3、登记事项变更后新核发的《企业法人营业执照》复印件;4、当地政府或有关职能部门改制批复,国有资产评估报告及评估结果确认文件;5、董事会决议和产权(股权)转让协议书;6、申报单位对申报资料的真实性作的保证声明。

《药品生产许可证》变更企业名称、法定代表人企业负责人、注册地址、质量负责人、日常监管人程序(2016年修订)《药品生产许可证》变更企业名称、法定代表人、企业负责人、注册地址、质量负责人、日常监管人程序(2016年修订)事项名称:《药品生产许可证》变更企业名称、法定代表人、企业负责人、注册地址、企业类型法定实施主体:江西省食品药品监督管理局设定依据:1、《药品生产监督管理办法》(国家食品药品监督管理局令第14号第十三条至二十三条)收费标准:不收费总时限:自受理之日起10个工作日(不含补正、送达时间)。
1、受理5个工作日(不计入审批时限);2、审核4个工作日;3、复审2个工作日;4、审定2个工作日;5、制作行政许可决定2个工作日;6、送达3个工作日(不计入审批时限)。
申请条件:本省行政区域内药品生产企业《药品生产许可证》变更企业名称、法定代表人、企业负责人、注册地址、企业类型的,由省食品药品监督局受理。
办理材料:申报材料要求申请人需提交以下申请材料:1、申请变更《药品生产许可证》的报告:要用正式文件,说明变更原因和变更事项,特别要说明是否发生了股权转让或改制,要有企业法人代表签字并盖有单位公章;2、《药品生产许可证》申请表(变更一,见附件),企业所在地药品监管部门签署意见;3、工商行政管理部门出具的有关事项变更的预先核准通知书,营业执照变更前正副本复印件、营业执照变更后正副本复印件等证明材料;4、企业主管部门同意有关事项变更的批件或其他有关证明材料(董事会决议或股东会决议);5、变更所涉及人员的任免文件及其他有关证明材料(董事会决议或股东会决议);6、拟任人员无《药品管理法》第七十六条规定的情形的自我保证声明;7、拟任人员的个人简历(简历至少包括任职时间、从事药品生产管理工作经历等)及有关复印件(职称证书、身份证、毕业证);8、新、旧企业章程;9、上一个任职企业的离职证明性材料;10、申请人对其申请材料全部内容真实性保证的自我声明(该声明在省局办事指南处下载);11、有关变更事项如果不是企业法人来办理,则要出具由法人签字并加盖企业公章的《授权委托书》及被授权人身份证复印件;12、《药品生产许可证》正、副本复印件.13、申报资料报省局一式一份,报所在地市局和日常监管机构各一份。

药品零售(连锁)企业变更企业法定代表人、企业负责人、质量负责人审批(十)一、法定依据:(一)《中华人民共和国药品管理法实施条例》(二)《药品经营许可证管理办法》二、申请条件:申请人在原许可事项发生变更30日前持四川省绵阳食品药品监督管理局发出的有效期内的《药品经营许可证》提出变更申请。
三、申请人应提交的资料目录:1、四川省绵阳市药品零售(连锁)企业变更申请表(附表十);2、《药品经营许可证》正、副本原件;3、许可证申报系统导出文件光盘或软盘(扩展名xml)。
4、企业、企业法定代表人或企业负责人、质量管理负责人无《药品管理法》第76条、第83条规定的情形的书面申明。
5、企业所在地食品药品监督管理部门提供的没有因违法经营已被食品药品监督管理部门立案调查,尚未结案的;或已经作出行政处罚决定,尚未履行处罚的的有关证明。
企业法定代表人、企业负责人、质量管理负责人变更的,提交变更法定代表人或企业负责人、质量负责人的学历、执业资格或职称证明复印件(交验原件)和个人简历;6、申报材料真实性申明。
四、办理程序:1、申请人备齐资料,交绵阳食品药品监督管理局政务服务处审查。
2、对资料不齐的,填写《行政许可补正材料通知书》。
3、填写《行政许可受理通知书》或《行政许可不予受理决定书》。
4、政务服务处在资料受理2个工作日作出是否准予行政许可的决定,并打印送达。
五、法定期限:15个工作日,承诺期限2个工作日。
六、收费标准:1、收费依据:《关于药品生产(经营)企业许可证收费标准的函》国家物价局、财政局价费字[1992]314号。
2、收费标准:10元。
七、是否年审:不年检(审)。
八、咨询服务:绵阳市行政服务中心绵阳食品药品监督管理局政务服务处地址:富乐路新益大厦东一楼。
电话:2316835网址:/附表十四川省绵阳市药品零售(连锁)企业变更申请表企业名称:隶属部门(签章):企业法定代表人:企业负责人:准予行政许可决定书绵食药许字〔〕第号受理通知书编号:联系人:联系电话:通讯地址:邮编:申请日期:年月日四川省绵阳食品药品监督管理局制企业基本情况表变更事项表注:“原事项的内容”栏中不涉及“变更事项的内容”也必须完整填写。

四川省食品药品监督管理局《药品生产许可证》核发(变更)办事指南一、法定依据《中华人民共和国药品管理法实施条例》(2002年8月4日国务院令第360号公布,自2002年9月15日起施行)“第四条药品生产企业变更《药品生产许可证》许可事项的,应当在许可事项发生变更30日前,向原发证机关申请《药品生产许可证》变更登记;未经批准,不得变更许可事项。
原发证机关应当自收到申请之日起15个工作日内作出决定。
申请人凭变更后的《药品生产许可证》到工商行政管理部门依法办理变更登记手续。
”二、申请条件持有《药品生产许可证》的企业,许可事项依法发生变更。
《药品生产监督管理办法》(国家食品药品监督管理局第14号令)第14条规定:由(食品)药品监督管理部门核准的许可事项为:企业负责人、生产范围、生产地址。
三、申报资料申请变更《药品生产许可证》许可事项须提交以下资料各一份:1、企业申请变更《药品生产许可证》的书面报告、变更申请表;2、《药品生产许可证》正、副本原件、复印件各1套,营业执照复印件;3、《药品生产许可证登记表》并附电子版申请文件;(登陆国家食品药品监督管理局网站/下载“药品生产许可证管理系统”,按要求填报)(点击下载);4、不同变更项目需报送的材料5、企业法人出具的确保申报资料内容真实有效的保证函;6、凡申请企业申报材料时,申请人不是法定代表人或负责人本人,应当提交《授权委托书》1份;7、组织机构代码证复印件。
四、办理程序《药品生产许可证》应载明许可证编号、企业名称、法定代表人、企业负责人、企业类型、注册地址、生产地址、生产范围、发证机关、发证日期、有效期限等项目。
其中由食品药品监督管理部门核准的许可事项为:企业负责人、生产范围、生产地址、有效期限。
1、企业在许可事项发生变更30日前向省政府政务服务中心省食品药品监督管理局窗口提出申请;2、省食品药品监督管理局受理并审核(变更生产地址及生产范围须安排现场检查);3、审核合格的同意变更,不合格的由省食品药品监督管理局下达不予许可的书面决定,并说明理由,同时告知申请人享有依法申请行政复议或提起行政诉讼的权利;4、批准变更的,企业向工商行政管理部门办理企业注册登记的变更手续。

药品信息变更操作流程药品生产企业(进口药品为国内总经销商或总代理商)是申报药品信息变更的主体。
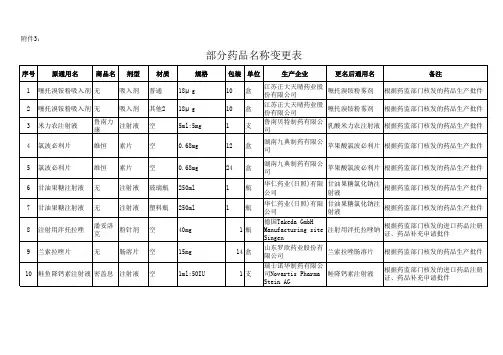
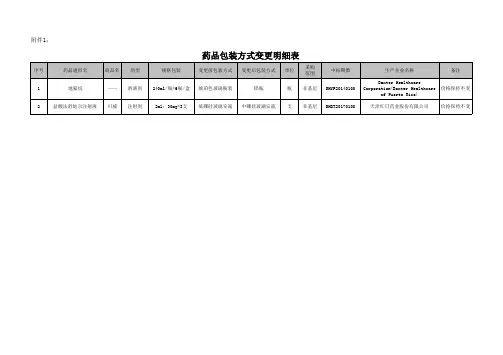
药品的各项信息变更,包括通用名、商品名、规格包装、包装方式、生产企业名称、委托生产、进口药品转国内分装、分装药品转国产、进口药品转国产、信息更正等。
药品信息变更作为日常管理工作开展,企业申报并通过审核后执行变更结果。
(中标药品下发红头文件,非中标、儿童用药、毒麻精放等药品不下发红头文件,企业可在“基础信息登记系统”查询变更结果)。
具体操作流程如下:企业在“上海市医药采购基础信息登记系统”中按要求如实申报相关信息。
一.企业名称申请变更(包括全部品规及部分品规)(正在申请挂网或者未完成的标期内药品请在挂网及投标公示执行后在上海市医药采购基础信息登记系统申请变更。
)(1)企业名称变更需要准备的材料:①企业(或代理)申请公文(格式企业自拟);②企业(或代理)法人授权书及被授权人身份证复印件;③药品生产许可证(进口药品注册证);④GMP证书;⑤补充申请批件(企业更名相关);⑥企业(或代理)营业执照;⑦进口药品国内委托代理协议(合同)。
以上材料都需盖上企业公章。
需要准备的材料:①企业(或代理)申请公文(格式企业自拟);②企业(或代理)法人授权书及被授权人身份证复印件;③药品生产许可证(进口药品注册证);④GMP证书;⑤补充申请批件(企业更名相关);⑥企业(或代理)营业执照;⑦进口药品国内委托代理协议(合同)。
⑧外观照片、药品说明书,需要填写本位码、批准文号、医院供应价;⑨生产注册批件(含补充申请);⑩质量标准相关材料及省、市药品检验报告。
以上材料都需盖上企业公章。
需要准备的材料:①企业(或代理)申请公文(格式企业自拟);②企业(或代理)法人授权书及被授权人身份证复印件;③药品生产许可证(进口药品注册证);④GMP证书;⑤补充申请批件(企业更名相关);⑥企业(或代理)营业执照;⑦进口药品国内委托代理协议(合同)。
⑧外观照片、药品说明书,需要填写本位码、批准文号、医院供应价;⑨生产注册批件(含补充申请);⑩质量标准相关材料及省、市药品检验报告。