生物化学氨基酸代谢知识点总结电子教案
- 格式:doc
- 大小:1.02 MB
- 文档页数:17


第七章氨基酸代谢【目的和要求】1、掌握体内氨基酸的来源与去路;氨的来源与去路;掌握氨基酸脱氨基方式及基本过程;2、掌握一碳单位的定义、种类、载体和生物学意义。
3、熟悉必需氨基酸的种类和蛋白质的营养价值与临床应用。
4、了解个别氨基酸代谢,了解氨基酸代谢中某个酶缺陷或活性低时所导致的氨基酸代谢病。
【本章重难点】1氨基酸的来源和去路2.氨的来源和去路3.鸟氨酸循环4.联合脱氨基作用学习内容第一节蛋白质的营养作用第二节氨基酸的一般代谢第三节个别氨基酸的代谢第一节蛋白质的营养作用一氨基酸的来源和去路㈠氨基酸的来源氨基酸是蛋白质的基本组成单位。
参加体内代谢的氨基酸,除经食物消化吸收来以外,还来自组织蛋白质分解和自身合成。
这些氨基酸混为一体,分布在细胞内液和细胞外液,构成氨基酸代谢库。
体内的氨基酸的来源和去路保持动态平衡,它有三个来源:⒈食物蛋白质经消化吸收进入体内的氨基酸。
组成蛋白质的氨基酸有二十种,其中有8种是人体需要而不能自身合成,必需由食物供给的,称为必需氨基酸。
它们为苏氨酸、色氨酸、缬氨酸、赖氨酸、亮氨酸、异亮氨酸,苯丙氨酸及蛋氨酸。
其余十二种氨基酸在体内可以合成或依赖必需氨基酸可以合成,称为非必需氨基酸。
食物蛋白质营养价值的高低取决于食物蛋白质所含必需氨基酸的种类、数量和比例。
种类齐全、数量大、比例与人体需要越接近,其营养价值越高。
为提高蛋白质的营养价值,把几种营养价值较低的蛋白质混合食用,必需氨基酸相互补充,从而提高氨基酸的利用率,称为蛋白质营养的互补作用。
蛋白质具有高度种属特异性,不能直接输入人体,否则会产生过敏现象。
进入机体前必先在肠道水解成氨基酸,然后吸收入血。
蛋白质的消化作用主要在小肠中进行,由内肽酶(胰蛋白酶、糜蛋白酶及弹性蛋白酶)和外肽酶(羧基肽酶、氨基肽酶)协同作用,水解成氨基酸,水解生成的二肽也可被吸收。
未被吸收的氨基酸及蛋白质在肠道细菌的作用下,进行分解代谢,其代谢过程可产生许多对人体有害的物质(吲哚、酚类、胺类和氨),此过程称为蛋白质的腐败作用。


第八章氨基酸代谢教学要求(一)掌握内容1. 氨基酸脱氨基作用方式:转氨基作用、氧化脱氨基作用、联合脱氨基作用。
2. 氨的来源和去路;氨的转运过程;丙氨酸-葡萄糖循环。
3. 尿素生成鸟氨酸循环的过程、部位及调节。
(二)熟悉内容1. 氮平衡及必需氨基酸的概念、蛋白质的生理功能。
2. 蛋白质消化中各种酶的作用及γ-谷氨酰基循环。
3. 氨基酸脱羧基作用及生成的生理活性物质。
4. 一碳单位的概念、载体及生理功能。
5. 熟悉活性甲基的形式。
(三)了解内容1. 蛋白质的腐败作用及腐败产物。
2. 甲硫氨酸循环和肌酸合成。
3. 苯丙氨酸和酪氨酸生成的生理活性物质。
教学内容(一)蛋白质的营养作用1. 蛋白质的生理功能2. 蛋白质的需要量和营养价值(二)蛋白质的消化、吸收与腐败1. 蛋白质的消化(1)胃中的消化;(2)小肠内的消化。
2. 氨基酸的吸收(1)主要部位;(2)吸收形式;(3)吸收机制。
3. 白质的腐败作用(1)胺类的生成;(2)氨的生成;(3)其他有害物质的生成。
(三)氨基酸的一般代谢1. 概述(1)细胞蛋白质降解的两条途径;(2)氨基酸代谢库(metabolic pool)。
2. 氨基酸的脱氨基作用(1)转氨基作用;(2)氧化脱氨基作用;(3)联合脱氨基作用。
(4)非氧化脱氨基作用。
3. α-酮酸的代谢(1)经氨基化生成非必需氨基酸;(2)经三羧酸循环氧化供能;(3)转变为糖及脂类。
(四)氨的代谢1. 体内氨的来源(1)氨基酸及胺分解产氨;(2)肠道吸收的氨;(3)肾小管分泌氨。
2. 氨的去路(1)合成尿素排出(主);(2)与谷氨酸合成谷氨酰胺;(3)合成非必需氨基酸及含氮物;(4)经肾脏以铵盐形式排出。
3. 氨的转运(1)丙氨酸-葡萄糖循环;(2)谷氨酰胺(Gln)的运氨作用。
4. 尿素的生成(1)尿素合成的主要器官;(2)尿素合成的鸟氨酸循环;(3)鸟氨酸循环的步骤;(4)尿素合成的调节。
5. 高血氨症和氨中毒(五)个别氨基酸的代谢1. 氨基酸的脱羧基作用(1)γ-氨基丁酸;(2)组胺;(3)牛磺酸;(4)5-羟色胺;(5)多胺。

氨基酸代谢一、教学大纲基本要求蛋白质的消化、吸收,氨基酸代谢库,必需氨基酸,氮平衡,氨基酸代谢概论,氨基酸的脱氨基、转氨基、联合脱氨基作用;蛋白质降解,尿素循环,氨基酸合成代谢;氨基酸的脱羧基作用,氨基酸的碳链代谢,氨的排出、转运。
二、本章知识要点(一)氨基酸代谢概述蛋白质作为动物体的主要组成成分,总是在不断地进行着新陈代谢。
而蛋白质的基本组成单位是氨基酸,所以氨基酸代谢是蛋白质代谢的重要内容。
1.蛋白质的消化、吸收(1)蛋白质的消化动物的唾液中虽有少量唾液蛋白质酶能分解蛋白质,但在整个消化过程中,其作用不大。
蛋白质食物主要是在胃和小肠中进行消化的。
胃粘膜主细胞可分泌胃蛋白酶原,胰液能提供胰蛋白酶原、糜蛋白酶原、弹性蛋白酶原和羧基肽酶原,这些酶原激活后可转变成有活性的酶,在这些酶以及动物体所含的氨肽酶、羧肽酶和二肽酶等共同作用下,来完成日粮中蛋白质的消化过程。
(2)蛋白质的吸收在正常情况下,只有氨基酸及少量二肽、三肽能被动物体吸收进入血液。
这种吸收主要在小肠粘膜细胞上进行,肾小管细胞和肌肉细胞也能吸收,这是一个耗能、需氧的主动运输过程。
关于氨基酸吸收的机理,目前仍未完全解决。
A.Meister在1968-1969年,从肾脏研究中,提出关于氨基酸吸收的“γ-谷氨酰基循环”假说,具有一定理论意义。
他认为氨基酸吸收或向各组织、细胞内转移是通过谷胱甘肽起作用,这个过程由六步连续的酶促反应完成。
2.氨基酸的代谢库动物体吸收进入血液的氨基酸与体内游离的氨基酸构成了氨基酸代谢库。
在正常情况下,氨基酸代谢库中的氨基酸维持在一个动态平衡中。
一方面,氨基酸被消耗,或用来合成蛋白质,或合成其它含氮物质,或氧化分解提供能量;另一方面,可由体外吸收、体内合成或体内蛋白质分解所产生的氨基酸补充。
3.必需氨基酸必需AA是指机动物体内不能合成或合成量不足,必须由日粮提供的一类氨基酸,构成天然蛋白质的20种氨基酸中有10种氨基酸是多数动物的必需氨基酸:3种碱性AA(赖AA、精AA、组AA),3种支链AA(亮AA、异亮AA、缬AA),2种芳香AA(苯丙AA、色AA),1种含硫AA(甲硫AA),1种羟基AA(苏AA)。


生化-氨基酸代谢知识点整理●氨基酸降解●对于大多数氨基酸而言,其降解第一步反应通常是依赖于PLP转氨基●多数氨基酸是通过脱掉氨基形成α-酮酸进行降解的,随后脱掉的氨基可以重新参与新氨基酸的合成、形成酰胺将氨基储存起来、形成铵盐、进入尿素循环;a-酮酸则可以参与脂肪的合成经过葡萄糖异生合成葡萄糖或者进入TCA循环彻底氧化成二氧化碳和水。
●氨基酸降解,是生物体的一种主动行为,是生物体利用氨基酸的又一种方式。
●过程●脱氨作用●氧化脱氨基作用●是以谷氨酸脱氢酶(该酶可用NAD+或者NADP+作为辅因子,该酶催化的反应能够产生NH4+,该酶催化谷氨酸转化为a-酮戊二酸)为主的脱氨方式●谷氨酸脱氢酶广泛存在于不同生物体中的各种细胞和组织中,因此氧化脱氨以及联合脱氨是氨基酸降解的主要方式●转氨基作用●由转氨酶(辅酶磷酸吡哆醛)催化●联合脱氨作用●动物体中,联合脱氨作用(以嘌呤核苷酸循环为核心)是氨基酸降解的主要脱氨方式●联合脱氨是转氨作用、氧化脱氨的结合方式,即在转氨酶的作用下,多数氨基酸将其氨基转移给α-酮戊二酸,产生谷氨酸与相应的酮酸,谷氨酸在谷氨酸脱氢酶的催化下发生氧化脱氨基作用产生α-酮戊二酸和氨离子,氨离子进入尿素循环。
●嘌呤核苷酸循环是指次黄嘌呤核苷酸(IMP)与天冬氨酸反应产生腺苷酰琥珀酸,后者被腺苷酰琥珀酸裂合酶催化产生腺嘌呤核苷酸(AMP)和延胡索酸,而后AMP水解脱氨,形成IMP,IMP继续参与上述反应的过程。
●非氧化脱氨基作用●脱酰胺基作用●脱羧反应●直接脱羧基作用●羟化脱羧基作用●降解产物的去向●氨的代谢转变●重新合成氨基酸●生成谷氨酰胺●生成铵盐●通过鸟氨酸循环生成尿素●鸟氨酸循环(尿素循环)●部位:部分发生在线粒体中,部分发生在细胞质中●参与尿素循环的酶有氨甲酰磷酸合成酶I、鸟氨酸转氨甲酰酶、精氨基琥珀酸合成酶、精氨基琥珀酸裂合酶(也叫精氨琥珀酸酶)和精氨酸酶,生成的脲中1个氮原子来自谷氨酸氧化脱掉的氨,1个氮原子来自天冬氨酸的氨基,碳骨架来自氨甲酰磷酸。


第九章氨基酸代谢第一节:蛋白质的生理功能和营养代谢蛋白质重要作用1.维持细胞、组织的生长、更新和修补2.参与多种重要的生理活动(免疫,酶,运动,凝血,转运)3.氧化供能氮平衡1.氮总平衡:摄入氮= 排出氮(正常成人)氮正平衡:摄入氮> 排出氮(儿童、孕妇等)氮负平衡:摄入氮< 排出氮(饥饿、消耗性疾病患者)2.意义:反映体内蛋白质代谢的慨况。
蛋白质营养价值1.蛋白质的营养价值取决于必需氨基酸的数量、种类、量质比2.必需氨基酸-----甲来写一本亮色书、假设梁借一本书来3.蛋白质的互补作用,指营养价值较低的蛋白质混合食用,其必需氨基酸可以互相补充而提高营养价值。
第二节:蛋白质的消化、吸收与腐败外源性蛋白消化1.胃:壁细胞分泌的胃蛋白酶原被盐酸激活,水解蛋白为多肽和氨基酸,主要水解芳香族氨基酸2.小肠:胰液分泌的内、外肽酶原被肠激酶激活,水解蛋白为小肽和氨基酸;生成的寡肽继续在小肠细胞内由寡肽酶水解成氨基酸氨基酸和寡肽的主动吸收1.吸收部位:小肠,吸收作用在小肠近端较强2.吸收机制:耗能的主动吸收过程○1通过转运蛋白(氨基酸+小肽):载体蛋白与氨基酸、Na+组成三联体,由ATP供能将氨基酸、Na+转入细胞内,Na+再由钠泵排出细胞。
○2通过r-谷氨酰基循环(氨基酸):关键酶----r--谷氨酰基转移酶,具体过程参P199图大肠下段的腐败作用1.产生胺:肠道细菌脱羧基作用生成胺,其中假神经递质:酪胺和苯乙胺未能及时在肝转化,入脑羟基化成β-羟酪胺,苯乙醇胺,其结构类似儿茶酚胺,它们可取代儿茶酚胺与脑细胞结合,但不能传递神经冲动,使大脑发生异常抑制。
2.产生氨:3.产生其他物质:有害(多),如胺、氨、苯酚、吲哚;可利用物质(少),如脂肪酸、维生素第三节:氨基酸的一般代谢体内氨基酸分解1.蛋白质降解速率---半衰期2.真核细胞内蛋白降解两大途径:○1溶酶体内ATP非依赖途径+○2蛋白酶体内ATP依赖途径(泛素化过程参课本P201):①溶酶体内ATP非依赖途径•不依赖ATP•利用溶酶体内组织蛋白酶(cathepsin)•降解外源性蛋白、膜蛋白和长寿命的细胞内蛋白○2蛋白酶体内ATP依赖途径(依赖泛素的降解过程)•依赖ATP•降解异常蛋白和短寿命蛋白泛素介导的蛋白质降解过程.E1:泛素活化酶,E2:泛素结合酶,E3:泛素蛋白连接酶氨基酸代谢库1.代谢“三进四出”:进---食物消化吸收,组织蛋白分解,非必需氨基酸转化出---脱氨基作用,脱羧基作用,代谢转变,组织蛋白合成氨基酸分解第一步:脱氨基脱氨基方式: 1.转氨基作用2.氧化脱氨基3.联合脱氨基转氨基和氧化脱氨基偶联转氨基和嘌呤核苷酸循环偶联转氨基作用:1. 定义在转氨酶(transaminase)的作用下,某一氨基酸去掉α-氨基生成相应的α-酮酸,而另一种α-酮酸得到此氨基生成相应的氨基酸的过程。
(一)维持组织的生长、更新和修复蛋白质是组织、细胞的重要结构物质,参与组织、细胞的组成。
膳食中必须提供足够质和量的蛋白质,才能维持组织、细胞的生长、更新和修复。
(二)参与多种重要的生理功能人体内有多种功能的蛋白质、多肽,执行多种特殊生理功能,如催化功能(如酶)、调节功能(如激素)、运输功能(如血红蛋白、脂蛋白)、储存功能(如肌红蛋白、铁蛋白)、保护功能(如抗体、补体、凝血酶原)、维持体液胶体渗透压(如清蛋白)等。
(三)氧化供能体内蛋白质、多肽分解成氨基酸后,经脱氨基作用生成的α酮酸可直接或间接参加三羧酸循环氧化分解。
每克蛋白质在体内氧化分解产生17.19kJ(4.1kcal)能量,是体内能量来源之一。
一般来说,成人每日约有18%的能量来自蛋白质。
因为蛋白质的这种功能可由糖及脂肪代替,所以供能是蛋白质的次要生理功能。
(四)转变为糖类和脂肪。
二、氮平衡蛋白质的含氮量平均约16%,食物中的含氮物质绝大多数是蛋白质,因此机体内蛋白质代谢的概况可根据氮平衡实验来确定。
即测定尿与粪中的含氮量(排出氮)及摄入食物的含氮量(摄入氮)可以反映人体蛋白质的代谢概况。
氮平衡有三种情况(1)氮总平衡:摄入氮=排出氮,反映正常成人的蛋白质代谢情况,即氮的“收支”平衡。
(2)氮正平衡:摄入氮>排出氮,部分摄入的氮用于合成体内蛋白质。
儿童、孕妇及恢复期病人属于此种情况。
(3)氮负平衡:摄入氮<排出氮。
例如饥饿或消耗性疾病患者。
三、蛋白质的营养价值人体内有8种氨基酸不能合成,即:缬氨酸、亮氨酸、异亮氨酸、苏氨酸、赖氨酸、色氨酸、苯丙氨酸和蛋氨酸,必须由食物供给,称营养必需氨基酸,含有必需氨基酸种类多和数量足的蛋白质营养价值高,反之营养价值低。
第二节蛋白质的消化、吸收与腐败一、蛋白质的消化与吸收(自学)二、蛋白质的腐败作用肠道细菌对未被消化的蛋白质和未被吸收的氨基酸所起的作用称为蛋白质的腐败作用。
因此,蛋白质的腐败作用是细菌的代谢过程,以无氧分解为主。
第九章氨基酸代谢第一节:蛋白质的生理功能和营养代谢蛋白质重要作用1.维持细胞、组织的生长、更新和修补2.参与多种重要的生理活动(免疫,酶,运动,凝血,转运)3.氧化供能氮平衡1.氮总平衡:摄入氮= 排出氮(正常成人)氮正平衡:摄入氮> 排出氮(儿童、孕妇等)氮负平衡:摄入氮< 排出氮(饥饿、消耗性疾病患者)2.意义:反映体内蛋白质代谢的慨况。
蛋白质营养价值1.蛋白质的营养价值取决于必需氨基酸的数量、种类、量质比2.必需氨基酸-----甲来写一本亮色书、假设梁借一本书来3.蛋白质的互补作用,指营养价值较低的蛋白质混合食用,其必需氨基酸可以互相补充而提高营养价值。
第二节:蛋白质的消化、吸收与腐败外源性蛋白消化1.胃:壁细胞分泌的胃蛋白酶原被盐酸激活,水解蛋白为多肽和氨基酸,主要水解芳香族氨基酸2.小肠:胰液分泌的内、外肽酶原被肠激酶激活,水解蛋白为小肽和氨基酸;生成的寡肽继续在小肠细胞内由寡肽酶水解成氨基酸氨基酸和寡肽的主动吸收1.吸收部位:小肠,吸收作用在小肠近端较强2.吸收机制:耗能的主动吸收过程○1通过转运蛋白(氨基酸+小肽):载体蛋白与氨基酸、Na+组成三联体,由ATP供能将氨基酸、Na+转入细胞内,Na+再由钠泵排出细胞。
○2通过r-谷氨酰基循环(氨基酸):关键酶----r--谷氨酰基转移酶,具体过程参P199图大肠下段的腐败作用1.产生胺:肠道细菌脱羧基作用生成胺,其中假神经递质:酪胺和苯乙胺未能及时在肝转化,入脑羟基化成β-羟酪胺,苯乙醇胺,其结构类似儿茶酚胺,它们可取代儿茶酚胺与脑细胞结合,但不能传递神经冲动,使大脑发生异常抑制。
2.产生氨:3.产生其他物质:有害(多),如胺、氨、苯酚、吲哚;可利用物质(少),如脂肪酸、维生素第三节:氨基酸的一般代谢体内氨基酸分解1.蛋白质降解速率---半衰期2.真核细胞内蛋白降解两大途径:○1溶酶体内ATP非依赖途径+○2蛋白酶体内ATP依赖途径(泛素化过程参课本P201):①溶酶体内ATP非依赖途径•不依赖ATP•利用溶酶体内组织蛋白酶(cathepsin)•降解外源性蛋白、膜蛋白和长寿命的细胞内蛋白○2蛋白酶体内ATP依赖途径(依赖泛素的降解过程)•依赖ATP•降解异常蛋白和短寿命蛋白泛素介导的蛋白质降解过程.E1:泛素活化酶,E2:泛素结合酶,E3:泛素蛋白连接酶氨基酸代谢库1.代谢“三进四出”:进---食物消化吸收,组织蛋白分解,非必需氨基酸转化出---脱氨基作用,脱羧基作用,代谢转变,组织蛋白合成氨基酸分解第一步:脱氨基脱氨基方式: 1.转氨基作用2.氧化脱氨基3.联合脱氨基转氨基和氧化脱氨基偶联转氨基和嘌呤核苷酸循环偶联转氨基作用:1. 定义在转氨酶(transaminase)的作用下,某一氨基酸去掉α-氨基生成相应的α-酮酸,而另一种α-酮酸得到此氨基生成相应的氨基酸的过程。
2.反应式:大多数氨基酸可参与转氨基作用,但赖氨酸、脯氨酸、羟脯氨酸除外。
3.转氨酶组成和分布:谷丙转氨酶(或称丙氨酸转氨酶,ALT,GPT),主要分布在肝;谷草转氨酶(或称天冬氨酸转氨酶,AST,GOT),主要分布在心脏. 血清转氨酶活性,临床上可作为疾病诊断和预后的指标之一4.作用机制: 转氨酶的辅酶是磷酸吡哆醛5. 转氨基作用的生理意义: 转氨基作用不仅是体内多数氨基酸脱氨基的重要方式,也是机体合成非必需氨基酸的重要途径。
通过此种方式并未产生游离的氨.氧化脱氨基(L-谷氨酸氧化脱氨基作用):不需氧的L-谷氨酸脱氢酶催化,主要分布在肝,脑,肾联合脱氨基:两种脱氨基方式的联合作用,使氨基酸脱下α-氨基生成α-酮酸的过程。
○1转氨基和氧化脱氨基偶联(脱氨基,合成非必需氨基酸主要方式,存在于肝,肾)○2转氨基和嘌呤核苷酸循环偶联(存在于肌肉组织)氨基酸分解第二步:a-酮戊二酸转化或分解①经氨基化生成非必需氨基酸②转变成糖及脂类(记少不记多:生酮要来亮盏灯,生糖生酮落一本色书)甘氨酸、丝氨酸、缬氨酸、组氨酸、精氨酸、羟脯氨酸、丙氨酸、谷氨酸、谷氨酰胺、蛋氨酸、天冬氨酸、天冬酰胺、脯氨酸、半胱氨酸类别氨基酸生糖氨基酸生酮氨基酸亮氨酸、赖氨酸生糖兼生酮氨基酸异亮氨酸、苯丙氨酸、酪氨酸、苏氨酸、色氨酸氨基酸生糖及生酮性质的分类③ 氧化供能:α-酮酸在体内可通过TAC 和氧化磷酸化彻底氧化为H 2O 和CO 2,同时生成ATP氨基酸、糖及脂肪代谢的联系第四节:氨的代谢血氨性质体内的氨主要在肝合成尿素(urea)而解毒。
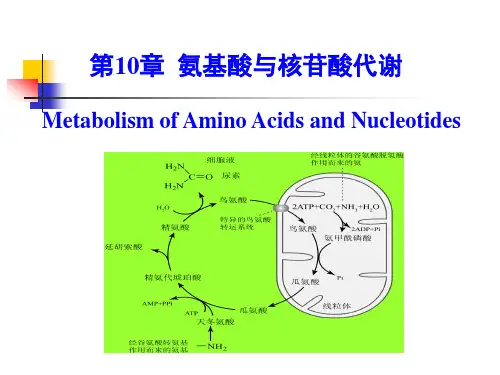
正常人体生理血氨浓度47-65μmol/L血氨的“三来四去”来源:①氨基酸脱氨基作用产生的氨是血氨主要来源, 胺类的分解也可以产生氨②肠道吸收的氨○3肾小管上皮细胞分泌的氨主要来自谷氨酰胺去路:①在肝内合成尿素,主要的去路②合成非必需氨基酸及其它含氮化合物③合成谷氨酰胺④肾小管泌氨:肾小管上皮细胞分泌的NH3在酸性条件下生成NH4+,随尿排出氨的转运1.转运形式:丙氨酸、谷氨酰胺骨骼肌丙酮酸-葡萄糖循环肝生成尿素丙氨酸-葡萄糖循环谷氨酰胺的运氨作用骨骼肌,脑谷氨酰胺合成肝或肾谷氨酰胺酶水解谷氨酸+氨氨基酸代谢中几大重要循环:1.r-谷氨酰基循环(见前文书P199)2.丙酮酸-葡萄糖循环(P207)3.尿素生成鸟氨酸循环(P211)4.甲硫氨酸循环(P215)尿素合成1.关键酶:精氨酸代琥珀酸合成酶2.定位:肝,胞液+线粒体3.原料:2 分子氨,一个来自于游离氨,另一个来自天冬氨酸4.耗能:3 个ATP,4 个高能磷酸键(其中一个ATP生成AMP)5.反应结果:鸟氨酸催化氨生成二氧化碳和尿素6.主要步骤:○1CO2 + NH3 + H2O + 2ATP缩合生成氨基甲酰磷酸○2氨基甲酰磷酸与鸟氨酸反生成瓜氨酸○3瓜氨酸与天冬氨酸反应生成精氨酸代琥珀酸○4精氨酸代琥珀酸裂解生成精氨酸与延胡索酸○5精氨酸水解释放尿素并再生成鸟氨酸6.合成调节:高蛋白质膳食促进尿素合成AGA激活CPS-I启动尿素合成精氨酸代琥珀酸合成酶活性促进尿素合成7.合成障碍疾病:高血氨症,氨中毒血氨浓度升高称高氨血症,高氨血症脑功能障碍,称氨中毒。
起因:肝功能严重损伤或尿素合成酶的遗传缺陷肝性脑病(详细内容参人代黄色教材)定义:肝性脑病是继发于严重肝炎,以代谢絮乱为基础的中枢神经系统功能失调综合征,其主要临床表现是意识障碍、行为失常和昏迷。
发病机制:1.氨中毒学说2.假性神经递质学说3.氨基酸代谢失衡学说4.GABA学说5.神经毒物协同学说治疗:1.消除病因2.减少肠内毒物的生成和吸收3.促进有毒物质的代谢,纠正氨基酸代谢的絮乱4.肝移植5.其他对症治疗第五节:个别氨基酸的代谢脱羧基作用1.普遍反应步骤:氨基酸脱羧酶胺醛羧酸2.生成各种胺:GABA,组胺,5-羟色胺,多胺,牛黄酸○1谷氨酸经谷氨酸脱羧酶催化生成γ-氨基丁酸:GABA(γ-氨基丁酸)是抑制性神经递质,对中枢神经有抑制作用○2牛磺酸:○3组胺:生理作用:强烈的血管舒张剂增加毛细血管的通透性刺激胃蛋白酶及胃酸的分泌○45-羟色胺:○5多胺:调节细胞生长在生长旺盛的组织(如胚胎、再生肝、肿瘤组织)含量较高,其限速酶鸟氨酸脱羧酶活性较强一碳单位生成1.定义:某些氨基酸代谢过程中产生的只含有一个碳原子的基团,称为一碳单位2.载体:四氢叶酸做为一碳单位运载体,在N5,N10位结合3.形式:一碳单位主要来源于氨基酸代谢4.转变:5.生理功能:作为合成嘌呤和嘧啶的原料把氨基酸代谢和核酸代谢联系起来含硫氨基酸代谢:含硫氨基酸:甲硫氨酸,半胱氨酸,胱氨酸(一)甲硫氨酸的代谢1.甲硫氨酸与转甲基作用产生SAM(S—腺苷甲硫氨酸),SAM为体内甲基的直接供体2. 甲硫氨酸循环甲硫氨酸循环生理意义:为机体甲基化反应提供甲基,N5—CH3—FH4 为甲基的间接供体。
3. 肌酸的合成:甘氨酸为骨架,精氨酸提供脒基,SAM提供甲基,终产物为肌酸酐(二)半胱氨酸与胱氨酸的代谢1. 半胱氨酸与胱氨酸的互变2. 硫酸根的代谢含硫氨基酸氧化分解均可产生硫酸根,但半胱氨酸是体内硫酸根的主要来源体内硫酸根代谢重要产物之一PAPS作用:参与硫酸软骨素、硫酸角质素等物质的合成,参与肝脏的生物转化3.半胱氨酸转变为牛磺酸芳香族氨基酸代谢芳香族氨基酸:苯丙氨酸,酪氨酸,色氨酸(一)苯丙氨酸和酪氨酸的代谢生成:苯乙酸,多巴胺,黑色素,尿黑酸代谢流程图:参书本P219图相关疾病:帕金森病,白化病,尿黑酸症,苯酮酸尿症(二)色氨酸代谢苯酮酸尿症(更多信息参人代黄色P63)1.定义:体内苯丙氨酸羟化酶缺陷,苯丙氨酸不能正常转变为酪氨酸,苯丙氨酸经转氨基作用生成苯丙酮酸、苯乙酸等,并从尿中排出的一种遗传代谢病。
2.临床表现:智力缺陷,毛发和皮肤较正常人略浅,尿液和汗液伴鼠臭味治疗:低苯丙氨酸膳食3.大概机制:支链氨基酸代谢(略)。