《有机化学》习题答案(胡宏纹,第三版)
- 格式:pdf
- 大小:549.72 KB
- 文档页数:57
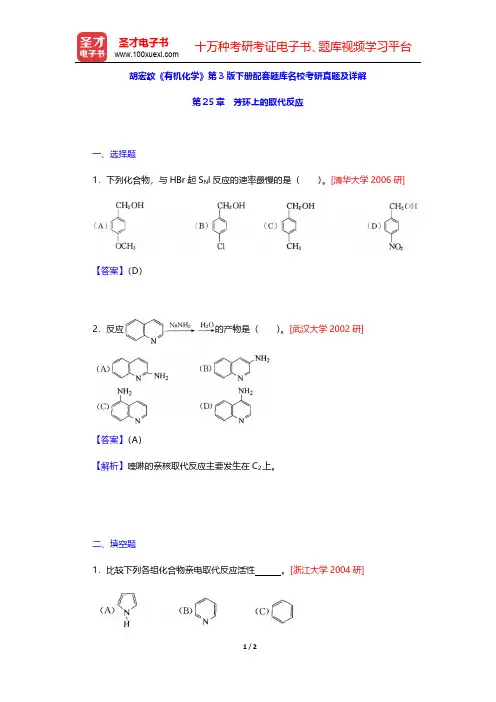
胡宏纹《有机化学》第3版下册配套题库名校考研真题及详解
第25章芳环上的取代反应
一、选择题
1.下列化合物,与HBr起S N l反应的速率最慢的是()。
[清华大学2006研]
【答案】(D)
2.反应的产物是()。
[武汉大学2002研]
【答案】(A)
【解析】喹啉的亲核取代反应主要发生在C2上。
二、填空题
1.比较下列各组化合物亲电取代反应活性。
[浙江大学2004研]
【答案】亲电取代反应活性:(A)>(C)>(B)
【解析】吡咯分子中环内每个碳原子提供1个p电子、氮原子提供2个p电子,组成大π键,氮原子的给电子共轭效应大于吸电子诱导效应,故吡咯中电子云密度比苯高;而吡啶分子中氮原子上的孤对电子没有参与大π键,氮原子的吸电子诱导效应大于给电子的共轭效应,故吡啶环内的电子云密度比苯低。
2.排出下列各化合物在亲电取代反应中的活性大小次序:。
[清华大学1999研、大连理工大学2003研]
【答案】亲电取代反应活性:(C)>(B)>(A)>D)
【解析】呋喃、噻吩电子云密度比苯高,相对而言,氧的给电子共轭效应比硫强,故呋喃的电子云密度比噻吩高,更易发生亲电取代反应,而吡啶中由于氮的电负性比碳强,故吡啶环上的电子云密度比苯低,其亲电取代反应活性不如苯。


胡宏纹《有机化学》(第3版)配套模拟试题及详解一、选择题(每题3分,共18分)1.下列烷烃沸点最低的是()。
A.正己烷B.2-甲基戊烷C.3-甲基戊烷D.2,3-二甲基戊烷【答案】C2.与化合物A互为对映异构体的是()。
A.B.C.D.【答案】B3.下列卤代烃在溶液不能发生消除反应的是()。
【答案】(c)4.下列化合物中哪一个是2R,3R-酒石酸的对映异构体:()。
【答案】A【解析】2R,3R-酒石酸的对映体为2S,3S-酒石酸。
5.下列化合物中具有芳香性的是()。
【答案】C6.下列构象中最稳定的是()。
【答案】D二、填空题(每题4分,共32分)1.排列下列化合物与进行双烯合成反应的活性:。
【答案】(C)>(A)>(D)>(B)【解析】连有给电子基的双烯体反应活性较强,反之,连有吸电子基的双烯体反应活性较弱。
2.比较下列碳正离子的稳定性:。
A.+B.+C.+D.+【答案】A>B>D>C【解析】考察碳正离子稳定性的顺序。
3.。
【答案】【解析】第一步为烯烃的反马氏加成反应;第二步为卤代烃的亲核取代反应;第三步为腈的水解反应;第四步为羧酸的α-H卤代。
4.。
【答案】【解析】在强酸作用下,杂环上氮原子接受质子,带正电荷,故杂环上的亲电取代反应比较困难,反应主要发生在苯环上。
5.。
【答案】【解析】-NO2是吸电子基,使邻、对位电子云密度降低较多,对位溴更易被取代。
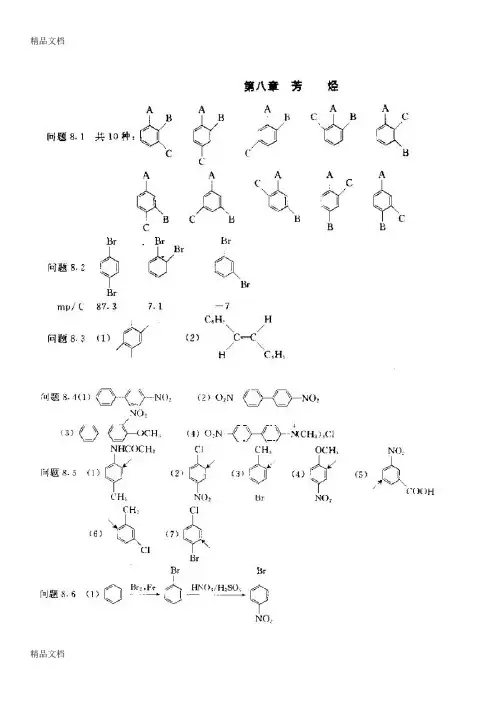
6.比较下列芳香化合物一次硝化反应的活性大小。
【答案】(A)>(D)>(B)>(C)【解析】根据定位基对苯环的影响,-NHCOCH3使苯环活化,-COOH使苯环钝化,-NO2也使苯环钝化,但钝化的程度比-COOH要强。
要比较硝化反应的活性大小,其实就是比较定位基对苯环活化程度的比较。
7.按沸点由高到低的顺序排列下列化合物:。
【答案】④>③>②>①【解析】能形成氢键沸点升高,且分子间氢键大于分子内氢键。
8.比较下列各组化合物水解反应速度大小。
【答案】(A)>(C)>(D)>(B)【解析】羧酸衍生物中,羰基缺电子程度越大,亲核反应活性越大,水解反应越快。

第16章杂环化合物16.1 复习笔记一、概念1.杂环、杂原子杂环是指由碳原子和至少一个其他原子所组成的环。
杂原子是指环内除了碳以外的原子称为,最常见的杂原子为氮、氧和硫。
2.杂环化合物杂环化合物是指含有杂环的有机化合物。
3.杂环化合物的命名对于杂环母核我国目前采取外文音译的方法命名。
例如:二、呲啶1.结构和物理性质(1)结构① 吡啶分子中所有的原子在同一平面内,测定的键长、键角为② 氮原子的孤电子对在sp2轨道上,与p轨道垂直,不参与π-电子的共轭。
③ 氮原子的存在使吡啶分子中六元环变形,并具有较大的偶极矩(7.34×10-30 C·m)。
④ 吡啶的共振结构如下:⑤ 吡啶环上碳原子带部分正电荷,是缺电子的芳环。
⑥ 用分子轨道法计算出来的吡啶环上的π-电子密度为⑦ 原子的编号从氮原子开始,2、6位,3、5位和4位原子也分别用α、β和γ表示。
(2)物理性质① 吡啶为无色液体,能与水混溶,气味与苯胺相似。
② 吡啶及其烷基取代物的沸点都比苯系化合物高。
③ 杂环上质子的化学位移与其所在碳原子周围的电子密度有关,与缺电子碳原子相连的质子的共振信号在低场出现。
2.氮原子上的亲电加成(1)吡啶环上的氮原子相当于脂肪族化合物中的亚胺,能与亲电试剂加成。
(2)吡啶的碱性在水溶液中(pK a=5.20)比脂肪胺(pK a=9~11)弱,而在气相中相近。
(3)由于甲基是给电子取代基,甲基吡啶碱性比吡啶强。
(4)一些吡啶盐是有机合成中有效的试剂:(5)吡啶是金属离子的良好配体,例如:(6)吡啶与酰氯、磺酰氯或酐生成季铵盐,后者与酰氯等相比,是更有效的酰化剂。
(7)吡啶与卤代烷或硫酸烷基酯生成季铵盐:3.碳原子上的亲电取代(1)吡啶是缺电子芳环,碳原子上的亲电取代速率非常慢,只得到3位取代产物。
如:(2)吡啶环上的给电子取代基使亲电取代较易进行,但速率仍低于苯系化合物。
如:(3)2,6-二叔丁基吡啶可以在液体SO2中用SO3磺化:(4)亲电取代生成3位取代物的原因是:亲电试剂进攻3位时,生成的中间体最稳定:进攻2位或4位时,生成的中间体中,正电荷在电负性较大的氮原子上,使其很不稳定:4.碳原子上的亲核取代(1)亲核取代是吡啶环特有的反应,苯系化合物没有类似反应。


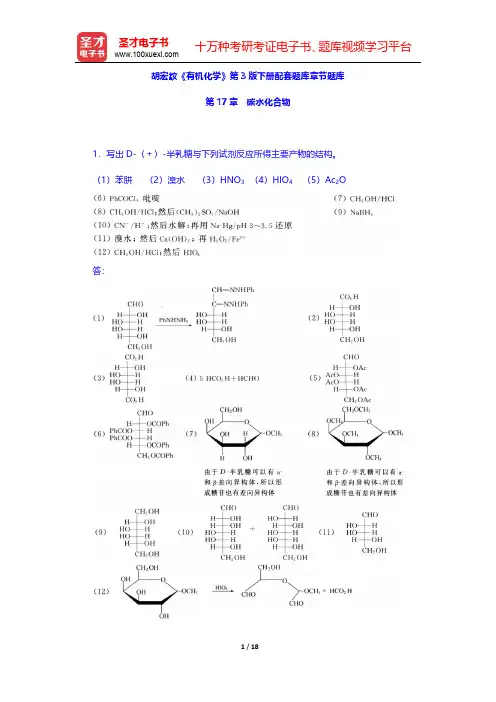
胡宏纹《有机化学》第3版下册配套题库章节题库第17章碳水化合物1.写出D-(+)-半乳糖与下列试剂反应所得主要产物的结构。
(1)苯肼(2)溴水(3)HNO3(4)HIO4(5)Ac2O答:2.某二糖分子式为C12H22O11,不还原费林试剂,没有变旋光作用,不生成脎,也不被Br2/H2O氧化成糖酸,用α-葡萄糖苷酶或酸催化水解仅得到D-葡萄糖,若先甲基化后再水解,则仅得到2,3,4,6-四-O-甲基-D-葡萄糖,试推测该二糖的结构。
答:该二糖为二分子葡萄糖经苷键连接,从其化学性质和被α-葡萄糖苷酶水解及先甲基化后再水解仅得到2,3,4,6-四-O-甲基-D-葡萄糖,说明是二分子α-葡萄糖在C1经苷键连接。
其结构式和相应的构象式为3.写出下列单糖的Haworth式:(1)α-D-(+)-吡喃葡萄糖;(2)β-D-(-)-呋喃果糖;(3)β-D-(+)-吡喃半乳糖;(4)-L-(+)-呋喃阿拉伯糖。
答:在糖的半缩醛环状结构的Fischer投影式中,半缩醛羟基与决定构型的羟基(倒数第二位的羟基)在同侧的定位α屏构体,在异侧的定为β异构体。
这种投影式不能准确地表示环状结构。
用Haworth式可较好地表示糖的环状结构。
把Fischer投影式转变成Haworth 投影式时,要遵循以下几条规则:①Fischer投影式中手性碳原子右侧的羟基都放在透视环的下面,而左侧的羟基都放在环的上面;②D构型糖的末端-CH2OH都放在环的上面,L构型的放在环的下面。
(1)(2)(3)(4)4.完成下列反应,给出中间物及产物的构型。
答:5.葡萄糖苷在碱性水溶液中无变旋现象,在酸性水溶液中却有变旋现象,试解释之。
答:因为葡萄糖苷是个缩醛,缩醛在碱性水溶液中稳定,因此无变旋现象;缩醛在酸性水溶液中发生互变,故呈变旋现象。
6.果糖是酮糖,为什么也可以像醛糖一样和Tollens、Fehling试剂反应?但却不能与溴水反应?答:果糖在碱性溶液中可差向异构化,存在如下平衡:Tollens和Fehling试剂呈碱性,果糖在其中发生差向异构化,部分转变为葡萄糖和甘露糖,因此显正反应。



十万种考研考证电子书、题库视频学习平台圣才电子书胡宏纹《有机化学》第3版下册配套题库章节题库第25章芳环上的取代反应一、选择题1.下列化合物中发生苯环上亲核取代反应速度最快的是()。
【答案】D2.比较亲电取代反应活性的大小()。
A.d>b>c>aB.a>d>c>bC.a>c>b>dD.c>b>a>d【答案】C 二、填空题1.。
【答案】【解析】此反应为亲核取代反应,考点在于芳烃上的两个氯,一个是非常活泼的烯丙基氯.一个是最不活泼的乙烯氯。
3.【答案】【解析】第一步为芳烃的侧链氧化反应;第二步为芳烃的亲电取代(连有间位定位基);第三步为羧酸成酰氯的反应;第四步为酰氯成酐的反应。
三、简答题1.由苯和不超过C3(含C3)的有机原料合成。
答:2.以苯或甲苯为原料合成对甲基苯甲酸苯酯。
答;3.指出下列化合物进行氯化时,氯原子主要将进攻苯环的哪个位置。
答:(1)该化合物两个取代基的定位影响一致,氯将进攻2,4位(见表25-1)。
表25-1氯原子的进攻位置(2)该化合物苯环上两个取代基,一个为间位定位基,一个为邻对位定位基。
当氯进攻时,将主要上邻对位定位基的邻、对位(见表25-1)。
(3)该化合物的两个取代基,一个为间位定位基,一个为邻对位定位基。
当氯进攻时,将主要进攻带有邻对位定位基的苯环(见表25-1)。
(4)两个邻对位定位基的定位作用有矛盾时,以强的邻对位定位基为主(见表25-1)。
4.以苯及小于等于3个碳原子的有机物为原料合成。
答:。
胡宏纹有机化学(第3版)(下册)知识点笔记课后答案第16章杂环化合物16.1 复习笔记⼀、概念1.杂环、杂原⼦杂环是指由碳原⼦和⾄少⼀个其他原⼦所组成的环。
杂原⼦是指环内除了碳以外的原⼦称为,最常见的杂原⼦为氮、氧和硫。
2.杂环化合物杂环化合物是指含有杂环的有机化合物。
3.杂环化合物的命名对于杂环母核我国⽬前采取外⽂⾳译的⽅法命名。
例如:⼆、呲啶1.结构和物理性质(1)结构①吡啶分⼦中所有的原⼦在同⼀平⾯内,测定的键长、键⾓为②氮原⼦的孤电⼦对在sp2轨道上,与p轨道垂直,不参与π-电⼦的共轭。
③氮原⼦的存在使吡啶分⼦中六元环变形,并具有较⼤的偶极矩(7.34×10-30 C·m)。
④吡啶的共振结构如下:⑤吡啶环上碳原⼦带部分正电荷,是缺电⼦的芳环。
⑥⽤分⼦轨道法计算出来的吡啶环上的π-电⼦密度为⑦原⼦的编号从氮原⼦开始,2、6位,3、5位和4位原⼦也分别⽤α、β和γ表⽰。
(2)物理性质①吡啶为⽆⾊液体,能与⽔混溶,⽓味与苯胺相似。
②吡啶及其烷基取代物的沸点都⽐苯系化合物⾼。
③杂环上质⼦的化学位移与其所在碳原⼦周围的电⼦密度有关,与缺电⼦碳原⼦相连的质⼦的共振信号在低场出现。
2.氮原⼦上的亲电加成(1)吡啶环上的氮原⼦相当于脂肪族化合物中的亚胺,能与亲电试剂加成。
(2)吡啶的碱性在⽔溶液中(pK a=5.20)⽐脂肪胺(pK a=9~11)弱,⽽在⽓相中相近。
(3)由于甲基是给电⼦取代基,甲基吡啶碱性⽐吡啶强。
(4)⼀些吡啶盐是有机合成中有效的试剂:(5)吡啶是⾦属离⼦的良好配体,例如:(6)吡啶与酰氯、磺酰氯或酐⽣成季铵盐,后者与酰氯等相⽐,是更有效的酰化剂。
(7)吡啶与卤代烷或硫酸烷基酯⽣成季铵盐:3.碳原⼦上的亲电取代(1)吡啶是缺电⼦芳环,碳原⼦上的亲电取代速率⾮常慢,只得到3位取代产物。
如:(2)吡啶环上的给电⼦取代基使亲电取代较易进⾏,但速率仍低于苯系化合物。
如:(3)2,6-⼆叔丁基吡啶可以在液体SO2中⽤SO3磺化:(4)亲电取代⽣成3位取代物的原因是:亲电试剂进攻3位时,⽣成的中间体最稳定:进攻2位或4位时,⽣成的中间体中,正电荷在电负性较⼤的氮原⼦上,使其很不稳定:4.碳原⼦上的亲核取代(1)亲核取代是吡啶环特有的反应,苯系化合物没有类似反应。