苯酚与溴水的反应2羟基对苯环的影响—取代反应试验
- 格式:ppt
- 大小:677.00 KB
- 文档页数:19

探究苯酚和溴水的反应一、苯酚溶液和溴水实验成功的关键实验室经常可能出现的状况1、当苯酚溶液浓度比较大时(不可能很高),当饱和溴水滴到苯酚溶液中先出现沉淀然后消失或甚至无法出现白色沉淀,原因是即便生成了三溴苯酚又可以溶于过量的苯酚溶液中。
讨论:这里是否可能会有第二个原因:溴水和苯酚并没有得到三溴苯酚,也许得到一溴苯酚或二溴苯酚,而一溴苯酚或二溴苯酚都不是白色沉淀。
2、当苯酚与浓溴水反应生成白色沉淀之后,继续加入浓溴水,就会发生如下反应:生成了黄色的2,4,4,6—四溴环己二烯酮,故析出的白色淀淀转变为黄色沉淀,这里显然溴水氧化了三溴苯酚。
3、显然,为了很好地完成该实验,溴水一定要逐渐滴入,苯酚的浓度不能太高。
4、成功的实际经验操作:把米粒大小的苯酚固体放入试管中,然后加水使之溶解→把试管中的苯酚溶液“完全”倒入到另一试管中(待用)→往原试管中注入蒸馏水5mL左右,振荡→逐滴滴入浓溴水→看到白色沉淀。
二、苯酚溶液中加溴水溶液的PH的变化情况在苯酚溶液中加溴水发生反应如下:从中可以看出,在苯酚溶液中加溴水,溶液的酸性大大增强,得到了氢溴酸这强酸和三溴苯酚,因此酸性大为增强。
另外三溴苯酚的酸性也大于苯酚的酸性。
三、一道04年浙江省化学竞赛题的解析某同学在做实验时,将少量溴水滴入苯酚溶液中,结果没有发生沉淀现象,他又继续在反应混合液中滴入足量的氢氧化钠溶液,此时他发现A仍无沉淀B产生白色沉淀C先产生沉淀后溶解D溶液呈橙色这是2004年浙江省高中学生化学竞赛试题第4题,在苯酚的性质实验中,加溴水后未发现沉淀的情况常常发生,而此处给出的是少量溴水,容易使考生认为是过量的苯酚溶液溶解了三溴苯酚沉淀,于是想到用足量的氢氧化钠溶液来中和过量的苯酚,假如苯酚不存在了,就应该看到有白色沉淀了,于是这样大多考生便选了答案B。
那么实际情况怎样呢?事实上溶液中仍无沉淀!该题的参考答案应是A。
【解析】当加入氢氧化钠溶液时,通俗的讲法就是氢氧化钠溶液首先和先前得到的氢溴酸反应得到溴化钠和水,然后可以和三溴苯酚作用得到三溴苯酚钠和水,因此得不到白色沉淀的三溴苯酚,当然这里我们必须知道三溴苯酚钠不是白色沉淀的。


第3讲 卤代烃 醇 酚考点一 卤代烃 1.概念烃分子中的氢原子被卤素原子取代后生成的化合物。
2.结构特点卤素原子是卤代烃的官能团。
C —X 之间的共用电子对偏向________,形成一个极性较强的共价键,分子中________键易断裂。
3.分类4.饱和卤代烃的性质 (1)物理性质 (2)化学性质 ①取代反应:R —X +NaOH ――→H 2O△____________(R 代表烃基); R —CHX —CH 2X +2NaOH ――→H 2O△______________。
②消去反应:R —CH 2—CH 2—X +NaOH ――→醇△______________或R —CH 2—CH 2—X ――→强碱、醇△______________;5.检验卤代烃分子中卤素的方法 (1)实验方法一.2.某卤代烷烃C 5H 11Cl 发生消去反应时,可以得到两种烯烃,则该卤代烷烃的结构简式可能为( )3.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )4.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都正确的是()选项反应类型反应条件A 加成反应、取代反应、消去反应KOH醇溶液/加热、KOH水溶液/加热、常温B 消去反应、加成反应、取代反应NaOH醇溶液/加热、常温、NaOH水溶液/加热C 氧化反应、取代反应、消去反应加热、KOH醇溶液/加热、KOH水溶液/加热D 消去反应、加成反应、水解反应NaOH水溶液/加热、常温、NaOH醇溶液/加热5. 证明溴乙烷中溴元素的存在,下列操作步骤中正确的是()①加入硝酸银溶液②加入氢氧化钠溶液③加热④加入蒸馏水⑤加入稀硝酸至溶液呈酸性⑥加入氢氧化钠醇溶液A.④③①⑤B.②③⑤①C.④⑥③①D.⑥③⑤①6.根下面的反应路线及所给信息填空。
(1)A的结构简式是__________,名称是__________。


酚1.能证明苯酚分子里羟基上的氢原子比乙醇分子里羟基上的氢原子活泼的事实是()A.苯酚能与浓溴水发生取代反应,而乙醇不能B.苯酚能与氢氧化钠反应,而乙醇不能C.常温下,苯酚微溶于水,而乙醇与水互溶D.苯酚有毒,而乙醇无毒2.下列物质中不能与苯酚发生反应的是()A. Na2CO3B. NaHCO3C. NaOH D. FeCl33.下列有关苯酚的实验事实中,能说明侧链对苯环性质有影响的是()A.苯酚与浓溴水反应生成三溴苯酚B.苯酚能和NaOH溶液反应C.苯酚燃烧产生带浓烟的火焰D. 1mol苯酚与3mol H2发生加成反应4.下列说法正确的是()A.苯中含有杂质苯酚,可用浓溴水来除杂B. 1mol在一定条件下与足量NaOH溶液反应,最多消耗3mol NaOHC.按系统命名法,的名称为3,3,6一三甲基﹣4﹣乙基庚烷D.已知C﹣C键可以绕键轴自由旋转,结构简式为的分子中至少有11个碳原子处于同一平面上5.下列有关说法正确的是()A.苯酚钠溶液中通入少量的二氧化碳,产物是苯酚和碳酸钠B.苯的同系物中,苯环和侧链相互影响,使得二者均易被氧化C.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2D.苯甲醛、苯乙烯分子中的所有原子可能处于同一平面6.苯酚()在一定条件下能与氢气加成得到环己醇(),下面关于这两种有机物的叙述中,错误的是()A.都能发生取代反应B.都能与金属钠反应放出氢气C.苯酚是比碳酸更强的酸,环己醇则显中性D.苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象7.日本冈山大学教授滨田博喜和研究员富良德等通过实验发现,桉树叶子的培养细胞能够消除有害化学物质双酚A的毒性。
双酚A的结构简式如下图所示,下列有关此物质的说法正确的是()A. 1 mol该物质与足量溴水反应消耗2 mol Br2B.该物质能与碳酸氢钠溶液反应放出CO2 C.该物质的所有碳原子可能在同一平面D.该物质与足量氢气发生加成反应后所得物质的分子式为C15H28O28.下列说法正确的是()A.苯酚显酸性,是因为羟基对苯环影响的结果B.分子式为C2H4和C3H6的物质一定互为同系物C.聚合物是苯酚和甲醛在一定条件下反应得到的高分子化合物D. 1mol与足量的NaOH溶液加热充分反应,最多能消耗5mol NaOH9.下列说法正确的是()A.苯中含有的苯酚杂质可通过加入足量溴水后过滤的方法而除去B.苯乙烯中至少有8个碳原子在同一个平面C.等质量的乙烯和聚乙烯完全燃烧,产生的二氧化碳的质量之比为1:1D.分子式为C5H10O2且可与氢氧化钠溶液反应的有机化合物有14种(不考虑立体异构)10.由碳、氢、氧3种元素组成的有机物A,相对分子质量为152,其分子中C、H原子个数比为1∶1,氧元素的质量分数为31.58%。

高中化学有机实验—苯酚的酸性2有机实验是高中化学学习的重要内容,是高考常考内容。
今天给大家分享重要有机物的性质实验及注意事项。
有机实验1.甲烷(1)甲烷通入KMnO4酸性溶液中实验:把甲烷通入盛有KMnO4酸性溶液的试管里,观察紫色溶液是否有变化?现象与解释:溶液颜色没有变化。
说明甲烷与KMnO4酸性溶液不反应,进一步说明甲烷的性质比较稳定。
(2)甲烷的取代反应实验:取一个100mL的大量筒,用排饱和食盐水的方法先后收集20mLCH4和80mLCl2,放在光亮的地方(注意:不要放在阳光直射的地方,以免引起爆炸),等待片刻,观察发生的现象。
现象与解释:大约3min后,可观察到量筒壁上出现油状液滴,量筒内饱和食盐水液面上升。
说明量筒内的混合气体在光照下发生了化学反应;量筒上出现油状液滴,说明生成了新的油状物质;量筒内液面上升,说明随着反应的进行,量筒内的气压在减小,即气体总体积在减小。
2.乙烯(1)乙烯的燃烧实验:点燃纯净的乙烯。
观察乙烯燃烧时的现象。
现象与解释:乙烯在空气中燃烧,火焰明亮,并伴有黑烟。
乙烯中碳的质量分数较高,燃烧时有黑烟产生。
(2)乙烯使KMnO4酸性溶液褪色实验:把乙烯通入盛有KMnO4酸性溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:KMnO4酸性溶液的紫色褪去,说明乙烯能被氧化剂KMnO4氧化,它的化学性质比烷烃活泼。
(3)乙烯使溴的四氯化碳溶液褪色实验:把乙烯通入盛有溴的四氯化碳溶液的试管里,观察试管里溶液颜色的变化。
现象及解释:溴的红棕色褪色,说明乙烯与溴发生了反应。
3.乙炔(1)点燃纯净的乙炔实验:点燃纯乙炔。
观察乙炔燃烧的现象。
现象及解释:乙炔燃烧时,火焰明亮,并伴有强烈的黑烟。
这是因为乙炔中碳的质量分数高于乙烯,碳没有完全燃烧。
(2)乙炔使KMnO4酸性溶液褪色实验:把纯净的乙炔通入盛有KMnO4酸性溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:KMnO4酸性溶液的紫色褪去,说明乙炔能与KMnO4酸性溶液反应。



课程篇人教版高中化学选修五《有机化学基础》第三章第一节第二课时酚的教学中涉及了苯酚与溴水的反应。
该演示实验既要让学生掌握苯酚与溴水的取代反应,更要让学生理解有机物分子中取代基对物质性质的影响(羟基活化苯环),因此该实验对学生化学思维的建立尤为重要。
课本中描述到“苯酚与溴的反应很灵敏,可用于苯酚的定性检验和定量测定”,实验3-4的实验步骤也强调“向盛有少量苯酚稀溶液的试管里逐滴加入饱和溴水,边加边振荡”,当溴水中滴入苯酚溶液后,立即有白色沉淀产生。
但实际实验过程中,当试剂浓度不相同时,实验现象不相同。
实验结果如下:组别实验药品实验现象组别实验药品实验现象1苯酚饱和溶液(3mL ),饱和溴水(5滴)产生的白色沉淀立即消失2苯酚饱和溶液(3mL ),饱和溴水(0.2mL )产生大量白色沉淀3苯酚饱和溶液(3mL ),饱和溴水(0.5mL )产生大量黄色沉淀4苯酚饱和溶液(3mL ),液溴(5滴)反应放热,产生大量白雾当苯酚饱和溶液中加入少量饱和溴水时,产生的白色沉淀立即消失,是因为生成的2,4,6—三溴苯酚易溶于有机溶剂,即溶解于苯酚溶液中;当继续滴加饱和溴水,可以观察到大量白色沉淀生成;当加入过量饱和溴水时,可以观察到生成的白色沉淀转化为淡黄色沉淀,即2,4,6—三溴苯酚进一步与溴反应生成黄色的2,4,4,6—四溴环己二烯酮。
经过大量实验验证,该实验的最佳试剂用量和实验操作可有两种:(1)苯酚溶液的浓度以0.05mol/L-0.1mol/L 为宜,溴水为饱和溴水,且逐滴滴加,观察到产生明显的白色沉淀时立即停止滴加;(2)苯酚的饱和溶液中,逐滴0.2-0.3mL饱和溴水即可。
但是,苯酚与溴的实验目的不仅要证明两种物质可以快速发生反应,更重要的是证明有机物分子中取代基对物质性质的影响,苯酚分子中羟基活化了苯环,让苯酚中苯环上的取代反应发生得更容易。
因此,该部分的教学设计可以对照苯与溴的反应进行对照实验,进行苯酚与液溴的演示实验,以满足教学需求。
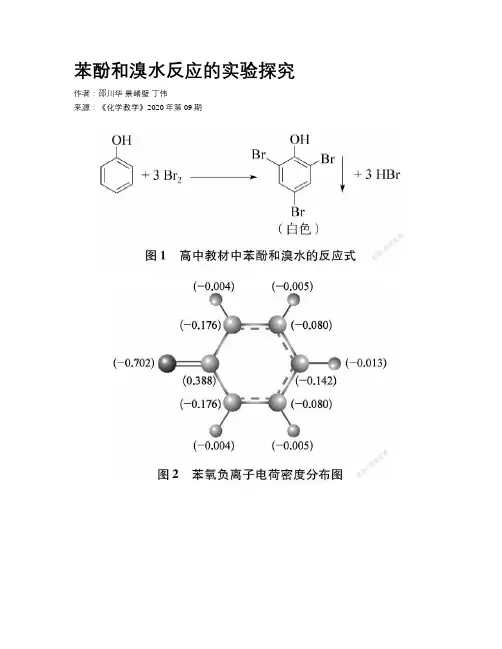
苯酚和溴水反应的实验探究作者:邵川华景崤壁丁伟来源:《化学教学》2020年第09期摘要:通過理论分析与电荷模拟,归纳苯酚邻、对位容易发生溴代反应的原因是酚羟基的共轭效应大于诱导效应。
通过实验探究,优化苯酚与溴水的反应,即向5~10mg/mL浓度的苯酚溶液逐滴滴加2%的浓溴水,可清晰看到明显的白色沉淀。
中学教材中介绍的苯酚定量测定的方法并非是简单的苯酚溴代,而是间接地利用苯酚与溴水的反应,是一个比较复杂的过程。
关键词:苯酚溴代反应; 苯酚定量测定; 实验探究文章编号:1005-6629(2020)09-0075-04中图分类号:G633.8文献标识码:B1问题的提出高中各版本化学教材都涉及到了苯酚和溴水的反应,以人民教育出版社的《有机化学基础》为例,教材中给出了苯酚和溴水的反应,该反应生成了2,4,6-三溴苯酚的白色沉淀[1],如图1所示。
学生在学习该部分内容时已先学习过苯和液溴的反应,该反应需要在FeBr3的催化下发生取代生成溴苯,由此学生会产生疑问:为什么苯酚容易溴代且不需要催化剂?另外,在学习苯酚时,会涉及到苯酚容易被空气中的氧气氧化生成红色物质,而溴水也具有一定的氧化性,溴水能不能氧化苯酚?还有,教材中介绍苯酚和溴水生成2,4,6-三溴苯酚的反应是定量发生的,常用于苯酚的定性和定量测定,是否可以认为溴水不能氧化苯酚?苯酚的定量测定又是如何进行的?如何回答解释上述疑问,本文试图作一些理论分析和实验探究。
2苯酚与溴水反应的原理2.1苯酚的电子效应苯酚中存在诱导和共轭的双重效应[2]。
诱导效应,由于与碳相连的羟基上氧的电负性大于碳,苯环上的电子通过σ键向羟基偏移,这种羟基的吸电子的效应会使苯环上电子云密度降低,钝化苯环发生亲电取代的能力,进而阻碍溴代反应的进行;共轭效应,由于氧的p轨道上的孤电子对与苯环π轨道上的电子云相互重叠,从而使苯环π轨道电子发生较大范围的离域,整个共轭体系由苯环的∏66体系转化为共轭度更高的∏87体系,羟基氧通过p-π共轭效应使苯环上电子云密度增大,提高了苯环发生亲电取代的能力,促进了苯环溴代的进行。

苯酚与溴水反应引言苯酚与溴水是一种常见的有机反应。
溴水是溴元素的水溶液,而苯酚是一个含有苯环和羟基的有机化合物。
在苯酚与溴水反应中,苯酚的羟基会与溴水中的溴原子发生置换反应,生成溴代苯酚。
这个反应在有机化学中具有重要的意义,它是生成许多其他有机化合物的中间步骤。
反应机理苯酚与溴水反应的机理可以分为两步: 1. 首先,苯酚的羟基上的氧原子与溴水中的溴原子生成一个溴代苯酚的中间体。
这个步骤是一个亲电取代反应,溴原子会取代苯酚上的羟基。
2. 然后,中间体中的负离子会与酸或碱反应,生成最终产物。
如果中间体与酸反应,最终产物是苯酚,如果与碱反应,最终产物是对应的溴代苯酚。
实验条件苯酚与溴水反应的实验条件通常为常温、常压下进行。
由于该反应为亲电取代反应,所以一般会添加一定量的催化剂,例如FeBr3,来加快反应速率。
实验步骤苯酚与溴水反应的具体步骤如下: 1. 准备实验条件:在实验室中设置好实验器材,准备好苯酚和溴水。
2. 在反应容器中加入苯酚:将适量的苯酚加入装有溶剂的反应容器中。
3. 加入溴水:缓慢地向反应容器中滴加溴水,同时搅拌反应混合物。
4. 加入催化剂:根据需要,可以在反应容器中加入一定量的催化剂,例如FeBr3。
5. 反应观察:观察反应混合物的颜色变化、气味等物理性质的变化。
6.分离产物:反应结束后,用适当的方法将产物与溶剂分离。
实验结果和讨论苯酚与溴水反应通常会生成溴代苯酚作为主要产物。
产物的种类和数量取决于反应物的摩尔比例、反应温度、反应时间以及添加的催化剂等因素。
通过控制这些条件,可以调整反应的产物分布。
此外,还可以使用其他有机溶剂、改变反应容器的形状和大小等方式来影响反应的产率和选择性。
需要注意的是,苯酚与溴水反应是一个有机合成中常用的反应,但在实验过程中需要注意安全问题。
苯酚具有毒性,可与氧气形成爆炸性混合物,而溴水也是一种强氧化剂。
在进行苯酚与溴水反应时,必须戴上适当的防护装备,遵守实验室的安全操作规程。
苯酚与溴水反应条件一、实验目的通过对苯酚与溴水反应条件的研究,探讨反应条件对反应速率和产物选择性的影响,为有机合成中的相关反应提供理论指导和实验依据。
二、实验原理苯酚与溴水反应是一种亲电取代反应,苯酚中的羟基与溴水中的溴离子发生亲电取代反应,生成溴代苯酚。
该反应可以通过控制反应温度、反应时间、溶剂性质等条件来调节反应速率和产物选择性。
三、实验条件对反应速率的影响1. 反应温度反应温度是影响反应速率的重要因素。
一定范围内,反应速率随着温度的升高而增加。
在较低温度下,反应速率较慢,反应物之间的碰撞频率较低,分子的活动性较弱。
而在较高温度下,反应速率显著增加,反应物分子的速度增大,碰撞频率增加,有利于反应的进行。
但温度过高时,反应可能会发生副反应或分解。
因此,在选择反应温度时需要考虑反应速率和产物选择性的综合影响。
2. 反应物浓度反应物浓度是影响反应速率的另一个重要因素。
反应速率与反应物浓度呈正相关关系,反应物浓度越大,反应速率越快。
这是因为反应物浓度的增加会增加反应物之间的碰撞频率,提高机会发生反应的可能性。
在实际应用中,可以通过控制反应物浓度来调节反应的速率。
3. 催化剂催化剂是促进反应进行的物质,在苯酚与溴水反应中的应用也能显著加快反应速率。
催化剂能够降低反应的活化能,使反应物更容易发生反应。
在苯酚与溴水反应中,一些金属离子如铁离子、铜离子等可作为催化剂,加快反应速率。
四、实验条件对产物选择性的影响1. 选择溶剂溶剂的选择对苯酚与溴水反应的产物选择性具有重要影响。
一般来说,非极性溶剂如苯、石油醚等有利于生成取代溴代苯酚,而极性溶剂如水、乙醇等有利于生成酚与卤仿。
这是因为非极性溶剂中反应物间的亲电取代反应更容易发生,而极性溶剂中的亲核取代反应更易进行。
2. 反应时间反应时间是影响产物选择性的因素之一。
苯酚与溴水发生反应后会生成苯酚的取代产物或酚与卤仿。
当反应时间较短时,取代溴代苯酚的生成较多;而当反应时间较长时,酚与卤仿的生成比例增加。
对羟基苯酚与溴水现象对羟基苯酚与溴水现象1. 引言在化学领域中,羟基苯酚与溴水反应的现象及其机理一直备受关注。
本文将深入探讨该反应的深度和广度,以帮助读者全面理解这一化学现象。
2. 羟基苯酚与溴水的基本概念羟基苯酚,化学式为C6H6O2,是一种具有羟基和苯环的有机化合物。
溴水,化学式为Br2,是一种淡黄色的液体,富含溴元素。
当羟基苯酚与溴水接触时,会引发一系列反应。
3. 反应过程的深度分析羟基苯酚与溴水的反应过程可以分为以下几步:1) 溴水分子中的一个溴原子通过取代反应取代掉羟基苯酚分子中的一个氢原子,生成溴代苯酚(C6H5BrO)。
2) 溴代苯酚中的溴原子再次发生取代反应,并取代另一个氢原子,生成二溴苯酚(C6H4Br2O)。
3) 二溴苯酚中的溴原子再次发生取代反应,并取代最后一个氢原子,形成三溴苯酚(C6H3Br3O)。
该反应过程表明,羟基苯酚中的羟基被溴原子取代,逐渐生成含有不同数量溴原子的苯酚类化合物。
4. 回顾与总结通过对羟基苯酚与溴水反应的深度分析,我们可以得出以下结论:1) 该反应是一个连续进行的化学反应过程,其中羟基被溴原子一步一步取代。
2) 通过增加溴水的浓度和反应温度,反应速度可以加快,生成更多的溴代苯酚、二溴苯酚和三溴苯酚。
3) 考虑到反应过程中的化学键断裂和形成,可以进一步探索溴水对羟基苯酚的取代反应机理。
5. 个人观点与理解羟基苯酚与溴水的反应是一种有趣的化学现象。
在没接触到这一现象之前,我们或许并不会想到羟基苯酚分子中的氢原子可以被溴原子取代。
然而,通过深入研究这一反应过程,我们不仅可以了解到分子之间发生的复杂相互作用,还可以更深入地理解有机化学中的取代反应机制。
了解羟基苯酚与溴水反应的深度和广度不仅有助于我们加深对化学反应机理的理解,还为我们在实验中精确控制反应条件提供了参考。
通过进一步研究该反应,我们可以拓展该领域的知识,并为某些医学和工业领域的应用提供可能性。
羟基苯酚与溴水反应是一个引人入胜的化学现象。
苯酚的化学性质 Prepared on 22 November 2020苯酚的化学性质(1)苯酚的弱酸性,是苯环上相连羟基的性质,而羟基不仅是苯酚的特征官能团,它还是醇的特征官能团。
①实验与解析:表1 苯酚化学性质实验现象与问题解析②列表比较:表2 乙醇和苯酚的比较③小结:由于乙醇和苯酚均具有相同的官能团——羟基,因而有相同化学性质的一面;但乙醇上的羟基不显酸性,而苯酚羟基上的氢原子比较活泼,可发生极微弱电离而显弱酸性(酸性极弱而不能使石蕊试剂变色),它们又具有不同化学性质的一面。
十分明显,这是由于两种化合物中羟基相连的烃基不同,影响了羟基上的氢原子活泼性也不同。
通过上述实验与比较,可以明显看出:苯酚、碳酸、乙醇其酸性大小的顺序应是:H2CO3>>C2H5OH(中性)(2)苯酚的取代反应,发生在苯环上。
可采用先复习苯的取代反应,然后讲授苯酚取代反应,最后列表总结。
也可采用边比较边讲解列表的方法以使学生的知识达到巩固加深、系统化的目的。
①苯酚与苯取代反应的比较:表3 苯酚与苯取代反应的比较②小结:在苯酚与溴的取代反应中,由反应物浓度、反应条件、取代氢原子多少、反应速度可知:苯酚比苯的取代反应容易进行得多,这是由于苯酚中苯环上连接的羟基能使苯基上的氢原子更加活泼,促使苯基上所发生取代反应更容易进行的必然结果。
总结:通过上面两个苯酚化学性质的学习,可知在苯酚的分子中,苯基影响了与其相连的羟基上的氢原子促使其较易电离,显示了比醇中羟基上的氢原子有较明显的酸性;而羟基则反过来能影响与其相连的苯基上的氢原子更活泼、更容易发生取代反应。
这是分子中官能团相互影响,相互制约的有力证明,它们是矛盾的又是统一的,二者存在于同一物质之中。
(3)苯酚和FeCl 3溶液的显色反应(略)。
(二)思考与练习③本节教学结束拟选一定的练习题,加深学生对苯的化学性质知识的巩固。
1.有机化合物A 中含碳%、氢%、氧%,它的密度是相同状态下H 2密度的54倍,该有机化合物水溶液遇FeCl 3溶液不呈紫色,试写出它的结构简式。