甘露醇注射液(250ml:50g)生产工艺规程
- 格式:doc
- 大小:147.00 KB
- 文档页数:12

甘露醇生产淀粉糖是指以淀粉为原料经水解、精制或再经深加工而获得的糖制品。
淀粉分子是由成千上万个葡萄糖分子(C6H12O6)连接而成,一个葡萄糖分子有6个碳原子,与下一个葡萄糖分子相连时有三种连法:一是第4个碳原子与下一个葡萄糖分子的第1个碳原子相连;二是第6个碳原子与下一个葡萄糖分子的第1个碳原子相连;三是第4个碳原子与下一个葡萄糖分子的第1个碳原子相连,同时第6个碳原子与另一个葡萄糖分子的第1个碳原子相连。
全部葡萄糖分子都以第一种连法连接的是直链淀粉,自然界很少存在;全部葡萄糖分子都以第二种连法连接无法形成长链,形不成淀粉;葡萄糖分子以三种连法混合连成的淀粉分子是自然界存在的淀粉的主流,其中以第三种连法连接的部位形成支叉,所以叫支链淀粉。
果糖与葡萄糖一样都是单糖,果糖的分子式也是C6H12O6,属于葡萄糖的同分异构体,通过异构酶的作用,葡萄糖的醛基变成酮基即得到果糖。
蔗糖、麦芽糖及异麦芽糖都属于双糖,一个葡萄糖的第4个碳原子另一个葡萄糖分子的第1个碳原子相连即为麦芽糖,一个葡萄糖的第6个碳原子另一个葡萄糖分子的第1个碳原子相连即为异麦芽糖,而蔗糖则由一个葡萄糖分子与一个果糖分子连接而成。
三个葡萄糖分子相连而成的三糖有麦芽三糖和潘糖。
4~8个葡萄糖连成的短链糖品叫低聚糖,9个以上葡萄糖连成的中分子物质叫做糊精,其甜味已经不明显,大量的葡萄糖连在一起就形成了淀粉或者形成更大分子量的纤维素。
以淀粉为原料选用不同的酶来水解或控制不同的水解程度可以得到不同的淀粉糖品。
以诺维信酶制剂为例:1、用耐温淀粉酶T ermamyl Supra将淀粉乳液化至DE6~10,经精制和喷雾干燥后可以制得糊精制品;2、用耐温淀粉酶Termamyl Supra将淀粉乳液化至DE13~15,选用葡萄糖淀粉酶Dextrozyme DX糖化到DE40~50,可以获得食品行业常用的葡萄糖浆;3、用耐温淀粉酶Termamyl Supra将淀粉乳液化至DE13~15,选用葡萄糖淀粉酶Dextrozyme DX糖化到DE99.5~101,可以得到葡萄糖含量97%以上的糖液。

主要工艺设备选型及计算(1)课程设计题目年产3500万瓶甘露醇注射液车间GMP工艺设计(2)年工作日250(3)生产班制一天二班制,按每班6h生产计。
(4)产品规格250ml/瓶,玻璃瓶。
(5)设计技术要求见“工艺设计平面布置图”(6)物料衡算年产量3500万瓶,250ml大输液。
年工作日250天。
产量计算每日14万,每小时1.2万,合计约200瓶/min;每班需配药液3.7t。
(7)主要设备选型说明①配料罐。
采用优质不锈钢反应容器。
浓配灌型号:1000L。
稀配罐型号:2000L。
②洗塞设备。
全自动湿法超声波胶塞清洗机。
型号BGX-2。
工作原理及结构特点:内胆部件采用316不锈钢材料制作,外壳采用304不锈钢材料制作,主要配套件和电子元件均选用进口产品,耐压、耐高温超声波和轴承、密封件、垫片均采用特殊材料。
产品的胶塞处理采用先进的真空吸料、超声波清洗、蒸汽灭菌、真空干燥工艺。
胶塞在自动吸料、强力喷淋、慢速翻滚、超声波等多项技术作用下洗涤、硅化、蒸汽灭菌、真空干燥、蒸汽再抽真空干燥至自动出料,全部在一机内由PLC程控器控制下自动操作完成,无中间转序,无交叉污染。
本机对各道工序的运行状态,能在显示屏上动态显示,直观了解机组运行情况并由记录仪自动记录各工序温度,以便备案查阅和打印。
主要技术参数:③注射用水制取设备。
列管多效蒸馏水机。
型号LD3000-5。
工作原理及结构特点:蒸发器:采用列管降膜蒸发技术,保证料水均匀的分布在各个蒸发管内壁,形成水膜蒸发。
上效纯蒸汽为下效蒸发器提供热能,自身完成蒸发、液化形成蒸馏水。
汽液分离器:采用分体式汽水四分离技术(汽水离心分离、下旋片隔板分离、丝网捕捉水滴分离、上旋片隔板分离)保证蒸馏水热源及内含量更低。
对纯水要求相对较低,单级反渗透(10us/cm)以下既可产出符合药典标准的蒸馏水。
主要技术参数:BSXGS50/18。
工作原理及结构特点:BSXGS50/18型玻璃瓶大输液洗灌塞联动机为玻璃瓶大输液生产中洗瓶、灌装、加塞三个工位合为一体的一台包装机。

试析复方甘露醇注射液的制备工艺及质量控制【摘要】目的:针对复方甘露醇注射液的制备工艺进行探究,寻找质量控制措施,并完善现有的质量控制标准体系;方法:将甘露醇与山梨醇分别作为主药与辅药,应用活性炭吸附法来制备复议甘露醇注射液,在105℃的环境下进行30分钟的灭菌,即得。
结果:依照本方法所制备的复议甘露注射液药品,主药成分损失量低,同时药液颜色外观符合于具体质量要求,同时包括热原在内的一系列其他项目也符合于我国药典在注射药剂方面的规定与需要;结论:该药剂的制备方式在工艺上存在着明显优势,工艺简便可靠,有良好的稳定性,所应用的质量控制方法也可以起到良好的控制效果,可以推广使用。
【关键词】复方甘露醇;注射液;质量控制;制备工艺甘露醇是己六醇药物的一种,该药物在溶解过程当中有较强的吸热性,甘味明显,因而对于口腔可以形成良好的刺激作用,可以用作醒酒剂,也常用于制备口中清凉剂咀嚼片,而该药物的颗粒剂型则可以直接应用为压片的赋形剂。
甘露醇注射液在临床应用当中有良好的降压效果,属于一种高渗透降压药物,经常用于抢救脑部疾患,以其自身的降压快、疗效准确的特点。
临床应用中的甘露醇注射液属于过饱和溶液,浓度为20%,因而在贮存过程当中,较容易产生结晶,如果处理不当,则会在使用过程中形成血栓,给患者造成生命危险。
因而本次研究当中,将20%甘露醇注射液作为复议甘露醇注射液,并且以2010版药典当甘露醇与山梨醇注射液相关内容结合具体规定进行检测。
复方甘露醇能保持并优于单方甘露醇的疗效,减少并发症的出现,达到安全、有效和方便,是一种理想的利尿新药。
但是关于本药品的注射液制备工艺以及质量控制方面资料并不完善,相关报道数量较少,本文针对其制备工艺以及控制标准方面的相关问题进行分析。
一、仪器与试药(一)仪器PHS-25数字酸度计仪(上海分析仪器厂);;电子天平;微孔滤器;微孔滤膜(0.22μm);量筒;移液管;洗耳球;烧杯;玻璃棒;电炉。

甘露醇的生产工艺及流程甘露醇概述甘露醇(Mannitol或mannite),又称D-甘露糖醇,己六醇,木蜜醇。
分子式C6H14O6,分子量182.17。
甘露醇是山梨醇的异构体。
甘露醇为白色结晶粉末,密度1.489,熔点166℃—168℃,沸点290℃—295℃(在0.4—0.467KPa),旋光度+28—+24。
甘露醇可溶于水(1克可溶于约5.5毫升水),微溶于甲醇乙醇,溶于吡啶和苯胺,不溶于乙醚。
甘露醇是山梨醇的异构体,山梨醇的吸湿性很强,但甘露醇完全没有吸湿性。
甘露醇甜度相当于蔗糖的70%。
人体能吸收,部分代谢,部分从尿中排出。
甘露醇主要用于医药和食品,作为食品添加剂、无糖甜食品、饲料添加剂。
甘露醇是常用糖醇食糖替代品之一,常用于无糖口香糖配料。
甘露醇是吸水性最小的糖醇,可用于食品防粘粉。
我国食品添加剂使用卫生标准GB2760规定,可用于无糖口香糖,最大用量200g/kg。
甘露醇市场及标准世界市场95%为粉状甘露醇,年消费1.8—2万吨,销售额1亿美元。
最大用户是无糖口香糖,约占市场的10%。
2004年粉状甘露醇用于口香糖价格4.87—5.9美元/kg,而2000为3.1美元/kg,但医药用的价更高。
2003年国内医药用甘露醇5600吨,其中注射用4500吨。
食品及添加剂用2200吨,包括出口总需求9500吨。
甘露醇生产过去我国甘露醇生产方法主要为天然提取法(如从海带中提取甘露醇的方法),之后逐渐发展为利用蔗糖水解、催化还原工艺以及葡萄糖酶异构化成果葡糖再氢化制取的方法得到甘露醇。
据报道,美国发明一种新的生物法生产甘露醇的方法,比过去氢化法能大幅降低成本。
美国农业部研究中心于2002年与伊利诺斯州一家化学公司进行扩试验证。
2003年这家化学公司从芬兰一生物技术公司取得专利权,用Lactobacillus生产高纯果糖浆,并转化成甘露醇。
2004年伊利诺斯州这家化学公司获FDA批准,生产生物法甘露醇。

【药品名称】通用名:复方甘露醇注射液商品名:丰海露英文名:Compound Mannitol Injection汉语拼音:Fufang Ganluchun Zhusheye【药品介绍】本品为复方制剂,其组份为:甘露醇、葡萄糖和氯化钠。
[性状]本品为无色的澄明液体。
[药理毒理]复方甘露醇注射液是高渗制剂,通过高渗性脱水产生直接的药理作用,消除脑水肿,能使脑水分含量减少,降低颅内压。
主要成份甘露醇为单糖,在体内不被代谢,经肾小球滤过后在肾小管内极少被重吸收,起到渗透利尿作用。
(1)组织脱水作用。
提高血浆渗透压,导致组织内(包括眼、脑、脑脊液等)水份进入血管内,从而减轻组织水肿,降低眼内压、颅内压和脑脊液容量及其压力。
1g甘露醇可产生渗透浓度为5.5m0sm,注射100g甘露醇可使2000ml细胞内水转移至细胞外,尿钠排泄50g。
(2)利尿作用。
甘露醇的利尿作用机制分两个方面:①甘露醇增加血容量,并促进前列腺素I2分泌,从而扩张肾血管,增加肾血流量包括肾髓质血流量。
肾小球入球小动脉扩张,肾小球毛细血管压升高,皮质肾小球滤过率升高。
②本药自肾小球滤过后极少(<10%)由肾小管重吸收,故可提高肾小管内液渗透浓度,减少肾小管对水及Na+、Cl-、K+、Ca2+、Mg2+和其它溶质的重吸收。
由于输注甘露醇后肾小管液流量增加,当某些药物和毒物中毒时,这些物质在肾小管内浓度下降,对肾脏毒性减小,而且经肾脏排泄加快。
葡萄糖是人体主要的热量来源之一,每1克葡萄糖可产生4千卡(16.7千焦)热能,用来补充热量,另外也有一定的组织脱水作用。
钠和氯是机体重要的电解质,主要存在于细胞外液,对维持人体正常的血液和细胞外液的容量和渗透压起着非常重要的作用。
正常血清钠浓度为135~145mmol/L,占血浆阳离子的92%,总渗透压的90%,故血浆钠量对渗透压起着决定性作用。
正常血清氯浓度为98~106mmol/L。
人体主要通过下丘脑、垂体后叶和肾脏进行调节,维持液体容量和渗透压的稳定。

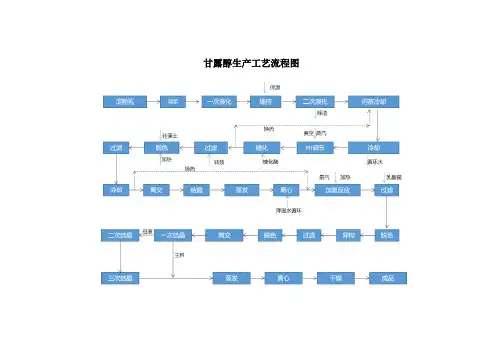
甘露醇生产工艺流程图
甘露醇生产工艺说明
1、生产甘露醇的原料可以是淀粉,葡萄糖,山梨醇,这些都是在一条生产链条上的产品。
2、在加氢反应之前的反应可以被认为是生产葡萄糖的反应。
3、在这个过程中,需要好几次的升温和降温,这里面需要注意换热,在降温过程中的热量为升温过程的环节预热,达到合理和节约利用能量的效果。
4、甘露醇生产中比较重要的工序是糖化工序,液化工序,加氢工序,结晶工序和离子交换工序。
5、加氢反应工序完毕之后的液体中,含有两种成分,分别是甘露醇和山梨醇,二者是同分异构体,甘露醇非常容易结晶,而甘露醇比较难以结晶,为此可以设置温度的差异,令甘露醇析出,而山梨醇留在母液中。
6、甘露醇一次析出的母液中还含有一定量的甘露醇,才需要进行三次结晶,然后离心干燥。
7、甘露醇是一种降压药的原料,可以降低颅脑压力,为颅脑外伤手术的必备药物。
8、甘露醇由于比较容易结晶,因此在浓度较大的时候,例如蒸发后工段,如果保温不好,容易堵住管线,因此在工艺处理中需要特别注意,尤其是在停车的时候,或者阶段性地停用管线的时候,需要注意用蒸汽置换。

甘露醇的制备甘露醇的制备背景甘露醇又名虫草酸,其含量一直是评价虫草质量的一个重要指标。
据报道冬虫夏草甘露醇含量为7%一29%bJ。
甘露醇保肺气,止血化痰,镇咳,是虫草有敬成分之一【4],现在甘露醇已作为人工发酵虫草的质量控制指标之一。
比色法测定甘露醇方法简便快速,特异性高,许多含羟基的物质乜括单糖对其无明显干扰。
试验步骤1试验材料1.1虫革来源。
九州虫草菌丝体、子座.蛹虫草子座,冬虫夏草菌丝体由山东大学微生物国家重点实验室提供,经60℃烘F、磨细而成。
1.2仪器。
分光光度计分析天平。
1.3试剂。
高碘酸钠,L鼠李糖.乙酸胺,冰醋酸,甘露醇,均为APt。
2试验方法2. 1样品制备。
精确称取样品(九州虫草子座,九州虫草菌丝体,蛹虫草子座,冬虫夏草菌避体)各2.5 g,分别用75【ld蒸馏水100℃水浴提取2 h,过滤,定容至100 ml,备用。
2.2试剂配置。
①Nash试剂:精确称取乙酸胺150 g,蒸馏水溶解,加入2 ml冰醋酸.2 ml乙酰丙酮,定容至1 000 ml。
②0.015 rml/1.高碘酸钠:精确称取高碘酸钠3.2 g容于0.12mol/L HCI,定容至1 000 ml。
③O.1%L鼠李糖:精确称取I,鼠李糖0.1 g,蒸馏水溶解,定容至100ml。
④甘露醇标准品溶液。
精确称取甘露醇标准品100 tag,溶于蒸馏水,定容至100ml,即为1 mg/m_l甘露醇标准溶液,分装为10 r出瓶。
2 3方法。
取菌粉样品溶液0.03 ral,补水至1 ml或甘露醇标准品溶液1 ml加人试管中,空白对照管加蒸馏水1 ml,然后加入0.015 mal/L高碘酸钠液I瑚,混匀,室温放置lOlllin,每个试管加0.1%鼠李糖2 ml,充分混匀后,加入№8Il试剂4 Trd,53℃水浴保温15min,即刻冷却,分光光度计413m处测光吸收,根据甘露醇标准品的光吸收计算样品中的甘露醇含量。
2.4标准曲线绘制:在分光光度计4t3 rim处,以甘露醇溶液为标样,利用高碘酸钠与甘露醇反应产生黄色的3,5一二乙酰.1,4脱氢二甲基吡啶,此显色化台物在波长413 nlll处有最大吸收,对应溶液浓度得到OD值。

甘露醇的生产方法1、生产方法甘露醇的生产方法颇多,但大部分产物都不是纯净物,而是山梨醇和甘露醇的混合物,如要得到单一产品,必须经过分离提纯。
1.1 海带提取法海带提取法是我国目前生产甘露醇的主要方法,是在海带提取碘及海藻酸钠后的废水中提取甘露醇,约10 t海带可得1t甘露醇。
该法可得到单一的甘露醇,免去了与山梨醇分离这一工序,精制纯度高,但该法收率低,精制手续麻烦,同时生产成本高,原料来源受地区、季节限制。
具体工艺过程:①干海带浸泡搓洗。
②用氢氧化钠溶液调pH,使胶状物沉淀,③用硫酸酸化清液,进一步除胶状物。
④清液蒸发,除盐,结晶,离心分离,得甘露醇粗制品。
⑤精制。
⑥在90℃左右烘干,即得药用甘露醇(99.08%)。
1.2 以蔗糖为原料的催化氢化法蔗糖水溶液加酸水解成葡萄糖和果糖,进行催化氢化反应,葡萄糖转化为山梨醇,果糖转化为大致等量的山梨醇和甘露醇。
实际产物中,山梨醇占80%,甘露醇占20%。
一般5.2t白糖可得到1t甘露醇,联产山梨醇4t。
该法以充足价廉的蔗糖为原料,工艺可靠,原料利用率高,与海带提取法相比,成本低,产品质量好,且原料不受地区季节限制。
工艺过程:①加热搅拌使蔗糖溶于清水,用HCl调pH,温度控制为90~105℃,保持1~2h,冷却备用。
②糖水经阴/阳离子交换树脂提纯,进入氢化釜催化氢化。
③进行真空浓缩、结晶、离心分离,得粗甘露醇,母液即为工业山梨醇。
④粗甘露醇二次结晶、离心分离、烘干、粉碎、过筛,得工业级甘露醇。
1.3 其他方法如:葡萄糖电化学还原、生物酶一化学催化剂共同作用制甘露醇、利用D-葡萄糖异构化、氢化制备甘露醇、从咖啡渣中提取、从生产右旋糖苷的废液中提取、利用微生物发酵、催化异构山梨醇。

20%甘露醇注射液配制工艺探讨摘要:目的:提高过滤速度;提高甘露醇注射液的澄明度合格率和减少药液结晶;提高甘露醇注射液的澄明度合格率、降低细菌内毒素阳性率。
方法:通过改进配制工艺中药用炭的使用方法,在过滤前先使用钛棒过滤器吸附一层药用炭起到助滤作用(即打炭底);分次吸附;改变过滤器的孔径。
结果:将药用炭量加大(0.3%~0.5%)和采用分次加入后,次日结晶率为1%,3个月后结晶为3%,6个月后结晶率为5%;药用炭量以0.3%~0.5%为宜,煮沸时间以10min为宜,药用炭量在20%甘露醇注射液过饱和溶液中显得更为主要。
结论:加大药用炭量;较少结晶;不宜选用非PVC软袋包装输液袋;生产环境和操作方法的控制,减少不溶性微粒的引入。
关键词:20%甘露醇注射液;配制;工艺1.1标准背景在《中国药典》2015年版二部中,20%甘露醇注射液的配制工艺[1]为:按处方计算称取甘露醇,投入浓配罐溶于适量的注射用水中,不断搅拌至甘露醇完全溶解,煮沸15分钟,降温至80℃再投入药用炭吸附10分钟,药液经5μm钛棒脱炭过滤至稀配罐内,加注射用水至总体积,用药用级稀盐酸或2mol/L氢氧化钠溶液调节PH至5.5~6.0,搅拌回流25分钟,取样测定药液PH值、含量,符合规定后,冷却药液至60℃以下,经聚醚砜微孔滤芯(0.45μm和0.22μm)折叠过滤器精滤后供灌装。
1.2工艺背景我公司依法配制时,常受下列情况困扰:因甘露醇浓度较高易结晶,常粘附于滤芯和管道影响滤速,甚至堵塞;澄明度合格率低;细菌内毒素阳性率高;甘露醇注射液结晶率高,临床使用不便等。
尽管甘露醇注射液属于过饱和溶液,出现结晶是正常现象,但我在长期工作实践中发现,以上现象的出现同配制工艺不当有很大关系,为此改进了此工艺。
2.1研究对象为了生产过程中提高过滤速度;提高甘露醇注射液的澄明度合格率和减少药液结晶;提高甘露醇注射液的澄明度合格率、降低细菌内毒素阳性率。

小容量注射剂的工艺流程设备及要求下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!小容量注射剂的工艺流程、设备及其要求小容量注射剂,通常是指容量在5毫升以下的注射液,广泛应用于医疗领域。
2.2甘露醇注射液详细处方、生产工艺、药品标准
与上次注册内容的比较
1. 甘露醇注射液的处方、生产工艺与上次注册内容没有改变。
2. 甘露醇注射液的药品标准与上次注册内容比较:
甘露醇注射液2002年注册时执行的标准为《中国药典》2000年版二部,现执行标准为《中国药典》2005年版二部。
2.3 药品处方和生产工艺真实性承诺书
根据河南省食品药品监督管理局《关于印发<河南省药品再注册工作方案>的通知》(豫食药监注〔2009〕212号)的要求,我公司对已申请并受理的再注册品种甘露醇注射液按要求重新进行了整理上报,保证提供的药品处方和生产工艺真实。
如有不实,由此引发的一切后果由本公司承担。
企业法人代表(签字)
河南天方药业股份有限公司
二OO九年十二月二十日。
大输液生产工艺规程大输液生产工艺规程大输液生产工艺规程部门:生产部题目:大输液生产工艺规程1/15文件编号:STP-PC-99000(01)新订:替代:起草:部门审阅:审核:批准:执行日:变更记录:修订人:批准执行日:变更原因及目的:目的:建立一个大容量注射液(大输液)生产的通用工艺规程,为车间提供一个通用技术标准适用范围:大输液的生产工艺责任者:生产部经理、输液车间主任、工艺技术员、质监员及操作员内容:一、生产工艺流程图(见下页)。
二、操作过程及工艺条件。
1、制水将饮用水(来自青城山)经石英砂过滤和活性碳过滤去除水中有机质及微粒,经电渗析初步脱盐(脱盐率75±5%后,再经过“阳—阴—阴—混”离子交换柱去离子化制得去离子水,再经过切割分子量为10000(相当于0.001μm)中空纤维滤材组成的超滤系统过滤后制得超纯水(纯化水),再经五效蒸馏水机制造蒸馏水,经微孔滤膜(孔径0.45μm)过滤后制得注射用水。
2、洗瓶将检验合格的输液瓶在车间外脱去外包装(麻袋或纸箱),在玻瓶进入口处转入周转箱中,运至理瓶室理瓶机旁,逐一上瓶于转盘上,开动外洗瓶机,淋水下对玻瓶进行外刷洗,同时灌入约100ml自来水,传送至内洗瓶(粗洗)机,先用0.5%NaOH 洗刷,再用自来水洗刷,再用自来水洗刷,最后用纯化水大输液生产工艺规程部门:生产部题目:大输液生产工艺规程2/15文件编号:STP-PC-99000(01)新订:替代:起草:部门审阅:审核:批准:执行日:变更记录:修订人:批准执行日:变更原因及目的:胶塞隔离膜输液瓶原辅料饮用水↓瓶外清洗碱酸处理乙醇浸泡↓称量离子交换清洁剂处理↓饮用水初洗蒸馏水清洗刷洗内壁浓配去离子水↓饮用水清洗蒸馏水煮沸蒸馏水清洗↓过滤蒸馏水去离子水清洗↓蒸馏水清洗注射用水清洗注射用水清洗稀配注射用水↓注射用水清洗粗滤精滤灌装放膜注射用水清洗上胶塞翻塞盖铝盖铝盖轧口出厂入库包装贴签灯检灭菌注:洁净级别100级1万级10万级大输液生产工艺规程部门:生产部题目:大输液生产工艺规程3/15文件编号:STP-PC-99000(01)新订:替代:起草:部门审阅:质量审核:批准:执行日:变更记录:修订人:批准执行日:变更原因及目的:药液经中间检验各项指标合格后输送至灌装机,开机灌装入洁净的输液瓶中,立即盖薄膜,膜必须放正,然后对准膜中心,垂直塞入胶塞,经翻塞机翻塞后传送到轧盖。
小容量注射剂的灌装生产工艺流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!小容量注射剂的灌装生产工艺流程详解小容量注射剂,作为一种常见的药物制剂形式,广泛应用于医疗领域。
甘露醇注射液生产工艺流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!甘露醇注射液生产工艺流程一、前期准备阶段。
在开始甘露醇注射液的生产之前,有诸多准备工作需要完成。
质量标准文件编号页码共3页第1页文件名称甘露醇质量标准版次01制定人制定日期审核人审核日期批准人批准日期颁发部门GMP办公室颁发日期执行部门质管部、供应部、生产部、仓储部生效日期分发部门:GMP办公室、质管部、供应部、生产部、仓储部取代:【药品名称】甘露醇【产品代号】【依据】中国药典2015年版二部(P124)、中国药典2015年版四部通则本品为D-甘露糖醇。
按干燥品计算,含C6H14O6应为98.0%~102.0%。
【性状】本品为白色结晶或结晶性粉末;无臭。
本品在水中易溶,在乙醇中略溶,在乙醚中几乎不溶。
熔点本品的熔点(中国药典2015年版四部通则0612)为166~170℃。
比旋度取本品约1g,精密称定,置100ml量瓶中,加钼酸铵溶液(1→10)40ml,再加入0.5mol/L的硫酸溶液20ml,用水稀释至刻度,摇匀,在25℃时依法检查(中国药典2015年版四部通则0621),比旋度为+1370~+1450。
【鉴别】(1)取本品的饱和水溶液1ml,加三氯化铁试液与氢氧化钠试液各0.5ml,即生成棕黄色沉淀,振摇不消失;滴加过量的氢氧化钠试液,即溶解成棕色溶液。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集1238图)一致。
【检查】酸度取本品5.0g,加水50ml溶解后,加酚酞指示液3滴与氢氧化钠滴定液(0.02mol/L)0.30ml,应显粉红色。
溶液的澄清度与颜色取本品1.5g,加水10ml溶解后,溶液应澄清无色;如显浑浊,与1号浊度标准液(中国药典2015年版四部通则0902第一法)比较,不得更浓。
有关物质取本品,加水溶解并稀释制成每1ml中含50mg的溶液,作为供试品溶液;质量标准文件编号页码共3页第2页文件名称甘露醇质量标准版次01精密量取1ml,置100ml量瓶中,用水稀释至刻度,作为对照溶液;另取甘露醇与山梨醇各0.5g,置100ml量瓶中,加水溶解并稀释至刻度,作为系统适用性试验溶液。
技术标准本品为甘露醇的灭菌水溶液。
1 品名:甘露醇注射液2 剂型:大容量注射剂3 规格:250ml:50g4 代码:Y4065 处方:5·1基准处方甘露醇200.0 g注射用水加至1000 ml5·2 标准生产量:1800000 ml/批所用的原辅料及数量名称代码数量甘露醇Y103 360.0 Kg针用活性炭F101 900g注射用水F108 至1800000 ml6 生产工艺及操作要求:6·1 配制(万级、温度18~26℃、湿度45~65%):本工序包括称量、浓配、稀配等。
6·1·1 称量:在备料间根据指令核对原辅料品名、规格、批号、生产厂家、数量,与本公司检验报告单一致。
称量前校准天平、电子秤并检查是否在效期内。
按处方要求进行原辅料的称量,并填写称量记录。
剩余原辅料扎紧袋口,标明原辅料名称、批号、剩余量、使用人,放置于暂存架。
换品种清场时,将剩余料密封,贴上卡片,标明名称、规格、批号、数量、日期,退回脱包间,返至仓库。
6·1·2 浓配:取规定量甘露醇在浓配间投入到放有适量注射用水(80~90℃)的SH-Ⅰ浓配罐中,搅拌溶解,使成50%~60%的浓溶液,加0.03%(g/ml,以稀配体积计) 针用活性炭,搅拌混匀,煮沸(100℃)15-20分钟,用钛棒过滤器加压过滤,内循环10分钟,泵入稀配罐。
6·1·3 稀配:在稀配间向SH-Ⅰ稀配罐中加注射用水至全量的约80%,加0.02%(g/ml,以稀配体积计)的针用活性炭,补加注射用水至全量,搅拌、回流15分钟,测pH值(规定:5.0~5.5,若不符合规定用稀盐酸或1M氢氧化钠调整)、含量(98.5%~102.5%)符合规定后,降温至60~70℃,用钛棒过滤器和0.65μm的膜滤芯加压过滤,终端用0.65μm的膜滤芯过滤至灌装。
生产结束后,操作者做好清场卫生工作(按清场操作规程和配制灌装系统清洗消毒规程),并做好记录。
6·2 制袋灌封(万级下的百级,温度18~26℃、相对湿度45~65%):用SRD4A 型非PVC膜软袋大输液生产线操作。
6·2·1上膜将检验合格的三层共挤输液用膜放置到膜架上,由开卷架完成自动送膜工作。
6·2·2 印字设置印版(内容包括产品名称、规格、批号、生产日期、有效期等),核对品名、规格、批号、生产日期、有效期等是否正确,开机进行试操作,检查打印的位置和清晰程度,确保准确无误。
印刷工位属于热转印技术,主要是通过加热加压的办法使色带上的颜料与色带基材剥离,转于三层共挤输液用膜的外表面,附着结合,从而在软袋的外面印上与药品有关的内容。
印字温度145~170℃,印字时间0.02秒,印字压力0.25-0.40MPa。
6·2·3 开膜和塑料输液容器接口的预热三层共挤输液用膜经过设备上的开模器时,膜的一侧被打开;同时塑料输液容器接口从料盘经传送装置输送到接口预热器,预热温度120-140℃,预热时间约为1.1秒。
6·2·4 袋周边焊接和塑料输液接口焊接三层共挤输液用膜经过焊接模具时,模具的上下两个部分对接,经加热加压,完成膜的周边焊接,热合温度125-145℃,热合时间约1.0秒;该工序热合的时间、压力、温度可调。
可根据情况调节操作参数,以便获得最佳的热合效果。
6·2·5 接口焊接和袋体冷却经预热的塑料输液接口被放入膜的开口侧,经加热加压,完成接口与膜的焊接,焊接温度135-150℃,压力为0.25-0.40MPa。
同时袋体进入冷却模具,冷却水进入冷却模具夹层。
6·2·6 接口冷却接口进入冷却模具,冷却水进入冷却模具夹层,冷却时间1.0秒。
6·2·7去除废边由机械手撕拉,去除废边。
6·2·8 软袋传送:已制成的空袋用一个机械夹具送入灌装设备的夹具中,被确认为坏袋的袋子将被自动剔除,落入坏袋收集盘中。
灌装前称量前四个袋重并记录,取平均值为单个袋重,并核对前四袋印字内容是否正确、清晰。
6·2·9 灌封:自动灌装,每袋250~255ml 。
待药液冷却到60-70℃时通过灌装系统灌装药液,由中心定位装置对灌装软管定中心,当灌装嘴到达最底极限位置时,对管的长度进行检查,并检查是否有口管存在。
如果出现错误信号,相应的灌装位将不执行灌装此袋。
该工位下移时,灌装嘴插入袋子的口管中,灌装阀即时打开,将药液灌入袋子中,达到灌装量时,质量流量计给出信号经控制系统将灌装阀关上,灌装头在驱动机构的带动下向上运动,结束灌装。
灌装过程中质监员每30分钟抽查一次装量和可见异物并记录,每次抽查4袋,装量用称重方式检查。
生产结束后,操作者做好清场卫生工作(按清场操作规程),并做好记录。
6·2·10加盖聚丙烯输液容器拉环式密封盖由带有震荡盘和线性盖加料滑槽的料斗自动送入。
经真空装置被放置在袋的口管的顶部。
加热片在盖和口管之间移动,用于非接触式加热,同时,要进行排气,以便把袋中的剩余空气量降至适量。
灌装好的袋加压直到一个固定液位。
最后,加热片缩回,盖放置在口管上。
如果袋没有灌装,袋将不会封口加盖,无盖的袋将被剔除。
6·2·11出袋灌封药液后的袋子经主传送机构从口管固定夹中滑出,落在出袋轨道上,送入上袋工序。
6·3上袋将灌封药液后的袋子摆放在灭菌车上,平铺摆放整齐,车满后每车贴上灭菌指示带,注明品名、规格、批号并挂待灭菌标示卡。
生产结束后,做好清场和卫生工作,并做好记录。
6·4 灭菌:在灭菌岗灭菌操作者检查装车排列是否整齐,检查蒸汽、压缩气、压力是否符合规定,电开关、灭菌柜情况,按灭菌岗操作规程将小车推入柜内,关闭灭菌柜门, 用SG-35型水浴式灭菌柜操作。
灭菌条件:115℃,30分钟,压力0.20MPa,F0≥8。
待灭菌温度达到恒定后,操作人员每10分钟检查一次灭菌温度与压力,探头容器每批一换。
灭菌结束后按操作法开门,拉出已灭菌产品。
无菌取样每柜取30袋。
生产结束后,操作者做好清场卫生工作(按清场操作规程),并做好记录。
6·5 卸袋检漏:6·5·1 卸袋操作人员根据指示带上的内容,按批号、车号的顺序拉车,不得混批。
核对灭菌指示带效果和标示卡后,撕下灭菌指示带,贴在第一袋待灯检产品上,将待灯检产品送上输送轨道,输送到RJL检漏机上进行检漏。
生产结束后,操作者做好清场卫生工作(按清场操作规程),并做好记录。
6·5·2检漏调整压轮左右位置到检漏的合适位置并调整好压轮转速,进行检漏。
检漏合格的产品通过输送带送至灯检岗位进行灯检;不合格产品挑出并计数。
每班生产结束后将不合格品拉到车间外的垃圾箱按不合格品管理规程处理。
生产结束后做好清场和卫生工作(按清场操作规程),并做好记录。
6·6 灯检:在灯检操作间灯检操作工核对产品名称、规格、批号、灭菌指示带效果后,按灯检岗位操作规程在RDJ灯检机上进行逐袋目检。
先检查袋的周边焊接、焊口是否有破裂和渗漏、打印是否清晰,然后检查可见异物。
灯检合格产品用玻璃铅笔(红、黄、绿、蓝、白、黑色)划上个人色标后,送包装工序;不合格品按白点、白块、色块、纤维、漏气、其它等分类统计后送车间不合格品存放间。
每班生产结束后将灯检不合格品拉到车间外的垃圾箱按不合格品管理规程处理。
生产结束后做好清场和卫生工作(按清场操作规程),并做好记录。
6·7 包装:250ml/袋×40袋/箱在包装室操作工将用DXD450下走膜多功能枕式板块全自动包装机塑封好的产品放入箱内,并随时检查品名、批号内外是否相符,放入说明书、合格证后,用FX450半自动封箱机封箱。
取样每批随机抽取27袋。
零头产品要求两个相邻批号一个合箱,在外包装上加盖“M”印章,并注明全部批号。
包装结束后准确统计包材的领用数、使用数、残损数及剩余数,并做好记录。
残损包材按规定处理。
生产结束后,操作者做好清场卫生工作(按清场操作规程)。
6·13 1800000 ml/批标准生产量所用包装材料的名称、代码及数量7物料、中间产品、成品的质量标准和技术参数及贮存注意事项7·1物料、中间品和成品的质量标准情况7·2 物料的质量标准和技术参数及贮存注意事项7·2·1 甘露醇代码:Y1037·2·1·1质量标准:应符合《中国药典》2010年版二部“甘露醇”项下规定:[性状] 本品为白色结晶或结晶性粉末;无臭、味甜。
本品在水中易溶,在乙醇中略溶,在乙醚中几乎不溶。
本品的熔点为166~170℃。
比旋度为+137°至+145°[鉴别] 应符合规定;[检查] 酸度应符合规定溶液的澄清度与颜色应符合规定有关物质应符合规定还原糖应符合规定氯化物应符合规定硫酸盐应符合规定草酸盐应符合规定炽灼残渣不得过0.1%干燥失重不得过0.5%重金属不得过百万分之十砷盐应符合规定[含量测定] 本品为D—甘露糖醇,按干燥品计算,含C6H14O6应为98.0%~102.0%。
7·2·1·2 贮藏:遮光,密封保存。
7·2·2 注射用水代码:F1087·2·2·1质量标准:应符合《中国药典》2010年版二部“注射用水”项下各项规定:[性状] 本品为无色澄明液体,无臭、无味。
[检查] pH值 5.0~7.0氨应符合规定硝酸盐应符合规定亚硝酸盐应符合规定电导率应符合规定总有机碳应符合规定不挥发物应符合规定重金属应符合规定细菌内毒素每1ml含内毒素量应小于0.25EU微生物限度细菌、霉菌和酵母菌总数每100ml不得过10个7·2·2·2 贮存注意事项:70℃以上保温循环,贮存时间不超过12小时。
7·2·3 针用活性炭代码:F1017·2·3·1质量标准:符合《中国药典》2010年版二部“药用炭”项下规定:[性状] 本品为黑色粉末;无臭,无味;无砂性。
[鉴别] 应符合规定。
[检查] 酸碱度应符合规定氯化物应符合规定硫酸盐应符合规定未碳化物应符合规定酸中溶解物遗留残渣不得过10mg干燥失重减失重量不得过10.0%炽灼残渣遗留残渣不得过3.0%铁盐应符合规定锌盐应符合规定重金属不得过百万分之三十吸着力应符合规定7·2·3·2 贮藏:密封保存。