湖南省长郡中学2019届高三上学期第五次月考化学试题扫描版含解析 (1)
- 格式:doc
- 大小:2.13 MB
- 文档页数:9

2021年高考化学总复习:过氧化钠性质的考查1.[2019江苏] 下列有关化学反应的叙述正确的是A.Fe在稀硝酸中发生钝化B.MnO2和稀盐酸反应制取Cl2C.SO2与过量氨水反应生成(NH4)2SO3D.室温下Na与空气中O2反应制取Na2O2明确过氧化钠的生成条件,掌握过氧化钠的电子式、过氧化钠与水及二氧化碳反应的实质,反应中的氧化剂、还原剂及转移电子数目。
氧化钠和过氧化钠物质氧化钠过氧化钠色、态白色固体淡黄色固体化学式Na2O Na2O2类别碱性氧化物过氧化物氧元素的化合价-2 -1稳定性较稳定稳定与H2O反应的方程式Na2O + H2O = 2NaOH 2Na2O2+2H2O = 4NaOH + O2↑与CO2反应的方程式Na2O + CO2 =Na2CO32Na2O2 + 2CO2 =2Na2CO3 + O2氧化性、漂白性无有用途制NaOH 呼吸面具、漂白剂一、考查Na2O2的制备典例1下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),生成物并不改变的有()组①NaHCO3溶液和NaOH溶液②Na和O2③NaOH和CO2④Na2O2和CO2⑤NaAlO2和HCl ⑥Na2CO3溶液和盐酸A.1组B.2组C.3组D.4组二、考查Na2O2的结构典例2(广西钦州市2019届高三4月综合能力测试三模)下列关于钠及其化合物的说法正确的是A.过氧化钠的电子式:B.金属钠可用来除去苯中的少量水分C.常温下Na与O2反应生成Na2O,随温度升高生成Na2O的速率加快D.测Na2CO3和Na2SiO3溶液的pH,可确定碳和硅两元素的非金属性强弱三、Na2O2在阿伏加德罗常数中的考查典例3(2018届辽宁省重点高中协作校高三第三次模拟考试)设N A为阿伏加德罗常数的数值。
下列说法不正确的是A.23gCH3CH2OH与30gCH3COOH反应,生成CH3COOCH2CH3的分子数为0.5N AB.15.6g由Na2S和Na2O2组成的混合物中,含有的阴离子数目为0.2N AC.32.5g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.5N AD.过量MnO2与浓盐酸反应产生1molCl2,转移的电子数目为2N A四、Na2O2与CO2、H2O反应的考查典例4(湖南省长沙市长郡中学2019届高三上学期第五次调研考试)如图装置中,容器甲内充入0.1 mol NO气体。

湖南省长郡中学2019届高三第五次月考化学试题及答案一、选择题(本题共16小题,每小题3分,共48分,每小题只有一个选项符合题意)1.下列说法错误的是A.浓氨水可用于检验氯气管道是否漏气B.明矾可用作除去污水中悬浮颗粒的絮凝剂C.Si用于制造光导纤维D.硬铝、青铜和不锈钢都属于合金2.下列试剂中,不会因为空气中的氧气而变质的是A.亚硫酸钠B.漂白粉C.硫酸亚铁D.氢硫酸3.某溶液中可能含有OH-、CO-23、AlO-2、SiO-23、SO-24、Na+、Mg2+、Al3+八种离子中的几种。
当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸的体积的变化如下图所示。
南此可知原溶液中A.不含SO-24B.含有的阴离子一定是OH-、AlO-2、SiO-23C.含有的阴离子一定是OH-、CO-23、AlO-2、SiO-23D.含有的AlO-2与SiO-23的物质的量之比为3:14.利用下图所示装置进行下列实验,能得出相应实验结论的是5.下列措施不合理的是A.用SO2漂白纸浆和草帽辫B.用硫酸清洗锅炉中的水垢C.高温下,用焦炭还原SiO2制取粗硅D.用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+6.有100 mL 3 mol·L-1NaOH溶液和100 mL l mol·L-1AlCl3溶液。
按如下两种方法进行实验:①将氢氧化钠溶液分多次加到AlCl3溶液中;②将AlCl3溶液分多次加到NaOH溶液中。
比较两次实验的结果是A.现象相同,沉淀量相等B.现象不同,沉淀量不等C.现象相同,沉淀量不等D.现象不同,沉淀量相等7.,嫦娥三号着陆器与巡视器分离,“玉兔号”巡视器顺利驶抵月球表面。
“玉兔”号是中国首辆月球车,成功实现对月面的科学探测。
“玉兔”号用23994Pu作为热源材料。
下列关于23994Pu的说法正确的是A.23894Pu写23994Pu具有相同的最外层电子数B.23894Pu与23994Pu互为同素异形体C.23894Pu与23892U具有完全相同的化学性质D.23894 Pu与23892U互为同位素8.下列有关物质性质的说法错误的是A.热稳定性:HCl>HBr>HIB.原子半径:Na>Mg>AlC.还原性:PH3>H2S>HC1D.结合H+能力:ClO->HCO-3>SiO-239.下列实验现象及相关的离子方程式均正确的是A.Cl2与FeI2溶液反应,当n(C12):n(FeI2)=1:1时:2Fe2++2I-+2C12 2Fe3++I2 +4C1-B.向Ba(NO3)2溶液中通人SO2气体,出现白色沉淀:Ba2++SO2+ H2O BaSO3↓+2H+C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2 MnO4+7 H2 O2+6 H 2Mn2++6O2↑+10 H2OD.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合: Ba2++SO-24+H++OH BaSO4↓+H2O10.下列各组离子中,能在指定溶液中大量共存的是①无色溶液中:K+、Cl-、Na+、HCO-3、OH-②使pH试纸变深蓝色的溶液中:K+、CO-23、Na+、AlO-2③由水电离出的c(H+)=10-12 mol·L-l的溶液中:ClO-、HCO-3、NO-3、NH+4④加入Mg能放出H2的溶液中:Mg2+、NH+4、Cl-、Na+、SO-24⑤使甲基橙变红的溶液中:MnO-4、NO-3、SO-24、Na+、Fe3+⑥pH=0的溶液中:Fe2+、Al3+、NO-3.Cl-、SO-23A.①③ B.②④⑤ C.①②⑤ D.③⑥11.N A代表阿伏加德罗常数的值,下列说法正确的是A.1 mol FeCl3完全水解生成N A个胶体粒子B.常温常压下,23 g NO2放置一段时间后分子总数小于0.5N AC.标准状况下,2.24 L CCl4中含有的C-Cl键数为0.4N AD.6.8 g熔融态KHSO4.中含有0.1N A个阳离子12.物质的量浓度相同的下列溶液:①Na2 CO3;②NaHCO3;③H2 CO3;④(NH4)2 CO3;⑤NH4 HCO3,按c(CO-23)由小到大排列顺序正确的是A.⑤<④<③<②<① B.③<⑤<②<④<①C.③<②<⑤<④<① D.③<⑤<④<②<①13.部分弱酸的电离平衡常数如下表:下列说法正确的是A.0.1 mol·L-l NaHCO3溶液中各离子浓度的大小顺序为:c( Na+)>c(HCO-3)c(HJ-)>c(OH-)B.少量的CO2通人到NaCN溶液中:CN-+H2 O+CO2 HCN+HCO-3C.用0.1 mol·L-l NaOH溶液中和等浓度的HCN溶液和HCOOH溶液时,前者所需NaOH溶液体积大D.相同体积的0.1 mol·L-l HCOONa溶液比0.1 mol·L-l NaCN溶液所含离子总数小14.下列有关溶液中微粒浓度关系的叙述正确的是A.c(NH+4)相等的(NH4)2 SO4、NH4HSO4、NH4Cl三种溶液中:c( NH4HSO4)>c[(NH4)2 SO4] >c(NH4Cl)B.已知HF的酸性比CH3 COOH的强,pH相等的NaF与CH3 COOK两种溶液中:c(Na+)-c(F-)<c(K+)-c(CH3 COO-)C.向醋酸钠溶液中加入适量醋酸,得到的酸性混含溶液中:c(CH3 COO-)>c(Na+)>c( H+)>c(OH-)D.溶有等物质的量NaClO、NaHCO3的溶液中:c( HClO)+c(ClO-)=c(HCO-3)+c(H2 CO3)+2 c(CO-23)15.在可逆反应2 A(g)+3B(g) xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为 5 m01·L-l, B为 3 mol·L-l,前 2 min内,用C表示的平均反应速率为0.5 mol·L-l·min-1。


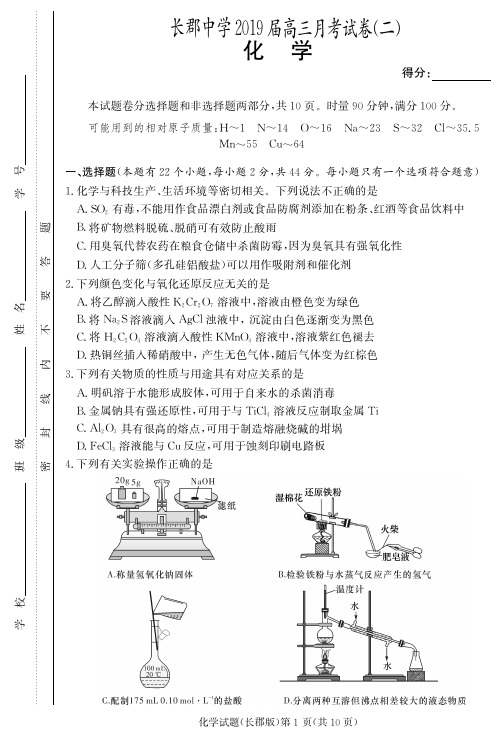

2019届湖南省长沙市长郡中学高三上学期第五次调研考试化学试题化学注意事项:1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
一、单选题1.化学与生产、生活、社会密切相关,下列说法正确的是A.常用危险化学品标签中的阿拉伯数字主要表示的是危险级别B.石油裂化和裂解制取乙烯、丙烯等化工原料不涉及化学变化C.误食重金属盐引起的人体中毒,可以喝大量的食盐水解毒D.少量的生石灰能作为鸡舍和猪栏的消毒剂2.设N A为阿伏加德罗常数的值,下列说法不正确的是A.31 g白磷()含有共价键的总数为1.5N AB.常温下,22.4 mL H2O中所含氢氧键的数目约为2.49N AC.8.7 g MnO2与40 mL 10 mol·L-1的浓盐酸充分反应,生成的氯气分子数为0.1N AD.常温下,1 L pH=11的Na2CO3溶液中由水电离出的H+数目为0.001N A3.部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92 g,经如下处理:下列说法正确的是①滤液A中的阳离子为Fe2+、Fe3+、H+ ;②样品中氧元素的物质的量为0.03 mol;③溶解样品的过程中消耗硫酸的总物质的量为0.04 mol;④V=224;⑤V=336。
A.①③④B.②③④C.②③⑤D.①③⑤4.下列化学用语的表述正确的是A.葡萄糖的实验式:CH2O B.NaClO的电子式:C.甲烷分子的球棍模型:D.次氯酸的结构式:H—Cl—O 5.有X、Y 、Z、M、N五种物质,进行的有关实验操作及现象如下:实验操作实验现象①气体X和气体Y混合气体变红棕色②Y、M、N分别与氢硫酸反应都产生淡黄色固体③用玻璃棒蘸取Z和M的浓溶液,相互靠近产生白烟④Z和N分别通入少量溴水中溴水都变成无色透明的液体X、Y、Z、M、N依次可能是A.NO、O2、NH3、HNO3、SO2B.O2、NO、NH3、HCl、SO2C.O2、NO、HCl、NH3、CO2D.NO、O2、NH3、HCl、CH46.如图装置中,容器甲内充入0.1 mol NO气体。
2018—2019学年高三第五次调研考试化学试卷一、选择题(本大题共22小题,每小题2分,共44分。
在每小题给出的四个选项中,只有一项是符合题意的)1•化学与生产、生活、社会密切相关,下列说法正确的是A. 常用危险化学品标签中的阿拉伯数字主要表示的是危险级别B. 石油裂化和裂解制取乙烯、丙烯等化工原料不涉及化学变化C. 误食重金属盐引起的人体中毒,可以喝大量的食盐水解毒D. 少量的生石灰能作为鸡舍和猪栏的消毒剂【答案】D【解析】A.常用危险化学品标签中的阿拉伯数字是危险化学品分类的危险特性分类号,错误; B.裂解、裂化均属于化学变化,错误; C.喝食盐水并不能解毒,应及时饮用大量牛奶,错误;D•生石灰与水反应能生成强碱且放热,可以使蛋白质变性,正确。
2. (2019湖南长沙长郡中学)设N A为阿伏加德罗常数的值,下列说法不正确的是A. 31 g白磷()含有共价键的总数为1. 5N AB. 常温下,22. 4 mL H2O中所含氢氧键的数目约为2. 49N AC. 8. 7 g MnO2与40 mL 10 mol L —1的浓盐酸充分反应,生成的氯气分子数为0. 1N AD. 常温下,1 L pH = 11的Na2CO3溶液中由水电离出的H+数目为0. 001N A【答案】C【解析】A.1mol白磷中含有6mol共价键,故31g白磷d )含有共价键的总数为1.5N A,正确;B.常温下m 22.4inL x Ig/cm"22.4mL水的物质的量. ….,故22.4 mL H2O中所含氢氧键的数目约为 2.49N A,M 18gmol正确;C. 4HCl(浓)+ Mn O2旦M nCl2+ 2出0+ CM,0.1mol Mn O2与0.4mol浓盐酸反应,因随着反应的进行,该反应将不再发生,故无法计算生成的氯气分子数目,错误;D.该溶液中N (OH-)=10-3N A,因Na2CO3 溶液中的OH-全部是水电离出来的,且水电离出的H+与OH-总量相等,故该溶液中水电离出H+数目为0.001N A。
2018—2019学年高三第五次调研考试化学试卷一、选择题(本大题共22小题,每小题2分,共44分。
在每小题给出的四个选项中,只有一项是符合题意的)1.化学与生产、生活、社会密切相关,下列说法正确的是A. 常用危险化学品标签中的阿拉伯数字主要表示的是危险级别B. 石油裂化和裂解制取乙烯、丙烯等化工原料不涉及化学变化C. 误食重金属盐引起的人体中毒,可以喝大量的食盐水解毒D. 少量的生石灰能作为鸡舍和猪栏的消毒剂【答案】D【解析】A. 常用危险化学品标签中的阿拉伯数字是危险化学品分类的危险特性分类号,错误;B.裂解、裂化均属于化学变化,错误;C.喝食盐水并不能解毒,应及时饮用大量牛奶,错误;D.生石灰与水反应能生成强碱且放热,可以使蛋白质变性,正确。
2.(2019湖南长沙长郡中学)设N A为阿伏加德罗常数的值,下列说法不正确的是A. 31 g白磷()含有共价键的总数为1.5N AB. 常温下,22.4 mL H2O中所含氢氧键的数目约为2.49N AC. 8.7 g MnO2与40 mL 10 mol·L-1的浓盐酸充分反应,生成的氯气分子数为0.1N AD. 常温下,1 L pH=11的Na2CO3溶液中由水电离出的H+数目为0.001N A【答案】C【解析】A.1mol白磷中含有6mol共价键,故31g白磷()含有共价键的总数为1.5N A,正确;B.常温下22.4mL水的物质的量,故22.4 mL H2O中所含氢氧键的数目约为2.49N A,正确;C. 4HCl(浓)+MnO2MnCl2+2H2O+Cl2↑,0.1mol MnO2与0.4mol浓盐酸反应,因随着反应的进行,该反应将不再发生,故无法计算生成的氯气分子数目,错误;D.该溶液中N(OH-)=10-3N A,因Na2CO3溶液中的OH-全部是水电离出来的,且水电离出的H+与OH-总量相等,故该溶液中水电离出H+数目为0.001N A。