物质组成的表示方法
- 格式:docx
- 大小:20.58 KB
- 文档页数:8


第四节物质组成的表示方法学习目标:1、知识与技能:(1)能正确书写化学式,知道化学式的含义,并能进行命名。
(2)能根据化学式进行各元素质量比、某元素的质量分数的简单计算。
2、过程与方法(1)结合具体物质,让学生理解化学式反映物质的组成;任何纯净物都有固定的组成。
(2)其次,让学生根据化合价正确书写化学式,并学会命名,熟练掌握化学用语。
(3)从量的角度深化对化学式的理解,对物质组成的认识。
这些质量关系为①化合物中各元素的质量比。
②某元素的质量分数。
3、情感态度价值观:培养定量处理事物的能力。
教法分析:化学式在前面的教学中也出现了多次,难点是化合价的引出。
建议:淡化化合价的概念,重点应在指导学生记忆常见化合价上。
化学式的读写,直接影响化学方程式的记忆,不少学生由于化学式读写没有真正过关,导致在学习化学方程式时出现死记符号的现象。
所以,一定要在读写上多花一点功夫,让学生养成习惯。
有关化学式的计算要让学生知道运算原理和运算方法。
重点:1、记忆常见化合价2、化学式的书写和读法3、根据化学式的简单计算难点:化合价的引出、化学式的书写和根据化学式的计算课时安排3课时第1课时:化学式反映物质的组成、化合价由学生自己书写已经认识的化学式。
【设问】指出大家已经对一些物质有了认识,从中你发现了什么问题?【讨论】组成物质的元素不同,化学式中的元素符号就不同,但是为什么有的化学式中元素右下角有数字,有的没有?【讲述】不同的物质分别有不同的化学式,化学式中的这些不同是怎么来的?P78页图3-24。
从17世纪以来,科学家就不断地对物质的组成进行研究,从最初的测定物质在化学反应中的质量关系对物质组成作出推测,到今天用现代仪器测定物质的组成,人们对物质组成奥秘有了一个较深的认识:任何纯净物都有固定的组成,化学式是物质组成的反映。
阅读P78——P79,完成下表:【阅读】p79联想与启示:通过上述练习,在头脑中建立了关系:物质化学式【提问】化学式的含义是什么?【练习】1、H2除了表示氢气外,还可以表示:①氢元素;②一个氢分子;③两个氢元素;④氢气是由氢元素组成;⑤每个氢分子由两个氢原子构成;⑥两个氢原子。


第三节物质组成的表示方法一.化学式反映物质的组成小结:纯净物都有固定的组成,化学式是物质客观组成的反映,化学式还能反映物质的微观构成情况,是国际通用的化学语言,一种物质只能有一种化学式。
1、化学式:就是用元素符号和数字的组合来表示纯净物组成的式子。
提出的依据:任何纯净物都有固定的组成,不同的物质组成不同。
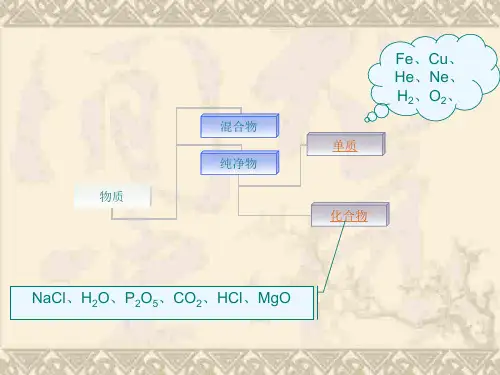
①.单质化学式的写法小结:金属单质、稀有气体、一些固态的非金属单质(如碳、硅、硫、磷等)直接用元素符号表示化学式,如铝Al、铁Fe、氖气Ne。
由分子构成的单质,则在元素符号右下角标出分子中所含原子的数目,如氧气O2、臭氧O3、氮气N2、氯气Cl2、足球烯C60、氢气H2 。
②.化合物的化学式写法物质名称所含原子或离子个数比化学式氧化铜Cu、O 1∶1 CuO氯化钙Ca2+、Cl 1∶2二氧化硅Si、O 1∶2碳酸钙Ca2+、CO32- 1∶12、化学式表示的意义议一议:“CO2”能表示哪几层含义?(1)表示二氧化碳这种物质;(2)表示二氧化碳由碳、氧两种元素组成;(3)表示一个二氧化碳分子;(4)表示一个二氧化碳分子由一个碳原子和两个氧原子构成。
小结:化学式表示的意义:(1)表示一种物质;(2)表示该物质由哪些元素组成;(3)表示该物质的一个分子或原子;(4)表示该物质的一个分子的构成。
练习:(1)用化学用语表示:五个水分子;10个氢气分子;铜;一氧化碳;四氧化三铁;氖气。
(2)写出下列符号中数字的含义:2H2SO4第一个2表示,氢右下角的2表示,氧右下角的4表示。
(3)维生素C的化学式为C6H8O6,关于“C6H8O6”表示的意义正确的是()A.表示维生素C这种物质B.表示维生素C由碳、氢、氧三种元素组成C.表示1个维生素C分子D.表示维生素C由6个碳原子、8个氢原子、6个氧原子构成二.如何书写化合物的化学式想一想:根据下列物质的化学式,找一找元素符号编写顺序有什么规律?氧化铝Al 2O 3、氯化钙CaCl 2、水H 2O 、二氧化碳CO 2、碳酸钙CaCO 3指出:书写化合物的化学式必须知道化合物由哪些元素组成、原子或离子的个数比,同时还应了解符号的编写顺序。


§3-4 物质组成的表示方法(一)一、学习目标:1、能说出物质化学式的含义;2、熟记常见元素的化合价及常用原子团;3、会根据元素及原子团化合价书写离子符号;二、教学重点、难点:常见元素的化合价及常用原子团化合价的熟记、正确书写化学式。
三、教学流程:(第一课时:化学式反映物质的组成、化合价)§3-4 物质组成的表示方法(二)一、学习目标:1、通过练习掌握化合价、化学式的表示;2、会根据化合价书写一般物质化学式;3、会根据化学式确定元素的化合价;4、了解化合物的命名。
二、教学重点、难点:掌握化学式的的含义§3-4 物质组成的表示方法(三)——根据化学式计算(第一课时)一、学习目标:1、学会根据化学式计算各原子的质量比;2、学会根据化学式计算纯净物中某元素的质量比。
二、教学重点、难点:根据化学式计算各原子的质量比、计算纯净物中某元素的质量比。
一、学习目标:1、加强相对分子质量、元素原子质量比、某元素的质量分数的计算训练。
2、不纯净物中元素质量分数、元素质量的计算。
二、教学重点、难点:物质中元素质量的计算一、教学目标了解不纯物的有关计算二、教学重点、难点:不纯物中元素质量分数的理解与应用三、教学过程:不纯物中,某纯物质的质量分数=混合物的质量纯物质的质量×100%公式转化:纯物质的质量=混合物的质量×某纯物质的质量分数混合物的质量=某纯物质的质量分数纯物质的质量练习:例1 硝酸铵样品中含有杂质10%(杂质中不含氮元素),求样品中氮元素的质量分数设不纯的硝酸铵中氮元素的质量分数为x ,则有如下关系:例2 某不纯的尿素[CO(NH2)2]中氮元素的质量分数为42.4%,求这种尿素中杂质(不含氮元素)的质量分数。
设不纯的尿素中含尿素的质量分数为x ,则有如下的关系。




物质组成的表示方法〖知识要点〗一、化学式反映物质的组成1、化学式:用元素符号和数字组合表示纯净物组成的式子,叫做化学式。
注意:任何纯净物都有固定的组成,不同的物质组成不同,化学式是对物质组成情况的真实反映。
2、化学式的涵义:(1)宏观上:a、表示一种物质;b:表示该物质由哪些元素组成。
(2)微观上:a、表示该物质的一个分子;b:表示一个分子里含有多少原子。
3、单质化学式的书写:(1)金属单质及稀有气体单质是由原子直接构成的。
因此它们的化学式直接用元素符号来表示,如铁用“Fe”表示,氦“He”用表示,常温下为固态的大多数非金属单质,由于它们的结构比较复杂,化学式也用元素符号来表示,如碳“C”用表示,磷用“P”表示。
(2)常见气态非金属单质,大多数是由两个原子构成一个分子(即双原子分子),它们的化学式是在其元素符号的右下角加小数字,以表示它们的组成,如氧气“O2”用表示;氢气用“H2”表示。
二、如何书写化合物的化学式1、化合价(1)在化合物中,不同元素原子的数目有确定的比值关系,体现这种关系的数值就是元素的化合价。
(2)常见元素和原子团的主要化合价常见元素的化合价口诀:氢钾钠银正一价;钙镁钡锌正二价;正三铝,氧负二,单质永远是零价。
常见原子团的化合价口诀:负一硝酸氢氧根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根。
(3)化合价的表示方法通常标在元素符号或原子团的正上方,且“+”或“-”号写在前,价数写在后。
例,常见的正价元素:……常见的负价元素:……常见原子团化合价:……2、化合物化学式的书写:(1)写化学式时,正价元素通常写在左边,负价元素写在右边,原子的数目用阿拉伯数字写在元素符号的右下角;(2)在金属化合物中,金属元素一般呈正价,非金属元素一般呈负价,在非金属氧化物中,非金属元素一般呈正价;(3)根据化合物中各种元素化合价的代数和等于零的原则,确定化合物中各种元素的原子数目。
注意:化学式只能表示物质的组成,用化合价法则推算化学式,只有在该化合物实际存在时才有意义,不能根据化合价凭空臆造,随意书写化学式。
【高中化学】化学知识物质组成的表示方法总结任何纯净物都有固定的组成,一种物质只能有一个化学式。
一般来说,一些简单物质是由原子组成的,如金属、稀有气体、钻石等。
对于由原子组成的简单物质,其化学式直接由元素符号表示。
有的单质由分子构成,如氢气、氮气、氧气、氯气,它们的每一个分子中都含有2个原子,称为双原子分子,它们的化学式:先写出元素符号,在元素符号的右下角加上数字“2”。
例如氢气:h2。
当元素相互结合形成化合物时,所含原子或离子的数量比是固定的。
这个数比反映了元素的性质——价。
会根据化合物中化合价的代数和等于零的原则书写化学式即可。
该公式可用于记忆常见元素或原子团的化合价:一价钾钠氢氯银,二价钙镁钡锌氧铝、硅、铁、碳二四六硫都齐全,铜汞二价最常见常见原子团的价态:负一硝酸氢氧根负硫酸氢碳酸盐正一价的是铵根原子团:在化学反应中,并非所有时间都作为一个整体参与反应;原子团不能单独存在,必须与其他原子或原子团结合才能成为物质的化学式。
化合价只有在元素之间形成化合物时才能表现出来的,当元素以单质的形式存在时,其化合价一定为零。
根据化合价写出化学式是学习化学的基础。
如果你不能熟练地写出化学式,你就不能写出化学方程式供以后学习。
它的重要性不言而喻。
写化学公式是一项技能。
技能的培养在于更多的实践。
反复练习,熟能生巧。
一般来说,书写化学式的正确顺序是:正价前,负价后;金属左,非金右,氧化物中氧在后。
① 当原子团簇的数量为1时,1被省略,不需要写在括号中;如果原子簇的数量是2或3,则原子簇被括在括号中,数字标记在括号的右下角。
②+2价的铁称亚铁。
③ 事实上不存在的物质的化学式不能根据化合价随机生成。
物质组成的定量表示方法物质(matter)是宇宙中最基本的构成单位,由原子或原子核组成,它构成了宇宙中所有的物理和化学物质,是各种化学物质的基本材料,是各种能量的媒介。
定量表示物质组成的方法,也即是表示某一物质各种化学组分在其中的多少比例,是现代化学中一个重要的内容。
现代化学中可以用不同的方法表示物质组成。
其中最常见的一种是分子式,分子式表示某一物质中所含原子的种类及其数量。
例如,水分子中包含二个氢原子和一个氧原子,它的分子式是H2O。
此外,也可以用摩尔质量来表示物质组成,即所有原子的质量总和,通常以g/mol或kg/mol表示。
例如,水的摩尔质量为18.02g/mol。
当物质的组成中包含成分复杂,比如液体或溶液时,用百分比表示其组成物质也是一种有用的方法。
百分比表示其中某种物质占其中总物质的百分比,一般用百分比记法来表示。
例如,水溶液中含有5%的醋酸,则可以表示成5% CH3COOH。
此外,也可以用摩尔浓度来表示物质组成,即某种物质在某一体积or某一质量中所含有的某种物质的数量,一般用mol/L或mol/kg 表示。
例如,某溶液中醋酸的摩尔浓度为0.5mol/L,则表示每升溶液中有0.5mol的醋酸分子。
另外,也可以使用其它的定性和定量分析方法来表示物质组成,例如,石英晶体的结构可以用X射线衍射分析(X-ray diffraction)的方法来表示;药物的测定可以采用液相色谱法(HPLC);对某种物质的检查可以用紫外分光光度法(UV-visible spectroscopy)等等。
总之,以上提到的多种方法可以用来表示物质组成,而不同表示方法各有优劣,也适用于不同的物质组成。
因此,当我们研究物质的内部组成时,应根据实际的情况,选择最合适的表示方法来进行研究,以取得最恰当的结果。
物质组成的表示方法
第四节物质组成的表示方法
知识与技能:
能说出化学式的含义;能依据物质组成、利用元素化合价书写常见物质的化学式;能根据化学式进行物质组成的简单计算。
过程与方法:
逐步形成对事物进行抽象概括和定量处理的能力。
情感态度价值观:
养成尊重客观实际,认真、严谨的科学态度。
学习目标:
1.能说出化学式的含义;
2.能依据物质组成、利用元素化合价书写常见物质的化学式;
3.能根据化学式进行物质组成的简单计算。
过程与方法:
逐步形成对事物进行抽象概括和定量处理的能力。
情感态度价值观:
养成尊重客观实际,认真、严谨的科学态度。
内容要点:
1.通常用化学式表示物质的组成。
2.可以利用元素化合价书写化学式。
3.写化学式时,正价元素通常写在左边,负价元素通常写在右边。
原子的数目用阿拉伯数字写在元素符号的右下角。
在金属化合物中,金属元素一般呈正价,非金属元素一般呈负价;在非金属氧化物中,非金属元素一般呈正价。
根据化合物中各种元素化合价的代数和等于零的原则,确定化合物中各种元素原子的数目。
4.简单化合物的中文命名原则。
5.两种元素组成的化合物,在两种元素中间用“化”字连接,如氧化铜(CuO)。
6.化学式中元素的名称从右向左读,与化学式的写法刚好相反,如氯化钠(NaCl)。
7.元素的原子个数在该元素之前先读出,如五氧化二磷(P2O5)。
8.含有复杂原子团的化合物,要根据其特征来称呼,不需读出原子或原子团的个数,如氢氧化钠(NaOH)、碳酸钙(CaCO3)、硫酸钠(Na2SO4)等。
教学内容:
一、化学式反映物质的组成
1、化学式(formular),就是用元素符号和数字的组合来表示纯净物组成的式子。
提出的依据:任何纯净物都有固定的组成,不同的
物质组成不同。
2、化学式所表示的含义(一般包括宏观和微观角度)
微观上:表示某物质;表示该物质由哪些元素组成的。
宏观上:表示该物质的一个分子或者一个原子;由分子构成的物质,还可以表示一个分子的构成情况。
我们以水(H2O)为例说明
化学式的涵义以H2O为例
宏观表示一种物质表示水这种物质
表示该物质有哪些元素组成的表示水由氧元素和氢
元素组成的
微观表示该物质的一个分子表示一个水分子
表示一个分子里有多少个原子表示一个水分子中由
2个氧原子和1个原子构成
质量表示物质的相对分子质量
Mr(H2O)=2Ar(H)+Ar(O)=2+表示物质中各种元素的原子个数比水中氢元素和氧元素的原子个数比为2:1 表示物质中各种元素的质量比水中氢元素和氧元素
的质量比为1:8
3、化学式中元素符号周围的数字的意义,如 aRbc a表示有a个这样的微粒
b 表示一个微粒中有b个原子或原子团
c 表示一个该离子中带有c个正(负)电荷
如:3H2SO4 Ca2+表示钙离子,一个钙离子带2个单位的正电荷
注意:同元素符号的意义相似,在化学式前有数字后,就不能表示宏观含义,只能表示微观含义
二、如何书写化合物的化学式
1、各种物质的化学式都是通过实验方法测定出来的,一种纯净物只能由一个化学式来表示,不能主观臆造。
2、化合价。
大量的化合物中不同元素的原子数目中都是一个固定的比值,体现这种关系的数值就是化合价某种元素的化合价数值与它原子的最外层电子数是密切相关的。
3、单质的化学式的写法
(1)金属单质、固体非金属单质、稀有气体单质用元素符号表示。
如金属单质:Fe(铁)、Na(钠);固体非金属:S(硫)、P(磷)等;稀有气体:He(氦)、Ne (氖)等
(2)氧气等多原子分子构成的单质,在元素符号的右下角添上下标,表示一个分子含有多少个该原子。
如:O2(氧气)、O3(臭氧),Cl2(氯气)
4、化合物的化学式的写法——根据化合价来写化学式
(1)一般是正价的元素(或原子团)写在左边,负价元素(或原子团)写在右边。
(2)在金属化合物中,金属元素一般呈正价,非金属呈负价;在化合物中,氧元素一般呈-2价,氢元素一
般呈+1价。
(3)化合物中,各种元素化合价的代数和为零。
+2 注意:(1)标注某元素的化合价时,务必要写在该元素符号的正上方,先标电性,后标数目,如 CuO
+2表示在氧化铜中铜元素呈+2价
(2)某些元素具有可变价态,它们表示在与其他元素化合形成化合物时,会出现多种可能。
特别:Fe 在命名时,+3价就是铁,而在+2价时要被称为亚铁
补充:初中一般常见的原子团及化合价
原子团化学式化合价原子团化学式化合价
氢氧根OH-1硝酸根NO3-1
碳酸氢根HCO3-1高锰酸根MnO4-1
碳酸根CO3-2锰酸根MnO4-2
氯酸根ClO3-1硫酸根SO4-2
磷酸根PO4-3亚硫酸根SO3-2
氨根NH4+1
识记:课本P80的常见元素的化合价
三、简单化合物的命名
1、两种元素组成的化合物的命名
根据元素的名称,从右往左读作“某化某”。
如NaCl 读作“氯化钠”,ZnO读作“氧化锌”,Fe3O4读作“四氧化三铁”。
但要注意,H2O就是“水”,不能读成“氧化氢”,NH3就是“氨气”。
2、含有OH原子团的化合物的命名:一般命名为“氢氧化某”
如:NaOH读作“氢氧化钠”,Cu(OH)2读作“氢氧化铜”
3、含有其他原子团的化合物的命名:一般根据原子团和另一元素的名称从右到左的顺序读作“某酸某”。
如:CaCO3读作“碳酸钙”,Cu(NO3)2读作“硝酸铜”
但注意,H2CO3就读作“碳酸”,H2SO4就读作“硫酸”等。
4、某些比较复杂物质的命名
如:Cu2(OH)2CO3读作“碱式碳酸铜”,H2O2读作“过氧化氢”等
四、纯净物中元素之间的质量关系
(1)某物质的相对分子质量的计算:
将化学式中所有的原子的相对原子质量加和,即是
该物质的相对分子质量,如:Ca(OH)2
答:
Mr[Ca(OH)2]=Ar(Ca)+2(Ar(O)+Ar(H))=40+2(16+1)(2)计算化合物中的原子个数之比:
在化学式中,元素符号右下角的数字就是表示该元
素原子的个数,因此这些数字的比值就是化合物中的原
子个数。
如:Fe2O3中,铁原子与氧原子个数比就是2:3,
碳酸钙CaCO3中钙、碳、氧原子个数比为1:1:3 但注意某些物质的化学式中,同种元素并不写在一
起的,这时要注意原子个数。
如:NH4NO3中,氮、氢、氧原子个数比应该为2:4:3
Cu2(OH)2CO3中,铜、碳、氢、氧原子个数比为2:1:2:5
(3)计算化合物中各元素质量之比
在化合物中,各元素质量之比就是各元素的原子个
数与它的相对原子质量积之间的比值
如:氯酸钾(KClO3)中,m(K):m(Cl):m(O)=39:35.5:16×3=78:71:96
硝酸铵(NH4NO3)中,m(N):m(H):m(O)=14×2:1×4:16×3=7::1:12
(4)计算一定质量的物质中某元素的质量
某元素的质量=物质的质量×该元素在物质中的质量分数
如:求60gMgSO4中含有氧的质量
m(O)=m(MgSO4)×ω(O)=60g×53.3%=32g。