醛的化学性质
- 格式:doc
- 大小:29.50 KB
- 文档页数:1


有机化学基础知识点醛的化学性质醛的化学性质醛是有机化合物的一类,它的化学性质主要由其分子结构和官能团决定。
醛具有许多特殊的化学性质,包括氧化性、亲核性、还原性和聚合性等。
在本文中,我们将探讨醛的主要化学性质及其在实际应用中的意义。
一、氧化性醛在氧化剂的作用下,容易被氧化为相应的酸。
常见的氧化剂有氧气、过氧化氢和碳酸盐等。
以乙醛为例,它可以被氧气氧化为乙酸。
这种氧化反应常常是在催化剂的作用下进行,例如使用银盐或铜盐作为催化剂。
氧化反应可以在常温下进行,速度较快,因此在实际应用中具有广泛的用途。
二、亲核性醛中的羰基碳原子具有较强的正电性,易被亲核试剂进攻。
醛与亲核试剂的反应通常发生在羰基碳原子上,形成加成产物。
常见的亲核试剂有水、饱和或不饱和的醇、胺等。
通过与亲核试剂的反应,可以得到相应的醇、醚、胺等有机化合物。
三、还原性醛是容易被还原的化合物,可以被还原剂还原为相应的醇。
常用的还原剂有金属氢化物、金属和碱金属水合物等。
例如,乙醛可以被氢气还原为乙醇。
还原反应通常在催化剂存在下进行,例如使用铂、钯或铑作为催化剂。
四、聚合性醛具有聚合性,可以通过缩合反应形成聚合物。
以甲醛为例,它可以通过缩合反应和环化反应形成三聚甲醛或呋喃醛。
这些聚合物具有重要的应用价值,如三聚甲醛被广泛应用于树脂和建筑材料的生产中。
综上所述,醛的化学性质包括氧化性、亲核性、还原性和聚合性。
这些性质使得醛在有机合成、化工等领域具有重要的应用价值。
通过了解和掌握醛的化学性质,可以更好地理解有机化学的基础知识,为实际的化学研究和应用提供支持。

醛类1 醛类的概述(1)醛的组成和结构名师提醒(1)醛基可写成或—CHO,但不能写成—COH。
(2)醛分子结构中一定含有醛基,但含有醛基的物质不一定是醛。
如甲酸、葡萄糖等都含有醛基,都具有醛的化学性质,但它们都不属于醛。
(2)醛的分类(3)醛的通式一元醛的结构通式是(R为烃基或氢原子)。
饱和一元脂肪醛的通式是C n H2n O(n =1,2,3…)或C n H2n+1CHO(n=0,1,2…)。
注意若烃C n H m衍变为x元醛,该醛的分子式为C n H m-2x O x。
(4)醛的命名注意—CHO中的碳原子一定在1号位,故命名时醛基无需用阿拉伯数字标明位置。
(5)醛的同分异构体类别分析方法举例碳链异构醛基一定连在链端,所以醛分子中烃基的碳链异构有几种,属于醛的同分异构体就有几种丁基(—C4H9)有4种结构,则分子式为C5H10O的有机物属于醛的同分异构体就有4种官能团异构含相同碳原子数的饱和一元醛、饱和一元酮、烯醇、脂环醇和环氧烷互为同分异构体分子式为C3H6O的有机物:属于醛的有CH3CH2CHO,属于酮的有,属于烯醇的有CH2=CH—CH2OH,属于脂环醇的有,属于环氧烷的有注意醛基一定连在链端,所以醛不存在官能团位置异构现象。
2 醛类的物理性质状态常温下,除甲醛是气体外,其余醛类都是无色液体或固体低级醛可溶于水,随着醛中碳原子数的增多,其在水中的溶解度减小,这是溶解度因为极性的—CHO在分子中所占的比例减小熔、沸点通常情况下,随着醛中碳原子数的增多,醛的熔、沸点逐渐升高3 醛类的化学性质醛类的官能团是醛基,与乙醛的结构相似,因而具有类似乙醛的化学性质。
醛基具有还原性,能发生氧化反应[银镜反应、与新制的Cu(OH)2反应、催化氧化反应、被强氧化剂氧化等]和加成反应等。
注意醛在烃的含氧衍生物转化中起桥梁作用,醇、醛、羧酸之间有如下转化关系:R—CH2OH R—CHO R—COOH4 重要的醛(1)甲醛①分子结构分子式电子式结构式结构简式CH2O HCHO甲醛是最简单的醛,通常把它归为饱和一元醛,但分子中又可以看成有2个醛基,其分子结构如图3-3-3所示,甲醛分子中4个原子都在同一个平面上。
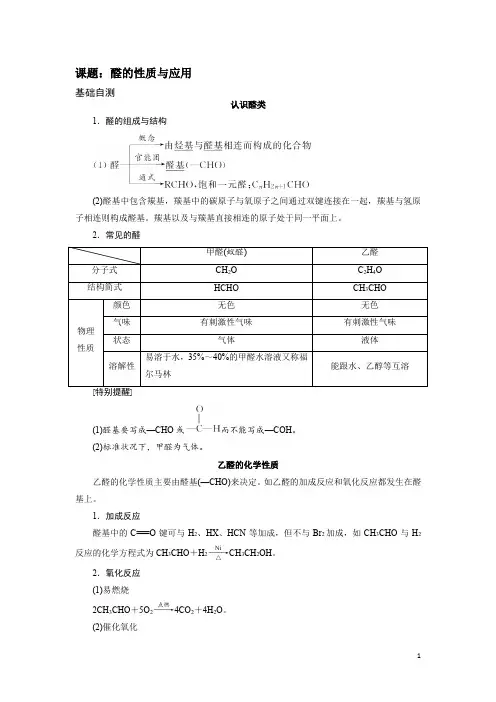
课题:醛的性质与应用基础自测认识醛类1.醛的组成与结构(2)醛基中包含羰基,羰基中的碳原子与氧原子之间通过双键连接在一起,羰基与氢原子相连则构成醛基。
羰基以及与羰基直接相连的原子处于同一平面上。
2.常见的醛(1)醛基要写成—CHO 或而不能写成—COH 。
(2)标准状况下,甲醛为气体。
乙醛的化学性质乙醛的化学性质主要由醛基(—CHO)来决定。
如乙醛的加成反应和氧化反应都发生在醛基上。
1.加成反应醛基中的C===O 键可与H 2、HX 、HCN 等加成,但不与Br 2加成,如CH 3CHO 与H 2反应的化学方程式为CH 3CHO +H 2――→Ni△CH 3CH 2OH 。
2.氧化反应 (1)易燃烧2CH 3CHO +5O 2――→点燃4CO 2+4H 2O 。
(2)催化氧化2CH 3CHO +O 2――→催化剂△2CH 3COOH 。
(3)被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化的化学方程式分别为CH 3CHO +2Ag(NH 3)2OH ――→水浴△CH 3COONH 4+2Ag ↓+3NH 3+H 2O 、 CH 3CHO +2Cu(OH)2+NaOH △,CH 3COONa +Cu 2O ↓+3H 2O 。
(4)乙醛能被酸性KMnO 4溶液或溴水氧化。
醛基的性质(1)能发生氧化反应生成羧基,能与H 2发生加成反应,被还原为羟基。
(2)有机物发生氧化反应、还原反应的判断:(1)银镜反应 ①配制银氨溶液:向AgNO 3稀溶液中逐滴加入稀氨水,直到最初生成的沉淀恰好溶解为止。
AgNO 3+NH 3·H 2O===AgOH ↓+NH 4NO 3 AgOH +2NH 3·H 2O===Ag(NH 3)2OH +2H 2O ②银镜反应示意图:③实验成功的关键: a .试管(玻璃器皿)要洁净。
b .混合溶液的温度不能太高,受热要均匀,以温水浴为宜。
c .在加热过程中,试管不能振荡。


时遁市安宁阳光实验学校高二化学选修5 醛的性质和应用要点:1 醛的命名及结构特点 2 醛的性质:(1)物理性质(2)化学性质:银镜反应与新制Cu(OH)2 悬浊液反应加氢还原制酚醛树脂一 醛的结构及命名1 醛的结构醛 = 醛基(-CHO ) + 烃基(—R )所以醛的结构可以表示为:R -CHO其中若烃基为H 原子或烷烃基,则该醛称为饱和一元醛,具有分子通式:C n H 2n O2 醛基的空间构型醛基:CH O其中C 原子采用sp 2杂化,所以醛基是平面型结构,即羰基以及与羰基直接相连的原子处于同一平面 【问】甲醛的空间构型是怎样的? 平面型 3 醛的命名(1)选取含有醛基(醛基作为主链的一部分)的最长碳链作为主链 (2)醛基参与编号,并且从醛基中的碳原子开始编号(3)根据主链上碳原子的多少称“某醛” 例:给下列有机物命名HCHO CH 3CH 2CHO CH 3CH CH 3CHOCH 3CHCH 2CH 3CHO甲醛 丙醛 2-甲基丙醛 2-乙基丙醛2,3-二甲基-1,4-丁二醛二 醛的性质及应用1 醛的物理性质常温下,甲醛是具有刺激性气味的气体,乙醛是具有刺激性气味的液体,它们都易溶于水。
35%~40%的甲醛水溶液称为福尔马林,可以作为防腐剂和消毒剂。
2 化学性质:(1)银镜反应实验:A 银氨溶液的配置在洁净的试管中加入AgNO 3溶液,再向其中逐滴滴加稀氨水,直至棕色沉淀刚好消失为止【问】在滴加氨水的过程中,开始产生的棕色沉淀是什么?后来怎么又消失了呢?【学生讨论】化学方程式:Ag ++ NH 3·H 2O = AgOH ↓ + NH 4+棕色AgOH + 2 NH3·H2O = [Ag (NH3)2]OH + 2H2O氢氧化银和氨水形成了能溶于水的配合物[Ag (NH3)2]OH,它的水溶液就是银氨溶液。
B 银镜反应向刚配置好的银氨溶液中加入乙醛,振荡,放入热水浴中加热,静置一段时间现象:一段时间候,在试管壁产生一层银镜注意:必须用水浴加热,并且在加热的过程中不能振荡试管化学方程式:CH3CHO + 2[Ag (NH3)2]OH 2Ag↓+ CH3COONH4+ 3NH3+ H2O 【讨论】银氨溶液是一种弱氧化剂,它能把醛基氧化成羧基,这说明醛基具有一定的还原性。

酮与醛的化学性质酮和醛是有机化合物中常见的两类官能团,它们具有许多相似的化学性质,但也存在一些重要的区别。
本文将重点讨论酮与醛的化学性质,并就它们在有机合成和生物体系中的重要性进行探讨。
一、酮与醛的结构酮和醛都含有碳氧双键,但在分子结构上有所不同。
酮分子中,碳氧双键与两个碳原子相连,而醛分子中,碳氧双键与一个碳原子和一个氢原子相连。
这种结构差异对它们的化学性质产生了影响。
二、酮与醛的还原反应酮和醛都可以通过还原反应转化为对应的醇。
还原反应是指通过添加氢化剂,在合适的条件下,将酮或醛中的碳氧双键还原为碳氢单键,生成相应的醇。
在这个过程中,氧原子获得了两个氢原子,形成了醇的羟基。
三、酮与醛的氧化反应与还原反应相反,酮和醛也可以发生氧化反应。
氧化反应是指将酮或醛中的一对氢原子替换为氧原子,形成羰基(C=O)连接的羧酸。
氧化反应可以通过氧化剂的作用实现,例如常用的氧化剂有高锰酸钾、过氧化氢等。
四、酮与醛的亲核加成反应酮和醛都具有活泼的羰基碳,可以发生亲核加成反应。
亲核加成反应是指通过亲核试剂的攻击,将酮或醛中的碳氧双键打开,形成新的碳-亲核试剂结合物。
这种反应常用于有机合成中,可以构建出多样化的有机分子骨架。
酮与醛的一个重要区别是酮分子中羰基碳上的两个碳原子连接其余官能团,这使得酮分子比醛分子更为稳定。
这些不同的化学性质使酮和醛在有机化学和生物化学领域中有着不同的应用。
在有机合成中,酮和醛是重要的中间体。
它们可以作为反应底物,参与到多种有机反应中,如羟醛缩合反应、烯醇化反应等。
同时,酮和醛也可以作为合成目标,通过合适的方法合成出具有生物活性的化合物。
在生物体系中,酮和醛也具有重要的生理功能。
例如,酮体作为能量的替代物质,在饥饿或长时间不摄入碳水化合物时,能够提供给脑部能量。
此外,酮和醛还参与到生物体内的一些重要代谢反应中,如葡萄糖新生途径和脂肪酸合成等。
需要注意的是,酮和醛在一定条件下可以相互转化。
例如,醛可以通过氧化反应生成酮,而酮则可以通过还原反应生成醛。

初中化学知识点归纳醛类和酮类化合物的性质与应用醛类和酮类化合物是化学中常见的有机化合物,在日常生活和工业生产中都有广泛的应用。
本文将对醛类和酮类化合物的性质及其应用进行归纳和介绍。
一、醛类化合物的性质与应用醛类化合物的结构中含有一个碳氧双键和一个碳氢单键。
以下是几种常见的醛类化合物及其性质与应用:1. 甲醛(HCHO):是最简单的醛类化合物,具有刺激性气味,能溶于水。
甲醛可以作为消毒剂使用,在医疗场所和实验室中进行消毒和灭菌。
此外,甲醛还用于制造人造板材和塑料。
2. 乙醛(CH3CHO):有水果和酒类的香味,可以用于食品和饮料添加剂中,使其具有特殊的香味。
乙醛还是合成其他有机物的重要原料,如乙酸、丙酮等。
3. 正丁醛(CH3CH2CH2CHO):是一种液体,有辛辣的味道。
正丁醛可以用作农药的添加剂,也是合成其他化合物的原料。
4. 非醛类卡宾(alkylidene):它们是一类具有双键结构的有机化合物,其中一个碳原子上还有两个取代基。
非醛类卡宾可以用于合成有机合成材料,如合成纤维等。
二、酮类化合物的性质与应用酮类化合物的结构中有一个碳氧双键,但没有碳氢单键。
以下是几种常见的酮类化合物及其性质与应用:1. 丙酮(CH3COCH3):是最简单的酮类化合物,是一种无色液体。
丙酮被广泛应用于溶剂、洗涤剂和化妆品等领域。
2. 甲基乙基酮(CH3COCH2CH3):是一种常见的酮类化合物,常用作溶剂。
甲基乙基酮还可以作为香料的成分,在食品工业中被广泛使用。
3. 顺-己安酮(CH3CO(C6H10O2)CH3):顺-己安酮是一种低毒、环保的溶剂,可以用于涂料、墨水和胶水的制造。
4. 马尾藻酮(Ketone Nates):马尾藻酮是一种具有增塑性和适应力的酮类化合物。
它可以用于塑料、涂料、橡胶和油墨等产品的制造。
醛类和酮类化合物由于其独特的结构和性质,在不同领域都有广泛的应用。
无论是作为溶剂、消毒剂还是合成其他有机化合物的原料,在工业生产和日常生活中都发挥了重要作用。



醛类化合物与醛类的性质与应用醛类化合物是一类有机化合物,其分子结构中含有一个或多个醛基(-CHO)。
醛类化合物的性质与应用广泛,涉及到有机化学、生物化学、医药化学等多个领域。
本文将重点介绍醛类化合物的性质与应用,以及它们在实际生活和工业中的应用。
一、醛类化合物的性质1. 结构特点醛类化合物的分子结构中,碳原子与一个氢原子和一个醛基(-CHO)相连。
醛基的存在使得醛类化合物具有特殊的性质。
2. 物理性质由于醛类化合物分子中含有极性的醛基,因此大多数醛类化合物具有较高的沸点和溶解度。
此外,醛类化合物也具有一定的活性,易于发生化学反应。
3. 化学性质醛类化合物是一类多功能化合物,它们既可以作为醛还原剂参与氧化还原反应,也可以作为醛试剂参与取代反应、加成反应、缩合反应等。
二、醛类化合物的应用1. 工业应用醛类化合物在工业生产中有广泛的应用。
例如,甲醛是一种重要的工业原料,用于生产合成树脂、染料和药物等。
乙醛是一种用途广泛的溶剂和去除剂,被广泛应用于制药、农药和化妆品等领域。
2. 生物化学应用醛类化合物在生物化学研究中起着重要的作用。
例如,甲醛可以作为组织固定剂,用于细胞和组织的固定和保存;乙醛是一种常用的脱水试剂,用于制备电子显微镜的标本。
3. 医药化学应用许多醛类化合物在医药化学中具有重要的应用价值。
例如,肝素是一种醛类多糖,被广泛用于抗凝血药物中。
醛类药物还用于治疗心血管疾病、抗癌药物的合成等。
4. 有机合成应用醛类化合物在有机合成中被广泛应用。
它们可以作为重要的合成中间体,参与多种有机反应,如羟醛的巴别夫反应、醛的缩聚反应等。
醛类化合物还可通过催化加氢、氧化反应等进行结构改造,合成出具有重要药理活性的化合物。
5. 日常生活中的应用醛类化合物也存在于日常生活中的许多物质中。
例如,酒精是一种醛类化合物,被广泛应用于消毒、清洁和饮料制作。
香料中也含有许多醛类化合物,给人以芳香的感觉。
三、总结醛类化合物作为一类重要的有机化合物,在各个领域中都有广泛的应用。
化学醛和醛类化合物的性质和应用化学醛和醛类化合物是一类重要的有机化合物,具有独特的结构和性质。
它们在自然界和人类社会中广泛存在,并具有重要的应用价值。
以下是关于化学醛和醛类化合物的性质和应用的详细介绍:1.结构与命名:醛类化合物的结构特点是含有醛基(-CHO),它由一个碳原子、一个氢原子和一个双键氧原子组成。
醛基连接在有机分子的链或环上,形成不同的醛类化合物。
根据醛基连接的原子或基团的不同,醛类化合物可以分为饱和醛、不饱和醛等。
醛类化合物的命名通常以“醛”结尾,前面加上其相应的碳链或环的名称。
2.物理性质:醛类化合物通常具有刺激性气味,具有一定的挥发性。
它们的沸点较低,易挥发。
饱和醛的熔点较高,而不饱和醛的熔点较低。
醛类化合物的溶解性通常较好,易溶于有机溶剂。
3.化学性质:醛类化合物具有较强的化学活性,易于发生加成反应、氧化反应等。
它们可以与醇反应生成缩醛,与卤素反应生成卤代烃,与氨反应生成酰胺等。
醛类化合物还可以被氧化剂氧化为相应的羧酸。
醛类化合物在工业和日常生活中有广泛的应用。
它们可以用作溶剂、香料、塑料添加剂、药物合成的中间体等。
例如,乙醛是合成塑料和合成纤维的重要原料;甲醛在制药工业中用于生产抗生素和维生素等。
大多数醛类化合物具有一定的毒性,对人体和环境有害。
它们可以通过呼吸道、皮肤等途径进入人体,对内脏和神经系统产生损害。
因此,在使用和处理醛类化合物时,应采取适当的安全措施,避免吸入、接触和摄入。
综上所述,化学醛和醛类化合物是一类具有独特结构和性质的有机化合物。
它们在自然界和人类社会中广泛存在,并具有重要的应用价值。
然而,由于其毒性和危害性,使用和处理醛类化合物时应谨慎,并采取相应的安全措施。
习题及方法:1.习题:写出下列化合物的名称:a)CH3CHOb)C6H5CHOc)CH3CH2CHOd)CH3CHO的名称为乙醛e)C6H5CHO的名称为苯甲醛f)CH3CH2CHO的名称为丙醛2.习题:下列哪个化合物属于醛类化合物?a)CH3COOHb)CH3CHOc)C6H5COOH选项b) CH3CHO属于醛类化合物,因为它含有醛基(-CHO)。
醛的性质1.醛类的物理性质常温下,除甲醛是气体外,其余醛类都是无色液体或固体。
随着碳原子数的增多,醛类的熔、沸点逐渐升高;在水中的溶解度逐渐减小,因为极性的—CHO在分子中所占的比例减小。
2.醛类的化学性质(以乙醛为例)醛类的化学性质主要由醛基(—CHO)决定。
醛基中的羰基()具有不饱和性,能与某些物质发生加成反应;中的H原子受羰基()影响,较活泼,使醛基易被氧化成羧基()。
(1)氧化反应①被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化a.实验探究教材P57实验3-5 银镜反应AgNO3+NH3·H2O===AgOH↓+NH4NO3AgOH+2NH3·H2O===Ag(NH3)2OH+2H2OCH3CHO+2Ag(NH3)2OH2Ag↓+CH3COONH4+3NH3+H2O名师提醒银镜反应实验过程中的注意点1.试管要洁净,否则会生成黑色疏松的银沉淀而不是光亮的银镜,可在实验前先用NaOH溶液洗涤试管,再用蒸馏水洗净试管。
2.银氨溶液必须现配现用,不可久置。
3.配制银氨溶液是向AgNO3溶液中逐滴加入稀氨水至最初生成的沉淀恰好溶解为止,滴加顺序不能颠倒,氨水不能过量,否则,最后得到的不是银氨溶液。
4.银镜反应要在碱性条件下进行,且需水浴加热;若用酒精灯直接加热,因受热不均匀,会有黑色的银生成。
5.实验结束后,试管内壁上附着的单质银可用稀硝酸进行洗涤。
6.该反应在实验室可用于检验醛基的存在。
b.实验探究教材P57实验3-6 与新制的Cu(OH)2反应2NaOH+CuSO4===Cu(OH)2↓+Na2SO4CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O名师提醒乙醛与新制的Cu(OH)2反应实验的注意点1.Cu(OH)2必须是新制的。
2.制取Cu(OH)2时,NaOH溶液一定要过量,保证所得溶液呈碱性,因为乙醛与新制的Cu(OH)2的反应要在碱性条件下进行。
高中化学:醛的性质知识点一、醛的结构与常见的醛1.概念醛是由烃基与醛基相连构成的化合物。
2.结构特点醛类官能团的结构简式是—CHO,饱和一元醛的结构通式为CnH2nO(n≥1)或CnH2n+1CHO。
3.常见的醛(1)甲醛:又名蚁醛,是结构最简单的醛,结构简式为HCHO。
通常状况下是一种无色有刺激性气味的气体,易溶于水。
它的水溶液又称福尔马林,具有杀菌、防腐性能等。
(2)乙醛:分子式为C2H4O,乙醛的结构简式为CH3CHO,是一种无色有刺激性气味的液体,密度比水小,沸点是20.8 ℃,易挥发,易燃烧,能跟水、乙醇等互溶。
二、醛的化学性质——以乙醛为例1.氧化反应(1)可燃性乙醛燃烧的化学方程式:2)催化氧化乙醛在一定温度和催化剂作用下,能被氧气氧化为乙酸的化学方程式:(3)与银氨溶液反应(4)与新制氢氧化铜反应5)乙醛能被酸性高锰酸钾溶液、溴水等强氧化剂氧化。
2.加成反应(还原反应)乙醛中的碳氧双键和烯烃中的碳碳双键性质类似,也能与氢气发生加成反应,化学方程式为3.醛的化学通性(1)醛可被氧化为羧酸,也可被氢气还原为醇,因此醛既有氧化性,又有还原性,其氧化、还原的关系为(2)有机物的氧化、还原反应①氧化反应:有机物分子中失去氢原子或加入氧原子的反应,即加氧去氢。
②还原反应:有机物分子中加入氢原子或失去氧原子的反应,即加氢去氧。
醛与弱氧化剂发生化学反应的注意事项(1)银镜反应①试管内壁必须洁净;②银氨溶液随用随配,不可久置;③水浴加热,不可用酒精灯直接加热;④醛用量不宜太多;⑤不可搅拌、振荡。
(2)与新制的Cu(OH)2反应①Cu(OH)2必须用新配制的;②配制Cu(OH)2时,所用NaOH必须过量;③反应液必须直接加热煮沸。
方法规律(1)只要有机物的分子中含有—CHO,就能发生银镜反应,也能被新制Cu(OH)2悬浊液氧化。
(2)银氨溶液或新制Cu(OH)2悬浊液为弱氧化剂,不能氧化碳碳双键,但溴水或KMnO4酸性溶液为强氧化剂,可氧化—CHO,故应先检验—CHO再检验碳碳双键。
醛的化合价
(原创版)
目录
1.醛的定义和性质
2.醛的化合价的概念
3.醛的化合价的计算方法
4.醛的化合价在化学反应中的应用
正文
醛是一种有机化合物,其分子中含有一个或多个羰基(C=O)与一个氢原子(-H)相连。
醛具有刺激性气味,通常为液体或气体。
醛广泛存在于植物中,是许多生物过程的重要组成部分。
醛的化合价是指醛分子中各原子的价态。
在醛分子中,氧原子的化合价通常为 -2,氢原子的化合价为 +1,而羰基上的碳原子的化合价则因醛的种类和反应条件而异。
计算醛的化合价,通常需要根据反应条件和反应物的价态进行。
在许多情况下,醛的化合价可以通过实验方法和计算方法得出。
例如,在氧化还原反应中,醛的化合价可以通过观察反应物和产物的价态变化来确定。
在理论计算中,可以采用量子化学方法来计算醛的化合价。
醛的化合价在化学反应中具有重要意义。
它可以影响反应的速率和选择性,以及反应产物的性质。
例如,在加成反应中,醛的化合价可以决定反应的方向和产物的结构。
在氧化还原反应中,醛的化合价可以影响反应的电子转移过程和反应的能量变化。
总之,醛的化合价是醛分子中各原子价态的总和,它对醛的性质和反应具有重要影响。
第1页共1页。
醛
一、选择题(每小题有一个或两个.....
选项符合题意。
) 5.有机物甲可氧化生成羧酸,也可还原生成醇,由甲生成的羧酸和醇在一定条件下,可以生成化合物乙,其分子式为C 2H 4O 2。
下列叙述中正确的是 ( )
A 甲分子中C 的质量分数为60%
B 甲在常温常压下为无色液体
C 乙比甲的沸点低
D 乙和甲的实验式相同
6.下列各组混合物中,只要总质量一定,不论以何种比例混合,完全燃烧产生的CO 2和H 2O 均为一恒
量的是( )
A .乙炔和苯酚
B .甲醛和丙酸
C 甲烷和乙烷
D .甲醛和甲酸甲酯
7.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。
二甘醇的结构简式是HO —CH 2CH 2—O —CH 2CH 2—OH 。
下列有关二甘醇的叙述正确的是( )
A .不能发生消去反应
B .能发生取代反应
C .能溶于水,不溶于乙醇
D. 不能氧化为醛 10. 乙烯酮(2CH =C =O )在一定条件下能跟含活泼氢原子的化合物发生加成反应,反应的通式可表示为
试指出,下列反应不合理的是 A 、COCl CH HCl O C CH 32−−−−→−+==一定条件
B 、COOH CH O H O
C CH 322−−−−→−+==一定条件
C 、OH CH COCH CH OH CH CH O C CH 223232−−−−→−+==一定条件
D 、O CO)(CH COOH CH O C CH 2332−−−−→−+==一定条件
11.取5.8 g 某种饱和一元醛与足量的银氨溶液混合,加热充分反应后析出21.6 g 金属银,则该醛为( )
A .甲醛
B .乙醛
C .丙醛
D .丁醛
12.橙花醛是一种香料,结构简式为:(CH 3)2C=CHCH 2CH 2C(CH 3)=CHCHO 。
下列说法正确的是( )
A.橙花醛不可以与溴发生加成反应
B.橙花醛可以发生银镜反应
C.1mol 橙花醛最多可以与2mol 氢气发生加成反应
D.橙花醛是乙烯的同系物
15.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯4种物质中的一种或几种,在鉴定时有下列现象:①可发生银镜反应;②加入新制Cu(OH)2悬浊液沉淀不溶解;③与含酚酞的NaOH 溶液共热发现溶液中红色逐渐消失以至无色。
下列叙述中正确的是( )
A.有甲酸和甲酸乙酯
B.有乙酸和甲酸乙酯
C .可能有甲醇,一定有甲酸乙酯 D.几种物质都有。