无机物的推断及检验--无机框架题--北师大版
- 格式:pdf
- 大小:280.11 KB
- 文档页数:10
无机推断的思路与技巧(附练习和答案)1、题型“三特点”:“无机推断题”作为高考考查元素化合物知识的热点题型,它的主要特点是:①结构紧凑、文字表述少②包含信息多、综合性强,思维能力要求高③具有很高的区分度和很好的选拔功能。
它不仅考查考生对元素及其化合物主干知识掌握的情况,更能考查考生思维的敏捷性、发散性、严密性和分析推理综合应用元素化合物知识的能力。
2、解题“五步曲”:(1).审: 审清题意,从题干→问题→框图迅速浏览一遍,尽量在框图中把相关信息表示出来,明确求解要求。
(2).找: 找“题眼”即找到解题的突破口,此步非常关键。
(3).析: 从题眼出发,联系新信息及所学的旧知识,大胆猜测,顺藤摸瓜,应用正逆向思维、发散收敛思维、横向纵向思维等多种思维方式、进行综合分析、推理,初步得出结论。
(4).验: 验证确认将结果放入原题检验,完全符合才算正确。
(5).答:按题目的要求写出答案。
3、破题最关键:找“题眼”4.常见“题眼”归类解析方法一:根据物质的特殊颜色推断知识准备:物质颜色(1)有色固体:红色:Cu 、Cu 2O 、Fe 2O 3; 褐色:Fe(OH)3; 黄色:AgI 、Ag 3PO 4;浅黄色:S 或Na 2O 2或AgBr ; 蓝色:Cu(OH)2; 紫黑色:KMnO 4 I 2 黑色:炭粉、CuO 、FeO 、FeS 、CuS 、Ag 2S 、PbS ; 白色:Fe(OH)2、CaCO 3、BaSO 4、AgCl 、BaSO 3;(2) 有色溶液:Fe 2+(浅绿色)、Fe 3+(黄色)、Cu 2+(蓝色)、MnO 4-(紫红色)、[]±y x SCN Fe )((x=1~6)(红色)(3).有色气体:Cl 2(黄绿色)、Br 2(g)(红棕色)、NO 2、(红棕色)、I 2(紫色)O 3(淡蓝色)例1、下图表示各物质之间的转化关系。
已知:A 、D 、F 、H 均为单质,X 常温下为无色液体,B 为淡黄色固体,J 溶于酸得到黄色溶液。

解答无机框图推断题的思路与技巧顾浩平无机框图推断题以其涉及知识面广,思维能力要求高等特点而倍受高考命题者的青睐,是近年高考的热点题型之一。
在高考试题中,无机框图推断通常作为一道大题出现,因此在高考试卷中的权重较大,理应引起广大迎考师生的重视!在解答框图推断题时,同学们常常会出现如下一些情况:思路顺畅时,解答这类试题会十分顺利,如果思路不畅时,或者一时想不到某一物质时,这类试题的解答常常会显得无从下手,即这类试题的解答对同学们来说,常常会出现时好时坏的现象,具有一定的偶然性和不稳定性,因此考试成绩也会因此而忽上忽下。
在高考成绩可能决定个人命运的今天,这种忽上忽下的成绩变化可能是致命的。
为帮助同学能顺利地解答这类试题,本文将重点介绍这类试题的解题思路和解题技巧,以供参考。
一、注意有关物质的特性,掌握常见的解题“题眼”,为顺利解题作好知识准备。
无机框图推断所涉及的知识主要是元素化合物的性质知识,因此若要顺利解答无机框图推断题,首先就应掌握相关物质的性质知识,否则解题是很难做到得心应手的。
其次要熟悉一些用作顺利解题的“题眼”,以便解题时能顺藤摸瓜,快速得出正确结论。
在解答框图推断题时,常用作解题“题眼”的知识有:1.既能与酸反应又能与碱反应(两性)的物质常常是解答框图推断题的“题眼”或切入点;这类物质通常有:①Al、Al2O3、A l(O H)3的两性;②弱酸的铵盐,如碳酸铵、碳酸氢铵、硫化铵、亚硫酸铵等;③除硫酸以外的多元弱酸的酸式盐,如碳酸氢钠、亚硫酸氢钠等;④氨基酸的两性;⑤酯的水解等。
2. 受热分解的物质或反应通常有:①2KMnO4K2MnO4+MnO2+O2↑②2KClO32KCl+3O2↑③难溶性碳酸盐,如:CaCO3CaO+CO2↑、C u2(O H)2C O32CuO+CO2↑+H2O ④酸式碳酸盐,如:2NaHCO3Na2CO3+CO2↑+H2O ⑤硝酸或硝酸盐,如:4HNO34NO2↑+O2↑+2H2O、2NaNO32NaNO2+O2↑、2C u(N O3)22CuO+4NO2↑+O2↑、2AgNO32Ag+2NO2↑+O2↑⑥铵盐,如:NH4HCO3NH3↑+CO2↑+H2O、(N H4)2C O32NH3↑+CO2+H2O、NH4Cl NH3↑+HCl等⑦难溶性碱,如:2F e(O H)3Fe2O3+3H2O等⑧2H2O22H2O+O2↑3.与水反应或溶于水时,既有沉淀又有气体产生的物质或反应通常有:①Al2S3+6H2O2A l(O H)3↓+3H2S↑②Mg3N2+6H2O3M g(O H)2↓+2NH3↑③CaC2+2H2O C a(O H)2↓+C2H2↑等。

以框图为基础的无机推断题主要考查钠、铁、铝、镁、铜、硫、氯、氮、硅等元素的单质及其化合物。
从题型上看,主要以元素及其化合物的综合推断为主,联系基本概念、基本理论命题,也可以通过无机化工流程图考查元素及化合物知识。
从联系上看,可以从社会、科技、环境等角度联系元素化合物知识,还可以将实验、化学反应原理等结合起来进行综合考查。
【例1】短周期元素组成的单质及化合物间能发生如下图所示的转化,其中甲、乙为单质,A、B、C、D为化合物,B为气体,C为白色沉淀。
回答下列问题:(1)若B为常见的碱性气体,C不溶于NaOH溶液。
①甲的电子式为________________。
②写出A→B+C的化学方程式_____________________。
(2)若B为具有臭鸡蛋气味的气体,乙与Fe2O3反应可用于焊接钢轨。
①工业上制取乙的化学方程式为_____________________。
②写出D溶液与过量氨水反应的离子方程式______________________________。
【答案】Mg3N2+6H2O=== 2NH3↑+3Mg(OH)2(或Li3N+3H2O===NH3↑+3LiOH)2Al2O34Al+3O2↑ Al3++3NH3•H2O=== 3NH4++Al(OH)3↓点睛:解决本题的关键是A的水解反应,常见物质的性质。
【例2】某研究小组为了探究一种浅绿色盐X(仅含四种元素,不含结晶水,M(X)<908g•mol﹣1)的组成和性质,设计并完成了如下实验取一定量的浅绿色盐X进行上述实验,充分反应后得到23.3g白色沉淀E、28.8g红色固体G和12.8g 红色固体H。
已知:①浅绿色盐X在570℃、隔绝空气条件下受热分解为非氧化还原反应.②常温下B呈液态且1个B分子含有10个电子。
请回答如下问题:(1)写出B分子的电子式 _________(2)请写出红色固体G与足量D溶液反应的离子方程式__________(3)X的化学式是_________【答案】Cu2O+2H+═Cu2++Cu+H2O Cu4(OH)6SO4【解析】浅绿色盐X在570℃、隔绝空气条件下受热分解为非氧化还原反应,得到A、B和黑色固体C,常温下B呈液态且1个B分子含有10个电子,B为水,A和水反应生成的D能和氯化钡反应生成白色沉淀E,E只能为硫酸钡,23.3g白色沉淀E的物质的量为n=m/M=23.3g/233g·mol-1=0.1mol,黑色固体C可能为四氧化三铁、氧化铜、碳等,黑色固体C隔绝空气在1000℃反应生成气体F和红色固体G,G能和硫酸反应生成红色固体和蓝色溶液应为氧化亚铜在酸性溶液中的歧化反应,所以红色固体G 为氧化亚铜,气体F为氧气,红色H为铜,蓝色溶液I为硫酸铜;逆推可得:一定量的浅绿色盐X中n(S)=0.1mol,28.8g红色固体G为氧化亚铜,n(Cu2O)=28.8g/144g·mol-1=0.2mol,12.8g红色固体H,n(Cu)=0.2mol,浅绿色盐X中n(Cu)=0.4mol,n(CuO)=0.4mol,浅绿色盐X在570℃、隔绝空气条件下受热分解为非氧化还原反应,n(S)=0.1mol,所以n(CuO):n(SO3)=1:4,浅绿色盐X,仅含四种元素,不含结晶水,设化学式为:Cu4(OH)mSO4,Cu4(OH)mSO44CuO+SO3↑+m/2H2O↑,根据氧元素守恒得:m=6,符合M(X)<908g·mol-1,则该反应流程为:X在隔绝空气、570℃温度下加热Cu4(OH)6SO44CuO+SO3↑+3H2O↑,A和B反应SO3+H2O=H2SO4,硫酸与足量氯化钡反应:H2SO4+BaCl2=BaSO4↓+2HCl,白色沉淀E为BaSO4,黑色固体C为氧化铜,在1000℃反应生成气体F为氧气,红色固体G为氧化亚铜4CuO2Cu2O+O2↑,G氧化亚铜和硫酸发生歧化反应:Cu2O+H2SO4=CuSO4+Cu+H2O,红色H 为铜,蓝色溶液I为硫酸铜。

专题无机物框图题一、高考考点:推断题是历年高考化学试题的组成部分,也成为化学测试的重要题型之一,它旨在检查学生掌握化学知识:包括元素知识,物质性质,化学实验等情况的程度。
借此考核学生的分析、判断、推理的能力。
推断题的特点:这类题涉及知识面广,综合性强,难度较大,知识网络化,要求有较高的思维能力,逻辑性也很强。
二、要点精讲:1、解题方法:推断题是反映某一知识点(元素、物质)的推断过程。
所以要抓住结构特征(元素),性质特征(物质),实验现象(化学实验)的特点为主线,并以此为依据,找到解题的突破口,然后再根据性质的衍变关系,变化规律和反应事实进行推理。
有时也可以在审清题意后,根据有关特征,提出假想(元素、物质),在根据元素结构特征,性质特征分析是否满足题意来加以验证。
物质推断题由于可全面考查无机化学知识的内在联系,及其分析问题的方法和解决问题的能力,而成为优秀的传统题型,主要分为限定范围推断(给出实验现象,或特定组合元素及必要数据)和不定范围推断(只给出物质类别或状态及转化框图)两大类。
(1)审题与析题:推断题的解答首先在审题与析题上下功夫,大凡推断题所涉及的元素及化合物都比较多,题目的文字叙述较长,往往顾此失彼。
在审题中准确、迅速找出关键词语,即所谓的“题眼”它是解题的钥匙。
审与析是相互联系的,把这一对矛盾贯穿在推断题的全过程,运用恰到好处就能游刃有余。
只有申清题意才能析出正确的结论,审是析的前提,析是审的结果。
审是理顺关系,而析是正确推理。
(2)推理的一般逻辑顺序:推理的一般逻辑顺序是:审析题意,明确已知条件和要求判断的结论由要求判断的结论出发,寻找材料的真实前提→进行论证,要有充分的理由并符合逻辑规则→得出结论并检验是否正确,是否符合题意。
解答推理题的关键在于熟悉掌握的化学理论与物质的性质,通过分析题意,问题知识的内在联系和性质的差异,抓住关键性的依据,找出一个熟悉、明显的特征反应或现象作突破口,然后层层分析各个击破。

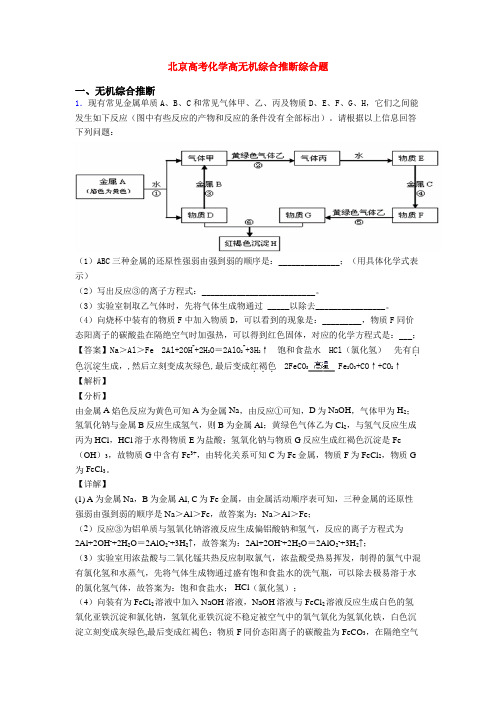
高二化学无机推断试题答案及解析1.下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。
常温常压下,化合物A是家庭生活中常用的一种调味品,A、C的焰色反应都呈黄色,B 是无色无味的液体,D是黄绿色气体,E、F都是无色气体,F的水溶液是盐酸,H的水溶液具有漂白、杀菌性,J在水溶液中生成时为红褐色沉淀。
(1)H的化学式为。
(2)F的电子式为。
(3)反应①的化学方程式为。
(4)反应②的离子方程式为。
【答案】(1)NaClO(1分)(2)HCl的电子式(略)(1分)(3)2NaCl+2H2O2NaOH+Cl2↑+H2↑(2分)(4)Fe3++3OH-=Fe(OH)3↓(2分)【解析】A、B、C、D、E、F、G、H、I、G、J分别为NaCl、H2O、NaOH、Cl2、H2、HCl、NaClO、FeCl3、FeCl2、Fe(OH)3。
(3)反应①为电解饱和食盐水,产生NaOH、Cl2、H2;(4)反应②为铁盐与碱反应生成氢氧化铁沉淀。
【考点】考查物质的转化有关问题。
2.A~F是中学化学中常见物质,常温下A、C、E、F为气体,B、D为液体,其中B的分子为4原子分子,D在常温下不具有挥发性。
F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末。
这些物质之间满足如下图所示的转化关系,图中部分生成物已略去。
(1)写出下列物质的化学式:A______,F______。
(2)B的电子式是______。
根据图中信息,B、C、X的氧化性由强到弱的顺序是_ _____(用化学式表示)。
(3)反应⑥的离子方程式是__ ____。
(4)在反应⑥中,F表现的性质是___ ____,当生成0.75mol C时,被氧化的还原剂的物质的量是___ ____。
【答案】(1)SO2 HCl(各1分)(2);MnO2>Cl2>H2O2(各1分)(3)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O(2分)(4)还原性、酸性(2分) 1.5 mol(2分)【解析】化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。
高考化学框图无机推断题练习及答案高考化学框图无机推断题练习:1.下图为某些物质之间的变化关系(未注明用量的物质间均按恰好充分反应处理)已知A的焰色反应呈黄色,常温下,甲为能使湿润的红色石蕊试纸变蓝的气体,乙为可燃性气体,甲、乙分子中质子数相等。
(1) A的化学式是;乙的化学式是。
(2) X是一种纯净物,X的化学式是;C中含有、。
(填化学式)(3) 能否确定B为何种物质?如果能,写出B的化学式;如果不能,请说明理由。
2.甲、乙、丙为短周期元素形成的常见单质,A、B、C、D、E、F、G、X均为常见的化合物。
B、X的式量(分子量)相同,E 的式量比D大16,在一定条件下各物质之间相互转化如下图所示:(1) X的电子式是,G的化学式是。
(2) 上述物质中能与水发生反应(不考虑单纯的盐的水解)且反应中水既不是氧化剂也不是还原剂的物质的代号是。
(3) 反应D+丙的化学方程式是。
(4) 写出X与D在稀硫酸中反应的离子方程式。
3.甲、乙、丙三种常见的单质,X、Y、Z三种常见的化合物,它们在一定条件下的相互转化关系如下:请填写以下空白:(1) 在X、Y、Z三种化合物中肯定含有乙、丙两种元素的化合物是。
(2) 在X、Z两种化合物的正价元素的化合价中,是。
A. 前者高B. 后者高C. 不一定原因是。
(3) 当X为两种非金属元素组成的化合物时,写出X跟甲反应的化学方程式。
写出丙跟乙反应的化学方程式。
(4) 当X为金属元素与非金属元素组成的化合物时,写出X跟甲反应的化学方程式。
写出丙跟乙反应的化学方程式。
4.有X、Y、Z三种单质,常温下X是固体,Y是液体,Z 是气体。
它们之间的反应关系如下图所示:请填写下列空白:(1) 据此推断X、Y、Z的化学式:X 、Y 、Z 。
(2) X是常见的单质,它是主族元素,还是副族元素,其理由是:。
(3) 写出C+Y A的离子方程式:。
6.甲、乙两种物质是常见的短周期元素的单质,其有关物质性质如图,其中C为白色沉淀,D为气体。
二、无机推断题标准答案 (1)极性(1分) (2)2Na 2O 2+2H 2O===4NaOH +O 2↑(2分) (3)NH 4HCO 3+2NaOH=====△Na 2CO 3+NH 3↑+2H 2O(2分) CO 2-3+H 2O HCO -3+OH -(2分) (4)2NH 3+6OH --6e -===N 2+6H 2O(2分) 减小(1分)(5)1.5 mol·L -1·min -1(2分) 0.15(2分) (6)ace(2分) 评分细则 (1)按标准答案评分。
(2)不标“↑”扣1分。
(3)少写条件或少写“↑”均扣1分,把“ ”写成“===”不得分。
(4)写成最简形式不扣分。
(5)漏掉单位或写错扣1分,有效数字保留错不得分。
(6)对一个或两个得1分,有错不得分。
题型特点 无机推断题,集元素化合物知识、基本概念和基本理论知识于一体,考查面广,综合性强,思维容量大。
无机推断题层次分明,区分度高。
由于此类题目具有较强的学科特色,考查知识点较多,是高考命题中一种重要的命题形式。
该题有四种命题类型:一是以阴、阳离子判断为中心的物质推断,二是以原子结构、元素周期律为中心的元素推断,三是以元素化合物知识为基础的无机框图推断,四是实验探究无机化合物成分类。
得分技巧 审题时要做到:迅速浏览全题―→找准突破口―→看准物质联系―→大胆假设认定―→全面进行分析―→最后验证确认。
答题时要细心:看准要求,规范书写。
类型一以阴、阳离子判断为中心的物质推断1.(12分)饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E是五种常见化合物,都是由下表中的离子形成:为了鉴别上述化合物,分别进行以下实验,其结果如下所示:①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成。
高三化学无机推断试题答案及解析1.A、J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去)。
回答以下问题:(1)A的原子结构示意图为,M的化学式为。
(2)A与NaOH溶液反应的离子方程式为。
(3)写出②的化学方程式。
(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。
X的水溶液与NaHCO3溶液混合,反应的离子方程式为。
【答案】(1),FeS;(2)2Al + 2OH- + 6H2O=2[Al(OH)4]- + 3H2↑;(3)4NH3+5O24NO+6H2O;(4)Al3+ + 3HCO3-= Al(OH)3↓ + 3CO2↑。
【解析】根据题意知,A、J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极,则A为铝;结合流程图知,C为偏铝酸钠,E为氢氧化铝,H为氧化铝,J为铁,M为硫化亚铁,D为氢气,F为氮气,G为氨气,I为一氧化氮,K为二氧化氮,L为硝酸。
(1)A为铝,原子结构示意图为,M为硫化亚铁,化学式为FeS;(2)铝与NaOH溶液反应生成四羟基合铝酸钠和氢气,离子方程式为2Al + 2OH- + 6H2O==2[Al(OH)4]- + 3H2↑;(3)反应②为氨的催化氧化,化学方程式4NH3+5O24NO+6H2O;(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。
X为明矾,其水溶液与NaHCO3溶液混合,反应的离子方程式为Al3+ + 3HCO3-="=" Al(OH)3↓ + 3CO2↑。
【考点】考查无机推断,涉及铝和氮元素单质及其化合物的性质及相互转化关系、化学方程式的书写。
2.A、B、C分别是元素甲、乙、丙的单质,它们都是常见的金属或非金属,D、E、F是常见的三种氧化物,且有如图所示转化关系,则下列说法不正确的是()A.D、E中一定都含有甲元素B.单质B肯定是氧化剂C.A、B、C中一定有一种是氧元素的单质D.若A是非金属,则B一定为金属【答案】B【解析】A是甲的单质,根据图示,E中必含甲元素,B是乙元素单质,与D反应生成A,该反应是置换反应,所以D中必含甲元素,A项正确;B项,D是氧化物,与B单质反应,一般B是还原剂,错误;C项,A与C单质反应生成氧化物E,所以必有一种是氧气,正确;D项,若A是非金属,则D与B的反应一般是类似于水与钠间的置换,即D项正确。