物质的标准摩尔生成焓(新)
- 格式:doc
- 大小:193.50 KB
- 文档页数:4

标准摩尔生成焓,标准摩尔燃烧焓,标
准摩尔焓变的定义和区别
标准摩尔生成焓、标准摩尔燃烧焓和标准摩尔焓变是物理学中的重要概念,它们之间有着明显的区别。
首先,标准摩尔生成焓是指在标准状态下,1摩尔物质生成的焓,它的定义是:在标准状态下,1摩尔物质生成的焓等于物质的标准化学反应所放出的焓。
其次,标准摩尔燃烧焓是指在标准状态下,1摩尔物质燃烧所放出的焓,它的定义是:在标准状态下,1摩尔物质燃烧所放出的焓等于物质的标准化学反应所放出的焓。
最后,标准摩尔焓变是指在标准状态下,1摩尔物质的焓变,它的定义是:在标准状态下,1摩尔物质的焓变等于物质的标准化学反应所放出的焓减去物质的标准化学反应所放出的焓。
从定义上可以看出,标准摩尔生成焓和标准摩尔燃烧焓的区别在于,前者是指1摩尔物质
生成的焓,而后者是指1摩尔物质燃烧所放出的焓。
而标准摩尔焓变则是指1摩尔物质的焓变,它是标准摩尔生成焓和标准摩尔燃烧焓的差值。
总之,标准摩尔生成焓、标准摩尔燃烧焓和标准摩尔焓变是物理学中的重要概念,它们之间有着明显的区别,它们的定义也不同。

标准摩尔生成焓摩尔生成焓的概念本来就是物理学家布鲁克斯摩尔于1847年提出的一种能量定义,它是一种动量平衡定律,以此来确定力学系统中能量的定义和传递。
摩尔生成焓是根据这个理论发展出来的,如此可以更加精确的计算出系统中的当量温度、压强等值,从而应用到物理学及以后的物理学应用领域中。
摩尔生成焓定义了本质性的能量场,它可以从能量的定义、传递及状态平衡等提供一种有效的方法,更好地描述系统中的物质的能量状态。
它的定义强调的是,摩尔生成焓是在一个完全封闭的系统中,当体积变化时,当量温度下的传热量必须与系统的变化量等效,而此变化量又必须与系统受到之外的外力相等。
基于此,在1850年,英国物理学家维斯特洛夫提出了一套计算摩尔生成焓的方程,从而使得系统中的能量变化量可以实现更为准确的计算。
维斯特洛夫方程主要由两个条件组成,第一条件是系统处在热力学平衡态,而第二条件则是压力的变化量必须与温度的变化量成正比。
两个条件结合在一起,就构成了摩尔生成焓的标准,为系统中的能量传递提供了一种新的定义方法,使得能量的计算变的更加准确、简单。
从此,摩尔生成焓就慢慢成为物理学中的关键词,它也被用到物理学以外的领域,如化学、化工、电子学等科学领域中。
摩尔生成焓也被用于一些技术性的计算,如热变形分析、压力容器分析、爆炸爆破安全性等类似的问题分析中。
同时,也用作基础理论,对密度变化、声学及热膨胀系数等进行定量分析。
摩尔生成焓的发展不仅使物理学获得了巨大的进步,也极大拓展了科学的范畴,为人类的科学研究提供了更好的参考标准和理论依据。
而摩尔生成焓的标准也成为物理学及后续物理应用领域中研究者们计算系统中有关能量的变化量所遵循的重要参考标准,从而使得物理学的研究更加准确、精确。
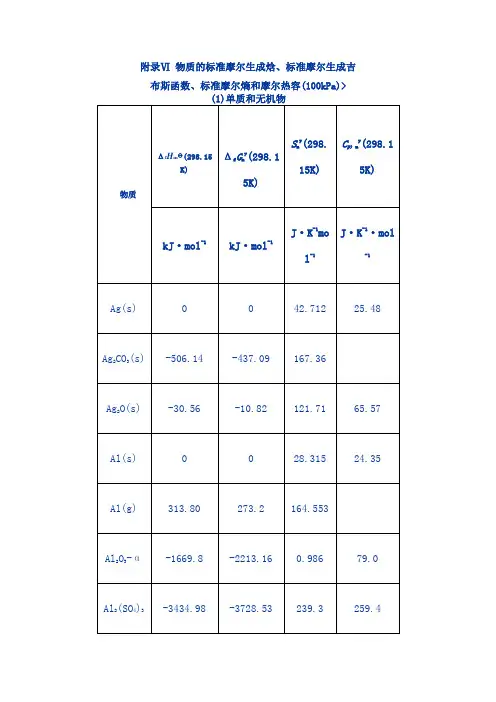
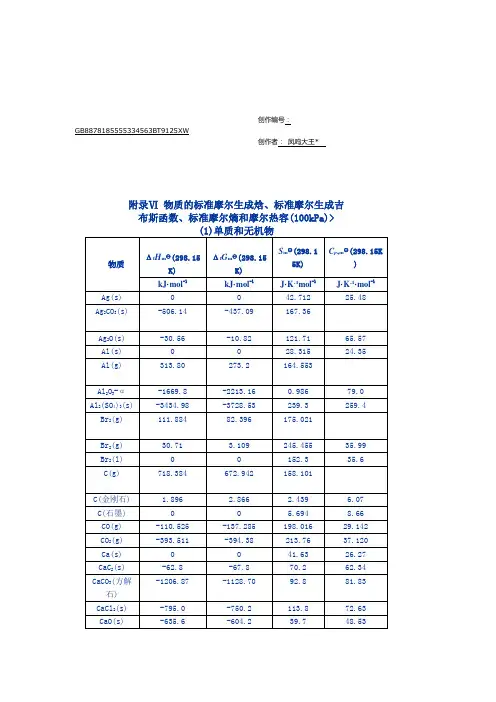



物质的标准摩尔生成焓
标准摩尔生成焓是指在标准状态下,将1摩尔物质从其元素的稳定形态生成所需的焓变化。
标准状态指的是25℃(298K)
和1个大气压下。
由于不同物质的生成焓与反应过程有关,因此标准摩尔生成焓的值也因物质而异。
在化学反应中,物质的生成或分解通常与能量变化有关,根据热力学第一定律,焓变化可以表示为反应物的焓减少与产物的焓增加的和。
标准摩尔生成焓可以通过实验测量或计算方法来确定。
例如,对于氧气(O2)的生成焓,可以通过以下反应来计算:1/2 O2(g) → O(g) ΔH° = ΔHf°(O(g))
在该反应中,氧气分解为氧原子,生成焓即为氧原子的标准摩尔生成焓。
该值通常通过实验测量得出,并被定义为0。
因此,氧气的标准摩尔生成焓为0。
对于其他物质的生成焓,可以通过类似的方法进行测量或计算,以确定其标准摩尔生成焓的值。
这些值对于理解和预测化学反应的能量变化非常重要。
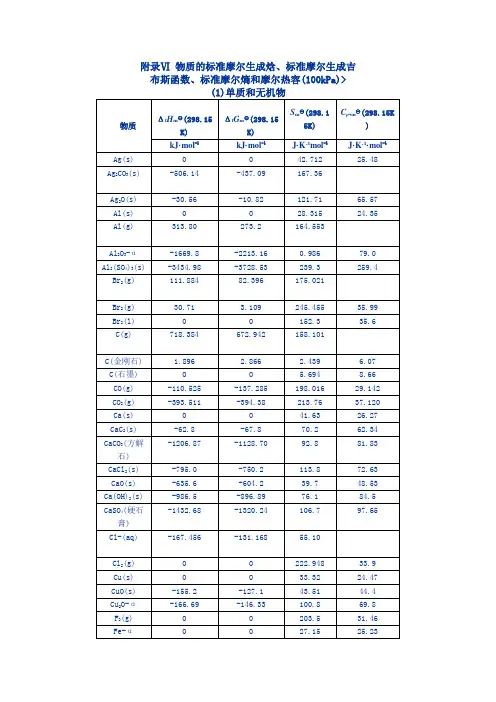

化合物的标准摩尔生成焓(ΔH°f)是指在标准状况下,形成1摩尔该化合物所释放或吸收的热量。
标准状况通常定义为温度为298K(25℃),压力为1个大气压(101.325 kPa),纯物质处于其稳定标准形态时。
标准摩尔生成焓的值是通过实验测定得到的,可以用来表示化学反应的热效应。
正值表示反应放热(热量从周围环境中释放出来),负值表示反应吸热(热量被吸收)。
化合物的标准摩尔生成焓可以通过以下方式确定:
1.通过热量计对反应进行直接测量。
2.根据其他相关反应的标准摩尔生成焓和热效应的关系进行间接计算。
3.使用计算化学方法,如密度泛函理论(DFT)等计算手段进行估算。
标准摩尔生成焓的单位一般为焦耳/摩尔(J/mol)或千焦耳/摩尔(kJ/mol)。
需要注意的是,不同化合物的标准摩尔生成焓值会有所差异,因此要根据具体的化合物进行查询或计算。
这些数据可以在化学参考书、化学数据库或相关科学文献中找到。

标准摩尔生成焓标准摩尔生成焓,也称为摩尔定律生成焓,是一种独特的平衡状态的物理模型,可以被用来衡量物质能量的存储和流动。
它最初是由美国物理学家爱德华摩尔于1961年提出的,后来得到了全世界物理学家的重视。
标准摩尔生成焓是个最低的恒定水平,有时也称为“最低温度”。
在这个温度之下,物质就不会放出任何能量。
它可以被衡量为一个固定的数值,就是常数。
标准摩尔生成焓也可以被认为是恒定的能量水平,就像在电路中,恒定的能量水平可以被看作是最低电压,而最低能量水平则是标准摩尔生成焓。
标准摩尔生成焓可以用来检查物质的物理性质,如它的温度、压强、密度等,这些影响物质能量流动和储存的因素,而标准摩尔生成焓可以有效地帮助理解这些因素。
此外,在量子力学中,标准摩尔生成焓可以用来预测物质的密度状态以及某些其他物理性质。
此外,标准摩尔生成焓还可以帮助我们理解物质能量的流动和储存。
它可以用来检测特定物质的熵,熵是物质本身和它所处环境之间的能量差值,可以用于理解物质在某一特定环境下的行为特性。
标准摩尔生成焓也可以用来识别物质的动力学性质,这一点也可以帮助我们理解物质在特定环境下的行为特性。
标准摩尔生成焓是一种不可替代的物理理论,可以用来识别和衡量物质能量的存储和流动。
它的应用已被应用于电路设计、热力学计算、量子物理研究、材料研究以及各种其他领域。
它还对传统机械工程、软件工程、材料科学、电子工程等领域的研究非常重要,它可以帮助科学家精确地衡量物质能量的储存和流动。
总之,标准摩尔生成焓在物理学、化学、机械学等多个领域具有重要的意义。
它可以帮助我们理解物质能量的存储和流动,以及物质之间的相互作用。
它也为科学家们提供了有用的理论框架,有助于他们精确衡量物质能量的存储和流动。

标准摩尔生成焓标准摩尔生成焓是一种重要的物理量,它是衡量一个系统能量变化所产生的热量的指标。
该物理量由克尔曼于1875年提出,他提出了一个基本定理:在一个固定的温度下,一定的物质的熵增量只有一定的质量的能量的损失是固定的。
因此,摩尔生成焓可以用来衡量一个系统的能量变化所产生的热量,或者说,衡量某种反应的化学反应的余热,这称之为摩尔热。
标准摩尔生成焓是当摩尔热发生时,所引起的能量变化的物理量,其定义如下:在给定温度下,系统发生1摩尔基本单位反应生成1摩尔基本单位产物时,所放出的平衡热所投入的能量。
一般来说,这种反应放出的热量越大,标准摩尔生成焓也就越大,反之亦然。
因此,标准摩尔生成焓反映了一种反应的活化能越大,反应的可能性越大,而活化能越小,反应的可能性则越小。
标准摩尔生成焓是一个有效的物理量,它可以用来描述物质间的化学反应,以及反应过程中释放出来的热量。
该物理量也可以用来分析和计算一种化学反应所需要的活化能,和该反应所释放出的热量。
标准摩尔生成焓可以给出若干反应能量的参考值,可以计算出活化能的大小,也可以判断一种反应的可能性。
此外,标准摩尔生成焓还可以用来对比不同物质的熵值,以及检验某种反应的反应机理。
标准摩尔生成焓也可以用来预测和指导采取措施来抑制或促进反应,从而控制反应的进程。
标准摩尔生成焓也可以用来估算材料的力学行为,通过它可以得出一种物质的特性,从而确定该物质的适用性。
另外,标准摩尔生成焓也可用来计算某种反应的自由能变化,这在化学热力学中常用来计算物质的反应性能,也可以指导物质的合成工艺。
综上所述,标准摩尔生成焓是一个重要的物理量,它衡量一个系统在发生化学反应时所释放出来的热量,并可用来描述物质间的反应机理,以及活化能的大小,它对于理解物质反应的过程,估计材料的力学行为以及指导物质合成工艺都有重要作用。