合成氨变换工段工艺设计
- 格式:doc
- 大小:889.50 KB
- 文档页数:50

合成氨变换工段工艺设计合成氨是化工工业中的重要原料,广泛应用于制取尿素、硝化铵等农业肥料,以及制取氨水、氨盐、化肥、染料等合成工艺中。
合成氨变换工段是合成氨生产中的关键环节,其工艺设计对合成氨的产量、质量以及能耗等方面有重要影响。
一、工艺概述合成氨的变换反应器是将反应物氮气和氢气通过催化剂的作用,在一定条件下发生气相合成反应,生成合成氨。
反应器通常采用固定床催化剂反应器,催化剂的选择和催化剂床层的设计都是工艺设计的重要环节。
冷凝器主要用于对反应产生的氨气进行冷凝回收,常见的冷凝器有直接冷凝器和间接冷凝器两种形式,工艺设计中需要根据具体情况选择适用的冷凝方式。
循环气压缩机主要用于将反应器中未反应的气体通入新的循环,提高气相合成反应的转化率。
在工艺设计中,需要考虑压缩机的压比、功率消耗等参数。
氨气的分离净化装置主要用于对合成氨中的杂质进行去除,提高合成氨的纯度。
常用的分离净化装置有吸附装置、膜分离装置等,具体的工艺设计需要根据生产要求和经济效益进行选择。
二、工艺参数及控制合成氨的变换工段的工艺参数主要包括反应温度、反应压力、空速、催化剂活性等。
这些参数直接影响合成氨的产率、选择性和能耗。
反应温度是合成氨变换反应的重要参数,通过控制温度可以提高反应速率和转化率,但过高的温度会导致副反应的发生,降低合成氨的选择性。
反应压力主要用于控制氨气的产量和能耗,压力越高产氨越多,但能耗也相应增加。
空速是指单位时间内通过反应器的氮气体积,可以通过调控压力和进气量来实现,过小的空速会影响反应的效果,而过大会导致固定床催化剂的床层冲击和阻力升高,影响反应转化率。
催化剂活性主要指催化剂的活性组分含量和粒径等参数,这些参数会影响合成氨的选择性和催化剂的寿命。
在工艺设计中,需要考虑这些参数的合理选择和控制,以提高合成氨的产量和质量,并降低能耗。
三、能耗控制合成氨的变换工段是合成氨生产中的能耗重点。
能耗的控制主要体现在压力控制、催化剂选择和热交换等方面。

合成氨是一种重要的工业原料,广泛应用于农业、化工、医药等领域。
本文基于年产10万吨合成氨的工段工艺设计,旨在优化工艺流程,提高生产效率和质量,同时满足环保要求。
合成氨的主要生产方法是哈柏-博斯曼(Haber-Bosch)工艺,该工艺通过高温高压条件下将氮气和氢气催化反应生成合成氨。
下面是年产10万吨合成氨变换工段的工艺设计:一、气体预处理:氮气和氢气作为原料需要经过脱氧、除尘、脱硫等处理。
首先,气体通过管路系统进入脱氧器,脱氧器中通过还原剂将氧气还原成水蒸气,并通过除尘装置去除颗粒杂质。
然后,气体进入脱硫装置,通过催化剂将硫化氢还原成硫。
最后,气体经过压缩机增压至反应器所需的高压。
二、反应器系统:反应器是合成氨的核心设备,采用多床连续负压式反应器。
氮气和氢气按照适当的配比通过输送装置进入反应器,反应器内通过催化剂将氮气和氢气催化反应生成合成氨。
反应器床层数可根据实际需要确定,废热可回收利用进行预热。
同时,反应器系统还要配备适当的温度、压力和流量控制装置,以保证反应器内的运行条件稳定。
三、合成氨分离:反应后的气体中含有未反应的氮气、氢气和合成氨,需要进行分离处理。
首先,将反应气体冷却至低温,通过液相分离装置将液态氨分离出来。
然后,将氨气经过压缩,通过冷凝器冷却至液态,并收集分离出的液态氨。
未反应的氮气和氢气通过管道再次回流到反应器进行循环利用。
此外,分离出的液态氨还需要经过精制和储存处理,以确保质量和安全。
四、废气处理:合成氨生产中会产生大量的废气,包括未反应的氮气、氢气、氨气和其他杂质气体。
废气处理主要包括低温分离、吸收、洗涤等步骤。
首先,废气通过低温分离装置将其中的液态氨和水分离出来。
然后,通过吸收剂将氨气吸收,以减少其排放。
最后,利用洗涤液去除废气中的其他杂质气体,确保废气达到环境排放标准。
五、能耗优化:为了降低能耗和提高生产效率,可以采用余热回收和过程优化等措施。
余热回收可通过换热器将反应废热回收利用,进行气体预热和水蒸气生产。

年产三万吨合成氨厂变换工段工艺设计一、工艺流程概述1.原料准备:将天然气(主要是甲烷)与空气作为主要原料,通过气体净化系统去除其中的杂质、硫化物和水分。
2.原料配送:将净化后的天然气和空气分别输送至气体净化系统进行进一步的处理和分析。
3.变换反应槽:将净化后的天然气和空气通过压缩机压缩至一定压力后,经过暖气交换器加热至高温(约500-600℃),再进入变换反应槽。
4.变换催化剂:在变换反应槽中,使用催化剂(通常是高温高压下的铁-钴催化剂)促进N2和H2的反应。
反应生成的合成氨会随气流从反应槽中流出。
5.除气系统:将反应槽中的气体通过除尘器,冷却器和吸附剂等设备进行处理,去除其中的固体颗粒、水分和其他杂质。
6.合成氨回收:经过除气系统处理后的气体中仍含有未反应的氮气和氢气,通过压缩机再次压缩进入蒸馏塔。
在蒸馏塔中,根据不同的沸点,将氨气和氮气分离开来,再通过冷凝器冷凝为液态氨。
7.废水处理:在工艺过程中产生的废水会经过处理系统去除其中的有机物和杂质,以保证排放的废水符合环保要求。
二、设备布置和操作要点1.变换反应槽的设计要考虑到温度、压力和气体流动速度的控制。
同时,需要定期更换催化剂,以维持优良的反应性能。
2.除气系统中的设备要进行定期维护和清洁,确保其正常工作和去除气体中的杂质、固体颗粒和水分。
3.合成氨回收装置要根据产品质量要求设置合适的操作参数,例如蒸馏塔的温度和压力。
此外,冷凝器的冷却水流需要保持稳定,以确保气体顺利冷凝为液态氨。
4.废水处理系统应配置适当的物理和化学处理单元,如过滤器、沉淀池和生物处理等,以达到废水排放标准。
5.需要建立相应的安全措施,如设立监测系统,确保气体和液体在整个工艺中的安全运输和使用。
三、工艺控制和性能优化1.在变换反应槽中,可以通过调节供气比例、压力和温度等参数来控制合成氨的产率和选择性。
同时,也可以根据反馈控制系统监测和调整催化剂的性能。
2.除气系统中的设备可以通过监测气体的组成和温度、压力等参数,来调整操作参数,以达到满足产品质量要求的除气效果。
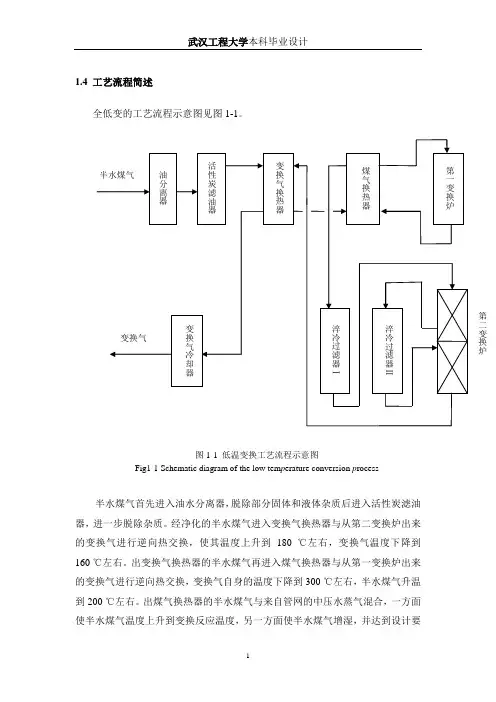
1.4 工艺流程简述全低变的工艺流程示意图见图1-1。
图1-1 低温变换工艺流程示意图Fig1-1 Schematic diagram of the low tem p erature conversion p rocess半水煤气首先进入油水分离器,脱除部分固体和液体杂质后进入活性炭滤油器,进一步脱除杂质。
经净化的半水煤气进入变换气换热器与从第二变换炉出来的变换气进行逆向热交换,使其温度上升到180 ℃左右,变换气温度下降到160 ℃左右。
出变换气换热器的半水煤气再进入煤气换热器与从第一变换炉出来的变换气进行逆向热交换,变换气自身的温度下降到300 ℃左右,半水煤气升温到200 ℃左右。
出煤气换热器的半水煤气与来自管网的中压水蒸气混合,一方面使半水煤气温度上升到变换反应温度,另一方面使半水煤气增湿,并达到设计要求所需要的汽气比进入第一变换炉发生变换反应,在第一变换炉内CO 的变换率可达到60%左右。
经第一变换炉变换后出来的变换气进入煤气换热器与半水煤气逆向换热后进入淬冷过滤器I ,逆向与喷淋下来的冷却水换热并使冷却水汽化,此时变换气的温度下降到230 ℃左右,冷却水和变换气换热后汽化,从而使蒸汽含量达到设计要求,湿变换气进入第二变换炉第一段催化剂床层进行变换反应。
经第二变换炉第一段催化剂床层变换反应后CO 的变换率可达到85%左右,温度上升到280 ℃左右进入淬冷过滤器II ,逆向与喷淋下的冷却水进行热交换,使其温度下降到190 ℃左右,同时补充水蒸气,达到设计要的汽气比进入第二变换炉第二段催化剂床层进行变换,最终CO 的变换率可达到99%。
出第二变换炉第二段的变换气经过变换气换热器后,再经过变换气冷却器降温至40 ℃左右,去后续工段。
第二章 物料衡算及热量衡算2.1设计条件计算基准:1吨NH 3。
设备生产能力:t/h 7222.92430010703=⨯⨯ 由设计所给条件取每吨氨耗用半水煤气3520Nm 3,则每小时的半水煤气用量为:3520×9.7222=34222.2 Nm 3/h初始半水煤气组成见下表2-1。

合成氨是一种重要的工业化学品,广泛用于农业肥料、化肥、塑料、炸药等领域。
为了满足市场需求,设计一个年产2万吨合成氨变换工段的工艺。
合成氨工艺通常包括三个主要步骤:气体净化、合成反应和分离纯化。
以下是一个基本的工艺设计方案。
1.气体净化从天然气中提取氢气(H2)和氮气(N2),一种常用的方法是通过蒸汽重整和高温转热反应。
天然气先经过脱硫除硫化氢(H2S)处理,然后进入蒸汽重整器,与水一起反应生成H2和CO。
再通过转热反应,将CO转化为CO2和H22.合成反应合成反应通常采用哈贝-博斯曼工艺(Haber-Bosch Process),即在高温(400-500摄氏度)和高压(200-300巴)下,将氢气与氮气催化反应生成氨。
反应器通常采用固定床催化剂,催化剂常用的是铁(Fe)或铁钼(Fe-Mo)催化剂。
反应器主要分为顶座和底座两部分,用以升温和降温,以保持恒定的反应温度。
3.分离纯化合成氨的产物中除了氨外还含有一些杂质,如副产物氮氧化物(NOx)和未反应的氢气。
因此,需要对产物进行分离纯化,以获得高纯度的合成氨。
分离纯化一般采用蒸馏、吸附和压缩等方法。
首先,通过蒸馏将氨与轻杂质分离。
然后,使用吸附剂去除重杂质,如CO、CO2和H2O。
最后,利用压缩机将氨气压缩,得到最终产品。
此外,为了实现连续生产,工艺中还需要一些辅助设备,如冷却器、加热器、循环泵和控制阀等。
以上是一个简单的年产2万吨合成氨变换工段的工艺设计方案。
实际设计中还需要考虑各种因素,如安全性、能源消耗、成本等。
同时,工艺设计还应根据具体情况进行优化和改进,以提高产量和效率。

合成氨变换工段是合成氨生产过程中的关键工艺环节之一,它将合成气中的氮气和氢气在催化剂的作用下,通过催化反应转化为合成氨。
本文将围绕年产二十万吨合成氨的变换工段工艺设计进行详细阐述,旨在提供一个完整的工艺设计方案。
首先,变换工段的催化剂选择非常重要。
对于年产二十万吨合成氨的工艺,常用的催化剂有铁素体、铁铬铝混合催化剂等。
这些催化剂在一定的操作条件下,能够实现高效的合成氨转化率和选择性。
在实际应用中,应根据具体工艺要求和经济效益进行选择。
其次,合成气的净化和预热是变换工段的重要准备工作。
合成气中常含有一定的杂质,如氧、水蒸气、二氧化碳等,这些杂质会影响催化剂的活性和寿命。
因此,合成气需要通过一系列净化设备,如除氧、除硫、除水等步骤,将其净化为适合变换反应的合成气。
同时,为了提高反应的热效应,还需要对合成气进行预热,一般可以采用换热器进行热量回收。
接下来是变换反应的具体设计。
变换反应是一个平衡反应,根据Le Chatelier原理,可以通过提高反应温度、降低反应压力、增加氢气过量等方式推动平衡向产氨方向偏移。
在实际设计中,应在考虑较高转化率的前提下,平衡反应速率和催化剂活性与寿命的关系,做出合理的选择。
另外,变换反应需要保持一定的循环气速和循环气气体组成。
循环气速过高会造成能耗增加,循环气速过低则会影响气体传质效果。
循环气气体组成应符合催化剂的操作条件,一般应保持一定的氢气过量,同时控制氮气和氢气的比例。
最后是变换工段的控制策略。
合成氨变换工段是一个高温高压的工艺过程,对于安全和稳定运行,需要建立完善的自动化控制系统。
控制策略应包括反应温度和压力的控制、循环气速和气体组成的控制、催化剂的修复和更换等。
在实际设计中,应结合具体的工艺要求和设备性能,进行综合技术经济分析,选取最佳的工艺参数和操作条件。
同时,在设计过程中还应考虑到工艺的可持续性和环境保护要求,合理利用资源,减少废物排放,实现工艺的可持续发展。

合成氨变换工段工艺设计1. 引言合成氨是一种重要的化工原料,在农业、化工和医药等行业广泛应用。
合成氨的生产过程中,合成氨变换工段是一个关键的工艺环节。
本文将介绍合成氨变换工段的工艺设计。
2. 工艺流程合成氨变换工段的工艺流程包括进料处理、反应器设计、温度控制和产品回收四个重要环节。
2.1 进料处理合成氨的主要原料是氮气和氢气,进料处理环节主要包括氮气和氢气的纯化和混合。
氮气和氢气需要通过特定的纯化设备去除杂质,以确保反应的纯度和效果。
然后,纯化后的氮气和氢气按照一定比例进行混合。
2.2 反应器设计反应器是合成氨变换工段的核心设备,根据反应器设计的不同,可以分为固定床反应器和流化床反应器两种。
固定床反应器是一种较为常见的反应器形式,氮气和氢气催化反应产生合成氨。
固定床反应器需要考虑催化剂的选择、填充物的设计以及反应器的传热设计等因素。
流化床反应器是近年来逐渐应用的一种反应器形式,其优点包括更好的热传递性能和更好的反应效果。
流化床反应器需要考虑反应器的气固分离、催化剂的循环和再生等因素。
2.3 温度控制温度对合成氨反应的影响非常重要,合适的反应温度可以提高反应速率和选择性。
在合成氨变换工段中,需要通过控制进料气体的温度和反应器的温度来实现对反应的控制。
温度控制还需要考虑热量的平衡问题,包括进料气体的预热和产物蒸汽的回收利用等。
2.4 产品回收合成氨变换工段的最终目标是获得高纯度的合成氨产品。
在产品回收环节中,需要进行氨的冷凝和气液分离。
冷凝过程中需要考虑温度和压力的控制,以确保氨的高效冷凝。
气液分离过程中,可以采用吸收液的方式将氨从气相中吸收出来,再进行后续处理和精制。
3. 设备选择合成氨变换工段的设备选择主要包括反应器、纯化设备、冷凝器和分离器等。
反应器的选择需要考虑反应速率、选择性和热传导等因素。
常用的反应器材料有不锈钢、镍基合金等。
纯化设备的选择需要考虑氮气和氢气的纯度要求以及生产规模等因素。

合成氨变换工段工艺过程设计
合成氨是一种氮肥的主要原材料,广泛应用于农业生产中。
合成氨的生产工艺比较复杂,需要经过多个过程的变换才能得到最终的产品。
以下是合成氨变换工段工艺过程的设计。
第一步:氨气合成
氨气合成是合成氨工艺的核心环节,是通过一系列反应将纯净的氢气和氮气合成氨气。
氮气主要来自于空分装置,而氢气主要来自于蒸汽重整装置。
氮气和氢气混合进入催化转化器,经过高温高压催化剂的作用,在催化剂的表面上发生一系列反应,生成氨气。
第二步:氨气变换
氨气变换是将氨气和过量的氮气通过低温催化转化器进行反应,生成高纯度的合成气体。
合成气体主要由氨气、氢气和少量的氮气组成。
合成气体进入变换反应器,在催化剂的作用下,发生一系列反应,将多余的氮气转化为氨气,提高合成气体的纯度。
为了提高合成氨的产率和纯度,还需要进行一系列辅助工艺,如排水处理、冷凝除尘等。
排水处理是为了去除合成氨中的水分,保证合成氨的纯度。
在排水处理过程中,合成氨中的水分会通过分离器分离出来,再经过干燥塔吸附去除水分,最后得到干燥的合成氨。
冷凝除尘是为了去除合成氨中的杂质,保证合成氨的纯度。
在冷凝除尘过程中,合成氨通过冷凝器冷却,使其中的杂质凝结成固体颗粒,然后经过除尘器除去颗粒物,最后得到纯净的合成氨。
综上所述,合成氨变换工段工艺过程的设计包括氨气合成和氨气变换两个主要步骤,同时还需要进行排水处理和冷凝除尘等辅助工艺。
这些步骤的设计要考虑反应温度、反应压力、催化剂的选择和管理,以及对产物的分离、干燥和净化等。
通过合理的工艺设计和操作管理,可以提高合成氨的生产效率和产品质量。

小合成氨厂低温变换工段工艺设计1.工艺流程合成氨的低温变换工艺流程包括氨气脱除、氢气供应、氮氢混合、压缩、变换反应和冷却净化等步骤。
具体流程如下:(1)氨气脱除:从合成气中去除氨气。
合成气通常包括氮气、氢气和少量的甲烷、一氧化碳等。
氨气脱除可以采用吸收剂或者低温冷凝的方式进行。
(2)氢气供应:合成氨需要大量的氢气供应。
氢气可以通过蒸汽重整、部分氧化等方式产生。
(3)氮氢混合:将氮气和氢气按照一定的比例混合,以提供合适的反应物组成。
(4)压缩:将混合气体压缩到合适的工艺压力,以增加反应速率和提高反应效果。
(5)变换反应:将压缩的气体通入低温变换器中,反应产生氨气。
这个过程是一个放热反应,需要控制反应温度和催化剂的作用。
(6)冷却净化:将变换产生的气体冷却,去除其中的杂质和不稳定的气体组分,以获得高纯度的合成氨。
2.工艺参数合成氨的低温变换工段的设计需要考虑多个工艺参数,包括反应温度、反应压力、气体流量、催化剂选择等。
(1)反应温度:低温变换反应需要控制在适当的温度范围内进行。
反应温度过高会导致催化剂失活,而温度过低则会影响反应速率和产氨量。
(2)反应压力:反应压力是影响反应平衡的重要参数,对氨气产率和选择性有很大影响。
通常情况下,反应压力较高可以提高氨气产率,但同时也增加了设备的投资和运行成本。
(3)气体流量:气体流量直接影响反应物在催化剂上的接触和反应速率。
合适的气体流量可以提高反应效果,但如果流量过大,会增加压力损失和能耗。
(4)催化剂选择:催化剂是低温变换反应的关键,其选择需要考虑活性、稳定性和寿命等因素。
常用的催化剂有铁、铂、钼等,可以单一使用或者组合使用。
3.安全控制在低温变换工段的设计中,安全控制是非常重要的。
一方面,低温反应需要保证设备和管道的密封性和抗冻性,以防止设备爆炸和泄漏事故。
另一方面,反应温度和压力需要在合适的范围内稳定控制,以防止设备超负荷运行和产生危险反应。
此外,还需要考虑废气处理、电力供应等问题,以确保低温变换工段的安全和稳定运行。

合成氨变换工段设计一、工艺简介合成氨(NH3)是一种重要的化学原料,广泛应用于肥料、化工、冶金等领域。
合成氨通常是通过哈伯-博士过程进行合成的,该过程主要有三个阶段:气化反应、变换反应和分离装置。
其中,变换反应是合成氨反应的核心环节。
二、工艺流程1.进料系统:将氮气(N2)和氢气(H2)以一定的比例通入反应器。
进料系统应包括氮气和氢气的净化装置,以确保进入反应器的气流中不含有不利于反应的杂质。
2.反应器:反应器是合成氨变换的关键装置,需要选择适当的催化剂,并控制合适的反应温度和压力。
反应器的设计应满足以下要求:具有高的转化率和选择性、较小的压力损失、对催化剂具有良好的分布和稳定性。
3.除尘装置:合成氨反应会产生一些固体杂质,如烟尘颗粒等。
除尘装置主要用于去除这些固体杂质,以确保产品的纯度。
4.产品收集系统:将合成氨收集并进行后续的分离和提纯。
收集系统应包括冷凝器、吸收塔等设备,以确保合成氨的回收率。
三、工艺参数1.反应温度:合成氨变换反应通常在300-500°C的温度范围内进行,具体温度的选择应考虑催化剂的活性和热力学平衡等因素。
2.反应压力:合成氨变换反应的压力通常在10-30MPa之间,压力的选择应使反应的平衡位置有利于产生高的氨气浓度。
3.氮气和氢气的比例:氮气和氢气的比例对合成氨反应的转化率和选择性有重要影响,一般通过调节氮气和氢气的流量比例来控制。
4.催化剂的选择:催化剂的选择应考虑其活性和稳定性,促使反应的进行,并提高催化剂的利用率。
四、工艺设备1.反应器:选用合适的反应器,如固定床反应器或流化床反应器,确保催化剂的分布均匀和反应的高转化率。
2.净化装置:包括氮气和氢气的净化装置,用于去除进料中的杂质。
3.冷凝器:用于冷却和冷凝反应器出口的气体,以便进行后续的分离和提纯。
4.吸收塔:用于收集合成氨气体,并进行后续的分离和提纯。
五、工艺控制1.温度控制:根据反应的热力学特性,控制反应温度在适当的范围内,以提高反应的转化率和选择性。

五万吨合成氨变换工段工艺初步设计合成氨(NH3)是一种广泛应用于肥料生产、化工工业和能源领域的重要中间体。
在这个问题中,我们将进行五万吨合成氨的变换工段工艺初步设计。
1.工艺选择合成氨的常见工艺路线包括谷氨酸法、煤气化法、重整法和协同催化法等。
鉴于规模和技术可行性,我们将选取协同催化法作为工艺路线。
2.原料准备合成氨的主要原料是氮气(N2)和氢气(H2)。
N2可通过空分设备分离出来,而H2可通过天然气蒸汽重整装置或制氢装置生产。
原料气体经过净化步骤去除杂质,确保质量符合要求。
3.催化反应催化反应采用协同催化剂,具体是煤基催化剂和铁基催化剂的组合。
反应器采用固定床反应器,进料气体在催化剂上进行反应。
反应条件包括压力、温度和气体配比等,根据实际情况进行确定。
常用的反应条件为高压(3-10MPa)、高温(350-550℃)和适当的氮氢比例。
4.产品分离反应生成的氨气通过冷却、减压和吸附等步骤进行分离。
氨气与水通过冷却器进行热交换,降低温度。
然后通过分离器进行减压,使氨气从溶液中析出。
氨气回收后,通过吸附剂去除残余的杂质,以达到纯度的要求。
最后,通过压缩机将氨气压缩到适当的压力,以供应下游工艺。
5.傍热回收在冷却和减压过程中,需要高能量输入。
为了节约能源,可以采用傍热回收技术,将部分废热回收利用。
具体的方案包括采用换热器进行热交换和采用适当的废热锅炉等。
6.废水处理合成氨过程中会产生废水,其中含有氨氢离子和少量的有机物。
为了达到环保要求,需要进行废水处理。
常见的废水处理方法包括中和、沉淀、过滤和氨气脱除等步骤。
7.安全措施在合成氨生产过程中,需要采取一系列安全措施,包括定期检查设备,防止泄漏和爆炸,储存和运输氨气等。
同时,要培训和教育操作人员,提升他们的安全意识。
8.自动化控制合成氨生产是一个复杂的过程,需要精确的控制和监测。
可以采用自动化控制系统,实时监控反应温度、压力、流量等参数,并进行相应的调整,以保证产品质量和工艺的稳定运行。
6万吨合成氨变换工段工艺设计合成氨变换工段是合成氨生产过程中的关键环节,它将通过合成产生的氨气进行变换,使其转化为氮气和水。
本文将对6万吨合成氨变换工段的工艺设计进行详细介绍。
1.工艺原理合成氨变换工段采用的是低温变换法,主要基于以下反应:2NH3⇌N2+3H2该反应是一个平衡反应,具有可逆性。
为了提高反应速率和收率,需满足一定的条件,包括适宜的温度、压力和催化剂。
2.工艺流程合成氨变换工段的工艺流程一般包括进料、加热、反应、冷却和分离等步骤。
(1)进料:合成氨气从合成回收装置进入变换工段。
(2)加热:合成氨气在加热炉中加热至适宜的反应温度。
常用的加热方式包括电阻加热和燃气加热。
(3)反应:加热后的氨气进入变换器中进行反应。
变换器一般采用多层催化剂填料,以提高反应效率。
反应温度和压力需根据反应动力学和平衡原理进行优化选择。
(4)冷却:反应后的气体在冷却器中冷却,以控制温度,防止反应逆向进行。
(5)分离:冷却后的气体经过分离装置进行分离,将氮气、水和未反应的氨气分离开。
一般采用冷凝器和吸附器等装置进行分离。
3.工艺参数合成氨变换工段的工艺参数包括反应温度、压力、催化剂选择和反应时间等。
(1)反应温度:反应温度对合成氨的变换速率和收率有着重要影响。
通常选择适宜的反应温度,一般在300-500℃之间。
(2)反应压力:反应压力也是一个重要的工艺参数,它会影响变换速率和收率。
一般选择适宜的反应压力,大致在15-35MPa之间。
(3)催化剂选择:催化剂选择直接关系到反应效果。
常用的催化剂有铁、镍、钼等。
催化剂要具有高效催化性能和较好的稳定性。
(4)反应时间:反应时间需要根据生产规模和设备容量进行确定。
一般情况下,生产规模越大,反应时间越长。
4.工艺优化为了提高工艺效果和经济性,还可以采取以下优化措施。
(1)催化剂再生:催化剂在反应过程中会发生失活,需要定期进行再生。
通过再生可以延长催化剂寿命,减少生产成本。
毕业设计任务书一.设计要求:1.进行工段工艺流程设计,绘制带主要控制点的工艺流程图。
2.进行工段物料计算、热量计算,并绘制物料衡算表、热量衡算表。
3.进行工段设备设计、选型,制备设备一览表。
4.编写工段工艺初步设计说明书。
5.绘制主要设备结构图和工艺流程图设计原始数据:以在某化工厂的实际数据为原始数据目录说明书 (4)前言 (4)1.工艺原理 (4)2. 工艺条件 (4)3. 工艺流程的选择 (5)4. 主要设备的选择说明 (5)5. 工艺流程的说明 (6)第一章物料与热量衡算 (7)1.水汽比的确定 (7)2.中变炉CO的实际变换率的求取 (8)3.中变炉催化剂平衡曲线 (9)4. 最佳温度曲线的计算 (10)5.中变炉一段催化床层的物料衡算 (11)6.中变一段催化剂操作线的计算 (17)7.中间冷淋过程的物料和热量衡算 (17)8.中变炉二段催化床层的物料与热量衡算 (19)9.中变二段催化剂操作线计算 (23)10.低变炉的物料与热量衡算 (24)11低变催化剂操作线计算 (29)12低变炉催化剂平衡曲线 (29)13.最佳温度曲线的计算 (30)14废热锅炉的物料和热量衡算 (31)15.水蒸汽的加入 (34)16主换热器的物料与热量的衡算 (34)17.调温水加热器的物料与热量衡算 (36)第二章设备的计算 (37)1. 中变炉的计算 (37)2. 主换热器的计算 (42)设计的综述 (6)参考文献 (49)致谢 (50)第一章 物料与热量衡算已知条件:计算基准:1吨氨计算生产1吨氨需要的变换气量:(1000/17)×22.4/(2×22.56)=2920.31 M 3(标)因为在生产过程中物料可能会有损失,因此变换气量取2962.5 M 3(标) 年产3万吨合成氨生产能力(一年连续生产330天): 日生产量:30000/330=90.9T/d=3.79T/h要求出中变炉的变换气干组分中CO %小于2%。
合成氨是一种重要的化工原料,用于生产化肥、烟火药、染料等多种产品。
年产万吨合成氨变换工段的工艺设计是合成氨生产过程中的重要环节,对生产效率和产品质量有着重要影响。
本文将针对年产万吨合成氨变换工段的工艺设计进行详细描述。
首先,年产万吨合成氨变换工段的主要反应是氮气与氢气的结合生成氨气,这是一个放热反应,需要在适当的条件下进行。
工艺设计中需要考虑到反应的速率、平衡和选择合适的催化剂以提高反应效率。
为了保证反应的连续性和稳定性,需要选择合适的反应器。
一般采用固定床反应器,在反应器内放置合适的催化剂,通过控制反应物的供给速率和控制温度,使反应物在反应器内进行有效的转化。
其次,变换工段还需要考虑气体的分离和净化问题。
在变换反应中,除了生成氨气外,还会伴随着一些不完全反应产物、杂质气体和催化剂颗粒等。
这些物质需要通过各种分离和净化操作进行处理,以获得纯度较高的合成氨。
常见的分离和净化操作包括压缩、冷却、洗涤、吸附等。
此外,工艺设计中还需考虑能量的回收和利用。
合成氨生产是一个能量密集型的过程,能源消耗占据了生产成本的很大比重。
因此,在工艺设计中需要考虑能源的回收和利用,以提高能源利用效率。
常见的能量回收和利用方法包括余热回收、废气利用等。
最后,工艺设计中还需要考虑安全和环境因素。
合成氨生产过程中涉及高压、高温、易燃易爆等危险因素,需要采取相应的安全措施来确保生产的安全性。
同时,工艺设计还需要考虑环境保护,减少污染物的排放,采取合适的处理措施进行废气、废水、废渣等的处理。
综上所述,年产万吨合成氨变换工段的工艺设计需要考虑反应速率、催化剂选择、反应器设计、气体分离与净化、能量回收利用、安全和环境等多个方面的因素。
只有充分考虑到这些因素,才能设计出高效、安全、环保的合成氨生产工艺,确保产品质量和生产效率的提高。
合成氨的变换工段是氨的生产过程中的重要环节,其设计与优化对于氨的产量和质量有着重要影响。
下面是一个关于年产50万吨合成氨中变换工段设计的1200字以上的介绍。
1.变换工段的作用和原理变换工段是合成氨工艺中的核心环节,其主要作用是将气态的合成气(由氮气和氢气组成)转化为合成氨。
这一过程是通过在催化剂的作用下,将氮气和氢气通过一系列反应逐步转化为合成氨。
其中最主要的反应是氮气与氢气的催化剂反应,也称为哈伯—波克反应。
2.变换反应的热力学和动力学特性合成氨的变换反应是一个热力学上的放热反应,即在常温下会产生大量的热量。
这一特性对于反应器的设计和操作有着重要影响。
同时,反应速率也是变换反应的重要特性之一、在变换工段中,反应速率的控制是通过反应器的温度、压力和催化剂的选择来实现的。
3.反应器的选择和设计在变换工段中,常用的反应器有固定床反应器和流化床反应器两种。
固定床反应器是将催化剂填充在反应器内,通过气流将气体输入反应器进行反应。
而流化床反应器则是将催化剂以固体颗粒的形式悬浮在气流中进行反应。
两种反应器都有各自的优点和适用范围,具体的选择需要考虑到反应条件、催化剂的活性和成本等因素。
4.反应条件的优化反应条件是指反应器中温度、压力和气体流速等因素的控制。
这些条件对于反应速率和产物质量有着重要的影响。
通常,较高的反应温度和压力可以促进反应速率,但同时也会增加能耗和催化剂磨损等问题。
因此,需要在考虑反应速率的基础上综合考虑能耗和催化剂寿命等因素,寻找最优的反应条件。
5.催化剂的选择和优化催化剂是变换反应中的关键因素,其选择和优化对于反应速率和产物质量有着至关重要的影响。
合成氨的变换反应通常采用铁基催化剂或铁铬双金属催化剂。
催化剂的活性和稳定性是选择催化剂的两个主要指标。
而在实际操作中,催化剂的中毒和失效问题也需要考虑。
综上所述,年产50万吨合成氨中变换工段的设计是一个复杂而重要的工作。
需要综合考虑反应速率、能耗、催化剂选择和产物质量等多个因素,并通过合理的反应器设计和反应条件的优化来实现高效的合成氨生产。
合成氨变换工段工艺过程设计合成氨是工业上重要的基础化工原料之一,广泛应用于农业、化工、制药和塑料等领域。
合成氨的工艺过程设计涉及到合成氨反应器、氨分离系统、废气处理系统以及其他辅助设备。
一、合成氨反应器合成氨的反应器一般采用固定床催化剂的方式进行,反应温度常在350-550℃,反应压力常在80-200atm之间。
催化剂常采用以铁为主的复合催化剂,其主要成分有铁、铝、钾等金属氧化物。
该反应器的主要作用是将反应物氮气和氢气在催化剂的催化下发生氧化还原反应生成氨气。
二、氨分离系统由于氨合成反应气体中还含有大量的未反应氢气、氮气以及少量的二氧化碳、水蒸汽和甲烷等杂质物,因此需要将氨与这些杂质物进行分离。
首先对反应气体进行冷凝和除湿处理,以去除水蒸汽;然后采用吸附剂进行氨的吸附和脱附,以去除未反应的气体;最后再通过精馏系统进行氢、氮等杂质物的分离,得到高纯度的氨。
三、废气处理系统氨合成反应会产生一些副产物和废气,包括尾气、废液、废水等。
尾气中主要含有未反应的氮气、未分离的氢气、氧气和少量氨等物质。
因此需要对这些废气进行深度处理,以降低对环境的污染。
常见的处理方法包括尾气洗涤、氨的催化氧化等。
四、其他辅助设备合成氨生产过程中还需要用到一些辅助设备,如氢气制备系统、氮气制备系统、冷却系统、压缩系统、脱硫系统、催化剂再生系统等。
这些设备的作用是为合成氨反应提供所需的气体原料、冷却剂以及对反应物质进行净化和处理。
总结起来,合成氨的工艺过程设计主要涉及合成氨反应器、氨分离系统、废气处理系统以及其他辅助设备。
通过合理设计和配置这些设备,能够实现高效、稳定和环保的合成氨生产过程。
摘要变换工序是合成氨中最重要的工序之一,在合成氨工艺的流程中起着非常重要的作用本次设计为70 kt/a合成氨变换工段的工艺设计。
本设计采用全低变的工艺流程.。
根据有关文献资料,完成物料、热量的计算。
并对第一变换炉、第二变换炉、煤气换热器以及变换气换热器等主要设备进行选型计算。
并做出了合成氨变换工段全低变的工艺流程图和设备布置图。
所得结果基本满足设计要求,工艺流程可行。
关键词:合成氨;低温变换;热量衡算;物料衡算.AbstractTransform processes is one of the most important processes, and it p lays a very important role in the industry of synthetic ammonia.The task is the design of shift process in 70 kt/a NH3. The low-temperature shift technology was adopted in this calculation.According to the relevant cultural heritage data, complete the calculation of material, calories. Furthermore, the size and type of the equipments were determined such as heat exchanger, shift converter, etc.Also do to synthesize an all of the ammonia transformation work segment low craft flow chart and equipments changing set out diagram.The results meet the requirements of the design task well, the craft process can go.摘要 (I)Abstract (II)第一章前言 (1)1.1 变换气反应原理 (1)1.2 CO变换反应化学平衡 (2)1.3 CO低温变换催化剂 (5)1.3.1 低变催化剂的发展 (5)1.3.2 低变催化剂的主要成分 (5)1.3.3 催化剂的活性降低和中毒 (7)1.4 工艺流程简述 (8)第二章物料衡算及热量衡算 (10)2.1设计条件 (10)2.2 CO全变换过程总蒸汽比的计算 (10)2.3第一变换炉催化剂床层物料与热量衡算 (11)2.3.1入第一变换炉催化剂床层汽气比 (11)2.3.2 CO平衡变换率及出催化剂床层气体的组成 (12)2.3.3 第一变炉热量衡算 (13)2.3.4第一变换炉催化剂层CO变换反应平衡曲线 (14)2.3.5 CO在第一变换炉催化剂床层最适宜温度 (15)2.3.6 CO在第一变换炉催化剂层变换反应操作线 (16)2.4 第二变换炉第一段催化剂层物料及热量衡算 (17)2.4.1 第二变换炉第一段催化剂层汽/气比 (17)2.4.2 第二变换炉第一段催化剂层CO的平衡转化率计算 (18)2.4.3 出口温度校核 (18)2.4.4 第二变换炉第一段催化剂热量衡算 (18)2.4.5 第二变换炉第一段催化剂床层平衡曲线计算 (19)2.4.6 CO在第二变换炉第一段催化剂层最适宜变换温度 (20)2.4.7 CO在第二变换炉第一段催化剂层变换反应操作线 (20)2.5 第二变换炉第二段催化剂床层物料及热量衡算 (21)2.5.1 第二变换炉第二段催化剂层CO的平衡转化率计算 (22)2.5.2第二变换炉第二段催化剂热量衡算 (22)2.5.3 平衡温距校核 (23)2.5.4 第二变换炉第二段催化剂床层平衡曲线计算 (24)2.5.5 CO在第二变换炉第二段催化剂层最适宜变换温度 (24)2.5.6 CO在第二变换炉第二段催化剂层变换反应操作线 (25)2.6 煤气换热器热量衡算 (26)2.7 变换气换热器热量衡算 (27)2.7.1进设备热量计算 (27)2.7.2出设备热量计算 (28)第三章主要设备计算 (29)3.1第一变换炉的计算 (29)3.1.1 催化剂用量计算 (29)3.1.2 催化剂床层阻力计算 (30)3.2第二变换炉的计算 (31)3.2.1 第二变换炉第一段催化剂用量计算 (31)3.2.2 第二变换炉第二段催化剂用量计算 (32)3.2.3 第二变换炉催化剂床层阻力的计算 (33)3.3煤气换热器的计算 (35)3.3.1 设备直径及管数确定 (36)3.3.2 设备规格的确定 (37)3.3.3 传热系数计算 (37)3.3.4 传热面积计算 (42)3.3.5 列管长度的计算 (42)主要设备一览表 (43)设计结果及总结 (44)参考文献 (45)致谢 (46)第一章 前言合成氨生产常用的原料包括:焦碳、煤、焦炉气、天然气、石脑油和重油。
不论以固体、液体或气体为原料,所得到的合成氨原料气中均含有一氧化碳。
固体燃料气化所得半水煤气中的一氧化碳含量为28%~30%,烃类蒸汽转化为12%~13%,焦炉转化气为11%~15%,重油部分氧化为44%~48%。
一氧化碳的清除一般分为两次。
大部分一氧化碳,先通过变换反应,即在催化剂存在的条件下,一氧化碳与水蒸气作用生成氢气和二氧化碳。
通过变换反应,既能把一氧化碳变为易于清除的二氧化碳,同时,又可制得与反应了的一氧化碳相等摩尔的氢,而所消耗的只是廉价的水蒸气。
因此,一氧化碳的变换既是原料气的净化过程,又是原料气制造的继续。
最后,残余的一氧化碳再通过铜氨液洗涤法、液氮洗涤法或甲烷化法等方法加以清除。
变换工段是指CO 与水蒸气反应生成二氧化碳和氢气的过程。
目前,变换工序主要有“全低变”工艺和“中低变”工艺,此次设计运用的是“全低变”工艺“全低变”工艺是90年代在我国小合成氨厂开始使用的,是从“中低变”演变而来,使用低温活性较好的B302Q 、B303Q 等耐硫变换催化剂,各段进口温度均在200 ℃左右。
经过几年的发展,随着耐硫低温催化剂的开发利用,“全低变”的工艺和设备不断完善,操作水平也进一部提高,目前“全低变”工艺已进入成熟阶段。
该工艺具有蒸汽消耗低、系统阻力小、生产强度大等优点。
1.1 变换气反应原理合成氨生产需要的原料气是H 2和N 2,而半水煤气中含有约30%左右的CO ,需要将其除去。
变换工段的目的就是将半水煤气中的CO 除去,在本质上是原料气净化的一个过程。
为了将CO 除去,工业上采用的方法是:在催化剂存在的条件下,利用较为廉价的水蒸气与CO 反应,生成H 2和CO 2。
原料气中的一氧化碳与水蒸汽的变换反应可用下式表示:222CO+H O CO +H Q =+ (1-1)此反应为可逆放热反应,反应热为40964 J/mol ,当开车正常生产后,即可利用其反应热来维持过程的继续进行。
在一般情况下,一氧化碳与水蒸汽直接进行反应,其变换反应的速度是很慢的,如果用催化剂催化,则可以加快反应速度,大大有利于变换反应的进行。
随着一氧化碳变换反应的进行,伴随着微量的副反应发生,主要有如下几种:(1)甲烷的生成Q ++=+242CO CH 2H 2CO (1-2)Q ++=+O H CH 3H CO 242 (1-3)Q ++=+O 2H CH 4H CO 2422 (1-4)(2)一氧化碳的分解反应Q ++=2CO C 2CO (1-5)(3)有机硫的转化反应S H CO H COS 22+=+ (1-6)S H CO O H COS 222+=+ (1-7)S 2H CO O 2H CS 2222+=+ (1-8)1.2 CO 变换反应化学平衡一氧化碳和水蒸汽的变换反应系可逆反应。
Q H CO O H CO 222++=+其平衡常数为:222222CO H CO H P CO H O CO H Oy y r r K y y r r =⋅ (1-9) 式中:y i ——各组分的摩尔分数r ——气体的逸度系数K p ——CO 的平衡常数由于小合成氨厂的变换反应多在压力<2.0 M P a ,温度为180~250 ℃条件下进行的,其逸度系数接近于1,即:2221CO H r CO H O r r k r r == (1-10)则式(1-9)可简化为:222222CO H CO H P CO H O CO H O y y P P K y y P P == (1-11)式中,P i --各组分的分压 由于变换反应是一个放热反应,考虑平衡常数是温度的函数,且随温度的升高而降低。
平衡常数与温度关系的表达式很多,数值各不相同,这是由于恒压热容等基础热平衡数据不同所致。
本设计可采用下面的公式计算[1]。
3722185lg 0.11021lg 0.621810 1.060410 2.218P K T T T T--=-+⨯-⨯- (1-12)式中,T ——温度,K3725025.163exp(0.0936ln 1.455510 2.488710 5.2894)P K T T T T--=-+⨯-⨯- (1-13)在变换范围内,平衡常数也可用下面简化式计算:4757ln 4.33P K T=- (1-14) 式(1-14)在低温下计算出的K p 与式(1-12)及(1-13)相差较大,温度越高误差越小。
CO 变换反应的化学平衡的影响因素:a. 温度温度对变换反应的影响较大:温度升高,反应速度加快。
从化学平衡来看,降低反应温度,增加蒸汽用量,有利于反应向生成氢气和二氧化碳的方向进行,可以提高CO 平衡转化率。
在变换反应的初期,反应物浓度高,提高反应温度,可加快正反应;在变换反应的后一阶段,二氧化碳和氢气的浓度增加,逆反应速度加快,因此,须设法降低反应温度,使逆反应速度减慢,这样可以得到较高的变换率。
但降低温度也减慢了反应速度,降低了催化剂的生产能力,应综合考虑。
对于一氧化碳含量较高的半水煤气,开始反应时,为了加快反应速度,一般要在较高的温度下进行,而在反应的后一阶段,为了使反应比较完全,就必须使温度降低一些,工业上采取的两段中温变换就是根据这一概念设计确定的。
对于一氧化碳含量在2%—4%的中温变换气体,只需要在230 ℃左右,用低温变换催化剂进行低温变换。
此外,反应温度与催化剂的活性有很大的关系,一般工业用的变换催化剂低于某一温度反应便不能正常进行,而高于某一温度也会损坏催化剂,因此一氧化碳变换反应必须在催化剂的适用温度范围内选择合理的工艺条件。