最新整理血清尿素氮的测定教程文件
- 格式:doc
- 大小:20.50 KB
- 文档页数:3

血清尿素的测定标准操作规程【目的】学习血清尿素(Urea)测定方法,了解其意义。
【原理】血清尿素(Urea)是蛋白质的正常代谢产物。
它的测定是常用的衡量肾小球功能的指标之一。
肾性血清尿素含量增加,提示肾小球损伤。
是研究药物肾毒性的重要指标之一。
【器材】兔固定架、注射器、烧杯、可见分光光度计、试管、水浴【药品】0.5%氯化高汞溶液、生理盐水【动物】家兔2只【方法】取家兔2只,1只注射氯化高汞5ml/kg(0.5%氯化高汞溶液1.0ml/kg),另1只注射等量的生理盐水。
48小时后,从家兔耳静脉取血1ml,制取血清,按血清尿素测定方法测定血清尿素含量。
【结果】记录2只家兔血清尿素含量,比较并分析其差别。
附血清尿素(Urea)测定方法【原理】尿素与二乙酰在酸性反应环境中加热,缩合生成色素原二嗪化合物。
因二乙酰不稳定,不宜直接加入,可由化学反应生成。
通常由反应系统中二乙酰一肟与强酸作用,产生乙二酰。
二乙酰和尿素反应,缩合生成红色的二嗪。
根据颜色深浅确定尿素含量的多少。
【试剂】(1)酸性试剂:在三角烧瓶中加蒸馏水约100ml,然后加入浓硫酸44ml及85%磷酸66ml。
冷至室温,加入硫氨脲50mg及硫酸镉(CdSO4·8H2O)2g。
溶解后用蒸馏水稀释至1L,置棕色瓶中冰箱保存,可稳定6个月。
(2)二乙酰-肟溶液:称取二乙酰-肟20g,加蒸馏水约900ml,溶解后,再用蒸馏水稀释至1L,置棕色瓶中,贮放冰箱内可保存半年。
(3)尿素标准贮存液(100mmol/L):称取干燥纯尿素(MW=60.06)0.6g,溶解于蒸馏水中,并稀释至100ml,加0.1g叠氮钠防腐,置冰箱内可稳定半年。
(4)尿素标准液应用液(5mmol/L):取5.0ml贮存液用无氨蒸馏水稀释至100ml.【操作】按表T4-1进行混匀后,置沸水中加热12分钟,置冷水中冷却5分钟后,用分光光度计在波长540nm,以空白管调至零点。
比色读取标准管及测定管的吸光度。

血、尿液尿素氮(BUN)测定作业指导书1.实验原理Vitros BUN/UREA试剂是一种干燥,多涂层的,在透明的聚合物支撑基片上涂有分析成份的化学干片。
将一滴患者样品滴于干片上,分布层会使之均匀地分布。
水和非蛋白质成份进入下面的试剂层,与尿素酶反应生成氨。
半透膜只允许氨进入呈色反应层,与指示剂发生反应。
经过一段固定的孵育时间后,通过测定呈色剂的反射强度可间接求出尿素氮的含量。
测定方式:比色法波长:670nm测试时间和温度:37℃约5分钟反应过程:尿素酶非蛋白质成份+水—————→氨+ 二氧化碳氨+氨指示剂—————→呈色剂2. 标本:2.1 病人准备:血清无特殊要求。
要留取24小时尿样。
2.2 样品类型:血清;肝素锂/钠和EDTA抗凝血浆。
定时收集的,稀释后的尿样。
2.3 标本采集与处理:2.3.1 血清和血浆样品特别要注意的是:血清;肝素锂/钠和EDTA抗凝血浆;不要用氟化钠作防腐剂,因为氟会抑制尿素酶。
样品采集后4小时内要离心标本,吸出血清。
处理样品时要将其当成生物污染品。
2.3.2 尿液样品定时或随时采集的尿液,特别要注意的是:不能使用以下防腐剂:冰醋酸,浓盐酸,硼酸,硼粉或甲酸钠硼酸,样品在测试前要冷藏。
测试前将1份样品加20 份试剂级别的水进行稀释。
将测试结果乘以21,就得到原始样品中尿素氮的浓度。
冷藏的样品不能立即测试。
处理样品时要将其当成生物污染品。
3. 标本的存放:血清、血浆室温下最多1天;4~8℃冷藏最多5天;-18℃冷冻保存可长达6个月。
尿液样品在测试前要冷藏。
4. 标本的运输:样品要放在带盖的容器内以防污染和蒸发。
5. 标本拒收的标准:污染、抗凝剂、防腐剂不符合要求,标本放置时间过长。
6. 试验材料:6.1测试BUN所需的物品包括:Vitros化学定标物Kit1;Vitros特制质控液;Vitros 7%BSA稀释液。
xx厂家提供原装进口,试剂盒外包装上标明了测试项目名称,试剂标签代码,有效期限和储藏温度。

血清尿素氮BUN谷氨酸脱氢酶测定法作业指导书1.实验原理脲酶-谷氨酸脱氢酶(Urease-GLDH)连续监测法。
尿素被脲酶水解产氨。
在NADH的存在下,氨和α-酮戊二酸反应生成谷氨酸,NADH同时被氧化成NAD+。
NADH的减少和样品中尿素浓度成正比。
本法是连续监测法。
脲酶尿素+ 2H2O 2 NH4++ 2 HCO3-谷氨酸脱氢酶NH4++α-酮戊二酸+NADH L-谷氨酸+NAD++H2O2 标本:2.1 病人准备:血清无特殊要求。
要留取24小时尿样。
2.2 类型:血清、血浆(不可使用肝素铵)、新鲜尿液。
无溶血和凝块的血清,如果必须使用血浆,建议使用无铵离子的抗凝血剂,如EDTA和肝素钠。
用新鲜尿液作样品时,用蒸馏水作1:100稀释。
3. 标本存放:血清或血浆稳定性:4~25℃保存可稳定7天;-20℃保存可稳定1年。
尿液稳定性:20~25℃保存可稳定2天;4~8℃保存可稳定7天;-20℃保存可稳定1个月。
4. 标本运输:常温条件下保存运输。
5. 标本拒收标准:细菌污染的标本。
6. 实验材料6.1 试剂:申能尿素测定试剂盒(142 3107170 1 试剂1:6×64ml+试剂2:6×16ml)6.1.1 试剂组成试剂1:Tris缓冲液pH7.8 120mmol/Lα-酮戊二酸7mmol/LADP 0.6mmol/L谷氨酸脱氢酶≥1000U/L脲酶≥6000U/L试剂2:NADH 0.25mmol/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存试剂保存于2~25℃,若无污染,可稳定至失效期。
试剂不可冰冻。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5 注意事项:此试剂为体外诊断用。
不要入口,吞下有害。
保护剂为叠氮钠,避免接触皮肤及粘膜,与下水管中的铅反应形成爆炸性化合物,即使只含有少量的叠氮钠,如果排向下水道请用大量的水冲洗。

实验十三血清尿素氮测定(脲酶—Berthelot比色法)一、实验目的与要求1 了解血液尿素氮(BUN)在人体营养学上的生理学意义及其在代谢上的重要性。
2 掌握血液尿素氮测定方法及721分光光度计或AT648半自动生化多用仪的使用方法和现代生化检测试剂盒的应用。
二、实验原理尿素在脲酶作用下分解生成氨。
在碱性条件下,经次氯酸氧化生成的氯胺与苯酚被亚硝基铁氰化钠催化生成蓝色的靛酶。
其反应式为: CH2NH2N尿素O+HOH脲酶NH3彩+CHOH2N氨基甲酸O-2NH3+CO2氨NH3+OCl-NH2Cl+OH-次氯酸氨胺催化剂NH2Cl+OH+OH-Cl-+H2O+HONH2苯酚P胺基苯酚HONH2+OH-+O2==N——O-+H2O酚靛三、实验仪器与试剂1 仪器(1) AT648半自动生化分析仪1台;(2) 4孔恒温水浴锅1个;(3)振动摇床1台。
2 分组及仪器2人一组,每组仪器包括:(1)试管架1个;(2) 2ml试管10个;(3) 20μl微量加样器1个;(4) 1ml移液管1个;(5) 5ml移液管2个;(6)吸耳球1个;(7)搪瓷盘1个;(8)微量加样滴头;(9)吸水纸。
3 本试剂盒内含5种试剂:(1)脲酶(冻干) 2瓶(2) pH 8.0缓冲液:由乙二胺四乙酸二钠盐和磷酸氢二钾组成 1×46ml(3)显色剂Ⅰ:由苯酚和亚硝基铁氰化钠组成 1×225ml(4)显色剂Ⅱ:由氢氧化钠和安替福民组成 1×225ml(5)尿素氮标准液(20mg/dl) 2×2ml四、实验步骤1 血清(1)取脲酶一瓶,用23.0ml pH 8.0缓冲液溶解。
(2)于一系列试管中,按下表加入各溶液。
表131系列反应管中所加溶液的量空白管标准管样品管样品(μl)——20标准液(μl)—20—酶液(μl)0.50.50.5 (3)于37℃水浴中保温15min,然后各管分别加入显色剂Ⅰ和显色剂Ⅱ各2.5ml。
![血清尿素氮的测定[方案]](https://uimg.taocdn.com/90f2e958ff4733687e21af45b307e87100f6f855.webp)
血清尿素氮的测定【目的要求】1.了解血清尿素氮测定的方法及临床意义。
2.复习尿素的生成机理及其意义。
【实验原理】血清(或血浆)中的尿素,在尿素氮试剂的酸性环境中与二乙酰-肟(DAM)共沸后,可缩合成一红色化合物,称为fearon反应。
其颜色的深浅与血清(或血浆)中尿素的含量成正比,与同样处理的尿素氮标准液比色,即可测算出血清(或血浆)中尿素氮的含量。
【实验材料】1.器材刻度吸管(0.1ml、2ml、10ml)恒温水浴箱分光光度计2.试剂(1)待测血浆(2)尿素氮试剂(3)二乙酰-肟试剂(4)尿素氮标准液【操作步骤】取试管三支按下表操作1:4稀释血清(或0.1血浆)尿素氮标准液0.1(0.02mg/ml)蒸馏水0.1二乙酰-肟0.5 0.5 0.5尿素氮试剂 5.0 5.0 5.0 混匀,置沸水浴中加热15min,立即用自来水冷却5分钟。
分光光度计选用540nm波长,以空白管调零点,读取各管吸光度。
计算及结果分析尿素(mg%)×尿素氮标准液浓度*5(mg/ml;mg/100ml)【注意事项】1. 此法灵敏度高,用量极微(一般只需0.02ml血清即可)。
本实验是先将血清用生理水以1:4加以稀释再取0.1ml,故最后计算时,应乘以稀释倍数“5”2. 试剂中加入硫胺脲和镉离子,可增进显色强度和色泽稳定性,但仍有轻度褪色现象(小于5%/h)。
3. 此法操作简单,特异性强,不受其他非蛋白质含氮化合物如尿酸、肌酸等影响,但应控制好实验条件。
4. 吸管必须校正,使用时务必注意清洁干净,加量务必准确。
5.尿液中的尿素氮也可用此法进行测定。
由于尿液中尿素氮含量高,标本需用蒸馏水以1:50稀释。
如果呈色后吸光度仍超过本法的线性范围,还需将尿液再稀释,重新测定。
【思考题】。


实验十三血清尿素氮测定(脲酶—Berthelot比色法)一、实验目的与要求1 了解血液尿素氮(BUN)在人体营养学上的生理学意义及其在代谢上的重要性。
2 掌握血液尿素氮测定方法及721分光光度计或AT648半自动生化多用仪的使用方法和现代生化检测试剂盒的应用。
二、实验原理尿素在脲酶作用下分解生成氨。
在碱性条件下,经次氯酸氧化生成的氯胺与苯酚被亚硝基铁氰化钠催化生成蓝色的靛酶。
其反应式为: CH2NH2N尿素O+HOH脲酶NH3彩+CHOH2N氨基甲酸O-2NH3+CO2氨NH3+OCl-NH2Cl+OH-次氯酸氨胺催化剂NH2Cl+OH+OH-Cl-+H2O+HONH2苯酚P胺基苯酚HONH2+OH-+O2==N——O-+H2O酚靛三、实验仪器与试剂1 仪器(1) AT648半自动生化分析仪1台;(2) 4孔恒温水浴锅1个;(3)振动摇床1台。
2 分组及仪器2人一组,每组仪器包括:(1)试管架1个;(2) 2ml试管10个;(3) 20μl微量加样器1个;(4) 1ml移液管1个;(5) 5ml移液管2个;(6)吸耳球1个;(7)搪瓷盘1个;(8)微量加样滴头;(9)吸水纸。
3 本试剂盒内含5种试剂:(1)脲酶(冻干) 2瓶(2) pH 8.0缓冲液:由乙二胺四乙酸二钠盐和磷酸氢二钾组成 1×46ml(3)显色剂Ⅰ:由苯酚和亚硝基铁氰化钠组成 1×225ml(4)显色剂Ⅱ:由氢氧化钠和安替福民组成 1×225ml(5)尿素氮标准液(20mg/dl) 2×2ml四、实验步骤1 血清(1)取脲酶一瓶,用23.0ml pH 8.0缓冲液溶解。
(2)于一系列试管中,按下表加入各溶液。
表131系列反应管中所加溶液的量空白管标准管样品管样品(μl)——20标准液(μl)—20—酶液(μl)0.50.50.5 (3)于37℃水浴中保温15min,然后各管分别加入显色剂Ⅰ和显色剂Ⅱ各2.5ml。
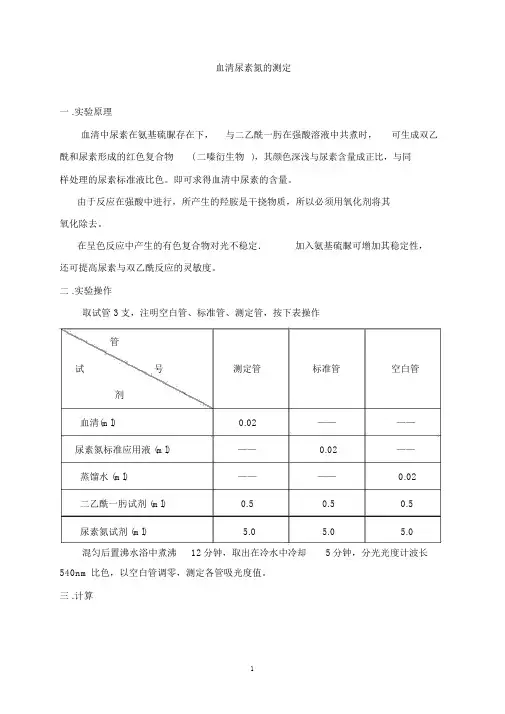
血清尿素氮的测定一 .实验原理血清中尿素在氨基硫脲存在下,与二乙酰一肟在强酸溶液中共煮时,可生成双乙酰和尿素形成的红色复合物( 二嗪衍生物),其颜色深浅与尿素含量成正比,与同样处理的尿素标准液比色。
即可求得血清中尿素的含量。
由于反应在强酸中进行,所产生的羟胺是干挠物质,所以必须用氧化剂将其氧化除去。
在呈色反应中产生的有色复合物对光不稳定.加入氨基硫脲可增加其稳定性,还可提高尿素与双乙酰反应的灵敏度。
二 .实验操作取试管 3支,注明空白管、标准管、测定管,按下表操作管试号测定管标准管空白管剂血清(ml) 0.02 ————尿素氮标准应用液 (ml) ——0.02 ——蒸馏水 (ml) ————0.02二乙酰一肟试剂 (ml) 0.5 0.5 0.5尿素氮试剂 (ml) 5.0 5.0 5.0混匀后置沸水浴中煮沸12分钟,取出在冷水中冷却5分钟,分光光度计波长540nm比色,以空白管调零,测定各管吸光度值。
三 .计算测定管吸光度血清尿素氮(mmol / L ) = ——————— X 17.85标准管吸光度正常值参考范围3. 57~ 14. 28mmol/ L四 .临床意义血液中非蛋白含氮化合物包括尿素、尿酸、肌酸、肌酐、胆红素及氨等。
其中尿素含量约占l / 3~ 1/ 2。
尿素是蛋白质代谢的产物.通过肾脏排出,故测血清尿素氮可作为检测肾脏功能的试验,并且其增高程度与病变的严重程度呈平行关系。
五 .试剂1.尿素氮试剂:蒸馏水lOOml ,浓硫酸 44ml, 85%磷酸 66ml,冷却至室温后,加氨基硫脲50mg,硫酸镉 (3CdSO4· 8H 2O)2g ,溶解后稀释至1000ml。
2.20g/ L 二乙酰一肟试剂:称取二乙酰一肟20g,加入蒸馏水约900ml,溶解后稀释至 1000ml.3.尿素氮标准贮存液 (357mmol/L):称取尿素 1.072g溶解于蒸馏水中定容至 1000ml。


一、实验目的1. 掌握血清尿素含量测定的原理和方法;2. 熟悉实验操作步骤,提高实验技能;3. 了解血清尿素在临床医学中的意义。
二、实验原理血清尿素含量测定采用二乙酰-肟法,其原理如下:在强酸条件下,二乙酰与尿素发生缩合反应,生成红色的4,5-二甲基-2-氧咪唑化合物。
该化合物的颜色深浅与尿素的含量成正比。
通过比色法,可以计算出血清中尿素的含量。
三、实验材料1. 试剂:二乙酰-肟试剂、血清、盐酸、氢氧化钠、蒸馏水等;2. 仪器:紫外可见分光光度计、移液器、试管、试管架等。
四、实验步骤1. 标准曲线绘制:(1)取6支试管,分别加入0、0.2、0.4、0.6、0.8、1.0ml的标准尿素溶液;(2)向各试管加入2ml的二乙酰-肟试剂,充分混匀;(3)将试管置于60℃水浴中反应30分钟;(4)取出试管,用蒸馏水定容至5ml;(5)以蒸馏水为空白,在波长540nm处测定各管的光密度(OD);(6)以尿素浓度为横坐标,OD值为纵坐标,绘制标准曲线。
2. 血清尿素含量测定:(1)取6支试管,分别加入0、0.2、0.4、0.6、0.8、1.0ml的血清样本;(2)按照标准曲线绘制步骤中的操作,进行反应和测定;(3)以蒸馏水为空白,在波长540nm处测定各管的光密度(OD);(4)根据标准曲线,计算血清中尿素的含量。
五、实验结果与分析1. 标准曲线绘制:绘制标准曲线,结果显示尿素浓度与光密度呈线性关系,相关系数R²=0.998。
2. 血清尿素含量测定:根据标准曲线,计算各血清样本中尿素的含量,结果如下:样本1:尿素含量为5.2mmol/L;样本2:尿素含量为6.8mmol/L;样本3:尿素含量为7.4mmol/L;样本4:尿素含量为8.2mmol/L;样本5:尿素含量为9.0mmol/L;样本6:尿素含量为10.0mmol/L。
六、实验讨论1. 实验过程中,二乙酰-肟试剂的浓度、反应时间、温度等因素对实验结果有较大影响,应严格控制实验条件,以保证结果的准确性。

尿素氮的测定1、原理:尿酸+H20 尿酶ZNH+4+CO32NH+4+2—酮戊二酸+NADH GLDH 谷氨酸+NAD+H2O2、标本采集与处理:2、1受检者准备:病人必须空腹12小时,不饮酒24小时后采集血样。
2、2静脉采血:除非是卧床的病人,一般采血取坐位,从肘静脉取血,使用止血带的时间不超过1分钟,穿刺成功后立即松开止血带;2、3标本应无溶血。
如不符合应重新采集2.4采血管要求:采血时要求使用一次性无菌注射器,一人一管,用后毁形,用500mg/L有效氯浸泡消毒30分钟,回收、焚烧、做好登记。
3、1试剂组成:RⅠ:脲酶﹥12u/ml谷氨酸脱氢酶﹥1.5u/mlNADH 0.3 mmol/LRⅡ:Tris 缓冲液80 mmol/La-酮戊二酸4mmol/L3、2标准液:7.14umoI/L3、3质控血清:应在测量未知样本的同时检测质控物并确保质控在可接受的范围内,并且结果必须在三个标准差范围内。
3、4试剂的贮存与稳定性:试剂在2—8℃保存,有效期内稳定。
混合后2—8℃稳定两周。
4、仪器:上海迅达公司的半自动生化分析仪XD811。
5、操作程序:试剂准备:取试剂Ⅱ5ml加入一瓶试剂1中混合。
波长: 340nm 比色杯光径:1cm5.4计算方法:BUN=A样品×F F=C 标准/A 标准6、操作性能:线性范围0—35.7 mmol/L ,如超出此范围,用生理盐水稀释后重测,结果乘以稀释倍数。
7、参考值:2.14——7.85 mmol/L 8、结果审核:8、1室内质控结果的判断:对质控结果进行分析是否在控。
8、2对检验结果进行审核,包括检验项目是否漏项,打印是否清楚。
9、临床意义:生理性:饮食(高蛋白)病理性:呕吐、消化道出血、腹泻、尿路结石。
10、参考文献:全国临床检验操作规程。
第1篇一、实验目的1. 熟悉生物化学实验的基本操作步骤。
2. 掌握血清尿素测定的原理和方法。
3. 了解血清尿素在临床诊断中的意义。
二、实验原理尿素是哺乳动物体内蛋白质代谢的终产物,主要由肝脏合成,通过肾脏排泄。
血清尿素氮(BUN)是血液中尿素的浓度,是反映肾功能和体内氮代谢状况的重要指标。
本实验采用二乙酰-肟法测定血清尿素,该方法基于二乙酰在强酸条件下与尿素缩合成红色的4,5-二甲基-2-氧咪唑化合物,颜色深浅与尿素含量成正比。
三、实验材料1. 血清样本:采集受试者空腹静脉血,分离血清。
2. 试剂:二乙酰试剂、强酸试剂、显色剂、空白试剂等。
3. 仪器:分光光度计、移液器、试管等。
四、实验方法1. 样本处理:取血清样本100μl,加入1ml强酸试剂,充分混匀后室温放置10分钟。
2. 显色:加入2ml显色剂,充分混匀,室温放置10分钟。
3. 测定:以空白试剂为参比,于540nm波长下测定吸光度。
4. 结果计算:根据标准曲线计算血清尿素含量。
五、实验结果1. 标准曲线绘制:将不同浓度的尿素标准品按照实验方法进行测定,绘制标准曲线。
2. 血清尿素含量测定:将受试者血清样本按照实验方法进行测定,得到吸光度值,根据标准曲线计算血清尿素含量。
六、结果分析1. 血清尿素正常范围为3.2~7.1mmol/L。
本实验受试者血清尿素含量在正常范围内,说明受试者肾功能正常。
2. 血清尿素升高可能见于以下情况:- 肾脏功能受损:如急性肾功能衰竭、慢性肾功能衰竭、肾小球肾炎等。
- 蛋白质摄入过多或分解代谢增强:如发热、创伤、肿瘤等。
- 肾前性少尿:如严重脱水、充血性心力衰竭、肝肾综合征等。
3. 血清尿素降低可能见于以下情况:- 蛋白质摄入减少:如营养不良、消化系统疾病等。
- 肝脏功能异常:如肝功能衰竭、肝脏病变等。
- 肾小球滤过功能下降:如肾小球肾炎、肾病综合征等。
七、实验讨论1. 本实验采用二乙酰-肟法测定血清尿素,该方法操作简便、准确度高,是临床常用的测定方法。
二乙酰一肟显色法测定血清尿素氮【目的】1. 掌握二乙酰一肟显色法测定血清尿素氮的实验方法。
2. 熟悉二乙酰一肟显色法测定血清尿素氮的实验原理。
3. 了解血清尿素氮测定的临床意义。
【原理】在酸性条件下加热,稳定的二乙酰一肟水解成不稳定的二乙酰,后者与血清中的尿素反应合成红色的二嗪化合物,其颜色深浅与尿素含量成正比。
与同样处理的尿素标准液比色可求得血清中的尿素含量。
其反应式如下:【器材】1 .血清;2 .微量移液器;3 .刻度吸量管;4. 沸水浴;5. 分光光度计。
【试剂】1 .血清新鲜人或动物血清,无溶血。
2 .酸性试剂(或称尿素氮试剂)在三角烧瓶中加蒸馏水约 100ml ,再加浓硫酸 4ml 及 85% 磷酸 66ml 。
冷至室温,加入氨基硫脲 50mg 及硫酸镉(CdSO 4 ·8H 2 O ) 2g (提高尿素与二乙酰反应灵敏度),溶解后用蒸馏水稀释至 1L 。
置棕色瓶在冰箱保存。
可稳定半年。
3 .二乙酰一肟溶液称取二乙酰一肟 20g 。
加蒸馏水约 900ml ,溶解后,再用蒸馏水稀释至 1L 。
置棕色瓶中,贮放冰箱内可保存半年不变。
4 .尿素氮标准液( 14mmol/L , 19.6mg/dl )称取干燥纯尿素 4 2mg ,加少量蒸馏水溶解后,移入 100ml 容量瓶,加氯仿数滴防腐,再加蒸馏水至刻度,在冰箱中可稳定半年。
如用 8mmol/L 苯甲酸溶液代替蒸馏水配制,此标准溶液防腐效果更好。
【操作】取 3 支试管,标明测定管、标准管及空白管,按下表操作。
试剂( ml )测定管标准管空白管血清0.02 - -尿素氮标准液- 0.02 -蒸馏水- - 0.02 二乙酰一肟溶液0.5 0.5 0.5酸性试剂 5.0 5.0 5.0混匀后,置沸水浴中加热 12min ,取出,置冷水中冷却 5min 后,用于波长540nm ,以空白管调 0 ,读取并记录标准管及测定管吸光度值。
【计算】【注意事项】1 .本法线性范围达 40mg/dl 尿素氮,即吸光度 0.7 。
尿素氮测定的标准规程【目的】体外检测血清中尿素氮(BUN)的含量。
【职责】1.实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
【标本类型及实验前准备】1.受检者的准备病人空腹12h,不饮酒24h后采集血样。
体检对象抽血前应有两周的的正常状况记录。
注意有无应用影响测试项目的药物。
此外,对于体检者,采血的季节都应做相关记录,因为样本中各项目的含量有季节性变动,为了前后比较应在每年同一季节检验。
应嘱体检对象在抽血前24小时内不做剧烈运动。
2.静脉采血除非是卧床的病人,一般在采血时取坐位。
体位影响水分在血管内外的分布,会影响测试项目的浓度。
在采血前至少应静坐5分钟,一般从肘静脉取血,使用止血带的时间不超过1分钟,穿刺成功后立即松开止血带。
【仪器设备】东芝TBA-FX8全自动生化分析仪,低速离心机一、检测原理本试剂采用由Talke和Schubert首先提出的酶学方法,为缩短和简化分析,计算基于Tiffany等的发现,即尿素浓度与固定时间间隔内的吸光度变化成正比。
其反应如下:尿素 + H2O−−→−尿素酶2NH3 + CO2NH3 + α-氧代戊二酸 + NADH−−→−GLDH谷氨酸 + NAD+注:GLDH为谷氨酸脱氢酶在上述反应中,酶反应速率与样本中尿素(尿素氮)的含量成正比。
在340 nm 处测定固定时间间隔内NADH吸光度下降的速率,即可测得样本中尿素(尿素氮)的浓度。
二、试剂1.试剂本科使用上海复星长征医学科学有限公司UREA试剂盒,为液体双试剂,各组分如下:试剂1(R1)α-氧代戊二酸7.5 mmol/L谷氨酸脱氢酶>800 U/LNADH 0.35 mmol/L二磷酸腺苷 1.5 mmol/LTris缓冲液115 mmol/L试剂2(R2)Tris缓冲液115 mmol/L尿素酶>40000 U/Lα-氧代戊二酸7.5 mmol/L2.校准要求2.1校准品:使用与试剂配套使用的复星长征临床化学校准血清(货号:4490050/4590050)对测定进行校准。
血清尿素氮的测定
【目的要求】
1.了解血清尿素氮测定的方法及临床意义。
2.复习尿素的生成机理及其意义。
【实验原理】
血清(或血浆)中的尿素,在尿素氮试剂的酸性环境中与二乙酰-肟(DAM)共沸后,可缩合成一红色化合物,称为fearon反应。
其颜色的深浅与血清(或血浆)中尿素的含量成正比,与同样处理的尿素氮标准液比色,即可测算出血清(或血浆)中尿素氮的含量。
【实验材料】
1.器材刻度吸管(0.1ml、2ml、10ml)恒温水浴箱分光光度计
2.试剂
(1)待测血浆(2)尿素氮试剂(3)二乙酰-肟试剂(4)尿素氮标准液
【操作步骤】
取试管三支按下表操作
1:4稀释血清(或0.1
血浆)
尿素氮标准液
0.1
(0.02mg/ml)
蒸馏水0.1
二乙酰-肟0.5 0.5 0.5
尿素氮试剂 5.0 5.0 5.0 混匀,置沸水浴中加热15min,立即用自来水冷却5分钟。
分光光度计选用540nm波长,以空白管调零点,读取各管吸光度。
计算及结果分析Array
尿素(mg%)
×尿素氮标准液浓度*5(mg/ml;mg/100ml)
【注意事项】
1. 此法灵敏度高,用量极微(一般只需0.02ml血清即
可)。
本实验是先将血清用生理水以1:4加以稀释再取
0.1ml,故最后计算时,应乘以稀释倍数“5”
2. 试剂中加入硫胺脲和镉离子,可增进显色强度和色
泽稳定性,但仍有轻度褪色现象(小于5%/h)。
3. 此法操作简单,特异性强,不受其他非蛋白质含氮
化合物如尿酸、肌酸等影响,但应控制好实验条件。
4. 吸管必须校正,使用时务必注意清洁干净,加量务
必准确。
5.尿液中的尿素氮也可用此法进行测定。
由于尿液中尿素氮含量高,标本需用蒸馏水以1:50稀释。
如果呈色后吸光度仍超过本法的线性范围,还需将尿液再稀释,重新测定。
【思考题】
血清尿素氮测定的方法及临床意义。